Данное изобретение относится к неописанным в литературе замещенным [I4] метилциклофенам общей формулы I
 где Х = Н, R - алкил-С4-С10, RI -алканоил-С16-С17;
где Х = Н, R - алкил-С4-С10, RI -алканоил-С16-С17;
или при Х - низший алкил, R-H, RI - алканоил-С12-С17, в качестве присадок к углеводородному топливу, а также топливной композиции, включающей их.
Известны присадки, представляющие собой сополимер этилена и амида кислоты, например винилформамида, винилацетамида с винил-N-метилацетамидом и топливная композиция на основе жидкого углеводородного топлива, включающая известные присадки в количестве 0,001-2,0 мас.%.
Недостаток известных присадок состоит в том, что композиции с использованием известных присадок имеют относительно высокую температуру помутнения (Т.п), температуру нарушения прохождения через фильтр при охлаждении (Т.нпф) и температуру текучести (Т.т).
Целью изобретения является изыскание присадок, которые бы при введении их в композицию улучшали бы указанные характеристики.
Поставленная цель достигается замещенными [I4]-метилциклофанами формулы I и композициями на основе жидкого углеводородного топлива, включающие замещенные [I4]-метилциклофаны формулы I в количестве 0,001-1,0 мас.%, в качестве присадок.
Предложенные композиции основаны на таких жидких углеводородах как легкое дизельное топливо и тяжелое жидкое топливо, известное как газойль. Термин газойль означает углеводородные фракции с диапазоном перегонки 150-450оС (ASTM D 86-67).
Присадки против помутнения общей формулы I можно добавить к газойлям или углеводородным фракциям, известным как газойль, непосредственно или растворенным в растворителях, желательно ароматических с высокой температурой кипения, имеющихся в продаже под маркой Shellsol AB, Shellsol A.E.R, Solvesso 100, 150, 200, НАN и т.п., либо непосредственно, либо в смеси с другими присадками, такими как антиокислители, моющие вещества, вещества против ржавчины, депрессанты текучести и т.п. Углеводородные фракции, содержащие тетрамеры общей формулы I понижают температуру помутнения более чем на 10оС. Указанные присадки обладают свойством замедлять осаждение парафинов при хранении, а также коррозию металлических поверхностей при контакте с обработанными углеводородными фракциями.
Примерами продуктов с общей формулой I (по тексту - тетрамины) в качестве присадок, снижающих температуру помутнения композиций данного изобретения, являются:
3.5.10.12.17.19.24.25-октаоктадеканоилокси- r-1, с-8, с-15, с-22-тетраенайкозан-[I4]-метациклофан;
3.5.10.11.12.17.18.19.24.25.26 - додека-эксадецилокси-r-1, с-8, с-15, с-22 - тетраметил - [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26 - додека-октадеканоилокси- r-1, с-8, с-15, с-22-тетраундецил- [I4]-метациклофан;
4.11.18.25 - тетраметил - 3.5.10.12. 17.19.24.25.26 - октадодеканоилокси - [I4]-метациклофан;
4.11.18.25 - тетраметил-3.5.10.12.17.19. 24.26-окта-октадеканоил-окси- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-ацетилокси- r-1, с-8, с-15, с-22 - тетраэптадецил- [I4] - метациклофан;
3.5.10.12.17.19.24.26-окта-октадеканоил- окси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-додеканоил- окси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-тетрадеканоил- окси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-п-додецилок- сибензоилокси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-эксаноилок- си- r-1, с-8, с-15, с-22-тетраэтил- [I4]-метациклофан;
3.5.10.12.17.19.24.26-окта-деканоилок- си- r-1, с-8, с-15, с-22-тетраэтил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- тридеканооилокси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- тетрадеканоилокси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- эксадеканоилокси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- октадеканоилокси- r-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- додеканоилокси- r-1, с-8, с-15, с-22-тетраэтил- [I4]-метациклофан;
3.4.5.10.11.12.17.18.19.24.25.26-додека- деканоилокси- r-1, с-8, с-15, с-22-тетраэтил- [I4]-метациклофан и другие.
Соединения формулы I можно синтезировать реакцией резорцина, возможно замещенного в положении 2, с альдегидом и последующей этерификацией полученного продукта. Реакция между резорцином и альдегидом происходит по следующей схеме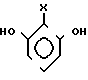 + RCHO
+ RCHO 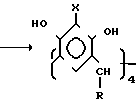 этерификацией, предпочтительно галогенидами органической кислоты или алкил-галогенидами.
этерификацией, предпочтительно галогенидами органической кислоты или алкил-галогенидами.
Примерами резорцинов являются резорцинол, пирогаллол, 2,6-дигидрокси-толуол и др.
Примерами молекул с альдегидной группой, которые могут использоваться в синтезе предлагаемых продуктов, являются следующие: формальдегид, ацетальдегид, лаурилальдегид, энантовый альдегид, бензальдегид, 1-докосанол, стеариновый альдегид, пальметиновый альдегид, 1-деканол и т.п.
Синтез обычно проводится при комнатной температуре в растворителе, предпочтительно метаноле или этаноле, и в присутствии кислотного катализатора.
Примерами катализаторов являются хлорводород, серная кислота, фосфорная кислота, пара-толуолсульфокислота и др. возможно разбавленные в воде концентрацией 25-50 мас.%.
Эти катализаторы используются в количествах 1-20 мас.% от общего количества реагентов.
Продукты, полученные таким образом, регенерированные из растворителя хорошо известной технологией, например испарением или осаждением без использования растворителей, этерифицируются по меньшей мере одним галогенидом формулы RI-Al, где RI имеет указанное значение; Al - галоген, такой как хлор, бром или ангидридом.
Примерами RI-Al могут быть: ацетил хлорид, лауроил хлорид, пальмитоил хлорид, стеароил хлорид, миристоил хлорид, деканоил хлорид, тридеканоил хлорид, 1-бромгексадекан, 1-бромдекан, 1-бромдодекан и др. В частности, реакция с соединением с формулой R-Al, где R- - алкил-С4-С30, производится предпочтительно в органическом растворителе, таком как диметилформамид (ДМФ) или диметилсульфоксид (ДМСО) и в присутствии органического основания, такого, как карбонат калия.
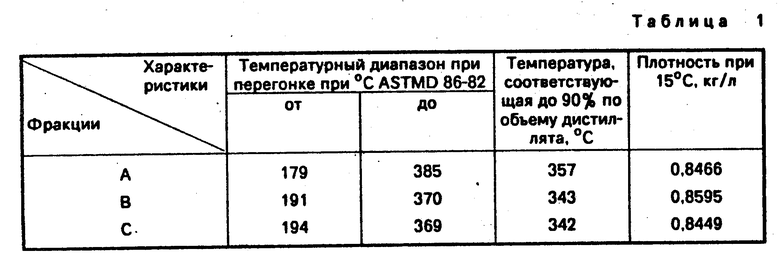
Чтобы сравнить противопомутнящие свойства заявленных присадок, принимаются в расчет характеристики углеводородных фракций, показанные в табл.1.
Тесты на следующие свойства углеводородных фракций: Т.П. - точка помутнения в соответствии с ASTMD 2500-81; Т нпф - температура нарушения прохождения через фильтр, в соответствии с IP 300/83.
Тт - температура текучести в соответствии с ASTMD 97-66.
П р и м е р 1. Получение 3.5.10.12.17. 19.24.26-октаоктадеканоилокси- r-1, с-8, с-15, с-22-тетраенэйкозан- [I4]-метациклофана.
Часть А. 1,65 г/25 ммоль, резорцина растворялись в аргоновой атмосфере в 6 мл этанола и 3 мл НСl при 37%. Раствор охлаждался в ледяной бане до 5оС и по каплям добавлялось 4,87 г/15 ммоль, 1-докосанола, растворенного в 70 мл этанола. Смесь нагревалась с обратным холодильником 8 ч. В конце она охлаждалась до комнатной температуры. Полученный осадок фильтровался, промывался водой до нейтрального состояния, высушивался в вакууме (25оС/1х10-3 мм рт. ст. ) и наконец, кристаллизовался из этанола. Было получено 4,31 г чистого тетрамера. Выход 69%.
Н-ЯМР (СDCl3):0,90(t1, 12H, CH); 1,28 {ls 152H, (CH2)19} 2,31 (bm, 8H, CH-CH2); 4,33 (t1, 4H, CH); 6,14 (S, 4H, Ar-HR/; 7,23 (S, 4H, Ar-Hb); 9,20 (S, 4H, OH); 9,50 (Sn, 4H, OHb).
Элементный анализ: С112Н192О8;
Вычислено,%: С 80,71; Н 11,61.
Найдено, %: С 81,0,5 Н 12,00.
Часть В. 0,420 г (0,25 ммоль) тетрамера, полученного таким образом, и 3.02 г (10 ммоль) стеароилхлорида нагревались 8 ч при 150оС при магнитном смешивании. В конце реакции избыток хлорида перегонялся в вакууме (140о С/1х10 мм рт.ст).
Полученный остаток растворялся в метиленхлориде, этот раствор экстрагировался NaOH 0,2, затем промывался водой до нейтрального состояния и наконец обезвоживался на безводном сульфате натрия.
Растворитель выпаривался и полученный остаток пропускался на силикагелиевой колонне с гексан/метилен хлоридом 65/35 в качестве растворителя для элюирования. Было получено 0,62 г чистого продукта. Выход 65%.
Масса (DCl-); М-СО-С17Н35 = 3527 (213С), 'Н-ЯМР(СDCl3): 0,86[M, 36H, (CH2)n-CH3)] ; 1,26 {bs, 376H, 2x[(CH2)14]+[(CH2)19}; 1,45(m, 8H, CH-CH2); 1,64(m, 16H, CO-CH2-CH2); 2,25 (m, 8H, CO-CH2), 2,56(m, 8H, CO-CH2); 4,09 (t, 4H, CH); 5,99 (S, 2H, Ar-Ha); 6,70 (S, 2H, Ar-Ha); 6,73 (S, 2H, Ar-H1b); 7,21 (S, 2H, Ar-H'a).
Элементный анализ для С256Н464О16:
Вычислено,%: С 80, 95; Н 12,31.
Найдено, %: С 81, 20; Н 12,57.
Полученный продукт растворялся в растворителе Shellsol AB (10%-ная концентрация), добавлялся к углеводородным фракциям, представленным в табл. 1. в указанных количествах.
В табл.2. показаны конечные результаты.
П р и м е р 2. Получение 3.4.5.10.11.12. 17.18.19.24.25.26-додека-эксадецилокси- V-1, с-8, с-15, с-22-тетраметил- [I4]-метациклофана.
0,609 г (2 ммоль) тетрамера, полученного как в примере 1, часть А а тем лишь исключением, что 1-докосанол замещен ацетальдегидом, а резорцина пирогаллол растворялся в 50 мл безводного ДМФ.
К раствору добавлялось 12, 21 г (40 ммоль) 1-бромгексадекана и 7,19 г (54 ммоль) карбоната калия. Смесь нагревалась до 80оС 48 ч. В конце реакции смесь разбавлялась в воде и экстрагировалась этиловым эфиром. Затем отделялась органическая фаза, промывалась водой до нейтрального состояния и обезвоживалась на безводном сульфате натрия. Растворитель выпаривался и остаток очищался на силикагелиевой колонне (проводились две последовательные очистки, первая с использованием растворителя для элюирования гексан/метилен хлорида 7/3, и вторая - гексан/метилен хлорида 75/25). Было получено 1,45 чистого продукта. Выход 44%.
Масса (DCl+) M+=3298 (213С)
'Н-ЯМР (СDCl3): 0,86 [t, 36H, (CH2)n-CH2], 1,24 [bs, 312H, (CH2)13]; 1,40 (m, 12H, O-CH2-CH2); 1,51 (d, 12 H, I=7,4 Fy CH-CH3); 1,61 (m, 12H, O-CH2-CH'2), 3,12/m, 4H, O-CH2), 3,61 (m, 8H, OCH2), 4,07 (m, 12H, O-CH2''); 4,58 (q, 4H, I=7,4 FyCH); 5,67 (S, 2H, Ar-H), 6,97 (S, 2H, Ar-H').
Элементный анализ для С224Н416О12:
Вычислено, %: С 81.48; Н 12.70.
Найдено, %: С 81.35; Н 12.81.
Полученный таким образом продукт, растворенный в растворителе Shellsol АВ (10%), добавлялся к углеводородным фракциям, указанным в табл.1.
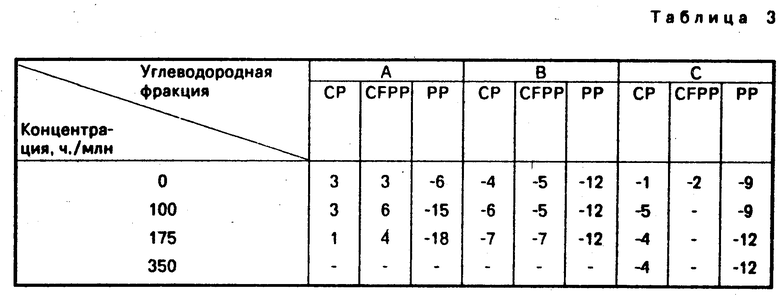
В табл.3 показаны конечные результаты.
П р и м е р 3. Получение 3.4.5.10.11.12. 17.18.19.24.25.26-додека-октадеканоилок- си- δ -1, с-8, с-15, с-22-тетраундецил- [I4]-метациклофана.
Часть А. 3,03 г (24 ммоль) пирогаллола растворялись в аргоновой атмосфере в 20 мл этанола и 3 мл НСl 37%. Раствор охлаждался в ледяной и соленой бане до 0оС и по каплям добавлялось 4,42 г (24 ммоль) лаурилальдегида. Раствор выдерживался при комнатной температуре и при помешивании 24 ч и затем подвергался нагреванию с обратным холодильником в течение 4 ч. Затем он медленно охлаждался до комнатной температуры. Полученный осадок фильтровался, промывался водой до нейтрального состояния и кристаллизовался из этанола. Полученный таким образом твердый продукт фильтровался и высушивался в вакууме (20оС/1х10 мм рт.ст). Было получено 1,60 г продукта, содержащего две молекулы этанола на каждую молекулу тетрамера.
Н-ЯМР (ацетон-dc): 0,88 (t1, 12Н, СН3) 1.31 (bs, 72Н, (СН2)9], 2,28 (m, 8Н, СН-СН2); 4,35 (t1, 4Н, СН); 7,09 (m, 4Н, Аr-Н); 9,20 (bs, 4Н, ОН b); 9,45 (bs 8H, OHb).
Элементный анализ для С72Н112О12х x 2С2Н5ОН.
Вычислено, %: С 72,34; Н 9,91.
Найдено, %: С 72,38; Н 9,81.
Часть В. С использованием способа, описанного в примере 1, упомянутый продукт был получен с выходом 60%, после очистки на силикагелиевой колонне с использованием гексан/метиленхлорида 7/3 в качестве растворителя для элюирования.
Масса (DCl- - : M- =4363/313С).
Н-ЯМР (CDCCl3) : 0,86 (m, 48Н, (СН2)n - СН3); 1,30 {m, 408Н, 3х/СН2) + (СН2/9} ; 1,45/m, 8Н, СН-СН2) 1,61 (m, 24Н, СО-СО2 СН2); 2,25 (m, 12Н, СО-СН2); 2,47 (m, 12Н, СО-СН2) 4,08(t1: 4Н, СН); 6,02 (S, 2Н, Аr - Н); 7,21 (S, 2Н, Аr-Н).
Элементный анализ для С228Н520О24
Вычислено, %: С 79,20; Н 12,00
Найдено, %: С 79,52; Н 12,29.
Полученный продукт, растворенный в растворителе Shellsol АВ (10%), добавлялся к углеводородным фракциям, указанным в табл.1.
В табл.4 показаны конечные результаты.
П р и м е р 4. Процедура использовалась та же, что и в примере 2, за исключением того, что полученный в первой части тетрамер реагирует с эквимолярной смесью следующих кислотных хлоридов: лаурил хлорида, пальмитоил хлорида, стеароил хлорида, докосаноил хлорида. После очистки на силикагеле метилен/хлорид/гексаном 8/2 получается смесь замещенных продуктов с мол.м. между 2792 и 4472.
Полученная смесь продуктов, растворенная в Shellsol AB (10%), была добавлена к углеводородным фракциям табл.1.
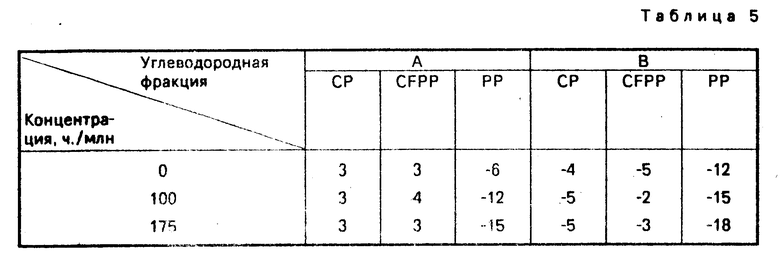
В табл.5 показаны конечные результаты.
П р и м е р 5. Получение 4.11.18.25-тетраметил-3.5.10.12.17.19.24.26-октадодеканоилокси- [I4] метациклофана.
Часть А. 37,3 г (300 ммоль) 2,6-дигидрокситолуола растворялись в аргоновой атмосфере в 120 мл дегазированного этанола и 30 мл 37%-ной НСl. Раствор охлаждался до 5оС в ледяной ванне, и в течение 2 ч каплями добавлялось 25,7 мл (326 ммоль 337% формальдегида в воде. Раствор выстаивался при комнатной температуре 48 часов и затем нагревался с обратным холодильником 6 часов. После охлаждения полученный осадок фильтровался. При добавлении воды к раствору получался еще осадок. Два осадка смешивались, промывались водой до нейтрального состояния и кристаллизовались из ацетона. Полученный осадок фильтровался и высушивался в вакууме (25оС/1х10-5 мм рт.ст). Получалось 25,0 г продукта. Выход 61%.
Н-ЯМР (DMCO-dc): 2,08 (S, 12H, CH3); 3,67 (S, 8H, CH2); 6,82 (S, 4H, Ar - H); 8,68 (S, 8H, ОН).
Элементный анализ для С32Н32О8.
Вычислено, %: С 70,5; Н 5.92.
Найдено, %: С 70.19; Н 5.62.
Часть В. При той же процедуре, описанной в примере 1, часть В, с использованием додеканоил хлорида. Упомянутый продукт был получен с выходом 75% после двойной кристаллизации из ацетона.
Масса (DCl +) : МН+ = 2002 (113С).
Н-ЯМР (СDCl3): 0,89 (t, 24H, (CH2/n - CH3); 1,25 [bs 128H (CH2)8 I]; 1,68 (t1, 16H CO-CH2 -CH2); 1,89 (s, 12H, Ar -CH3); 2,51 (m, 16H, CO-CH2); 3,50 (S, 8H, Ar -CH2-Ar); 6,38 (S, 4H, Ar -Н).
Элементный анализ для С128Н208О16:
Вычислено, %: С 76,75; Н 10,47.
Найдено, %: С 76,67; Н 10,51.
Продукт, полученный таким образом, растворенный в растворителе Shellsol AB (10%, был добавлен к углеводородным фракциям, показанным в табл.1.
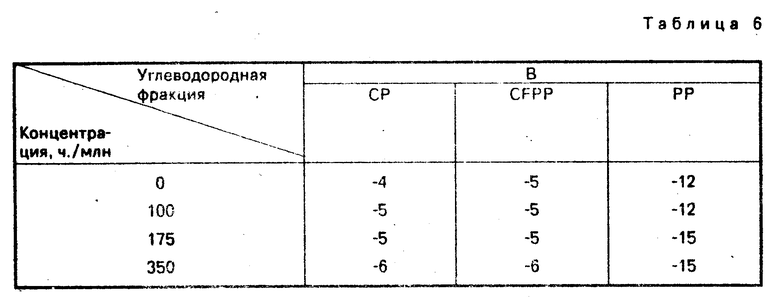
В табл.6 показаны конечные результаты.
П р и м е р 6. Получение 4.11.18.25-тетраметил-3.5.10.12.17.19.24.26-октаоктадеканоилокси- [I4]-метациклофана. Используется та же процедура, что и в примере 1, часть В с реакцией стеароилхлорида с тетрамером примера 5 часть А. Был получен указанный продукт с выходом 60% после очистки на силикагелиевой колонне с использованием в качестве растворителя для элюирования метиленхлорид/гексана 9/1.
Масса (DCl+): М+ = 2673 (113С).
Н-ЯМР (СDCl3): 0,86 (t1, 24H,/CH2/n -CH3); 1,24 [bs, 224H, (CH2)n]; 1,66 (m, 16H, CO-CH2 -CH2); 1,88 (S, 12H, Ar -CH3); 2,47 (S, 16H, CO-CH2), 3,49 (S, 8H, Ar -CH2-Ar); 6,36 (S, 4H, Ar -Н).
Элементный анализ для С175Н204О16:
Вычислено, %: С 78,98; Н 11,45.
Найдено, %: С 78,88; Н 11,62.
Полученный продукт, растворенный в растворителе Shellsol AB (10%), добавлялся к углеводородным фракциям табл.1.
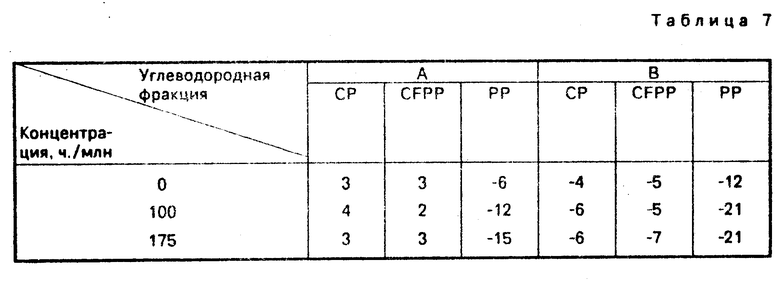
В табл.7 показаны конечные результаты.
П р и м е р 7. Получение 3.5.10.12.17. 19.24.26-окта-ацетилокси-V-1, с-8, с-15, с-22 -тетраэптадецил- [I4]-метациклофана.
Часть А. Использовалась та же процедура, что и в примере 1, часть А с применением стеаринового альдегида вместо 1-докосанола, с выходом 82%.
Н-ЯМР (СD3OO, 84oC): 0,91 [t1, 12H (CH2/n -CH3] ; 1,36 [bs, 12OH (CH2/15] ; 2,16 (m, 8H, CH-CH2); 4,29/t1, 4H, CH); 6,21 (S, 4H, Ar - H2); 7,16/S, 4H, Ar - Hb).
Элементный анализ для С96Н160О8
Вычислено, %: C 79,94; Н 11.18.
Найдено, %: С 79.59; Н 10.79.
Часть В. 1.50 г (1,04 ммоль) суспендировались в 10 мл ацетальдегида, содержащего две капли пиридина. Смесь нагревалась с обратным холодильником при перемешивании в течение 1 ч. Полученный твердый осадок после охлаждения фильтровался, промывался водой до нейтрального состояния и кристаллизовался из этанола. Осадок высушивался в вакууме (1х10-3 мм рт.ст.). Получалось 1,38 г чистого продукта.
Выход 75%.
Масса (DCl+): МН+ = 1778 (113С).
Н-ЯМР (СDCl3): 0,89 [t1, 12H, (CH2)n -CH3]; 1,29 [bs 12OH, (CH2/15]; 1.84 (m 8H, CH-CH2); 2,13 (bs, 24H, CO-CH3); 4.12 (t1, 4H, CH); 6,10 (S, 4H, Ar -Ha); 6,89 (S, 4H, Ar -Hb).
Вычислено, %: С 75.63; Н 9,97;
Найдено, %: С 75.42; Н 9,83;
Полученный продукт, растворенный в растворителе Shellsol AB (10%), добавлялся к углеводородным фракциям в табл.1.
В табл.8 показаны конечные результаты.
П р и м е р 8. Получение 3.5.10.12.17. 19.24.26-окта-октадеканоилокси-r-1, с-8, с-15, с-22-тетраметил-[I4]-метациклофана.
0,545 г (1 ммоль) тетраметра, полученного в первой части примера 1, за исключением того, что вместо 1-докосанола использовался ацетальдегид и 19,5 г стеароил хлорида нагревались до 180оС 6 ч при перемешивании. В конце реакции избыток хлорида перегонялся в вакууме (140о С/1х10-2 мм рт.ст.). Осадок растворялся в метилен хлориде и полученный раствор сначала смешивался и встряхивался с NaOH 0,2 N, затем промывался водой до нейтрального состояния и наконец обезвоживался на безводном сульфате натрия. Растворитель выпаривался и остающийся остаток пропускался 2 ч на силикагелиевой колонне с использованием метиленхлорид/гексана 7/3 и диметилен хлорид/гексана 6/4 в качестве растворителей для элюирования. Было получено 1.66 г чистого продукта. Выход 62%. Масса (DCl+):M+ = 2673 (113С).
Н-ЯМР (СDCl3): 0,87 [t1, 24H, (CH2/n - CH2)], 1,28 [bs, 224H, (CH2)14]; 1,43 (d, 12H I= 7,5 Гц CH-CH3); 1,51 (m, 8H, CH-CH2-CH2); 1,75 (m1, 8H, CO-CH2-CH2); 2,22 (m, 8H, CO-CH2); 2,57 (m, 8H, CO-CH2); 4,22 (q, 4H, I=7,5 Гц, CH); 5,91 (S, 2H, Ar -Ha); 6,72 (S, 2H, Ar - Hb); 6,88 (S, 2H, Ar -Hb); 7,38 (S, 2H, Ar -Ha').
Элементный анализ для С176Н304О16.
Вычислено, %: С 78,98; Н 11,45.
Найдено, %: С 78,80; Н 11,38.
175 частей на миллион продукта, полученного таким образом, было добавлено после растворения 10% в растворителе Shellsol AB к углеводородным фракциям А и В и точка текучести снизилась соответственно с -6 до -18оС и с -12 до -21оС.
350 ч.млн. того же продукта, добавленного к фракции С, снизило ее точку помутнения с -1 до -4оС.
П р и м е р 9. Получение 3.4.5.10.11.12. 17.19.24.25.26-додека-октадеканоилокси-V-1, с-8, с-15, с-22 тетраметил- [I4]-метациклофана.
0,609 г ммоль тетрамера, полученного в первой части примера 2, и 12.12 г (40 ммоль стеароил хлорида реагировали по той же схеме, что в примере 8. В этом случае продукт очищался двойной кристаллизацией из метилен хлорид/этилового эфира. Выход 83%. Масса (DCl-): M- = 3802 (213C).
Н-ЯМР (СDCl3):0,89 [t1, 36H,/CH2/n -CH3]; 1,30 [bs, 336H,/CH2/14]; 1,46 (d, 12Н, I = 7,4 Гц, CH-CH3); 1,70 (m, 24H, CO-CH2-CH2); 2,30 (m, 12H, CO-CH2); 2,51 (m, 12H, CO-CH2); 4,23 (q, 4H, I= 7,4 Гн, CH); 6,03 (I, 12H, Ar -H); 7,30 (S, 2H, Ar -Ha').
Элементный анализ для С248Н440О24
Вычислено,%: С 78.26; Н 11,65.
Найдено, %: С 78.30; Н 11,70%.
175 ч. /млн. полученного продукта после 10%-ного разбавления растворителем Shellsol AB было добавлено к А углеводородным фракциям и точка текучести снизилась с 3 до 0оС.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТОПЛИВНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2041921C1 |
| БИАРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ И КОСМЕТИЧЕСКАЯ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1998 |
|
RU2185373C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ АМИНОВ, СОДЕРЖАЩИХ ЭТЕНИЛБЕНЗИЛЬНЫЕ ЗАМЕСТИТЕЛИ | 2015 |
|
RU2732296C2 |
| АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЛЕЧЕНИЯ ВОСПАЛЕНИЯ | 1994 |
|
RU2130011C1 |
| ПРОИЗВОДНЫЕ 3,3`-ДИТИОБИС(ПРОПИОНОВОЙ КИСЛОТЫ) ИЛИ ИХ СТЕРЕОИЗОМЕРЫ И СОСТАВ, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 1991 |
|
RU2041208C1 |
| Четвертичные аммониевые соединения на основе производных пентаэритрита и пиридоксина, обладающие антибактериальной активностью | 2023 |
|
RU2811203C1 |
| 17БЕТА-ЗАМЕЩЕННЫЕ 3-КАРБОКСИСТЕРОИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМКОМПОЗИЦИЯ | 1992 |
|
RU2104283C1 |
| КОНТРАСТНЫЕ АГЕНТЫ И ИХ ПРИМЕНЕНИЕ | 1993 |
|
RU2122432C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ЗАМЕЩЕННЫХ АНТРАЦИКЛИНОНОВ | 1989 |
|
RU2071463C1 |
| N-ИМИДАЗОЛИЛЬНЫЕ ПРОИЗВОДНЫЕ ЗАМЕЩЕННЫХ АЛКОКСИИМИНОТЕТРАГИДРОНАФТАЛИНОВ ИЛИ ХРОМАНОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ АНТАГОНИСТА ТРОМБОКСАНА И ИНГИБИТОРА ТРОМБОКСАНСИНТАЗЫ | 1992 |
|
RU2083566C1 |



Использование: в качестве присадки к углеводородному топливу для снижения температуры помутнения, температуры нарушения прохождения через фильтр при охлаждении и снижения температуры текучести. Сущность изобретения: замещенные [ 14 ]-метациклофаны имеют общую формулу I, приведенную в описании, где при X-H; R-алкил- C4-C30 , R'-алканоил- C16-C17 ; или при X - низший алкил, R - H, R' - алканоил- C12-C17 . Топливная композиция на основе углеводородного топлива содержит 0,01 - 1,0 мас.% присадки. 2 с.п. ф-лы, 8 табл.
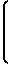
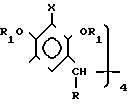
где Х - Н;
R - С4 - С30-алкил;
R1 - С16 - С17-алканоил;
или при Х-низший алкил R - H,
R1 - С12 - С17-алканоил,
в качестве присадок к углеводородному топливу для снижения температуры помутнения, температуры нарушения прохождения через фильтр при охлаждении и снижения температуры текучести.
где Х - Н;
R1 - С4 - С30-алкил;
R - С16 - С17-алканоил,
или при Х - низший алкил R - H,
R1 - С12 - С17-алканоил.
| Патент ФРГ N 3112456, кл | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
1994-07-15—Публикация
1991-06-07—Подача