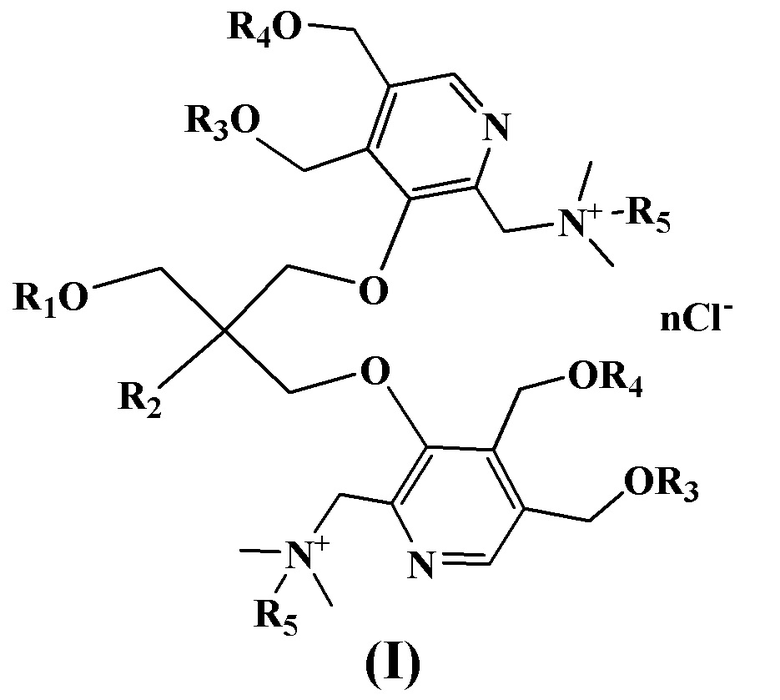
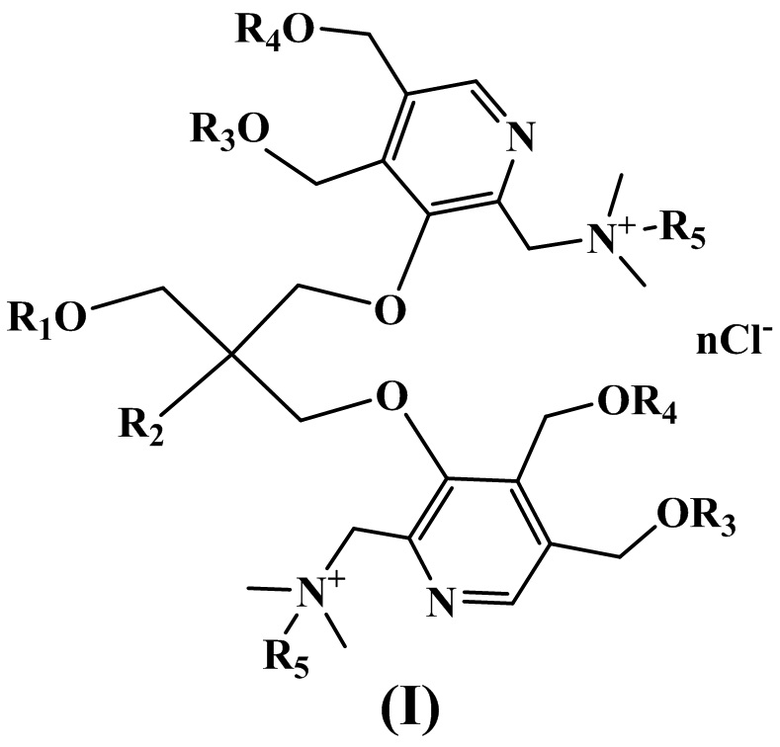
Изобретение относится к химии органических гетероциклических соединений, а именно к новым четвертичным аммониевым соединениям на основе производных пентаэритрита и пиридоксина общей формулы I, проявляющим антибактериальные свойства. Соединения могут найти применение в медицине и ветеринарии.
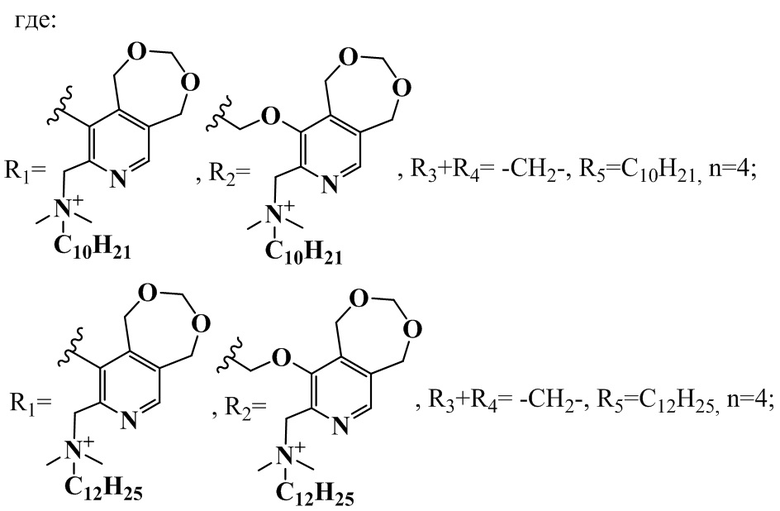
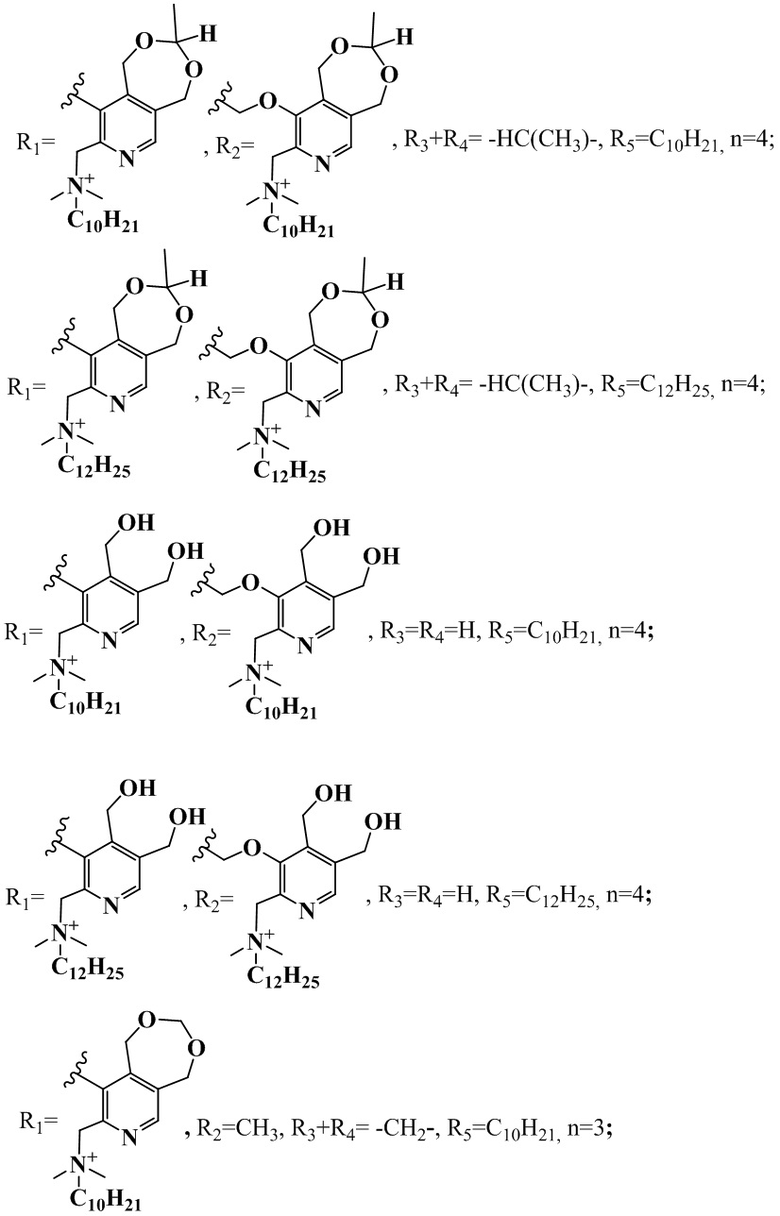
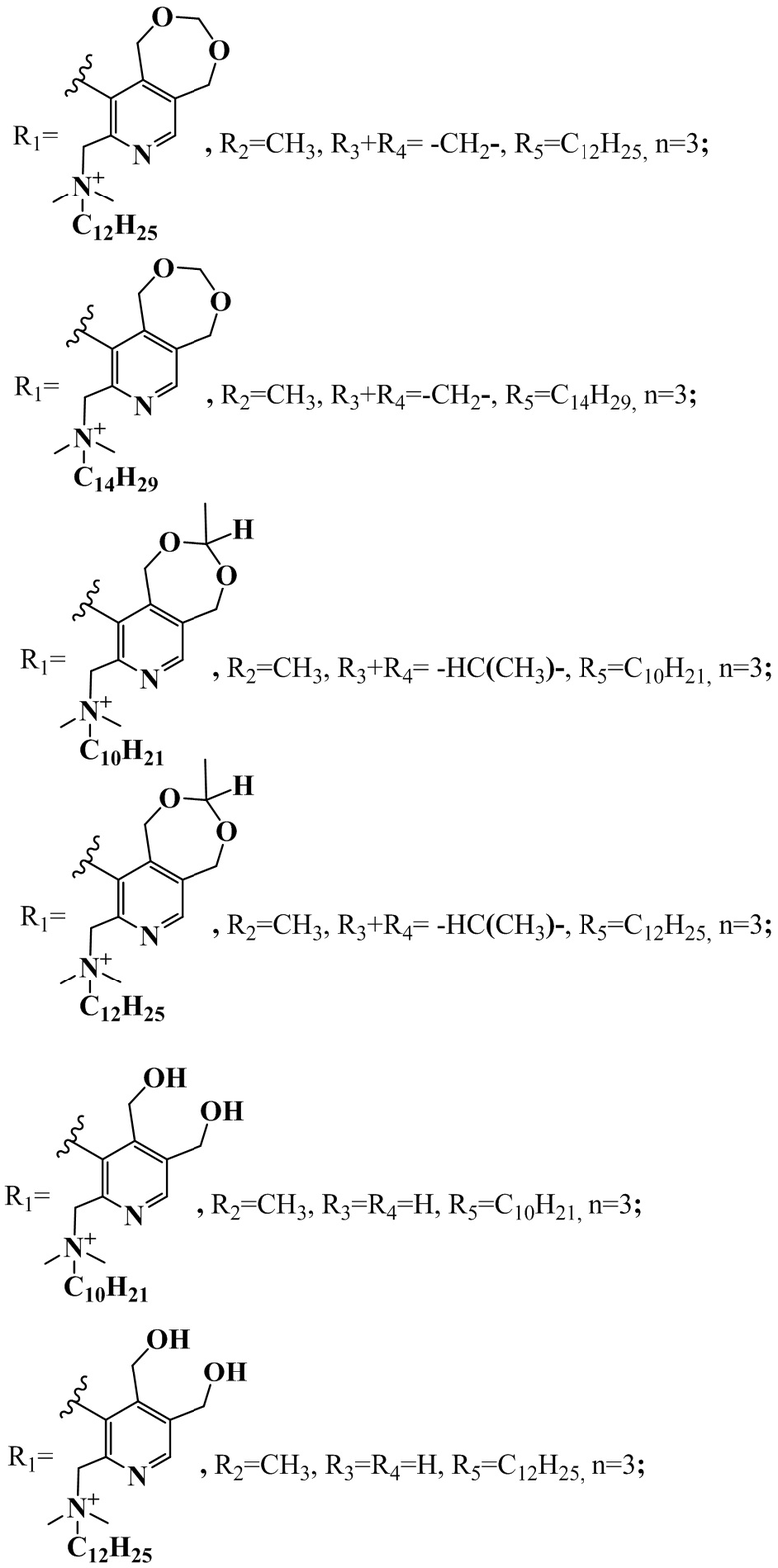
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C10H21, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C12H25, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C14H29, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C12H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C14H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C12H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C14H29, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C10H21, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C12H25, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C14H29, n=2.
Четвертичные аммониевые соединения (ЧАС) являются одним из важнейших классов антисептических и дезинфицирующих средств. Механизм их антибактериального действия основан на дезорганизации фосфолипидного бислоя клеточной мембраны бактерий. Это приводит к изменению конфигурации мембранных белков и утечки цитоплазматического содержимого бактериальной клетки, что вызывает ее гибель. Такие факторы, как широкий спектр действия в отношении различных патогенов (бактерии, грибы, простейшие, вирусы) и низкое раздражающее действие на слизистые оболочки человека и животных позволяют применять данный класс соединений для терапии местных гнойно-воспалительных процессов, обработке неповрежденной кожи перед хирургическими операциями, дезинфекции медицинских инструментов и оборудования [Gilbert, P. Cationic antiseptics: Diversity of action under a common epithet / P. Gilbert, L. Moore // J. Appl. Microbiol. – 2005. – V. 99, Iss. 4. – P. 703-715].
Стоит отметить ряд наиболее важнейших соединений на основе ЧАС, которые применяются в качестве лекарственных средств:
Бензалкония хлорид – представляет собой смесь хлоридов алкилдиметилбензиламмония. С 1935 г. бензалкония хлорид применяется в качестве дезинфектанта и антисептика. Он обладает широким спектром действия в отношении грамположительных и грамотрицательных бактерий, грибов, вирусов. Из недостатков бензалкония хлорида необходимо отметить его сильное раздражающее действие на кожу и глаза человека, а также высокую токсичность. Стоит также отметить, что из-за широкого применения бензалкония хлорида наблюдается его накопление в объектах окружающей среды, что приводит к постепенному снижению чувствительности к нему бактерий [Pereira, B.M.P. Benzalkonium chlorides: Uses, regulatory status, and microbial resistance / B.M.P. Periera, I. Tagkopoulos // Appl. Environ. Microbiol. – 2019. – V. 85, Iss. 13. – P. e00377-19].
Цетилпиридиния хлорид (гексадецилпиридиний хлорид) – соединение, которое используется с 1930-х годов и сегодня также широко применяется для дезинфекции кожи, слизистых оболочек, очистки твердых поверхностей, дезодорации и создания косметических составов. Из недостатков следует отметить его высокую токсичность и выработку резистентности у микроорганизмов [Mao, X. Cetylpyridinium chloride: mechanism of action, antimicrobial efficacy in biofilms, and potential risks of resistance / X. Mao, D. Auer, W. Buchalla, K.-A. Hiller, T. Maisch, E. Hellwig, F. // Antimicrob. Agents Chemother. – 2020. – V. 64, Iss. 8. – P. 10.1128/aac. 00576-20].
Мирамистин (бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид) – представляет собой разработанный еще во времена Советского Союза малотоксичный антисептик широкого спектра действия, активный в отношении бактерий, патогенных грибов и вирусов [Osmanov, A. The antiseptic Miramistin: a review of its comparative in vitro and clinical activity / A. Osmanov, Z. Farooq, M. D. Richardson, D. W. Denning // FEMS Microbiol. Rev. – 2020. – V. 44, Iss. 4. – P. 399-417]. Однако по своей эффективности этот антисептик уступает бензалконию хлориду и цетилпиридинию хлориду.
Хлоргексидин – катионный антисептик, синтезированный при разработке противомалярийных препаратов в 1947 году. Хлоргексидин является антисептиком с антибактериальным, противогрибковым и противовирусным действием. Исследование на мышах показало, что при годе непрерывного применения хлоргексидин оказывает раздражающее действие на кожу и глаза [Зверьков А.В. Хлоргексидин: прошлое, настоящее и будущее одного из основных антисептиков / А.В. Зверьков, А.П. Зузова // Клин. микробиол. антимикроб. химиотер. – 2013. – Т.15, № 4. – С.279-285].
Одним из современных подходов к разработке противомикробных средств является введение в молекулу нескольких четвертичных аммониевых фрагментов. Последние исследования показывают, что к поликатионным соединениям затруднена выработка резистентности и данный класс соединений особенно эффективен в отношении грамотрицательных бактерий [Morrison, K.R. More QACs, more questions: Recent advances in structure activity relationships and hurdles in understanding resistance mechanisms / K.R. Morrison, R.A. Allen, K.P.C. Minbiole, W.M. Wuest // Tetrahedron lett. – 2019. – V. 60, Iss. 37. – P. 150935].
В работе [Al-Khalifa, S.E. The Development of Next-Generation Pyridinium-Based multiQAC Antiseptics / S.E. Al-Khalifa, M.C. Jennings, W.M. Wuest, K.P.C Minbiole // ChemMedChem. – 2017. – V. 12, Iss. 4. – P. 280-283] были получены аналоги цетилпиридиния хлорида, содержащие в своем составе два или три пиридиниевых фрагмента. Ряд из полученных соединений обладали высокими показателями антибактериальной активности на штаммах грамположительных и грамотрицательных бактерий и превосходили по своей активности цетилпиридиния хлорид.
Бис-аммониевые соединения, содержащие в своем составе кватернизированный пиридиниевый атом азота и алкилдиметилбензиламмониевые фрагменты, показали превосходящую бензалкония хлорид и цетилпиридиния хлорид антибактериальную активность на штаммах грамположительных и грамотрицательных бактерий [Schallenhammer, S.A. Hybrid BisQACs: Potent Biscationic Quaternary Ammonium Compounds Merging the Structures of Two Commercial Antiseptics / S.A. Schallenhammer, S.M. Duggan, K. R.Morrison, B. S Bentley, W.M. Wuest, K.P.C. Minbiole // ChemMedChem. – 2017. – V. 12, Iss. 23. – P. 1931-1934].
Следует отметить, что описанные выше лекарственные препараты и биологически активные соединения, по мнению заявителя, не могут рассматриваться в качестве аналогов к заявленному изобретению вследствие того, что они не совпадают с заявляемым соединением по химической структуре, хотя и обладают сходной в целом антибактериальной активностью (совпадают по назначению), сопоставимой с заявленным техническим решением, в большей или меньшей степени.
Технической проблемой, решаемой заявленным изобретением, и техническим результатом заявленного технического решения является расширение арсенала известных средств указанного назначения путем создания новых соединений общей формулы (I) на основе производных пентаэритрита и производных пиридоксина и обладающих антибактериальной активностью.
Сущностью заявленного технического решения являются четвертичные аммониевые соединения на основе производных пентаэритрита и производных пиридоксина (I):
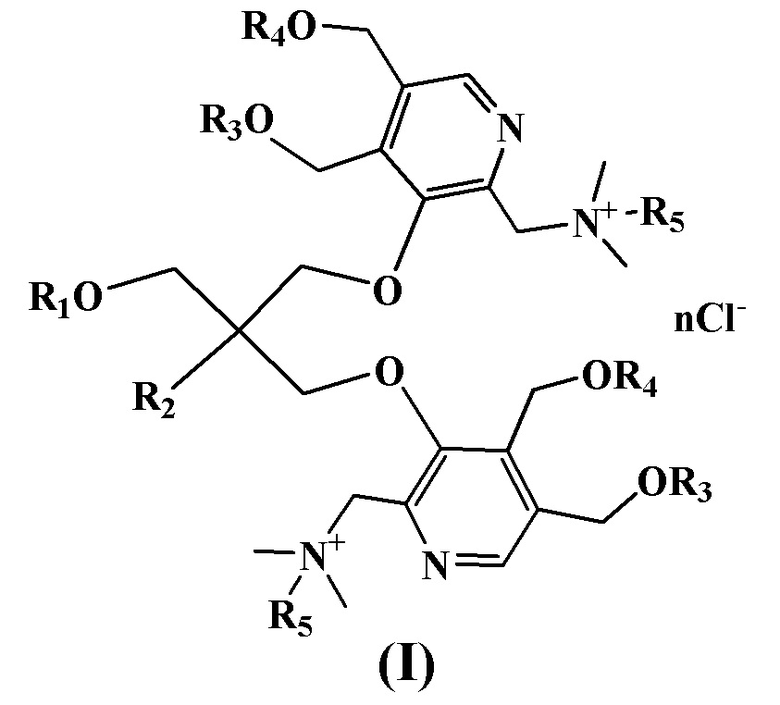
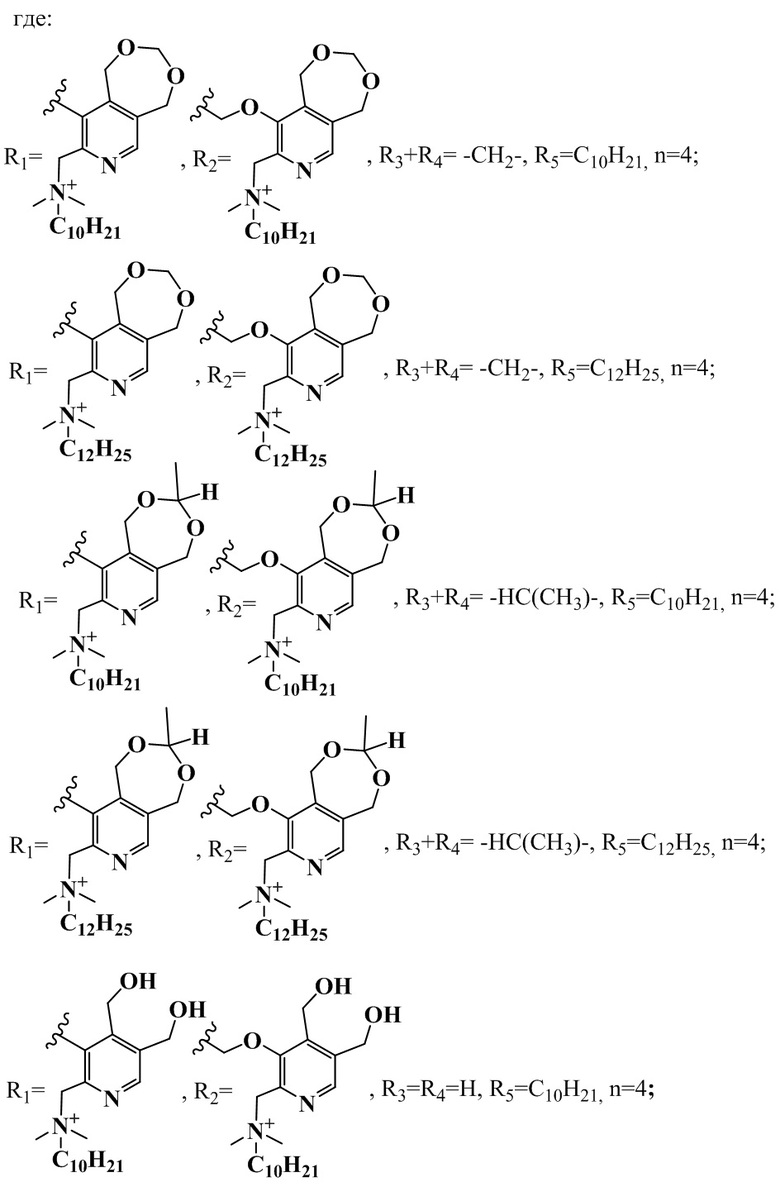
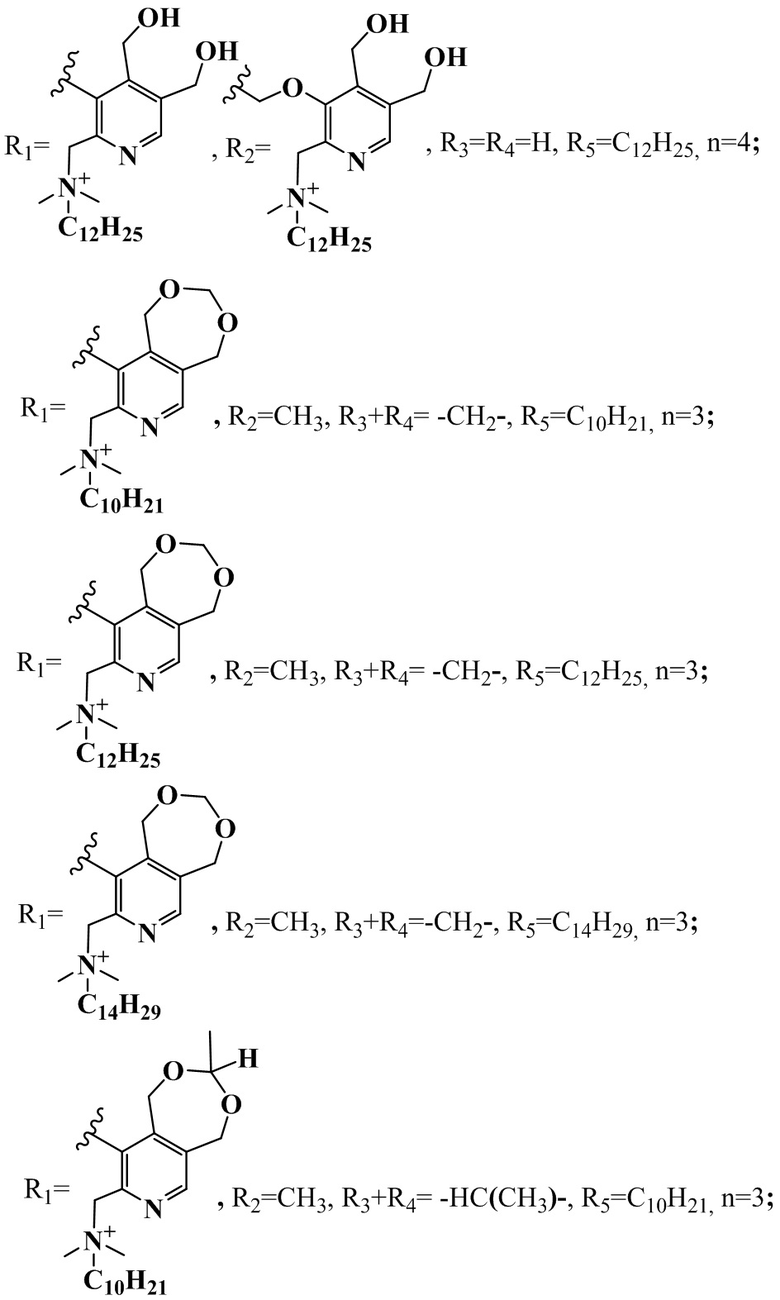
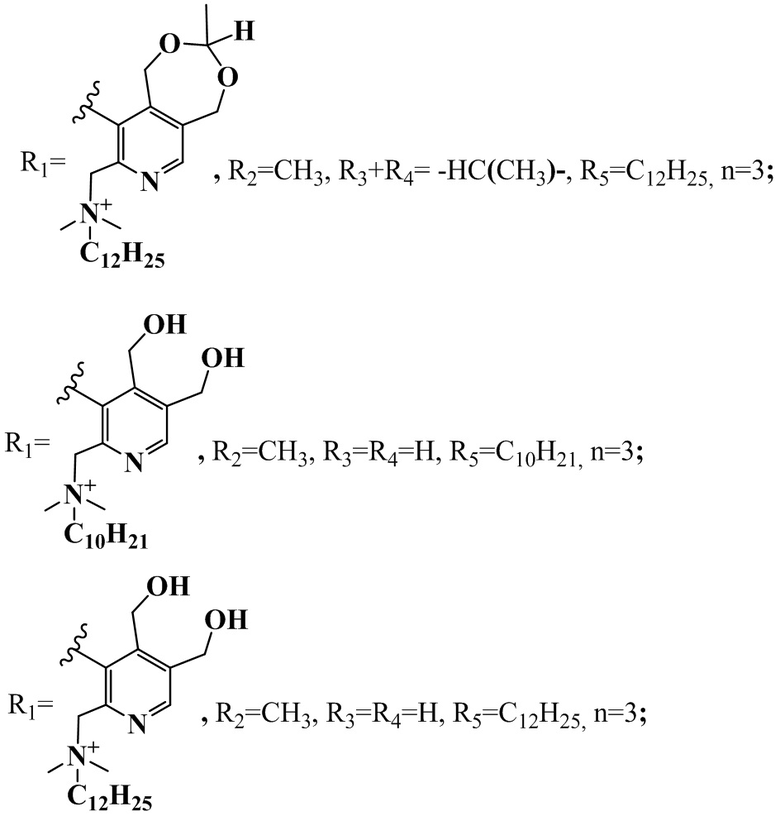
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C10H21, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C12H25, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C14H29, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C12H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C14H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C12H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C14H29, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C10H21, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C12H25, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C14H29, n=2.
Заявленное техническое решение иллюстрируется Фиг.1 – Фиг.3
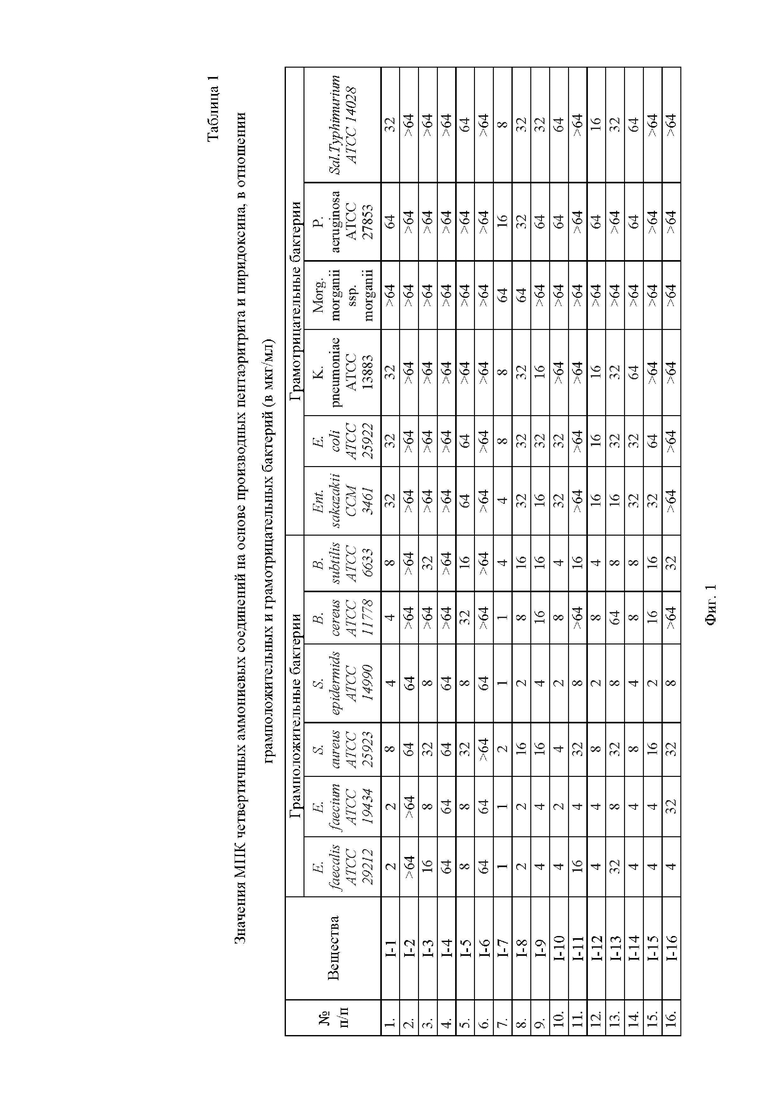
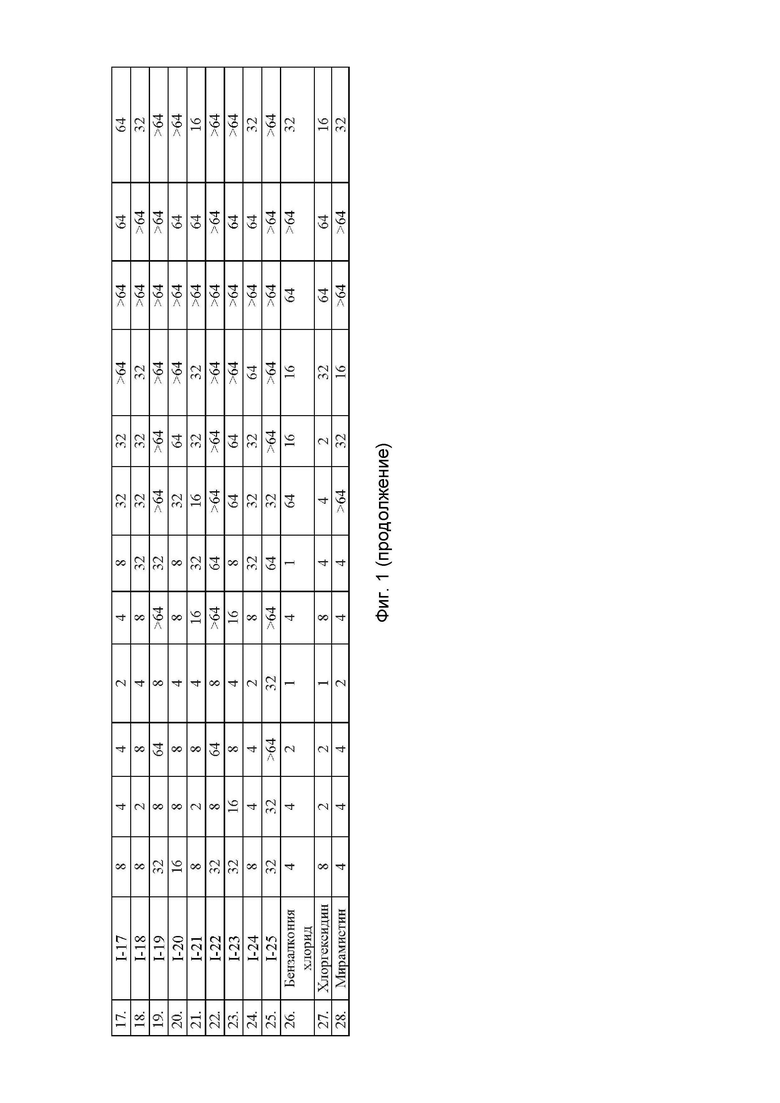
На Фиг.1 приведена Таблица 1, в которой представлены значения МПК (минимальная подавляющая концентрация) четвертичных аммониевых соединений на основе производных пентаэритрита и пиридоксина, в отношении грамположительных и грамотрицательных бактерий (в мкг/мл).
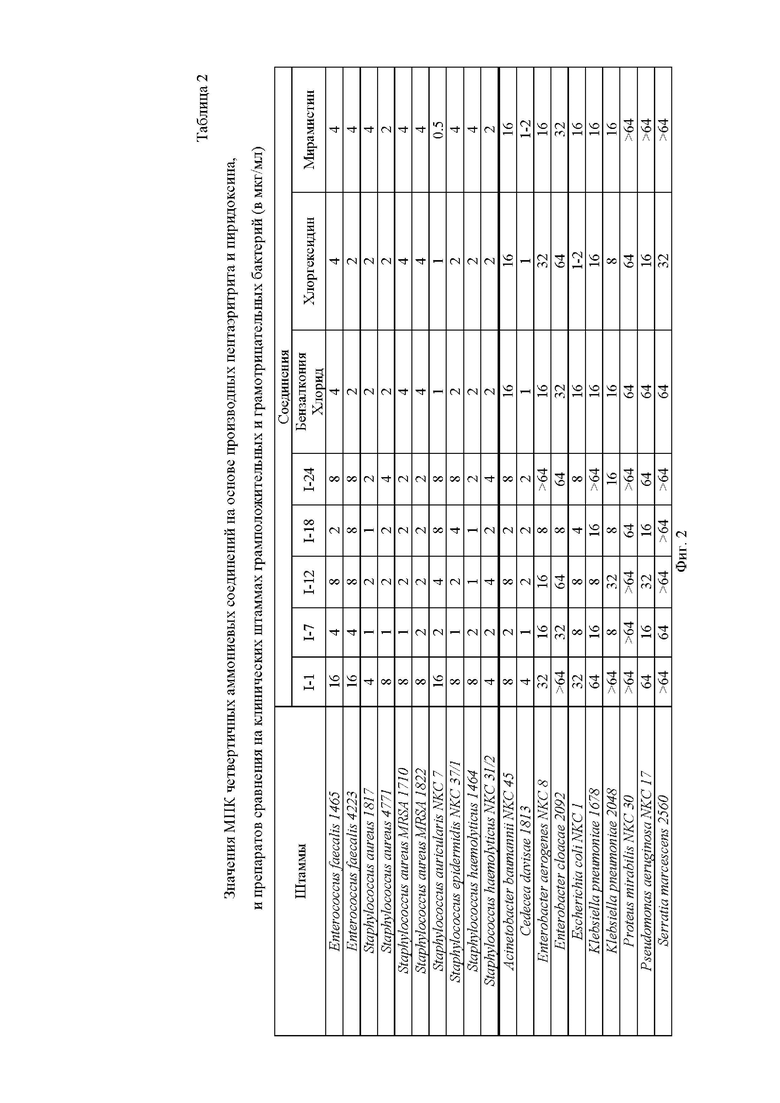
На Фиг.2 приведена Таблица 2, в которой представлены значения МПК четвертичных аммониевых соединений на основе производных пентаэритрита и пиридоксина, и препаратов сравнения на клинических штаммах грамположительных и грамотрицательных бактерий (в мкг/мл).
На Фиг.3 приведена Таблица 3, в которой представлены значения концентрации полумаксимального ингибирования роста клеток СC50 (мкг/мл) для исследуемых соединений и препаратов сравнения на условно-нормальных клеточных линиях.
Далее заявителем приведено осуществление заявленного технического решения
Заявленные соединения получают по следующим схемам 1, 2, 3, 4.
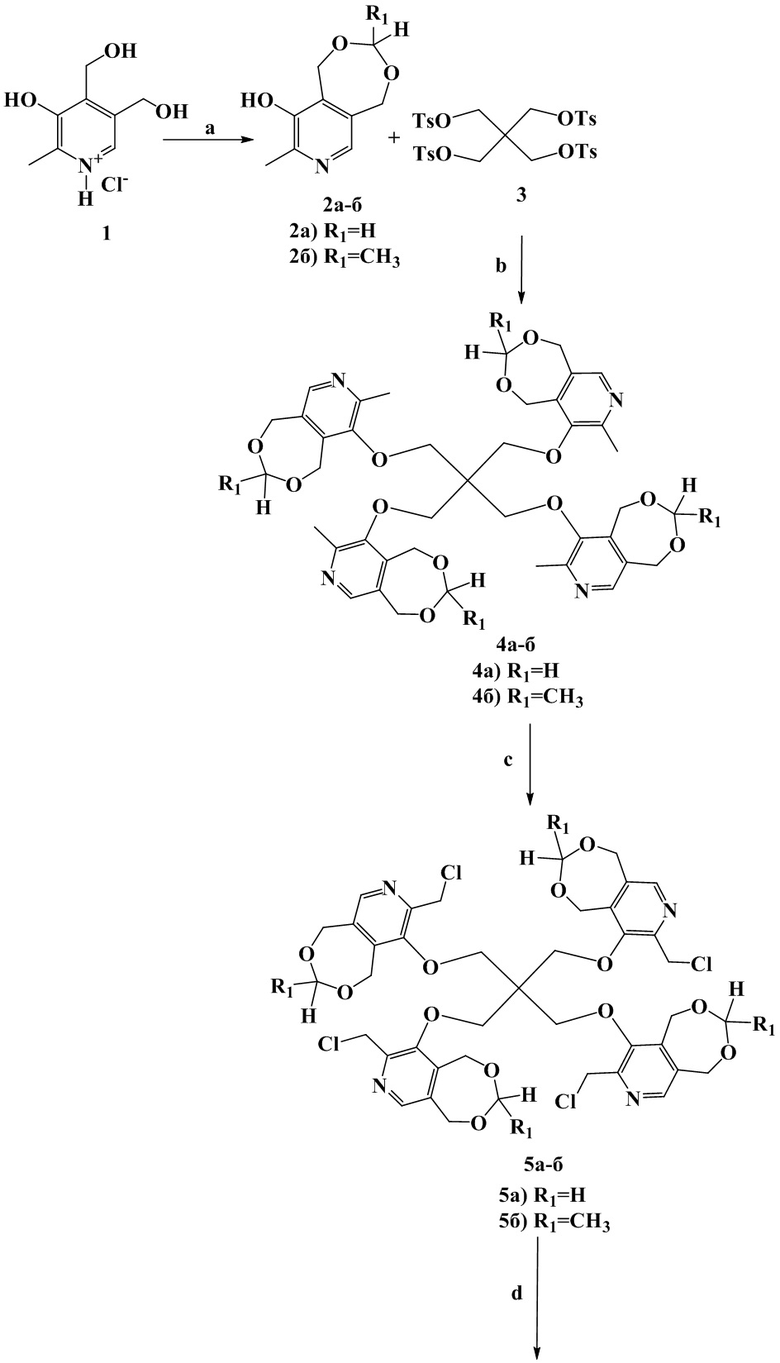
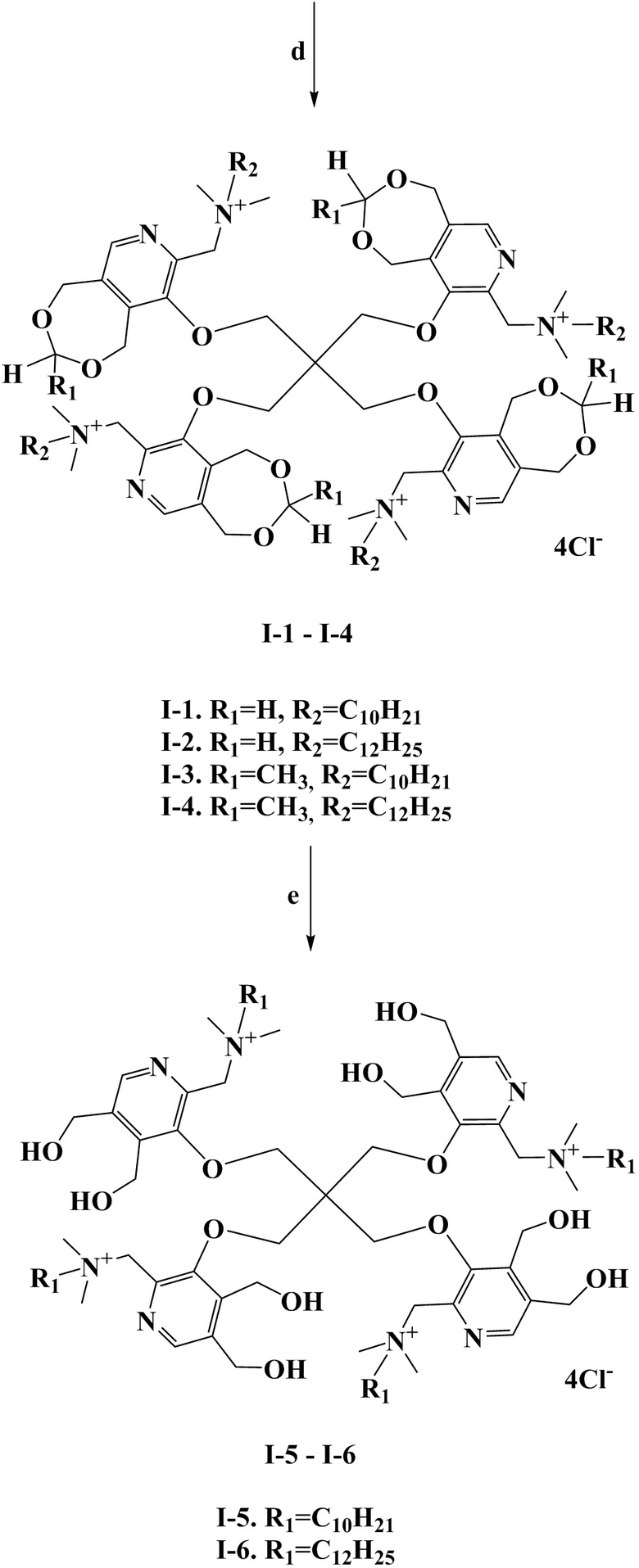
Схема 1. (a) для 2а - параформ, п-толуолсульфокислота, толуол, кипячение c насадкой Дина-Старка, 7 ч; для 2б - CH3C(O)H, HCl, 3-5 °C, 2 ч; (b) соединение 3, K2CO3, ДМФА, кипячение, 3 ч; (c) трихлоризоциануровая кислота (TCICA), CHCl3, кипячение, 1 ч; (d) соединения 5а-б, (CH3)2N(C10-C12), ДМФА, 80 °C, 8 ч; (e) соединения I-3 – I-4, HCl, H2O, 70 °C, 6 ч.
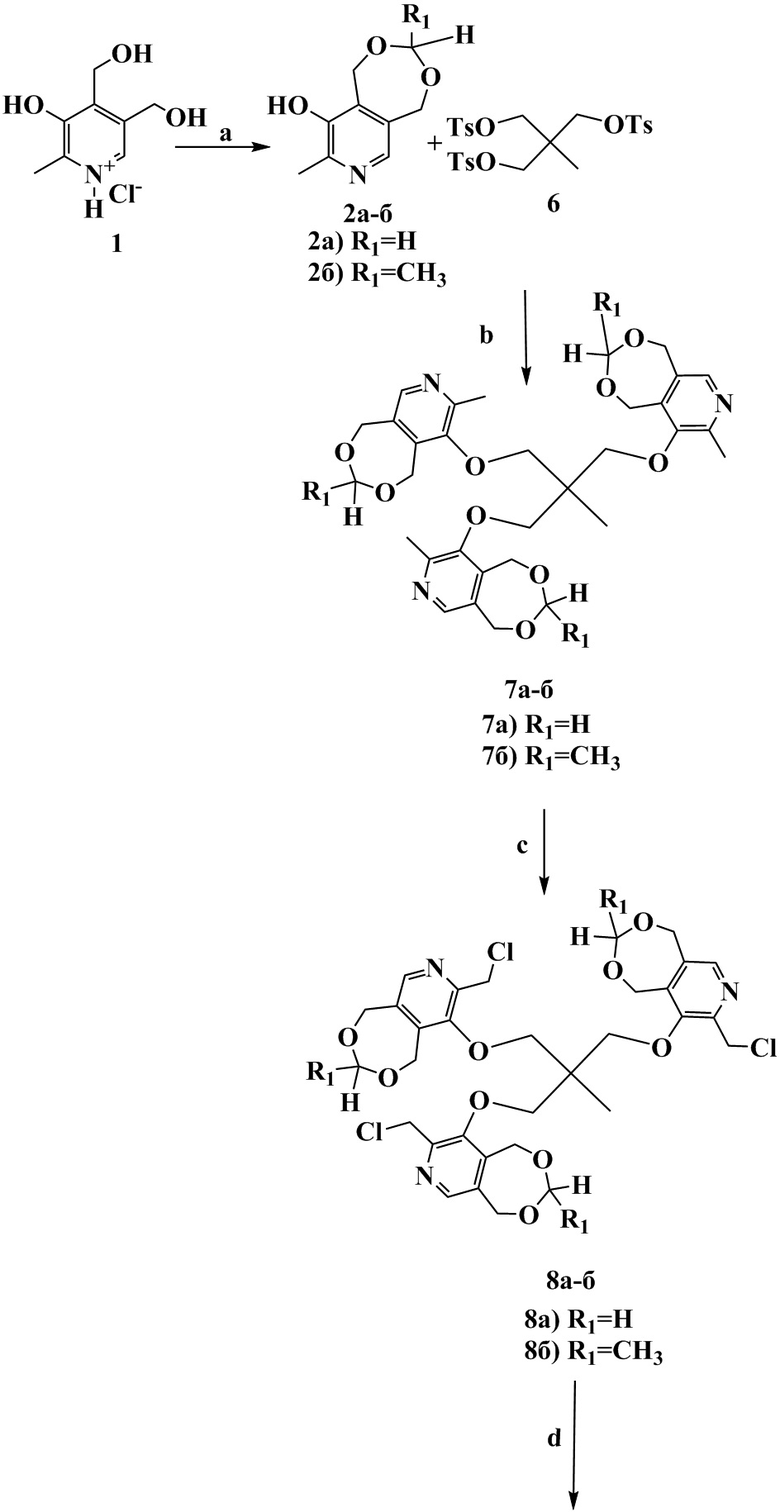
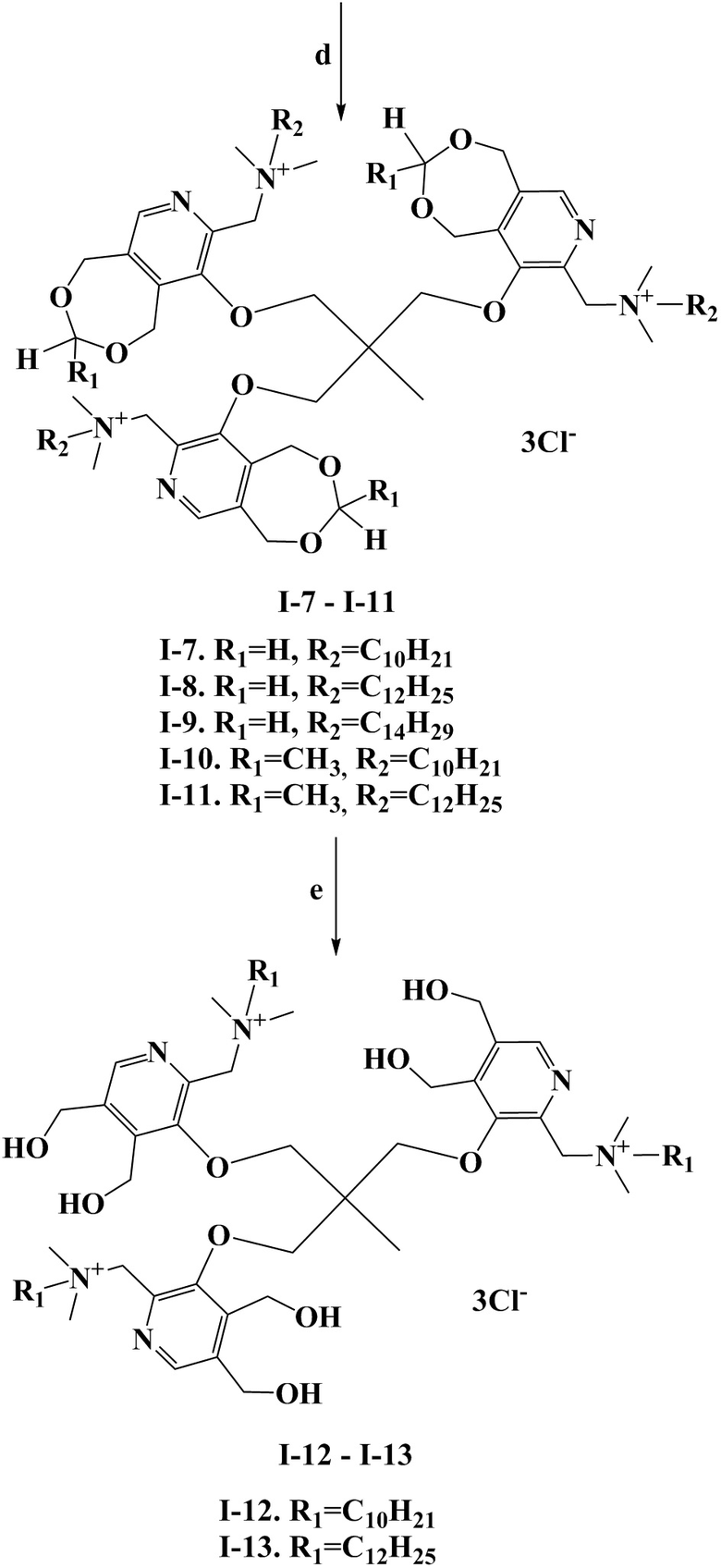
Схема 2. (a) для 2а - параформ, п-толуолсульфокислота, толуол, кипячение c насадкой Дина-Старка, 7ч; для 2б - CH3C(O)H, HCl, 3-5 oC, 2 ч; (b) соединение 6, K2CO3, ДМФА, кипячение, 3ч; (c) трихлоризоциануровая кислота (TCICA), CHCl3, кипячение, 2 ч; (d) соединения 8а-б, (CH3)2N(C10-C14), ДМФА, 80 oC, 8 ч; (e) соединения I-10 – I-11, HCl, H2O, 70 oC, 6 ч.
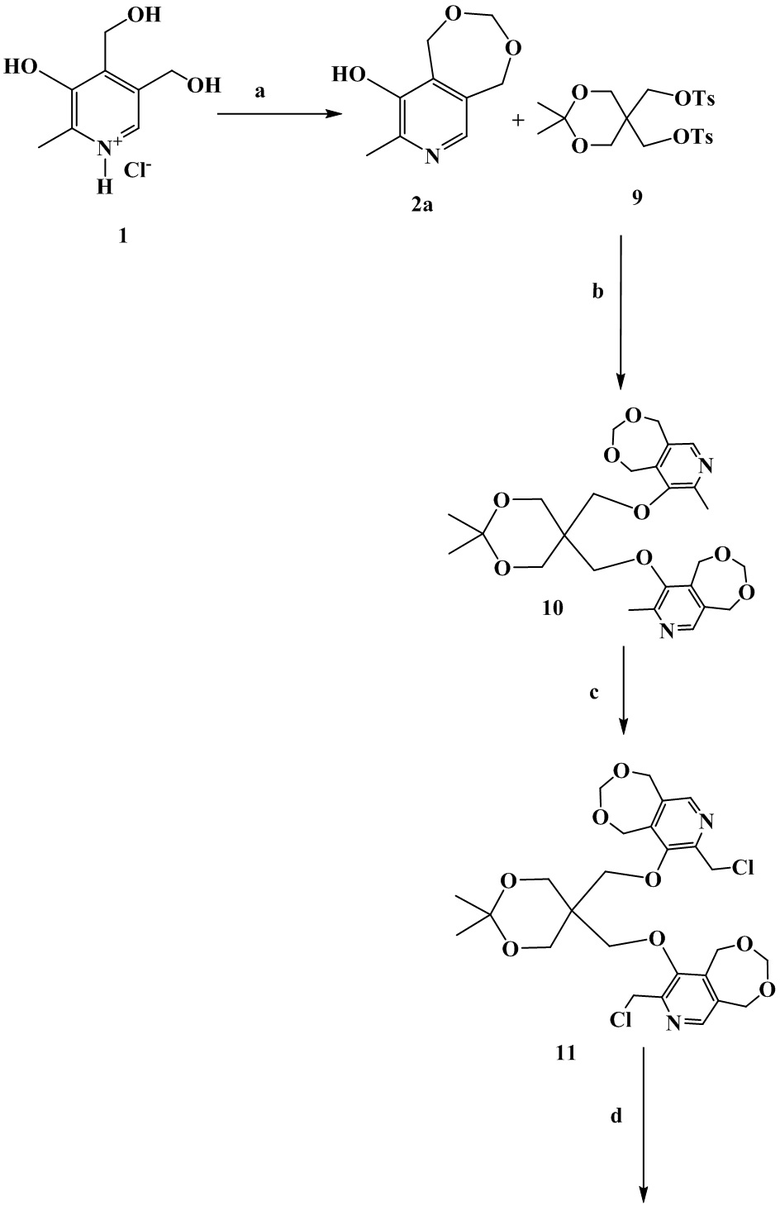
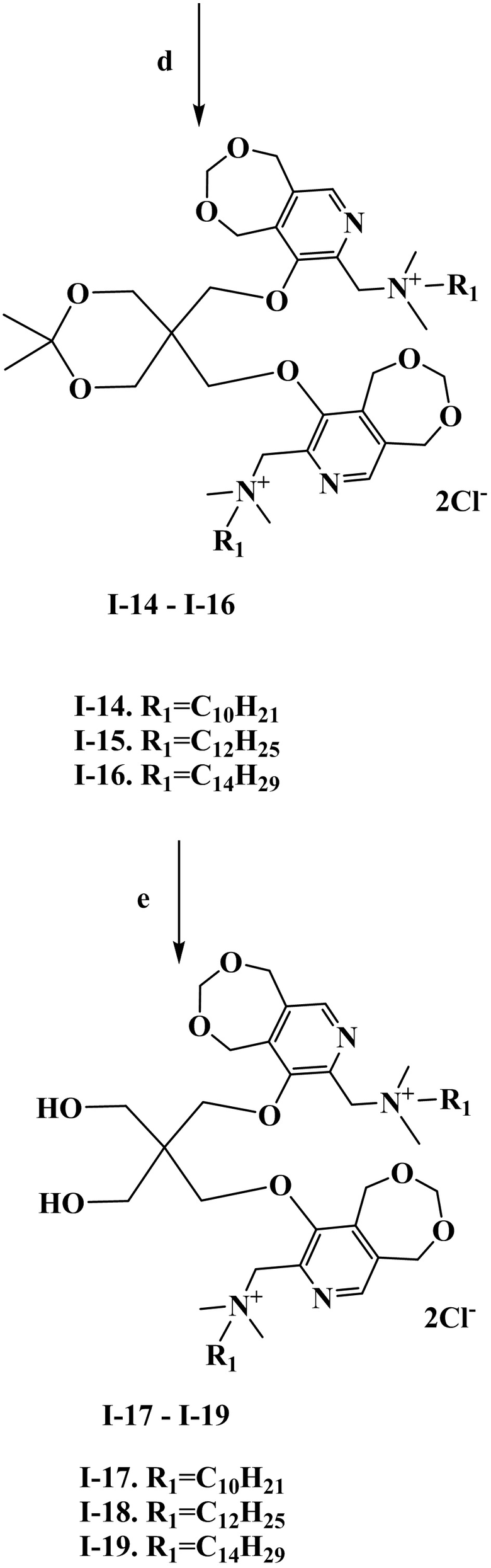
Схема 3. (a) параформ, п-толуолсульфокислота, толуол, кипячение c насадкой Дина-Старка, 7ч; (b) соединение 9, K2CO3, ДМФА, кипячение, 3 ч; (c) трихлоризоциануровая кислота (TCICA), CHCl3, кипячение, 1 ч; (d) соединение 11, (CH3)2N(C10-C14), ДМФА, 80 oC, 8 ч; (e) соединения I-14 – I-16, HCl, H2O, 70 oC, 6 ч.
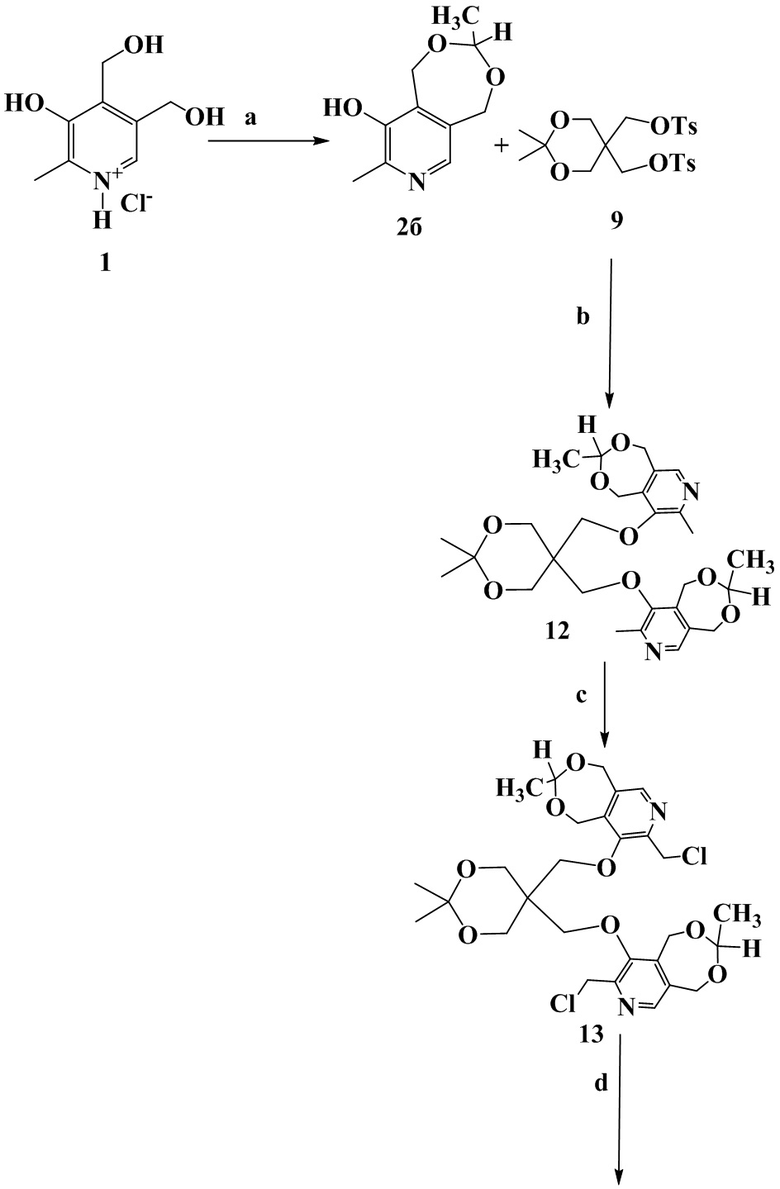
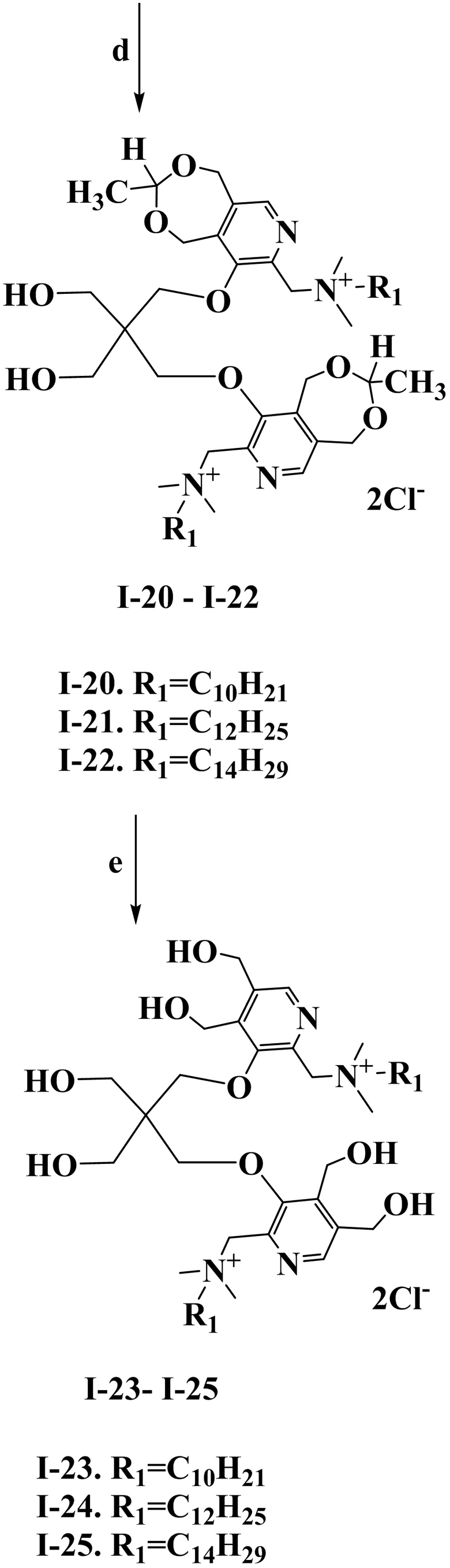
Схема 4. (a) CH3C(O)H, HCl, 3-5 oC, 2 ч; (b) соединение 9, K2CO3, ДМФА, кипячение, 3ч; (c) трихлоризоциануровая кислота (TCICA), CHCl3, кипячение, 1 ч; (d) соединение 13, (CH3)2N(C10-C14), ДМФА, 80 oC, 8 ч, HCl, 0.1М 12 ч; (e) соединения I-20 – I-22, HCl, H2O, 70 oC, 6 ч.
Характеристики новых соединений приведены далее в примерах конкретного выполнения. Структуры полученных соединений подтверждены с использованием методов масс-спектрометрии и ЯМР-спектроскопии. Спектры ЯМР соединений регистрировались на приборе «Bruker AVANCE 400» с рабочей частотой 400.13 МГц (1H) и 100.62 МГц (13C{1H}). Химические сдвиги измеряли относительно сигналов TMS (тетраметилсилана) и по отношению к остаточным протонам дейтерорастворителей (ДМСО-d6, 1Н, 2.50 м.д., 13С, 39.52 м.д; CDCl3, 1Н, 7.26 м.д., 13С, 77.16 м.д; СD3OD, 1H, 4.87 м.д., 13C, 49.00 м.д.). Константы связи (J) приведены в герцах (Гц). Для описания связи используются следующие сокращения: с – синглет; д – дублет; т – триплет; кв – квартет; м – мультиплет; АВ – AB система.
Масс-спектры MS были получены на тройном квадрупольном масс-спектрометре c линейной ионной ловушкой AB Sciex QTrap 6500 (AB SCIEX PTE. Ltd., Сингапур) с использованием детектора высокой энергии IonDriveTM и источником ионизации IonDrive Turbo V (газообразный азот распылителя, положительная полярность ионизации, напряжение иглы 5200 В). Запись спектров проводилась в режиме “Q1” с энергией столкновения 10 эВ, потенциалом декластеризации 90 эВ. Образцы с концентрацией анализируемого вещества 1 мкмоль/л готовили путем растворения исследуемых соединений в метанолe (LC-MS, Merck).
Температура плавления веществ определялась на приборе OptiMelt МPA100 (Stanford Research Systems).
Контроль за ходом реакций и чистотой соединений осуществлялся методом тонкослойной хроматографии (ТСХ) с использованием пластин силикагеля Sorbfil (Краснодар, Россия) с УФ-светом (λ, 254 нм/365 нм) или хлорида железа (III) в качестве проявляющего агента. Колоночную хроматографию проводили на силикагеле (60–200 mesh) от Acros или жидкостной хроматографией гидрофильного взаимодействия (HILIC) на приборе PuriFlash450.
Примеры конкретного выполнения заявленного технического решения
Следующие соединения были получены по известным литературным методикам:
- соединения 2а-б [Производные пиридоксина с нелинейными оптическими свойствами. Патент РФ 250180 от 2013-12-20];
- соединение 3 [Shigematsu, A. Selective Separation of Water, Methanol, and Ethanol by a Porous Coordination Polymer Built with a Flexible Tetrahedral Ligand /A. Shigematsu, T Yamada, H. Kitagawa // J. Am. Chem. Soc. – 2012. – V. 134, Iss. 32. – P. 13145–13147];
- соединение 6 [Beaufort, L. A new tripodal ligand system based on the iminophosphorane functional group. Part 1: Synthesis and characterization / L.A. Beaufort, L. Delaude, A.F. Noels // Tetrahedron. – 2007. – V. 63, Iss. 30. – P. 7003–7008];
- соединение 9 [Simmons, T.R. The mixed diol-dithiol 2,2-bis-(sulfanylmethyl)propane-1,3-diol: Characterization of key intermediates on a new synthetic pathway / T.R Simmons, C.J. Pickett, J.A. Wright // Acta. Crystallogr. C. – 2011. – V. 67, Iss. 1. – P.1-5].
Пример 1. Получение 1,3-бис(8-диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин)-9-окси)-2,2-бис((8-диметил)децил)аммоний)метил)- 1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-окси)метил)пропан тетрахлорида (I-1)
Получение 1,3-Бис(8-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)-2,2-бис(8-метил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-окси)метил)пропана (промежуточное вещество 4а):
К раствору ацеталя 2а (4.07 г, 22.4 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.08 г, 22.4 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 3 (4.14 г, 5.6 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 24% (1.07 г); бледно-желтое кристаллическое вещество; т.пл. 89 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 2.51 (с, 12Н, 4СН3), 4.32 (с, 8Н, 4СН2О), 4.87 (с, 8Н, 4СН2О), 4.96 (с, 8Н, 4СН2О), 4.97 (с, 8Н, 4СН2О), 8.11 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д: 20.19 (c, CH3), 46.76 (с, C(CH2O)4), 64.90 (c, CH2O), 68.21 (c, CH2O), 73.33 (c, C(CH2O)4), 98.25 (c, OCH2O), 134.35 (c, Сpyr), 140.47 (c, Сpyr), 143.15 (c, Сpyr), 149.76 (c, Сpyr), 151.12 (c, Сpyr).
Получение 1,3-Бис(8-хлорметил-1,5-дигидро-[1,3] диоксепино[5,6-с] пиридин-9-окси)-2,2-бис(8-хлорметил-1,5-дигидро-[1,3] диоксепино[5,6-c] пиридин-9-окси) метил) пропан (промежуточное вещество 5а):
0.99 г (1.3 ммоль) соединения 4а растворяли в 25 мл хлороформа и добавляли 1.17 г (5.2 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 1 часа. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 37% (0.44 г); желтое кристаллическое вещество; т.пл. 128-130 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 4.61 (с, 8Н, 4СН2), 4.70 (с, 8Н, 4СН2), 4.91 (с, 8Н, 4СН2), 4.96 (с, 8Н, 4СН2), 5.03 (с, 8Н, 4СН2), 8.22 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 42.52 (с, СН2Cl), 47.28 (с, C(CH2O)4), 64.53 (c, CH2O), 67.89 (c, CH2O), 74.65 (c, C(CH2O)4), 97.99 (c, OCH2O), 137.51 (c, Сpyr), 142.11 (c, Сpyr), 143.98 (c, Сpyr), 149.21 (c, Сpyr), 150.07 (c, Сpyr).
Получение 1,3-бис(8-диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5, 6-с]пиридин)-9-окси)-2,2-бис((8-диметил)децил)аммоний)метил)- 1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-окси)метил)пропан тетрахлорида (I-1):
0.15 г (0.2 ммоль) соединения 5а растворяли в 5 мл ДМФА и добавляли 0.15 мл (0.6 ммоль) N,N-диметилдециламина. Реакционную смесь перемешивали в течение 8 часов при температуре 80 °С. Растворитель удаляли в вакууме. Осадок перекристаллизовывали из ацетона. Выход 0.11 г (40%); желтое кристаллическое вещество; т.пл. 83-85 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 0.86 (т, 12Н, 3JHH = 6.6 Гц, 4CH3C9H18), 1.06-1.31 (м, 56Н, 28СН2), 1.61-1.71 (м, 8H, 4CH2), 3.41 (с, 24Н, 8CH3N+), 3.73 (м, 8Н, 4CH2N+), 4.87 (с, 8Н, 4СН2), 4.90 (с, 8Н, 4СН2), 5.05 (с, 8Н, 4СН2), 5.36 (с, 8Н, 4СН2), 5.55 (с, 8Н, 4СН2), 8.08 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 14.23 (с, СН3), 22.72 (с, СН2), 22.77 (с, СН2), 26.31 (с, СН2), 29.26 (с, СН2), 29.38 (с, СН2), 29.53 (с, СН2), 29.61 (c, CH2), 31.96 (с, СН2), 47.38 (с, C(CH2O)4), 50.64 (с, CH3N+), 62.24 (c, CH2), 64.86 (c, CH2), 65.52 (c, CH2), 68.44 (c, CH2), 75.80 (c, C(CH2O)4), 98.56 (c, OCH2O), 136.68 (c, Сpyr), 142.28 (c, Сpyr), 143.09 (c, Сpyr), 145.10 (c, Сpyr), 150.10 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 797.7 [М-2Cl]2+. Вычислено для [C89H152Cl2N8O12]2+ - 797.6.
Пример 2. Получение 1,3-бис(8-диметил(додецил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5, 6-с]пиридин)-9-окси)-2,2-бис((8-диметил(додецил)аммоний)метил) - 1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9-окси)метил)пропан тетрахлорида (I-2)
Синтезировали и разрабатывали аналогично соединению I-1. Использовали 0.15 г (0.2 ммоль) соединения 5а и 0.18 мл (0.8 ммоль) N,N-диметилдодециламина. Выход 0.12 г (34%); белое кристаллическое вещество; т.пл. 92 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 0.86 (т, 12Н, 3JHH = 6.7 Гц, 4СН3C11H22), 1.07-1.33 (м, 72Н, 36СН2), 1.61-1.71 (м, 8Н, 4СН2), 3.41 (с, 24Н, 8СН3), 3.71-3.75 (м, 8Н, 4СН2) , 4.89 (с, 8Н, 4СН2), 5.04 (с, 8Н, 4СН2), 5.36 (с, 8Н, 4СН2), 5.56 (с, 8Н, 4СН2), 8.07 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 14.24 (с, СН3), 22.73 (с, CH2), 22.79 (с, СН2), 26.33 (с, СН2), 29.28 (c, CH2), 29.44 (c, CH2), 29.59 (с, СН2), 29.63 (c, CH2), 29.73 (с, СН2), 32.01 (с, СН2), 47.41 (с, C(CH2O)4), 50.63 (с, CH3N+), 62.34 (c, CH2), 64.92 (c, CH2), 65.49 (c, CH2), 68.35 (c, CH2), 75.76 (c, C(CH2O)4), 98.49 (c, OCH2O), 136.64 (c, Сpyr), 142.24 (c, Сpyr), 143.09 (c, Сpyr), 145.15 (c, Сpyr), 150.16 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 853.7 [М-2Cl]2+. Вычислено для [C97H168Cl2N8O12]2+ - 853.6.
Пример 3. Получение N,N'-((((2,2-бис(((8-((диметил(децил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминия) тетрахлорида (I-3)
Получение 9,9'-((2,2-бис(((3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил) пропан-1,3-диил)бис(окси))бис(3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 4б):
К раствору ацеталя 2б (5.00 г, 25.6 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.60 г, 25.6 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 3 (4.82 г, 6.4 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 28% (1.53 г); желтое кристаллическое вещество; т.пл. 97 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.37 (д, 12Н, 3JHH = 5.1 Гц, 4СН3), 2.52 (с, 12Н, 4СН3), 4.31, 4.37 (AB-система, 8H, 2JHH = 8.3 Гц, 4CH2), 4.71, 5.20 (AB-система, 8H, 2JHH = 15 Гц, 4CH2), 4.77, 4.93 (AB-система, 8H, 2JHH = 14.5 Гц, 4CH2), 5.06-5.11 (м, 4H, CH3CH), 8.26 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 20.17 (c, CH3), 20.21 (c, CH3), 20.29 (c, CH3), 20.37 (c, CH3), 46.81 (c, C(CH2O)4), 63.03 (c, CH2O), 63.22 (c, CH2O), 63.42 (c, CH2O), 63.59 (c, CH2O), 66.47 (c, CH2O), 66.51 (c, CH2O), 73.49 (c, C(CH2O)4), 104.07 (c, CHCH3), 104.22 (c, CHCH3), 104.37 (c, CHCH3), 104.42 (c, CHCH3), 134.34 (c, Сpyr), 140.54 (c, Сpyr), 140.56 (c, Сpyr), 143.02 (c, Сpyr), 143.03 (c, Сpyr), 149.83 (c, Сpyr), 151.19 (c, Сpyr), 151.24 (c, Сpyr), 151.30 (c, Сpyr), 151.37 (c, Сpyr).
Получение 9,9'-((2,2-бис(((8-(хлорметил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил) окси)метил)пропан-1,3-диил)бис(окси))бис(8-(хлорметил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 5б):
1.48 г (1.8 ммоль) соединения 4б растворяли в 25 мл хлороформа и добавляли 1.63 г (7.2 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 1 часа. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 30% (0.53 г); желтое кристаллическое вещество; т.пл. 92-93 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.37 (д, 12Н, 3JHH= 5.2 Гц, 4СН3), 4.57-4.73 (м, 20H, 10CH2), 4.80, 4.97 (AB-система, 8H, 2JHH = 14.7 Гц, 4CH2), 5.07-5.13 (м, 4H, CH3CH), 5.21-5.27 (м, 4H, 2CH2), 8.23 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 19.80 (c, CH3), 19.88 (c, CH3), 19.97 (c, CH3), 20.06 (c, CH3), 42.29 (c, CH2Cl), 47.22 (c, C(CH2O)4), 62.30 (c, CH2O), 62.58 (c, CH2O), 62.38 (c, CH2O), 63.06 (c, CH2O), 66.06 (c, CH2O), 74.78 (c, C(CH2O)4), 103.60 (c, CHCH3), 103.75 (c, CHCH3), 103.92 (c, CHCH3), 104.10 (c, CHCH3), 137.35 (c, Сpyr), 142.04 (c, Сpyr), 142.06 (c, Сpyr), 144.02 (c, Сpyr), 144.04 (c, Сpyr), 149.32 (c, Сpyr), 149.37 (c, Сpyr), 149.42 (c, Сpyr), 149.49 (c, Сpyr), 150.04 (c, Сpyr).
Получение N,N'-((((2,2-бис(((8-((диметил(децил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминия) тетрахлорида (I-3):
0.25 г (0.3 ммоль) соединения 5б растворяли в 5 мл ДМФА и добавляли 0.24 мл (1.2 ммоль) N,N-диметилдециламина. Растворитель удаляли в вакууме. Осадок очищали с помощью жидкостной хроматографии гидрофильного взаимодействия на колонке HILIC (элюент: ацетонитрил-вода). Выход 0.28 г (54%); желтое кристаллическое вещество; т.пл. 103 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 0.87 (т, 12Н, 3JHH = 6.9 Гц, 4СН3С9H18), 1.04-1.30 (м, 56Н, 28СН2), 1.36 (д, 12Н, 3JHH = 5.1 Гц, 4СН3), 1.58-1.72 (м, 8H, 4CH2), 3.39 (с, 12Н, 4CH3N+), 3.42 (с, 12Н, 4CH3N+), 3.65-3.90 (с, 8Н, 4CH2N+), 4.68-5.81 (м, 28Н, 4CH2O+4CH2N++4CH3CH) 4.90 (с, 8Н, 4СН2О), 8.13 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 14.10 (c, CH3), 14.13 (c, CH3), 20.55 (c, CH2), 20.61 (c, CH2), 22.56 (c, CH2), 22.64 (c, CH2), 22.66 (c, CH2), 26.20 (c, CH2), 29.11 (c, CH2), 29.26 (c, CH2), 29.27 (c, CH2), 29.40 (c, CH2), 29.49 (c, CH2), 47.17 (с, C(CH2O)4), 50.05 (с, CH3N+), 50.28 (с, CH3N+), 50.42 (с, CH3N+), 50.57 (с, CH3N+), 61.97 (c, CH2), 62.00 (c, CH2), 63.88 (c, CH2), 64.05 (c, CH2), 64.86 (c, CH2), 66.87 (c, CH2), 76.13 (c, C(CH2O)4), 104.55 (c, CHCH3), 104.68 (c, CHCH3), 136.66 (c, Сpyr), 136.68 (c, Сpyr), 136.71 (c, Сpyr), 136.73 (c, Сpyr), 142.51 (c, Сpyr), 142.86 (c, Сpyr), 143.01 (c, Сpyr), 143.12 (c, Сpyr), 144.78 (c, Сpyr), 144.92 (c, Сpyr), 149.92 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 539.3 [М-3Cl]3+. Вычислено для [C93H160ClN8O12]3+ - 538.7.
Пример 4. Получение N,N'-((((2,2-бис(((8-((диметил(додецил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминия) тетрахлорида (I-4)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.25 г (0.3 ммоль) соединения 5б и 0.28 мл (1.2 ммоль) N,N-диметилдодециламина. Выход 0.36 г (65%); желтое кристаллическое вещество; т.пл. 108 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 0.87 (т, 12Н, 3JHH = 6.8 Гц, 4СН3С11H22), 1.04-1.31 (м, 72Н, 36СН2), 1.36 (д, 12Н, 3JHH = 5.1 Гц, 4СН3), 1.60-1.71 (м, 8H, 4CH2), 3.40 (с, 12Н, 4CH3N+), 3.42 (с, 12Н, 4CH3N+), 3.66-3.88 (м, 8Н, 4CH2N+), 4.64-5.79 (м, 28Н, 3CH2O+4CH2N++CH3CH), 8.13 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 14.16 (c, CH3), 20.57 (c, CH2), 20.63 (c, CH2), 22.61 (c, CH2), 22.71 (c, CH2), 26.24 (c, CH2), 29.16 (c, CH2), 29.36 (c, CH2), 29.50 (c, CH2), 29.54 (c, CH2), 29.65(c, CH2), 31.93 (c, CH2), 47.22 (с, C(CH2O)4), 50.07 (с, CH3N+), 50.29 (с, CH3N+), 50.44 (с, CH3N+), 50.60 (с, CH3N+), 61.89 (c, CH2), 62.07 (c, CH2), 63.92 (c, CH2), 64.08 (c, CH2), 64.89 (c, CH2), 66.91 (c, CH2), 76.14 (c, C(CH2O)4), 104.55 (c, CHCH3), 104.71 (c, CHCH3), 136.68 (c, Сpyr), 136.75 (c, Сpyr), 142.54 (c, Сpyr), 143.04 (c, Сpyr), 144.81 (c, Сpyr), 144.96 (c, Сpyr), 149.98 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 423.6 [М-4Cl]4+. Вычислено для [C101H176N8O12]4+ - 423.3.
Пример 5. Получение N,N'-((((2,2-бис(((2-((диметил(децил)аммонио)метил)-4,5-бис(гидроксиметил)пиридин-3-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) тетрахлорида (I-5)
К 0.10 г (0.1 ммоль) соединения I-3 в смеси 15 мл воды и 5 мл этилового спирта добавляли 0.1 мл концентрированной HCl. Реакционную смесь перемешивали в течение 6 часов при температуре 70 оС. Растворитель отгоняли в вакууме. Выход 0.10 г (~100%); белое кристаллическое вещество; т.пл. 151-153 (разл.) °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д.: 0.91 (т, 12Н, 3JHH = 6.4 Гц, 4СН3С9H18), 1.10-1.41 (м, 56Н, 28СН2), 1.67-1.88 (м, 8H, 4CH2), 3.16 (с, 24Н, 4(CH3)2N+), 3.46-3.53 (с, 8Н, 4CH2N+), 4.82 (с, 8H, 4CH2), 4.88 (с, 8H, 4CH2), 4.91 (с, 8H, 4CH2), 5.04 (с, 8H, 4CH2), 8.63 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д.: 14.49 (c, CH3), 23.74 (c, CH2), 23.77 (c, CH2), 27.37 (c, CH2), 30.18 (c, CH2), 30.51 (c, CH2), 30.65 (c, CH2), 30.67 (c, CH2), 30.70 (c, CH2), 33.10 (c, CH2), 48.05 (с, C(CH2O)4), 51.83 (с, CH3N+), 55.54 (с, CH2), 60.32 (c, CH2), 63.11 (c, CH2), 67.37 (c, CH2), 79.19 (c, C(CH2O)4), 141.29 (c, Сpyr), 143.52 (c, Сpyr), 143.76 (c, Сpyr), 145.98 (c, Сpyr), 154.20 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 369.6 [М-3-4Cl]4+. Вычислено для [C85H152N8O12]4+ - 369.3.
Пример 6. Получение N,N'-((((2,2-бис(((2-((диметил(додецил)аммонио)метил)-4,5-бис(гидроксиметил)пиридин-3-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) тетрахлорида (I-6)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-4. Выход 0.10 г (~100%); белое кристаллическое вещество; т.пл. 149-151 (разл.) °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д.: 0.91 (т, 12Н, 3JHH = 6.6 Гц, 4СН3С11H22), 1.09-1.44 (м, 72Н, 36СН2), 1.70-1.82 (с, 8H, 4CH2), 3.15 (с, 24Н, 4(CH3)2N+), 3.42-3.51 (м, 8Н, 4CH2N+), 4.80 (с, 8H, 4CH2), 4.87 (с, 8H, 4CH2), 4.90 (с, 8H, 4CH2), 5.03 (с, 8H, 4CH2), 8.61 (с, 4Н, 4СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д.: 14.45 (c, CH3), 23.68 (c, CH2), 23.74 (c, CH2), 27.34 (c, CH2), 30.15 (c, CH2), 30.50 (c, CH2), 30.66 (c, CH2), 30.78 (c, CH2), 30.81 (c, CH2), 33.08 (c, CH2), 48.01 (с, C(CH2O)4), 51.73 (с, CH3N+), 55.47 (c, CH2), 60.28 (c, CH2), 63.12 (c, CH2), 67.29 (c, CH2), 79.14 (c, C(CH2O)4), 140.95 (c, Сpyr), 143.10 (c, Сpyr), 144.07 (c, Сpyr), 146.27 (c, Сpyr), 154.08 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 397.5 [М-4Cl]4+. Вычислено для [C93H168N8O12]4+ - 397.3.
Пример 7. Получение 1-метил-2,2-бис(8-((диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)метил)-3-(8 ((диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)пропан трихлорида (I-7)
Получение ,9'-((2-метил-2-(((8-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)пропан -1,3-диил)бис(окси))бис(8-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (7а):
К раствору ацеталя 2а (4.56 г, 25.2 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.50 г, 25.2 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 6 (5.00 г, 8.4 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 1.84 г (36%); желтое кристаллическое вещество; т.пл. 76 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 1.60 (с, 3Н, СН3C), 2.50 (с, 9Н, 3СН3), 3.96 (с, 6Н, 3СН2О), 4.86 (с, 6Н, 3СН2О), 4.96 (с, 6Н, 3СН2О), 4.99 (с, 6Н, 3СН2О), 8.08 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3) δ, м.д: 18.03 (с, СН3), 19.81 (с, СН3), 42.41 (с, C(CH2O)3), 64.95 (c, CH2O), 68.08 (c, CH2O), 76.18 (c, C(CH2O)3), 98.10 (c, OCH2O), 134.17 (c, Сpyr), 140.61 (c, Сpyr), 142.91 (c, Сpyr), 149.80 (c, Сpyr), 151.56 (c, Сpyr).
Получение 9,9'-((2,2-бис(((8-(хлорметил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)пропан-1,3-диил)бис(окси))бис(8-(хлорметил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (8а):
1.80 г (2.9 ммоль) соединения 7а растворяли в 25 мл хлороформа и добавляли 2.01 г (8.7 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 2 часов. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 29% (0.61 г); белое кристаллическое вещество; т.пл. 110-112 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 1.68 (с, 3Н, СН3), 4.20 (с, 6Н, 3СН2), 4.69 (с, 6Н, 3СН2), 4.90 (с, 6Н, 3СН2), 4.98 (с, 6Н, 3СН2), 5.00 (с, 6Н, 3СН2), 8.20 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3) δ, м.д.: 17.69 (с, СН3), 42.14 (с, СН2Cl), 42.62 (с, C(CH2O)3), 64.50 (c, CH2O), 67.75 (c, CH2O), 77.65 (c, CH2O), 97.84 (c, OCH2O), 137.21 (c, Сpyr), 142.07 (c, Сpyr), 143.75 (c, Сpyr), 149.46 (c, Сpyr), 150.21 (c, Сpyr).
Получение 1-метил-2,2-бис(8-((диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)метил)-3-(8((диметил(децил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)пропан трихлорида (I-7):
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.15 г (0.2 ммоль) соединения 8а и 0.15 мл (0.6 ммоль) N,N-диметилдециламина. Выход 0.18 г (71%); желтое кристаллическое вещество; т.пл. 94-96 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 0.87 (т, 9Н, 3JHH = 6.9 Гц, 3СН3C9H18), 1.20-1.30 (м, 42Н, 21CH3), 1.69-1.79 (м, 6H), 1.89 (с, 3H, CH3C), 3.48 (с, 18Н, 3(СН3)2N+), 3.77-3.81 (м, 6Н, 3СН2N+), 4.39 (с, 6Н, 3СН2), 4.91 (с, 6Н, СН2), 5.05 (с, 6Н, 3СН2), 5.13 (с, 6Н, 3СН2), 5.37 (с, 6Н, 3СН2О), 8.13 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 14.21 (с, СН3), 18.42 (с, СН3C), 22.75 (с, СН2), 22.85 (с, СН2), 26.33 (с, СН2), 29.24 (с, СН2), 29.35 (с, СН2), 29.52 (с, СН2), 31.94 (с, СН2), 42.83 (с, C(CH2O)3), 51.34 (с, СН3N+), 61.89 (c, CH2), 64.82 (c, CH2), 65.02 (c, CH2), 68.33 (c, CH2), 78.49 (c, C(CH2O)3), 98.44 (c, OCH2O), 137.11 (c, Сpyr), 142.70 (c, Сpyr), 142.90 (c, Сpyr), 144.38 (c, Сpyr), 150.55 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 387.6 [М-3Cl]3+. Вычислено для [C68H117N6O9]3+ - 387.3.
Пример 8. Получение 1-метил-2,2-бис(8-((диметил(додецил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)метил)-3-(8 ((диметил(додецил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)пропан трихлорида (I-8)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.15 г (0.2 ммоль) соединения 8а и 0.17 мл (0.6 ммоль) N,N-диметилдодециламина. Выход 0.23 г (85%); желтое кристаллическое вещество; т.пл. 103 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 0.87 (т, 9Н, 3JHH = 6.8 Гц, 3СН3C11H22), 1.18-1.35 (м, 54H, 28CH2), 1.69-1.79 (м, 6H), 1.89 (с, 3H, CH3C), 3.48 (с, 18Н, 3(СН3)2N+), 3.79-3.81 (м, 6Н, 3СН2N+), 3.81 (м, 6Н,3СН2), 4.39 (с, 6Н, 3СН2), 4.91 (с, 6Н, 3СН2), 5.05 (с, 6Н, 3СН2О, 5.13 (с, 6Н, 3СН2), 5.37 (с, 6Н, 3СН2), 8.13 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 14.23 (с, СН3), 18.43 (с, СН3C), 22.79 (с, СН2), 22.87 (с, СН2), 26.35 (с, СН2), 29.27 (с, СН2), 29.44 (с, СН2), 29.56 (с, СН2), 29.58 (с, СН2), 29.72 (с, СН2), 32.00 (с, СН2), 42.85 (с, C(CH2O)3), 51.35 (с, СН3N+), 61.93 (c, CH2), 64.82 (c, CH2), 65.05 (c, CH2), 68.36 (c, CH2O), 78.51 (c, C(CH2O)3), 98.46 (c, OCH2O), 137.10 (c, Сpyr), 142.69 (c, Сpyr), 142.91 (c, Сpyr), 144.43(c, Сpyr), 150.58 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 415.6 [М-3Cl]3+. Вычислено для [C74H129N6O9]3+ - 415.3.
Пример 9. Получение 1-метил-2,2-бис(8-((диметил(тетрадецил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)метил)-3-(8-((диметил(тетрадецил)аммоний)метил)-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-окси)пропан трихлорида (I-9)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.15 г (0.2 ммоль) соединения 8а и 0.19 мл (0.6 ммоль) N,N-диметилтетрадециламина. Выход 0.11 г (38%); желтое кристаллическое вещество; т.пл. 86-87 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 0.87 (т, 9Н, 3JHH = 6.8 Гц, 3СН3C13H26), 1.19-1.38 (м, 66Н, 22CH3), 1.70-1.79 (м, 6Н), 1.89 (с, 3H, CH3C), 3.49 (с, 18Н, 3(СН3)2N+), 3.78-3.80 (м, 6Н, 3СН2N+), 4.39 (с, 6Н, 3СН2), 4.91 (с, 6Н, 3СН2), 5.05 (с, 6Н, 3СН2О), 5.13 (с, 6Н, 3СН2), 5.38 (с, 6Н, 3СН2), 8.13 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 14.24 (с, СН3), 18.45 (с, СН2), 22.80 (с, СН2), 22.89 (с, СН2), 26.37 (с, СН2), 29.29 (с, СН2), 29.47 (с, СН2), 29.60 (с, СН2), 29.78 (с, СН2), 32.03 (с, СН2), 42.87 (с, C(CH2O)3), 51.38 (с, СН3N+), 61.95 (c, CH2), 64.84 (c, CH2), 65.06 (c, CH2), 68.36 (c, CH2), 78.52 (c, C(CH2O)3), 98.47 (c, OCH2O), 137.11 (c, Сpyr), 142.69 (c, Сpyr), 142.92 (c, Сpyr), 144.42 (c, Сpyr), 150.59 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 443.6 [М-3Cl]3+. Вычислено для [C80H141N6O9]3+ - 443.4.
Пример 10. Получение N,N'-((((2-(((8-((диметил(децил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)-2-метилпропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминия) трихлорида (I-10)
Получение 9,9'-((2-(((3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)-2- метилпропан-1,3-диил)бис(окси))бис(3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (7б):
К раствору ацеталя 2б (5.00 г, 25.5 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.60 г, 25.5 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 6 (4.97 г, 8.5 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 1.12 г (20%); желтое кристаллическое вещество; т.пл. 78 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.40 (д, 9Н, 3JHH = 5.2 Гц, 3СН3), 1.61 (с, 9Н, 3СН3CH), 2.50 (с, 9Н, 3СН3), 3.92-4.03 (м, 6Н, 3СН2), 4.73, 5.16 (AB-система, 6H, 2JHH = 15.1 Гц, 3CH2), 4.75, 4.93 (AB-система, 6H, 2JHH = 14.6 Гц, 3CH2), 5.11 (кв, 3Н, 3JHH = 5.2 Гц, , CH3CH), 8.09 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 18.00 (с, СН3), 19.88 (с, СН3), 20.17 (с, СН3), 20.23 (с, СН3), 20.28 (с, СН3), 42.42 (с, C(CH2O)3), 63.12 (c, CH2O), 63.28 (c, CH2O), 63.43 (c, CH2O), 66.37 (c, CH2O), 76.26 (c, C(CH2O)3), 76.28 (c, C(CH2O)3), 76.31 (c, C(CH2O)3), 104.06 (с, СНСН3), 134.00 (c, Сpyr), 134.02 (c, Сpyr), 134.03 (c, Сpyr), 140.47 (c, Сpyr), 140.48 (c, Сpyr), 140.50 (c, Сpyr), 142.91 (c, Сpyr), 142.93 (c, Сpyr), 142.94 (c, Сpyr), 149.79 (c, Сpyr), 151.71 (c, Сpyr), 151.75 (c, Сpyr), 151.78 (c, Сpyr).
Получение 9,9'-((2-(((8-(хлорметил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил )-2-метилпропан-1,3-диил)бис(окси))бис(8-(хлорметил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (8б):
1.08 г (1.7 ммоль) соединения 7б растворяли в 25 мл хлороформа и добавляли 1.15 г (5.1 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 2 часов. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 36% (0.46 г); желтое кристаллическое вещество; т.пл. 95 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.40 (д, 9Н, 3JHH = 5.2 Гц, 3СН3), 1.68 (с, 3Н, СН3CH), 4.16-4.27 (м, 6Н, 3CH2), 4.67-4.72 (м, 9H, 3CH2+3HCH), 4.78, 4.98 (AB-система, 6H, 2JHH = 14.8 Гц, 3CH2), 5.12-5.15 (м, CH3CH), 5.16-5.20 (м, 3HCH), 8.21 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 17.68 (с, СН3), 19.83 (с, СН3), 19.89 (с, СН3), 19.95 (с, СН3), 42.17 (с, СН2Cl), 42.62 (с, C(CH2O)3), 62.45 (c, CH2O), 62.63 (c, CH2O), 62.82 (c, CH2O), 65.88 (c, CH2O), 77.75 (c, C(CH2O)3), 77.77 (c, C(CH2O)3), 77.79 (c, C(CH2O)3), 103.51 (с, СНСН3), 103.62 (с, СНСН3), 103.63 (с, СНСН3), 103.74 (с, СНСН3), 137.07 (c, Сpyr), 141.99 (c, Сpyr), 142.01 (c, Сpyr), 143.77 (c, Сpyr), 149.54 (c, Сpyr), 149.58 (c, Сpyr),149.62 (c, Сpyr), 150.19 (c, Сpyr), 150.21 (c, Сpyr), 150.22 (c, Сpyr).
Получение N,N'-((((2-(((8-((диметил(децил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)-2-метилпропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминия) трихлорида (I-10):
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.20 г (0.3 ммоль) соединения 8б и 0.19 мл (0.9 ммоль) N,N-диметилдециламина. Выход 0.24 г (61%); желтое кристаллическое вещество; т.пл. 84 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 0.85 (т, 9Н, 3JHH = 6.7 Гц, 3СН3C9H18), 1.13-1.29 (м, 42H, 21CH2), 1.39 (д, 9Н, 3JHH = 4.7 Гц, 3СН3CH), 1.63-1.74 (м, 6H, 3CH2), 1.77 (с, 3H, CH3C), 3.43-3.46 (м, 18H, 3(CH3)2N+), 3.66-3.86 (м, 6H, 3CH2N+), 4.25-4.54 (м, 6H, 3CH2), 4.84-5.54 (м, 21H, 3CH2 +3CH3CH), 8.12 (с, 3Н, 3СНpyr), 8.13 (с, 3Н, 3СНpyr), 8.15 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 14.21 (с, СН3), 18.30 (с, СН3), 20.40 (с, СН3), 20.54 (с, СН3), 20.70 (с, СН3), 20.83 (с, СН3), 22.75 (с, СН2), 26.33 (с, СН2), 29.19 (с, СН2), 29.24 (с, СН2), 29.35 (с, СН2), 29.52 (с, СН2), 31.94 (с, СН2), 42.74 (с, C(CH2O)3), 51.16 (с, CH3N+), 51.26 (с, CH3N+), 51.32 (с, CH3N+), 51.41 (с, CH3N+), 61.96 (c, CH2), 63.23 (с, CH2), 63.66 (с, CH2), 63.83 (с, CH2), 64.56 (с, CH2), 64.79 (с, CH2), 65.12 (с, CH2), 66.69(с, CH2), 66.79 (c, CH2), 67.29 (с, CH2), 67.41 (c, CH2), 78.51 (c, C(CH2O)3), 78.59 (c, C(CH2O)3), 104.30 (с, СНСН3), 104.54 (с, СНСН3), 104.93 (с, СНСН3), 105.22 (с, СНСН3), 136.80 (c, Сpyr), 136.98 (c, Сpyr), 137.02 (c, Сpyr), 137.06 (c, Сpyr), 142.76 (c, Сpyr), 142.83 (c, Сpyr), 142.94 (c, Сpyr), 143.06 (c, Сpyr), 144.34 (c, Сpyr), 144.41 (c, Сpyr), 144.61 (c, Сpyr), 145.03 (c, Сpyr), 150.27 (c, Сpyr), 150.36 (c, Сpyr), 150.54 (c, Сpyr), 150.60 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 620.2 [М-2Cl]2+. Вычислено для [C71H123ClN6O9]2+ - 619.5.
Пример 11. Получение N,N'-((((2-(((8-((диметил(додецил)аммонио)метил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ил)окси)метил)-2-метилпропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c ]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминия) трихлорид (I-11)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.20 г (0.3 ммоль) соединения 8б и 0.22 мл (0.9 ммоль) N,N-диметилдодециламина. Выход 0.29 г (69%); желтое кристаллическое вещество; т.пл. 100 °С. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 0.86 (т, 9Н, 3JHH = 6.8 Гц, 3СН3C11H22), 1.15-1.30 (м, 54H, 27CH2), 1.39 (д, 9Н, 3JHH = 5.0 Гц, 3СН3CH), 1.66-1.75 (м, 6H, 3CH2), 1.78 (с, 3H, CH3C), 3.43-3.48 (м, 18H, 3(CH3)2N+), 3.67-3.87 (м, 6H, 3CH2N+), 4.25-4.53 (м, 6H, 3CH2), 4.86-5.53 (м, 21H, 3CH2 +3CH3CH), 8.13 (с, 3Н, 3СНpyr), 8.14 (с, 3Н, 3СНpyr), 8.16 (с, 3Н, 3СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 14.22 (с, СН3), 18.29 (с, СН3), 20.38 (с, СН3), 20.52 (с, СН3), 20.68 (с, СН3), 20.82 (с, СН3), 22.77 (с, СН2), 26.32 (с, СН2), 29.18 (с, СН2), 29.25 (с, СН2), 29.42 (с, СН2), 29.55 (с, СН2), 31.98 (с, СН2), 42.72 (с, C(CH2O)3), 42.81 (с, C(CH2O)3), 51.17 (с, CH3N+), 51.25 (с, CH3N+), 51.31 (с, CH3N+), 51.39 (с, CH3N+), 61.92 (c, CH2), 63.21 (с, CH2), 63.62 (с, CH2), 63.81 (с, CH2), 64.55 (с, CH2), 64.78 (с, CH2), 66.69(с, CH2), 66.79 (c, CH2), 67.27 (с, CH2), 67.39 (c, CH2), 78.50 (c, C(CH2O)3), 78.53 (c, C(CH2O)3), 78.99 (c, C(CH2O)3), 104.29 (с, СНСН3), 104.54 (с, СНСН3), 104.92 (с, СНСН3), 105.21 (с, СНСН3), 136.81 (c, Сpyr), 136.98 (c, Сpyr), 137.01 (c, Сpyr), 137.06 (c, Сpyr), 142.76 (c, Сpyr), 142.84 (c, Сpyr), 142.94 (c, Сpyr), 143.04 (c, Сpyr), 144.33 (c, Сpyr), 144.60 (c, Сpyr), 144.98 (c, Сpyr), 150.26 (c, Сpyr), 150.35 (c, Сpyr), 150.52 (c, Сpyr), 150.58 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 661.7 [М-2Cl]2+. Вычислено для [C77H135ClN6O9]2+ - 661.5.
Пример 12. Получение N,N'-((((2-(((2-((диметил(децил)аммонио)метил)-4,5-бис(гидроксиметил)пиридин-3-ил)окси)метил)-2-метилпропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) трихлорида (I-12)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.06 г (0.1 ммоль) соединения I-10. Выход 0.06 г (~100%); белое кристаллическое вещество; т.пл. 115-117 °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д.: 0.91 (т, 9H, 3JHH =5.7 Гц, 3СН3C9H18), 1.21-1.36 (м, 42H, 21CH2), 1.77-1.87 (м, 6H, 3CH2), 2.00 (c, 3H, CH3), 3.09 (с, 18H, 3(CH3)2N+), 3.40-3.46 (м, 6H, 3CH2N+), 4.60 (с, 6Н, 3СН2), 4.65 (с, 6Н, 3СН2), 4.84 (с, 6Н, 3СН2), 4.90 (с, 6Н, 3СН2), 8.62 (с, 3H, 3CHpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д.: 14.48 (с, СН3), 18.29 (с, СН3), 23.76 (с, CH2), 27.33 (с, CH2), 30.14 (с, CH2), 30.49 (с, CH2), 30.62 (с, CH2), 30.65 (с, CH2), 33.09 (с, CH2), 43.85 (с, C(CH2O)3), 51.73 (с, CH3N+), 55.39 (с, CH2), 60.23 (с, CH2), 63.10 (с, CH2), 67.27 (с, CH2), 81.33 (с, C(CH2O)3), 141.52 (c, Сpyr), 143.38 (c, Сpyr), 143.54 (c, Сpyr), 146.23 (c, Сpyr), 154.97 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 375.3 [М-3Cl]3+. Вычислено для [C65H117N6O9]3+ - 375.3.
Пример 13. Получение N,N'-((((2-(((2-((диметил(додецил)аммонио)метил)-4,5-бис(гидроксиметил)пиридин-3-ил)окси)метил)-2-метилпропан-1,3диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) трихлорида (I-13)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-11. Выход 0.10 г (~100%); белое кристаллическое вещество; т.пл. 121-123 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.85 (т, 9H, 3JHH =6.6 Гц, 3СН3C11H22), 1.02-1.35 (м, 54H, 27CH2), 1.64-1.70 (м, 6H, 3CH2), 1.83 (c, 3H, CH3), 3.08 (c, 18H, 3(CH3)2N+), 3.39-3.47 (м, 6H, 3CH2N+), 4.51 (c, 6H, 3CH2), 4.60 (c, 6H, 3CH2), 4.69 (c, 6H, 3CH2), 4.75 (c, 6H, 3CH2), 8.52 (с, 3H, 3CHpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 14.03 (с, СН3), 18.75 (с, СН3), 21.89 (с, CH2), 22.18 (с, CH2), 25.74 (с, CH2), 28.46 (с, CH2), 28.82 (с, CH2), 28.94 (с, CH2), 29.03 (с, CH2), 29.13 (с, CH2), 29.16 (с, CH2), 31.40 (с, CH2), 42.00 (с, C(CH2O)3), 50.30 (с, CH3N+), 53.24 (с, CH2), 58.16 (с, CH2), 61.37 (с, CH2), 64.82 (с, CH2), 80.05 (с, C(CH2O)3), 139.88 (c, Сpyr), 141.04 (c, Сpyr), 141.99 (c, Сpyr), 144.13 (c, Сpyr), 152.38 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 403.4 [М-3Cl]3+. Вычислено для [C71H129N6O9]3+ - 403.3.
Пример 14. Получение N,N'-(((((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-14)
Получение 9,9'-(((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(8-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 10):
К раствору ацеталя 2а (4.86 г, 26.8 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.72 г, 26.8 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 9 (6.50 г, 13.4 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 3.80 г (56%); желтое кристаллическое вещество; т.пл. 167 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 1.48 (с, 6Н, (СН3)2C), 2.51 (с, 6Н, 2СН3), 3.90 (с, 4Н, 2СН2), 4.11 (с, 4Н, 2СН2), 4.86 (с, 4Н, 2СН2), 4.98 (с, 4Н, 2СН2), 4.99 (с, 4Н, 2СН2), 8.08 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д.: 19.43 (с, СН3), 23.89 (с, СН3), 39.80 (с, C(CH2O)3), 62.17 (с, СН2O), 64.91 (с, СН2O), 68.01 (с, СН2O), 72.73 (c, C(CH2O)4), 98.11 (c, OCH2O), 98.75 (c, (CH3)2C), 134.24 (c, Сpyr), 140.99 (c, Сpyr), 142.71 (c, Сpyr), 149.76 (c, Сpyr), 151.66 (c, Сpyr).
Получение 9,9'-(((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(8-(хлорметил)-1,5-дигидро- [1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 11):
3.7 г (7.4 ммоль) соединения 10 растворяли в 25 мл хлороформа и добавляли 3.4 г (14.8 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 1 часа. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 30% (1.26 г); желтое кристаллическое вещество; т.пл. 83-86 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д.: 1.51 (с, 6Н, (СН3)2C), 4.08 (с, 4Н, 2СН2), 4.18 (с, 4Н, 2СН2), 4.70 (с, 4Н, 2СН2), 4.90 (с, 4Н, 2СН2), 4.99 (с, 4Н, 2СН2), 5.00 (с, 4Н, 2СН2), 8.20 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3) δ, м.д.: 23.87 (с, СН3), 39.96 (с, C(CH2O), 41.96 (с, СН2Cl), 61.90 (c, CH2O), 64.48 (c, CH2O), 67.71 (c, CH2O), 74.37 (c, CH2O), 97.86 (c, OCH2O), 98.88 (c, (CH3)2C), 137.18 (c, Сpyr), 142.26 (c, Сpyr), 143.64 (c, Сpyr), 149.58 (c, Сpyr), 150.15 (c, Сpyr).
Получение N,N'-(((((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-14):
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.40 г (0.7 ммоль) соединения 11 и 0.33 мл (1.4 ммоль) N,N-диметилдециламина. Выход 0.33 г (50%); желтое кристаллическое вещество; т.пл. 70-73 oC. Спектр ЯМР 1Н (400 МГц ДМСО-d6), δ, м.д.: 0.85 (т, 6H, 3JHH = 6.8 Гц, 2CH3C9H18), 1.18-1.32 (м, 32H, 16CH2), 1.45 (с, 6H, 2CH3), 1.71-1.85 (м, 4H, 2CH2), 3.13 (с, 12H, 2(CH3)2N+), 3.40-3.46 (м, 4H, 2CH2N+), 4.07 (с, 4H, 2CH2), 4.14 (с, 4H, 2CH2), 4.67 (с, 4H, 2CH2), 4.96 (с, 4H, 2CH2), 4.99 (с, 4H, 2CH2), 5.02 (с, 4H, 2CH2), 8.41 (с, 2H, 2CHpyr).Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 13.95 (с, СН3), 21.85 (с, СН2), 22.10 (с, СН2), 23.82 (с, СН2), 25.75 (с, СН2), 28.48 (с, СН2), 28.66 (с, СН2), 28.79 (с, СН2), 28.90 (с, СН2), 31.29 (с, СН2), 50.48 (с, C(CH2O)4), 60.85 (с, СН2), 61.07 (с, СН2), 64.06 (с, СН2), 64.47 (с, СН2), 67.17 (с, СН2), 74.43 (с, СН2O)4), 97.41 (с, C(CH3)2), 98.16 (c, OCH2O), 138.32 (c, Сpyr), 142.31 (c, Сpyr), 142.52 (c, Сpyr), 149.91 (c, Сpyr), 151.36 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 435.6 [М-2Cl]2+. Вычислено для [C50H86N4O8]2+ - 435.3.
Пример 15. Получение N,N'-(((((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) дихлорида (I-15)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.30 г (0.5 ммоль) соединения 11 и 0.28 мл (1.1 ммоль) N,N-диметилдодециламина. Выход 0.32 г (60%); желтое кристаллическое вещество; т.пл. 61-64 oC. Спектр ЯМР 1Н (400 МГц ДМСО-d6), δ, м.д.: 0.85 (т, 6H, 3JHH = 6.6 Гц, 2CH3C11H22), 1.20-1.30 (м, 40H, 20CH2), 1.45 (с, 6H, 2CH3), 1.72-1.80 (м, 4H, 2CH2), 3.13 (с, 12H, 2(CH3)2N+), 3.41-3.47 (м, 4H, 2CH2N+), 4.08 (с, 4H, 2CH2), 4.15 (с, 4H, 2CH2), 4.67 (с, 4H, 2CH2), 4.96 (с, 4H, 2CH2), 4.99 (с, 4H, 2CH2), 5.02 (с, 4H, 2CH2), 8.41 (с, 2H, 2CHpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 13.93 (с, СН3), 21.84 (с, СН2), 22.08, 23.81 (с, СН2), 25.74 (с, СН2), 28.47 (с, СН2), 28.70 (с, СН2), 28.78 (с, СН2), 28.93 (с, СН2), 29.01 (с, СН2), 31.28 (с, СН2), 50.45 (с, C(CH2O)4), 60.82 (с, СН2), 61.05 (с, СН2), 64.04 (с, СН2), 64.47 (с, СН2), 67.14 (с, СН2), 74.42 (с, СН2), 97.39 (с, C(CH3)2), 98.13 (c, OCH2O), 138.27 (c, Сpyr), 142.33 (c, Сpyr), 142.51 (c, Сpyr), 143.62 (c, Сpyr), 151.32 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 463.8 [М-2Cl]2+. Вычислено для [C54H94N4O8]2+ - 463.4.
Пример 16. Получение N,N'-(((((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилтетрадецил-1-аминий) дихлорида (I-16)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.40 г (0.7 ммоль) соединения 11 и 0.43 мл (1.4 ммоль) N,N-диметилтетрадециламина. Выход 0.45 г (60%); желтое кристаллическое вещество; т.пл. 57-60 oC. Спектр ЯМР 1Н (400 МГц ДМСО-d6), δ, м.д.: 0.85 (т, 6H, 3JHH = 6.7 Гц, 2CH3C13H26), 1.19-1.29 (м, 48H, 24CH2), 1.45 (с, 6H, 2CH3), 1.70-1.82 (м, 4H, 2CH2), 3.13 (с, 12H, 2(CH3)2N+), 3.40-3.47 (м, 4H, 2CH2N+), 4.04 (с, 4H, 2CH2), 4.14 (с, 4H, 2CH2), 4.67 (с, 4H, 2CH2), 4.96 (с, 4H, 2CH2), 4.99 (с, 4H, 2CH2), 5.02 (с, 4H, 2CH2), 8.41 (с, 2H, 2CHpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 13.98 (с, СН3), 21.87, 22.12, 23.83, 25.77 (с, СН2), 28.51 (с, СН2), 28.75 (с, СН2), 29.05 (с, СН2), 29.10 (с, СН2), 31.32 (с, СН2), 50.45 (с, СН2), 60.82 (с, СН2), 61.06 (с, СН2), 64.05 (с, СН2), 64.48, 67.16 (с, СН2), 74.42, 97.40 (с, C(CH3)2), 98.14 (c, OCH2O)), 138.30 (c, Сpyr), 142.35 (c, Сpyr), 142.53 (c, Сpyr), 143.65 (c, Сpyr), 151.34 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 491.3 [М-2Cl]2+. Вычислено для [C58H102N4O8]2+ - 491.4.
Пример 17. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-17)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-14. Выход 0.10 г (~100%); бежевое кристаллическое вещество; т.пл. 93-95 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.85 (с, 6H, 3JHH = 6.5 Гц, 2CH3C9H18), 1.17-1.40 (м, 28H, 14CH2), 1.73-1.84 (м, 4H, 2CH2), 3.09 (c, 12H, 2(CH3)2N+), 3.31-3.35 (м, 4H, 2CH2N+), 3.70 (с, 2H, CH2OH), 3.71 (c, 2H, CH2OH), 4.69 (с, 4Н, 2СН2), 4.95 (с, 4Н, 2СН2), 4.99 (с, 4Н, 2СН2), 5.04 (с, 4Н, 2СН2), 8.40 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 14.44 (с, СН3), 22.30 (с, СН2), 22.58 (с, СН2), 26.53 (с, СН2), 28.98 (с, СН2), 29.16 (с, СН2), 29.29 (с, СН2), 29.39 (с, СН2), 31.76 (с, СН2), 46.82 (с, C(CH2O)4), 50.79 (с, CH3N+), 59.38 (c, CH2), 61.42 (c, CH2), 64.28 (c, CH2), 64.41 (c, CH2), 67.77 (c, CH2), 73.68 (c, CH2), 98.00 (c, OCH2O), 139.00 (c, Сpyr), 142.90 (c, Сpyr), 143.40 (c, Сpyr), 144.24 (c, Сpyr), 150.38 (c, Сpyr), 152.38 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 415.5 [М-2Cl]2+. Вычислено для [C47H82N4O8]2+ - 415.3.
Пример 18. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) дихлорида (I-18)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-15. Выход 0.10 г (~100%); бежевое кристаллическое вещество; т.пл. 96 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.85 (с, 6H, 3JHH = 6.7 Гц, 2CH3C11H22), 1.17-1.33 (м, 36H, 18CH2), 1.73-1.84 (м, 4H, 2CH2), 3.09 (c, 12H, 2(CH3)2N+), 3.31-3.35 (м, 4H, 2CH2N+), 3.70 (с, 2H, CH2OH), 3.71 (с, 2H, CH2OH), 4.69 (с, 4Н, 2СН2), 4.95 (с, 4Н, 2СН2), 4.99 (с, 4Н, 2СН2), 5.04 (с, 4Н, 2СН2), 8.40 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 14.00 (с, СН3), 21.86 (с, СН2), 22.14 (с, СН2), 25.79 (с, СН2), 28.55 (c, CH2), 28.77 (с, СН2), 28.86 (с, СН2), 29.00 (с, СН2), 29.07 (с, СН2), 31.34 (с, СН2), 46.38 (с, C(CH2O)4), 50.35 (с, CH3N+), 58.94 (c, CH2), 60.98 (c, CH2), 63.86 (c, CH2), 63.96 (c, CH2), 67.33 (c, CH2), 73.24 (c, CH2), 97.56 (c, OCH2O), 138.56 (c, Сpyr), 142.46 (c, Сpyr), 142.96 (c, Сpyr), 143.81 (c, Сpyr), 151.94 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 443.4 [М-2Cl]2+. Вычислено для [C51H90N4O8]2+ - 443.4.
Пример 19. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилтетрадецил-1-аминий) дихлорида (I-19)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.7 ммоль) соединения I-16. Выход 0.10 г (~100%); бежевое кристаллическое вещество; т.пл. 99-101 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.85 (т, 6H, 3JHH = 6.1 Гц, 2CH3C13H26), 1.20-1.40 (м, 44H, 22CH2), 1.72-1.83 (м, 4H, 2CH2), 3.08 (c, 12H, 2(CH3)2N+), 3.33-3.34 (м, 4H, 2CH2N+), 3.70 (с, 2H, CH2OH), 3.71 (c, 2H, CH2OH), 4.68 (с, 4Н, 2СН2), 4.95 (с, 4Н, 2СН2), 5.00м (с, 4Н, 2СН2), 5.03 (с, 4Н, 2СН2), 8.40 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 14.46 (с, СН3), 23.74 (с, СН2), 27.43 (с, СН2), 30.26 (с, СН2), 30.49 (с, СН2), 30.59 (с, СН2), 30.67 (с, СН2), 30.78 (с, СН2), 30.81 (с, СН2), 30.82 (с, СН2), 33.08 (с, СН2), 48.11 (с, C(CH2O)4), 51.86 (с, СН2), 60.89 (с, СН2), 62.49 (с, СН2), 65.53 (с, СН2), 66.37 (с, СН2), 68.70 (с, СН2), 74.78 (с, СН2), 99.06 (c, OCH2O), 140.98 (c, Сpyr), 143.32 (c, Сpyr), 145.05 (c, Сpyr), 145.54 (c, Сpyr), 153.81 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 471.4 [М-2Cl]2+. Вычислено для [C55H98N4O8]2+ - 471.4.
Пример 20. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-20)
Получение 9,9'-(((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 12):
К раствору ацеталя 2б (5.20 г, 26.8 ммоль) в 100 мл диметилформамида добавляли K2CO3 (3.70 г, 26.8 ммоль). Смесь перемешивали при комнатной температуре в течение 20 минут. Затем к полученному раствору добавляли соединение 9 (6.50 г, 13.4 ммоль) и реакционную смесь кипятили в течение 3 часов. Растворитель отгоняли в вакууме. Далее твердый остаток растворяли в воде, нерастворимый осадок отфильтровывали и очищали с помощью колоночной хроматографии (элюент – изопропанол:хлороформ = 1:6). Выход 4.25 г (60%); желтое кристаллическое вещество; т.пл. 74 oC. Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.41 (д, 6Н, 3JHH = 5.2 Гц, 2СН3CH), 1.48 (с, 6Н, (СН3)2C), 2.51 (с, 6Н, 2СН3), 3.85-3.96 (м, 4H, 2CH2), 4.12 (с, 8H, 4CH2), 4.72-4.94 (м, 6H, 3CH2), 5.08-5.14 (м, 2H, 2CH3CH), 5.16-5.19 (м, 2H, CH2), 8.09 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 19.43 (с, СН3), 20.09 (с, СН3), 20,16 (с, СН3), 23.79 (с, СН3), 39.69 (с, C(CH2O)4), 61.99 (с, СН2), 62.05 (с, СН2), 62.16 (с, СН2), 62.90 (с, СН2), 63.10 (с, СН2), 66.32 (с, СН2), 72.76 (с, СН2), 98.58 (с, СНСН3), 103.85 (c, (CH3)2C), 103.99 (c, (CH3)2C), 133.97 (c, Сpyr), 140.63 (c, Сpyr), 142.76 (c, Сpyr), 149.60 (c, Сpyr), 151.77 (c, Сpyr), 151.81 (c, Сpyr).
Получение 9,9'-(((2,2-диметил-1,3-диоксан-5,5-диил)бис(метилен))бис(окси))бис(8-(хлорметил)-3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин) (промежуточное вещество 13):
4.00 г (7.5 ммоль) соединения 12 растворяли в 25 мл хлороформа и добавляли 3.50 г (15.0 ммоль) трихлоризоциануровой кислоты. Смесь перемешивали при кипении в течение 1 часа. Осадок отфильтровывали. Растворитель отгоняли в вакууме. Сухой остаток очищали колоночной хроматографией (элюент – этилацетат). Выход 21% (0.94 г); бежевое кристаллическое вещество; т.пл. 80-83 oC (разл.). Спектр ЯМР 1Н (400 МГц, СDCl3), δ, м.д. (смесь изомеров): 1.42 (д, 6Н, 3JHH = 5.2 Гц, 2СН3CH), 1.51 (с, 6Н, (СН3)2C), 4.04-4.15 (м, 4H, 2CH2), 4.19-4.20 (м, 8H, 4CH2), 4.70 (c, 4H, 2CH2), 4.77-4.99 (м, 6H, 3CH2), 5.13-5.16 (м, 2H, 2CH3CH), 5.16-5.20 (м, 2H, CH2), 8.21 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СDCl3), δ, м.д. (смесь изомеров): 14.31 (с, СН3), 23.86 (с, СН2), 39.95 (с, C(CH2O)4), 41.90 (c, CH2Cl), 61.88 (с, СН2), 64.46 (с, СН2), 67.69 (с, СН2), 74.36 (с, СН2), 97.84 (с, СНСН3), 98.86 (c, (CH3)2C), 137.19 (c, Сpyr), 142.32 (c, Сpyr), 143.55 (c, Сpyr), 149.51 (c, Сpyr), 150.15 (c, Сpyr).
Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-20):
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.25 г (0.4 ммоль) соединения 13 и 0.20 мл (0.8 ммоль) N,N-диметилдециламина. После отгонки ДМФА проводили кислотный гидролиз: к полученному остатку добавляли 20 мл воды и 3.6 мл 0.1М соляной кислоты и грели при 70 °С в течение 12 ч. Выход 0.24 г (50%); бежевое кристаллическое вещество; т.пл. 86-88 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д. (смесь изомеров): 0.86 (т, 6Н, 3JHH = 6.6 Гц, 2СН3C9H18), 1.22-1.28 (м, 28H, 14CH2), 1.30 (д, 3JHH = 5.2 Гц, 6Н, 2СН3CH), 1.72-1.84 (м, 4H, 2CH2), 3.03-3.09 (м, 12H, 2(CH3)2N+), 3.26-3.34 (м, 4H, 2CH2N+), 3.64-3.93 (м, 4H, 2CH2OH), 4.43-5.34 (м, 22H, 10CH2+2CH3CH), 8.40-8.56 (м 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д. (смесь изомеров): 14.03 (с, СН3), 20.12 (с, СН3), 21.87 (с, СН3), 22.17 (с, СН3), 25.81 (с, СН2), 28.56 (с, СН2), 28.75 (с, СН2), 28.88 (с, СН2), 28.98 (с, СН2), 31.35 (с, СН2), 46.52 (с, C(CH2O)4), 46.62 (с, C(CH2O)4), 50.24 (с, CH3N+), 50.29 (с, CH3N+), 58.21 (c, CH2), 59.35 (c, CH2), 59.73 (c, CH2), 61.03 (c, CH2), 62.33 (c, CH2), 63.96 (c, CH2), 65.52 (c, CH2), 73.37 (c, CH2), 73.81 (c, CH2), 74.36 (c, CH2), 74.79 (c, CH2), 103,27 (с, СНСН3), 138.46 (c, Сpyr), 140.42 (c, Сpyr), 141.71 (c, Сpyr), 141.75 (c, Сpyr), 141.83 (c, Сpyr), 142.51 (c, Сpyr), 142.98 (c, Сpyr), 143.73 (c, Сpyr), 144.19 (c, Сpyr), 151.98 (c, Сpyr), 153.22 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 429.6 [М-2Cl]2+. Вычислено для [C49H86N4O8]2+ - 429.3.
Пример 21. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) дихлорида (I-21)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.25 г (0.4 ммоль) соединения 13 и 0.23 мл (0.8 ммоль) N,N-диметилдодециламина. После отгонки ДМФА проводили кислотный гидролиз: к полученному остатку добавляли 26 мл воды и 3.8 мл 0.1М соляной кислоты и грели при 70 °С в течение 12 ч. Выход 0.14 г (33%); бежевое кристаллическое вещество; т.пл. 87 °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д. (смесь изомеров): 0.90 (т, 6Н, 3JHH = 6.7 Гц, 2СН3C11H22), 1.26-1.35 (м, 36H, 18CH2), 1.37 (д, 3JHH = 5.1 Гц, 6Н, 2СН3CH), 1.88-1.98 (м, 4H, 2CH2), 3.13 (c, 12H, 2(CH3)2N+), 3.35-3.42 (м, 4H, 2CH2N+), 3.89-4.08 (м, 4H, 2CH2OH), 4.70-5.23 (м, 22H, 10CH2+2CH3CH), 8.60-8.62 (м, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д. (смесь изомеров): 14.29 (с, СН3), 20.36 (с, СН3), 21.39 (с, СН3), 23.66 (с, СН2), 23.73 (с, СН2), 27.38 (с, СН2), 30.21 (с, СН2), 30.47 (с, СН2), 30.56 (с, СН2), 30.65 (с, СН2), 30.76 (с, СН2), 33.06 (с, СН2), 48.26 (с, C(CH2O)4), 51.63 (с, CH3N+), 51.69 (с, CH3N+), 51.79 (с, CH3N+), 52.11 (с, CH3N+), 55.36 (с, CH3N+), 55.51 (с, CH3N+), 60.28 (с, СН2), 61.10 (с, СН2), 61.37 (с, СН2), 62.52 (с, СН2), 62.81 (с, СН2), 63.69 (с, СН2), 66.29 (с, СН2), 66.65 (с, СН2), 67.02 (с, СН2), 67.10 (с, СН2), 69.50 (с, СН2), 75.05 (с, СН2), 75.50 (с, СН2), 75.94 (с, СН2), 76.66 (с, СН2), 77.85 (с, СН2), 101.12 (с, СНСН3), 105.10 (с, СНСН3), 140.50 (c, Сpyr), 141.02 (c, Сpyr), 142.91 (c, Сpyr), 143.39 (c, Сpyr), 143.80 (c, Сpyr), 144.09 (c, Сpyr), 144.74 (c, Сpyr), 145.25 (c, Сpyr), 146.82 (c, Сpyr), 153.66 (c, Сpyr), 154.68 (c, Сpyr), 155.30 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 457.4 [М-2Cl]2+. Вычислено для [C53H94N4O8]2+ - 457.4.
Пример 22. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(3-метил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9,8-диил))бис(метилен))бис(N,N-диметилтетрадецил-1-аминий) дихлорида (I-22)
Синтезировали и разрабатывали аналогично соединению I-3. Использовали 0.25 г (0.4 ммоль) соединения 13 и 0.25 мл (0.8 ммоль) N,N-диметилтетрадециламина. После отгонки ДМФА проводили кислотный гидролиз: к полученному остатку добавляли 20 мл воды и 3.2 мл 0.1М соляной кислоты и грели при 70 °С в течение 12 ч. Выход 0.21 г (47%); бежевое кристаллическое вещество; т.пл. 89-90 °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д. (смесь изомеров): 0.90 (т, 6Н, 3JHH = 6.8 Гц, 2CH3C13H26), 1.27-1.35 (м, 44H, 22CH2), 1.37 (д, 3JHH = 5.1 Гц, 6Н, 2СН3CH), 1.88-1.97 (м, 4H, 2CH2), 3.14 (c, 6H, (CH3)2N+), 3.15 (c, 6H, (CH3)2N+), 3.35-3.42 (м, 4H, 2CH2N+), 3.88-4.06 (м, 4H, 2CH2OH), 4.68-5.28 (м, 22H, 10CH2+2CH3CH), 8.60-8.62 (м, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д. (смесь изомеров): 14.47 (с, СН3), 20.33 (с, СН3), 20.35 (с, СН3), 23.66 (с, СН2), 23,76 (с, СН2), 27.39 (с, СН2), 27.42 (с, СН2), 30.23 (с, СН2), 30.51 (с, СН2), 30.58 (с, СН2), 30.68 (с, СН2), 30.79 (с, СН2), 30.82 (с, СН2), 30.83 (с, СН2), 33.10 (с, СН2), 48.32 (с, C(CH2O)4), 51.65 (с, CH3N+), 60.30 (c, CH2), 61.12 (c, CH2), 62.54 (c, CH2), 62.81 (c, CH2), 63.65 (c, CH2), 66.26 (c, CH2), 67.00 (c, CH2), 75.05 (c, CH2), 75.74 (c, CH2), 105.11 (с, СНСН3), 140.57 (c, Сpyr), 140,96 (c, Сpyr), 141.01 (c, Сpyr), 143.46 (c, Сpyr), 143.79 (c, Сpyr), 144.19 (c, Сpyr), 144.74 (c, Сpyr), 145.34 (c, Сpyr), 146.92 (c, Сpyr), 153.62 (c, Сpyr), 153.68 (c, Сpyr), 155.35 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 485.4 [М-2Cl]2+. Вычислено для [C57H102N4O8]2+ - 485.4.
Пример 23. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдецил-1-аминий) дихлорида (I-23)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-20. Выход 0.10 г (~100%); желтое кристаллическое вещество; т.пл. 74-76 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.86 (т, 6Н, 3JHH = 6.4 Гц, 2СН3C9H18), 1.19-1.33 (м, 28H, 14CH2), 1.74-1.85 (м, 4H, 2CH2), 3.05 (c, 12H, 2(CH3)2N+), 3.29-3.33 (м, 4H, 2CH2N+), 3.79 (с, 4H, 2СН2), 3.91 (с, 8H, 4СН2), 4.58 (с, 4H, 2СН2), 4.70 (с, 4H, 2СН2), 4.75 (с, 4H, 2СН2), 8.55 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 13.97 (с, СН3), 21.81 (с, СН2), 22.11 (с, СН2), 25.77 (с, СН2), 28.48 (с, СН2), 28.69 (с, СН2), 28.81 (с, СН2), 28.91 (с, СН2), 31.30 (с, СН2), 46.58 (с, C(CH2O)4), 50.23 (с, CH3N+), 53.48 (с, СН2), 58.23 (с, СН2), 59.82 (с, СН2), 61.15 (с, СН2), 63.95 (с, СН2), 74.80 (с, C(CH2O)2), 140.10 (c, Сpyr), 141.43 (c, Сpyr), 141.95 (c, Сpyr), 144.48 (c, Сpyr), 153.13 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 403.6 [М-2Cl]2+. Вычислено для [C45H82N4O8]2+ - 403.3.
Пример 24. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис(метилен))бис(N,N-диметилдодецил-1-аминий) дихлорида (I-24)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-21. Выход 0.10 г (~100%); желтое кристаллическое вещество; т.пл. 110-112 °С. Спектр ЯМР 1Н (400 МГц, СD3OD), δ, м.д.: 0.90 (т, 6Н, 3JHH = 6.63Гц, 2СН3C11H22), 1.24-1.48 (м, 36H, 18CH2), 1.86-2.00 (м, 4H, 2CH2), 3.14 (c, 12H, 2(CH3)2N+), 3.35-3.47 (м, 4H, 2CH2N+), 3.97 (с, 4H, 2СН2), 4.06 (с, 4H, 2СН2), 4.79 (с, 4H, 2СН2), 4.86, 4.89 (с, 4H, 2СН2), 8.60 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, СD3OD), δ, м.д.: 14.45 (с, СН3), 23.74 (с, СН2), 27.43 (с, СН2), 30.24 (с, СН2), 30.49 (с, СН2), 30.57 (с, СН2), 30.67 (с, СН2), 30.77 (с, СН2), 33.08 (с, СН2), 51.68 (с, CH3N+), 55.59 (с, СН2), 60.33 (с, СН2), 66.40 (с, СН2), 76.04 (с, C(CH2O)2), 141.02 (c, Сpyr), 143.51 (c, Сpyr), 144.14 (c, Сpyr), 146.89 (c, Сpyr), 155.38 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 431.6 [М-2Cl]2+. Вычислено для [C49H90N4O8]2+ - 431.4.
Пример 25. Получение N,N'-((((2,2-бис(гидроксиметил)пропан-1,3-диил)бис(окси))бис(4,5-бис(гидроксиметил)пиридин-3,2-диил))бис (метилен))бис(N,N-диметилтетрадецил-1-аминий) дихлорида (I-25)
Синтезировали и разрабатывали аналогично соединению I-5. Использовали 0.10 г (0.1 ммоль) соединения I-22. Выход 0.09 г (~100%); желтое кристаллическое вещество; т.пл. 57-60 °С. Спектр ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.85 (т, 6Н, 3JHH = 6.7 Гц, 2СН3C13H26), 1.21-1.28 (м, 44H, 22CH2), 1.73-1.84 (м, 4H, 2CH2), 3.06 (c, 12H, 2(CH3)2N+), 3.27-3.37 (м, 4H, 2CH2N+), 3.78 (с, 8H, 4СН2), 3.91 (с, 8H, 4СН2), 4.58 (с, 8H, 4СН2), 4.71 (с, 8H, 4СН2), 4.75 (с, 8H, 4СН2), 8.55 (с, 2Н, 2СНpyr). Спектр ЯМР 13С {1H} (100 МГц, ДМСО-d6), δ, м.д.: 13.96 (с, СН3), 21.82 (с, СН2), 22.11 (с, СН2), 25.78 (с, СН2), 28.51 (с, СН2), 28.73 (с, СН2), 28.84 (с, СН2), 28.99 (с, СН2), 29.05 (с, СН2), 29.07 (с, СН2), 29.10 (с, СН2), 31.31 (с, СН2), 46.59 (с, C(CH2O)4), 50.22 (с, CH3N+), 53.47 (с, СН2), 58.22 (с, СН2), 59.77 (с, СН2), 61.13 (с, СН2), 63.98 (с, СН2), 74.77 (с, C(CH2O)2) , 140.18 (c, Сpyr), 141.54 (c, Сpyr), 141.88 (c, Сpyr), 144.40 (c, Сpyr), 153.15 (c, Сpyr). Масс-спектр (MS-ESI): Найдено 459.4 [М-2Cl]2+. Вычислено для [C53H98N4O8]2+ - 459.4.
Пример 26. Исследование антибактериальной активности заявленных четвертичных аммониевых соединений на основе производных пентаэритрита и пиридоксина in vitro
Измерение антибактериальной активности заявленных соединений проводилось на музейных штаммах Enterococcus faecalis ATCC 29212, Enterococcus faecium ATCC 19434, Staphylococcus aureus ATCC 25923, Staphylococcus epidermidis ATCC 14990, Bacillus cereus ATCC 11778, Bacillus subtilis ATCC 6633, Ent. sakazakii CCM 3461, Escherichia coli ATCC 25922, Klebsiella pneumoniae ATCC 13883, Morg. morganii ssp. Morganii, Pseudomonas aeruginosa ATCC 27853, Sal. Typhimurium ATCC 14028. Штаммы получены из коллекции ФБУН «Государственный научный Центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Серпухов, пос. Оболенск, Россия). Сравнительная оценка спектра антибактериального действия на эталонных штаммах и клинических изолятах грамположительных и грамотрицательных бактерий проводилась с использованием микрометода определения минимальной подавляющей концентрации (МПК) методом серийных разведений в бульоне Мюллера-Хинтон [Определение чувствительности микроорганизмов к антибактериальным препаратам (Методические указания МУК 4.2.1890-04) / М.: Федеральный центр госсанэпиднадзора Минздрава России, 2004. - 91 с.].
Метод разведения основан на использовании двойных последовательных разведений концентраций заявленных соединений от максимальной к минимальной. Оценку роста культур проводят визуально, сравнивая рост микроорганизмов в присутствии и отсутствии изучаемых тест - соединений. Наличие роста микроорганизма в бульоне (помутнение бульона) свидетельствует о том, что данная концентрация заявленного соединения недостаточна, чтобы подавить его жизнеспособность. По мере увеличения концентрации заявленного соединения рост микроорганизма ухудшается.
Первую наименьшую концентрацию заявленного соединения (из серии последовательных разведений), где визуально не определяется бактериальный рост, принято считать минимальной подавляющей концентрацией (МПК).
Для приготовления инокулюма использовали чистую, суточную культуру бактерий, выросших на плотной питательной среде (агаризованная среда Мюллера-Хинтона (МХ)). В стерильном изотоническом растворе хлорида натрия готовили взвесь микроорганизмов, доводя плотность инокулюма до 0.5 по стандарту МакФарланда (1.5∙108 КОЕ/мл). Затем полученную суспензию микроорганизмов разводили до концентрации 107 КОЕ/мл МХ-бульоном. Инокулюм использовали в течение 15 минут после приготовления; чистота бактериальных штаммов контролировалась перед каждым экспериментом.
В лунки каждого планшета вносили по 100 мкл бульона Мюллера-Хинтон; в первую лунку вносили исследуемое соединение в концентрации 128 мкг/мл в объеме 100 мкл и последовательным двукратным разведением доводили его концентрацию до 0.06 мкг/мл. Затем в каждую лунку вносили приготовленный инокулюм, разводя тем самым вдвое концентрацию заявленных соединений (начальной концентрация составила 64.0 мкг/мл). Для каждого соединения в эксперименте выполняли три технических повтора. В качестве контроля дополнительно включали лунки, не содержащие тестируемых соединений (контроль роста культуры). Кроме того, ставился контроль чистоты питательных сред и растворителей. Планшеты инкубировали в термостате при 37 °С в течение 18-24 часов.
В качестве препаратов сравнения использовали широко применяемые известные антисептические средства – мирамистин, бензалкония хлорид и хлоргексидин.
Как видно из представленных в Таблице 1 на Фиг. 1 данных, ряд из заявленных соединений (I-1, I-7, I-10, I-12, I-17, I-18, I-20, I-21, I-24) обладают активностью сопоставимой с бензалконием хлоридом, мирамистином и хлоргексидином. Особенно можно выделить соединение I-7, для которого показана наибольшая антибактериальная активность в отношении изученных штаммов.
Для соединений I-1, I-7, I-12, I-18 и I-24 было проведено углубленное исследование антибактериальной активности на клинических штаммах микроорганизмов (Enterococcus faecalis 1465, Enterococcus faecalis 4223, Staphylococcus aureus 1817, Staphylococcus aureus 4771, Staphylococcus aureus MRSA 1710, Staphylococcus aureus MRSA 1822, Staphylococcus auricularis NKC 7, Staphylococcus epidermidis NKC 37/1, Staphylococcus haemolyticus 1464, Staphylococcus haemolyticus NKC 31/2, Acinetobacter baumannii NKC 45, Cedecea davisae 1813, Enterobacter aerogenes NKC 8, Enterobacter cloacae 2092, Escherichia coli NKC 1, Klebsiella pneumoniae 1678, Klebsiella pneumoniae 2048, Proteus mirabilis NKC 30, Pseudomonas aeruginosa NKC 17, Serratia marcescens 2560), результаты представлены в Таблице 2 на Фиг. 2 Бактериальные штаммы получены из Казанского института эпидемиологии и микробиологии (Казань, Россия) и из лаборатории бактериологии республиканской клинической больницы (Казань, Россия). В качестве препаратов сравнения использовались мирамистин, бензалкония хлорид и хлоргексидин. Все изученные соединения продемонстрировали схожую антибактериальную активность, на штаммах грамположительных и грамотрицательных бактерий, не уступающую референсным препаратам.
Пример 27. Исследование цитотоксичности заявленных четвертичных аммониевых соединений на основе производных пентаэритрита и пиридоксина in vitro
Цитотоксичность наиболее активных из заявленных соединений (I-1, I-7, I-12, I-18, I-24), в отношении условно-нормальных клеток (клетки печени человека CHL), определяли в сопоставлении с коммерческими антисептиками - бензалкония хлоридом и мирамистином. Исследование включало в себя пролиферативный МТТ-тест с последующим построением кривой доза-эффект и определения концентраций полумаксимального ингибирования роста условно-нормальных клеток (СС50).
Клетки культивировали в среде α-MEM (содержащей глутамин, 10 %-ную эмбриональную телячью сыворотку, 1 % пенициллин-стрептомицин) в стандартных условиях (атмосфере 5 %-го СО2 при 37 °С) до образования монослоя. Для получения клеточной суспензии монослой клеток трипсинизировали с последующей инактивацией трипсина добавлением среды α-MEM с сывороткой. Подсчёт клеток производили в камере Нэйбауэра методом исключения трипанового синего. Клетки пересевали 2 раза в неделю в отношении 1:6.
Для осуществления трехдневного теста в лунки 96-луночного планшета вносили 30000 клеток в 200 микролитрах культуральной среды. Перед внесением в планшет клетки тщательно суспензировали. Клеточную суспензию вносили в лунки планшета с помощью многоканального дозатора и стерильных наконечников. Далее планшеты с клетками инкубировали 24 часа в стандартных условиях для адгезии клеток к субстрату.
По истечении этого времени в стерильном 96-ти луночном планшете готовили серийные разведения (8 концентраций) анализируемых соединений в стерильной очищенной воде. В лунки планшета с клетками вносили аликвоты приготовленных растворов исследуемых соединений в объеме 22 микролитра в каждую лунку. После внесения исследуемых веществ клетки культивировали в стандартных условиях в течение 72 часов. По истечении времени инкубации культуральную среду с исследуемыми веществами удаляли из планшета с помощью вакуумного аспиратора. Далее в каждую лунку планшета вносили краситель MTT (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид) (5 мг/мл в растворе Хэнкса), краситель добавляли в соотношении 1 к 9 (где 1 мл красителя и 9 мл культуральной среды). Приготовленную реакционную смесь вносили в объеме 100 мкл в каждую лунку планшета и инкубировали в СО2 инкубаторе 3 часа, после чего удаляли смесь культуральной среды с красителем вакуумным аспиратором. Далее в каждую лунку планшета вносили 100 мкл ДМСО и инкубировали 5-10 минут, по истечении времени инкубации детектировали сигнал оптического поглощения при помощи планшетного ридера при 550 нм (референтная длина волны – 700 нм).
Далее рассчитывали концентрацию полумаксимального ингибирования роста клеток (CС50), принимая жизнеспособность клеток в контрольных лунках за 100%. Результаты представляли в процентном отношении к контролю, который не обрабатывали исследуемыми препаратами. Для препаратов строили кривую «доза-эффект» и определяли величины СC50 с помощью программного обеспечения OriginPro8.
Исследование проводили в двух независимых повторах.
Результаты исследования представлены в таблице 3 на Фиг. 3.
По результатам исследования цитотоксической активности можно сделать вывод, что среди исследованных соединений менее токсичными, по сравнению с применяемыми в клинической практике препаратами, являются соединения I-1, I-12, I-18 и I-24. Соединение I-7 незначительно уступает мирамистину и превосходит по безопасности бензалкония хлорид.
Таким образом, из описанного выше можно сделать вывод, что заявителем решена техническая проблема и достигнут заявленный технический результат, а именно – расширен арсенал известных средств указанного назначения путем создания новых соединений общей формулы (I), содержащих в своем составе фрагмент производных пентаэритрита и четвертичные аммониевые фрагменты, и обладающих антибактериальной активностью, в т.ч. в отношении клинических бактериальных штаммов.
Заявленное техническое решение соответствует условию патентоспособности «новизна», предъявляемому к изобретениям, так как из исследованного уровня техники не выявлены технические решения, обладающие заявленной совокупностью отличительных признаков, обеспечивающих достижение заявленных результатов.
Заявленное техническое решение соответствует условию патентоспособности «изобретательский уровень», предъявляемому к изобретениям, так как не является очевидным для специалиста в данной области науки и техники.
Заявленное техническое решение соответствует условию патентоспособности «промышленная применимость», так как может быть реализовано на любом специализированном предприятии с использованием стандартного оборудования, известных отечественных материалов и технологий.
| название | год | авторы | номер документа |
|---|---|---|---|
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| ФОСФОНИЕВЫЕ СОЛИ НА ОСНОВЕ ПРОИЗВОДНЫХ ПИРИДОКСИНА | 2011 |
|
RU2466728C1 |
| Четвертичные аммониевые соединения на основе производных пиридоксина и жирных карбоновых кислот, обладающие антибактериальной активностью | 2022 |
|
RU2795265C1 |
| АНТИБАКТЕРИАЛЬНЫЕ СРЕДСТВА НА ОСНОВЕ ЧЕТВЕРТИЧНЫХ АММОНИЕВЫХ СОЛЕЙ | 2014 |
|
RU2561281C1 |
| Бис-аммониевые соединения на основе пиридоксина, обладающие антибактериальными и антимикотическими свойствами | 2020 |
|
RU2731999C1 |
| Оксазолидиноны на основе производных пиридоксина, обладающие антибактериальной активностью | 2024 |
|
RU2836570C1 |
| Четвертичные аммониевые соединения на основе 3-гидроксипиридина, обладающие антибактериальной активностью | 2021 |
|
RU2778507C1 |
| Азопроизводные аминофенолов, обладающие способностью ингибировать образование конечных продуктов гликирования | 2024 |
|
RU2839138C1 |
| Способ получения 5,8-(бис(метилен(N,N-диметил-N-додециламмоний))-2-этил-4H-[1,3]диоксино[4,5-c]пиридиний дихлорида | 2019 |
|
RU2697848C1 |
| Антибактериальные средства на основе производных ципрофлоксацина | 2016 |
|
RU2636751C1 |

Изобретение относится к химии органических гетероциклических соединений, а именно к новым четвертичным аммониевым соединениям на основе производных пентаэритрита и пиридоксина формулы (I). Технический результат – получены новые соединения, которые могут найти применение в медицине и ветеринарии в качестве средств, проявляющих антибактериальную активность. 1 з.п. ф-лы, 3 ил., 27 пр.

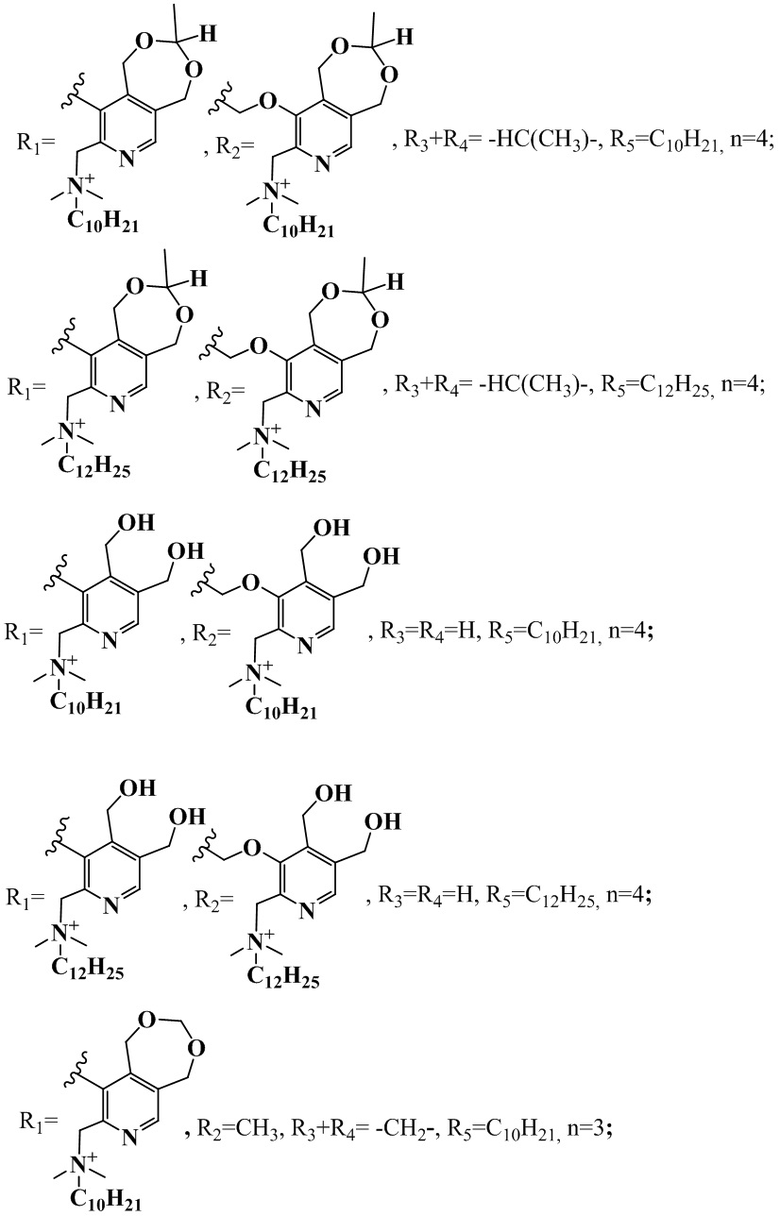
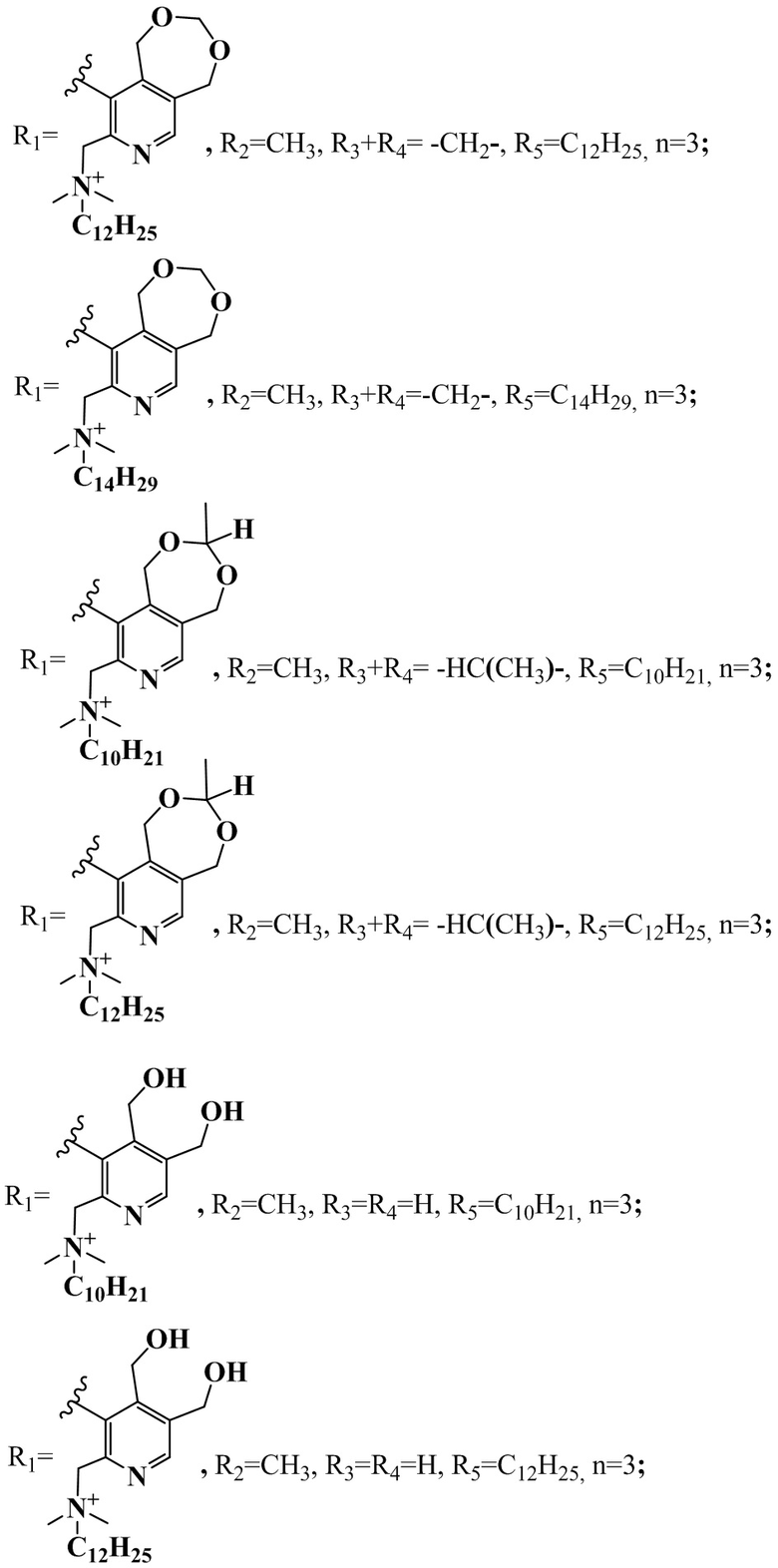
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C10H21, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C12H25, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C14H29, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C12H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C14H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C12H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C14H29, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C10H21, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C12H25, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C14H29, n=2.
1. Четвертичные аммониевые соединения на основе производных пентаэритрита и пиридоксина общей формулы (I)
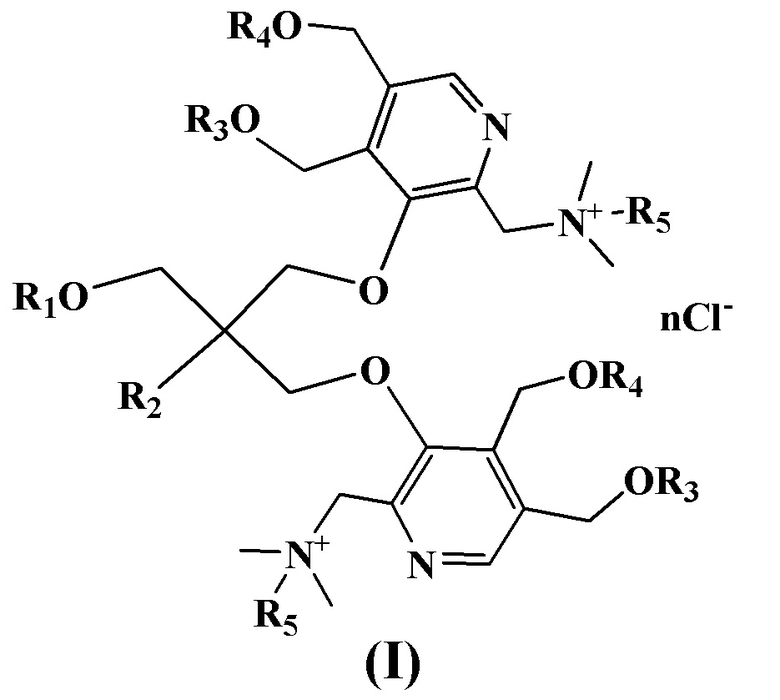
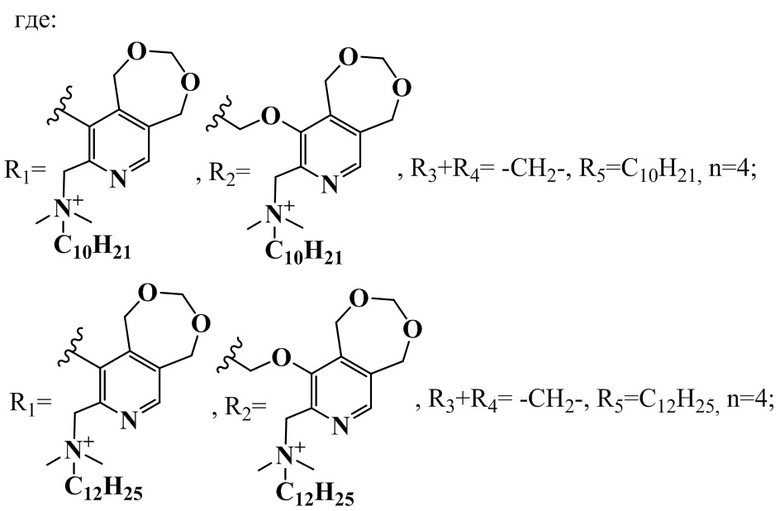
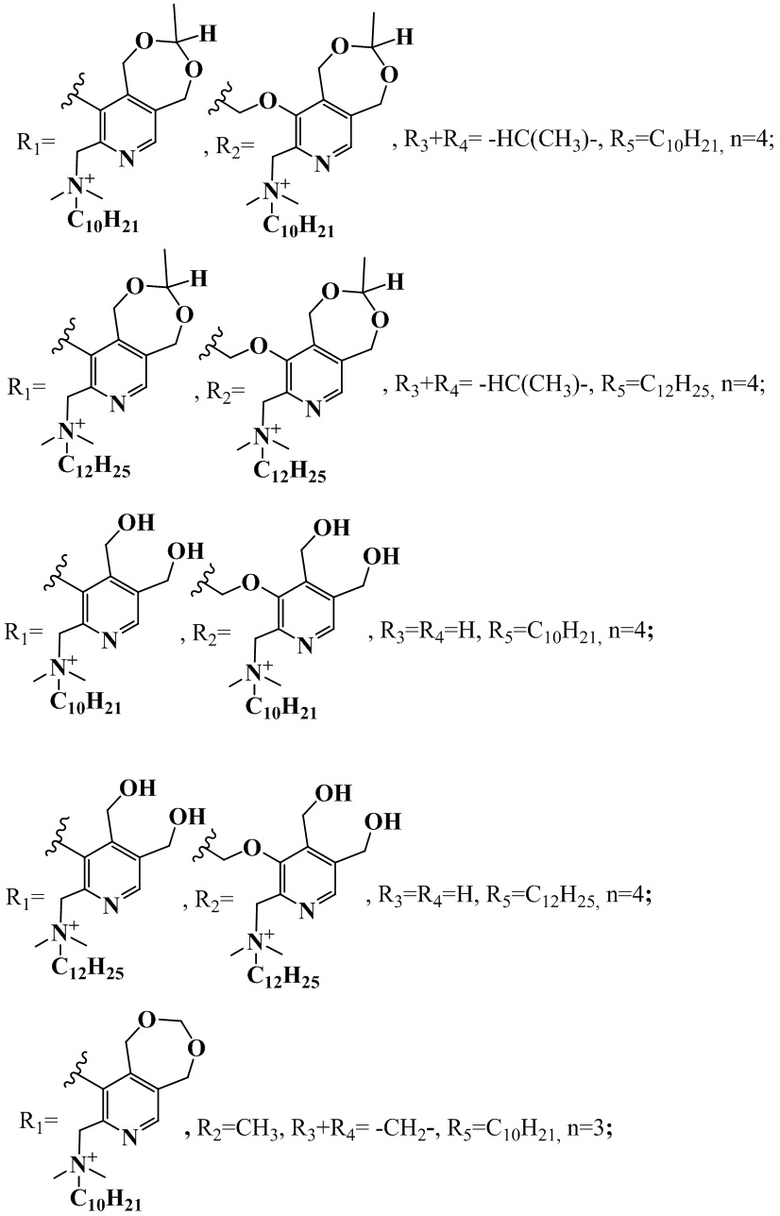

R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C10H21, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C12H25, n=2;
R1+R2=-C(CH3)2OCH2-, R3+R4= -CH2-, R5=C14H29, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C12H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH2-, R5=C14H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C10H21, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C12H25, n=2;
R1=H, R2=CH2OH, R3+R4= -CH(CH3)-, R5=C14H29, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C10H21, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C12H25, n=2;
R1=R3=R4=H, R2=CH2OH, R5=C14H29, n=2.
2. Четвертичные аммониевые соединения на основе производных пентаэритрита и пиридоксина общей формулы по п.1, обладающие антибактериальной активностью.
| A | |||
| N | |||
| VERESHCHAGIN et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Музыкальный инструмент со звучащими металлическими пластинками и ручной клавиатурой | 1922 |
|
SU545A1 |
| АНТИБАКТЕРИАЛЬНЫЕ СРЕДСТВА НА ОСНОВЕ ЧЕТВЕРТИЧНЫХ АММОНИЕВЫХ СОЛЕЙ | 2014 |
|
RU2561281C1 |
| Четвертичные аммониевые соединения на основе производных пиридоксина и жирных карбоновых кислот, обладающие антибактериальной активностью | 2022 |
|
RU2795265C1 |
| АНТИСЕПТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2641309C1 |
| Бис-аммониевые соединения на основе пиридоксина, обладающие антибактериальными и антимикотическими свойствами | 2020 |
|
RU2731999C1 |
Авторы
Даты
2024-01-11—Публикация
2023-11-17—Подача