Изобретение касается использования соединений формулы RO-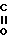 -
-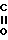 -
-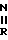 -
-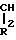 -
-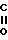 -OR1 (I) где R и R1 - одинаковые и означают метил, этил Nа и К;
-OR1 (I) где R и R1 - одинаковые и означают метил, этил Nа и К;
R1 - означает водород или метил;
R2 - означает водород, С1-С3-алкил, бензил или тиометил, либо R1 и R2 совместно образуют этиленовую цепь.
Алкильные цепи из трех и более атомов углерода могут быть как линейными, так и разветвленными. Под арилом подразумеваются ароматические углеводороды, в первую очередь, фенил и нафтил.
Получение соединений, отвечающих формуле I, известно. Наиболее просто оно осуществляется в том случае, когда 1-3 эквивалента гидрогалогенида, предпочительно гидрохлорида, эфира аминокислоты смешивают с 1-5 эквивалентами основания, например карбонатом или гидрокарбонатом, таким как карбонаты натрия или калия либо гидрокарбонаты натрия или калия, или третичными аминами, такими как триэтиламин, трибутиламин, этилдиизопропиламин, или гетероциклическими аминами, такими как П-алкилморфолин, пиридин, хинолин или диалкиланилин.
При желании одновременно могут быть использованы несколько оснований. Температура проведения реакции лежит в диапазоне от -30оС до 150оС, предпочтительно от -20оС до 100оС. При необходимости можно использовать растворители, такие как диэтиловый эфир, диметилцеллозольв или тетрагидрофуран, хлорированные углеводороды, такие как хлористый метилен, хлороформ, три- или тетрахлорэтилен, бензол, толуол, а также полярные растворители, такие как диметилформамид, ацетон, спирты, например метанол или этанол, или диметилсульфоксид. Непосредственно затем при температурах от -78оС до 100оС, предпочтительно от -20оС до 20оС, медленно прибавляют 1-3 эквивалента хлорангидрида эфира щавелевой кислоты. При желании также возможно работать в присутствии растворителя как описано выше. Окончание реакции определяется, например, методом тонкослойной хроматографии.
Разделение продуктов может осуществляться, например, путем экстракции или хроматографии, например, на силикагеле. Выделенный продукт можно перекристаллизовать.
Соединения формулы I c R и/или RI = щелочной металл, например, Na или К могут быть получены из соответствующих соединений формулы I c R и/или RI = C1-C4-алкокси в щелочной среде методом омыления до соответствующих солей, например с помощью NaOH или КОН в растворе низкомолекулярного спирта, такого как метанол или этанол, или же в таких эфирах, как диметилцеллозольв или тетрагидрофуран, в данных условиях и в присутствии воды. Катион щелочного металла в полученных солях может быть обычным способом при подкислении в ионообменнике заменен на любой другой катион. Для этого, например, ксилоты пропускают через колонку, заполненную катионообменником, (таким как ® Amberlite Cg-150 или ®Dowex - CCR-2) на основе системы полистирол-дивинилбензол. Катионообменник загружен требуемым катионом, например, ионами аммония, образующимися из первичного, вторичного или третичного амина. Желаемую соль получают выпариванием элюата.
Аммониевые соли кислот, образованные от первичного, вторичного или третичного амина, можно также получить, добавив свободную кислоту в спиртовой раствор эквимолекулярного количества соответствующего амина и упарив растворитель.
Получение преимущественно энантиомерных D- или L-соединений из рацематов осуществляется по известным методикам, например, путем фракционной кристаллизации или путем ферментной обработки. Другая возможность состоит в прямом синтезе энантиоомерных соединений из соответствующих D- или L-интермедиатов.
Отвечающие изобретению вещества действуют как обратимые ингибиторы пролилгидроксилазы. По этой причине они осуществляют селективное ингибирование коллагенспецифической реакции гидроксилирования, в ходе которой протеиносвязанный пролит гидроксилируется ферментом пролилгидроксилазой. При прекращении данной реакции с помощью ингибитора возникает не способная к функционированию недогидроксилированная молекула коллагена, которая может быть возвращена клеткой во внеклеточное пространство лишь в незначительных количествах. Кроме того, недогидроксилированный коллаген не способен встраиваться в коллоагенновую матрицу и легко подвергается протеилитической деструкции. Вследствие этого эффекта уменьшается общее количество коллагена, отлагаемого вне клетки. Поэтому ингибиторы пролингидроксилазы являются инструментом, пригодным для лечения заболеваний, при которых отложения коллагена вносят решающий вклад в клиническую картину. Сюда среди прочих относятся фиброзы легких, печени и кожи (склеродермия), а также атеросклероза.
Кроме того, известно, что ингибирование пролингидроксилазы известными ингибиторами, такими как α , α -дипиридил, приводит к ингибированию CLg-биосинтеза макрофагов (В. Мюллер и др. FEBS Lett 90, 218f, 1978). Это является причиной отказа от классического пути дополнительного активирования: в этом случае ингибиторы пролилгидроксилазы одновременно действуют как иммунодепрессанты, например, при общих иммуных заболеваниях.
Исходя из этого, отвечающие изобретению вещества могут быть использованы в качестве фибродепрессантов, иммунодепрессантов и противоатеросклеротических препаратов.
Противофибромное действие может быть изучено на примере фиброза печени, вызванного четыреххлористым углеродом. Для этого крыс дважды в неделю обрабатывают CCl4 (1 мг на кг), растворенным в оливковом масле. Исследуемое вещество вводится ежедневно, в данном случае даже дважды в день, перорально или внутрибрюшинно, в виде раствора в переносимом растворителе. Размер фиброза печени определяется гистологически, а доля коллагена в печени исследуется через определение гидроксипролина, как описано Кивирикко и др. (Anal. Biochem. 19, 249 f, 1967).
Активность фиброгенеза может быть определена путем радиоиммунологического обнаружения фрагментов коллагена и проколлагеновых пептидов в сыворотке. Отвечающие изобретению соединения активным в этих опытах при концентрациях от 1 до 100 мг/кг. Другой моделью для оценки антибиотического действия является описанный Келлеем и др. (Lab. Clin. Med. 96, 956, 1980). Фиброз легких, вызываемый биомицином. Для оценки эффективности отвечающих изобретению соединений грануляционная ткань может рассматриваться в приближении к модели гранулемы ватного тампона, как описано у Майера и др., Experimentia 6, 469, 1950.
П р и м е р ы. Общая пропись для получения соединений из примеров 1-6.
Один эквивалент гидрохлорида эфира аминокислоты ,два эквивалента триэтиламина и 2 эквивалента N,N-диметиламинопиридина вносят в хлористый метилен при комнатной температуре в атмосфере азота. Затем при 0-10оС медленно прикапывают один эквивалент хлорангидрида эфира щавелевой кислоты, растворенного в хлористом метилене. Перемешивают 12 ч при комнатной температуре, прибавляют насыщенный раствор гидрокарбоната натрия и экстрагируют. Отделяют органическую фазу, промывают ее раствором хлорида натрия, сушат сульфатом магния и упаривают. Сырой продукт хроматографируют.
П р и м е р 1. Диметиловый эфир (N-оксалил)-L-аланина
R = RI = CH3; R1 = H; R2 = CH3 5 г гидрохлорида метилового эфира L-аланина и 3,3 мл хлорангидрида метилового эфира щавелевой кислоты образуют 6 г образца I в виде масла.
Хроматография: эфир (метанол 5)1
П р и м е р 2. Диметиловый эфир (N-оксалил)-L-фенилаланина
R = RI = CH3; R1 = H; R2 = CH2C6H5 5 г гидрохлорида метилового эфира L-фенилалалнина и 2,2 мл хлорангидрида метилового эфира щавелевой кислоты образуют 6,5 г образца 2 в виде масла.
Хроматография: эфир (СН3ОН 5)1
П р и м е р 3. Диметиловый эфир (N-оксалил)-L-глицина
R = RI = CH3; R1 = H; R2 = H 15 г гидрохлорида метилового эфира L-глицина и 11 мл хлорангидрида монометилового эфира щавелевой кислоты образуют 23 г образца 3. Т.пл. 49оС, хроматография: эфир.
П р и м е р 4. Диметиловый эфир (N-оксалил)-L-пролина
R = RI = CH3; R1 = CH2 - CH2 = R2 2 г гидрохлорида метилового эфира L-пролина и 2,9 г хлорангидрида монометилового эфира щавелевой кислоты образуют 1,5 г в виде масла, хроматография: эфир.
П р и м е р 5. Диметиловый эфир (N-оксалил)-L-валина
R = RI =CH3; R1 = H; R2 = -CH(CH3)2 2 г гидрохлорида метилового эфира L-валина и 2,8 г хлорангидрида монометилового эфира щавелевой кислоты образуют 2 г в виде масла. Хроматография: хлороформ (эфир) .
П р и м е р 6. Диметиловый эфир (N-оксалил)-L-цистеина
R = RI = CH3; R1 = H; R2 = CH2SH 2 г гидрохлорида метилового эфира L-цистеина и 3,9 г хлорангидрида монометилового эфира щавелевой кислоты образуют 1,5 г в виде масла. Хроматография: хлороформ (эфир 1)1
П р и м е р 7. Диэтиловый эфир (N-оксалил)-саркозина
R = RI CH3; R1 = CH3; R2 = H.
2 г гидрохлорида этилового эфира саркозина прибавляют к 50 мл этанола и при комнатной температуре прикапывают раствор 3,5 мл (2 эквивалента) диэтилоксалата и 1,8 мл триэтиламина в 25 мл этанола. Перемешивают 5 ч при 50оС, затем 2 ч нагревают с обратным холодильником. Раствор охлаждают и упаривают досуха. Остаток растворяют в хлористом метилене, однократно промывают водой, сушат органическую фазу над сульфатом магния и упаривают.
Сырой продукт хроматографируют: эфир (хлороформ 1)1
Выход: 0,35 г
Общие прописи для получения соединений из примеров 8-14.
Один эквивалент соединений из примеров 1-7 при комнатной температуре растворяют в 2 эквивалентах 0,1 и спиртовой щелочи. Перемешивают 12 ч при комнатной температуре и упаривают досуха. Из остатка дважды удаляют дымящиеся продукты толуолом, несколько раз промывают пентаном и высушивают в глубоком вакууме.
П р и м е р 8. Дикалиевая соль (N-оксалил)-L-аланина
R = RI = K; R1 = H; R2 = CH3 300 мг соединения образца 1 вводят в реакцию обмена с 32,5 мл 0,1 н. раствора калийной щелочи в этаноле.
Выход: 370 мг белых кристаллов Т. пл. > 300оС
П р и м е р 9. Динатриевая соль (N-оксалил)-L-фенилаланина
R = RI = Na; R1 = H; R1 = CH2C6H5 420 мг соединения образца 2 вводят в реакцию обмена с 32,5 мл 0,1 н. раствора натриевой щелочи в этаноле. Выход: 440 мг белых кристаллов, Т. пл. > 300оС
П р и м е р 10.
Дикалиевая соль (N-оксалил)-L-глицина
R = RI = K; R1 = H; R2 = H 5,5 г соединения образца 3 вводят в реакцию обмена с 314 мл 0,1 н. раствора гидроокиси калия в метаноле.
Выход: 5,4 г белых кристаллов, Т. пл. > 300оС
П р и м е р 11. Динатриевая соль (N-оксалил)-L-пролина
R = RI = Na; R1 = CH2-CH2 = R2 300 мг соединения образца 4 вводят в реакцию обмена с 1,5 мл 0,1 н. раствора гидроокиси натрия в этаноле. Выход 290 мг белых кристаллов, Т. пл. > 300оС
П р и м е р 12. Динатриевая соль (N-оксалил)-L-валина
R = RI= Na; R1 = H; R2 = CH(CH3)2 300 мг соединения образца 5 вводят в реакцию обмена с 14 мл 0,1 н. раствора гидроокиси натрия в этаноле. Выход: 235 мг белых кристаллов, Т. пл. > 300оС.
П р и м е р 13. Динатриевая соль (N-оксалил)-L-цистеина
R = RI = Na; R1 = H; R2 = CH2H 300 мг соединения образца 6 вводят в реакцию обмена с 13,7 мл 0,1 н. раствора гидроокиси натрия в метаноле. Выход: 300 мг белых кристаллов, Т. пл. > 300оС.
П р и м е р 14. Дикалиевая соль (N-оксалил)саркозина.
R = R' = K; R1 = CH3, R2 = H 120 мг соединения образца 7 вводят в реакцию обмена с 11,4 мл 0,1 н. раствора гидроокиси калия в этаноле. Выход 130 мг белых кристаллов, Т. пл. 300оС
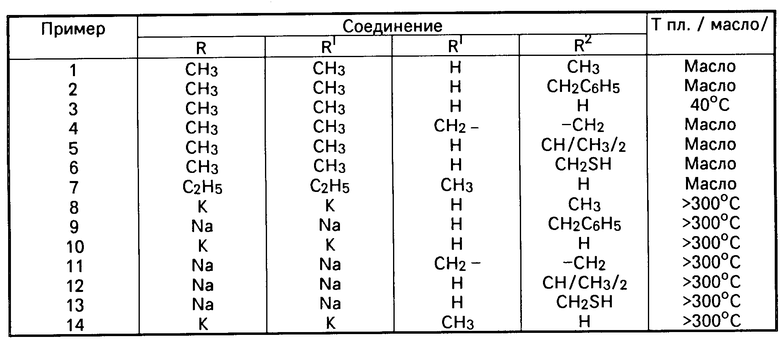
Соединения примеров 1-14 представлены в таблице.
Ингибирующее действие отвечающих изобретению соединений определялось по форментному тесту, аналогичному методу В. Петеркофского и Р. Диблазис. Anal. Biochem 6 6, 279-286 (1975).
При этом недогидроксилированный коллаген ферментно гидроксилируется пролилгидроксилазой в присутствии ионов железа (II), α -кетоглютарата и аскорбата и определяется та концентрация прибавленного соединения, отвечающего изобретению, которая приводит к 80%-ному ингибированию активности фермента) значение выражается через Ki (соли). Для соединений примера 8 Ki 0,04 мМ, примера 10 Ki 0,01 мМ
Ингибирующее действие можно также определять в культуре клеток или ткани. Для этого можно использовать фибропласты или иные предуцирующие коллаген клетки и соответственно Calvarien или другие продуцирующие коллаген органы. Далее представлено ингибирующее действие предлагаемых веществ в культуре Calvarien. Указана концентрация, приводящая к 50%-ному снижение частного гидроксипролин / пролин при метаболитическом маркировании с помощью 14С-пролина (IC50) (эфиры): пример 1 0,35 мМ, пример 3 0,002 мМ.
Изобретение касается применения производных оксалиламинокислот формулы 1 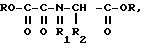 где R1 и R2 одинаковы или различны и означают C1-C3 - алкилы, Na или K, R1 - означает водород или метил, R2 - означает водород, C1-C3 - алкил, бензил или тиометил, либо R1 и R2 совместно образуют алкиленовую цепь. Соединения зарекомендовали себя как отличные ингибиторы пролин- и лизингидроксилаз, фибро- или иммунодепрессанты, лечебные средства при расстройствах метаболизма коллагена или коллагеноподобных веществ. 1 табл.
где R1 и R2 одинаковы или различны и означают C1-C3 - алкилы, Na или K, R1 - означает водород или метил, R2 - означает водород, C1-C3 - алкил, бензил или тиометил, либо R1 и R2 совместно образуют алкиленовую цепь. Соединения зарекомендовали себя как отличные ингибиторы пролин- и лизингидроксилаз, фибро- или иммунодепрессанты, лечебные средства при расстройствах метаболизма коллагена или коллагеноподобных веществ. 1 табл.
RO-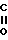 -
-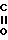 -
-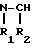 -
-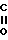 -OR1
-OR1
где R и R1 - одинаковые или различные, C1 - C3-алкил, Na или K;
R1 - водород или метил;
R2 - водород, C1 - C3-алкил, бензил или тиометил,
либо R1 и R2 вместе образуют этиленовую цепь, в качестве ингибиторов пролин- или лизингидроксилазы.
RO-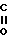 -
-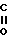 -
-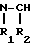 -
-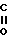 -OR1
-OR1
где R и R1 - одинаковые или различные, C1 - C3-алкил, Na или K;
R1 - водород или метил;
R2 - водород, C1 - C3-алкил, бензил или тиометил,
либо R1 и R2 - вместе образуют этиленовую цепь, в качестве фибро- или иммунодепрессантов.
RO-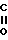 -
-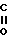 -
-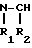 -
-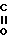 -OR1
-OR1
где R и R1 - одинаковые или различные, C1 - C3-алкил, Na или К;
R1 - водород или метил;
R2 - водород, C1 - C3-алкил, бензил или тиометил,
либо R1 и R2-совместно образуют этиленовую цепь,
в качестве лечебного средства при расстройствах метаболизма коллагена или коллагеноподобных веществ.
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА РИФОРМИНГА БЕНЗИНОВЫХ ФРАКЦИЙ | 1992 |
|
RU2010601C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1994-12-30—Публикация
1991-05-10—Подача