Изобретение относится к ветеринарной биотехнологи. Целью изобретения является создание препарата для эффективного лечения и специфической профилактики сальмонеллеза кур.
В последние годы наблюдается рост заболеваемости кур сальмонеллезом, вызываемым S. enteritidis. Возбудитель заболевания хорошо адаптировался к организму кур. Сальмонеллез энтеритидис вызывает значительную гибель цыплят и сопровождается длительным сальмонеллоносительством у взрослой птицы. Инфицированные S. enteritidis продукты птицеводства являются основным источником возбудителя токсикоинфекций человека.
Широкая распространенность S. enteritidis среди кур, значительный материальный ущерб, причиняемый птицеводству, опасность для человека, отсутствие эффективных лечебных препаратов, делают необходимым изыскание средств лечения и специфической профилактики этого заболевания.
Известна инактивированная вакцина против сальмонеллеза энтеритидис кур [1].
Однако эта вакцина низкоиммуногенна, особенно при интраперитонеальном способе введения.
Известна живая вакцина из термочувствительного мутанта S. enteritidis, не способного расти при 37оС, но эффективно размножающегося при 25оС [2]. Вакцина находится на стадии разработки и применялась на ограниченном поголовье птицы.
Использование вакцин в качестве средства борьбы с сальмонеллезом энтеритидис кур малоэффективно по следующим причинам.
Активный иммунитет у иммунизированных цыплят формируется лишь на 7-10-й день после вакцинации. Известно, что массовая гибель цыплят (достигающая 10-15% поголовья) приходится из цыплят до 10-дневного возраста, вследствие этого вакцинация не может предотвратить ущерб от заболевания в этом возрасте.
Вакцины не обладают лечебным эффектом. Вакцинация не способна ликвидировать сальмонеллоносительство у инфицированной птицы. Инфицированные продукты птицеводства являются источником возбудителя токсикоинфекций человека, что определяет весомую эпидемиологическую значимость сальмонеллеза энтеритидис.
Целью изобретения является создание эффективного препарата для лечения и специфической профилактики сальмонеллеза кур, а также разработка рационального способа лечения и профилактики заболевания.
Предлагаемый препарат в сравнении с имеющимися аналогами обладает следующими существенными отличиями:
способен предохранять 1-10-дневных цыплят от заболевания сальмонеллезом;
обладает лечебным эффектом и санирует сальмонеллоносителей.
Цель достигается созданием препарата, содержащего аттенуированный штамм. S. enteritidis и стабилизатор, отличающегося тем, что он дополнительно содержит суспензию фаговых частиц штамма Phagum enteritidis ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см3 в культуральной среде, консервированной хинозолом, из аттенуированных штаммов он содержит фагоустойчивый штамм S. enteritidis ВГНКИ N 204-R, а в качестве стабилизатора сахарозу и желатин, при следующем соотношении компонентов, об.%: Суспензия частиц штамма фага ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см3 в культуральной среде 45,0-50,0 Хинозол 0,005-0,01 Суспензия клеток фагоустойчивого штамма S. enteritidis ВГНКИ N 204-R с концентрацией 150-250 млрд. БОЕ/см3 22,5-27,5 Сахароза 2,5-3,7 Желатин 0,75-1,0 Дистиллированная вода Остальное
Способ лечения и профилактики сальмонеллеза кур предусматривает введение в организм цыплят 1-3-дневного возраста препарата, содержащего смесь суспензий фаговых частиц штамма фага ВГНКИ NF-6 и клеток фагоустойчивого штамма S. enteridis ВГНКИ N 204-R, консервант и стабилизатор, при следующем соотношении компонентов, об.%: Суспензия частиц штамма фага ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см3 45,0-50,0 Хинозол 0,005-0,01 Суспензия клеток фагоустойчивого штам- ма S. enteritidis ВГНКИ N 204-R с концентрацией 150-250 млрд. кл/см3 22,5-27,5 Сахароза 2,5-3,7 Желатин 0,75-1,0 Дистиллированная вода Остальное из расчета по 100-200 млн. фаговых частиц и 0,5-1 млрд. клеток вакцинного штамма на одного цыпленка перорально, двукратно, с интервалом в 3 дня.
Штамм Phagum enteritidis F-6 депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов, имеет регистрационный N 6.
Штамм бактериофага обладает следующими свойствами.
Морфология вириона. Вирион бактериофага обладает бинальным типом симметрии, состоит из гексагональной головки размером 50х50 нм, длинного отростка размером 112 нм, имеет несокращающийся чехол отростка и базальную пластинку. Относится к IV морфологической группе по классификации А.С.Тихоненко.
Морфология негативных колоний. Бактериофаг формирует при посеве на штамме-хозяине в течение 18 ч культивирования при 37оС негативные прозрачные круглые колонии, диаметром 1,5-2 мм, с четкими ровными краями.
Культуральные свойства.
Штамм фага обладает высокой литической активностью, титр фага, определенный методом Аппельмана, составляет 10-9. Оптимальная множественность инфицирования бактериальных клеток хозяина штаммом фага находится в диапазоне 0,01-0,1.
Бактериофаг характеризуется высокой урожайностью и скоростью роста. В стационарных условиях культивирования при 37оС в течение 4 ч в 1 см3среды содержится 2,0-3,5 х 1010 фаговых частиц.
Спектр литического действия. Штамм бактериофага обладает широким спектром литического действия по отношению к изолятам S. enteritidis, выделенным в неблагополучных по сальмонеллезу птицеводческих хозяйствах, лизирует 97% выделенных сальмонелл.
Штамм S. enteritidis 204-R получен целенаправленным снижением вирулентности путем внедрения транспозона Тп7 в геном устойчивого к рифампицину мутанта эпизоотического штамма, с последующей селекцией клонов, устойчивых к действию фага F-6.
Штамм S. enteritidis 204-R депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов.
Штамм обладает следующими свойствами.
Морфология - мелкие, грамотрицательные палочки без спор и капсул размером 2-3 х 0,6-0,7 мк, перитрих.
Ферментативные свойства - сбраживает с образованием кислоты и газа глюкозу, мальтозу, маннит, сорбит, левулезу, галактозу, декстрин глицерин, инозит, образует сероводород, не образует индол, нитриты редуцирует в нитраты.
Антигенная структура - агглютинируется монорецепторными сальмонеллезными "0" сыворотками: 1,9,12 и "Н" сыворотками: g,1,7.
Генетические маркеры - устойчив к стрептомицину (150 мкг/см3), рифампицину (200 мкг/см3), триметоприму (200 мкг/см3). Маркеры стабильно сохраняются после 10-кратных пересевов на мясопептонном агаре и при 5-кратных пассажах на белых мышах и цыплятах.
Устойчив к действию штамма бактериофага F-6.
Вирулентность - ЛД50 для белых мышей линии Валв/с - 5,6х106микробных клеток.
Иммуногенность - выживаемость белых мышей и цыплят, иммунизированных аттенурованным штаммом, после заражения 5-7 ЛД50вирулентного штамма составляет 80-95% от числа зараженных животных, при гибели в контроле 90-100%.
П р и м е р 1. Изготовление бактериофага. Реактор емкостью 1000 л заполняют наполовину мясопептонным бульоном, разведенным до концентрации аминного азота в среде 40-50 мг%. Питательную среду стерилизуют при 120оС в течение 1 ч. В реактор вносят матовые расплодки штамма-хозяина из расчета 1 л на 500 л среды и 1,5-3,0 л расплодки штамма фага. После посева содержимое тщательно перемешивают мешалкой и подают стерильный воздух при давлении 0,1-0,2 атм. В дальнейшем содержимое реактора перемешивают каждые 30 мин в течение 2-3 мин, при постоянной аэрации и температуре 37 ±1оС.
После наступления лизиса бактерий бактериофаг консервируют, добавляя 2% -ный раствор хинозола до его конечной концентрации в препарате 0,01-0,02%. Затем бактериофаг фильтруют через пластины марки СФ-300 в стерильный реактор и расфасовывают во флаконы.
Бактериофаг серии 1 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 1 млрд. БОЕ/см3 в культуральной среде 99,9 Хинозол 0,01
Бактериофаг серии 2 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 10 млрд. БОЕ/см3 в культуральной среде 99,9 Хинозол 0,01
Бактериофаг серии 3 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 1 млрд. БОЕ/см3 в культуральной среде 99,8 Хинозол 0,02
П р и м е р 2. Изготовление вакцины.
Реактор емкостью 200-500 л заполняют на одну треть объема бульоном Хоттингера и стерилизуют при 120оС в течение 1 ч. Матровую расплодку фагоустойчивого вакцинного штамма вносят в реактор в количестве 4-6% от объема среды. Культивирование проводят в течение 10-12 ч при 37оС и постоянно работающей мешалке со скоростью 120 об/мин и подаче стерильного воздуха в количестве 2 ±0,3 объема в 1 мин. Накопление микробных клеток составляет 40-60 млрд. в 1 см3 среды. Выращенную культуру осаждают на роторной центрифуге типа СГО-100 при 12-15 об/мин. Бактериальную массу снимают с ротора в ламинарном боксе и смешивают в соотношении 1:2 со стабилизатором, содержащим сахарозу, желатин и дистиллированную воду. Вакцину расфасовывают во флаконы объемом 20 см3 и лиофильно высушивают.
Вакцина 3 изготовленных серий имела следующий компонентный состав, об.%:
Серия 1 Серия 2 Серия 3 Суспензия клеток фагоустойчивого штамма S. enteritidis 204-R с концентрацией 150-250 млрд. кл/см3 52,0 45,0 55,0 Сахароза 5,0 7,5 7,5 Желатин 2,0 1,5 2,0 Дистиллированная вода Остальное
П р и м е р 3. Определяют эффективность фаговой части препарата для белых мышей. Используют белых мышей массой 14-16 г. Препарат вводят перорально в объеме 0,5 см3.
Первой группе мышей вводят препарат, полученный смешением фаговой и вакцинной частей из расчета 1 млрд. частиц фага и 1 млн. клеток аттенуированного штамма. Половину мышей опытной группы заражают 4-5 ЛД50вирулентного штамма S. enteritidis через 1 сутки, половину через 7 сут после введения препарата.
Второй группе мышей вводят только вакцинную часть препарата из расчета 1 млн. клеток аттенуированного штамма на голову.
Заражают животных в те сроки, что и мышей первой опытной группы. В качестве контроля используют неиммунизированных мышей.
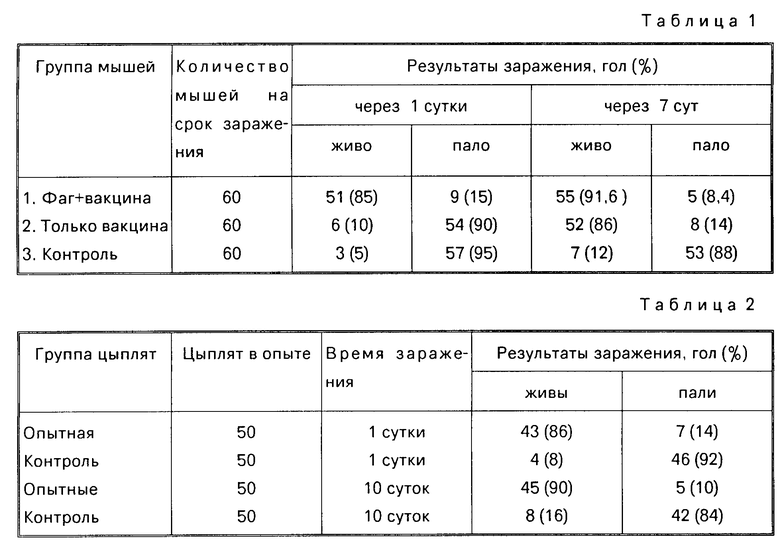
Результаты представлены в табл.1.
Введение в состав препарата бактериофага предохраняет от гибели 85% животных при заражении их через 1 сутки. Гибель мышей, получивших только вакцину из аттенуированного штамма, зараженных в тот же срок, составляет 90%, неиммунизированных животных 95%.
Заражение мышей через 7 сут вызывает гибель животных контрольной группы в 88% случаях, при сохранении 91,6% животных, получивших фаг и вакцину, и 86% мышей получивших только вакцинную часть препарата.
П р и м е р 4. Определяют защитный эффект предлагаемого препарата для цыплят 1-3-дневного возраста. Цыплятам выпаивают препарат, полученный смешением фаговой и вакцинной частей из расчета: 100 млн. фаговых частиц и 0,5 млрд. живых микробных клеток фагоустойчивого вакцинного штамма на одного цыпленка. Препарат применяют перорально, двукратно, с интервалом в 3 дня. Половину цыплят опытной группы заражают 5 ЛД50 вирулентного штамма через 1 сутки, половину через 10 сут после введения препарата. В качестве контроля используют равное количество неиммунизированных цыплят, зараженных в те же сроки.
Результаты представлены в табл.2.
Препарат предохраняет от гибели 86% цыплят при заражении их через 1 сутки при падеже 92% цыплят в контрольной группе. Заражение цыплят через 10 сут вызывает гибель 84% цыплят контрольной группы при выживании 90% птицы в опытной группе.
Использование предлагаемого препарата в ветеринарной практике позволит повысить эффективность проводимых мероприятий по лечению и профилактике сальмонеллеза кур.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА КУР И СПОСОБ ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА КУР | 1992 |
|
RU2030916C1 |
| БИОПРЕПАРАТ НА ОСНОВЕ БАКТЕРИОФАГОВ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ САЛЬМОНЕЛЛЕЗА ЖИВОТНЫХ | 2002 |
|
RU2232808C1 |
| ПРЕПАРАТ ПРОТИВ САЛЬМОНЕЛЛЕЗА ГОЛУБЕЙ И СПОСОБ ЛЕЧЕНИЯ САЛЬМОНЕЛЛЕЗА ГОЛУБЕЙ | 2007 |
|
RU2366456C1 |
| БИОПРЕПАРАТ НА ОСНОВЕ БАКТЕРИОФАГОВ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ КОЛИБАКТЕРИОЗА (ЭШЕРИХИОЗА) ЖИВОТНЫХ | 2002 |
|
RU2244747C2 |
| ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА СВИНЕЙ | 2003 |
|
RU2255763C2 |
| ПРЕПАРАТ БАКТЕРИОФАГА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ КОЛИБАКТЕРИОЗА | 1987 |
|
RU1533330C |
| ШТАММ БАКТЕРИЙ SALMONELLA DUBLIN, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ САЛЬМОНЕЛЛЕЗА ТЕЛЯТ | 1984 |
|
SU1197186A1 |
| СПОСОБ ЛЕЧЕНИЯ ПТИЦ ПРИ САЛЬМОНЕЛЛЕЗЕ, ВЫЗВАННОМ SALMONELLA TYPHIMURIUM | 2008 |
|
RU2375075C1 |
| ШТАММ БАКТЕРИЙ Salmonella enteritidis № 22, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИН И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2002 |
|
RU2218177C2 |
| Антибактериальная композиция на основе штаммов бактериофагов для профилактики или лечения сальмонеллеза и/или эшерихиоза сельскохозяйственных животных или птиц, или человека | 2019 |
|
RU2705302C1 |
Использование: ветеринарная биотехнология, препарат для лечения и специфической профилактики сальмонеллеза кур. Сущность изобретения: препарат состоит из двух частей - бактериофага S.enteritidis с широким спектром литического действия, представляющего собой суспензию частиц штамма фага F-6 в культуральной среде, консервированной хинозолом, и вакцины, содержащей суспензию клеток фагоустойчивого аттенуированного штамма S.enteritidis ВГНКИ N 204 - R и сахарозо-желатиновый стабилизатор. Препарат способен предохранять 1-10-дневных цыплят от заболевания сальмоннелезом, обладает лечебным эффектом, санирует сальмонеллоносителей и создает иммунитет высокой напряженности. 2 с.п. ф-лы, 2 табл.
ПРЕПАРАТ ПРОТИВ САЛЬМОНЕЛЛЕЗА КУР И СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА КУР.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Onozuka K., SHinimiga H., Cho N., et al | |||
| The adjuvant effect of muramyl dipeptid (MDP) analog an temperaturesensetive Salmonella mutant vaccine | |||
| Int-I-Immunolopharmacol., 1989, 11, (7), p | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ ИСПОЛЬЗОВАНИЯ АТМОСФЕРНОГО ЭЛЕКТРИЧЕСТВА | 1924 |
|
SU781A1 |
Авторы
Даты
1995-01-09—Публикация
1992-07-24—Подача