Изобретение относится к новым химическим соединениям, имеющим применение в аналитической химии, в частности соединению бис[N-(1-оксил-2,2,6,6-тетраметилпиперидил-4)-N-этилдитиокарбамато- S, S'] медь (II) формулы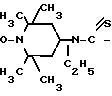 S
S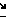 C
C -
-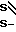 C
C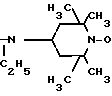 , в количественном определении ртути (II) методом электронного парамагнитного резонанса (ЭПР).
, в количественном определении ртути (II) методом электронного парамагнитного резонанса (ЭПР).
Известно применение диэтилдитиокарбамата меди (II) формулы
H5C2-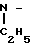 C
C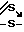 C
C -
-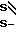 C-
C-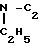 H5 для косвенного определения ртути (II) спектрофотометрическим методом [1]. В этом случае измеряют изменение светопоглощения при 438 нм, которое падает с ростом концентрации ртути (II). Основной недостаток при данном способе определения ртути заключается в том, что примесь окрашенных веществ, экстрагирующиеся в органическую фазу, существенно затрудняет спектроскопическое определение ртути.
H5 для косвенного определения ртути (II) спектрофотометрическим методом [1]. В этом случае измеряют изменение светопоглощения при 438 нм, которое падает с ростом концентрации ртути (II). Основной недостаток при данном способе определения ртути заключается в том, что примесь окрашенных веществ, экстрагирующиеся в органическую фазу, существенно затрудняет спектроскопическое определение ртути.
Также применяют диэтилдитиокарбамат меди (II) для определения ртути (II) методом ЭПР, используя для этой цели падение интенсивности одной из четырех линий спектра ЭПР этого комплекса [2].
Цель изобретения - расширение ассортимента средств для определения ртути (II), а также поиск более универсальных реагентов.
Поставленная цель достигается тем, что в качестве реагента для определения ртути (II) используют бис[N-(1-оксил-2,2,6,6-тетраметилпиперидил-4)-N-этилдитиокарбамато- S,S'] медь (II), которую получают взаимодействием 2,2,6,6-тетраметил-4(N-этиламино)пиперидин-1-оксила с сероуглеродом и гидроксидом натрия в присутствии солей меди (II).
П р и м е р 1. В плоскодонную колбу емкостью 150 см3 помещают 12,5 г (63 ммоль) 2,2,6,6-тетраметил-4-(N-этиламино)пиперидин-1-оксила, 5,0 г (66 ммоль) сероуглерода, 2,5 г (63 ммоль) гидроксида натрия в 50 мл дистиллированной воды.
Смесь перемешивают на магнитной мешалке при комнатной температуре в течение 15 мин. Затем в реакционную смесь добавляют 8,0 г (32 ммоль) сульфата меди (II) в 25 мл дистиллированной воды. Перемешивание продолжают еще в течение 5 мин после выпадения спин-меченого дитиокарбамата меди (II). Затем осадок переносят на стеклянный фильтр, промывают 50 мл дистиллированной воды и сушат на воздухе.
Выход бис[N-(1-оксил-2,2,6,6-тетраметилпиперидил-4)-N-этилдитиокарбамато- S, S'] меди (II) количественный. Продукт представляет собой поликристаллический порошок темно-коричневого цвета, разлагающийся при нагревании выше 205оС. Элементный анализ на углерод, водород и азот соответствует теоретическому.
Спектр в видимой области, в хлороформе,нм: 435 (ε = 13000),
Спектр ИК, ν,см-1: 1490, 1480, 1455 (C...N), 1380, 1085, 985 (C...S),
Спектр ЭПР, в хлороформе: g1 = 2,018, aCu = 27 Э,
g2 = 2,006, aN = 15,5 Э.
Структура соединения доказана по аналогии с аналогичными соединениями.
П р и м е р 2. Изучено распределение реагента, т.е. бис[N-(1-оксил-2,2,6,6-тетраметилпиперидил-4)-N-этилдитиокарбамато- S, S'] меди (II), в системе хлороформ-вода в зависимости от рН водной фазы. рН создавали с помощью буферного раствора тартрата (≈ 0,025 моль) с добавлением водного раствора гидроксида натрия. Установлено, что содержание реагента в органической фазе практически постоянно в области рН 6,5-11. При контакте хлороформного раствора реагента [(Rdtc)2Cu] с водным раствором ртути (II), равной концентрации в течение 1-2 мин происходит полный обмен меди на ртуть с образованием (Rdtc)2Hg по схеме:
Hg
При этом интенсивность спектра ЭПР возрастает, по сравнению с описанными в [4,5] , с исходной более, чем на порядок, причем спектр ЭПР из четырехкомпонентного медного с примесью триплета переходит в чисто триплетный (см.фиг.1).
На фиг. 1 показано влияние концентрации Hg2+ на спектр ЭПР (Rdtc)2Cu, где а) - исходный спектр ЭПР (Rdtc)2Cu;
b) - переходный спектр ЭПР, когда концентрация Hg2+ меньше концентрации (Rdtc)2Cu;
с) конечный спектр ЭПР, когда (Rdtc)2Cu полностью переходит в (Rdtc)2Hg.
При меньших концентрациях ртути (II) спектр имеет переходный вид, но с явно выраженной триплетной частью.
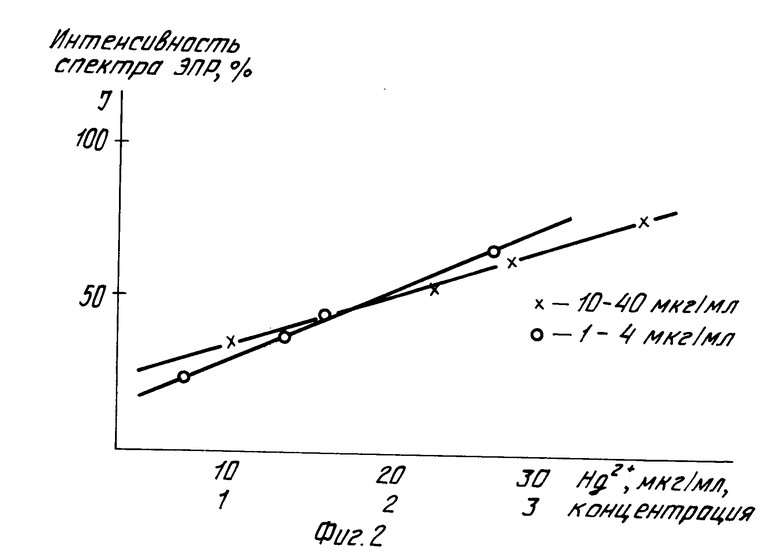
В интервале рН 6,5-11 рост интенсивности триплета прямо пропорционален росту концентрации Hg2+. Поэтому, построив калибровочный график зависимости I от концентрации Hg2+, можно точно определить содержание Hg2+ в водном растворе с неизвестным содержанием ртути (II) (фиг.2).
Изучено влияние посторонних ионов Tl3+,Ag+, I-,So3-, Bi3+,Pb2+,Co2+, Cu2+,Zn2+, ЭДТА на определение Hg2+ спин-меченым дитиокарбаматом меди (II). Установлено, что определению мешают ионы Ag+,I-,SO3-, присутствие которых дает занижение результатов по Hg2+. Присутствие Tl3+ дает завышение результатов Hg2+, поэтому от этих ионов надо избавляться в предварительном порядке.
Двухкратный избыток Bi3+, 50-кратный избыток ЭДТА, 100-кратный избыток Pd2+,Co2+,Cu2+ и 1000-кратный избыток Zn2+ не мешают определению Hg2+.
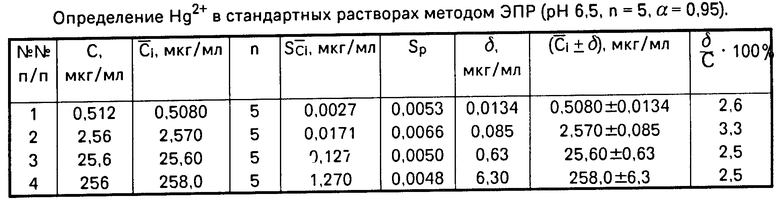
Разработанная методика определения Hg2+ проверена на приготовленных стандартных растворах Hg2+, что иллюстрируется таблицей.
Результаты измерений обрабатывались с применением методов математической статистики [3], где n - число параллельных определений, где C - концентрация стандартного раствора Hg2+;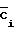 - среднее значение концентрации Hg2+, определенное методом ЭПР;
- среднее значение концентрации Hg2+, определенное методом ЭПР;
S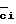 - средняя квадратичная ошибка отдельного определения или выборочное стандартное отклонение:
- средняя квадратичная ошибка отдельного определения или выборочное стандартное отклонение:
S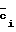 =
= 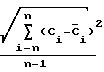 ;
;
Sp - относительная квадратичная ошибка или коэффициент вариации: Sp= 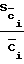 ;
;
δ - воспроизводимость опыта: δ = tgα, k· 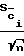 ;
;
tg α,k - коэффициент Стьюдента, (α = =0,95), k = n-1; δ - доверительный интервал для среднего результата;
δ - доверительный интервал для среднего результата;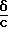 ·100 % - относительная погрешность.
·100 % - относительная погрешность.
Использование спин-меченого дитиокарбамата меди (II) как реагента для определения ртути (II) методом ЭПР имеет свои преимущества, по сравнению с прототипом. Во-первых, триплетный спектр ЭПР от нитроксильного радикала более интенсивный, чем квартет линий меди (II). Во-вторых, с ростом количества ртути (II) идет рост триплетной составляющей спектра ЭПР, что позволяет более точно измерять концентрацию. В случае прототипа с ростом концентрации ртути (II) интенсивность спектра ЭПР уменьшается, что затрудняет точное определение ртути (II).
Тот факт, что коэффициент экстинкции спин-меченого дитиокарбамата меди (II) при длине волны 435 нм равен ε = 13000 и соответствует таковому у немеченого диэтилдитиокарбамата меди (II), Позволяет применять предложенный нами реагент не только для определения ЭПР ртути (II), но и для спектрофотометрического ее определения по описанной ранее методике [1].
| название | год | авторы | номер документа |
|---|---|---|---|
| Бис-/2,2,6,6-тетраметилпиперидин-1-оксил-4-(N-метилдитиокарбамат)/цинка,в качестве реагента-собирателя для изучения процесса флотации минералов | 1980 |
|
SU973540A1 |
| Способ определения меди /п/ | 1984 |
|
SU1262372A1 |
| N',N"'-((5-Гидрокси-4,7-диметил-2-оксо-2Н-хромен-6,8-диил)бис(метанилилиден))бис(4-бромбензогидразид)-амбидентатный хромогенный и флуоресцентный хемосенсор на Hg и F | 2016 |
|
RU2621701C1 |
| @ -Карбоксиундециловый эфир 1-оксил-2,2,6,6-тетраметилпиперидин-4-ксантогеновой кислоты в качестве флотореагента для изучения процесса флотации несульфидных минералов | 1985 |
|
SU1310393A1 |
| Реагент для определения изотопного состава меди | 1988 |
|
SU1562815A1 |
| Способ количественного определения жирных кислот | 1985 |
|
SU1293616A1 |
| СПОСОБ ПОЛУЧЕНИЯ N,N'-БИС(3-ТРИАЛКИЛСИЛИЛПРОПИЛ)- ИЛИ N,N'-БИС(3-ТРИАЛКОКСИСИЛИЛПРОПИЛ)ТИОКАРБАМИДОВ | 1994 |
|
RU2074187C1 |
| Способ определения хлора | 1987 |
|
SU1516922A1 |
| S-Металлил-N,N-диэтилдитиокарбамат в качестве противозадирной присадки к смазочным маслам | 1990 |
|
SU1761748A1 |
| Полимерная композиция | 1988 |
|
SU1557148A1 |

Сущность изобретения: продукт - бис [N(1 - оксил - 2,2,6,6 - тетраметилпиперазил - 4) -N-этилдитиокарбамато- S,S′ -медь (2), выход количественный. Поликристалический порошок темно-коричневого цвета, разлагающийся при нагревании выше 205°С. Реагент 1: 2,2,6,6-тетраметил - 4 - (N-этиламино)пиперидин - 1 - оксил. Реагент 2: сероуглерод. Реагент 3: сульфат меди. Условия реакции: в воде, в присутствии гидроксида натрия. 2 ил., 1 табл.
БИС [N-(1-OKCИЛ-2,2,6,6-TETPAMETИЛПИПEPИДИЛ-4)-N-ЭTИЛДИTИOKAPБAMATO-S, S'] МЕДЬ (II) КАК РЕАГЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ РТУТИ (II).
Бис[N-(1-оксил-2,2,6,6- тетраметилпиперидил-4)-N-этилдитиокарбамато- S, S'-медь (II) формулы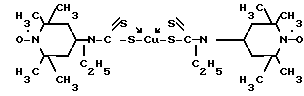
как реагент для определения ртути (II).
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ДАН СССР, 1984, т.274, N 1, с.88-90. | |||
Авторы
Даты
1995-01-27—Публикация
1990-06-07—Подача