Изобретение относится к иммунной биотехнологии, конкретно к выявлению антител против вируса иммунодефицита человека, и наиболее эффективно может быть использовано для диагностики синдрома приобретенного иммунодефицита человека у бессимптомных носителей инфекции.
Синдром приобретенного иммунодефицита человека (СПИД) был впервые описан в 1981 году. Спустя три года французские и американские ученые выделили и охарактеризовали новый ретровирус возбудитель СПИД, который впоследствие получил название вируса иммунодефицита человека (ВИЧ). В связи с актуальностью проблемы ВИЧ-инфекции и низкой эффективностью терапии СПИД наиболее перспективным путем ограничения распространения ВИЧ в мире является разработка специфической лабораторной диагностики заражения вирусом иммунодефицита. Для первичного звена скрининга наиболее приемлемым методом диагностики ВИЧ-инфекции является выявление специфических антител к антигенам ВИЧ. В настоящее время для обнаружения антител к ВИЧ широко используются метод иммуноблоттинга (ИБ Immunoblot или Western Blot/WB) и твердофазный иммуноферментный анализ ТФИФА Enzyme Linked Immunosorbent Assay (ELISA). Так как антитела в основном присутствуют в крови, все способы тестирования предполагают забор крови у обследуемых лиц. Использование метода сокультивирования образцов биологических жидкостей ВИЧ-инфицированных лиц с клетками пермиссивной линии неопластических Т-лимфоцитов человека позволило обнаружить инфекционный ВИЧ в сыворотке крови, цереброспинальной жидкости, семенной жидкости, слюне, слезах, цервикальной жидкости и молоке. Поэтому инвазивная процедура с целью получения крови для анализа присутствия антител к ВИЧ не исключает некоторую степень риска для здоровья медицинского персонала. Кроме того, индивиды, подвергающиеся обследованию, часто необоснованно боятся заразиться при сдаче крови и поэтому отказываются от процедуры тестирования. Эти проблемы преодолеваются неинвазивным методом определения антител к ВИЧ, который мог бы быть успешно использован для массового обследования населения.
У серопозитивных лиц специфические антитела были обнаружены в слюне и моче. Отсутствие инфекционного ВИЧ в моче инфицированных с виремией указывает на непроницаемость базальной мембраны почек для вируса, что делает более предпочтительным использование мочи для разработки неинвазивных методов диагностики СПИД. Основным препятствием для разработки таких методов является то, что антитела в моче присутствуют в более низкой концентрации, чем в сыворотке крови. Было описано использование концентрированных проб мочи инфицированных ВИЧ для тестирования специфических антител, т.е. впервые был предложен способ определения антител к ВИЧ, являющийся наиболее близким по совокупности признаков к изобретению и заключающийся в том, что отобранные пробы мочи центрифугировали при 1500 об/мин, осадок отбрасывали, а надосадок концентрировали в 200 раз в концентраторе Minicon B15 (Amicon, Danvers, MA) с диаметром пор концентрационной мембраны 60 000 Дальтон. Концентрированные пробы тестировали методом ТФИФА и ИБ. Исследователи идентифицировали антитела в моче как IgG и IgA методом радиальной иммунодиффузии. Пробы мочи брали от больных с признаками СПИД, СПИД-ассоциированного комплекса и от бессимптомных вирусоносителей. При тестировании концентрированных проб мочи методом конкурентного ТФИФА, где в качестве антигенного сорбента использовали бусы, покрытые рекомбинантными белками ВИЧ (gp 41), процент ВИЧ-инфицированных с выявленными антителами в моче составлял 72,2. При тестировании тех же проб мочи методом ИБ антитела к белку gp 160 были обнаружены у 93,2% инфицированных ВИЧ.
Цель изобретения заключается в разработке простого неинвазивного метода тестирования на инфицированность ВИЧ путем определения специфических антител в моче.
Технический результат достигается предложенным способом определения антител к ВИЧ путем концентрирования антител в пробах мочи с последующим тестированием концентрированного образца, отличием которого является то, что концентрирование антител в пробах мочи осуществляется полным замораживанием образца, размораживанием его до момента исчезновения льда при комнатной температуре, центрифугированием при 3000 об/мин, отбором осадка, его разведением в разводящей жидкости и тестированием в нем антител методом ТФИФА и методом ИБ.
П р и м е р 1. Способ концентрирования антител в моче.
В работе были использованы 20 образцов проб мочи от инфицированных ВИЧ. Отдельным больным были присвоены номера в арабских цифрах. Ни один из инфицированных не имел клинических проявлений заболевания почек. Пробы мочи неинфицированных лиц были использованы в качестве контроля.
Концентрирование антител в моче включало следующие этапы:
1. Сбор проб мочи в конические пробирки объемом 5 мл;
2. Замораживание проб мочи;
3. Размораживание проб мочи при комнатной температуре до момента исчезновения льда;
4. Центрифугирование при 3 000 об/мин 15 мин;
5. Отбрасывание надосадка;
6. Разведение осадка в 100 мкл разводящей жидкости;
7. Тестирование антител к ВИЧ в криоосадке.
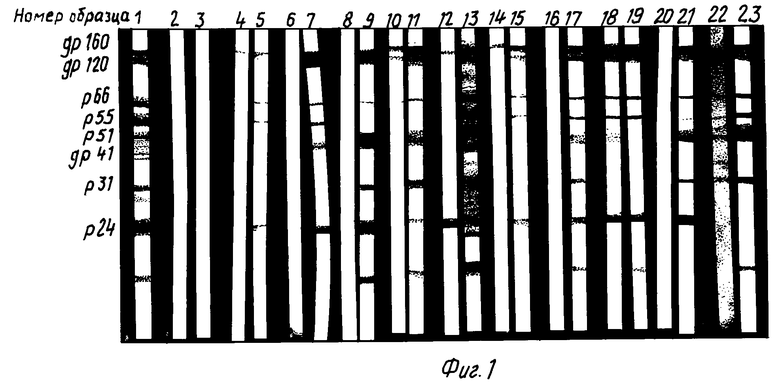
На фиг. 1 представлена картина иммунореактивности криоосадков и надосадков проб мочи инфицированных ВИЧ пациентов; К+ серопозитивная контрольная сыворотка; К- проба мочи неинфицированного донора; 5, 7, 9, 11, 13, 15, 17, 19, 21, 23- образцы криоосадков проб мочи ВИЧ инфицированных лиц; 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 образцы надосадков, образованных в результате криоосаждения проб мочи ВИЧ-инфицированных лиц.
П р и м е р 2. Сравнительный анализ иммунореактивности криоосадков и надосадков проб мочи инфицированных ВИЧ в ИБ.
При тестировании антител к ВИЧ в полученных описанным способом криоосадках проб мочи инфицированных лиц на первом этапе предпочтение было отдано методу ИБ (BIOTECH/DUPONT HIV-1, США), как более чувствительному по сравнению с ТФИФА и позволяющему выявлять характерные спектры антител к индивидуальным вирусным белкам. Иммунореактивность связывания криоосадка 2 мл мочи, разведенного в 2 мл разводящей жидкости из набора, сравнивали с иммунореактивностью 2 мл надосадка той же пробы мочи. В качестве положительного контроля использовалась сыворотка, содержащая антитела к антигенам ВИЧ в высоком титре, а в качестве отрицательного контроля проба мочи здорового донора, обработанная описанным способом (см. фиг. 1).
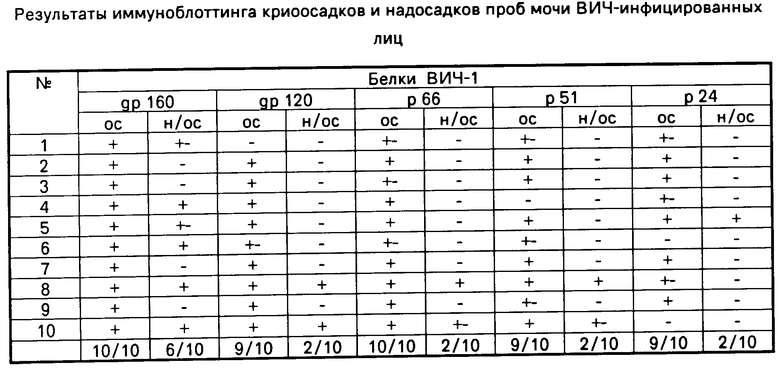
Параллельный попарный анализ иммунореактивности проб криоосадка и надосадка представлен в таблице 1.
Пробы оценивались на присутствие антител к отдельным белкам ВИЧ-1 как негативные (-), слабопозитивные (+ -) и позитивные (+) при сравнении интенсивности окрашивания полос исследуемыми пробами мочи и контрольной сывороткой. Из приведенных в таблице данных следует, что выявляемость антител к отдельным белкам ВИЧ-1 в криоосадках выше, чем в надосадках.
Полученные результаты позволяют сделать вывод о том, что в криоосадках проб мочи инфицированных ВИЧ концентрируются антитела к антигенам ВИЧ-1, которые выявляются методом ИБ по спецификации, предложенной фирмой-изготовителем для тестирования образцов сывороток на наличие антител к ВИЧ.
П р и м е р 3. Сравнительный анализ иммунореактивности криоосадков и надосадков проб мочи инфицированных ВИЧ в ТФИФА на основе вирусного лизата.
Сравнительный анализ иммунореактивности фракционированных проб мочи инфицированных ВИЧ был проведен с использованием диагностической ИФА тест-системы "VIRONOSTIKA anti-HTLV-III" ORGANON TECNIKA, Голландия). Тестирование проводилось согласно специфированной инструкции, приложенной к набору. Исключение составила стадия N 2, предусматривающая разведение тестируемых образцов сыворотки. Для определения антител к ВИЧ в моче 100 мкл нефракционированной мочи и 100 мкл надосадка, образующегося после процедуры криоосаждения, вносили в лунки с вирусным лизатом без разведения. Криоосадок 2 мл исследуемой пробы мочи разводили в 100 мкл разводящей жидкости из набора и вносили в лунки.
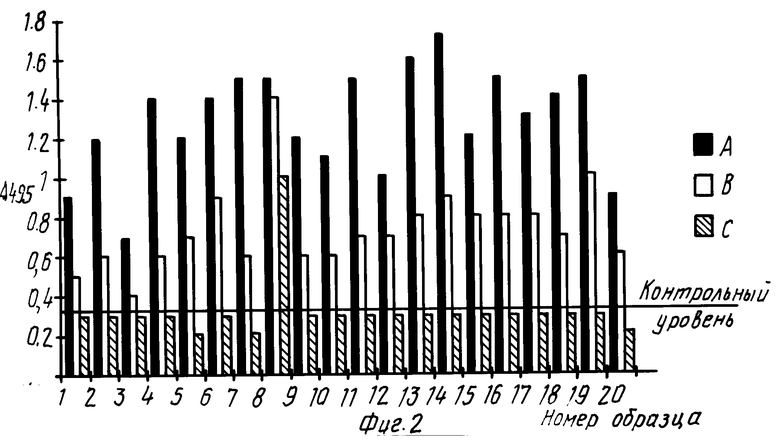
На фиг. 2 отражены значения оптической плотности в лунках с вирусным лизатом после проведения ИФА проб криоосадков, надосадков мочи и нефракционированных проб мочи ВИЧ-инфицированных лиц; А криоосадок; В нефракционная проба мочи; С надосадок; А 495 оптическая плотность.
Анализ полученных результатов показал, что наиболее высокие значения поглощения возникают при внесении в лунки образцов криоосадков. При этом среднее значение величин оптической плотности для криоосадков инфицированных ВИЧ составило 1,26±0,065 ед. (р < 0,05), а для нефракционированных проб мочи инфицированных лиц 0,69±0,034 ед. (р < 0,05). Величина оптической плотности в лунках с надосадком, полученным в результате криоосаждения проб мочи ВИЧ-инфицированных лиц, а также величина оптической плотности в лунках с криоосадком и надосадком проб мочи неинфицированных доноров и в лунках с нефракционированными пробами мочи неинфицированных доноров совпадали с величиной контрольного уровня, вычисленной по формуле, предложенной в спецификации к диагностическому набору. Исключение составила проба мочи ВИЧ-инфицированного под N 8, для которой величина оптической плотности после внесения в лунки проб криоосадка и надосадка была высокой и составляла 1,5 ед. и 1,0 ед. соответственно.
Таким образом, приведенные в данном примере результаты свидетельствуют о том, что в пробах мочи инфицированных ВИЧ, сконцентрированных по объему в 20 раз методом криоосаждения, концентрируются антитела к антигенам ВИЧ, которые могут быть выявлены методом ТФИФА на основе вирусного лизата. При этом величина оптической плотности в лунках с криоосадками проб мочи инфицированных ВИЧ статистически достоверно превышала величину оптической плотности в лунках с нефракционированными пробами мочи от тех же больных, что может способствовать увеличению чувствительности тестирования антител в моче методом ТФИФА на основе вирусного лизата.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОФЕРМЕНТНАЯ ТЕСТ-СИСТЕМА ДЛЯ ИДЕНТИФИКАЦИИ СПЕКТРА АНТИТЕЛ К ВИЧ 1 И 2 ВЫЯВЛЕНИЯ АНТИГЕНА ВИЧ 1 (p24) "ДС-ИФА-АНТИ-ВИЧ 1 И 2, ВИЧ 1 ГРУППЫ О-СПЕКТР+АГ p24 ВИЧ 1" | 2005 |
|
RU2283497C1 |
| ВАКЦИНА ПРОТИВ ВИЧ/СПИД | 2010 |
|
RU2475264C2 |
| ШТАММ ПЕРЕВИВАЕМЫХ КЛЕТОК МОНОЦИТОВ ЧЕЛОВЕКА - ПРОДУЦЕНТ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА I ТИПА | 1988 |
|
SU1554370A1 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1-ГО ТИПА ИВ742 СУБТИПА А ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2012 |
|
RU2513693C1 |
| ИММУНОТОКСИН ПРОТИВ СПИДА | 1996 |
|
RU2191596C2 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1-ГО ТИПА ИВ735 СУБТИПА В ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2012 |
|
RU2520813C2 |
| МОНОКЛОНАЛЬНОЕ АНТИИДИОТИПИЧЕСКОЕ АНТИТЕЛО Ab2, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ИСПОЛЬЗОВАНИЯ ПРОТИВ БОЛЕЗНЕЙ, СОПРОВОЖДАЮЩИХСЯ ЭКСПРЕССИЕЙ Lewis Y6 АНТИГЕНА, И ДЛЯ ОЧИСТКИ ВАРИАНТА BR55-2 АНТИТЕЛА, ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ СОСТАВ | 1993 |
|
RU2208642C2 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1-ГО ТИПА ИВ741 СУБТИПА АЕ ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2012 |
|
RU2520814C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТАЛОННЫХ ПОЛОЖИТЕЛЬНЫХ СЫВОРОТОК ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ | 1996 |
|
RU2123862C1 |
| СПОСОБ ДИАГНОСТИКИ СТАДИЙ ВИЧ-ИНФЕКЦИИ | 2004 |
|
RU2251701C1 |
Использование: в медицине, в частности в иммунной биотехнологии, и может быть использовано для диагностики синдрома приобретенного иммунодефицита человека у бессимптомных носителей инфекции. Сущность изобретения: от ВИЧ-инфицированных пациентовотбирают пробу мочи и проводят ее концентрирование путем полного замораживания, затем размораживания, пробы при комнатной температуре до момента исчезновения льда, центрифугирования и отбора осадка. Полученный осадок пробы мочи тестируют на присутствие антител к ВИЧ в вирусной тест-системе фирмы "Organon" и методом вестерн-блота (DU/PONT). Предложенный способ прост в исполнении, безопасен и позволяет обследовать большой контингент лиц на наличие ВИЧ-инфекции. 2 ил., 1 табл.
СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ВИРУСУ ИММУНОДЕФИЦИТА ЧЕЛОВЕКА, включающий отбор проб мочи, их концентрирование, инкубацию с тестирующей системой и регистрацию результатов, отличающийся тем, что концентрирование проводят замораживанием пробы мочи с последующим оттаиванием при комнатной температуре до полного исчезновения льда и отделением осадка центрифугированием.
| Шланговое соединение | 0 |
|
SU88A1 |
Авторы
Даты
1995-04-10—Публикация
1992-06-08—Подача