Изобретение относится к вирусологии, биотехнологии, в частности к культивированию вирусов, а именно получению клеточной линии - продуцента вируса иммунодефицита человека I типа (ВИЧ-I) для решения задач разработки и совершенствования диагностических и вакцинных препаратов против вируса СПИД.
Целью изобретения является получение технологического штамма клеток-продуцентов ВИЧ-I, обладающего высоким и стабильным уровнем вируспродукции и не требующего при культивировании специальной питательной среды с дорогостоящими добавками.
Штамм клеток-продуцентов ВИЧ-I ЭВК-ИРА/3 получен на основе трансформированных моноцитов человека (штамм П-937) путем заражения ВИЧ-I, выделенным от больного СПИД, клонирования и выделения клона клеток, хронически инфицированных ВИЧ-I, постоянно продуцирующих этот вирус. Штамм депонирован в Государственной коллекции вирусов под номером 4005.
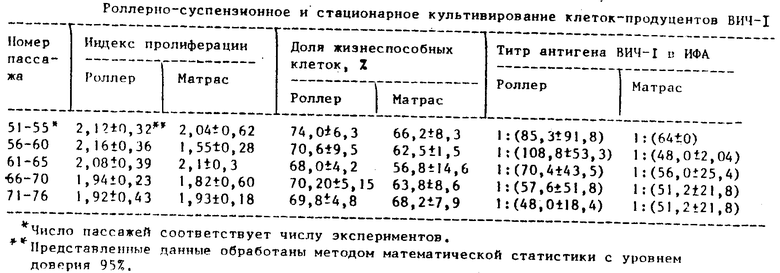
Морфологические признаки культуры: клетки округлые, крупные, на их поверхности различаются многочисленные выросты. Клетки могут образовывать кластеры по 10-30 клеток, границы клеток в них четко различимы. Цитоплазма мелкозернистая. Культура содержит гигантские многоядерные клетки (от 5 до 25% ). По данным электронной микроскопии клетки свободны от посторонней вирусной контаминации, грибков и бактерий. Выявляется микроплазменная контаминация. Хромосомный анализ клеток показывает, что они не имеют маркерных хромосом, по данным гистограммы модельный класс составляет 60 хромосом. Культуральные свойства: клетки культивируют в роллерносуспензионном или стационарном режимах с использованием питательной среды RPMI-1640, содержащей 15% сыворотки плода коров, 0,06% L-глутамина, 160 мкг/мл гентамицина, 100 мкг/мл канамицина. Посевная доза (5-8) х 105 кл/мл. Результаты культивирования представлены в таблице.
Как видно из приведенных в таблице данных, штамм клеток ЭВК-ИРА/3 при длительном непрерывном культивировании без подсева неинфицированных клеток сохраняет стабильную вируспродукцию и пролиферацию клеток, как при стационарном, так и при роллерно-суспензионном культивировании на протяжении по крайней мере 76 пассажей. Это доказывает возможность длительного культивирования данного штамма клеток в роллерно-суспензионном режиме с сохранением вируспродукции и характеризует его как технологичный штамм клеток-продуцентов ВИЧ-I.
Специфичность продуцируемого штаммом клеток ЭАК-ИРА/3 вируса подтверждают методами электронной микроскопии, вестерн-блота, ДНК-РНК гибридизации, непрямой иммунофлюоресценции (НИФ).
Электронная микроскопия клеток ЭВК-ИРА/3 (метод негативного контрастирования) показывает, что вирусные частицы, продуцируемые этими клетками, имеют размеры до 110 А и обладают морфологией, типичной для лентивирусов.
Методом вестерн-блота выявляют наличие вирусспецифических белков gp 120, gp 41, р 24 в лизате инфицированных клеток.
Наличие вирусспецифической РНК в культуре клеток ЭВК-ИРА/3 подтверждают методом ДНК-РНК гибридизации.
Метод непрямой иммунофлюоресценции с использованием сыворотки крови больного, содержащей антитела к ВИЧ-I, показывает наличие специфически светящихся инфицированных клеток (20-40% ) (специфическое свечение в виде перстня характерно для данного вируса).
Инфекционность продуцируемого вируса подтверждают путем заражения чувствительных к ВИЧ-I перевиваемых (ССRF (CЕМ), Н-9) и первичной культур лимфоцитов человека супернатантом культуральной вируссодержащей жидкости.
Криоконсервацию штамма осуществляют по общепринятой методике, используя среду RPMI-1640, содержащую 30-50% сыворотки плода коров, 10% глицерина или 10% диметилсульфоксида, 0,06% L-глутамина и антибиотики. Пролиферационные и вируспродуцирующие свойства штамма клеток полностью восстанавливаются к 3-5 пассажу после размораживания.
П р и м е р 1. Криоконсервирование маточной культуры клеток ЭВК-ИРА/3 - продуцента ВИЧ-I.
Для криоконсервирования берут культуру клеток на 3-4 сут. культивирования, оценивают ее по морфологическим признакам и жизнеспособности.
Клетки имеют типичную морфологию моноцитов человека, доля жизнеспособных клеток составляет 60-80% . Концентрацию клеток определяют с помощью камеры Горяева, предварительно окрашивая мертвые клетки 0,4% -ным раствором трипанового синего. Питательную среду для криоконсервирования готовят, приливая к 290±20 мл среды RPMI-1640 150±10 мл сыворотки плода коров, 10±1 мл 3% -ного раствора глутамина, 1,0±0,1 мл 30% -ного линкомицина, 50±2 мл стерильного глицерина высокой степени очистки, добавляя 80±10 мг гентамицина.
Для получения клеточной взвеси содержимое роллерной бутыли переносят в центрифужный стакан вместимостью 400 мл и центрифугируют при температуре 20±2оС и частоте вращения 800-1000 об/мин в течение 10 мин. Супернатант сливают, осадок клеток ресуспендируют в среде для криоконсервации, чтобы концентрация клеток составила (7-10)х106 кл/мл. Полученную клеточную взвесь разливают по ампулам, герметично запаивают их и помещают в 96% -ный охлажденный спирт. Криоконсервацию проводят в следующем режиме: снижают температуру по 1оС в 1 мин до минус 40оС, затем по 10оС в 1 мин до минус 70оС и помещают замороженные ампулы в жидкий азот, где они и хранятся.
П р и м е р 2. Восстановление штамма клеток ЭАК-ИРА/3 после размораживания.
Восстанавливают культуру в следующем режиме: ампулу вынимают из жидкого азота и помещают в водяную баню (40оС). Оттаявшую ампулу встряхивают, протирают спиртом и переносят содержимое в центрифужную пробирку, по каплям приливают ростовую среду при легком перемешивании. Клетки инкубируют 15 мин при комнатной температуре, затем цинтрифугируют в течение 10 мин при 800 об/мин, надосадочную жидкость удаляют, клеточный осадок ресуспендируют в свежей ростовой среде (до концентрации 1 млн. кл/мл). Клетки переносят в культуральный флакон и инкубируют в термостате при температуре 36-37оС в течение 1 сут. Через 1 сут клеточную суспензию центрифугируют при 800 об/мин в течение 5 мин для удаления погибших клеток. Осадок клеток ресуспендируют в свежей ростовой среде. Концентрация клеток должна составлять 1 млн. кл/мл. Клетки инкубируют в термостате при температуре 36-37оС в течение 4-5 сут. , в дальнейшем продолжают культивировать по описанному способу.
П р и м е р 3. Подтверждение стабильности репродукции ВИЧ-I в культуре клеток ЭВК-ИРА/3 при длительном культивировании.
Культивирование моноцитов человека ЭВК-ИРА/3 проводят в стационарном режиме (пластиковые матрасы вместимостью 250 мл) с интервалом пассирования 4-6 сут в течение нескольких месяцев.
Питательную среду для культивирования готовят следующим образом: к 415±20 мл питательной среды RPMI-1640 приливают 75±10 мл сыворотки плода коровы, 10±1 мл 3% -ного раствора L-глутамина, 1,0±0,1 мл 30% -ного раствора линкомицина (или канамицин 100 мкг/мл), 80±10 мг гентамицина.
При пассировании сливают примерно половину клеточной суспензии и добавляют такое же количество свежей готовой среды так, чтобы посевная концентрация клеток составила (5-8)х105 кл/мл. Культивирование проводят с соблюдением соотношения жидкой и газовой фаз 1: 5 соответственно при температуре 36-37оС в термостате в течение 4-6 сут.
В конце каждого пассажа определяют концентрацию и долю жизнеспособных клеток с помощью камеры Горяева с предварительным окрашиванием мертвых клеток 0,4% -ным раствором трипанового синего, отбирают пробы для анализа по 1 мл культуральной жидкости. Подготовку образцов для ИФА осуществляют путем инактивации ВИЧ-I добавлением к пробе твин 80 до его конечной концентрации 0,1% с последующей инкубацией при температуре 6±2оС не менее 24 ч. Из приготовленных таким образом препаратов готовят ряд двухкратных последовательных разведений, которые затем вносят попарно (100±1 мл) в лунки сенсибилизированных планшетов тест-системы "Вектор" и "Abbott". Дальнейшие операции и учет результатов производят в соответствии с инструкциями, прилагаемыми к тест-системам. За титр вирусного антигена принимают то конечное разведение исходного материала, в котором достоверно выявлялся антиген ВИЧ-I. Как правило, титр вирусного антигена в ИФА составляет 1: 32, 1: 64 (таблица).
Таким образом, впервые получен штамм моноцитов человека, постоянно продуцирующих ВИЧ-I. (56) Заявка Франции N 2572736, кл. С 12 N 7/00, 1985.
Патент США N 4647773, кл. С 12 N 7/00, 1986.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ культивирования штамма-продуцента вируса иммунодефицита человека I типа | 1988 |
|
SU1597388A1 |
| Способ получения антигена вируса иммунодефицита человека 1 типа | 1990 |
|
SU1717631A1 |
| ШТАММ КУЛЬТУРЫ КЛЕТОК ЧЕЛОВЕКА НТНIV 27 - ПРОДУЦЕНТ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 1994 |
|
RU2067116C1 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА I ТИПА, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ ТЕСТ-СИСТЕМ | 1992 |
|
RU2046138C1 |
| Ингибитор размножения вируса иммунодефицита человека | 1990 |
|
SU1804848A1 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ПЕРВОГО ТИПА | 2008 |
|
RU2375073C1 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 1997 |
|
RU2144956C1 |
| ШТАММ ПЕРЕВИВАЕМЫХ КЛЕТОК ЧЕЛОВЕКА СЕМ-К, УСТОЙЧИВЫЙ К ВИЧ-ИНФЕКЦИИ | 1995 |
|
RU2102477C1 |
| Способ титрования вируса иммунодифицита человека | 1988 |
|
SU1696474A1 |
| СПОСОБ ИНГИБИРОВАНИЯ РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 1997 |
|
RU2136752C1 |
Изобретение относится к вирусологии, биотехнологии, в частности к культивированию вирусов, а именно получению клеточной линии - продуцента вируса иммунодефицита человека 1 типа (ВИЧ - 1) для решения задач разработки и совершенствования диагностических и вакцинных препаратов против вируса СПИД. Целью изобретения является получение технологического штамма клеток-продуцентов ВИЧ - 1, обладающего высоким и стабильным уровнем вируспродукции и не требующего при культивировании специальной питательной среды с дорогостоящими добавками. Перевиваемый штамм моноцитов человека ЭВК - ИРА/3 - продуцент вируса иммунодефицита человека 1 типа получен на основе трансформированных клеток моноцитов человека (штамм клеток - 937) путем заражения ВИЧ - 1, выделенным от больного СПИД, клонирования и выделения клона клеток, хронически инфицированных ВИЧ - 1, постоянно продуцирующих этот вирус. Полученный штамм клеток-продуцентов ВИЧ - 1 ЭВК - ИРА/3 стабилен при культивировании (не требует подсева неинфицированных клеток), неприхотлив (не требует культивирования в атмосфере CO2, специальных питательных сред с дорогостоящими добавками), технологичен, так как выдерживает длительное непрерывное культивирование в роллерно-суспензионном режиме. Музейная закладка штамма клеток ЭВК - ИРА/3 хранится в коллекции Института вирусологии им. Д. И. Ивановского N 4005 и в коллекции ВНИИ молекулярной биологии. 1 табл.
Штамм перевиваемых клеток моноцитов человека ГКВ N4005 - продуцент вируса иммунодефицита человека 1 типа.
Авторы
Даты
1994-01-30—Публикация
1988-08-08—Подача