Изобретение относится к ветеринарии, в частности к биологически активным препаратам, обладающим противовирусной активностью, способам их получения и применения, предназначенным для профилактики и лечения инфекционных и незаразных болезней, повышения продуктивности лошадей.
Известны биопрепараты, способы их получения и применения, обладающие противовирусной активностью и обеспечивающие повышение сохранности и продуктивности лошадей. Это вакцины, гипериммунные сыворотки, препараты иммуноглобулинов, интерферонов.
В качестве аналогов наиболее предпочтительным по сути изобретения являются препараты интерферона, способы его получения и применения [1,2]
Недостатком известных способов получения и применения препаратов интерферонов (лейкоцитарных) является низкая активность (титр 1:256-1:512), что требует существенного повышения производства при широком применении для лошадей. Технология получения препаратов интерферонов (лейкоцитарных) не позволяет получить нативные препараты с активностью более 1:103.
Целью изобретения является обеспечение повышения противовирусной активности препарата и увеличение эффективности его производства и применения.
Поставленная цель достигается определением эффективной композиции препарата, высокоэкономичной и производительной технологией изготовления и оптимальной схемой применения.
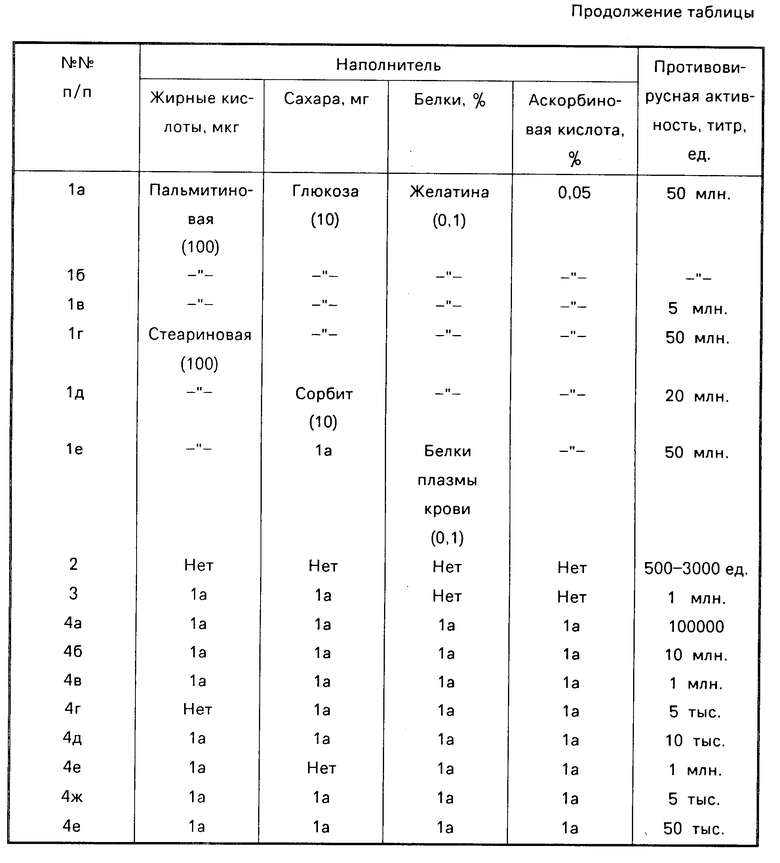
Сущность изобретения заключается в следующем. Биологически активный препарат для лошадей состоит из продуктов культивирования индуцированных лимфоидных клеток лошадей при следующем соотношении компонентов (в сухом препарате), мас. белки 5,0-60,0; аминокислоты 1,6-5,0; жирные кислоты 0,11-12,0; сахара 2,0-20; аскорбиновая кислота 0,6-10; вода 1-5; соли до 100. Противовирусная активность препарата (титр) составляет 1:500-1:108.
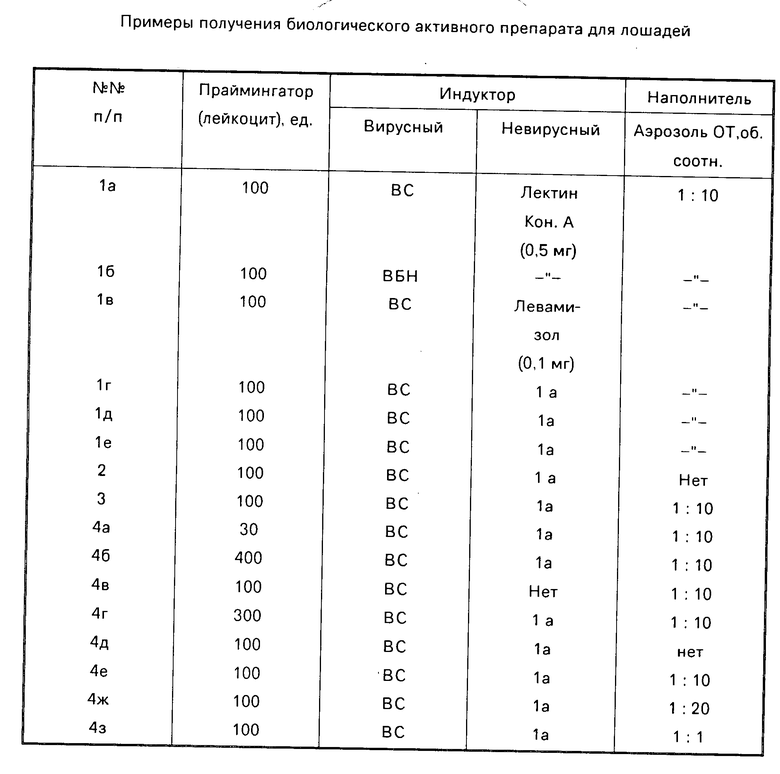
Препарат получают при культивировании в течение 12-72 ч лимфоидных клеток (селезенки, крови, лимфоузлов) лошадей в присутствии вирусных (ВБН, ВС) и невирусных (лектины, энтеротоксины и др.) индукторов с последующим концентрированием белков и внесением жирных кислот и сахаров и объединением фракций неконцентрированных и концентрированных продуктов в соотношении 1: 1-10000: 1 с добавлением наполнителей. Получаемый таким образом препарат с охарактеризованными свойствами (по противовирусной активности) эффективен по применению в лечебных и профилактических дозах (соответственно 106 и 104 ед. ) при парентеральном или интраназальном введении лошадям.
П р и м е р 1 (оптимальный вариант). Биологически активный препарат получают следующим образом.
1 стадия. Культивируют лимфоидные клетки (селезенки, крови, лимфоузлы) лошадей (10-60 млн.клеток/см3) при добавлении последовательно лейкоцитарного интерферона лошадей (50-200 ед/см3), инсулина (0,0020 ед/см3), невирусных индукторов (лектины, например, конканавалин А (Кон. А 0,5-1 мг/л); фитогемагглютинин (ФГА 10-20 мг/л); энтеротоксины (липополисахариды) 0,05-0,1 мг/л; левамизол, другие производные тиозола 0,1 мг/см3 или другие) и/или вирусных индукторов (вирус болезни Ньюкастла (ВБН 10-40 ТЦД50/см3 на клетку; вирус Сендай 10-30 ТЦД50/см3 на клетку). Продукты культивирования индуцированных клеток (режим биосинтеза 12-72 ч при 36,5-37,5оС, концентрация клеток 2-18 млн. клеток/см3 в перемешивающейся суспензии, питательные среды типа 199, РПМИ-1640) центрифугируют. В случае применения вирусных индукторов центрифугат подкисляют до рН 2,5 и выдерживают не менее 72 ч, затем рН выравнивают до 6,0-6,5 добавлением растворов КОН или NaOH. Далее фильтруют через стерилизующие фильтры и часть фильтрата (1-10-) лиофилизуют.
2 стадия. Лиофилизованный полупродукт растворяют в буферном боратном растворе (10 мг/см3) и вносят в соотношении 1:10 в раствор поверхностно-активных веществ, например 0,2-0,4 М раствор аэрозоля ОТ (натриевая соль ди-2-этилгексилового эфира сульфоянтарной кислоты), а затем добавляют раствор жирной кислоты (например пальмитиновая, стеариновая) (10-1000 мкг) и насыщенный раствор сахаров (например глюкоза, сорбит и др.) в количестве 2-20 мг. Далее к системе добавляют избыточное количество (1-5-кратное) ацетона и выпавший осадок промывают 3-5 раз ацетоном. Последний удаляют испарением.
3 стадия. Объединяют часть препарата, полученного на 1 стадии, и растворенную в физиологическом растворе (буфер) часть препарата, полученную на 2 стадии в соотношении 2:1-1:1 (соотношение белковой фракции в частях 1:1-10000: 1), добавляют желатину или белки плазмы крови до конечной ее концентрации 0,1-1% аскорбиновую кислоту (до конечной концентрации 0,03-0,3%) и используют либо в жидком виде, либо в лиофилизованном виде.
Состав композиции следующий, мас. Белки 5,0-60,0 Аминокислоты 1,6-5,0 Жирные кислоты 0,10-12,0 Сахара 2,0-20,0
Аскоpбиновая кислота 0,6-10 Вода 1-5 Соли До 100
Противовирусная активность (титр) 1:500-1:100000000 (500-100 млн.ед.).
П р и м е р 2 (отрицательный вариант, пример 2 по таблице).
Препарат получают таким способом, как описано в примере 1, но используют только процедуры, изложенные в 1 стадии.
Противовирусная активность препарата в этом случае не превышает (титр) 1:500-1:1000 (500-1000 ед.). В составе препарата нет жирных кислот, сахаров, аскорбиновой кислоты.
П р и м е р 3 (недостаточно эффективный вариант, пример 3 по таблице).
Препарат получают так как описано в примере 1, но используют только процедуры, изложенные в стадиях 1 и 2 (без третьей стадии).
Противовирусная активность препарата составляет 105-107 ед/мг. В составе препарата отсутствует 60-90% белка, 100% аскорбиновой кислоты. Получаемый препарат в 10-100 раз менее активен, чем при изготовлении по технологии, изложенной в примере 1. Еще один недостаток препарат можно расфасовывать только в сухом виде, что технологически крайне сложно.
П р и м е р 4 (см.таблицу).
П р и м е р 5. Препарат получают, как описано в примере 1, но содержание белка менее 5,0% В этом случае не достигается необходимой активности препарата (104-107 ед.) из-за потери противовирусной активности в процессе приготовления препарата потеря активности в 100-1000 раз. При повышении концентрации белка свыше 60,0% в препарате технологический процесс получения препарата является экономически нецелесообразно в этом случае время лиофилизации превышает 82 ч, что приводит к большим энергетическим затратам.
П р и м е р 6. Препарат получают, как описано в примере 1, но содержание жирных кислот менее 0,10% В этом случае не достигается получения активности препарата выше 1000 ед. что не обеспечивает необходимой активности препарата (104-108 ед.). При повышении концентрации жирных кислот выше 12,0% в препарате наблюдается снижение активности препарата в 100 раз и более.
П р и м е р 7. Препарат получают, как описано в примере 1, но содержание сахаров (например глюкоза, манноза, сорбит и др.) менее 2,0. При этом получаемый на 2 стадии полупродукт является малорастворимым, что не обеспечивает получение препарата с активностью выше 1000 ед. При повышении концентрации сахаров свыше 20% наблюдается снижение активности препарата в 10 раз и более (очевидно за счет блокирования мембрано-активных противовирусных компонентов препарата).
П р и м е р 8. Препарат получают, как описано в примере 1, но содержание аскорбиновой кислоты менее 0,6% В этом случае при хранении продукта свыше 1 месяца наблюдается постепенное снижение активности препарата в 10 раз и более. При повышении концентрации аскорбиновой кислоты свыше 10% наблюдается снижение активности препарата в 15-20 раз и более.
П р и м е р 9. Препарат под названием эквовирэкс с активностью (противовирусной, титр) 1000-1000000 ед. применяют с целью повышения уровня неспецифического иммунитета, стимуляции роста и развития, профилактики и лечения инфекционных и незаразных болезней лошадей (болезни органов дыхания, желудочно-кишечного тракта, например грипп, инфекционная анемия и др.) путем интраназального или внутримышечного введения в дозе 2-4 мл один-два раза в сутки в течение 2-3 дней или двукратно через 48 ч или через 48 ч после вакцинаций в дозе 2-4 мл.
При снижении активности препарата менее 1000 ед. применение его по указанной схеме является менее эффективным. В этом случае сохранность лошадей повышается не более, чем на 5% в прирост массы тела на 5% (экономическая целесообразность).
При повышении активности препарата (эквовирэкса) свыше 105 ед. применение его с профилактической целью является экономически нецелесообразным (из-за повышенного расхода препарата).
П р и м е р 10. Препарат под названием эквовирэкс-вак с активностью (противовирусной, титр) 105-108 ед. применяют для лечения болезней лошадей (перечислены в описании примера 9) в комплексе с антибиотиками, витаминами, другими препаратами путем парентерального введения один раз в сутки в дозе 4 мл в течение 3-4 дней.
При снижении активности препарата менее 100000 ед. применение его по указанной схеме является менее эффективным. В этом случае не обеспечивается снижение заболеваемости лошадей свыше 20% например при инфекционной анемии, гриппе (экономическая целесообразность). А применение по этой же схеме эквовирэкс-вака с активностью свыше 108 ед. для лечебных целей является экономически нецелесообразным (из-за повышенного расхода препарата).
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ ТЕЛЯТ | 1992 |
|
RU2034566C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ СОБАК | 1992 |
|
RU2034567C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ ОВЕЦ | 1992 |
|
RU2034569C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ КРОЛИКОВ | 1992 |
|
RU2034568C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ КУР И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ КУР | 1992 |
|
RU2034565C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ ДЛЯ НОРОК | 1992 |
|
RU2034571C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2050854C1 |
| Способ получения препарата для перорального введения | 1989 |
|
SU1637808A1 |
| РАСТВОР ПРОТИВОВИРУСНОЙ КОМПОЗИЦИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2499601C1 |
| Способ подавления репродукции вирусов | 1989 |
|
SU1730144A1 |
Использование: в ветеринарии, в частности в биологически активных препаратах для профилактики и лечения вирусных заболеваний у лошадей. Сущность изобретения: препарат содержит, мас.%: белки 5 - 60; аминокислоты 1,6 - 5; жирные кислоты 0,1 - 12; сахара 2 - 20; аскорбиновая кислота 0,6 - 10; вода 1 - 5; соли минеральных кислот - остальное. Препарат получают культивированием вирус- или невирус-индуцированных лимфоидных клеток лошадей с последующей фильтрацией. Далее одну часть фильтрата лиофилизируют, растворяют в буферном растворе и вносят (1 : 10) в раствор аэрозоля ОТ, добавляют жирные кислоты ( 10 - 1000), сахара (2 - 20 мг) и смешивают с 2 - 5-кратным раствором ацетона. Полученный осадок растворяют в физиологическом растворе, смешивают с второй частью фильтрата и леофилизируют. Препарат с активностью 10 тыс. ед. для профилактики болезней вводят 2 - 3-кратно интераназально, или парентерально в дозе 2 - 4 мл, а для лечения с активностью 1 млн. ед. вводят 3 - 4-кратно в дозе 4 мл. 3 с. и 2 з.п ф-лы, 1 табл.
Белки 5,0 60,0
Аминокислоты 1,6 5,0
Жирные кислоты 0,10 12,0
Сахара 2,0 20,0
Аскорбиновая кислота 0,6 10,0
Вода 1,0 5,0
Соли минеральных кислот Остальное
2. Способ получения биологически активного препарата для лошадей из сырья животного происхождения, включающий инкубирование его в питательной среде с индуктором с последующим выделением, отличающийся тем, что в качестве сырья животного происхождения используют лимфоидные клетки лошадей, которые культивируют в присутствии индукторов как вирусных, так и невирусных в течение 12 72 ч, полученную суспензию центрифугируют, фильтруют через стерилизующие фильтры, фильтрат разделяют на 2 части: одну часть в количестве 1 10% лиофилизуют, растворяют в боратном буферном растворе из расчета 10 мг/см3 и вносят в соотношении 1 10 в 0,2 0,4 М раствор аэрозоля натриевой соли ди-2-этилгексилового эфира сульфоянтарной кислоты, добавляют 10 1000 мкг жирной кислоты, 2 20 мг сахара и осаждают 1 5-кратным количеством ацетона, полученный осадок, растворенный в физиологическом растворе, смешивают с второй частью фильтрата в соотношении 1 1 2, добавляют белки плазмы крови и/или желатину до конечной концентрации 0,1 - 1,0% аскорбиновую кислоту до конечной концентрации 0,03 0,3% и лиофилизуют.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Лазарева Д | |||
| и Алехин Е | |||
| Стимуляторы иммунитета | |||
| М.: Медицина, 1985, с.285. | |||
Авторы
Даты
1995-05-10—Публикация
1992-02-13—Подача