Изобретение относится к области получения новых соединений - сложных эфиров 7нитро-8-оксихинолина, обладающих ценными фармакологическими свойствами. Известен способ получения эфиров окагхинолина взаимодействием ундециловой кислоты или ее производных - ангидрида или хлорангидрида с 8-аксихинолином.
Однако П:ри этом получают только один определенный эфир 8-оксихинолина. Иопользуя способ-аналог и применив в качестве исходных соединений другие кислоты, авторы синтезировали очень разнообразные по своему строению сложные эфиры З-оксихинолина. Описываемый способ получения сложных эфиров 7-нитро-8-оксихинолина формулы:
ненасыщенный, имеющий прямую или разветвленную цепь,
R - атом водорода, арил или остаток формулы:
г
10
K1
где RI и R2 - атом водорода, галоид, нитро-, ОКСИ-, амино-, алкоксигрулпа или алкил, или если RI -атом водорода, то R2 - фенил, феНОКСИ-, фенилтио- или алкилтиогруппа или остаток формулы: 25 -ч. где Ra, R4, R5-aлкил или алкоксигруппа, Rg - атом водорода или Rs, R4, Rs, R6-aлкил или
СбН,
где R - атом водорода или атом хлора, Ra- атом водорода, метил, галоид или нитрогруппа, Rg - атом водорода «ли фенил, Rio - атом водорода, метил или NH2-групла, Rn-агом водорода, или метил, Ri2-атом водорода, метил или алкоксигруппа, кислород, сера или NH - группа, заключается в том, что 7-нитро-8-оксихиноли,н подвергают взаимодействию с кислотой формулы:
R-X-СООН.
где R и X имеют вышеуказанные значения, с выделением целевого продукта известными приемами.
7-нитро-8-оксихи,нолин получают гидролизом 7-нитро-8-ок€ихинолин-5-1сульфокислоты.
Известно, что 7-нитро-8-оксих.инолин-5-сульфокислота может быть получена нитрованием 8-окоихинолин-5-сульфокислоты. Одна.ко, в прежних условиях, нитрование было мало эффективным и значительные количества 5,7динитро-8-оксихинолина образовывались в качестве побочного продукта. Тенерь же обнаружилось, что побочный продукт образуется в существенно ничтожных количествах, когда
нитрование проводится при температуре от -5° С до 4-5° С. Кроме того, нитрование лучше проводить добавлением по каплям 30- 50%-го водного раствора азотной кислоты к охлажденному раствору 8-оксихинолин-5сульфокислоты в концентрированной серной кислоте в течение 4-8 час.
Пример 1. 7-нитро-8-оксихинолин-5-сульфокислота.
45 г (0,2 моля 8-аксихи,нолин-5-сульфокислоты растворяют в 126 мл холодной концентрированной серной кислоты. Поддерживая температуру этого раствора в пределах от -5°С до +5°С, 77 мл 30-50%-го водного раствора азотной кислоты добавляют в течение 8 час. Реакционную смесь выливают затем на 400 г льда.
Образовавшийся осадок собирают фильтрацией и промывают В:одой. Получают 43-48 г сырого 7-нитро-8-оксихинолин-5-сульфокислоты, плавящейся при 264° С с разложением (80-90% от теоретического выхода). Этот продукт используют для последующей стадии, без очистки, хотя в пем содержится небольшое количество 5,7дин,итро-8-ок10ихинолина. 7-нитро-8-оксихинолин.
Раствор 54 г 7-нитро-8-оксихинолин-5-сульфокислоты нагревают в 290 мл 60%-ной серной кислоты в течение 6 час. при температуре
150° С. Раствор сливают на 500 г льда, фильтруют для удаления 5,7-динитро-8-оксихинолина (5-10 г; исходный материал содержит эту примесь). Подд-ерживая температуру ниже 20° С, фильтрат нейтрализуют при рН 5-6
щелочью, такой как NaOH или NH4OH.
Осадок собирают центрифугированием и сушат. О.Н плавится при температуре 162- 163°С после кристаллизации из 40% уксусной кислоты. Выход: 27-30 г (70-80% от теоретического).
Анализ: найдено в % С 56,76; П 3,41; N 14,65.
Рассчитано для CgHgNaOa: С 56,84; Н 3,18; N 14,73.
Следующие примеры иллюстрируют способ получения 7-нитро-8-оксих,инолиновых сложных эфиров.
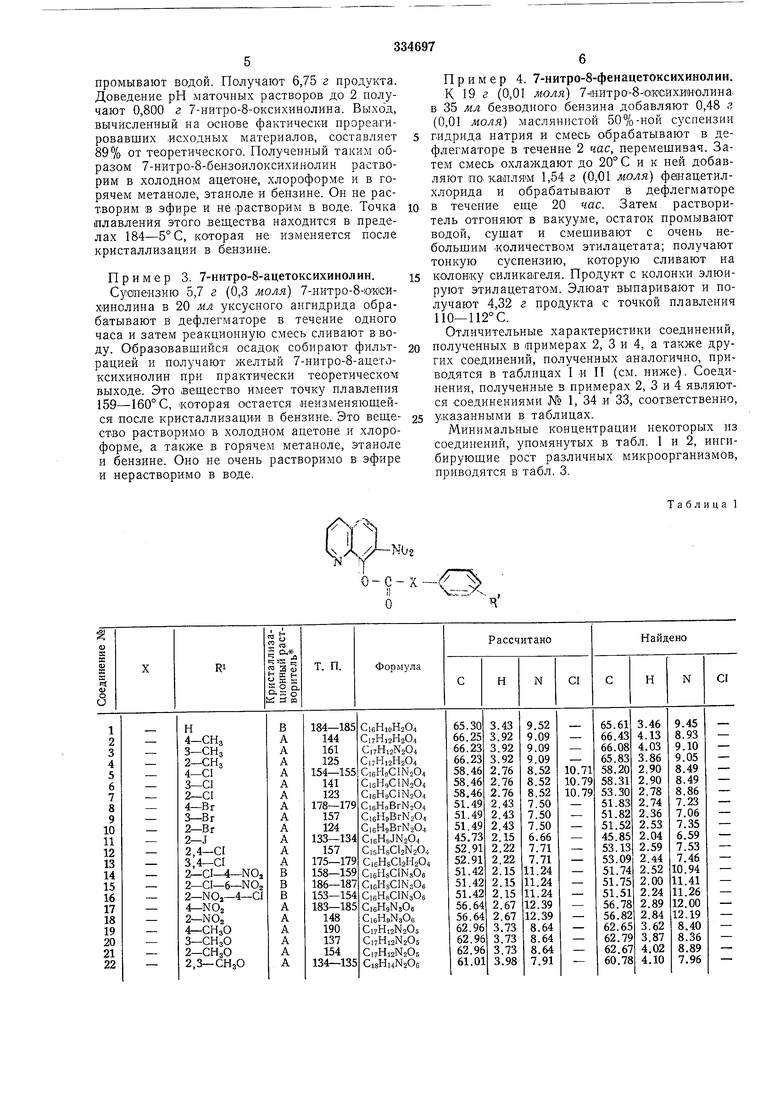
Пример 2. 7-нитро-8-бензоилоксихинолин. К раствору 5,7 г (0,03 моля) 7-нитро-8-оксихинолина в 50 мл пиридина, охлажденного до 15° С, приливают по каплям 4,2 г (0,03 моля) бензОилхлорида в течение 5 мин. Смесь выдерживают при температуре 15° С в течение 3 час, затем сливают в холодную воду. Обрапромывают водой. Получают 6,75 г продукта. Доведение рН маточных растворов до 2 получают 0,800 г 7-нитро-8-оксихинолина. , вычисленный на основе фактически прореагировавших исходных материалов, составляет 89% от теоретического. Полученный таким образом 7-нитро-8-|бензоиЛОксихинолин растворим в холодном ацетоне, хлороформе и в горячем метаноле, этаноле и бензине. Он не растворим в эфире и не .растворим в воде. Точка |Плавления этого .вещества находится в пределах 184-5° С, которая не изменяется после кристаллизации в бензине. Пример 3. 7-нитро-8-ацетоксихинолин. Суонензию 5,7 г (0,,3 толя} 7-.нитро-8-1о«сихинолина в 20 мл уксусного ангидрида обрабатывают в дефлегматоре в течение одного часа и затем реакционную смесь сливают в воду. Образовавшийся осадок собирают фильтрацией и получают желтый 7-нитро-8-ацетоксихинолин при практически теоретическом выходе. Это ,веш;ество имеет точку плавлепия 159-160° С, которая остается «еизменяюшейся после кристаллизации в бензине. Это вещество растворимо в холодном ацетоне и хлороформе, а также в горячем метаноле, этаноле и бензине. Оно не очень растворимо в эфире и нерастворимо в воде. Пример 4. 7-нитро-8-фенацетоксихинолин. К 19 г (0,01 моля 7чЕИтро-8- 01исихииолина в 35 мл безводного бензина добавляют 0,48 . (0,01 моля) маслянистой 50%-ной суспензии гидрида натрия и смесь обрабатывают в дефлегматоре в течение 2 час, перемешивая. Затем смесь охлаждают до 20° С и к пей добавляют по. каплям 1,54 г (0,01 моля} фанацетилхлорида п обрабатывают в дефлегматоре в течение еш,е 20 час. Затем растворитель отгоняют в вакууме, остаток промывают водой, сушат и смешивают с очень небольшим .количеством этилацетата; получают тонкую суспензию, которую сливают на колонку силикагеля. Продукт с колонки элюируют этил ацетатом. Элюат выпаривают и получают 4,32 г продукта с точкой плавления 110-112°С. Отличительные характеристики соединений, полученных в примерах 2, 3 и 4, а также других соединений, полученных аналогично, приводятся в таблицах I и П (см. ниже). Соединения, полученные в примерах 2, 3 и 4 являются соединениями № 1, 34 и 33, соответственно, указанными в таблицах. Минимальные концентрации некоторых из соединений, упомянутых в табл. 1 и 2, ипгибирующие рост различных микроорганизмов, приводятся в табл. 3.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных бензола или их солей | 1968 |
|
SU443509A1 |
| Добавка к корму или питьевой воде для домашней птицы | 1970 |
|
SU561492A3 |
| Способ получения производных индолилуксусной кислоты или их солей | 1971 |
|
SU503517A3 |
| Способ получения производных имидазола | 1972 |
|
SU446505A1 |
| Способ получения фенилгидразонов, а также их физиологически переносимых солей | 1990 |
|
SU1826967A3 |
| ДИАЗОТИПНЫЙ МАТЕРИАЛ | 1971 |
|
SU311473A1 |
| Способ получения производного хинолина или его соли | 1989 |
|
SU1838301A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ГОМОПИРИМИДАЗОЛА ИЛИ ИХ СОЛЕЙ | 1969 |
|
SU415877A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ БЕНЗИМИДАЗОЛОВ | 1969 |
|
SU237735A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФЕНОКСИ-2-ГИДРОКСИ-3- ЦИКЛОАЛКИЛАМИНОПРОПАНОВ ИЛИ ИХ СОЛЕЙ | 1972 |
|
SU327664A1 |

о-с-х-е
liv:,r,,-
ОR
Продолжение табл. I
А - этилацетат; В -бензин; D -диоксан; L -лигроин.
Про яолжение табл. 1
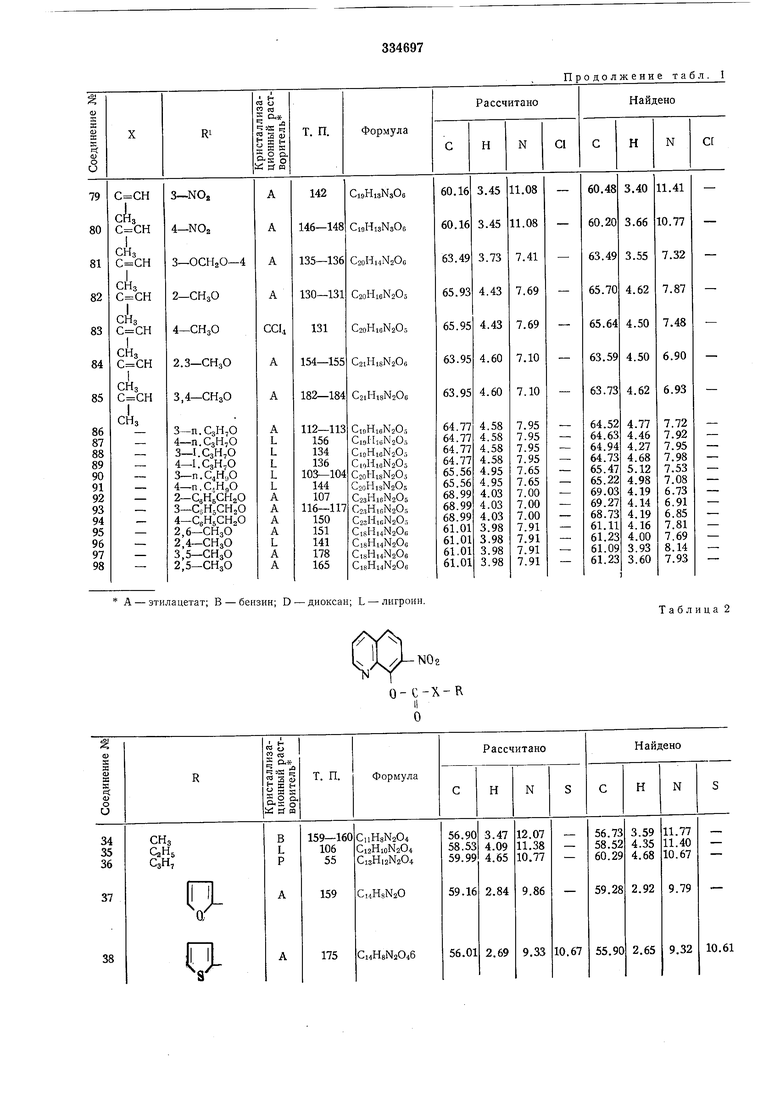
Таблица 2
МОг
Прод олжение табл. 2 А -
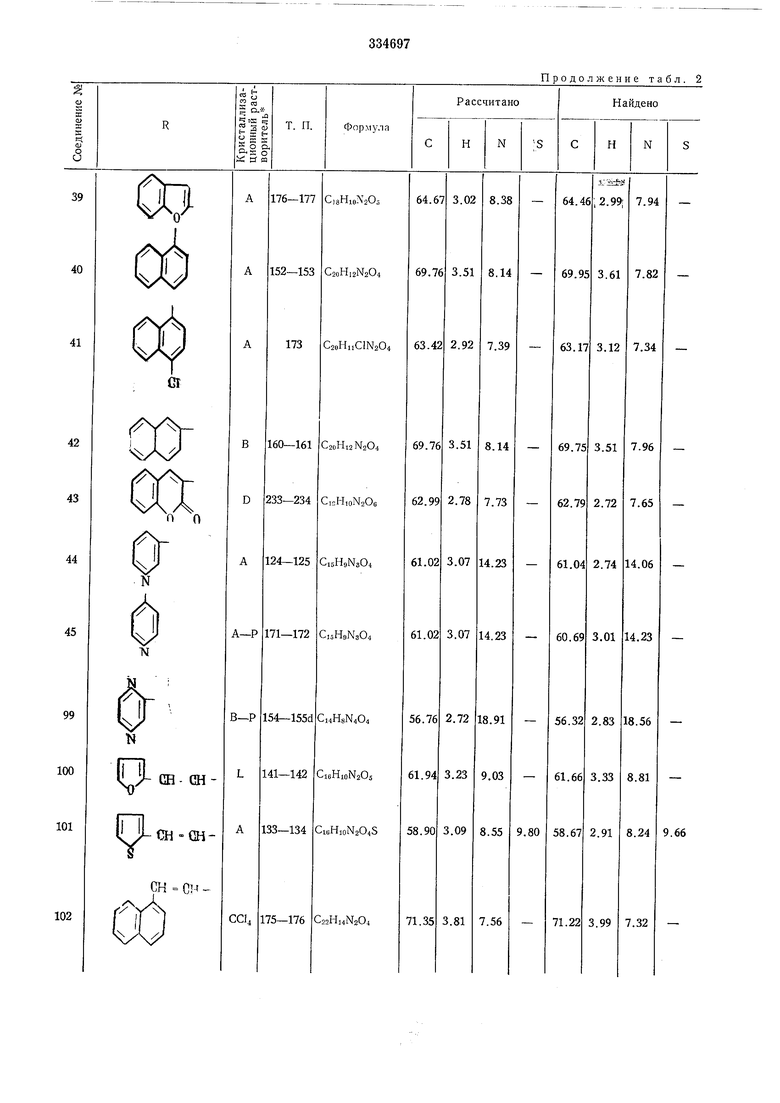
Продолжение табл. 2
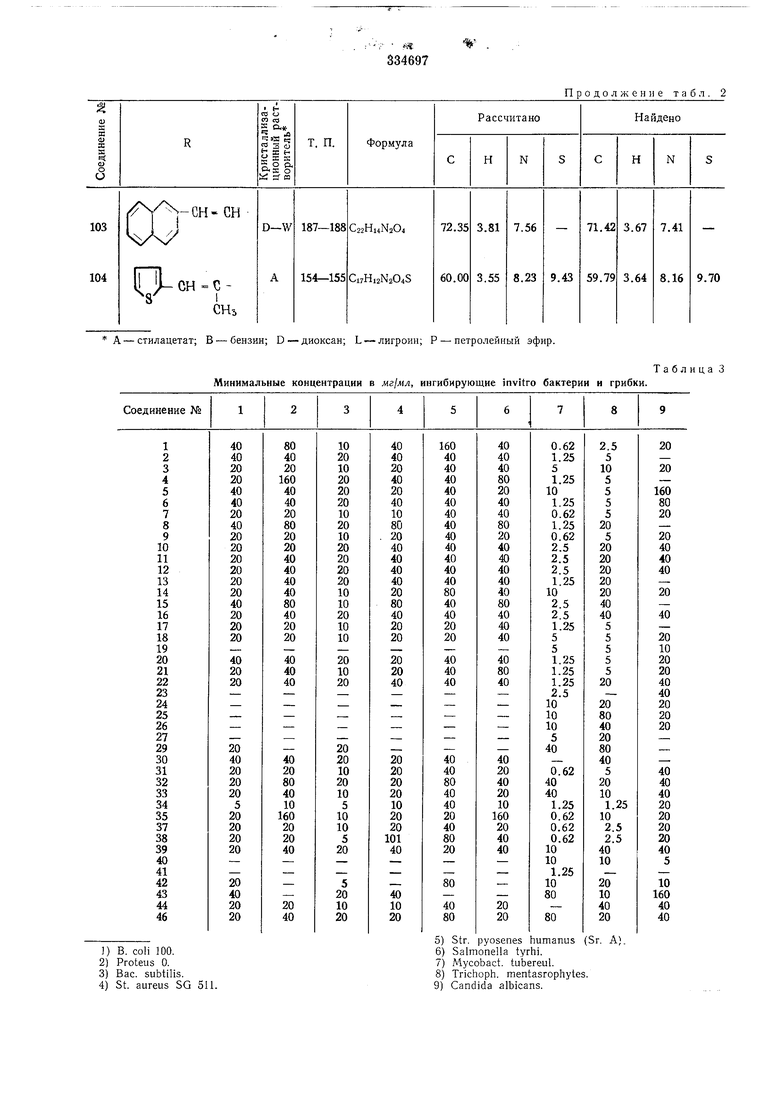
5)Str. pyosenes humanus (Sr. A). стилацетат; В -бензин; D-диоксан; L - лигроин; Р - петролейный эфир. Минимальные концентрации в мг1мл, ингибирующие invitro бактерии и грибки. Таблица 3
г
15
г
16
Предмет изобретения
Способ получения сложных эфиров 7-нитро-оксихинолипа формулы:
где X - простая связь или углеводородный остаток алифатического ряда, насыщенный или ненасыщенный, имеющий прямую или разветвленную цепь;
R - атом водорода, арил или остаток формулы:
Ra
{/
оде RI и Ra-aTCM водорода, галоид, нитро-, окСИ-, амине-, алкоксигруппа или алкил, или, если Ri-атом водорода, то Н2-фенил, фенокси-, фенилтио- или алкилтиогруппа, или остаток формулы:
Кз
//
5
ЬБ
«ЭR9
N
е л
КПк ш
где Rs, R4, R5-aлкил или алкоксигруппа, Reатом водорода .или Rs, R4, Rs, R6-aлкил, Или R-замещенные или незамещенные гетероциклические остатки формул:
где R -атом водорода или атом хлора, Ra- атом водорода, метил, галоид или нитрогруппа, Rg - атом водорода или фенил, Rjo-атом водорода, метил или NH2-rpynna, Ru - атом водорода или метил, Ri2 - атом водорода, метил или алкоксигруппа, Z - кислород, сера или NH-rpynna, отличающийся тем, что 7-нитро-8-оксихинолин подвергают взаимодействию с кислотой формулы:
R-X-СООН,
где R .и X имеют вышеуказанные значения, с выделением целевого продукта известными приемами.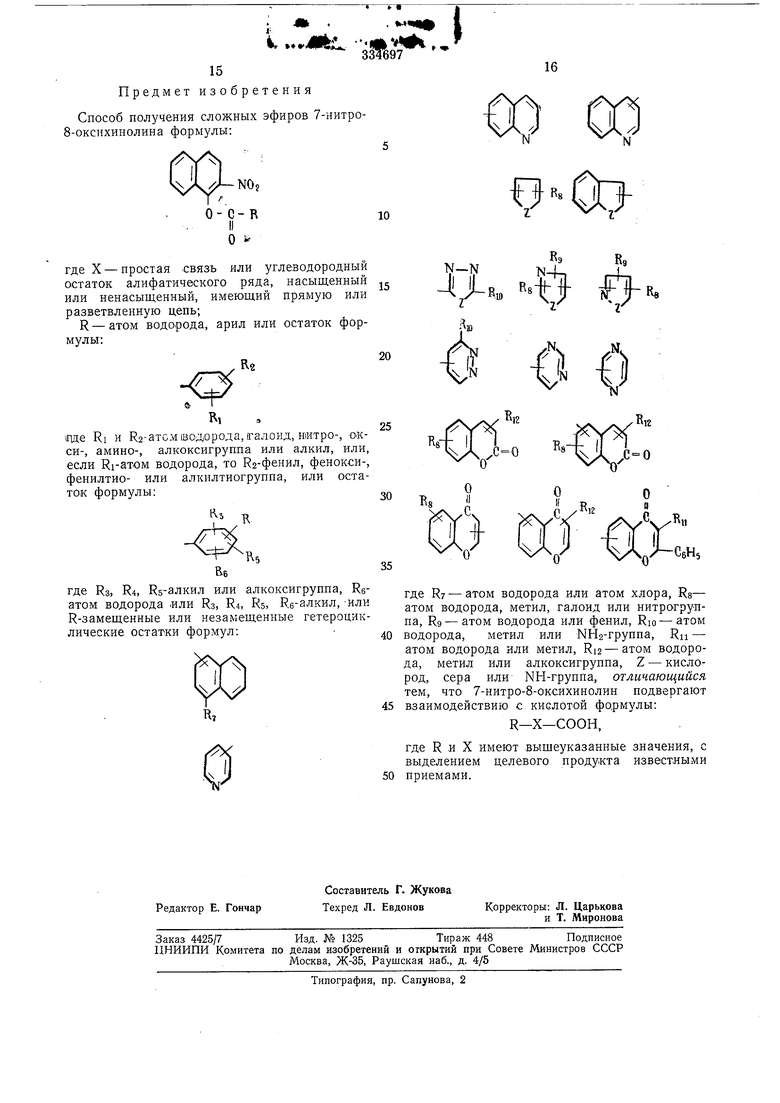
Даты
1972-01-01—Публикация