Изобретение относится к новым антибактериальным композициям в виде фармацевтических препаратов, пищевых составов для людей и животных кормов, которые должны использоваться для терапевтической и/или профилактической обработки при инфекциях, вызванных Streptococcus pneumoniae и/или Heamophilus influenzae.
Предметом данного изобретения является получение композиций для профилактической и/или терапевтической обработки для лечения инфекционных заболеваний, вызванных Streptococcus pneumoniae и Heamophilus influеnzae в верхних дыхательных путях, например, инфекций носоглотки, а также в нижних дыхательных путях, например, легких, за счет предотвращения адгезионного связывания этих бактерий и/или их умертвления.
Гликоконьюгаты взаимодействуют специфически с микробными лектинами, например белками оболочки вируса, бактериальными адгезинами и токсинами. Специфичность этого взаимодействия обеспечивается сахаридными последовательностями, например, CMI ганглизидом, распознаваемым токсином холеры Gal1 ->> 4Gal; распознаваемым уропатогенным E.coli или GlC NAc1-3Gal, распознаваемыми Streprococcus pneumoniae. При связывании оболочки гликоконьюгаты действуют как рецепторы и взаимодействие их, например с бактериями приводит в результате к их связыванию с несущей рецептор клеткой. При секретировании эти олигосахаридные последовательности имеют другие функции. Например, присутствие в наружных секрециях олигосахаридных последовательностей, соответствующих клеточно-связанным рецепторам, обеспечивает основу для конкурентного ингибирования микробного связывания. Поскольку связывание с эпиталиальными клетками является очень важным фактором для патогенеза многих бактериальных инфекций, то ингибирование связывания секретируемыми олигосахаридами может обеспечить защиту от инфекции.
Человеческое молоко является богатым источником свободных олигосахаридов и гликоконьюгатов. Человеческое молоко ингибирует связывание носоглоточных эпителиальных клеток S. pneumoneai и H.influenzae в условиях "ин витро". В фракции свободного олигосахарида были идентифицированы ингибиторы пневмококкового связывания, как это можно было предвидеть из содержания их в лакто- и неолактотетразе с известной активностью рецептора для пневмококков.
Другие компоненты с мол.массой > 5000 Дальтон, но неиммуноглобулинового происхождения также взаимодействуют с S.pneumoniae и H.influenzae. В настоящем изобретении описывается идентификация этих неиммуноглобулиновых компонентов в высокомолекулярной фракции человеческого молока, такой как казеин.
Впервые была обнаружена возможность улучшения антибактериального эффекта против инфекций, вызванных S.pneumoniae и/или H.influenzae, путем ввода с профилактической или лечебной целью композиции, включающей казеин, наряду с общеизвестными инертными пригодными для использования наполнителями и носителями или питательными веществами. Другие отличительные особенности данного изобретения будут ясны из формулы изобретения.
Термин "молоко", используемый в данном описании, означает либо созревшее молоко, либо молозиво, если не оговорено особо. Используемое молоко может быть человеческим, свиным, коровьим, буйволовым, овечьим, козьим, верблюжьим или кенгуру.
Бактерии. Во всех данных экспериментах используются S.pneumoniae (CCUG 3114) и H.influenzae (Hi 198). Эти штаммы первоначально были выделены из носоглотки детей с частыми приступами острого отита. CCUG 3114 (капсулярного типа 6А) был ранее использован как модельный штамм при исследованиях, определяющих олигонуклеотидное связывание и рецепторную специфичность пневмококка. Данные штаммы сохранились лиофилизированными. Лиофилы перенеслись в кровяной агар (CCUG 3114) или в чашки с агаровой средой Левинталя (Н 198). CCUG 3114 культивировался в течение 10 ч при температуре 37оС в жидкостной среде, извлекался путем центрифугирования с ускорением центрифуги 1500xg в течение 15 мин и суспензировался в 1 мл 0,85%-ного NaCl с 1% холина, H.influenzae Hi 198 культивировался в течение 4 ч в среде гомофилуса, извлекался путем центрифугирования и суспензировался в солевом растворе фосфатного буфера, PBS (Hi 198).
Молоко. Для питательных целей использовалась порция человеческого молока от здоровой женщины-донора, когда оно было созревшим. Свиное молоко было получено со свинофермы от здоровых животных, и доение свиноматок осуществлялось вручную. Коровье молозиво и созревшее коровье молоко получали на молочной ферме. Созревшее молоко центрифугировали с ускорением центрифуги 2500 в течение 15 мин, и жир удаляли.
Ингибирование адгезии. Эпителиальные клетки из ротовой части глотки здоровых доноров (105 мм) смешивались с бактериальными суспензиями (109/мл). После центрифугирования с ускорением 400x g и инкубирования бактерий и эпителиальных клеток несвязанные бактерии удалялись для повторных циклов центрифугирования с ускорением центрифуги 100x g и повторного суспензирования в NaCl с 1% холина.
Испытание на ингибирующее действие молока и компонентов молока осуществлялось путем предварительного инкубирования бактерий в течение 30 мин при 37оС. Затем вводились эпителиальные клетки и продолжалось испытание на адгезионное связывание. Число бактерий, связанных с эпителиальными клетками, подсчитывали с помощью интерференционной контрастной микроскопии (микроскоп Orpolux 11) с интерференционным контрастным устройством ТЕ Leitz, Wetzbar ФРГ. Связывание определялось, как среднее число бактерий на клетку для 40 эпителиальных клеток. Ингибирование определялось в процентах от величины контрольного буфера. EID50 это эффективная ингибирующая доза, необходимая для ингибирования связывания на 50%
Различие в адгезионном связывании между контрольным солевым раствором и образцами молока определялось с использованием метода Chi-квадрата для данной среды. Ингибирующее действие компонентов молока определялось путем парного испытания с осуществлением повторных экспериментов.
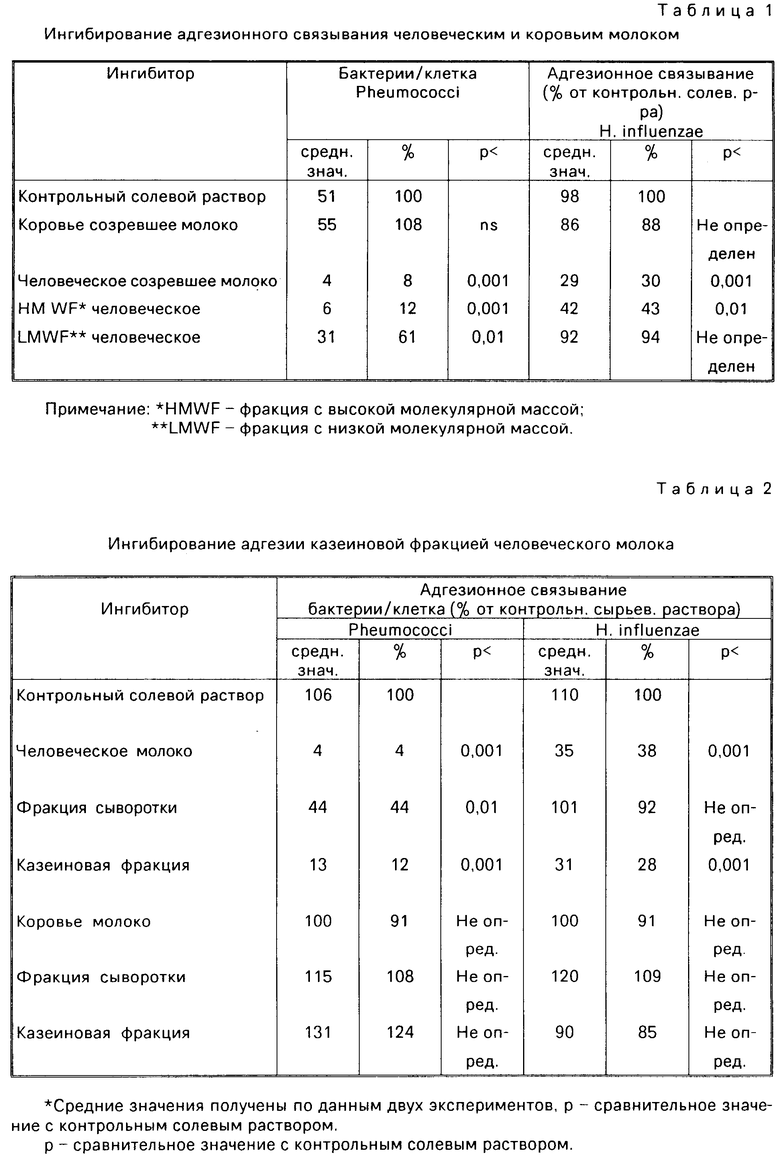
Связывание с человеческими носоглоточными эпителиальными клетками S.pneumoniae и H. influenzae ингибировалось созревшим человеческим молоком, но несозревшим коровьим молоком (табл.1). В противоположность созревшему коровьему молоку, коровье молоко также ингибировало связывание обоих типов бактерий.
В табл.1 средние значения взяты по данным двух экспериментов, сопоставляется с контрольным солевым раствором.
Тип ингибирующих компонентов человеческого молока сначала анализировали путем разделения по молекулярной массе. Все молоко и фракции молочной сыворотки разделялись на фракции, включающие компоненты с высокой и низкой молекулярными массами, путем пропускания их через колонку с SephadexR С-25 (фракция с мол. массой 5000 Дальтон, РД 10, Pharmacia AB, Uppsala Швеция). Фракция с большой молекулярной массой (HMWF) (в 3,5 мл дистиллированной воды) подвергалась непосредственной обработке. Как видно из предыдущих исследований, ингибирующее действие на S.pneumoniae обнаруживалось во фракции мол.массой < 5000 Дальтон, содержащей свободные олигосахариды. Однако фракция с низкой молекулярной массой (LMWF) не оказывала влияния на связывание H. influenzse (см. табл.1).
Казеин выделяли, например, методом Mellander. В 0,5 л свободного от жира человеческого молока вводили 13,5 мл 10%-ного аксалата калия. После инкубирования в течение ночи при температуре +4оС осадок удаляли путем центрифугирования при ускорении центрифуги 2500x g в течение 15 мин. Вводили дистиллированную воду и добавляли в суспензию 0,5 ммоля HCl с медленным перемешиванием до тех пор, пока конечная величина пор не составляла 4,6. Раствор нагревался до 30оС в течение 1 ч и затем его оставляли на ночь при температуре 14оС. После центрифугирования с ускорением центрифуги 2500x g в течение 15 мин поверхностный слой удаляли и осадок промывали 3-5 циклами повторного суспензирования в дистиллированной воде и центрифугирования. Данный препарат использовался в свежеприготовленном состоянии или после лиофилизации.
Далее молоко разделялось на фракции казеина и сыворотки. При концентрации, соответствующей концентрации в молоке (2 мг/мл) казеиновой фракции (HMWF), осуществлялось ингибирование связывания как S.pneumoniae, так и H. influenzae (см. табл.2).
Ингибирующее действие казеиновой фракции подтверждалось очищенным коммерчески доступным человеческим казеином. Казеиновая фракция и коммерчески доступная фракция в эквивалентных весовых количествах одинаково активны. При концентрации 10 мг/кг казеиновая фракция снижает связывание пневмококков более чем на 80% Величина EID50 составляет примерно 2 мг/кг. Для H.influenzae кривая аналогичной реакции на дозу была получена с максимальным ингибированием 86% при 10 мг/кг и величиной EID50, составляющей 2 мг/кг.
Различие характера ингибирующего действия между созревшим человеческим молоком и коровьим молоком подтверждалось для казеина и фракций сыворотки коровьего молока, ни одна из которых не ингибировала связывание S.pneuminoae и H.influenzae (см. табл.2).
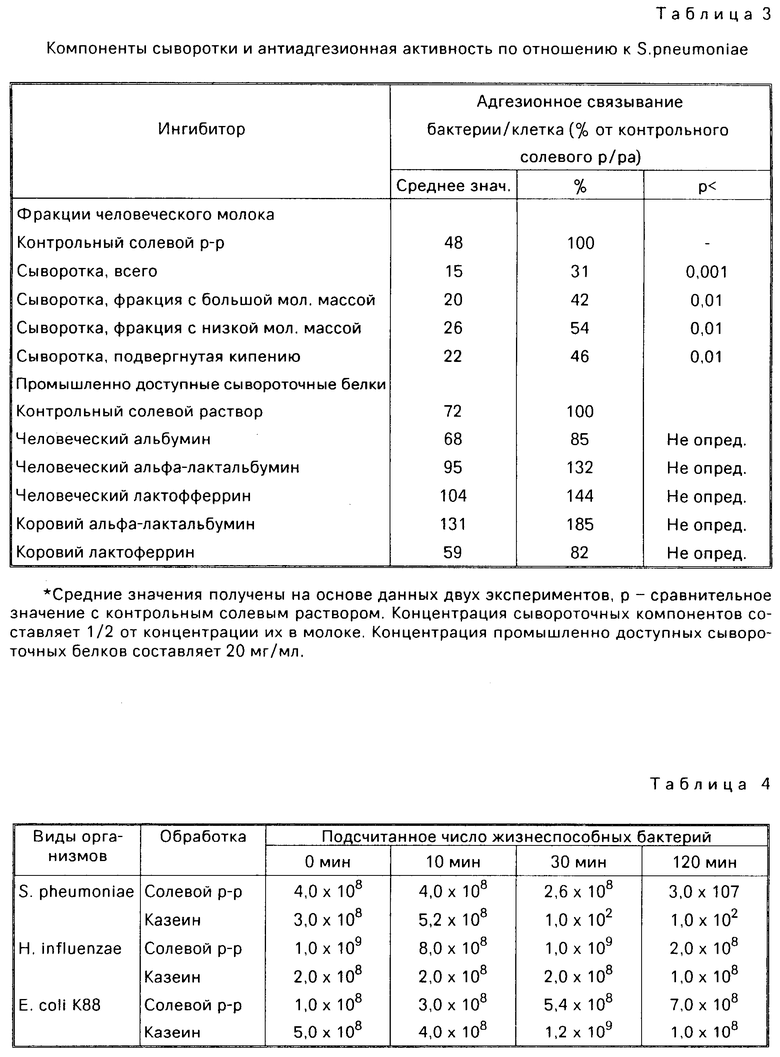
Ингибирующая активность H.influenzae ограничивалась казеиновой фракцией человеческого молока, никакой активности не сохранялось во фракции сыворотки (табл. 2). В отличие от этого связывание пневмококков ингибировалось также сывороточной фракцией. Молекулярный размер ингибиторов сывороточной фракции определяли после разделения на компоненты с молекулярной массой более и менее 5000 Дальтон. Фракции как с высокой, так и с низкой молекулярной массой обладали ингибирующей активностью (см. табл.3).
Очищенные коммерчески доступные компоненты человеческого молока: альбумин, казеин, альфа-лактальбумин и лактоферрин приобретаются у фирмы "Сигма Кемикл Компани", Ст.Луиз, Миссури, США.
Коммерчески доступные сывороточные белки человеческого и коровьего происхождения не обладают ингибирующей активностью по отношению к S.pneumoniae (табл.3)) или H.influenzae.
Фракция, обогащенная каппа-казеиновым гликопептидом, была получена способом Jolles и др. следующим образом. Химозин (Сигма, фермент: субстрат 1: 2000) вводили в 2%-ный раствор всего казеина в 0,2 мол. буферном растворе пиридина уксусной кислоты с рН 5,5. После вываривания в течение 1,5 ч при 30оС вводилась трихлоруксусная кислота (конечной концентрации 12%) и смесь слегка перемешивалась в течение 16 ч при +4оС. Поверхностный слой, полученный после центрифугирования при ускорении центрифуги 14300x g в течение 2 ч при температуре 14оС, содержал каппа-казеиновый гликопептид. Последний промывался 6 раз диэтиловым эфиром, деализировался с использованием дистиллированной воды при 4оС и лиофилизировался.
Было определено, что данная казеиновая фракция, состоящая главным образом из каппа-казеина, ингибирует связывание как S.pneumoniae, так и H.influenzae (фиг. 3). Для S. pneumoniae величина EID50 составляет примерно 2 мг/мл, то есть она сопоставима неразделенной казеиновой фракцией. В противоположность этому ингибирующая активность, направленная против H.influenzаe, значительно снижена до EID50, примерно 10 мг/мл. При концентрации 10 мг/мл остаточный альфа- и бета-казеин не обладает ингибирующей активностью.
Испытание на бактерицидную активность казеина осуществляли следующим образом: 1х109 бактерий/клетку, определяемые в гемецитометре, и казеин смешивали и инкубировали при 37оС в течение 30 мин. После разбавления до концентрации в пределах от 1х102 до 1х108 бактерий/л бактерии выращивались на агаровых пластинах в течение ночи. Подсчитывали число бактериальных колоний на пластинах и сравнивали их с бактериями, инкубированными с солевым буферным раствором.
Определяли количество жизнеспособных бактерий S.pneumoniae (CCUG 3114) после обработки казеиновой фракцией человеческого молока (2 мг/мл), а также определяли количество жизнеспособных бактерий H.influenzae (Hi 198) и положительное К88 E.coli. Полученные результаты представлены в табл.4.
Как видно из табл.4, число жизнеспособных бактерий значительно снижается при использовании казеина человеческого молока, и это говорит о том, что казеин человеческого молока не только ингибирует адгезионное связывание, но и обладает бактерицидным эффектом.
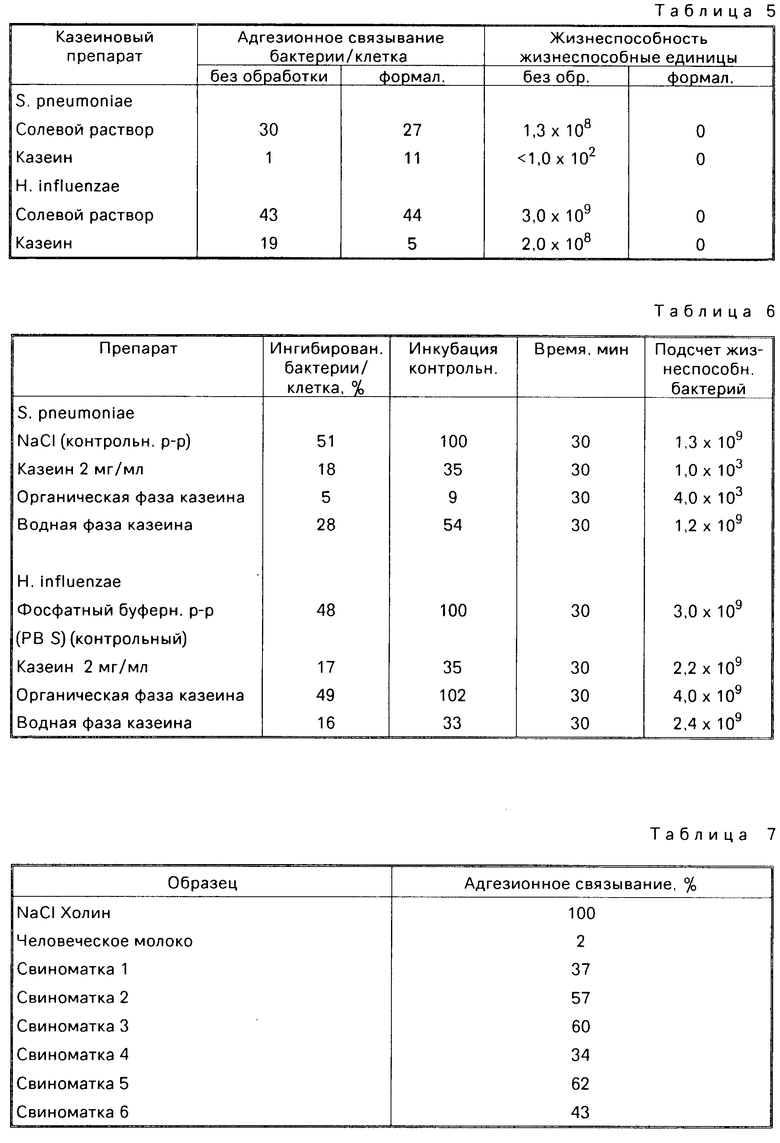
Как установлено, ингибирование адгезионного связывания и бактерицидный эффект независимы друг от друга. Адгезионная активность к S.pneumoniae и H. influenzae сохранялась после фиксации формалином и казеин ингибировал также связывание фиксированных бактерий.
Результаты представлены в табл.5.
Бактерицидный и противоадгезионный компоненты казеина разделялись в органической и водной фазе. Полученные результаты по ингибированию адгезионного связывания и жизнеспособности даются ниже в табл.6.
Таким же образом, как описано выше, проводили испытание на ингибирование адгезионного связывания с использованием свиного молока, определенное число здоровых свиноматок подвергалось ручному доению, казеин от каждого образца молока осаждался согласно описанной выше процедуре и осуществлялось испытание на S.pneumoniae.
Результаты представлены в табл.7.
В испытании казеиновая фракция экстрагировалась хлороформом-метанолом и осуществлялось испытание на ингибирование адгезионного связывания S.pneumoniae и на H.influenzae до и после экстракции. Как видно из табл.8, на казеиновую фракцию не оказывала влияние экстракционная обработка и таким образом такое денатурирование не оказывало влияния на характеристики ингибирования адгезионного связывания.
Никакого изменения ингибирования адгезионного связывания не наблюдалось после экстракции по сравнению с ингибированием до экстракции.
Организмы S. pneumoniae и H.influenzae являются очень серьезными источниками заболеваемости и смертности для всех возрастных групп. Инфекции дыхательных путей, например менингиты, отиты и синуситы, вызываются бактериями, которые вводятся через носоглотку. Образование колоний в данном месте может быть серьезным фактором, определяющим заболевание. То открытие, что человеческий казеин и казеин коровьего молозива ингибируют связывание обоих видов организмов, открывает возможность предотвращения образования колоний за счет специфического препятствия адгезионному связыванию с использованием этих структур. Другое открытие, заключающееся в том, что казеиновые фракции обладают бактерицидным эффектом против по крайней мере S.pneumoniae вне связи с эффектом ингибирования адгезионного связывания, обеспечивает расширение объема данного изобретения.
Как ясно из приведенных данных, казеиновая фракция человеческого молока ингибирует связывание S.pneumoniae и H.influenzae с эпителиальными клетками дыхательных путей человека в условиях "ин витро". Таким образом, было продемонстрировано, что казеиновая фракция ингибирует адгезионное связывание, хотя она, как таковая, не исключает то, что активные эпитопы на казеине эффективны.
Способность человеческого молока ингибировать связывание была показана на различных системах. Молоко содержит антитела к бактериальным адгезинам, например фибрин. Неиммуноглобулиновая фракция ингибирует гемаглютинацию V. cheleroе и E.coli, связывание с кишечным трактом морской свинки и защищает от вызванной энтеротоксином диареи у кроликов. Хотя такое действие обусловлено гликопротеинами и свободными олитиосахаридами, точные структуры до настоящего времени не были определены. В отличие от этого, олигосахариды молока, которые ингибируют связывание пневмококка, идентифицированы как специфические свободные олигосахариды лактосерий.
Ингибирующая активность олигосахаридов молока сравнивалась посредством синтетических аналогов и агглютинированных с бактериями сфер латекса, ковалентно связанных с рецепторами синтетических олигосахаридов. В отличие от S. pneumoniae, фракция данного казеина заключает в себе полную антиадгезионную активность молока по отношению к H.influenzae и эта активность не остается ни во фракции низкой молекулярной массой, ни в сывороточной фракции. Так, олигосахаридные последовательности, находящиеся в свободной форме в молоке, не проявляют функцию рецепторов. Однако, как и для S.pneumoniae, ингибирующая активность обнаруживается в человеческом молоке и в коровьем молозиве, но не с созревшем коровьем молоке. Дальнейшие исследования, имеющие целью идентифицировать структуры рецептора для H.influenzae, могут быть основаны на данном специфическом различии.
В зависимости от условий хранения и других факторов казеиновая фракция молока может претерпевать вредные изменения, отрицательно влияющие на ингибирование адгезионного связывания. Так, ингибирование адгезионного связывания на 40% или более, предпочтительно на 50% или более, и еще более предпочтительно на 65% или более по сравнению с контрольным солевым раствором, может рассматриваться, как вполне достаточная степень ингибирования.
Казеин человеческого, свиного и/или коровьего происхождения может вводиться в организм в виде дозированного препарата через слизистую оболочку рта, в виде инъекционной композиции, или в виде композиции локального внесения. В любом случае казеин обычно вводится вместе с общеизвестными наполнителями и/или носителями, которые фармацевтически приемлемы.
В случае ввода казеина в форме раствора для локального внесения этот раствор содержит эмульгирующий агент для казеина вместе с разбавителем, который может быть впрыснут в носоглотку, или который можно вдыхать, то есть, который может иметь форму мельчайших капель, попадающих в верхние дыхательные пути.
При оральном применении казеин обычно вводится вместе с носителем, который может представлять собой твердый, полутвердый или жидкий разбавитель или иметь форму капсулы. Эти фармацевтические препараты составляют еще один объект данного изобретения. Обычно количество активного соединения составляет 1-99 мас. от состава препарата, предпочтительно 0,5-20 мас. в препаратах для инъекции и 2-50 мас. в препаратах для инъекции и 2-50 мас. в препаратах для орального ввода.
В фармацевтических препаратах, содержащих казеин, отвечающий данному изобретению, имеющих единичную дозированную форму для орального ввода в организм, данное соединение может быть смешано с твердым распыленным носителем, таким как лактоза, сахароза, сорбит, маннит, крахмал, например картофельный крахмал, кукурузный крахмал, амилопектин, целлюлозные производные желатина, а также может быть смешано с антифрикционным реагентом, таким как стеарат магния, стеарат кальция, полиэтиленгликолевые парафины, а эта смесь спрессована в таблетки. Могут быть приготовлены также гранулы неединичной дозированной формы. Таблетки указанных препаратов, служащих в качестве ядра, могут быть покрыты полимерами, которые изменяют скорость растворения препарата в желудочно-кишечном тракте, такими как анионные полимеры, имеющие величину рН более 5,5. Такие полимеры могут представлять собой фталат оксипропилметилцеллюлозы, фталат ацетата целлюлозы и полимеры, выпускаемые в продажу под торговыми марками Eudrait 100 и < 100.
Препараты в форме желатиновых капсул могут быть мягкие или твердые. В первом случае активное соединение смешивается с маслом, во втором случае гранулы неединичной дозированной формы заполняют капсулу.
Жидкие препараты для орального ввода могут иметь форму сиропов или суспензий, например растворов, содержащих примерно 02,-20 мас. описанного активного соединения, и глицерин и пропиленгликоль. При желании такие препараты могут заключать в себе окрашивающие агенты, ароматизирующие агенты, сахарин и карбокси- метилцеллюлозу как загустители.
Дневная доза активного соединения изменяется в зависимости от способа ввода в организм, но, как правило, она составляет 1-100 мг активного соединения на дозу при оральном вводе, 2-200 мг на дозу при локальном внесении. Число вводов за 24 ч зависит от способа ввода, не может быть изменено, например в случае локального внесения через нос оно составляет 3-8 раз за 24 ч в зависимости от тока слизи, образуемой в организме при лечении. При использовании с профилактической целью это число может составлять нижние значения указанного предела.
Локальный ввод используется предпочтительно при профилактической обработке, предпочтительно от инфекции, вызванной вирусом ринита.
Казеин может использоваться также как добавка к детскому питанию, в частности для профилактических целей, что является легким способом ввода его в организм детей. Дети обычно не воспринимают лечебные препараты по различным причинам. Пищевой продукт может быть таким образом приготовлен в виде распыленной овсяной каши, в виде жидкой каши, молочной каши или может иметь более сложную форму продукта, например форму ломтиков по-шотландски (мелко нарубленных ломтиков, поджаренных с луком), включающих растительные и мясные кусочки, часто в размолотой форме.
В случае ввода казеина в организм животных он обычно вводится в пищевые корма, которые кроме казеина содержат обычно используемые питательные вещества.
Согласно следующему аспекту данного изобретения, предусматривается способ определения присутствия S.pneumoniae H.influenzae в образце, взятом из дыхательных путей животного и человека. Этот способ основан на приеме определения степени взаимодействия между бактериями образца и композиций, отвечающей данному изобретению. Такое взаимодействие может быть определено ингибированием или индукцией адгезионного связывания бактерий с клетками или другими поверхностями.
Изобретение иллюстрируется следующими примерами.
П р и м е р 1.
Активная фракция с моле-
кулярной массой не менее 5000 Дальтон, мг 200 Кремофор (эмульгатор), мл 5 Вода, мл 100
Протеиновую активную фракцию эмульгируют в воде с использованием эмульгатора. Водный раствор впрыскивают в ноздри.
П р и м е р 2.
Аэрозоль, содержащая активное начало: активное начало, мг 200 трихлорфторметан, г 3,44 дихлордиофторметан, г 6,88 дихлортетрафторэтан, г 3,44
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ВТОРИЧНЫХ ИНФЕКЦИЙ ПОСЛЕ ВИРУСНОЙ ИНФЕКЦИИ | 2008 |
|
RU2481844C2 |
| НОВЫЕ ВЕЩЕСТВА, СВЯЗЫВАЮЩИЕСЯ С HELICOBACTER PYLORI, И ИХ ПРИМЕНЕНИЕ | 2000 |
|
RU2283115C2 |
| ПЕПТИДЫ ГОРОХОВОГО БЕЛКА С АНТИ-Helicobacter pylori АКТИВНОСТЬЮ | 2011 |
|
RU2558304C2 |
| ФЕРМЕНТИРОВАННОЕ ПИТАНИЕ С НЕУСВОЯЕМЫМИ ОЛИГОСАХАРИДАМИ С ПОВЫШЕННОЙ БИОДОСТУПНОСТЬЮ ЖЕЛЕЗА | 2014 |
|
RU2650569C2 |
| НОВЫЕ РЕЦЕПТОРЫ ДЛЯ Helicobacter pylori И ИХ ПРИМЕНЕНИЕ | 2002 |
|
RU2306140C2 |
| ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ВОСПАЛЕНИЯ СРЕДНЕГО УХА С ПОМОЩЬЮ НЕПАТОГЕННЫХ ШТАММОВ БАКТЕРИЙ | 2007 |
|
RU2445361C2 |
| ВЫСОКОЛАКТОЗНОЕ ФЕРМЕНТИРОВАННОЕ ПИТАНИЕ С ПОВЫШЕННОЙ БИОДОСТУПНОСТЬЮ ЖЕЛЕЗА | 2014 |
|
RU2677924C2 |
| ПРИМЕНЕНИЕ БЫЧЬЕГО ЛАКТОФЕРРИНА ДЛЯ СОЗДАНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, ПРЕДНАЗНАЧЕННОГО ДЛЯ ИНГИБИРОВАНИЯ РОСТА БАКТЕРИЙ | 2006 |
|
RU2399380C2 |
| ФЕРМЕНТИРОВАННАЯ ФОРМУЛА С НЕПЕРЕВАРИВАЕМЫМИ ОЛИГОСАХАРИДАМИ ДЛЯ ПРИМЕНЕНИЯ ПРИ ИНФЕКЦИИ, ВЫЗВАННОЙ РОТАВИРУСОМ | 2020 |
|
RU2801538C2 |
| КОМПОЗИЦИИ МАТРИКСНЫХ ПРОТЕИНОВ ДЛЯ ЗАЛЕЧИВАНИЯ РАН | 1999 |
|
RU2241489C2 |

Область применения: изобретение относится к медицине, пищевой промышленности. Сущность изобретения: применение казеиновой фракции молока с мол.м. не менее 5000 Дальтон в качестве средства, ингибирующего связывание S. pnehmoniae и/или H. Ynflunzac, а также в виде композиций с приемлемыми наполнителями. 2 с.п. ф-лы, 8 табл.
| Многоступенчатый пресс для прессования блоков и других керамических изделий | 1955 |
|
SU126043A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-05-27—Публикация
1991-06-28—Подача