Изобретение относится к биотехнологии и иммунологии и представляет собой набор рекомбинантных белков, синтезированных в бактериальных клетках и позволяющих проводить серодиагностику синдрома приобретенного иммунодефицита (СПИД). СПИД возникает в результате заражения вирусом иммунодефицита человека (ВИЧ). ВИЧ при попадании в организм поражает клетки иммунной системы (Т-лимфоциты, моноциты и макрофаги) и клетки центральной нервной системы. Заболевание характеризуется длительным (от 2-х до 10-и лет) бессимптомным периодом в течение которого в крови инфицированного определяются только антитела к вирусным белкам, затем следует прогрессирующая деградация иммунной и центральной нервной системы. Поэтому для проведения экстренных противоэпидемических, профилактических мероприятий и своевременного начала лечения ВИЧ-инфекции крайне актуальна разработка диагностических препаратов, позволяющих выявлять инфицированных ВИЧ на ранних этапах инфекции.
Многочисленные исследования ВИЧ позволили определить его структуру, организацию генома, выяснить механизм экспрессии и фукнкции отдельных вирусных белков. В настоящее время известно два типа вируса иммунодефицита человека (ВИЧ-1 и ВИЧ-2), имеющих сходную организацию генома и различающихся по антигенной структуре вирусных белков.
ВИЧ имеет наиболее сложное из всех известных ретровирусов строение генома. Помимо генов gag, pol и env, направляющих синтез основных верионных белков и общих для всех ретровирусов, геном ВИЧ-1 содержит еще шесть генов: vif, tat, rev (или art, или trs). 3'-nef, vpr и vpu. Геном ВИЧ-2, в отличие от ВИЧ-1, не содержит гена vpu, но содержит ген vpx. Большинство этих генов кодирует продукты, которые необходимы для жизненного цикла вирусов. tat-ген кодирует 14 кД белок, определяющий экспрессию и репликацию ВИЧ, rev-ген регулирует репликацию генома и производство структурных белков, например белков оболочки. При этом ген не является необходимым для синтеза регуляторных белков, таких как tat и 3'-nef, vif-ген кодирует 23 кД белок, ответственный за вирусную инфекционность, 3'-nef, локализованный на 3'-конце вирусного генома, кодирует 27 кД белок, функция которого пока не установлена.
Большинство методов диагностики ВИЧ-инфекции основано на определении антител к белкам ВИЧ в сыворотках крови и других биологических жидкостях (серодиагностика). Для этих целей используются различные подходы, в которых применяется принцип иммуноферментного анализа (ИФА), реакции агглютинации (латекса, эритроцитов), иммунофлюоресценции, иммуноблотинга и радиоиммунопреципитации. Одним из наиболее перспективных путей совершенствования всех этих диагностических тест-систем является использование в качестве антитело-связывающего субстрата рекомбинантных белков ВИЧ, синтезированных в различных экспрессирующих системах. Использование таких рекомбинантных белков, сохраняющих антигенные детерминанты ВИЧ, вместо вирусных антигенов не только увеличивает специфичность и чувствительность тест-систем, но и делает их безопасными в работе. В частности, известны диагностические композиции, включающие полипептиды продуктов генов env и gag вируса иммунодефицита человека. Композиции предназначены для обнаружения антител против ВИЧ в сыворотках и биологических жидкостях.
Известны диагностические композиции, составленные на основе иммуногенных фрагментов белков env и pol и предназначенных для диагностики СПИД. Известны диагностические наборы, иммуносорбенты, тест-системы, включающие полипептиды продукты гена gag вируса иммунодефицита человека. Это техническое решение выбрано в качестве прототипа.
Сущность данного технического решения состоит в том, что предложена серия наборов для определения антител к вирусу иммунодефицита человека. Наборы включают ряд рекомбинантных антигенов ВИЧ-1 и/или ВИЧ-2, полученных с помощью методов генетической инженерии из штаммов-продуцентов, трансформированных рекомбинантными ДНК, включающими фрагменты генов env1 или gag1, и/или pol1, и/или pol-int1, и/или env11. В качестве контрольного антигена набор может содержать β-галактозидазу E.coli. При этом антигены, входящие в набор, иммобилизуют на твердом носителе, либо в смеси, либо по отдельности, в зависимости от решаемой задачи. Твердым носителем могут служить полистироловые или полихлорвиниловые планшеты для иммунологических реакций или шарики, нитроцеллюлоза, найлон, латексы, эритроциты, а также другие твердофазные носители. Введение в набор дополнительных (по сравнению с прототипом) рекомбинантных антигенов позволяет повысить чувствительность и специфичность набора, определить тип вируса и спектр антител к индивидуальным вирусным белкам.
П р и м е р 1. Набор для массового серологического исследования образцов сыворотки или плазмы крови на присутствие антител к рекомбинантным антигенам продуктам фрагментов генов env1, gag1 ВИЧ-1 и env11 ВИЧ-2.
Штаммы бактерий E. coli продуценты полипептидов продуктов фрагментов генов env1 с аминокислотной последовательностью
I F R P G G G N M R D N W R S E L Y K Y K V V K I E
P L G V A P Y K A K R R V V Q R E K R A V G I G A L
F L G F L G A A G S T M G A A S M T L T V Q A R L L
L S G I V Q Q Q N N L L R A I E A Q Q H L L Q L T V
W G I K Q L Q A R V L A V E R Y L K D Q Q L L G I W
G C S G K L I C T T A M P W N A S W S N K S L D Q I
W N N M T W M E W D R E I N N Y T S L I H S L I E D
S Q D Q Q E K N E Q E L L E L D K W A S L W N W F N
I T N W L W Y I K L F I M I V G G L V G L R I V F A
V L S I V N R V Q G Y S P L S F Q T H L S I P R G
P D R P E G I E E E G G E R D R D R S I R L V N G S gag1 с аминокислотной последовательностью
S L Y N T V A T L Y C V H Q R I D I K D T K E A L D K
I E E E Q N K S K K K A Q Q A A A D T G N S S Q V S Q
N Y P I V Q N I Q G Q M V H Q A I S P R T L N A W V
K V I E E K A F S P E V I P M F S A L S E G A T P Q D
L N T M L N T V G G H Q A A M Q M L K E T I N E E A A
E W D R I H P V H A G P I A P G Q M R E P R G S D I
A G T T S T L Q E Q I G W M T N N P P I P V G D I Y K
R W I I L G L N K I V R M Y S P T S I L D I R Q G P K
E P F R D Y V D R F Y K T L R A E Q A S Q E V K N W
M T E T L L V Q N A N P D C K T I L K A L G P A A T L
E E M M T A C Q G V G G P G H K A R V L A E A M S Q V
T N T A A I M M Q R G N F R N Q R K M V K C F N C G
K E G H T A R N C R A P R K K G C W K C G R E G H Q M
K D C T E R Q A N F L G K I env11 с аминокислотной последовательностью
G S F S A E V A E L Y R L E L G D Y K L V E V T P I
G F A P T A E K R Y S S A P G R H K R G V P V L G F
L G F L T T A G A A M G A A S L T L S A Q S R T L L
A G I V Q Q Q Q Q L L D V V K R Q Q E M L R L T V W
G T K N L Q A R V T A I E K Y L A D Q A R L N S W G
C A F R Q V C H T T выращивают на среде LB с селективными добавками, клетки собирают центрифугированием, разрушают ультразвуком. Тельца включения, содержащие рекомбинантные полипептиды промывают с помощью центрифугирования, солюбилизируют. Полипептиды очищают с помощью хроматографических методов, чистоту полученных полипептидов анализируют с помощью ДДС-Na-электрофореза. При изготовлении иммуносорбента для наборов сорбируют смесь полипептидов продуктов фрагментов генов gag1 (концентрация 2,5 мкг/мл), env1 (6 мкг/мл) и env11 (6 мкг/мл), растворенных в 0,06 М карбонат-бикарбонатном буфере рН 9,6. Сорбцию ведут при 10-12оС в течение 10-14 ч.
Конъюгат пероксидазы хрена с белком A St.aureus или с антивидовыми антителами получают с помощью периодатного окисления с последующей хроматографической очисткой готового конъюгата. Конъюгат, контрольные сыворотки и буферную смесь с гидроперитом (БСГ) для пероксидазной реакции лиофилизируют в ампулах, запаивают в атмосфере инертного газа. В качестве контрольного положительного иммунореагента используют сыворотку крови человека или животных, содержащую антитела к ВИЧ (К+). В качестве контрольного отрицательного иммунореагента (К-) используют сыворотку крови человека или животных, не содержащую антитела к ВИЧ. Иммуносорбент представляет собой полистироловые или полихлорвиниловые планшеты для иммунологических реакций с иммобилизованной смесью рекомбинантных антигенов ВИЧ-1 и ВИЧ-2.
Иммуносорбент перед использованием трехкратно промывают. Для промывок используют фосфатный буферный раствор рН 7,2 с 0,5%-ным Твином-20 (ФСБ-Т) с помощью автоматического или ручного промывателя, внося не менее 0,2 мл раствора в лунку. По окончании промывки удаляют влагу из планшета.
В 88 из 96 лунок вносят по 90 мкл раствора для разведения сывороток, содержащего 4%-ный раствор клеток E.coli, лизированных ультразвуком, в ФСБ-Т и добавляют по 10 мкл предварительно разведенных (1:10) исследуемых сывороток, перемешивая содержимое лунок пипетированием или с помощью встряхивателя. В незаполненном ряду, например в 1-м, в две лунки вносят 100 мкл К-, в 4 лунки по 100 мкл К+ и в 2 лунки по 100 мкл раствора для разведения сывороток (контроль конъюгата). Планшет заклеивают пленкой и выдерживают в течение 60 мин при температуре 37 ± 1оС.
Содержимое лунок удаляют с помощью промывателя, затем планшет 5-кратно промывают и полностью удаляют влагу. Во все лунки планшета вносят по 100 мкл конъюгата. Планшет заклеивают новым листом пленки и выдерживают в течение 30 минут при температуре 37 ±1оС.
Содержимое лунок удаляют, планшет 5-кратно промывают и полностью удаляют влагу. В каждую лунку планшета вносят по 100 мкл 0,05% ортофенилендиамина в растворе БСГ. Планшет помещают в защищенное от света место на 15-20 мин при температуре 15-25оС. Реакцию останавливают внесением во все лунки по 50 мкл 2 н. серной кислоты.
Регистрацию проводят немедленно на спектрофотометре типа "Мультискан", измеряя оптическую плотность (ОП) при длине волны 492 нм. Выведение спектрофотометра на нулевой уровень осуществляют по воздуху или по чистому сухому планшету.
Вычисляют среднее значение ОП (ОПср) для контроля конъюгата, которое должно быть не более 0,15; ОПср К- не более 0,2; ОПср К+ 0,8-1,8. Пороговое значение ОП вычисляют по формуле: ОПср К+, умноженное на расчетный коэффициент, указываемый в паспорте набора. Сыворотку учитывают как положительную, если значение ОП образца выше порогового. Чувствительность препарата не менее 99,8% специфичность не менее 99,5%
П р и м е р 2. Набор для повторного (уточняющего и дифференцирующего) серологического исследования образцов сыворотки или плазмы крови на присутствие антител к каждому из соответствующих антигенов ВИЧ-1 и ВИЧ-2.
Штаммы бактерий E.coli продуценты полипептидов продуктов фрагментов генов env1 с аминокислотной последовательностью
I F R P G G G N M R D N W R S E L Y K Y K V V K I E
P L G V A P T K A K R R V V Q R E K R A V G I G A L
F L G F L G A A G S T M G A A S M T L T V Q A R L L
L S G I V Q Q Q N N L L R A I E A Q Q H L L Q L T V
W G I K Q L Q A R V L A V E R Y L K D Q Q L L G I W
G C S G K L I C T T A M P W N A S W S N K S L D Q I
W N N M T W M E W D R E I N N Y T S L I H S L I E D
S Q D Q Q E K N E Q E L L E D K W A S L W N W F N
I T N W L W Y I K L F I M I F G G L V G L R I V F A
V L S I V N R V R Q G Y S P L S F Q T H L S I P R G
P D R P E G I E E E G G E R D R D R S I R L V N G S gag1 с аминокислотной последовательностью
S L Y N T V A T L Y C V H Q R I D I K D T K E A L D
K I E E E Q N K S K K K A Q Q A A A D T G N S S Q V
S Q N Y P I V Q N I Q G Q M V H Q A I S P R T L N A
W V K V I E E K A F S P E V I P M F S A L S E G A T
P Q D L N T M L N T V G G H Q A A M Q M L K E T I N
E E A A E W D R I H P V H A G P I A P G Q M R E P R
G S D I A G T T S T L Q E Q I G W M T N N P P I P V
G D I Y K R W I I L G N K I V R M Y S P T S I L D
I R Q G P K E P F R D Y V D R F Y K T L R A E Q A S
Q E V K N W M T E T L L V Q N A N P D C K T I L K A
L G P A A T L E E M M T A C Q G V G G P G H K A R V
L A E A M S Q V T N T A A I M M Q R G N F R N Q R K
M V K C F N C G K E G H T A R N C R A P R K K G C W
K C G R E G H Q M K D C T E R Q A N F L G K I pol1 с аминокислотной последовательностью
F F R E D L A F L Q G K A R E F S S E Q T R A N S P
T I S S E Q T R A N S P T R R E L Q V W G R E N N S
P S E A G A D R Q G T V S F N F P Q I T L W Q R P F
V T I K I G G Q L K E A L L D T G A D D T V L E E M
S L P G R W K P K M I G G I G G F I K V R Q Y D Q I
L I E V C G H K A I G T V L V G P T P V N I I G R N
L L T Q I G C T L N F P I S P I E T V P V K L K P G
M D G P K V K Q W P L T E E K I K A L V E I C T E M
E K E G K I S K I G P E N P Y N T P V F A I K K K D
S T K W R K L V D F R E L N K R T Q D F W E V Q L G
I P H P A G L K K K K S V T V L D V G D A T F S V P
L D E E F R K Y T A F T I P S I N N E T P G I R Y Q
Y N V L P Q G W K G S P A I F Q S S M T K I L E P F
R K Q N P D I V I Y Q M D D L Y V G S D L E I G Q
H R T K I E E L R Q H L L R W G L T T P D K K H Q K
E P P F L W M G Y E L H P D K W T V Q P V V L P E K
D S W T V N D I Q K L V G K L N W A S Q I Y P G I K
V R Q L C K L L R G T K A L T E V V P L T E E A E L
E L A E N R E I L K E P V H G V Y Y D P S K D L I A
E I Q K Q G Q G Q W T Y Q I Y Q E P F K N L K T G K
Y A R I R G A H T N D V K Q L T E A V Q K I T T E S
I V I W G K T P K F K L P I Q K E T W E T W W T E Y
W Q A A W I P E W E F V N T P P L V K L W Y Q L E K
E P I V G A E T F Y V D G A A N R E T K L G K A G Y
V T N R G R Q K V V P L T N T T N Q K T E L Q A I Y
L A L Q D S G L E V N I I T D S Q A L G I I Q A Q
P D K S E S E L V N Q I I E Q L I K K E K V Y L A W
V P A H K G I G G N E Q V D K L V S A G I R K V L F
L D G I D K A Q D E H E K Y H S N W R A M A S D F N
L P P V V A K E I V A S C D K C Q L K G E A M H G Q
V D C S P G I W Q L D C T H L E G K V I L V A V H V
A S G Y I E A E I I P A E T G Q E T A Y F L L K L A
G R W P V K T I H T D N G S N F A S A T V K A A C W
W A G I K Q E F G I P Y N P Q S Q G V V E S M N K E
L K K I I G Q V R D Q A E H L K T A V Q M A V F I H
N F K R K G G I G G Y S A G E R V V D I I A T D I Q
T K E L Q K Q I T K I Q N F R V Y Y R D S R P L W
K G P A K L L W K G E G A V V I Q D N S D I K V V P
R R K A K I I R D Y G K Q M A G D D C A S R Q D E
D pol-int1 с аминокислотной последовательностью
D K A Q D E H E H Y H S N W R A M A S D F N L
P P V V A K E I V A S C D K C Q L K G E A M H G Q V
D C S P G I W Q L D C T H L E G K V I L V A V H V A
S G Y I E A E I I P A E T G Q E T A Y F L L K L A G
R W P V K T I H T D N G S N F A S A T V K A A C W W
A G I K Q E F G I P Y N P Q S Q G V V E S M N K E L
K K I I S Q V R D Q A E H L K T A V Q M A V F I H N
F K R K G G I G G Y S A G E R V V D I I A T D I Q T
K E L Q K Q I T K I Q N F R V Y Y R D S R D P L W K
G P A K L L W K G E G A V V I Q D N S D I K V V P R
R K A K I I R D Y G K Q M A G D D C V A S R Q D E env11 с аминокислотной последовательностью
G S F S A E V A E L Y R L E L G D Y K L V E V T P I
G F A P T A E K R Y S S A P G R H K R G V P V L G F
L G F L T T A G A A M G A A S L T L S A Q S R T L L
A G I V Q Q Q Q Q L L D V V K R Q Q E M L R L T V W
G T K N L Q A R V T A I E K Y L A D Q A R L N S W G
C A F R Q V C H T T а так же продуцент β-галактозидазы выращивают на среде LB с селективными добавками. Клетки собирают центрифугированием, разрушают ультразвуком. Тельца включения, содержащие рекомбинантные полипептиды, промывают с помощью центрифугирования, солюбилизируют. Полипептиды очищают с помощью хроматографических методов, чистоту полученных полипептидов анализируют с помощью ДДС-Na-электрофореза. При изготовлении иммуносорбента для наборов готовят шесть растворов вышеперечисленных полипептидов и "КАг" (контрольный антиген β-галактозидаза), каждый в виде отдельного раствора в 0,06 М карбонат-бикарбонатном буфере рН 9,6 в концентрациях соответственно 15,10,15,15,15,10 мкг/мл. Сорбцию ведут при 10-12оС в течение 10-14 ч.
Конъюгат пероксидазы хрена с белком A St.aureus или с антивидовыми антителами получают при помощи периодатного окисления с последующей хроматографической очисткой готового конъюгата. Конъюгат, контрольные сыворотки и буферную смесь с гидроперитом (БСГ) для пероксидазной реакции лиофилизируют в ампулах, запаивают в атмосфере инертного газа. В качестве контрольного положительного иммунореагента используют сыворотку крови человека или животных, содержащую антитела к ВИЧ-1 (К1+) и антитела к ВИЧ-2 (К2+).
В качестве контрольного отрицательного иммунореагента (К-) используют сыворотку крови человека или животных, не содержащую антитела к ВИЧ. Иммуносорбент представляет собой полистироловые или полихлорвиниловые планшеты для иммунологических реакций с рекомбинантными антигенами продуктами фрагментов генов gag1, env1, pol1, pol-int1 и контрольным антигеном, иммобилизованными по отдельности.
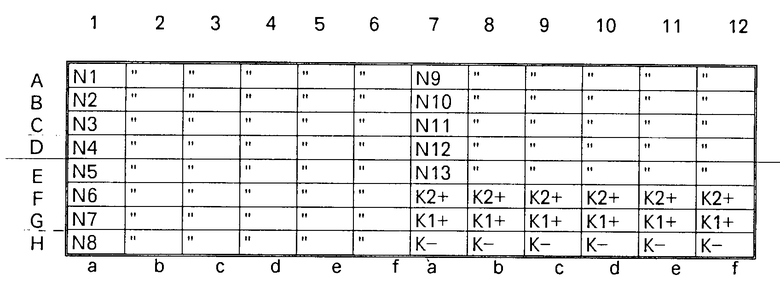
Иммуносорбент перед использованием трехкратно промывают раствором ФСБ-1, удаляют влагу из планшета. В 78 из 96 лунок вносят по 90 мкл раствора для разведения сывороток, оставляя, как указано в таблице, пустыми лунки для К-, К1+ и К2+.
Таблица показывает расположение сорбированных рекомбинантных антигенов и КАг в рядах планшета a b c d e f, соответственно.
Добавляют по 10 мкл предварительно разведенных (1:10) исследуемых сывороток в каждую из 6-и лунок горизонтального ряда, перемешивая содержимое лунок пипетированием или с помощью встряхивателя. В незаполненные ряды в соответствии с таблицей вносят К-,К1+ и К2+ по 100 мкл в каждую из 6-и лунок.
Планшет заклеивают пленкой и выдерживают в течение 60 мин при температуре 37±1оС.
Содержимое лунок удаляют с помощью промывателя, затем планшет 5-кратно промывают и полностью удаляют влагу. Во все лунки планшета вносят по 100 мкл конъюгата. Планшет заклеивают новым листом пленки и выдерживают в течение 30 мин при температуре 37±1оС.
Содержимое лунок удаляют, планшет 5-кратно промывают и полностью удаляют влагу. В каждую лунку планшета вносят по 100 мкл 0,05% ортофенилендиамина в растворе БСГ. Планшет помещают в защищенное от света место на 15-20 мин при температуре 15-25оС. Реакцию останавливают внесением во все лунки по 50 мкл 2 н. серной кислоты.
Регистрацию проводят немедленно на спектрофотометре типа "Мультискан", измеряя оптическую плотность (ОП) при длине волны 492 нм. Выведение спектрофотометра на нулевой уровень осуществляют по воздуху или по чистому сухому планшету.
Вычисляют среднее по 6-и лункам значение ОП для К-, которое должно быть не более 0,2. Значение ОП К1+ по лунке 8G должно быть не менее 0,8. Значение ОП К2+ по лунке 8F должно быть не менее 0,8. Значение ОП К1+ и К2+ по лункам с контрольным антигеном (12G,12F) должны быть не более 0,2.
Для каждой сыворотки вычисляют отношения ОП по каждому рекомбинантному антигену к ОП по контрольному антигену. Сигнал по антигену учитывают как положительный, если соответствующее отношение превышает коэффициент R, указанный в паспорте. Сигнал по антигену учитывают как отрицательный, если соответствующее отношение меньше коэффициента N, указанного в паспорте. Промежуточный вариант учитывают как сомнительный.
Чувствительность препарата не менее 99,8% специфичность не менее 99,9%
В качестве твердого носителя для нанесения рекомбинантных антигенов могут быть использованы не только планшеты для иммунологических реакций, но и любая другая твердая фаза. Например, полистироловые шарики, нитроцеллюлоза, латекс, эритроциты и др. В этих случаях рекомбинантные антигены выделяют тем же методом, что и в примерах 1 и 2, используют те же, либо другие иммунохимические реакции, например, агглютинации, и результаты учитывают как спектрофотометрически, так и визуально, либо при помощи других приборов.
Таким образом, изобретение позволяет повысить чувствительность и специфичность набора за счет определения типа вируса и спектра антител к индивидуальным вирусным белкам.
Изобретение относится к биотехнологии и иммунологии. Сущность изобретения: предложена серия наборов для определения антител к вирусу иммунодефицита человека 1 и 2 типов. Наборы включают ряд рекомбинантных антигенов, синтезированных в клетках E. coli, трансформированных рекомбинантными ДНК. Рекомбинантные ДНК включают фрагменты генов env 1 и/или gag 1, и/или pol 1, и/или pol-int 1, и/или env 2. В качестве контрольного антигена наборы могут содержать бета-галактозидазу E. coli. 1 табл.
НАБОР ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ВИРУСУ ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ПЕРВОГО И ВТОРОГО ТИПОВ, включающий иммуносорбент на основе антигенов вируса иммунодефицита человека, реагенты для определения присутствия антител, отличающийся тем, что антигены представляют собой рекомбинантные белки, являющие продуктами фрагментов генов вируса иммунодефицита человека (первого и второго типов) env 1 с аминокислотой последовательностью, приведенной в описании.
| ЕПВ, N 0311228, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-09-10—Публикация
1992-01-05—Подача