Это изобретение связано с некоторыми производными триазолопиримидина, способом их получения, составами, содержащими такие соединения и их использованием в качестве фунгицидов.
Европейская заявка N 92204097.7, находящаяся одновременно на рассмотрении раскрывает соединения общей формулы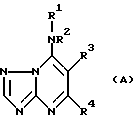
в которой R1 представляет собой возможно замещенный алкил, алкенил, алкадиенил, циклоалкил, бициклоалкил или гетероциклил группы;
R2 представляет собой атом водорода или алкилгруппу;
R1 и R2 вместе с атомом азота между ними представляет собой возможно замещенный гетероциклический остаток;
R3 представляет собой возможно замещенную арильную группу;
R4 представляет собой атом водорода, атом галогена или группу -NR5R6, где R5 - атом водорода или амино, алкил, циклоалкил или бициклоалкил, группы и R6 - атом водорода или алкилгруппа.
Эти соединения проявляют фунгицидную активность, особенно против грибов из класса аскомицетов, таких как Venturia inaequalis, Botrytis cinerea u Alternaria solani.
В настоящее время найдено, что некоторые циклоалкильные и гетероциклические аналоги соединений формулы A также проявляют фунгицидную активность.
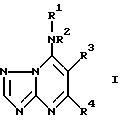
Согласно изобретению предлагаются соединения формулы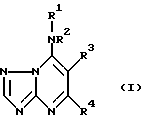
в которой R1 представляет собой возможно замещенный алкил, алкенил, алкандиенил, циклоалкил, бициклоалкил или гетероциклил;
R2 представляет собой атом водорода или алкилгруппу, или R1 и R2 вместе с атомом азота между ними представляет собой возможно замещенный гетероциклический остаток;
R3 представляет собой возможно замещенный циклоалкил или гетероциклил;
и R4 - атом водорода, атом галогена или группа -NR5R6, где R5 - атом водорода или амино, алкил, циклоалкил или бициклоалкил и R6 - атом водорода или алкилгруппа.
Если соединения этого изобретения содержит алкил, алкенил, алкинил или алкадиенил заместители, то эти заместители могут быть линейными или разветвленными и могут содержать до 12, преимущественно до 6 и особенно до 4 атомов углерода. Циклоалкильная группа может содержать от 3 до 8, преимущественно 3 - 6 атомов углерода. Бициклоалкильная группа может содержать от 4 до 12, преимущественно 4 - 8 атомов углерода. Арильная группа может быть любой ароматической углеводородной группой, особенно фенильной или нафтильной группой. Гетероциклическое кольцо может быть любой насыщенной или ненасыщенной системой колец, содержащей по крайней мере один гетероатом, предпочтительны 3 - 6-членный кольца и 5- и 6-членные кольца особенно предпочтительны. Наиболее предпочтительны азот-, кислород-, серосодержащие гетероциклы, такие как пиридинил, пиримидинил, пирролидинил, фурил, пиранил, морфолинил, тиенил.
Если любой из вышеприведенных заместителей указывается как возможно замещенный, то заместитель, который возможно присутствует, может быть одним или более из заместителей обычно используемых при создании пестицидных соединений и/или модификаций таких соединений для того, чтобы влиять на соотношение структура/активность, персистентность, проникновение или другие свойства. Специфическим примером таких заместителей являются, например атомы галогена, нитро, циано, тиоциано, гидроксил, алкил, галогеналкил, цианато, алкоксил, галогеналкоксил, амино, алкиламино, диалкиламино, формил, алкоксикарбонил, карбоксил, алканоил, алкилтио, алкилсульфинил, алкилсульфонил, карбамоил, алкиламино, фенил, бензил, бензилокси, гетероциклил, особенно фурил, циклоалкил, особенно циклопропилгруппы. Обычно может присутствовать 0 - 3 заместителя. Если любой из приведенных выше заместителей содержит или представляет собой арильную или циклоалкильную часть, то арильная или циклоалкильная часть может сама по себе быть замещена одним или более атомами галогена, нитро, циано, алкилом, галогеналкилом, алкоксилом или галогеналкоксилом. В случае групп циклоалкила и гетероциклила возможные заместители включают группы, которые вместе с двумя промежуточными атомами углерода циклоалкил- или гетероциклилгрупп образуют насыщенное или ненасыщенное углеводородное кольцо. Другими словами, насыщенное или ненасыщенное углеводородное кольцо может быть сконденсированно с циклоалкил или гетероциклил группой.
Предпочтительно, что R1 представляет собой C1-12 алкил, C2-6 алкенил, C2-6 алкинил, C4-12 алкадиенил, C3-8 циклоалкил или C4-8 бициклоалкилгруппа или 3 - 6-членное гетероциклическое кольцо, каждая группа или кольцо может быть замещена одним или более заместителями, выбранным из атома галогена, нитро, циано, гидроксил, C1-4 алкил, C1-4 галогеналкил, C1-4 алкоксил, C1-4 галогеналкоксил, амино, C1-4 алкиламино, ди-C1-4 алкиламино, формил, C1-4 алкоксикарбонил, карбоксил, фенил, C1-4 галогеналкилфенил, ди-C1-4 алкоксифенил, фурил, дигалоген-C3-6 циклоалкилгруппы или, в случае где R1 представляет собой C3-8 циклоалкильную группу или 3 - 6-членное гетероциклическое кольцо, возможно сконденсированное в ортоположении с бензольным кольцом.
Более предпочтительно, R1 представляет собой C1-12 алкил, C2-6 алкенил, C2-4 алкинил, C4-8 алкадиенил, C3-8 циклоалкил, C4-8 бициклоалкилгруппа или 3 -6-членное азотсодержащее гетероциклическое кольцо, которое может включать до трех заместителей, выбранных из атомов галогена, особенно хлор, гидроксила, C1-4 алкил, особенно метил, C1-4 галогеналкил, особенно метоксиалкил, C1-4 галогеналкилокси, особенно трифторметокси, фенил, C1-4 галогеналкилфенил, ди-C1-4 алкоксифенил, фурил, дигалоген-C3-6 циклоалкилгрупп или в случае если R1 представляет собой C3-8 циклоалкильную группу или 3 - 6-членное гетероциклическое кольцо, возможно конденсирование с бензольным кольцом в ортоположении.
Предпочтительно R2 представляет собой атом водорода или C1-4 алкилгруппу.
Также предпочтительно, что R3 представляет собой C3-8 циклоалкилгруппу или 3 - 6-членное гетероциклическое кольцо, каждая группа или кольцо могут быть замещенными одним или более заместителями, выбранными из атомов галогена, нитро, циано, гидроксил, C1-4 алкил, C1-4 галогеналкил, C1-4 алкоксил, C1-4 галогеналкилокси, амино, C1-4 алкиламино, ди-C1-4 алкиламино, формил, C1-4 алкоксикарбонил, карбоксил, фенил, фенокси и бензилоксигрупп.
Более предпочтительно R3 представляет собой C3-6 циклоалкилгруппу или 5 - 6-членное гетероциклическое кольцо, каждая группа или кольцо может включать до трех заместителей, выбранных из атомов галогена, C1-4 алкил, C1-4 галогеналкил, C1-4 алкоксил и C1-4 галогеналкилоксигрупп.
Предпочтительно R4 представляет собой атом водорода или атом галогена, или группу - NR5R6, где R5 представляет собой атом водорода или амино, C1-4 алкил, особенно метил, C3-6 циклоалкил или C4-8 бициклоалкилгруппу и R6 представляет собой атом водорода или C1-4 алкил, особенно метилгруппу.
Особенно предпочтительными являются соединения формулы I, в которых R1 представляет собой пропил, циклопентил, бициклогептил; R2 - атом водорода; R3 - тиенил группа; R4 - атом хлора.
Настоящее изобретение также предлагает способ для получения соединений формулы I, приведенных выше, который включает: (a) реакцию соединения общей формулы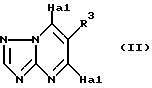
в котором R3 - как представлен выше и HaI - хлор или бром, с соединением общей формулы
HNR1 R2, III
в котором R1 и R2 - как описано выше,
с образованием соединения формулы I, в котором R4 представляет собой атом хлора или брома; (b) если требуется, реакцию соединения формулы I, полученного способом (a), с фторирующим агентом до образования соединения формулы I, в котором R4 представляет собой атом фтора; (c) если требуется, реакцию соединения формулы, полученного способом (a), с восстановителем до образования соединения формулы I, в котором R4 представляет собой атом водородов; (d) если требуется, реакцию соединения формулы I, полученного способом (a), с соединением общей формулы
HNR5 R6, (IV)
в котором R5 и R6 - как описано выше,
до образования соединения формулы I, в котором R4 представляет собой - NR5R6; (e) если требуется, реакцию соединения формулы I, полученного способом (d), в котором R5 и R6 оба представляют собой атом водорода, с дийодметаном в присутствии диазотирующего агента до образования соединения формулы I, в котором R4 представляет собой атом иода.
Способ (a) обычно выполняется в присутствии растворителя. Пригодные растворители включают эфиры, такие как диоксан, диэтиловый эфир, особенно тетрагидрофуран, гидрогалогенированные углеводороды, такие как дихлорметан и толуол. Реакция хорошо выполняется при температурах в ряду от 0oC до 70oC, предпочтительная температура реакции - от 10oC до 35oC. Также предпочтительно, что реакция проводится в присутствии основания. Пригодными основаниями являются третичные амины, такие как триэтиламин, неорганические основания, такие как карбонат калия и карбонат натрия. Или же основанием может служить избыток соединения формулы III.
Способ (b) удобно выполнять в присутствии растворителя. Пригодными растворителями являются сульфонал, диметилформамид смесь ацетонитрила и краун-эфира. Если в качестве растворителя используется сульфолан или диметилформамид, то полезно в качестве сорастворителя использовать толуол, чтобы добиться деградации фторирующего агента. Реакцию обычно проводят при температуре в ряду от комнатной температуры (около 15oC) до температуры кипения реакционной смеси, предпочтительная температура реакции - от 40oC до температуры кипения реакционной смеси. Подходящим фторирующим агентом являются фториды щелочных металлов, особенно фторид калия, и фторид сурьмы.
Восстановителем на стадии (C) обычно является каталитически гидрирующий реагент, это - водород, используемый при повышенном давлении в присутствии катализатора. Предпочтительно катализатором является палладий на углероде. Также предпочтительно, что этот способ проводится в присутствии основания. Пригодные основания включают третичные амины, такие как триэтиламин, и неорганические основания, такие как карбонат натрия или, особенно, гидроксид натрия. Эта ступень может также обычно проводиться в присутствии растворителя. Пригодными растворителями являются спирты, такие как метанол. Реакция обычно выполняется при температуре в ряду от 0oC до 70oC, предпочтительная температура реакции - от 10oC до 35oC.
Способ (d) обычно выполняется в присутствии растворителя. Пригодными растворителями являются эфиры, такие как диоксан, диэтиловый эфир и тетрагидрофуран, галогенированные углеводороды, такие как дихлорметан, и особенно толуол. Реакция обычно проводится при температуре в ряду от 20oC до температуры кипения реакционной смеси, предпочтительная температура реакции от 40oC до температуры кипения реакционной смеси. Предпочтительно, что реакция выполняется в присутствии основания. Пригодными основаниями являются третичные амины, такие как триэтиламин, и неорганические основания, такие как карбонат калия или карбонат натрия. Или же в качестве основания может использоваться избыток соединения формулы IV.
Когда R1 представляет собой тот же заместитель, что и R5 и R2 представляет собой тот же заместитель что и R6 в конечном соединении формулы I, соединение формулы III будет таким же, что и соединение формулы IV и стадии (a) и (d) могут поэтому быть выполнены в одну стадию с использованием двойного количества амина формулы III/IV.
Диазотирующим агентом, используемым на стадии (e), может быть любой алкиловый эфир азотистой кислоты, особенно предпочтителен изопентилнитрит. Если используется алкиловый эфир азотистой кислоты, то он может служить в качестве сорастворителя и дийодметаном. Реакция обычно выполнялась при температуре от 60oC до 120oC, предпочтительная температура реакции - от 70oC до 110oC.
Соединения формулы II могут быть получены реакцией соединения общей формулы
в которой R3 представлен выше,
с хлорирующим или бромирующим агентом, такими как хлорокись фосфора или бромокись фосфора.
Соединения формулы V могут быть получены реакцией 3-амино-1,2,4-триазола с соответствующим эфиром малоновой кислоты при в щелочных условиях в соответствии с методом J.Makisumi, Chem. Pharm. Bull., 9, 801 (1961).
Соединения формулы II и IV являются известными соединениями и могут быть получены аналогично известными методиками.
Было обнаружено, что соединения общей формулы I обладают фунгицидной активностью. Соответственно изобретение также обеспечивает фунгицидные составы, которые включают носитель и в качестве активного ингредиента соединение формулы I, которое описано выше. Метод получения таких составов также предлагается, метод включает внесение соединения формулы I, которое описано выше, в составы с по крайней мере одним носителем. Такие составы могут включать одно соединение или смесь различных соединений настоящего изобретения.
Составы соответствующие изобретению преимущественно содержат от 0,5 до 95 мас.% активного ингредиента.
Носителем в составах, соответствующих изобретению, является любой материал, с которым активный ингредиент рецептурируется для удобного применения при обработке растений, семян, почвы или для удобного хранения, транспортировки и обращения. Носителям могут быть твердые или жидкие материалы, включая те, которые в обычном состоянии газообразные, но которые сжижаются до жидкости, и любые носители, обычно используемые для рецептурирования фунгцидных препаратов, могут применяться.
Пригодные твердые носители включают природные и синтетические глины и силикаты, например природные силикаты, такие как кизельгур; силикаты магния, например тальк; алюмосиликаты магния, например аттапулгиты и вермикулиты; силикаты алюминия, например каолин, монтомориллонит и слюда; карбонат кальция; сульфат кальция; сульфат аммония; синтетический гидратированный оксид кремния и синтетические силикаты кальция или алюминия; элементы, например углерод и сера; природные и синтетические смолы, например смола коумарона, полимеры и сополимеры на основе поливинилхлорида и стирола; твердые полихлорфенолы; битум; воск, например пчелиный воск, парафиновый воск хлорированный минеральный воск; твердые удобрения, например суперфосфаты.
Пригодными жидкими носителями является вода; спирты, например изопропанол и гликоли; кетоны, например ацетон, метилэтилкетон, метилизобутилкетон и циклогексанон; эфиры; ароматические или аралифатические углеводороды, например бензол, толуол и ксилол; фракции нефти, например, керосин и легкие минеральные масла; хлорированные углеводороды, например, четыреххлористный углерод, пентахлорэтилен и трихлорэтан. Часто пригодны смеси различных жидких носителей.
Фунгицидные препараты часто рецептурируются и транспортируются в концентрированной форме, которая в дальнейшем разбавляется непосредственно перед применением. Присутствие небольших количеств поверхностно-активных веществ улучшает этот процесс разбавления. Таким образом предпочтительно, чтобы по крайней мере один носитель в препарате, соответствующем изобретению, являлся поверхостно-активным веществом. Например препарат может содержать по крайней мере два носителя, по крайней мере один из которых является поверхностно-активным веществом.
Поверхностно-активное вещество может быть эмульгирующим агентом, диспергирующим агентом или смачивающим агентом; он может быть неионным и ионным. Примерами подходящих поверхностно-активных веществ являются соли натрия и кальция полиакриловых и лигнинсульфоновых кислот; продукты конденсации жирных кислот и алифатических аминов или амидов, содержащих по крайней мере 12 атомов углерода в молекуле с этиленоксидом и/или пропиленоксидом; эфиров жирных кислот глицерина, сорбитола, сахарозы или пентаэритритола; конденсаты их с этиленокисдом и/или пропиленоксидом; продукты конденсации жирных спиртов или алкилфенолов, например, п-октилфенола или п-октилкрезола, с этиленоксидом и/или пропиленоксидом; сульфаты или сульфонаты этих продуктов конденсации; соли щелочных и щелочноземельных металлов, преимущественно натриевые соли, эфиров серной сульфоновой кислот, содержащие по крайней мере 10 атомов углерода в молекуле, например лаурилсульфат натрия, (вторичный алкил) сульфат натрия, натриевая соль сульфонированного касторового масла и алкиларилсульфонаты натрия, такие как додецилбензолсульфонат; и полимеры этиленоксида и сополимеры этиленоксида и пропиленоксида.
Препараты изобретения могут, например, рецептурироваться как смачивающиеся порошки, дусты, гранулы, растворы, эмульгирующиеся концентраты, эмульсии, суспензионные концентраты и аэрозоли. Смачивающиеся порошки обычно содержат 25, 50 или 75 мас.% активного ингредиента и обычно включают в дополнение к твердому инертному носителю 3 -10 мас.% диспергирующего агента и, если это необходимо, 0 -10 мас.% стабилизатора(ов) и/или других добавок, таких как смачивающее вещество или связующее вещество. Дусты обычно рецептурируются как концентрат дуста, имеющего состав, подобный составу смачивающегося порошка, но без диспергирующего агента, и может разбавляться в полевых условиях с твердым носителем до получения состава, обычно содержащего 0,5 -10 мас.% активного ингредиента. Гранулы обычно готовят так, чтобы иметь размер между 10 и 100 ВS mesh (1.676-0.152 мм), они могут быть получены спеканием или импрегнированием. Обычно гранулы будут содержать 0,5 -75% активного ингредиента и 0 -10% добавок, таких как стабилизаторы, поверхностно-активные вещества, модификаторы медленного высвобождения и связывающие агенты. Так называемые "сухие текучие порошки" состоят из гранул относительно маленького размера, имеющих относительно высокую концентрацию активного ингредиента. Эмульгирующиеся концентраты обычно содержат, кроме растворителя, если необходимо, сорастворитель, 1 - 50% вес./об. активного ингредиента, 2 - 20% вес./об. эмульгирующего агента и 0 - 20% других добавок, таких как стабилизаторы, смачивающие добавки и ингибиторы коррозии. Суспензионные концентраты обычно готовят так, чтобы получить стабильный, неседиментирующийся текучий продукт, они обычно содержат 10 -75% активного ингредиента, 0,5 -15 мас.% диспергирующего агента, 0,1 -10 мас.% суспендирующих агентов, таких как защитные коллоиды и тиксоторопные агенты, 0-10% вес других добавок, таких как противопенные присадки, ингибиторы коррозии, стабилизаторы, смачивающие агенты и связующие вещества, воду или органический растворитель, в которых активный ингредиент обычно нерастворим; некоторые органические твердые вещества или неорганические соли могут присутствовать в препаратной форме растворенными для того, чтобы помочь предохранить их от седиментации или как антифризы для воды.
Водные дисперсии и эмульсии, например составы, полученные разбавлением смачивающихся порошков или концентратов изобретения водой, также принадлежат к области изобретения. Вышеназванные эмульсии могут быть типа вода в масле или масло в воде и могут быть "майонезо"-подобной консистенции.
Препараты изобретения могут также содержать другие ингредиенты, например другие соединения, обладающие гербицидными, инсектицидными или фунгицидными свойствами.
Особый интерес для увеличения продолжительности защитного действия соединений этого изобретения представляет использование носителя, который будет обеспечивать медленное высвобождение фунгицидных соединений в окружающую среду растений, которые защищают. Такие препаративные формы с медленными высвобождением действующего вещества, могут например помещаться в почву между корнями виноградной лозы эти формы могут включать клеющие компоненты, позволяющие прикреплять их непосредственно к средству виноградной лозы.
Изобретение более того обеспечивает использование в качестве фунгицидов соединений общей формулы I, которое описано выше или составов, которые описаны выше, метод борьбы с помощью таких соединений или составов с грибами в местах их обитания обработкой этих мест, которые могут быть например растениями, подвергающимися или уже подвергшиеся фунгальной атаке, семенами таких растений или средой, в которой такие растения растут или росли.
Настоящее изобретение широко применимо для защиты различных культур от воздействия грибов. К культурам, которые могут быть защищены этими препаратами, относятся виноградная лоза, зерновые, такие как пшеница и ячмень, яблони и томаты. Продолжительность защиты обычно зависит от выбранного индивидуального соединения, разнообразных внешних факторов, таких как климат, чье воздействие обычно уменьшается с помощью применения подходящей формы применения. Далее изобретение иллюстрируется следующими примерами.
Пример 1
Получение 5- хлор-6-тиен-3-ил-7-циклопентиламино-1,2,4-триазоло[1,5-a] пиримидина
(R1=циклопентил; R2=H; R3=тиен-3-ил; R4=Cl)
К 5,7-дихлор-6-тиен-3-ил-1,2,4-триазоло[1,5-a]пиримидину (0,54 г, 0,002 моля) в тетрагидрофуране (20 мл) прибавляли смесь циклопентиламина (0,2 г 0,002 моля), тетрагидрофурана (2 мл) и триэтиламина (0,25 г, 0.002 моля), перемешивали 1 час, затем отгоняли растворитель в вакууме, остаток обрабатывали этилацетатом и водой (50 мл каждого). Органический слой отделяли, сушили над сульфатом натрия, фильтровали и упаривали растворитель в вакууме. Остаток очищали хроматографией на силикагеле с использованием в качестве элюента смеси этилацетат: петролейный эфир (8:2) (300 мл) и получали 0,45 г 5-хлор-6-тиен-3-ил-7-циклопентиламино-1,2,4-триазоло[1,5-a]-пиримидина в виде бесцветных кристаллов, т.пл.78oC. Выход: 71% от теоретического.
Пример 2 и 3
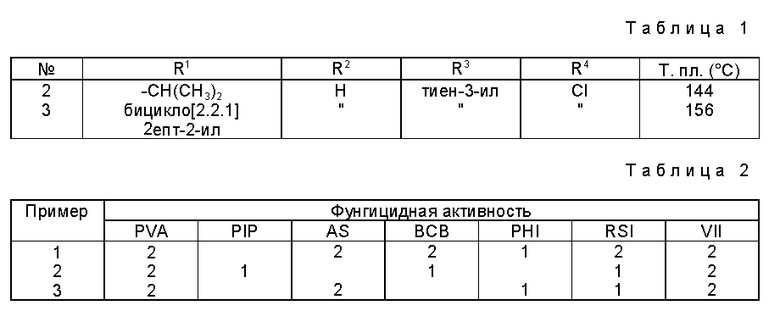
С помощью способа, описанного в примере 1 далее получали соединения, приведенные в таблице 1. В этой таблице соединения приведены по формуле 1.
Пример 4.
Фунгицидная активность соединений изобретения была изучена с помощью следующих тестов.
(a) Антиспорулационная активность против ложной мучнистой росы виноградной лозы (Piasmopara viticola; PVA)
Тест на антиспорулационную активность включает непосредственное опрыскивание листьев. Нижнюю поверхность листа виноградного растения (сорта Кабернет Саувигнон), приблизительно 8 см высотой инокулируют водной суспензией, содержащей 5•104 зооспорангиев/мл. Инокулированные растения выдерживают 24 часа при 21oC в камерах с высокой влажностью, затем 24 часа в теплице при 20oC и 40% относительной влажности. Зараженные листья по их нижней поверхности опрыскивали раствором тестируемого соединения в воде/ацетоне (1: 1), содержащим 0,04% "TWEEN 20" (торговое название поверхностноактивного вещества, -полиоксиэтилированного эфира сорбитана). Растения опрыскаивают с использованием опрыскивателя с 2 воздушными распыляющими соплами. Концентрация соединения - 600 частей на миллион и объем опрыскивания - 70 л/га. После сушки растения возвращаются в теплицу при 20oC и 40% относительной влажности на 96 часов и затем переносятся в камеру с высокой влажностью на 24 часа для индуцирования споруляции. Оценка проводится по проценту поверхности листа, на которой идет споруляция в сравнении с аналогичной поверхностью контроля.
(b) Прямая защитная активность против фитофтороза томатов (Phytophthora infestans; PIP)
Тест на прямое защитное действие включает опрыскивание листьев. Растения томата с двумя раскрывшимися листами (сорт "Первый в поле" опрыскивают тестируемым соединением в дозе 600 частей 1 млн. в растворе, приготовленное по способу (a). После сушки растения выдерживали 24 часа в теплице при 20oC и 40% относительной влажности. Верхнюю поверхность листа инокулируют водной суспензией, содержащей 2•105 зооспорангиев/мл. Инокулированные растения оставляют на 24 часа при 18oC в камерах с высокой влажностью и затем на 5 дней в камерах роста при 15oC и 80% относительной влажности с 14 часовым световым днем. Оценку проводят по проценту площади пораженного листа в сравнении с той же величиной в контроле.
(c) Активность против ранней гнили томатов (Alternaria solani, As).
Тест проводят используя опрыскивание листьев. Рассаду томата (сорт Outdoor Girl) на стадии второго листа опрыскивают раствором тестируемого соединения в дозе 600 частей на млн., приготовленным как описано в методике (a). Растения сушат и оставляют на 24 часа в теплице при 20oC и 40% относительной влажности, далее инокулируют верхнюю поверхность листа водной суспензией конидий A.Solani содержащей 1•104 конидий/мл, выдерживают в камере с высокой влажностью при 21oC 4 дня и оценивают по проценту поверхности пораженного листа в сравнении с этой величиной для контроля.
(d) Прямое защитное действие против серой плесени бобов (Botrytis cinerea; BCB)
Тест на прямое защитное действие проводят используя опрыскивание листьев. Растения бобов (сорт The Sutton) с двумя парами листьев опрыскивают раствором тестируемого соединения в дозе 600 частей на 1 млн., приготовленным как описано в методике (a), сушат, помещают на 24 часа в теплицу при 20oC и 40% относительной влажности, затем верхнюю поверхность листа инокулируют водной суспензией, содержащей 1•106 конидий/мл. Растения оставляют на 4 дня при 22oC в камере с высокой влажностью. Оценку проводят по проценту поверхности пораженного листа в сравнении с этой величиной в контроле.
(e) Активность против глазковой пятнистости пшеницы in vitro (Pseudocercosporella herpotrichoides; PHI)
Этот тест определяет активность in vitro соединений против грибков, вызывающих глазковую пятнистость пшеницы. Тестируемое соединение растворяют или суспендируют в ацетоне и добавляют в 4 мл аликвот картофельного декстрозного бульона половинной крепости в 25-ячеичную чашку Петри до получения конечной концентрации 30 частей на млн. тестируемого соединения и 0.825% ацетона. Инокулят гриба состоит из мицелиевых фрагментов P.herpotrichoides. выращенных на декстрозном картофельном бульоне половинной крепости во встряхиваемой колбе и добавленных к бульону до получения 5•104 мицелиевых фрагментов/мл бульона. Чашки Петри инкубируют при 20oC в течение 10 дней до оценки мицелиевого роста.
(f) Активность против ризоктонии in vitro (Rhozoctonia Solani; PSI)
Тест определяет активность in vitro соединений против Rhizoctonia solani, которые вызывают стеблевые и корневые гнили. Тестируемое соединение растворяют или суспендируют в ацетоне и добавляют в 4 мл аликвот картофельного декстрозного бульона половинной крепости в 25-ячеичную чашку Петри до получения конечной концентрации 30 частей на млн. соединения и 0.825% ацетона. Инокулят гриба состоит из фрагментов мицелий R.Solani, выращенных в декстрозном бульоне половинной крепости во встряхиваемой колбе и добавленных к бульону до получения 5•104 мицелиевых фрагментов/мл бульона. Чашки Петри инкубируют при 20oC в течение 10 дней до оценки мицелиевого роста.
(g) Активность против парши яблок in vitro (Venturia inaequalis; VII)
Этот тест определяет активность in vitro соединений против Venturia inaequalis, которые вызывают паршу яблок. Тестируемое соединение растворяют или суспендируют в ацетоне и добавляют в 4 мл аликвот картофельного декстрозного бульона половинной крепости в 25-ячеистой чашке Петри до получения конечной концентрации 30 частей на млн. и 0.825% ацетона. Инокулят гриба состоит из мицелиевых фрагментов и спор. V.inaequalis, выращенных на солодовом агаре и добавленных к бульону до получения 5•104 пропагул/мл бульона. Чашки Петри инкубируют при 20oC в течение 10 дней до оценки роста мицелий.
Степень подавления болезни во всех приведенных выше тестах выражается как оценка при сравнении с необработанным контролем или с контролем, обработанным только растворителем без соединения, в соответствии с критериями:
0 = менее, чем 50% подавления болезни
1 = 50-80% подавления болезни
2 = более, чем 80% подавления болезни
Результаты этих тестов помещены в таблицу 2.
Примеры композиций
Пример 5 (концентрат эмульсии (КЭ))
Активный ингредиент - 30% (в/о)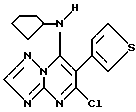
(Пример 1)
Эмульгатор(ы) Atlox®4856 B/Atlox® 4858 B1) (смесь, содержащая алкиларилсульфонат кальция, этоксилаты спиртов жирного ряда и легкокипящие ароматические соединения/смесь, содержащая алкиларилсульфонат кальция, этоксилаты спиртов жирного ряда и легкокипящие ароматические соединения) - 5% (в/о)
Растворитель Shellsol® A2) (смесь C9-C10-ароматических углеводородов) - До 1000 мл
Пример 6 (Концентрат суспензии (KC))
Активный ингредиент - 50% (в/о)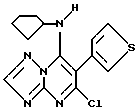
(Пример 1)
Диспергатор Soprophol® FL3) (полиоксиэтилен полиарил фенилэфирфосфат, соль с амином) - 3% (в/о)
Пеногаситель Rhodorsil® 4223) (неионная водная эмульсия полидиметилсилоксанов) - 0,2% (в/о)
Структурообразователь Kelzan® S4) (ксантановая камедь) - 0,2% (в/о)
Антифриз Пропиленгликоль - 5% (в/о)
Биоцидное средство Proxel®5) (водный раствор дипропиленгликоля, содержащий 20% 1,2-бенхотиазолин-3-он) - 0,1% (в/о)
Вода - До 1000 мл
Пример 7 (Смачиваемый порошок (СП))
Активный ингредиент - 60% (в/в)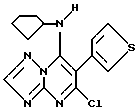
(Пример 1)
Смачивающее вещество Atlox® 49951) (алкиловый эфир полиэтилена) - 2% (в/в)
Диспергатор Witcosperse® D-606) (смесь натриевых солей конденсированной нафталинсульфокислоты и алкиларилполиоксиацетатов) - 3% (в/в)
Носитель/наполнитель Каолин - 35% (в/в)
Пример 8 (Вододиспергируемые гранулы (ВГ))
Активный ингредиент - 50% (в/в)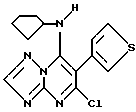
(Пример 1)
Диспергатор/связующее Witcosperse® D-4508) (смесь натриевых солей конденсированной нафталинсульфоновой кислоты и алкилсульфонатов) - 8% (в/в)
Смачивающее вещество Morwet®8) (продукт конденсации формальдегида) - 2% (в/в)
Пеногаситель Phodorsil® EP 6703 3) (капсулированный силикон) - 1% (в/в)
Дезинтегрант Agrimer® ATF 7) (поперечно-сшитый гомополимер N-винил-2-пирролидона) - 2% (в/в)
Носитель/наполнитель Каолин - 35% (в/в)
Пример 9 (Концентрат эмульсии (КЭ))
Активный ингредиент - 30% (в/о)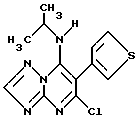
(Пример 2)
Эмульгатор(ы) Atlox®4856 B/Atlox® 4858 B 1) (смесь, содержащая алкиларилсульфонат кальция, этоксилаты спиртов жирного ряда и легкокипящие ароматические соединения/смесь, содержащая алкиларилсульфонат кальция, этоксилаты спиртов жирного ряда и легкокипящие ароматические соединения) - 5% (в/о)
Растворитель Shellsol®2) (смесь C9-C10-ароматических углеводородов) - До 1000 мл
Пример 10 (Концентрат суспензии (КС))
Активный ингредиент - 50% (в/о)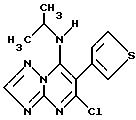
(Пример 2)
Диспергатор Soprophor® FL 3) (полиоксиэтилен полиарил фенилэфирфосфат, соль с амином) - 3% (в/о)
Пеногаситель Rhodorsil® 422 3) (неионная водная эмульсия полидиметилсилоксанов) - 0,2% (в/о)
Структурообразователь Kelzan® S 4) (ксантановая камедь) - 0,2% (в/о)
Антифриз Пропиленгликоль - 5% (в/о)
Биоцидное средство Proxel®5) (водный раствор дипропиленгликоля, содержащий 20% 1,2-бенизотиазолин-3-он) - 0,1% (в/о)
Вода - До 1000 мл
Пример 11 (Смачиваемый порошок (СП))
Активный ингредиент - 60% (в/в)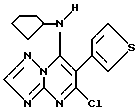
(Пример 2)
Смачивающее вещество Atlox® 4995 1) (алкиловый эфир полиэтилена) - 2% (в/в)
Диспергатор Witcosperse® D-60 6) (смесь натриевых солей конденсированной нафталинсульфокислоты и алкиларилполиоксиацетатов) - 3% (в/в)
Носитель/наполнитель Каолин - 35% (в/в)
Пример 12 (Вододиспергируемые гранулы (ВГ))
Активный ингредиент - 50% (в/в)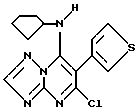
(Пример 2)
Диспергатор/связующее Witcosperse® D-450 6) (смесь натриевых солей конденсированной нафталинсульфокислоты и алкилсульфонатов) - 8% (в/в)
Смачивающее вещество Morwet® TFW 6) (продукт конденсации формальдегида) - 2% (в/в)
Пеногаситель Rhodorsil® EP 6703 3) (капсулированный силикон) - 1% (в/в)
Дезинтегрант Agrimer® ATF 7) (сшитый гомополимер N-винил-2-пирролидона) - 2% (в/в)
Носитель/наполнитель Каолин - 35% (в/в)
1) Продукт в продаже от ICI Surfactants
2) Продукт в продаже от Deutsche Shell AG
3) Продукт в продаже от Rhone-Poulenc
4) Продукт в продаже от Kelco Co.
5) Продукт в продаже от Zeneka
6) Продукт в продаже от Witco
7) Продукт в продаже от International Speciality Products
Производные триазолопиримидина общей формулы I, где R1 - возможно замещенный алкил, циклоалкил или бициклоалкил; R2 - атом водорода; R3 - 3 - 4-членный, содержащий один атом S гетероцикл; R4 - атом галогена, получают взаимодействием соединения формулы II, в котором Hal - хлор или бром, с соединением формулы HNR1R2 с получением соединения формулы I, в котором R4 - атом хлора или брома, и необязательно реакцию полученного соединения I с фторирующим агентом с получением соединения I, в котором R4 - атом фтора. Соединения формулы I проявляют фунгицидную активность, особенно против грибов из класса аскомицетов, таких как Venturia inaequalis, Botrytis cineria и Alternaria solani. 5 с. и 6 з.п. ф-лы, 2 табл.

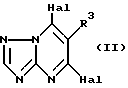
где R1 представляет собой возможно замещенный алкил, циклоалкил или бициклоалкил;
R2 представляет собой атом водорода;
R3 представляет собой 3 - 4-членный содержащий один атом S гетероциклил;
R4 представляет собой атом галогена.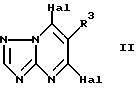
где R3 - как определено в пп.1 - 4;
Hal представляет собой хлор или бром,
с соединением общей формулы III
HNR1R2
где R1 и R2 - как определено в любом из предыдущих пунктов,
с получением соединения формулы I, в котором R4 представляет собой атом хлора или брома, и необязательно (в) реакцию полученного соединения формулы I с фторирующим агентом с получением соединения формулы I, в котором R4 - атом фтора.
| АППАРАТ ДЛЯ СШИВАНИЯ КРОВЕНОСНЫХ СОСУДОВ | 1947 |
|
SU71792A1 |
| Способ получения производных имидазо-симм-триазина | 1975 |
|
SU600142A1 |
| Способ получения 2- @ - @ -алкилтио-7-оксо-4,7-дигидро-1,2,4-триазоло/5,1- @ / /1,2,4/-триазинов | 1982 |
|
SU1066999A1 |
| SU 1175936 A, 1985 | |||
| Паросиловая установка | 1975 |
|
SU569734A1 |
| Прибор для автоматического бесконтактного измерения толщины листовых материалов | 1960 |
|
SU141317A1 |
| Гербицидное и рострегулирующее средство | 1987 |
|
SU1658808A3 |
| DE 3533050 A, 1987. | |||
Авторы
Даты
1999-02-20—Публикация
1994-03-03—Подача