Изобретение относится к ветеринарии и может быть использовано для неспецифической иммуностимулирующей профилактики аллерготоксикозов молодняка сельскохозяйственных животных: отечной болезни поросят, пневмоэнтеритов телят и т.п.
При промышленном ведении животноводства селекция животных по продуктивности, стандартизация их по породе, полу и возрасту, а также большая концентрация поголовья в животноводческих помещениях приводят к возникновению таких заболеваний животных, как "болезнь скученности", "болезнь концентрации" или "факторные инфекции". В основе большинства этих заболеваний лежат аллерготоксикозы, связанные с нарушением режима и рациона питания, при стрессах, гипокинезии и т.п. Множественность этиологических факторов таких болезней не позволяет в условиях хозяйства провести четкую границу между незаразной и инфекционной патологией, что затрудняет ведение эффективной терапии и специфической профилактики. К числу таких многофакторных болезней относятся отечная болезнь свиней, пневмоэнтериты телят (диспепсия, бронхопневмония) и т.п.
Несмотря на многочисленные исследования, проведенные учеными в разных странах, природа отечной болезни до сих пор до конца не раскрыта. Одни считают специфическим возбудителем ее бета-гемолитические штаммы кишечной палочки разных серотипов, другие кишечный вибрион, третьи кокковую микрофлору, четвертые утверждают, что это кормовая аллергия, возникающая у поросят в период интенсивного обмена веществ и усиленного роста. Некоторые относят отечную болезнь в группу авитаминозов В. Отсутствие единой точки зрения на этиологию болезни затрудняет разработку эффективных мер борьбы с ней [1]
Однако анализ литературы дает основание утверждать, что отечная болезнь свиней это неконтагиозное, острое или подострое заболевание, характеризующееся поражением центральной нервной системы и желудочно-кишечного тракта, острой сердечной недостаточностью и наличием студенистых отеков в тканях. Патогенетической сущностью этой болезни является аллерготоксикоз. Существенное значение в его развитии имеют нарушение механизма регуляции иммунных реакций кишечника и взаимодействие иммунной системы желудочно-кишечного тракта с кормовыми антителами. В возникновении отечной болезни решающую роль играет дисбактериоз кишечника, характеризующийся резким уменьшением количества нормальной микрофлоры и бурным размножением бета-гемолитической кишечной палочки, гемолитических кокков и стафилококков на фоне кормовой аллергии и различных неблагоприятных факторов, снижающих резистентность организма. Толчком к возникновению отечной болезни, наряду с такими стрессовыми факторами, как транспортировка, вакцинация, смена помещения, являются погрешности в содержании и кормлении, часто имеющими место при отъеме поросят.
Ведущим фактором в развитии отечного синдрома является гистаминовая интоксикация в связи с избыточным накоплением его в организме в результате бактериального декарбоксилирования гистидина при кишечном дисбактериозе, что служит основной причиной гемодинамических расстройств и гибели свиней от коллапса или шока.
Болезнь поражает свиней всех возрастных групп, однако наиболее часто поросят в период отъема. Продолжительность болезни колеблется от нескольких часов до нескольких суток. Заболеваемость превышает 40% смертность может достигать 100% [2]
Для профилактики и лечения отечной болезни свиней известно применение различных антибиотиков, химиотерапевтических и биопрепаратов (иммунных сывороток, вакцин) как отдельно, так и в сочетании.
Для подавления токсигенной микрофлоры в кишечнике внутрь назначают неомицин, мономицин, полимиксин, хлортетрациклин, левомицетин и другие антибиотики в дозе 0,015-0,02 г/кг массы 2-3 раза в день в течение трех дней подряд. Антибиотики выбирают путем подтитровки.
Известно также использование сульфадимезина, сульфадиметоксина перорально в дозе 1 г и фуразолидона в дозе 0,25 г на одно животное 2-3 раза в день в течение трех дней подряд, а внутримышечно или внутрибрюшинно 10% раствора глюконата кальция с 1% раствором новокаина в дозе 15-20 мл.
Явно больным поросятам с признаками энтеротоксемии, кроме указанных выше препаратов, подкожно вводят кордиамин в дозе 0,07 мл/кг массы 2-3 раза в день до полного исчезновения симптомов сердечно-сосудистой недостаточности и улучшения общего состояния животных, внутримышечно-витамины В1 в дозе 10-20 мг/животное, В12 в дозе 30-50 мг/животное один раз в день 3-4 дн подряд.
На заключительном этапе превентивной терапии после прекращения дачи антибиотиков всем поросятам-отъемышам дают ацидофильные препараты [1]
Недостатки указанных методов профилактики и лечения отечной болезни свиней состоят в том, что при длительном применении антибиотиков или сульфаниламидных препаратов возможно возникновение резистентных к ним рас микробов, развитие дисбактериоза кишечника, побочных явлений токсикоаллергического характера.
Хорошим лечебным и профилактическим действием при отечной болезни обладают ацидофильные препараты, рекомендованные профессором Ф.Ф.Пороховым в 1960 г. Однако ограниченное их производство сдерживает широкое применение.
Известны попытки использования вакцин для профилактики отечной болезни, однако не имевшие успеха в связи с множественностью субтипов кишечной палочки, участвующих в патогенезе, и вовлеченностью в это процесс кормовых белков [3]
В механизме развития болезни важная роль принадлежит активным биогенным аминам и в первую очередь гистамину. Для снижения содержания гистамина в организме поросят при отечной болезни применяют антигистаминные препараты, способствующие повышению естественной резистентности организма. С этой целью рекомендуют вводить поросятам до и после отъема внутримышечно 5%-ный раствор новарсенола в дозе 1 мл/кг массы. В качестве десенсибилизирующих средств назначают димедрол, пипольфен, дипразин и др.
Однако широкому использованию их в ветеринарной практике препятствуют побочные действия, привыкание. Кроме того, при неоднократных введениях они вызывают аллергические реакции [4]
Наиболее близким к изобретению по совокупности существенных признаков является антигистаминный препарат гистаглобин, включающий гамма-глобулин в качестве носителя, гистамин и физиологический раствор при следующем соотношении компонентов, мг/мл:
Гамма-глобулин 4 8
Гистамин 0,00005 0,0001
Физиологический раствор Остальное
При смешивании гистамина с гамма-глобулином образуется антигенный комплекс, против которого организм вырабатывает защитные антитела. Активным началом этого комплексного препарата является гистамин. Гистаглобин не препятствует реакции антиген-антитело и в то же время нейтрализует вредное действие избыточного гистамина [5]
Основные недостатки гистаглобина заключаются в следующем:
входящий в его состав гамма-глобулин является плохо стандартизируемым препаратом, так как его качество и биологическая активность зависят от используемого способа выделения: осаждением спиртом, риванолом или полиэтиленгликолем, что снижает профилактический эффект от применения гистаглобина;
образование комплекса гистамин-гамма-глобулин не сопровождается созданием ковалентной связи между ними, что приводит к нестабильности состава и свойств препарата и снижению профилактического эффекта от его применения.
Известен также способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных путем использования антигистаминного препарата гистаглобина следующего состава, мг/мл:
Гистамин 0,00005-0,0001
Гамма-глобулин 4 8
Физиологический раствор Остальное,
который вводят животным подкожно за неделю до отъема в дозе 2 мл три раза с интервалом в 7 дн [5]
Данное решение взято за прототип.
Недостатки способа-прототипа состоят в том, что он обладает высокой трудоемкостью, связанной с многократным введением препарата животным, и низкой профилактической эффективностью по причине нестабильности препарата.
В задачу создания изобретения входил поиск носителя иммуностимулятора, стандартного по качеству и пригодного для образования ковалентной связи с гистамином, а также разработка на его основе антигистаминного препарата, обладающего стабильным составом и свойствами и более высоким по сравнению с гистаглобином профилактическим эффектом, и способами профилактики аллерготоксикозов молодняка сельскохозяйственных животных, направленного на снижение трудоемкости введения антигистаминного и повышение его профилактической эффективности.
Поставленная задача решена созданием группы изобретений, образующих единый изобретательский замысел и включающих совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается объем правовой охраны.
Предлагаемая группа изобретений включает антигистаминный препарат и способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных.
Антигистаминный препарат (авторское наименование "гисталит") включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается объем правовой охраны:
Гистамин 0,00005 0,0001
Сополимер винилпирролидона с органической кислотой в качестве носителя - 0,00154 0,0611
Растворитель Остальное
Антигистаминный препарат "гисталит" характеризуется также другими признаками, выражающими конкретные формы его выполнения:
в качестве носителя препарат содержит сополимер винилпирролидона с акриловой кислотой;
в качестве носителя препарат содержит сополимер винилпирролидона с кротоновой кислотой;
в качестве растворителя препарат содержит физиологический раствор;
в качестве растворителя препарат содержит смесь физиологического раствора и масляного адьюванта в соотношении 1:1;
в качестве растворителя препарат содержит смесь физиологического раствора и 3 5%-ный водной суспензии двуокиси кремния в соотношении 1:1.
Признаками изобретения, характеризующими антигистаминный препарат и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
антигистаминный препарат, который включает:
гистамин;
носитель гистамина;
растворитель.
По сравнению с прототипом существенным отличительным признаком изобретения является включение в состав гисталита в качестве носителя сополимера винилпирролидона с органической кислотой.
Другими отличительными признаками изобретения, выражающими конкретные формы его выполнения, являются:
в качестве носителя препарат содержит сополимер винилпирролидона с акриловой кислотой;
в качестве носителя препарат содержит сополимер винилпирролидона с кротоновой кислотой;
в качестве растворителя препарат содержит физиологический раствор;
в качестве растворителя препарат содержит смесь физиологического раствора и масляного адьюванта в соотношении 1:1;
в качестве растворителя препарат содержит смесь физиологического раствора и 3 5%-ный водной суспензии двуокиси кремния в соотношении 1:1.
Сополимер винилпирролидона с органической кислотой, в качестве которой используют акриловую и кротоновую кислоты, имеет следующую структурную формулу:
Полимер 1: R-H сополимер винилпирролидона с акриловой кислотой.
Полимер 2: R-CH3 сополимер винилпирролидона с кротоновой кислотой.
Известно, что указанные сополимеры обладают адьювантными свойствами и используются для стимуляции иммунного ответа против вирусных агентов [6, 7, 8]
В изобретении впервые предложено использовать полимеры 1 и 2 в качестве носителя для создания эффективных препаратов против невирусных заболеваний молодняка сельскохозяйственных животных, вызванных избыточным накоплением в их организме гистамина, при этом указанные полимеры используются для коньюгации с биогенным амином, который в несвязанном виде антигеном не является.
Функциональной группой полимеров 1 или 2, реакционноспособной по отношению к гистамину, является карбоксильная группа акриловой или кротоновой кислоты. Структурная формула мономерного звена, модифицированного остатком гистамина, имеет следующий вид:
Следует отметить, что термин "носитель" по отношению к гамма-глобулину употреблен условно, поскольку образование комплекса не сопровождается созданием ковалентной связи между гистамином и белком, тогда как в соответствии с изобретением в результате коньюгации гистамина с мономерным звеном акриловой или кротоновой кислоты в составе сополимера образуется ковалентная амидная связь и высокомолекулярный полиэлектролит становится носителем для гистамина низкомолекулярного гаптена.
Состав используемых в качестве носителей полиэлектролитов можно задавать, смешивая разное количество взятых для сополимеризации мономерных звеньев. Соотношение молей мономерных звеньев в полученном сополимере определяют химическими методами, после чего становится возможным рассчитать количество полиэлектролита, необходимое для реакции коньюгации с гистамином. Поскольку реактивным в составе используемых полиэлектролитов является звено акриловой или кротоновой кислоты полиэлектролит брали в количестве, обеспечивающем соотношение 2 или 20 моль кислоты на 1 моль гистамина. Избыток кислоты должен обеспечивать полное присоединение гистамина к полиэлектролиту. Количество остальных компонентов реакционной смеси рассчитывали, исходя из количества взятого гистамина: на 1 моль гистамина в реакцию вводили 20 моль водорастворимого карбодиимида и 40 моль глицина по окончании коньюгации.
Испытания свойств коньюгата в опытах на поросятах показали, что протективный эффект в соотношении отечной болезни был выше в случае применения коньюгата, полученного при соотношении 1 моль гистамина на 2 моль кислоты в составе полиэлектролита. Данное обстоятельство позволяет признать указанное соотношение оптимальным.
Для коньюгации с гистамином пригодны также сополимеры винилпирролидона с такими производными акриловой или кротоновой кислоты, как их активированные, например, N гидроксисукцинимидные эфиры. При введении в реакционную смесь сополимера винилпирролидона с активированным эфиром кислоты не требуется использования водорастворимого карбодиимида, но в результате образуется коньюгат аналогичного состава.
Обычно коньюгат получают в виде концентрата, содержащего 100000 доз в объеме 15 мл. Для приготовления указанного количества доз берут 10 мг гистамина дигидрохлорида. Для практического использования, т.е. для получения 1 дозы препарата в 1 мл его объема, коньюгат разбавляют различными растворителями. В качестве растворителя предлагается использовать физиологический раствор, смесь физиологического раствора и масляного адьюванта в соотношении 1:1 или смесь физиологического раствора и 3 5%-ный водной суспензии двуокиси кремния в соотношении 1:1.
Известно использование физиологического раствора в качестве растворителя лекарственных препаратов, в том числе и гистаглобина, предназначенных для парентерального введения. В качестве растворителей сложные (физиологические) растворы не имеют преимуществ перед простыми изотоническими растворами хлорида натрия или глюкозы [5, 9]
Известно использование масляных адьювантов при изготовлении эмульсионных вакцин. Адьюванты обеспечивают выраженную иммунологическую стимуляцию при смешивании их с растворенным в воде антигеном и получении водно-масляной эмульсии. В качестве основы масляного адьюванта известно использование масел различного происхождения: байоль F, дракеол 6VR, маркол 52, вазелиновое, парфюмерное, вакцинное масло, масло для противоящурных биопрепаратов, белое гидрированное масло, полиальфаолефиновое масло, полиэтилсилоксановые жидкости и др.
В качестве эмульгаторов известно использование в составе масляных адьювантов арлацела А, спана, ланолина, монтанидов, сукцинимида, эмульгатора ВHИИЗЖ, ЭПОЛ продукта этерификации смеси олеиновой и стеариновой кислот с полиглицерином и др. образующих эмульсии обратного типа. Масляный адьювант содержит 9 частей масляной основы и 1 часть эмульгатора [10, 11, 12, 13, 14]
В избретении впервые включен масляный адьювант в состав растворителя гисталита, при этом указанный адьювант наряду с иммуностимулирующей активностью проявляет новое, ранее не известное, свойство стабилизировать коньюгат "гистамин-полиэлектролит". Гисталит с масляным адьювантом обладает более высокой профилактической активностью по сравнению с препаратом на физиологическом растворе.
Масляный адьювант эмульгируют с физиологическим раствором в соотношении 1:1.
В изобретении впервые включена 3-5%-ная водная суспензия двуокиси кремния в состав растворителя гисталита, при этом двуокись кремния проявляет в составе гисталита иммуностимулирующую активность. Также впервые обнаружено новое свойство двуокиси кремния в составе гисталита стабилизировать коньюгат "гистамин-полиэлектролит". Гисталит с двуокисью кремния обладает примерно одинаковой профилактической активностью по сравнению с препаратом, содержащим масляный адьювант, и более высокой по сравнению с препаратом на физиологическом растворе. Для получения растворителя физиологический раствор и 3-5% -ную водную суспензию двуокиси кремния смешивают в равных объемах.
Благодаря использованию новой совокупности известных и отличительных признаков, характеризующих предлагаемый препарат, достигается технический результат, заключающийся в повышении стабильности состава и свойств и профилактической активности гисталита по сравнению с препаратом-прототипом гистаглобином, что подтверждено результатами исследований, сведения о которых приведены ниже.
Способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается объем правовой охраны:
1) использование в качестве антигистаминного препарата гисталита следующего состава, мг/мл:
Гистамин 0,00005 0,0001
Сополимер винилпирролидона с органической кислотой в качестве носителя - 0,00154 0,0611
Растворитель Остальное;
2) гисталит вводят животным внутримышечно;
3) гисталит вводят животным одно- или двукратно;
4) гисталит вводят животным в объеме 1-3 мл;
5) гисталит вводят поросятам однократно за 7-10 сут до отъема в объеме 1-2 мл;
6) гисталит вводят поросятам двукратно за 14-20 сут до отъема с интервалом 6-8 сут в объеме 2 мл на каждую инъекцию;
7) гисталит вводят телятам в первый день жизни в объеме 2-3 мл.
Признаками изобретения, характеризующими способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных и совпадающими с признаками способа-прототипа, в том числе родовое понятие, отражающее его назначение, являются
способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных;
использование для этого антигистаминного препарата.
По сравнению с прототипом существенными отличительными признаками изобретения "Способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных" являются:
1) использование в качестве антигистаминного препарата гисталита следующего состава, мг/мл:
Гистамин 0,00005 0,0001
Сополимер винилпирролидона с органической кислотой в качестве носителя - 0,00154 0,0611
Растворитель Остальное;
2) гисталит вводят животным внутримышечно;
3) гисталит вводят животным одно- или двукратно;
4) гисталит вводят животным в объеме 1-3 мл;
5) гисталит вводят поросятам однократно за 7-10 сут до отъема в объеме 1-2 мл;
6) гисталит вводят поросятам двукратно за 14-20 сут до отъема с интервалом 6-8 сут в объеме 2 мл на каждую инъекцию;
7) гисталит вводят телятам в первый день жизни в объеме 2-3 мл.
В результате анализа известных решений из уровня техники нами установлено, что существенный отличительный признак предлагаемого способа, заключающийся в использовании нового антигистаминного препарата гисталита, не известен. Другие отличительные признаки предлагаемого способа, характеризующие возраст иммунизируемых животных, метод, кратность, дозировку и сроки введения препарата животным, не могут рассматриваться в отрыве от отличительного признака, характеризующего используемый препарат.
Достижение технического результата изобретения можно объяснить более высокой стабильностью состава и свойства гисталита и его способностью повышать содержание антигистаминных факторов в крови у животных, что позволяет сократить количество инъекций препарата (по сравнению с прототипом) и проводить эти операции до отъема поросят и в первый день жизни телят.
Благодаря использованию совокупности признаков, характеризующих предлагаемый способ, достигается технический результат изобретения повышение профилактического эффекта от применения гисталита и снижение трудоемкости его введения животным.
Пример 1. Коньюгат "гистамин-полимер 1 или 2" готовят следующим образом.
При использовании полимером 1 или 2 готовят водный раствор полимера, pH раствора доводят 1M раствором едкого кали или едкого натра до значения 5,0.
Добавляют водорастворимый карбодиимид, перемешивают 20 мин и доводят pH до 7,0 добавлением 0,1 M раствора едкого кали или едкого натра, после чего приливают 0,1% -ный водный раствор дигидрохлорида гистамина. Смесь перемешивают 72 ч при комнатной температуре, затем в нее добавляют глицин и продолжают перемешивать еще 24 ч. На 1 моль гистамина в реакцию вводят 20 моль водорастворимого карбодиимида и 2 или 20 моль органической кислоты (акриловой или кротоновой) в составе сополимера с винилпирролидоном и 40 моль глицина по окончании коньюгации. Обычно коньюгат получают в виде концентрата, содержащего 100000 доз в 15 мл. Для приготовления указанного количества доз берут 10 мг дигидрохлорида гистамина.
Пример 2. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 1 0,00154
Растворитель Остальное
Коньюгат "гистамин-полимер 1" получают так, как описано в примере 1.
В качестве растворителя используют физиологический раствор. Для приготовления гисталита коньюгат растворяют в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 2 мл раствора хлорида натрия содержалось 0,00005 мг гистамина и 0,00154 мг полимера 1. Такой объем препарата готовят для более точного введения дозы препарата с помощью автоматического инъектора. Гисталит представляет собой прозрачную с легкой опалесценцией жидкость.
Пример 3. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 1 0,04
Растворитель Остальное
В качестве растворителя используют физиологический раствор. Коньюгат "гистамин-полимер 1" получают так, как описано в примере 1.
Для приготовления гисталита коньюгат растворяют в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 2 мл раствора хлорида натрия содержалось 0,000075 мг гистамина и 0,04 мг полимера 1. Гисталит представляет собой прозрачную с легкой опалесценцией жидкость.
Пример 4. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 1 0,0611
Растворитель Остальное
Коньюгат "гистамин-полимер 1" получают так, как описано в примере 1.
В качестве растворителя используют физиологический раствор.
Для приготовления гисталита коньюгат растворяют в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 2 мл раствора хлорида натрия содержалось 0,0001 мг гистамина и 0,0611 мг полимера 1. Гисталит представляет собой прозрачную с легкой опалесценцией жидкость.
Пример 5. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 2 0,00154
Растворитель Остальное
Гисталит готовят так, как описано в примере 2.
Пример 6. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 2 0,04
Растворитель Остальное
Гисталит готовят так, как описано в примере 3.
Пример 7. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 2 0,0611
Растворитель Остальное
Гисталит готовят так, как описано в примере 4.
Пример 8. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 1 0,00154
Растворитель Остальное
Коньюгат "гистамин-полимер 1" получают так, как описано в примере 1.
В качестве растворителя используют смесь физиологического раствора и масляного адьюванта, взятых в соотношении 1:1.
Для приготовления гисталита коньюгат растворяют сначала в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,00005 мг гистамина и 0,00154 мг полимера 1. После этого полученный раствор смешивают с масляным адьювантом в соотношении 1:1 путем диспергирования смеси на коллоидной мельнице в течение 15 мин.
Полученный гисталит представляет собой жидкую эмульсию белого цвета.
Пример 9. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 1 0,04
Растворитель Остальное
Гисталит готовят так, как описано в примере 8. Отличие состоит в том, что коньюгат растворяют в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,000075 мг гистамина и 0,04 мг полимера 1.
Пример 10. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 1 0,0611
Растворитель Остальное
Гисталит готовят так, как описано в примере 8. Отличие состоит в том, что коньюгат растворяют сначала в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,0001 мг гистамина и 0,0611 мг полимера 1.
Пример 11. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 2 0,00154
Растворитель Остальное
Гисталит готовят так, как описано в примере 8.
Пример 12. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 2 0,04
Растворитель Остальное
Гисталит готовят так, как описано в примере 9.
Пример 13. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 2 0,611
Растворитель Остальное
Гисталит готовят так, как описано в примере 10.
Пример 14. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 1 0,00154
Растворитель Остальное
Коньюгат "гисталит-полимер 2" получают так, как описано в примере 1.
В качестве растворителя используют смесь физиологического раствора и 4% суспензии двуокиси кремния pH 7,2-7,4 в соотношении 1:1.
Для приготовления гисталита коньюгат растворяют сначала в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,00005 мг полимера 1. После этого полученный раствор смешивают с 4%-ной суспензией двуокиси кремния pH 7,2-7,4 в соотношении 1:1.
Пример 15. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 1 0,04
Растворитель Остальное
Гисталит готовят так, как описано в примере 14. Отличие состоит в том, что коньюгат растворяют сначала в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,000075 мг гистамина и 0,04 мг полимера 1.
Пример 16. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 1 0,0611
Растворитель Остальное
Гисталит готовят так, как описано в примере 14. Отличие состоит в том, что коньгат растворяют сначала в стерильном 0,9% растворе хлорида натрия pH 7,2-7,4 с таким расчетом, чтобы в 0,5 мл раствора хлорида натрия содержалось 0,0001 мг гистамина и 0,0611 мг полимера 1.
Пример 17. Состав гисталита, мг/мл:
Гистамин 0,00005
Полимер 2 0,00154
Растворитель Остальное
Гисталит готовят так, как описано в примере 14.
Пример 18. Состав гисталита, мг/мл:
Гистамин 0,000075
Полимер 2 0,04
Растворитель Остальное
Гисталит готовят так, как описано в примере 15.
Пример 19. Состав гисталита, мг/мл:
Гистамин 0,0001
Полимер 2 0,061
Растворитель Остальное
Гисталит готовят так, как описано в примере 16.
Пример 20. Гисталит, полученный так, как описано в примере 2, используют для профилактики отечной болезни поросят. При однократной инъекции препарат вводят животным внутримышечно за 7-10 сут до отъема в объеме 2 мл, а при двукратной за 14-20 сут до отъема с интервалом 7 сут в объеме 2 мл на каждое введение.
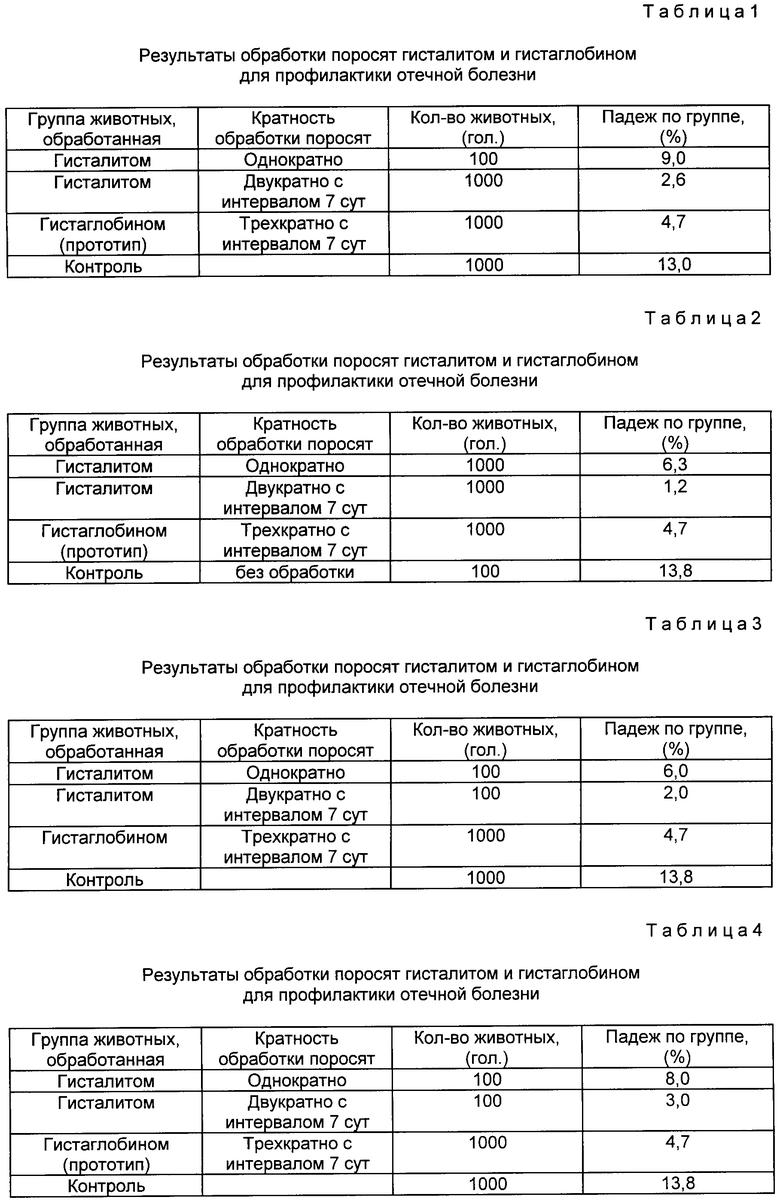
Результаты испытания препарата по сравнению с прототипом приведены в табл. 1.
Согласно табл. 1 после одно или двукратной обработки поросят гисталитом падеж животных от отечной болезни составил соответственно 9,0 и 2,6% В то время, как после трехкратной обработки поросят гистаглобином падеж составил 4,7%
Пример 21. Гисталит полученный так, как описано в примере 3, используют для профилактики отечной болезни поросят. Препарат вводят животным так, как описано в примере 20.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 2.
Из табл. 2 видно, что после одно- и двукратной обработки поросят гисталитом падеж животных от отечной болезни был 6,3 и 1,2% соответственно. В то время как, после трех инъекций поросятам гистаглобина падеж составил 4,7%
Пример 22. Гисталит, полученный так, как описано в примере 4, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 20.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 3.
Из табл. 3 следует, что результаты проверки эффективности профилактики отечной болезни гисталитом, приготовленным в соответствии с примером 4, аналогичны результатам, приведенным в табл 2.
Пример 23.
Гисталит, полученный так, как описано в примере 5, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 20.
Результаты испытания препарата по сравнению с прототипом приведены в табл. 4.
Из табл. 4 видно, что результаты применения гисталита, полученного так, как описано в примере 5, не отличаются от результатов испытания гисталита, приготовленного так, как описано в примере 2.
Пример 24. Гисталит, полученный так, как описано в примере 6, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 20.
Результаты испытания препарата по сравнению с прототипом приведены в табл. 5.
Из табл. 5 следует, что падеж поросят от отечной болезни после одно- и двукратной обработки гисталитом был равен 5,3 и 1,6% соответственно.
Пример 25. Гисталит, полученный так, как описано в примере 7, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 20.
Результаты испытания препарата в сравнению с прототипом приведены в табл. 6.
Из табл. 6 видно, что результаты профилактики отечной болезни поросят гисталитом, приготовленным так, как описано в примере 7, были аналогичны результатам, отраженным в примере 24.
Пример 26. Гисталит, полученный так, как описано в примере 8, используют для профилактики отечной болезни поросят.
Препарат вводят животным внутримышечно за 7-10 сут до отъема в объеме 1 мл однократно.
Результаты испытания препарата по сравнению с прототипом приведены в табл. 7.
Согласно табл. 7 после однократной обработки поросят гисталитом падеж животных от отечной болезни составил 4,0%
Примкр 27. Гисталит, полученный так, как описано в примере 9, используют для профилактически отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
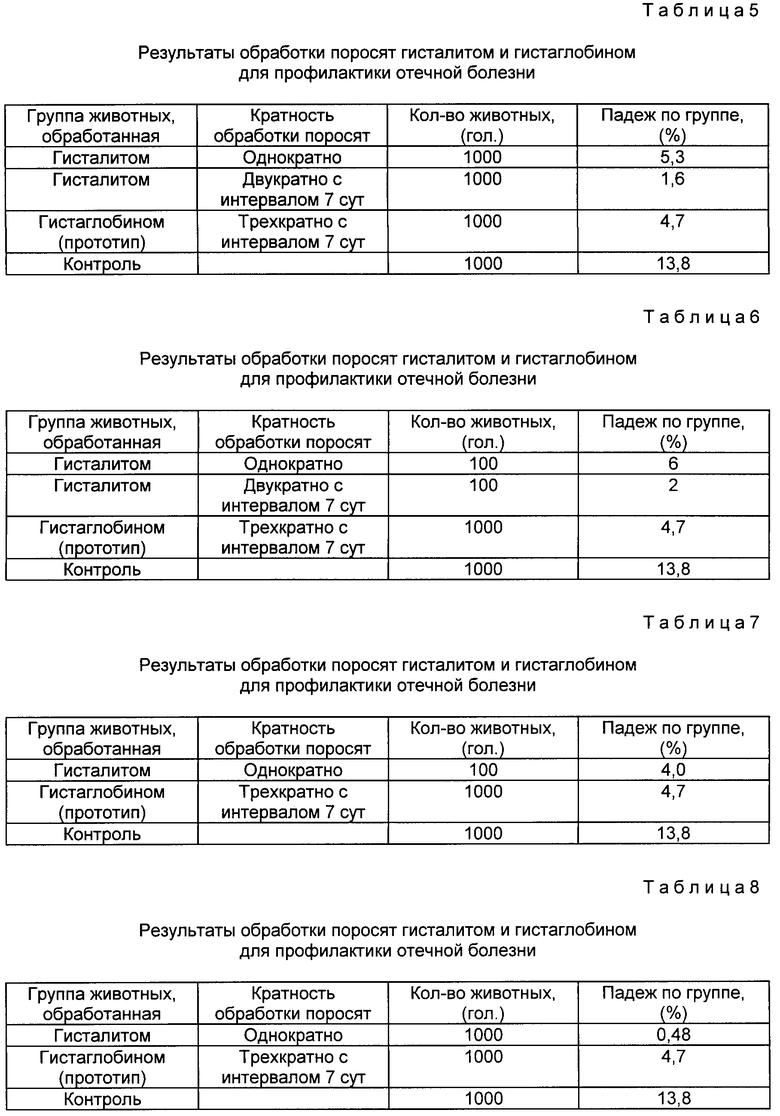
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 8.
Анализируя данные табл. 8, можно заключить, что падеж поросят от отечной болезни после одной обработки эмульсионным гисталитом был равен 0,48% Вторая инъекция не приводила к снижению падежа.
Пример 28. Гисталит, полученный так, как описано в примере 10, используют для профилактически отечной болезни поросят.
Препарат вводят животным так, как описано а примере 26.
Результаты испытания препарата по сравнению с прототипом приведены в табл. 9.
Из табл. 9 видно, что падеж поросят от отечной болезни после однократной обработки гисталитом был исключен.
Пример 29. Гисталит, полученный так, как описано в примерах 8 или 11, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 10.
Из табл. 10 видно, что результаты обработки поросят гисталитом для профилактики отечной болезни были аналогичны результатам, описанным в примере 26.
Пример 30. Гисталит, полученный так, как описано в примерах 9 или 12, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания препарата по сравнению с прототипом проведены в табл. 11.
Из табл. 11 следует, что результаты профилактики отечной болезни поросят гисталитом не отличаются от данных, описанных в примере 27.
Пример 31. Гисталит, полученный так, как описано в примерах 10 или 13, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания препарата по сравнению с прототипом проведены в табл. 12.
Из табл. 12 видно, что падеж поросят от отечной болезни после обработки гисталитом был равен 1%
Пример 32. Гисталит, полученный так, как описано в примере 14, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
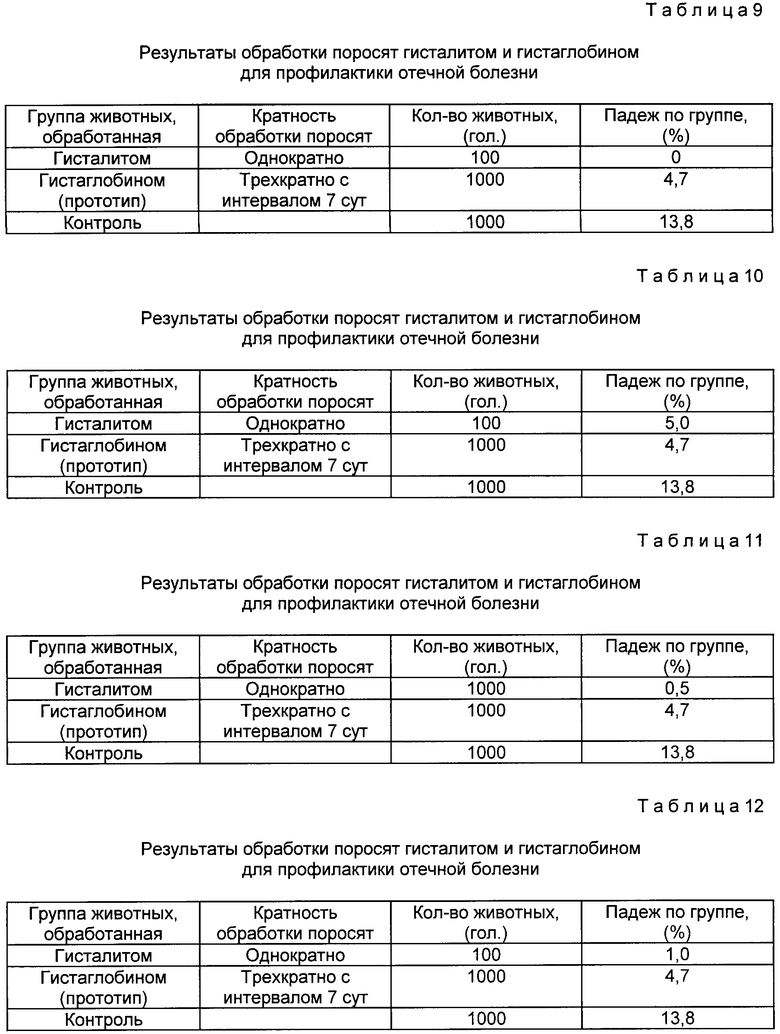
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 13.
Из табл. 13 следует, что падеж поросят от отечной болезни после профилактики гисталитом после однократной обработки составил 5,0%
Пример 33. Гисталит, полученный так, как описано в примере 15, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 14.
Из табл. 14 видно, что после однократной обработки поросят гисталитом, падеж от отечной болезни был равен 0,6%
Пример 34. Гисталит, полученный так, как описано в примере 16, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 15.
Согласно табл. 15 падеж поросят от отечной болезни после однократной обработке гисталитом составил 1%
Пример 35. Гисталит, полученный так, как описано в примерах 14 или 17, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 16.
Из табл. 16 видно, что результаты обработки поросят гисталитом для профилактики отечной болезни были аналогичны данным, приведенным в примере 32.
Пример 36. Гисталит, полученный так, как описано в примерах 15 или 18, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
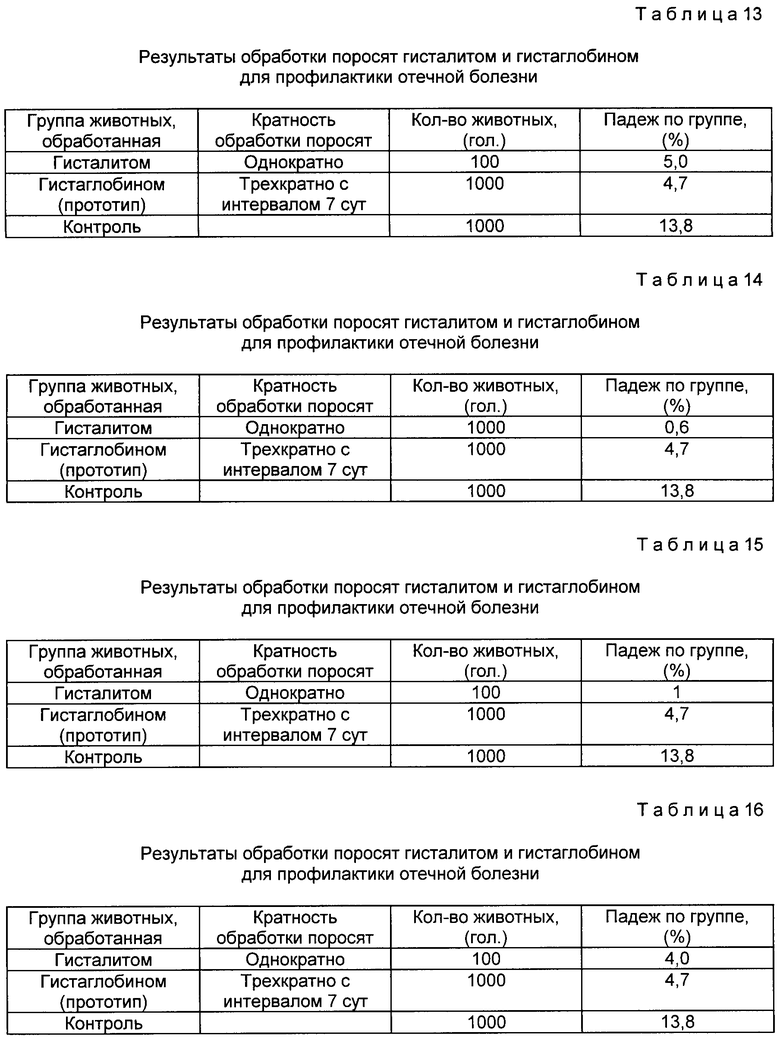
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 17.
Из табл. 17 следует, что падеж поросят от отечной болезни в первой группе был равен 0,6%
Пример 37. Гисталит, полученный так, как описано в примерах 16 или 19, используют для профилактики отечной болезни поросят.
Препарат вводят животным так, как описано в примере 26.
Результаты испытания гисталита по сравнению с прототипом приведены в табл. 18.
Из табл. 18 видно, что после обработки поросят гисталитом однократно падеж от отечной болезни составил 1%
Пример 38. В опытах на лабораторных животных (белые мыши массой 16 18 г) была проверена острая токсичность и местная (кожная) реакция путем введения свободного гистамина и его коньюгатов. Результаты исследований приведены в табл. 19.
Представленные в табл. 19 результаты свидетельствуют о том, что гисталит и гистаглобин не вызывают как местной, так общей реакции. При этом гистамина в составе гисталита было введено в 44 раза больше, чем в составе гистаглобина (введение более высокой дозы прототипа технически невозможно). В то же время введение свободного гистамина в такой же дозе вызывало местную реакцию, проявляющуюся в форме отека, покраснения ткани и изменения общего состояния, напоминающего анафилактический шок.
Таким образом показано, что гисталит является нетоксичным препаратом. Следовательно, входящий в его состав гистамин надежно иммобилизирован.
Пример 39. В серии опытов было изучено влияние носителя гистамина на проявление протективной активности антигистаминных препаратов. Для этого сформировали 5 групп поросят в возрасте 20 дн. по 150 голов в каждой. Результаты исследований представлены в табл. 20.
Из представленных в табл. 20 результатов видно, что среди поросят контрольной группы отечная болезнь поразила 3,3% животных несмотря на то, что в течении 20 дн, после отъема поросят этой группы содержались на полуголодной диете. В тоже время в 4 группе (опытная), в которой животные содержались на полуголодной диете в течении 7-10 дн, заболело меньшее количество поросят. При использовании в качестве носителя гамма-глобулина (спиртового) и полимера 1 заболеваемость составила 0,7% что существенно ниже, чем в контрольной группе. При использовании в качестве носителя БСА протективный эффект отсутствовал. Таким образом, полимер 1 оказался эффективным носителем при создании антигистаминного препарата.
Пример 40. В серии опытов была изучена эффективность образцов гисталита на основе полимера 1, но с различной гистаминовой нагрузкой. При одинаковом содержании количество полимера 1 в препарате А было в 10 раз больше, чем в препарате В. При этом суммарная доза гистамина в прививной дозе составила 0,2 мкг дигидрохлорида гистамина. Результаты исследований представлены в табл. 21.
Из представленных в табл. 21 данных видно, что при использовании гисталита "высокой нагрузкой гистамина" (группа В) протективный эффект в отношении отечной болезни был высоким. При "низкой гистаминовой нагрузке" (группа А) эффективность гисталита снижалась.
Исходя из этих данных в дальнейшей работе использовали гисталит с полимером 1, содержащий в одной прививной дозе 0,2 мкг дигидрохлорида гистамина в составе коньюгата.
Пример 41. За 7-10 сут до отъема поросят обрабатывали однократно в объеме 1 мл гисталитом с полимером 2, который содержал 0,2 мкг дигидрохлорида гистамина при соотношении гистамин: полимер 2, равном 1:2. Аналогичная группа была оставлена в качестве контроля для наблюдения. Результаты исследований приведены в табл.22.
Из представленных в табл. 22 результатов видно, что гисталит обеспечил не только снижение заболеваемости в опытной группе на 4,2% по сравнению с контролем, но и позволил перейти с полуголодной диеты на полнорационное кормление на 18 дн, что гарантирует в целом лучшее развитие поросят и большие привесы.
Пример 42. Поскольку аллергические реакции играют определенную роль при пневмоэнтеритах (диспепсия, бронхопневмония) телят были проведены опыты по использованию гисталита для профилактики данных заболеваний.
Для определения эффективности гисталита в качестве средства профилактики пневмоэнтеритов телят в неблагополучном по данному заболеванию хозяйстве были сформированы две группы по 12 телят в каждой. Телятам первой группы подкожно в область средней трети шеи вводили гистаглобин в дозе 1,2 и 3 мл (в возрасте 1,4 и 7 дн), телятам второй группы гисталит в первый день жизни в объеме 2-3 мл. Аналогичная группа оставалась под наблюдением в качестве контроля. За животными вели наблюдение в течение 21 дн, регистрируя заболеваемость, количество гемоглобина в крови и общую иммунологическую реакцию (ОИР) внутрикожной реакцией по Иоффе. Результаты исследований приведены в табл. 23.
Поставленные в табл. 23 данные свидетельствуют о том, что после гистаглобина и гисталита заболеваемость телят снизилась на 50% У телят опытной группы возрастало содержание гемоголобина в крови, тогда как у животных контрольной группы количество гемоголобина в образцах крови уменьшилось. Кроме этого, при определении ОИР в ответ на введение антивидовой сыворотки отмечено увеличение кожной складки более, чем на 0,6 мм.
Таким образом, гисталит не уступает по своей активности прототипу. Авторами предложены антигистаминный препарат гисталит и способ профилактики аллерготоксикозов у молодняка сельскохозяйственных животных с применением гисталита, использование которых обеспечивает с прототипами следующие преимущества:
гисталит проявляет заметную антиаллергическую активность и обеспечивает выраженный профилактический эффект при отечной болезни поросят и пневмоэнтеритах телят:
гисталит легко поддается стандартизации, так как коньюгации гистаминаи полимеров 1 и 2 происходит при определенных задаваемых физико-химических параметрах, а на сам носитель не вырабатываются антитела;
стоимость полимеров 1 и 2 ниже стоимости гамма-глобулина;
снижение трудоемкости введения гисталита.
Гисталит и способ профилактики аллерготоксикозов молодняка сельскохозяйственных животных с использованием гисталита найдут применение в сельскохозяйственном производстве для профилактики отечной болезни поросят и пневмоэнтеритов телят.
Источник информации:
1. Прохоров Ф.Ф. Отечная болезнь поросят. (Этиология, клиника, лечение). Ветеринария, 1984, 8, 36-38.
2. Матюшев П.С. Мероприятия по борьбе с отечной болезнью (колиэнтеротоксемией) свиней. Ветеринария, 1994, 4, 9-13.
3. Еремеев М.Н. О патогенности кишечной палочки, выделяемой при отечной белезни поросят. Ветеринария, 1971, 2, 52-53.
4. Матюшев П.С. Профилактика отечной болезни свиней. Ветеринария, 1985, 7, 38-39.
5. Матюшев П.С. Профилактика отечной болезни поросят. Ветеринария, 1973, 3, 62-63 (прототип).
6. Петров Р.В. Иммуная биотехнология: достижения и перспективы. ЖВХО им. Д.И.Менделеева, 1988, XXXIII, 5, 484-493.
7. Петров Р. В. Кабанов В.А. Хаитов Р.М. Искусственные антигены и вакцины. ЖВХО им. Д.И.Менделеева, 1988, 5, 502-522.
8. Скворцов В.Ю. Мастернак Т.Б. и др. Изучение иммуномодулирующих и токсических характеристик сополимеров винилпирролидона с кротоновой кислотой и виниламином. Иммунология, 1989, 3, 63-65.
9. БМЭ, М. "Сов.Энциклопедия", 1978, изд. 3, т.9, с.57.
10. Ящур. Бурдов А.Н. Дудников А.И. Малярец П.В. и др./Под ред. А.Н.Бурдова. М. Агропромиздат, 1990, 239-250.
11. Патент РФ N 1615917, кл. A 61 K 39/135, 35/06; 10.05.89.
12. Патент РФ N 1615918, кл. A 61 K 39/135, 35/06; 22.05.89.
13. Патент РФ N 1692022, кл. A 61 K 39/135, 35/06; 31/23. 30.11.89.
14. Патент РФ N 1743027, кл. A 61 K 39/135, 35/06; 30.11.89.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ МАСТИТА, РАН, ТРАВМ И ОЖОГОВ КОЖИ ВЫМЕНИ ЖИВОТНЫХ | 2000 |
|
RU2170575C1 |
| СПОСОБ ОЧИСТКИ И СТЕРИЛИЗАЦИИ КУЛЬТУРАЛЬНОГО ВИРУСА ЯЩУРА | 1992 |
|
RU2054039C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ОСТРЫХ ФОРМ ТИМПАНИИ РУБЦА У ЖВАЧНЫХ ЖИВОТНЫХ И/ИЛИ ОСТРОГО МЕТЕОРИЗМА КИШЕЧНИКА У ЛОШАДЕЙ | 2000 |
|
RU2170088C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИННОГО ПРЕПАРАТА ПРОТИВ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ ЖИВОТНЫХ И ПТИЦ | 2000 |
|
RU2173560C1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ MUS MUSCULUS L. - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ВИРУСУ ВЕЗИКУЛЯРНОЙ БОЛЕЗНИ СВИНЕЙ ШТАММ Т-75 | 1997 |
|
RU2117700C1 |
| АДЪЮВАНТ | 1996 |
|
RU2108111C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭМУЛЬСИОННОЙ ПРОТИВОПАСТЕРЕЛЛЕЗНОЙ ВАКЦИНЫ | 2000 |
|
RU2162339C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЫВОРОТКИ ДЛЯ СЕРОДИАГНОСТИКИ ЯЩУРА ТИПА A | 1999 |
|
RU2140290C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-ГЛОБУЛИНА ДЛЯ ЛЕЧЕНИЯ ЭПИЗООТИЧЕСКОГО ЛИМФАНГОИТА ЛОШАДЕЙ | 1997 |
|
RU2116082C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ КЛЕТОК ГОНАД CAPRA HIRCUS L-ПРОДУЦЕНТ ВИРУСОВ ЖИВОТНЫХ | 1994 |
|
RU2061753C1 |


Использование: для неспецифической иммуностимулирующей профилактики аллерготоксикозов молодняка сельскохозяйственных животных: отечной болезни поросят, пневмоэнтеритов телят и т.п. Сущность изобретения: гисталит содержит, мг/мл: гистамин 0,00005- 0,0001; сополимер винилпирролидона с органической кислотой в качестве носителя 0,00154-0,0611 и растворитель остальное. В качестве растворителя препарат содержит физиологический раствор или смесь физиологического раствора и масляного адъюванта в соотношении 1:1, или смесь физиологического раствора и 3-5% водной суспензии двуокиси кремния в соотношении 1: 1. Гисталит получен в результате конъюгации гистамина со звеном органической кислоты в составе сополимера с винилпирролидоном. Для профилактики аллерготоксикозов гисталит вводят животным внутримышечно: поросятам за 7-10 сут. до отъема в объеме 1-2 мл при однократном введении, при двукратном: за 14-20 сут до отъема с интервалом 6-8 сут. в объеме 1-2 мл на каждую инъекцию; телятам - в первый день жизни в объеме 2-3 мл. Изобретения позволяют повысить стабильность состава и свойств препарата, а также эффективность профилактики аллерготоксикозов и снижение трудоемкости при обработке животных. 2 с. и 8 з.п. ф-лы, 23 табл.
Гистамин 0,00005 0,0001
Сополимер винилпирролидона с органической кислотой 0,00154 0,00611
Растворитель Остальное
2. Препарат по п. 1, отличающийся тем, что в качестве носителя препарат содержит сополимер винилпирролидона с акриловой кислотой.
Гистамин 0,00005 0,0001
Сополимер винилпирролидона с органической кислотой 0,00154 0,0611
Растворитель Остальное
который вводят животным внутримышечно одно- или двукратно с интервалом 6 8 дней в объеме 1 3 мл на каждую инъекцию.
| Матюшев П.С | |||
| Профилактика отечной болезни поросят | |||
| - Ветеринария, 1973, N 3, с | |||
| Способ крашения тканей | 1922 |
|
SU62A1 |
Авторы
Даты
1997-08-27—Публикация
1995-10-16—Подача