Изобретение относится к области технологии получения биологически активных веществ, конкретно касается получения рибонуклеозид-5'-фосфатов, находящих применение в медицине, биохимии и биологии.
Таким образом изобретение относится к способу получения 5'-монофосфатов, 5'-дифосфатов и 5'-трифосфатов аденозина, уридина и цитидина.
Наиболее общем методом получения рибонуклеозид-5'-фосфатов является ферментативное фосфорилирование нуклеозида в присутствии пивных дрожжей. При этом, как правило, получают смесь моно-, ди- и трифосфатов, а также исходного нуклеозида. Методом колоночной хроматографии эту смесь разделяют на отдельные компоненты.
Основная сложность в проведении реакции ферментативного фосфорилирования заключается в необходимости использования такого ингредиента как дрожжи, активность которых определяется качеством каждой партии дрожжей, которое определяет время протекания реакции с получением оптимальных результатов.
Описан способ получения аденозин-5'-трифосфата [1] в соответствии с которым аденозин при рH 6,2-7,0 фосфорилируют в присутствии неорганических фосфатов, углеводов, пивных дрожжей, толуола, хлористого калия и хлористого магния. Ход реакции контролировали по изменению рH реакционной среды. Для завершения процесса добавляли ледяную уксусную кислоту до рH 4,5-4,8 и охлаждали смесь до +4oС. Фильтрацией отделяли дрожжевой шлам. Фильтрат разбавляли водой и вели сорбцию продуктов реакции на сильноосновном анионите. После сорбции анионит промывали водой и 0,004 н. соляной кислотой. Элюцию вели сначала 0,02 н. раствором хлористого натрия в 0,01 н. соляной кислоте при этом выделяли аденозин-5'-монофосфат.
Затем элюируют аденозин-5'-дифосфат 0,02 раствором хлористого натрия в 0,01 н. соляной кислоте и аденозин-5'-трифосфат 0,5 н. раствором хлористого натрия в 0,02 Н соляной кислоте. Из элюатов ди- и трифосфаты выделяли осаждением в избыток этилового спирта при комнатной температуре. При этом из первого элюата осаждается мононатриевая соль дифосфата с чистой до 96% и выходом 10-12%
Осадок из второго элюата растворяют в воде, добавляют хлористый натрий, устанавливают рH 1,8-2,3 и смешивают с равным объемом этанола. В результате кристаллизации получают динатриевую соль трифосфата с чистой 98-99% и выходом 66-68% Выходы рассчитывали на введенный в реакцию аденозин.
Основным недостатком известного способа является относительно невысокие выходы целевого продукта. Это можно объяснить косвенным методом определения времени реакции по изменению рH реакционного раствора. Кроме того, при масштабировании процесса значительную сложность начинает представлять удаление дрожжевого шлама из-за его плохой фильтруемости и неполного удаления водорастворимых белков. Наконец, целевые продукты содержат повышенные количества ионов тяжелых и многовалентных металлов.
Описан также способ получения аденозин-5'-трифосфата [2] в соответствии с которым аденозином ферментативно фосфорилируют в присутствии пивных дрожжей в условиях, описанных в вышеуказанном способе-аналоге [1] Дрожжевой шлам отделяют при рH 4,5-4,8 и при +4oС. Фильтрат, содержащий 78-84% аденозин-5'-трифосфата, 10-17% аденозин-5'-дифосфата, 2-3% аденозин-5'-монофосфата и около 3% аденозина, разделяют на сильноосновном анионите, как это описано выше. Выход кристаллического аденозин-5'-трифосфата 60-66% чистота 98-99% Дополнительное количество трифосфата получают, используя в качестве источника нуклеозида элюенты, содержащие ди- и монофосфат, ионы калия и магния.
Недостатки, присущие первому аналогу и основанные на плохой воспроизводимости реакции фосфорилирования при косвенном методе определения времени реакции, которое является оптимальным для целевого продукта, не преодолены вторым способом-прототипом.
Задачей предлагаемого изобретения является создание способа получения любого из рибонуклеозид-5'-фосфатов с повышенным выходом при более высокой степени полноты удаления дрожжевого шлама, белковых примесей и ионов тяжелых и многовалентных металлов.
Задача была решена способом получения рибонуклеозид-5'-фосфатов, который реализуется совокупностью следующих существенных признаков:
1. Проводят ферментативное фосфорилирование рибонуклеозида в присутствии неорганических фосфатов, сахаров, хлористого калия, хлористого магния, толуола и пивных дрожжей при рH 6,2-7,0 и при 37 ± 1oС.
2. Реакцию завершают после количественного исчерпания исходного нуклеозида и получения максимального количества целевого продукта с завершением реакции подкислением реакционной смеси ледяной уксусной кислотой до рH 4,5 4,8.
3. Смесь охлаждают до +10-20oС и отделяют дрожжевой шлам.
4. Надосадочный раствор подкисляют до рH 3,0-5,0 и выдерживают при 45-75oС в течение 20-60 мин, затем охлаждают до комнатной температуры и отделяют осадок.
5. Фильтрат подают на колонку с сильноосновным анионитом, после сорбции колонку промывают водой.
6. Элюцию нуклеозид-5'-моно- и -дифосфатов в виде мононатриевой соли ведут раствором 0,02 н. хлористого натрия в 0,01 н. соляной кислоты.
7. Элюцию нуклеозид-5'-трифосфата в виде натриевых солей ведут 0,5 н. хлористым натрием в 0,02 н. соляной кислоте.
8. Элюент приливают в избыток смешивающегося с водой растворителя, осадок отфильтровывают, растворяют в воде и деионизуют.
9. Деионизацию проводят, пропуская водный раствор через сульфокатионит в H+ форме с последующим приливанием деонизованного раствора в избыток смешивающегося с водой растворителя.
10. Деионизацию проводят, добавляя в водный раствор 0,001-1% трилона Б с последующим приливанием деионизованного раствора в избыток смешивающегося с водой растворителя.
11. В качестве смешивающегося с водой растворителя используют ацетон или этанол, охлажденный до -8-12oС.
Отличительными от способа-прототипа признаками являются признаки 2, 4, 8-11.
Прежде всего, реакцию фосфорилирования завершает сразу же после количественного исчерпания исходного рибонуклеозида и получения максимального количества целевого продукта. Во-вторых, смесь после отделения дрожжевого шлама подкисляют до рH 3,0-5,0 и выдерживают 20-60 мин при 45-75oС, затем охлаждают до комнатной температуры и отделяют выпавшие балластные вещества, сформировавшие легко отделяемый осадок. В-третьих, целевые продукты выделяют осаждением в смешивающийся с водой растворитель, взятый в избытке. В качестве такого растворителя берут либо ацетон, либо этанол, охлажденный до -8
-2oС.
Анализ известного уровня науки и техники не позволил обнаружить информацию о способе получения рибонуклеозид-5'-фосфатов, полностью идентичном предлагаемому по совокупности существенных признаков.
Это подтверждает соответствие предлагаемому изобретения требованию "новизна".
До сих пор не было предложено решения, позволяющего контролировать условия протекания процесса фосфорилирования нуклеозидов при непосредственном определении динамики изменения концентрации продукта, который является целевым.
Это не позволило оптимизировать условия проведения процесса получения отдельных производных рибонуклеозид-5'-фосфатов в зависимости от активности используемых дрожжей и таким образом увеличить выход любого целевого продукта.
Удалось подобрать условия проведения экспресс-тонкослойной хроматографии с количественным определением производных, несмотря на сложный состав реакционной смеси, содержащей большое количество неорганических и органических ионов, низко- и высокомолекулярных веществ.
Поскольку рибонуклеозид-5'-фосфаты производятся в течение длительного времени и в промышленных масштабах, то можно утверждать, что настоящим изобретением решена задача, которая давно стояла перед обществом, но до сих пор решена не была.
Вторая важная проблема, решенная изобретением, состоит в том, что достигается более полная очистка растворов, идущих на хроматографическое разделение, от примесей неполностью отделенного дрожжевого шлама, балластных белков, ионов тяжелых металлов и многовалентных металлов. Все эти примеси затрудняют и удлиняют процесс сорбции, промывания, элюции и регенарации анионита. Кроме того, они снижают качество целевых продуктов.
Более полная очистка достигается за счет использования новой стадии - термоосаждения при нагревании подкисленного до рH 3,0-5,0 реакционной смеси после первичного удаления дрожжевого шлама до 45-75oС в течение 20-60 мин. Эта стадия, не изменяя состава целевых продуктов, содействует образованию сформированного в виде хорошо фильтрующегося осадка из остатков дрожжевого шлама, балластных белков и ионов тяжелых и многовалентных металлов. Хорошо известно, что выделенный из природных источников аденозин-5'-трифосфат может содержать значительное количество ионов тяжелых металлов, например, может специально оговариваться содержание ванадия [4]
Предлагаемый способ позволяет получать целевые вещества с низким содержанием ионов тяжелых и многовалентных металлов (железа не более 0,1% свинца не более 20 ррм, мышьяка не более 1,0 ррм), что соответствует требованиям отечественной и зарубежной фармакопеи.
В известных способах количества таких ионов в нуклеозид-5'-фосфатах существенно выше. При этом экспериментально было обнаружено, что очистка растворов с помощью сульфокатионитов в H+ форме в условиях способа-прототипа не давало необходимого по фармакопее уровня концентрации ионов тяжелых и многовалентных металлов. Только использование совокупности стадий термоосаждения в сочетании с последующей очисткой на сульфокатионитах или добавлении трилона Б в указанных концентрациях обеспечивало требуемую степень очистки от ионов металлов.
Анализ существующего уровня науки и техники не позволил выявить информацию о таких технологиях в области получения рибонуклеозид-5'-фосфатов, которые были бы основаны на использовании стадии термоосаждения. Не было также ранее известно, что термоосаждение одновременно повышает эффективность как удаления остатков дрожжевого шламма, балластных веществ, так и ионов тяжелых и многовалентных металлов.
Найденная новая зависимость "признак эффект" еще раз подтверждает соответствие предлагаемого решения требованию "изобретательский уровень".
Для лучшего понимания сущности предлагаемого изобретения, а также для подтверждения соответствия требованию "промышленная применимость" приводим примеры его конкретной реализации, которыми однако не исчерпывается сущность изобретения.
Пример 1. Получение аденозин-5'-трифосфата. 100 г аденозина растворяют в 3600 мл воды. К раствору добавляют 430 г Na2HPO4 • 12H2PO4, 100 г KH2PO4, 7 г хлористого калия, 200 г сахарозы, 11 г шестиводного хлористого магния, 7,2 л пивных дрожжей, 150 мл толуола. Устанавливают рH 7,0 и температуру 37oС. Ход реакции контролируют с помощью экспресс-тонкослойной хроматографии, фиксируя момент полного исчерпания аденозина достижения максимального количества аденозин-5'-трифосфата.
Хроматография проводится в системе 1,4-диоксан:изопропанол: 5 М водный раствор аммиака: 1 М ацетат аммония в соотношении соответственно 300 18 49 3. Для анализа применяют тонкослойные пластины из силикагеля на алюминиевой фольге. Время анализа 10-12 мин.
Реакцию прекращают добавлением ледяной уксусной кислоты с установлением рH 4,5. Время реакции 2 ч. Смесь охлаждают до +8o, с помощью отстойной центрифуги отделяют дрожжевой шлам. В фугате устанавливают рH 4,3 и нагревают смесь при 65oС в течение 300 мин. Раствор охлаждают до 20oС, выпавший осадок отделяют центрифугированием. Прозрачный раствор (10 л) разбавляют до общего объема 50 л и подают на колонку (диаметр 6 см, высота 500 см, объем смолы 1500 мл) с анионитом АРА-5П в хлор-форме гранул 250-500 мкм. После сорбции колонку промывают 10 л дистиллированной воды. Элюцию аденозин-5'-моно- и -дифосфата проводят раствором 0,02 н. хлористого натрия в 0,01 H соляной кислоте. Аденозин-5'-трифосфат элюируют 0,5 н. хлористым натрием в 0,02 н. соляной кислоте. Аденозин-5'-трифосфат осаждают, приливая элюат в 10-ти кратное по объему количество этилового спирта, охлажденного до 10oС.
Осадок отфильтровывают, растворяют в 1500 мл воды и пропускают через колонку со 100 мл сульфокатионита КУ-2-8 в H+ форме (диаметр колонки 3 см, высота 14,5 см). Колонку промывают 500 мл воды, промываны е воды объединяют с основной частью раствора. Целевой продукт получают осаждением раствора в 10-ти кратное количество по объему этилового спирта, охлажденного до -12oС. Осадок кристаллизуется в течение 1,5 ч. Затем его отделяют и сушат в вакууме при 70oС.
Выход аденозин-5'-трифосфата 150 г или 78% содержание основного вещества 99% Общее время реакции и выделения 35 ч.
Содержание тяжелых металлов определялось по принятым в фармакопее методикам и полностью удовлетворяет требованиям фармакопеи.
Содержание ионов тяжелых и многовалентных металлов в продукте, полученном без стадии термоосаждения, существенно выше, чем этого требуют нормы.
Катионы многовалентных металлов определялись с помощью так называемой оксалатной пробы.
Пример 2. Получение аденозин-5'-дифосфата. 100 г аденозина растворяют в 3600 мл воды. К раствору добавляют 430 г Na2HPO4 • 12H2O, 100 г KH2PO4, 7 г хлористого калия, 11 г шестиводного хлористого магния, 200 г сахарозы, 7,2 л пекарских дрожжей и 150 мл толуола, устанавливают рH 6,2 и температуру 37oС. За ходом реакции следят с помощью экспресс-тонкослойной хроматографии в условиях, описанных в примере 1. Фиксируют моменты полного исчерпания аденозина и достижения максимальной концентрации аденозин-5'-дифосфата в реакционной смеси. Реакцию прекращают добавлением ледяной уксусной кислоты до рH 4,8. Время фосфорилирования 3 ч 15 мин. Смесь охлаждают до +10oС и отделяют дрожжевой шлам с помощью центрифугирования. Недосадочную жидкость подкисляют до рH 3,7 и выдерживают 20 мин при 45oС. Выпавший осадок отделяют. Прозрачный раствор (10 л) разбавляют до общего объема 50 л и подают на хроматографическую колонку (диаметр 6 см, высота 50 см), заполненную 1500 мл анионита АРА-5П в хлор-форме. Элюцию ведут 0,02 н. хлористым натрием в 0,01 н. соляной кислоте (объем элюента 6000 мл). Целевой продукт выделяют осаждением, приливая элюент в 10-ти кратное по объему количество ацетона. Выход аденозин-5'-дифосфата 130 г (71%), содержание основного вещества 85% Продукт растворяют в 1500 мл воды и пропускают через колонку со 100 мл сульфокатионита КУ-2-8 в H+-форме (диаметр колонки 3 см, высота 14,5 см). Сорбент промывают 500 мл воды, промывные воды соединяют с основной частью раствора. Аденозин-5'-дифосфат осаждают, приливая соединенный раствор в 10-ти кратное количество по объему ацетона. Выход целевого продукта 110 г. (65%) с чистотой 95% Содержание ионов тяжелых и многовалентных металлов соответствует требованиям фармакопеи.
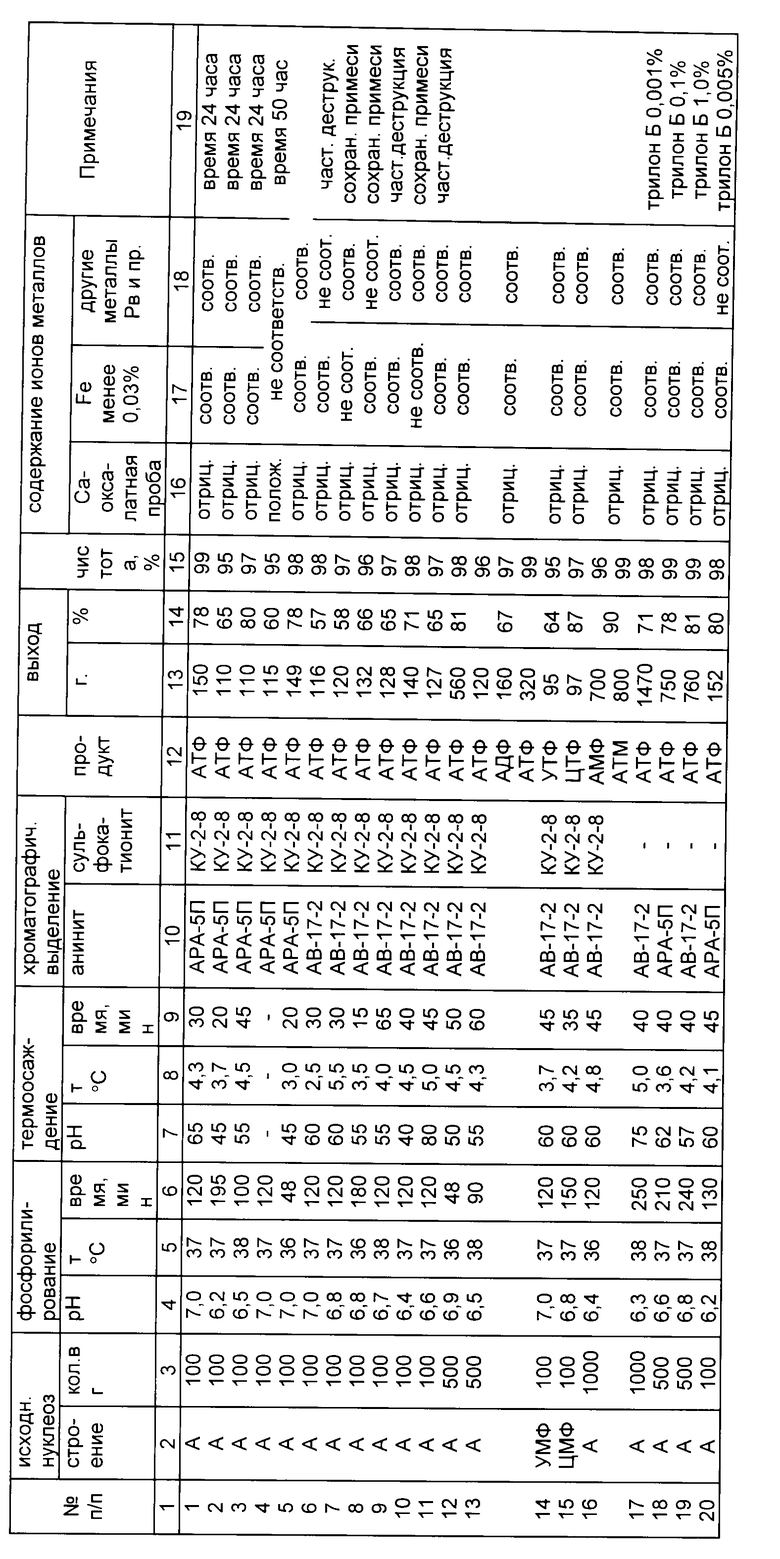
Примеры 3-20 проведены в условиях примеров 1 и 2, все данные приведены в таблице. При этом примеры 14 и 15 реализованы с использованием уридин-5'-монофосфата и цитидин-5'-монофосфата соответственно в качестве исходных веществ для фосфорилирования из-за крайне низкой растворимости уридина и цитидина в водных растворах.
Примеры 17-20 проводились в условиях примера 1, однако стадия деионизации реализовалась путем замены очистки с помощью сульфокатионитов растворением в деионизуемом растворе трилона Б с последующим осаждением в избыток ацетона или этанола, охлажденного до -8 -12oС. В примерах, изложенных в таблице, не указывается каким растворителем пользуются при осаждении, потому что ацетон и этанол, охлажденный до -8 -12oСоказались эквивалентными и обеспечивали одинаковый эффект.
В таблице использованы следующие сокращения: А-аденозин, У- уридин, Ц-цитидин, МФ -5'-монофосфат, ДФ -5'-дифосфат, ТФ -5'-трифосфат.
Анализ данных таблицы позволяет утверждать, что все поставленные задачи решены изобретением. Регулируя время реакции прямым методом удалось получить любое производное с высокими выходами, высокой чистотой и соответствующее требованиям фармакопеи по содержанию ионов металлов.
Примеры также подтверждают, что практически невозможно определить зависимости между условиями реакции фосфорилирования и временем ее протекания, поскольку использовались различные партии как пивных, так и пекарских дрожжей, обладающие различной биологической активностью. Поэтому особенно нужно регулирование времени процесса прямым методом на основе экспресс-тонкослойной хроматографии.
В таблице практически подтверждены предлагаемые предельные значения интервалов процессов: температур, рH, времени. Выход за предлагаемые пределы приводит к ухудшению достигаемого эффекта.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения аденозин-5 -трифосфата | 1978 |
|
SU722920A1 |
| Способ получения аденозин-5-трифосфата | 1979 |
|
SU941384A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДЕНОЗИН МОНОФОСФАТА | 1992 |
|
RU2094437C1 |
| СПОСОБ ВЫДЕЛЕНИЯ БЕТУЛИНОЛА | 2002 |
|
RU2206572C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРНЫХ ЭФИРОВ ТИАМИНА | 1992 |
|
RU2041229C1 |
| АДАПТОГЕННОЕ СРЕДСТВО | 1998 |
|
RU2139082C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ 5'-ТРИФОСФАТОВ ДЕЗОКСИРИБО- И РИБООЛИГОНУКЛЕОТИДОВ | 2006 |
|
RU2326888C1 |
| Способ получения оксида скандия | 2015 |
|
RU2608033C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2003 |
|
RU2251407C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2013 |
|
RU2545337C2 |
Изобретение относится к получению биологически активных веществ, конкретно рибонуклеозид-5'-фосфатов, находящих использование в медицине, биохимии, биологии. 5'-моно-, ди- и трисфосфаты аденозина, уридина и цитидина получают путем биофосфорилирования рибонуклеозидов ферментной системой дрожжей в присутствии неорганических фосфатов, источников ионов калия и магния, углеводов и толуола. Реакцию проводят при прямом контроле за количественными соотношениями компонентов реакции. Реакцию завершают подкислением до рH 4,5-4,8, отделяют дрожжевой шлам. Затем проводят термообработку при рH 3,0-5,0 при 45-75oС в течение 20-60 мин и дополнительно отделяют образовавшийся осадок. Из фильтрата с помощью сильноосновного анионита выделяют продукты реакции фракционной элюцией: моно - и дифосфаты элюируют раствором 0,02 H хлористого натрия в 0,01 н соляной кислоте, трифосфаты элюируют раствором 0,5 н хлористого натрия в 0,02 H соляной кислоте. Из элюента выделяют продукты реакции осаждением в избыток смешивающегося с водой органического растворителя из ряда: ацетон и этанол, охлажденный до -8 - -12oС. Затем водные растворы выделенных продуктов реакции деионизируют либо обработкой раствора сульфокатионитом в H+ -форме, либо добавляя трилон Б в концентрации 0,001-1,0%. Целевое вещество выделяют повторным высаживанием вещества из деионизованного раствора в избыток смешивающегося с водой органического растворителя. 3 з. п. ф-лы, 1 табл.
4. Способ по пп.1 3, отличающийся тем, что выделение целевых продуктов проводят высаживанием из элюента после деионизации в смешивающийся с водой органический растворитель, выбранный из ряда, включающего ацетон, этанол, охлажденный до -8 -12oС.
Авторы
Даты
1997-09-27—Публикация
1994-09-08—Подача