Изобретение относится к медицинской микробиологии, в частности, к вакцинопрофилактике коклюша, способам определения токсичности коклюшных препаратов.
Несовершенство применяемых коклюшных вакцинных препаратов, в частности, высокая реактогенность корпускулярной коклюшной вакцины (В.П.Брагинская, А. Ф. Соколова. Активная иммунизация детей. М. Медицина, 1990, с.208) и недостаточная эпидемиологическая эффективность предложенных в последнее время бесклеточных вакцинных препаратов делают актуальной задачу создания вакцинных коклюшных препаратов с максимально сниженным повреждающим эффектов при сохранении выраженных протективных свойств (Р.М.Волгарева с соавт. Цитотоксический анализ действия бесклеточных коклюшных вакцин в костном мозге бестимусных мышей и мышей гетерозигот (Журн. микробиол. эпидемиол. и иммунодиол. 1992, N 11-12, с.60 61). Создание ареактогенных коклюшных препаратов может быть связано с применением бесклеточных препаратов, содержащих токсические и антигенные субстанции коклюшных микробов, детоксицированные химическими и генноинженерными методами.
В связи с этим большой интерес представляет совершенствование методов оценки их остаточной токсичности.
Проведенными исследованиями по научной и патентной литературе выявлен ряд способов оценки повреждающего действия бактериальных препаратов. Так, в инструкции института ИЭМ АМН СССР им. И.Ф.Гамалеи, 1972, описан "Способ оценки токсичности коклюшных вакцин по изменению веса мышей". Использование вышеописанной методики не дает полной информации о характере повреждающего действия бактериальных препаратов на макроорганизм, отличается длительным сроком исследования и большим количеством дорогостоящих экспериментальных животных.
Более современными являются методы оценки остаточной токсичности коклюшных препаратов на уровне отдельных клеток организма, в частности, тимоцитов (Нуридинова Н.Р. с соавт. /Журн. микробиол. эпидемиол. и иммунобиол. 1990, N 7, с.50 55), а также клеток яичника китайского хомячка, предложенный Хардиной А.А. с соавт. и опубликованный в Журн. Микробиол. эпидемиол. и иммунобиол. 1991, N 8, с. 21 23. Однако и эти методы достаточно трудоемки, требуют длительных сроков исследования и используют в качестве источника клеток экспериментальных животных, которых трудно стандартизировать по возрасту, полу, биологической активности. Эти методы недостаточно информативны относительно токсичности коклюшных препаратов для человека, так как не всегда допустима экстраполяция на человека данных, используемых на клетках экспериментальных животных.
Наиболее близким по технический сущности является "Способ оценки токсичности коклюшных вакцин" (патент N 1321227,1992), взятый за прототип. Он осуществляется следующим образом. Мышам внутрибрюшинно вводятся эритроциты барана в доза 1•103 кл/мл, через 4 5 сут. животных забивают, извлекают селезенки, готовят из них взвеси клеток, к которым добавляют коклюшную вакцину в доза 1•108 5•108 м.т. и объеме 0,5 мл; 30 40 мин выдерживают при комнатной температура, затем определяют число АОК и по их снижения от 30 до 100% по сравнению с контролем судят о токсичности испытуемых препаратов.
Этот способ удобен, однако обладает рядом недостатков: он трудоемок, требует длительного срока для получения результатов (6 7 суток) и использует в качестве биологической системы лабораторных животных, которых трудно стандартизировать по возрасту, полу, биологической активности, он недостаточно информативен относительно токсичности коклюшных препаратов для человека, так как не всегда допустима экстраполяция на человека данных, полученных на экспериментальных животных.
Целью настоящего изобретения является повышение информативности и достоверности, а также ускорение и упрощение способа оценки токсичности коклюшных препаратов.
Поставленная цель достигается применением в качестве биологической модели для оценки токсичности коклюшных препаратов перевиваемой моноцитоподобной линии клеток человека И 937, поддерживаемой в музее клеточных культур института.
Подробное описание способа и примеры его осуществления.
Разные дозы коклюшных препаратов (0,1 10,0 оптических единиц мутности (МОЕ) для корпускулярных препаратов и 1,0 100,0 мкг по белку для отдельных антигенов коклюшного микроба и их комплексов) растворяют в 0,1 мл среды 19 и добавляют к 1 мл клеток моноцитоподобной перевиваемой линии клеток человека И 937 (4• 106 кл/мл), предварительно выращенных в течение суток при 37oC. Полученную взвесь помещают пенциллиновые флаконы с покровными стеклами и 1 мл среды 199, содержащей 20% сыворотки крови рогатого скота. После 5 7 ч инкубации при 27oC покровные стекла извлекают из пенициллиновых флаконов, трижды промывают в емкостях с раствором Хэнкса, фиксируют в смеси Никифорова, и окрашивают по Романовскому-Гимзе, и просматривают окрашенные мазки в световом микроскопе. В мазках исследуют морфологию 300 клеток и определяют процент поврежденных клеток (ПК,). О повреждении клеток судят по вакуолизации цитоплазмы, нарушению цитоплазматической мембраны, округлению и пикнозу ядра, кариорексису и изменению окраски. Повышение процента поврежденных клеток в опытных образцах по сравнению с контролем более чем на 10% свидетельствует об остаточной токсичности исследуемых препаратов. Чем выше процент поврежденных клеток, тем выше остаточная токсичность коклюшных препаратов.
Пример 1.
Корпускулярную коклюшную вакцину (ККВ) в дозах 0,1; 1,0 и 10,0 МОЕ и объеме 0,1 мл добавляли к 1,0 мл клеток перевиваемой моноцитоподобной линии И 937 (4•106 кл/мл) и культивировали на покровных стеклах в пенициллиновых флаконах, содержащих 1 мл среды 199 с 20% сыворотки крови крупного рогатого скота. Через 5 ч инкубации при 37o C покровные стекла извлекали из флаконов и промывали в растворе Хэнкса, фиксировали в смеси Никифорова, окрашивали по Романовскому-Гимзе, просматривали окрашенные мазки в световом микроскопе и определяли процент поврежденных клеток (ПК,). О повреждении клеток судили по вакуолизации цитоплазмы, нарушению цитоплазматической мембраны, округлению и пикнозу ядра, кариорексису изменению окраски.
Параллельно определяли токсические свойства ККВ в общепринятом тесте лейкоцитоз-стимулирующий активности (ЛСА) препаратов согласно "Инструкции по отбору, проверке и хранению производственных штаммов коклюшных бактерий" (1987): мышам массой 14 16 г вводили однократно внутрибрюшинно ККВ в дозах 0,1; 1,0 и 10,0 МОЕ. Контрольных животным вводили 0,5 мл апирогенного 0,15 М раствора хлорида натрия (pH 7,0 ±0,2). Через 72 ч у опытных и контрольных животных брали кровь из ретроорбитального синуса, определяли количество лейкоцитов в 1 мм3 крови в камере Горяева и рассчитывали индекс ЛСА как отношение количества лейкоцитов опытных мышей в числу лейкоцитов животных, получивших ОСО-3. Кроме того, определяли количество единиц ЛСА. За 1 ЕД ЛСА принимали увеличение числа лейкоцитов в 1 мм3 крови на 104 по сравнению с контролем.
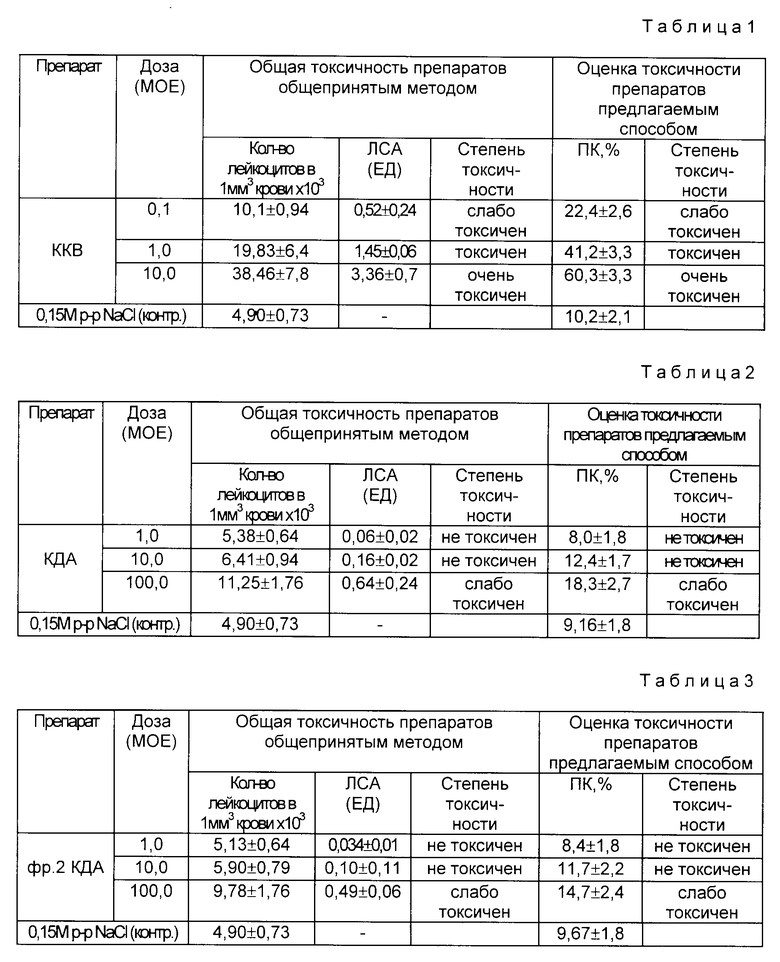
Полученные данные представлены в табл.1
Из таблю.1 видно, что существует строгая корреляция между данными, полученными при оценке токсичности ККВ общепринятым методом по ЛСА (ЕД), и данными, полученными при изучении цитотоксического эффекта этого препарата на клетки И 937. Коэффициент корреляции рангов Спирмена приближается к 1,0 (0,973). ККВ обладает токсичностью особенно резко выраженной в дозах 1,0 - 10,0 МОЕ.
Пример 2.
Условия опыта те же, что и в примере 1. Изменен только срок инкубации клеток. Он составляет 6 ч. В качестве коклюшного препарата взят коклюшный диализатный антиген (КАД) в дозах 1,0; 10,0 и 100,0 мкг по белку. Полученные данные представлены в табл. 2.
Из табл.2 видно, что существует строгая корреляция между данными, полученными при оценке токсичности КДА общепринятым методом по ЛСА (ЕД), и данными, полученными при изучении цитотоксического эффекта КДА на клетки B 937. Коэффициент корреляции рангов Спирмена приближается к 1,0 (0,973). КДА не токсичен в дозах 1 10 мкг по белку и обладает слабо выраженной токсичностью в дозе 100 мкг.
Пример 3.
Условия опыта те же, что в примере 1. Изменен только срок инкубации клеток с коклюшными препаратами. Он составляет 7 ч. В качестве коклюшного препарата взята фракция 2 КДА в дозах 1,0; 10,0 и 100,0 мкг по белку. Полученные данные представлены в табл.3.
Из табл. 3 видно, что существует строгая корреляция между данными, полученными при оценке токсичности фр. 2 КДА общепринятым методом по ЛСА (ЕД), и данным, полученным при изучении цитотоксического эффекта этого препарата на клетки И 937. Коэффициент корреляции Спирмена приближается к 1,0 (0,973). Фракция 2 КДА нетоксична во всех изученных дозах.
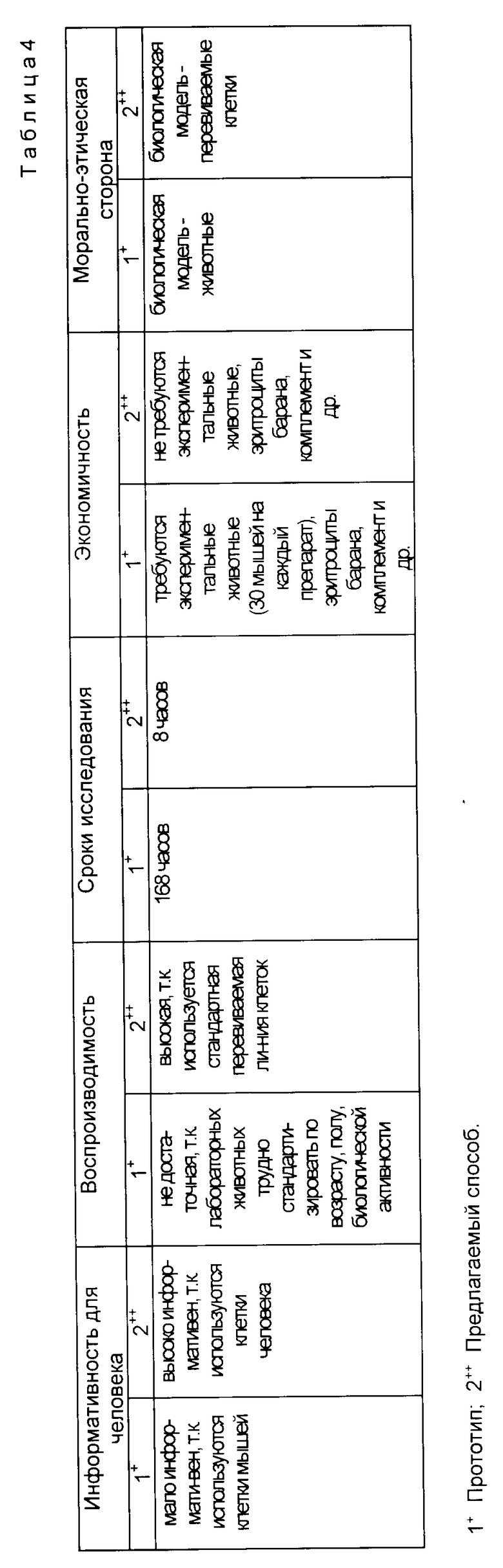
Таким образом, приведенные примеры свидетельствуют, что предлагаемый способ может быть использован для оценки остаточной токсичности коклюшных препаратов. Кроме того, он имеет преимущество перед прототипом (табл.4). Преимущество предлагаемого способа по сравнению с базовым объектом (прототипа) является:
1) большая информативность относительно токсичности коклюшных препаратов для человека, так как используются клетки человека, а не экспериментальных животных;
2) лучшая воспроизводимость, так как в качестве биологической модели используется стандартная перевиваемая in vitro линия клеток, а не лабораторные животные, которых трудно стандартизировать по возрасту, полу, биологической активности;
3) ускорение сроков исследования в 20 раз (с 7 суток до 8 ч);
4) упрощение за счет сокращения числа методических приемов;
5) удешевление способа, так как не требуются экспериментальные животные, эритроциты барана, комплемент и полистироловые планшеты.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ТОКСИЧНОСТИ КОКЛЮШНЫХ ВАКЦИН | 2001 |
|
RU2227293C2 |
| СПОСОБ ОЦЕНКИ ТОКСИЧНОСТИ КОКЛЮШНЫХ ВАКЦИН | 1999 |
|
RU2174229C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕКТИВНОГО КОКЛЮШНОГО АНТИГЕНА | 1999 |
|
RU2148412C1 |
| АТТЕНУИРОВАННЫЕ БАКТЕРИИ BORDETELLA PERTUSSIS, ВАКЦИНА ПРОТИВ ВОЗБУДИТЕЛЯ КОКЛЮША | 2010 |
|
RU2455024C1 |
| СПОСОБ ОЦЕНКИ ИММУНОГЕННОСТИ КОКЛЮШНЫХ ВАКЦИН | 2003 |
|
RU2231793C1 |
| Способ лиофильного высушивания аттенуированных бактерий B. pertussis, аттенуированная бактерия B. pertussis, штамм аттенуированных бактерий B. Pertussis, вакцина, лиофилизированный вакцинный препарат | 2017 |
|
RU2709657C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЕЛПЕРНЫХ ФРАКЦИЙ НЕЙТРОФИЛОКИНОВ, СИНТЕЗИРОВАННЫХ НЕЙТРОФИЛАМИ ПЕРИТОНЕАЛЬНОГО ЭКССУДАТА ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ ПОД ВЛИЯНИЕМ КЛЕТОК ВАКЦИННОГО ШТАММА ЧУМНОГО МИКРОБА | 2007 |
|
RU2341561C1 |
| Способ иммунизации бактериальными препаратами,содержащими эндотоксин | 1982 |
|
SU1306582A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВТОРИЧНОГО ИММУНОДЕФИЦИТНОГО СОСТОЯНИЯ ПО Т-КЛЕТОЧНОМУ ТИПУ | 1992 |
|
RU2050020C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕСКЛЕТОЧНОЙ ВАКЦИНЫ ДЛЯ ИММУНОПРОФИЛАКТИКИ КОКЛЮША | 2006 |
|
RU2332231C2 |
Изобретение относится к медицинской микробиологии и может быть использовано для проверки токсических свойств коклюшных вакцинных препаратов, выпускаемых в серийное производство. Цель изобретения - повышение информативности и достоверности, а также ускорение и упрощение способа оценки токсичности коклюшных препаратов. Способ осуществляется следующим образом. К 1,0 мл взвеси перевиваемой моноцитоподобной линии клеток человека И 937 (4•106 кл/мл) добавляют коклюшные препараты в разных дозировках (0,1 - 10,0 МОЕ для корпускулярных препаратов и 1,0 - 100,0 мкг по белку для отдельных антигенов коклюшного микроба или их комплексов) и через 5 - 7 ч совместного культивирования в термостате при 37oC на покровных стеклах в пенициллиновых флаконах с 1 мл среды 199, содержащей 20% сыворотки крупного рогатого скота, покровные стекла извлекают из пенициллиновых флаконов, промывают в растворе Хэнкса, фиксируют в смеси Никифорова, окрашивают по Романовскому-Гимзе, просматривают 300 клеток в световом микроскопе, определяют процент поврежденных клеток и по увеличению процента поврежденных клеток, по сравнению с контролем, оценивают токсичность коклюшных препаратов: 10 - 20% - слабо токсичен; 20 - 40% - токсичен; более 40% - очень токсичен. Предлагаемый способ более информативен, экономичен, сокращает сроки исследования токсичности коклюшных препаратов в 20 раз, не требует лабораторных животных, отличается высокой чувствительностью и хорошей воспроизводимостью. 4 табл.
Способ оценки токсичности вакцинных коклюшных препаратов путем их введения в биологическую модель, отличающийся тем, что в качестве биологической модели используют перевиваемую моноцитоподобную линию клеток человека И 937, к 1 мл взвеси которой (4•106 кл/мл) добавляют коклюшные препараты в разных дозировках (0,1 10,0) МОE для корпускулярных препаратов и 1 100 мкг по белку для отдельных антигенов коклюшного микроба или их комплексов и через 5 7 ч совместного культивирования в термостате при 37oС на покровных стеклах в пенициллиновых флаконах с 1 мл среды 199, содержащей 20% сыворотки крупного рогатого скота, покровные стекла извлекают из пенициллиновых флаконов, промывают в растворе Хэнкса, фиксируют в смеси Никифорова, окрашивают по Романовскому Гимзе, просматривают 300 клеток в световом микроскопе, определяют процент поврежденных клеток и по увеличению процента поврежденных клеток по сравнению с контролем оценивают токсичность коклюшных вакцинных препаратов: 10 20% слаботоксичны, 20 40% токсичны, более 40% очень токсичны.
| Микробиология, эпидемиология и иммунобиология | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
Авторы
Даты
1997-10-10—Публикация
1994-08-05—Подача