Изобретение относится к области биологии и медицины и может быть использовано для индикации клинико-цитогенетических эффектов неконтролируемого хронического облучения населения, проживающего в районах, загрязненных радионуклидами.
Известны аналогичные способы исследования мутагенной активности метаболитов, содержащихся в плазме крови. Так, мутагенную активность метаболитов в плазме крови крыс Sprague Dawley обработанных циклофосфамидом в дозах 2,5, 5,0, 10,0, 20,0 мг/кг веса, оценивали по частоте CXO в лимфоцитах человека и крыс. Показано, что увеличение частоты CXO в лимфоцитах человека и крыс было сравнимо по дозам и амплитуде и носило дозово-зависимый характер. Известно, что через 4 24 ч после γ- облучения в дозе 8 Гр биологическую активность (токсичность) плазмы крови крыс-самцов линии Вистар определяли по выживаемости бактерий E. coli и по образованию мутаций у бактериофага T4Br+. Плазму крови контрольных или γ- облученных животных, разбавленную в 2 раза от исходной концентрации, добавляли к бактериофагу T4Br+ и к водной суспензии бактерий E. coli. Подсчет выживших колоний E.coli проводили через 24 ч, а r -мутантов фагочастиц через 18 ч инкубации. В результате проведенных исследований было высказано предположение об образовании аддуктов альбумина с хиноидными радиотоксинами и возможной роли этих соединений в развитии радиационного поражения критических тканей организма.
Прототипом данного изобретения может быть способ, который состоит в том, что исследовали частоту спонтанных и индуцированных блеомицином аберраций хромосом в культуре лимфоцитов, а также частоту микроядер в культивированных лимфоцитах периферической крови и некультивированных клетках слизистой рта и волосяных луковиц у больных атаксией-телеангиэктазией (АТ) и в контроле. Микроядерный тест в лимфоцитах выполняли методом блокирования цитокинеза. Получен различный цитогенетический ответ на культивируемых и некультивируемых клетках больных АТ: частота спонтанных и индуцированных аберраций хромосом и микроядер в культурах лимфоцитов была в 3 раза выше у больных АТ по сравнению с контролем, тогда как микроядерный тест в клетках слизистой рта и волосяных луковиц больных АТ показал норму. С целью выяснения вопроса о том, связаны ли указанные различия с культуральными условиями, в культуру добавляли сыворотку крови больных АТ. Авторы не смогли обнаружить какие-либо факторы в плазме больных АТ, которые увеличивали бы аберрации хромосом у нормальных людей или гетерозиготных носителей.
Однако данный способ не может быть использован в таком виде, так как он имеет ряд существенных недостатков:
1) в качестве тест-системы используется синхронизированная культура лимфоцитов, которая затрудняет экстраполяцию полученных данных на гетерогенную популяцию клеток целостного организма, находящихся на различных стадиях клеточного цикла и имеющих различную радиочувствительность;
2) для получения препаратов хромосом лимфоцитов периферической крови требуется обработка культур дефицитными реактивами (митогенами и препаратами, вызывающими цитокинетический блок делящихся клеток) производства зарубежных фирм, что делает этот способ экономически затруднительным;
3) используемый способ не связан с выявлением действия фактора радиационного происхождения на выход цитогенетических повреждений в организме человека.
Цель данного изобретения состоит в индикации клинико-цитогенетических эффектов неконтролируемого хронического облучения населения, проживающего в районах, загрязненных радионуклидами для проведения профилактических и лечебных мероприятий.
Эта цель достигается тем, что для раннего обнаружения признаков радиационной интоксикации введено:
1) использование тест-системы на основе диплоидной культуры эмбриональных кожно-мышечных клеток человека;
2) исследование на мутагенную активность факторов плазмы крова жителей загрязненных радионуклидами территорий Беларуси.
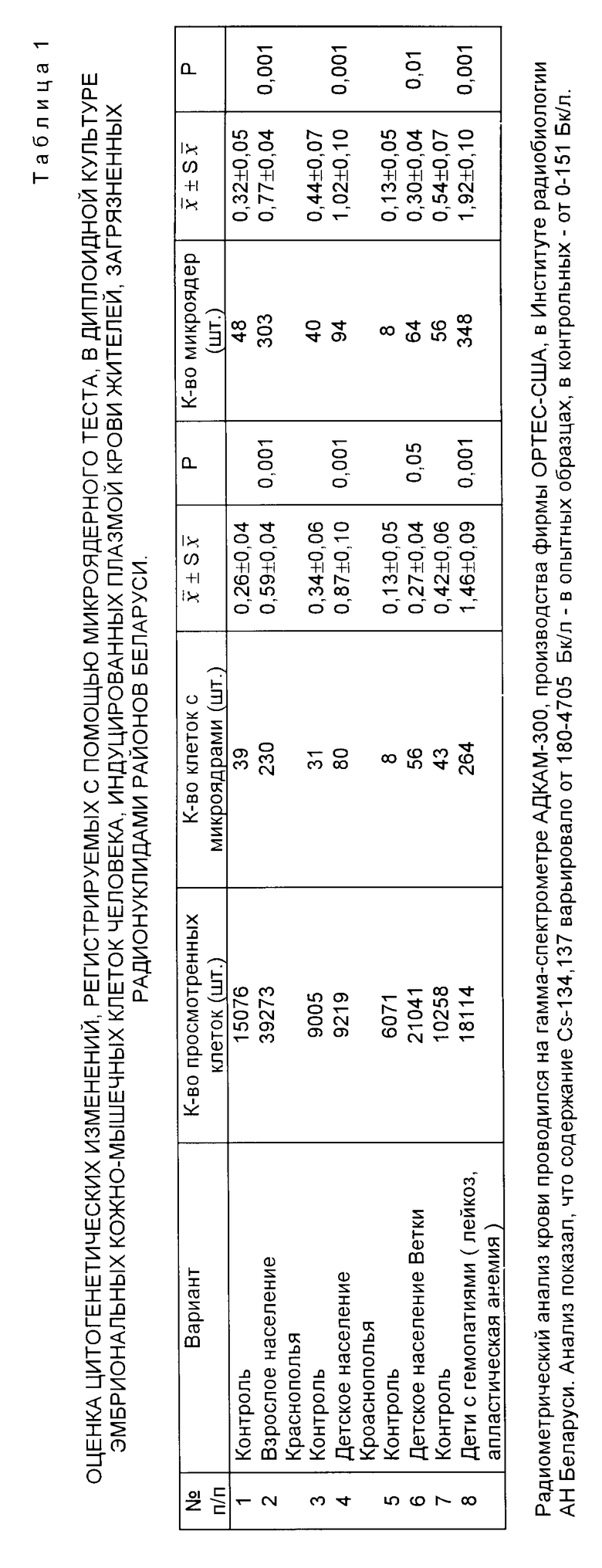
В таблице приведена оценка цитогенетических изменений, регистрируемых с помощью микроядерного теста, в диплоидной культуре эмбриональных кожно-мышечных клеток человека, индуцированных плазмой крови жителей, загрязненных радионуклидами районов Беларуси.
Способ реализован следующим образом.
В качестве тест-системы для изучения генотоксичности плазмы крови была выбрана диплоидная культура эмбриональных кожно-мышечных клеток человека 8 - 12 пассажей.
Диплоидная культура эмбриональных кожно-мышечных клеток человека это полуперевиваемая культура, сохраняющая нормальный кариотип (2 п 46), ограниченный рост и период размножения, а также другие свойства исходных клеток организма, что дает возможность экстраполировать полученные результаты на организм человека.
Клетки выращивали в модифицированных флаконах Карреля на предметных стеклах в питательной среде, содержащей: 5%-ный раствор гемогидролизата - продукта ферментативного гидролиза сгустков крови крупного рогатого скота или человека (отходы производства гаммаглобулина), который представляет собой концентрат 20 аминокислот, солевой раствор Хенкса, 8 витаминов. Кроме того, в ростовую среду добавляют 10% по объему бычьей сыворотки и антибиотики в виде пенициллина и стрептомицина.
Флаконы после добавления 15 мл клеточной суспензии в каждый (концентрация клеток в питательной среде составляла 105 кл/мл) термостатировали при температуре 57oC. При указанных условиях культивирования логарифмическую стадию роста отмечали на 2-е сутки после пересева на свежую питательную среду. Именно в этот период (на вторые сутки роста клеток) во флаконы с клеточной суспензией добавляли по 0,5 мл плазмы крови обследуемого, полученной путем отстаивания периферической крови в течение 60 мин при комнатной температуре. Кровь обследуемого получали методом венопункции или из пальца и в стерильных флаконах с гепарином доставляли к месту проведения эксперимента в стационарный бокс, работу в котором проводили с соблюдением всех правил асептики. Контролем служила параллельная культура кожно-мышечных клеток человека того же пассажа и концентрации, что и опытная культура с добавлением 0,5 мл плазмы крови доноров клинически здоровых людей в возрасте до 30 лет, полученной на Республиканской станции переливания крови г. Минска. Культивирование эмбриональных клеток человека в присутствии плазмы крови доноров и обследуемых проводили в течение 24 ч, после чего опытные и контрольные стекла, на которых имелся достаточно плотный монослой клеток, для фиксации помещали в свежеприготовленную охлажденную смесь этилового спирта и ледяной уксусной кислоты в соотношении 3:1. Затем препараты окрашивали 3 - 5%-ным водным раствором Гимза и промывали проточной водой.
В качестве теста при изучении генотоксичности плазмы крови был выбран микроядерный тест, предложенный в 1973 году. Показано, что этот тест является достаточно чувствительным, более простым и экономически выгодным по сравнению с общепризнанным цитогенетическим методом исследования аберраций хромосом в метафазе митоза. Применение микроядерного теста дает возможность проведения автоматизации исследований.
В результате изучения генотоксичности эндогенных факторов плазмы крови обследовано 29 человек. Проведен популяционный (7 детей Ветковского р-на Гомельской области, 3 детей и 15 взрослых Краснопольского р-на Гомельской области с уровнем загрязнения по 90Sr (0,8 2,0 Ки/км2) и по 137Cs (20 100 Ки/км2), а также целевой цитогенетический мониторинг, основанный на клиническом диагнозе гемопатий (апластическая анемия, лейкоз), у 6 детей, проживающих в условиях длительного неконтролируемого облучения и находившихся с целью обследования или лечения в Детском гематологическом центре г.Минска.
Данные таблицы свидетельствуют о достоверном увеличении частоты клеток с микроядрами во всех обследованных группах: дети и взрослые Краснопольского р-на, дети Ветковского р-на, а также дети с гемопатиями (P <0,001, 0,001, 0,05, 0,001 соответственно). У всех обследованных также отмечено достоверное увеличение количества микроядер на 100 проанализированных клеток (P < 0,001, 0,001, 0,01, 0,001 соответственно). Выход микроядер в свободной выборке (население Гомельской и Могилевской областей) варьирует от 0,30 до 1,02 на 100 клеток, превышая в 2 2,5 раза контрольный уровень. Максимальный цитогенетический эффект (1,92 на 100 клеток) отмечен в группе детей с гемопатиями, проживающих на загрязненных радионуклидами территориях Беларуси. При сравнении выхода микроядер в группах детей, обследованных по медицинским показаниям, и в свободной выборке (население Гомельской и Могилевской областей) обнаружен параллелизм цитогенетического эффекта плазмы крови детей и взрослых из зоны радиоактивного загрязнения и детей с гемопатиями, находящихся на лечении в Детском гематологическом центре г.Минска.
Таким образом, полученные данные позволяют сделать заключение о том, что
Обнаруженное достоверное повышение уровня цитогенетических нарушений в тест, культуре эмбриональных кожно-мышечных клеток человека, индуцированных эндогенными факторами плазмы крови доноров, принадлежащих к различным группам населения Беларуси, подвергшегося длительному неконтролируемому облучению, является косвенным свидетельством развития процессов радиационной интоксикации в организме обследованных.
Предлагаемая тест, система на основе диплоидной культуры эмбриональных кожно-мышечных клеток человека является удобным объектом для исследования генетической активности плазмы крови, что открывает возможность ранней диагностики гемопатий (основанной на процессах радиационной интоксикации) и проведения профилактических и лечебных мероприятий.
Использование данного способа позволит:
1.Сократить расходы на проведение цитогенетического обследования.
2. Сократить время проведения цитогенетического обследования,
3. Ускорить выявление цитогенетического эффекта хронического действия внутреннего и внешнего облучения на соматические клетки людей, проживающих в зоне радиоактивного загрязнения.
4. Проводить профилактику с целью выявления радиационной интоксикации.
5. Раннее прогнозирование и выявление гемопатий у населения, проживающего в условиях длительного неконтролируемого облучения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИНДИКАЦИИ НАСЛЕДСТВЕННОГО КЛЕТОЧНО-ЛЕТАЛЬНОГО ЭФФЕКТА НЕКОНТРОЛИРУЕМОГО ХРОНИЧЕСКОГО ОБЛУЧЕНИЯ IN VIVO ЛИМФОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ДЕТЕЙ ИЗ ЗАГРЯЗНЕННЫХ РАДИОНУКЛИДАМИ РАЙОНОВ | 1996 |
|
RU2126539C1 |
| СПОСОБ ЭКСПРЕСС-ВЫЯВЛЕНИЯ ОБЛУЧЕННЫХ ПАЦИЕНТОВ С ПОВЫШЕННЫМИ ЧАСТОТАМИ ХРОМОСОМНЫХ АБЕРРАЦИЙ | 1997 |
|
RU2141658C1 |
| СПОСОБ БИОИНДИКАЦИИ РАДИАЦИОННОГО ВОЗДЕЙСТВИЯ НА ЩИТОВИДНУЮ ЖЕЛЕЗУ | 2009 |
|
RU2442161C2 |
| СПОСОБ ДИАГНОСТИКИ ВОЗДЕЙСТВИЯ МАЛЫХ ДОЗ РАДИАЦИИ НА ОРГАНИЗМ ЧЕЛОВЕКА | 1995 |
|
RU2089904C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕСТАБИЛЬНОСТИ ГЕНОМА У ДЕТЕЙ С ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ | 2005 |
|
RU2295130C1 |
| СПОСОБ АНАЛИЗА ПОПУЛЯЦИИ ФИБРОБЛАСТОВ ЧЕЛОВЕКА | 1990 |
|
RU2017818C1 |
| СПОСОБ ОЦЕНКИ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ ГЕНОМА ЧЕЛОВЕКА К ВОЗДЕЙСТВИЮ ПОВЫШЕННЫХ ДОЗ ИЗЛУЧЕНИЙ РАДОНА И ПРОДУКТОВ ЕГО РАСПАДА | 2012 |
|
RU2501015C1 |
| Способ биологической индикации внутреннего альфа-облучения | 2020 |
|
RU2735927C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИМУТАГЕННЫМ ДЕЙСТВИЕМ | 2004 |
|
RU2258528C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕСТАБИЛЬНОСТИ ГЕНОМА У ДЕТЕЙ, БОЛЬНЫХ ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ С ПЕРИВЕНТРИКУЛЯРНОЙ ЛЕЙКОМАЛЯЦИЕЙ | 2009 |
|
RU2413226C1 |
Изобретение относится к области биологии и медицины. С целью индикации клинико-цитогенетических эффектов неконтролируемого хронического облучения населения, проживающего в районах, загрязненных радионуклидами, проводили исследование выхода цитогенетических нарушений в тест-культуре эмбриональных кожно-мышечных клеток человек, индуцируемых эндогенными факторами плазмы крови доноров, что является косвенным свидетельством развития признаков радиационной интоксикации. 1 табл.
Способ определения интоксикации, вызванной неконтролируемым хроническим радиационным облучением человека, включающий стерильный забор крови из вены или пальца, приготовление и двухсуточное культивирование диплоидной культуры эмбриональных кожно-мышечных клеток человека 8 12 пассажей до получения монослоя клеток на предметных стеклах в модифицированных флаконах Карреля, фиксацию клеток смесью 96o-ного этилового спирта и ледяной уксусной кислоты в соотношении 3 1, окраску препаратов 3 5%-ным водным раствором Гимза, цитогенетический анализ по микроядерному тесту, отличающийся тем, что при обнаружении цитогенетических нарушений в тест-культуре эмбриональных кожно-мышечных клеток человека, индуцируемых плазмой крови доноров, и при содержании 2 5 микроядер на 1 микроядерную клетку определяют наличие интоксикации в результате хронического радиационного облучения.
| Hum | |||
| Genet | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
Авторы
Даты
1997-10-20—Публикация
1992-03-17—Подача