Изобретение относится к учебным приборам по физике, предназначенным для проведения лабораторных работ, и может быть использовано в вузах и средних школах в ходе изучения явления электролиза в курсе электричества.
Известен способ определения параметров электролиза, включающий измерение массы катода до и после пропускания через электролит электрического тока [1]
Недостаток способа низкая точность при малых массах катода.
Известен также способ определения параметров электролиза, при котором катод выполняют из материала, аналогичного осаждающемуся на нем, измеряют параметры катода до и после прохождения электрического тока через электролиты и вычисляют прирост массы катода.
Недостатком данного способа является ограниченная точность измерений при малых значениях массы катода.
Техническим результатом изобретения является повышение точности измерений при малых значениях массы катода.
Указанный технический результат достигается тем, что в известном способе определения параметров электролиза катод изготавливают в виде цилиндра, приводят его во вращательное движение относительно продольной оси и измеряют электрическое сопротивление катода до и после прохождения тока через электролит, при этом прирост массы вычисляют по формуле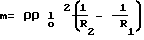 ,
,
где ρ плотность материала, из которого выполнен катод;
ro удельное сопротивление катода;
l длина катода;
R1 и R2 электрическое сопротивление катода соответственно до и после прохождения тока через электролит.
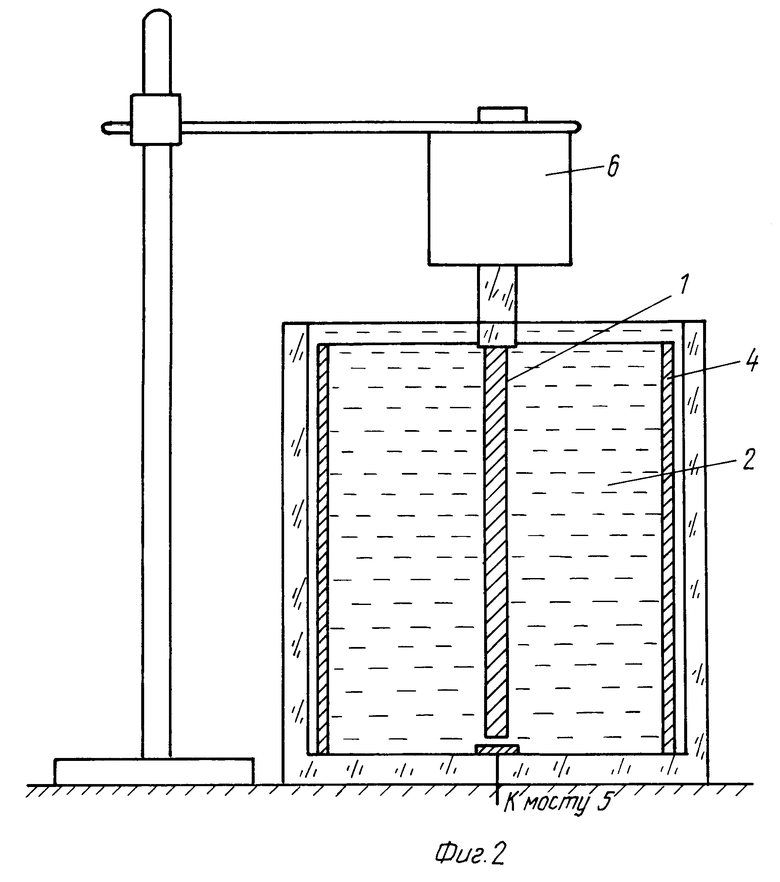
На фиг. 1 приведена электрическая схема установки для реализации предлагаемого способа; на фиг. 2 схема приведения катода во вращательное движение.
Вывод расчетной формулы. При малых значениях массы катода при измерении массы выделяющегося вещества допускается значительная погрешность, так как в формуле относительной погрешности (Δm/m) масса m катода стоит в знаменателе. Поэтому для этих случаев необходимо искать другие более точные способы измерения массы катода.
Предлагаемый способ основан на измерении электрического сопротивления катода.
Если взять катод цилиндрической формы длиной l и площадью поперечного сечения S, то его электрическое сопротивление R может быть вычислено по формуле
R = ρol/S, (1)
где ρo удельное сопротивление материала катода /для меди ρo 1,7•10-8 Ом•м/.
Если катод 1 (фиг. 1) длиной l и площадью поперечного сечения S1 поместить в электролит 2 и подключить так, чтобы клемма "-" источника 3 питания соединилась с катодом 1, а клемма "+" с цилиндрическим анодом 4, то в процессе электролиза на катоде 1 произойдет осаждение ионов металла, находящихся в растворе электролита (например, ионов меди, если в качестве электролита взять раствор медного купороса в воде). При этом происходит увеличение площади поперечного сечения до значения S2. В соответствии с формулой (1) это вызывает изменение сопротивления катода.
Таким образом, если каким-либо известным способом (на фиг. 1 для этой цели использован реохордный мост 5, например, марки Р-38), измерим электрическое сопротивление до электролиза R1 и после него R2, то изменение поперечного сечения катода, произошедшее в результате электролиза, можно вычислить по формуле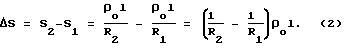
Массу m вещества, выделившегося на катоде, вычисляют, исходя из зависимости его от площади поперечного сечения катода (при неизменной длине катода)
m = ρlΔS, (3)
где ρ плотность материала вещества, из которого изготовлен катод.
Подставив значение изменения площади поперечного сечения из формулы (2) в формулу (3), получим окончательное выражение для нахождения массы выделившегося на катоде вещества по измеренным значениям его электросопротивления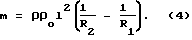
Таким образом, прирост массы вещества, происходящий в ходе электролиза на катоде 1, можно найти путем измерения сопротивления катода до и после электролиза при помощи моста 5.
В формуле (4) пренебрегли сопротивлением соединительных проводов. Если учесть, что их вклад в измеряемое мостом 5 сопротивление одинаков в обоих случаях, то формулу (4) нужно записать в следующем виде: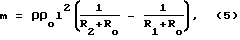
где R0 сопротивление соединительных проводов.
В ходе постановки эксперимента по предложенному способу выяснилось, что поверхность катода без его вращения получается шероховатой, что вызывает значительный разброс значений его электрического сопротивления. Поэтому в окончательной схеме реализации предлагаемого способа катод приводится во вращательное движение электродвигателем 6 (фиг. 2), имеющим частоту 60 об/мин.
Электрохимический эквивалент K вещества, выделяющегося на катоде, определяют по известной формуле
K m/(It), (6)
где I сила тока, протекающего через электролит, измеряемый амперметром 7;
t время его протекания, измеряемое секундомером (не показан).
По вычисленному значению K определяют величину числа Фарадея F по формуле
F M/(KZ), (7)
где M молярная масса вещества катода (для меди составляет 63,54 г/моль);
Z его валентность (для Z 2).
Заряд одновалентного иона (элементарный заряд) находим по формуле
e F/N, (8)
где N 6,026•1026 моль-1 число Авогадро.
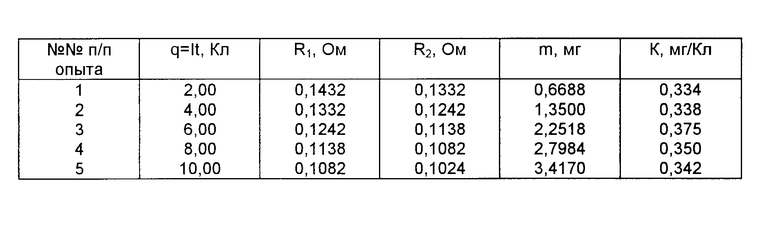
Полученные результаты измерения сопротивления катода и вычисленные по этим данным приросты масс катода и соответствующие значения электрохимического эквивалента приведены в таблице (ρ = 8900 кг/м3; ρo = 1,7•10-7 Ом•м; l = 10,5 см).
Инструментальная погрешность определения электрохимического эквивалента составляла 5,5%
Расхождение между экспериментально полученным средним значением из пяти опытов (0,350 мг/Кл) и табличным значением (0,330 мг/Кл) составило 6,2%
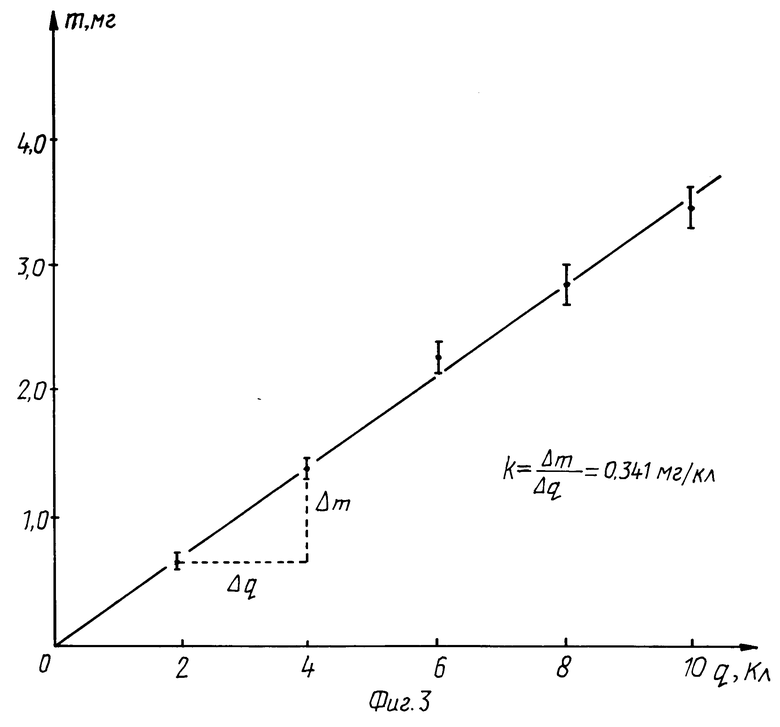
Дополнительного снижения погрешности можно добиться графическим способом обработки результатов.
На фиг. 3 показан график зависимости массы выделяющегося вещества m от прошедшего через электролит заряда. Вычисленное из графика значение электрохимического эквивалента составило 0,341 мг/Кл. Сравнение этого значения с табличным показывает еще меньшее расхождение их между собой (3,2%).
Таким образом, предлагаемый способ вполне может быть использован для вычисления таких параметров как электрохимический эквивалент, число Фарадея, заряд одновалентного иона (элементарный заряд).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения параметров электролиза | 1989 |
|
SU1640735A1 |
| Прибор для определения параметров электролиза | 1989 |
|
SU1663621A1 |
| ПРИБОР ДЛЯ ОПРЕДЕЛЕНИЯ ВЕЛИЧИНЫ ЭЛЕМЕНТАРНОГО ЗАРЯДА | 2005 |
|
RU2337409C2 |
| Способ измерения коэффициента диффузии при неравновесной концентрации ионов в электролитах и устройство для его реализации | 2020 |
|
RU2761448C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОТДЕЛЬНЫХ ВИДОВ ЭЛЕКТРОХИМИЧЕСКИХ И БИОХИМИЧЕСКИХ КОРРОЗИОННЫХ ПРОЦЕССОВ | 2005 |
|
RU2319947C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДНО-СОЛЕВЫХ РАСТВОРОВ | 2003 |
|
RU2270803C2 |
| СПОСОБ СВАРКИ МЕТАЛЛОВ И СПЛАВОВ | 1991 |
|
RU2014979C1 |
| СПОСОБ НАНЕСЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ НА ИЗДЕЛИЯ ТИПА ТЕЛ ВРАЩЕНИЯ | 2009 |
|
RU2427672C1 |
| СПОСОБ ДЕМОНСТРАЦИИ ЭЛЕКТРИЧЕСКОГО ПОЛЯ | 1992 |
|
RU2079895C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ПОЛУЧЕНИЯ НИКЕЛЬ-ПОЛИТЕТРАФТОРЭТИЛЕНОВЫХ ПОКРЫТИЙ | 1991 |
|
RU2033482C1 |
Использование: для проведения лабораторных работ при изучении электролиза. Сущность изобретения: катод изготавливают в виде цилиндра из материала, аналогичного осаждающемуся, приводят его во вращательное движение относительно продольной оси, измеряют электрическое сопротивление катода до и после прохождения тока через электролит и вычисляют прирост массы катода по формуле. 3 ил., 1 табл.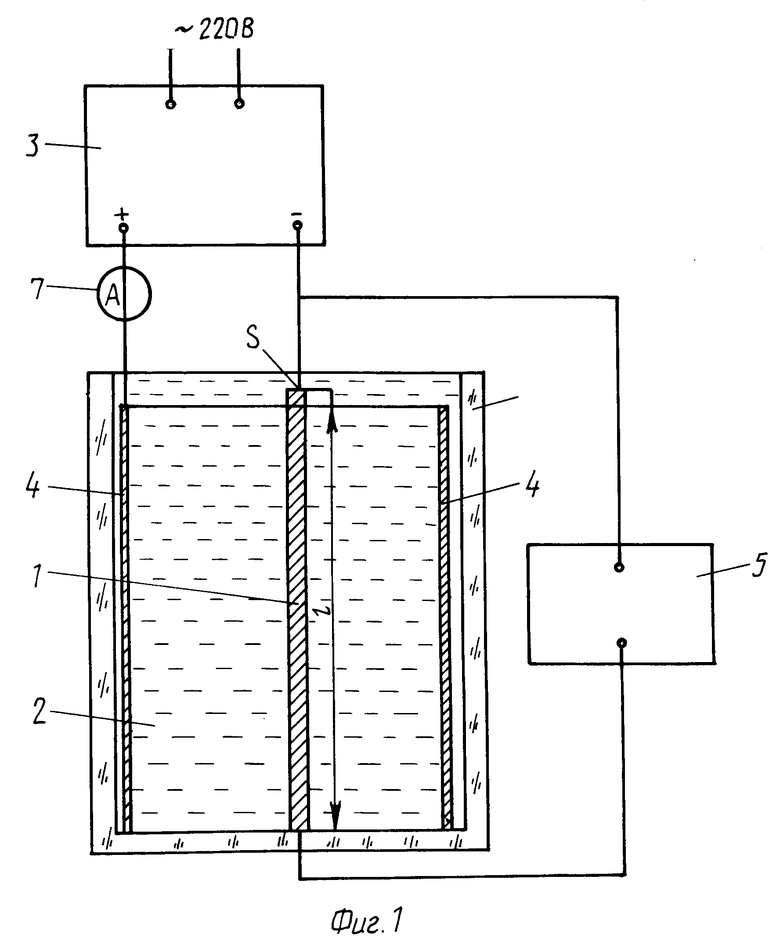
Способ определения параметров электролиза, при котором катод выполняют из материала, аналогичного осаждающемуся на нем, измеряют параметры катода до и после прохождения электрического тока через электролит и вычисляют прирост массы катода, отличающийся тем, что катод изготавливают в виде цилиндра, приводят его во вращательное движение относительно продольной оси и измеряют электрическое сопротивление катода до и после прохождения тока через электролит, при этом прирост массы вычисляют по формуле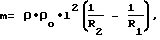
где ρ - плотность материала, из которого выполнен катод;
ρo- удельное сопротивление катода;
l длина катода;
R1 и R2 электрическое сопротивление катода соответственно до и после прохождения тока через электролит.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Калашников С.Г | |||
| Электричество, учебное пособие., 5 изд | |||
| - М.: Наука, гл | |||
| редакция физико-математической литературы, 1985, с | |||
| Прибор, автоматически записывающий пройденный путь | 1920 |
|
SU110A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ определения параметров электролиза | 1989 |
|
SU1640735A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
1997-10-27—Публикация
1995-03-17—Подача