Изобретение относится к приготовлению моховых масел, которые характеризуются пониженной аллергенностью, т.е. сильно пониженным аллергенным потенциалом и превосходными ольфактивными свойствами в составе ароматических композиций.
Моховые масла высоко ценятся парфюмерами за их типичные лесные оттенки и играют важную роль в создании духов, например так называемого типа "Шипр" или "Фужер". Их получают растворительной экстракционной обработкой лишайников, в частности Evernia prunastri L. для масла дубового мха и Evernia furfuracea L. для масла древесного мха. Общее количество лишайников, перерабатываемых во всем мире для парфюмерных целей, может быть оценено в 6000 т/год (P. Vigne, Parfums, Cosmetiques, Aromes, (78), стр.97-105, 1987), что по оценкам соответствует ежегодному обороту около $ 35 млн.
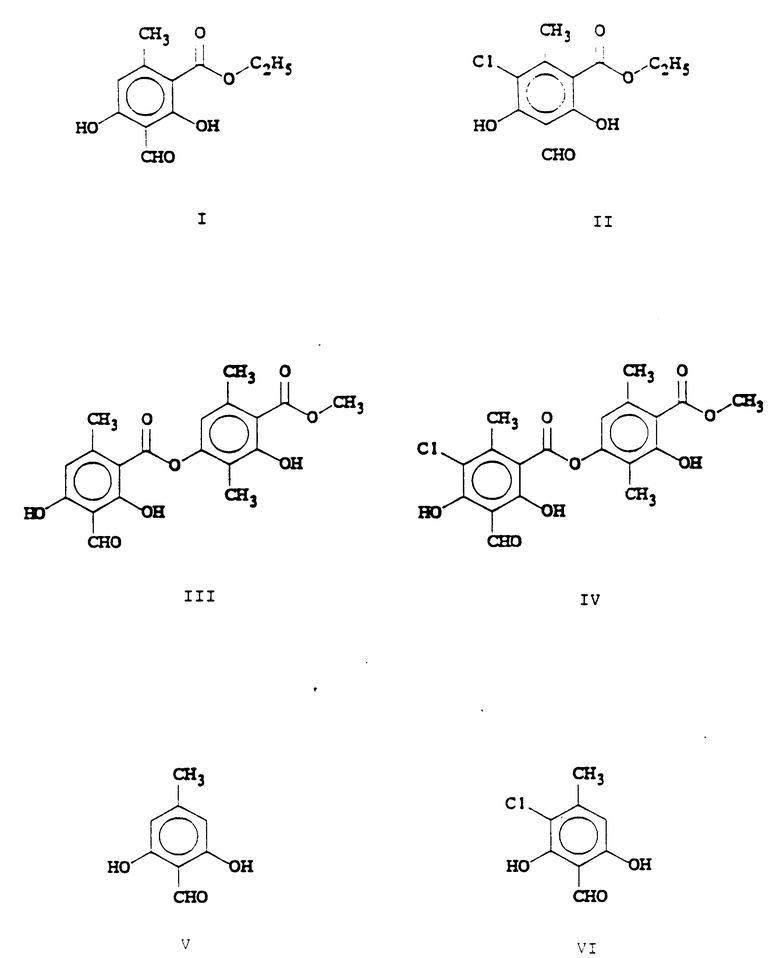
Моховые экстракты, например моховые абсолюты и конкреты, которые являются наиболее часто используемыми моховыми масляными продуктами, вызывают, как сообщается, сенсибилизацию кожи человека, и рядом исследовательских групп было показано, что такие аллергические реакции вызваны некоторыми компонентами моховых масел, в частности этилгематомматом I, этилхлоргематомматом II, атранорином III и хлоратранорином IV, формулы которых приведены в конце описания.
В европейской патентной публикации N 202.647 (Shiseido Company Ltd.) предлагается способ получения гипоаллергенных моховых масел путем удаления аллергенных веществ из моховых масел хроматографической обработкой, растворительной экстракцией, противоточным разделением и мембранным разделением с последующими каталитической гидрогенизацией и/или щелочной обработкой. Аллергены, удаляемые таким путем, представляют собой альдегиды, которые охватывают вышеупомянутые этилгематоммат I, этилхлоргематоммат II, атранорин III и хлоратранорин IV.
В более поздней европейской публикации N 468 189 (Roure S.A.) описан способ получения гипоаллергенных моховых масел, например реакцией моховых абсолютов или конкретов в спиртовом растворе с аминокислотами в однофазных условиях с последующим удалением нерастворившихся аллергенных веществ I-VI.
Концентрации аллергенов I-VI, которые при этом достигаются, существенно ниже критических уровней (0,05-1%), как это было экспериментально установлено проведением испытаний на аллергенность.
Целью настоящего изобретения является удаление в еще большей степени вышеупомянутых альдегидов I-VI осуществлением экономичного способа практически без воздействия на первоначальную окраску и ольфактивные свойства исходного мохового масла с получением, таким образом, моховых абсолютов или конкретов, обладающих сильно пониженным аллергическим потенциалом. Это достигается реакцией моховых экстрактов, например конкретов или абсолютов, с соответствующими восстановительными агентами, например с боргидридами щелочных металлов, которые конкретно воздействуют и восстанавливают исключительно альдегиды I-VI до соответствующих первичных спиртов.
Дополнительное достоинство нового способа состоит в возможности избежать сопутствующего образования небольших количеств красителей, которые могут создать неудобства в некоторых областях парфюмерного применения.
Таким образом, предметом настоящего изобретения является реакция между моховыми экстрактами, например маслами, конкретами или абсолютами, и соответствующими альдегидвосстановительными агентами, например комплексными гидратами металлов, предпочтительнее боргидридами щелочных металлов, в частности боргидридом лития или натрия, в системах органических растворителей.
Исходные моховые экстракты, подвергаемые такой обработке, могут быть с успехом получены растворительной экстракцией из лишайников и охватывают, в частности, конкрет дубового мха Evernia prunastri L. и конкрет древесного мха Evernia furfuracea L. предпочтительнее их абсолюты.
Из литературы (например, из работы Reagents for Organic Synthesis, L.F. Fieser and M.Fieser, стр. 599-603 и 1049-1055, издание John Wiley and Sons, Inc. 1967) известно, что комплексные гибриды щелочных металлов, в частности боргидриды или алюминийгидриды, способны восстанавливать альдегиды, кетоны и даже сложные эфиры. Альдегидные аллергены I-VI вносят незначительный вклад в общий запах моховых экстрактов, в то время как многочисленные сложные эфиры, другие альдегиды и кетоны являются, насколько это известно, ольфактивно важными малыми или большими компонентами таких экстрактов (см. Ter Heide et al. Qualitative Analysis of the Odorieferous Fraction of Oakmoss Evernia prunastri L. Ach.), J.Agric. Food Chem. 23 (5), стр. 950-957, 1975 г.).
Следовательно, неожиданностью явилось установление того факта, что предлагаемый новый способ позволяет достичь селективного восстановления аллергенов I-VI без ухудшения органолептических свойств мохового масла или, другими словами, из исходного мохового экстракта; при этом, по-видимому, не удаляется ни один из вышеупомянутых сложных эфиров, связанный с органолептическими характеристиками, как это было установлено по данным газовой хроматографии. Кроме того, было установлено, что величины концентрации соединений I-VI при этом значительно ниже требуемых пределов (см. табл 1) и тех уровней, которые достигались согласно литературным сообщениям (Европейская патентная публикация N 468.189 и работа C. Ehret, P.Maupetit, M.Petrzilka, G.Klecak, Int.J.of Cosm. Science, 14, 121-130, 1992 г.). Наконец, по окраске получаемые неаллергенные моховые масла очень близки к исходным маслам, благодаря чему они приемлемы для большинства областей парфюмерного применения.
В соответствии с наиболее широким аспектом настоящего изобретения аллергенное моховое масло растворяют в подходящем органическом растворителе и обрабатывают (предпочтительнее избыточным количеством) соответствующим альдегидвосстанавливающим реагентом. Подходящими восстановительными агентами являются те, которые способны восстанавливать исключительно или по меньшей мере преимущественно альдегиды в сравнении со сложными эфирами и которые относятся к соединениям различных типов (см. работу R.C.Larock, Comprehensive Organic Transformations, A Guide to Functional Group Preparations, опубликованную VCH Publishers, Inc. Нью-Йорк, стр. 527-535, 1989г.), например:
комплексные гибриды металлов или аммония, в частности натрия, лития, калия, цинка, тетраэтиламмонийборгидриды и тому подобное;
замещенные комплексные гибриды металлов или аммония, в частности триацетоксиборгидрид натрия, триацетоксиборгидрид калия, цианборгидрид натрия и тетра-n-бутиламмонийтриацетоксиборгидрид;
гидриды металлов, в частности диборан, гидриды щелочных металлов и алюминия и тому подобное.
Предпочтительными восстановителями являются литийборгидрид и натрийборгидрид.
Реакцию восстановления можно проводить в соответствии с известными методами. Обычно ее проводят в органической среде, например, в растворе с использованием возможно галоидированных, алифатических или ароматических углеводородных растворителей, в частности гексана, циклогексана, толуола и тому подобного, сложных эфирных растворителей, в частности этилацетата, изопропилацетата и тому подобного, или спиртовых растворителей, в частности метанола, этанола и тому подобного. В других вариантах можно также использовать простые эфирные растворители, в частности третбутилметиловый эфир, тетрагидрофуран и тому подобное, или галоидированные растворители, в частности хлористый метилен. Еще одной возможностью является использование смесей вышеперечисленных растворителей.
Концентрация моховых экстрактов, вводимых в реакцию, может варьироваться в интервале приблизительно 5-50 мас. предпочтительнее примерно 5-15 мас.
Приемлемые количества восстановителей, например боргидридов щелочных металлов, составляет приблизительно 0,02-0,1 г, предпочтительнее примерно 0,03-0,07 г, на каждый грамм мохового экстракта. Это количество соответствует приблизительно 2-5-кратному молярному избытку, то есть 8-20-кратному избытку восстановительного эквивалента.
Температура реакции составляет приблизительно 20-80oC, предпочтительнее примерно 20-30oC, в случае использования, например, литийборгидрида, а при использовании боргидрида натрия предпочтительная температура должна быть равной точке кипения, например спирта, в частности этанола.
Реакцию обычно прекращают по истечении приблизительно от 30 мин до 3 ч, предпочтительнее по истечении примерно от 30 до 60 мин в случае использования боргидрида натрия, и через 1-2 ч в случае использования литийборгидрида.
Когда для проведения реакции применяют водонерастворимые растворители, в частности углеводороды, сложные эфиры, галоидированные и алифатические простые эфирные растворители, обработка состоит в интенсивной промывке реакционной смеси водой или водными растворами кислот (например, 1-10%-ным, предпочтительнее 1-3%-ным, раствором соляной кислоты), а затем водой до нейтральной реакции. В конце органический растворитель отгоняют под пониженным давлением, причем температура не должна превышать приблизительно 85oC. В другом варианте, когда используют водорастворимые растворители, например спирт или циклический простой эфир, в частности тетрагидрофуран, в начале под пониженным давлением отгоняют растворитель. Затем полученный остаток вновь растворяют в водонерастворимом растворителе, например в растворителях, перечисленных выше, и обрабатывают аналогично вышеизложенному в предыдущем варианте.
Примеры
1) Аллергенность
Сильно пониженный аллергенный потенциал продукта в каждом случае определяли в соответствии с обычными, всецело признанными методами сенсабилизации кожи и определения кожных реакций, т.е. с конкретно с так называемыми
* модифицированными методами Бюхлера с использованием морских свинок и
* методом испытаний с повторными инсультными пятнами (ИПИП) с использованием людей.
2) Анализ
Содержание альдегидов I, II, V и VI
Содержание продуктов I, II, V и VI с успехом определяют газохроматографическим анализом с применением внутреннего эталона и осуществлением процедур в нижеследующих условиях:
* колонка: 50 м с внутренним диаметром 0,32 мм, сплавленная двуокись кремния
* стационарная фаза: CP Sil 5CB (силикон)
* детектор: пламенно-ионизационный детектор (ПИД)
* векторный газ: гелий, 2 мл/мин
* температурный режим: 100-240oC/мин
* внутренний эталон: метил-2,4-диокси-3,6-диметилбензоат.
Содержание альдегидов III и IV
Содержание альдегидов III и IV с успехом определяют высокоэффективной жидкостной хроматографией с использованием внешнего эталона и осуществлением процедуры в нижеследующих условиях:
* колонка: длиной 250 мм с внутренним диаметром 4,6 мм
* стационарная фаза: RP 18 (обратимая фаза, размер частиц 7 мкм)
* детектор: ультрафиолетовый при 260 нм
* подвижная фаза А: вода, подкисленная до величины pH 2,8 концентрированной ортофосфорной кислотой
В: ацетонитрил
* градиент:(см.табл.1а).
При таком градиенте обеспечивается эффективное отделение вышеуказанных нелетучих альдегидов III и IV.
Пример 1. Получение абсолюта дубового мха с сильно пониженным потенциалом с помощью литийборгидрида.
В 500-миллилитровую трехгорлую колбу, снабженную механической мешалкой, холодильником и капельной воронкой, загрузили 15 г расплавленного технически доступного абсолюта дубового мха (фирма "Живоден-Рур", температура плавления
примерно 70oC), который далее при комнатной температуре и в токе азота растворили в 200 мл смеси циклогексана с изопропилацетатом в соотношении 3:1. Затем в этот гомогенный раствор по каплям в течение приблизительно 30 мин добавили суспензию 480 мг (22 ммол) литийборгидрида в 100 мл смеси циклогексана с изопропилацетатом в соотношении 3:1. Немедленно после добавления выпал осадок и наблюдалось слабое повышение температуры реакционной смеси (примерно на 6oC). После перемешивания реакционной смеси в течение дополнительных 2 ч при комнатной температуре реакцию в ней осторожно прекратили добавлением 150 мл 0,5%-ного (по весу) водного раствора соляной кислоты и подвергли экстракционной обработке 3 порциями по 300 мл смеси циклогексана с изопропилацетатом в соотношении 3:1. Органические слои промыли одной 150-миллилитровой порцией воды, объединили и сконцентрировали под пониженным давлением (20 мбар) на водяной бане, не превышая температуры приблизительно 85oC. Таким образом получили 12,78 г (выход 85,2%) абсолюта дубового мха, который, как показали газохроматографический и высокоэффективный жидкостной анализы, содержал крайне незначительные количества альдегидов I-VI (см. табл.2).
Пример 2. Получение абсолюта дубового мха с сильно пониженным аллергенным потенциалом с помощью боргидрида натрия.
В 250-миллилитровую трехгорлую колбу, снабженную механической мешалкой, холодильником и капельной воронкой, загрузили 14,9 г расплавленного технически доступного абсолюта дубового мха (фирма "Живодэн-Рур", температура плавления примерно 70oC), который далее при комнатной температуре и в токе азота растворили в 90 мл 96%-ного этанола. Затем в этот гомогенный раствор по каплям в течение приблизительно 5 мин добавили суспензию 1 г (26,4 ммол) натрийборгидрида в 60 мл 96%-ного этанола. В процессе такого добавления наблюдалось слабое повышение температуры (приблизительно на 12oC). После перемешивания реакционной смеси при температуре кипения в течение 45 мин под пониженным давлением (20 мбар) отогнали этанол и остаток растворили в 300 мл третбутилметилового эфира (ТБМЭ). Затем реакцию в реакционной смеси осторожно прекратили добавлением 150 мл воды с последующей экстракцией 3 порциями по 300 мл ТБМЭ. Органические слои промыли одной 150-миллилитровой порцией воды, объединили и сконцентрировали под пониженным давлением (20 мбар) на водяной бане, не превышая температуры примерно 85oC. Таким образом получили 12,78 г (выход 85,2%) абсолюта дубового мха, который, как показали газохроматографический и высокоэффективный жидкостной анализы, содержал крайне незначительные количества альдегидов I-VI (см. табл. 3).
Пример 3. Получение абсолюта дубового мха с сильно пониженным аллергенным потенциалом с помощью боргидрида натрия(кислотная обработкая).
В 250-миллилитровую трехгорлую колбу, снабженную механической мешалкой, холодильником и капельной воронкой, загрузили 15 г расплавленного технически доступного абсолюта дубового мха (фирма "Живодэн-Рур", температура плавления
примерно 70oC), который далее при комнатной температуре и в токе азота растворили в 100 мл 96% -ного этанола. Затем в этот гомогенный раствор по каплям в течение приблизительно 5 мин добавили суспензию 1 г (26,4 ммол) натрийборгидрида в 60 мл 96% -ного этанола. В процессе такого добавления наблюдалось слабое повышение температуры (приблизительно на 15oC). После перемешивания реакционной смеси при температуре кипения в течение 45 мин под пониженным давлением (20 мбар) отогнали этанол и остаток растворили в 300 мл третбутилметилового эфира. Затем реакцию в реакционной смеси осторожно прекратили добавлением 100 мл воды и подкислили до величины pH 1,5 добавлением приблизительно 15 мл 6%-ного водного раствора соляной кислоты. Органические слои промыли одной 150-миллилитровой порцией воды, объединили и сконцентрировали под пониженным давлением (20 мбар) на водяной бане, не превышая температуры примерно 65oC. Таким образом получили 14,42 г (выход 96,1%) абсолюта дубового мха, который, как показали газохроматографический и высокоэффективный жидкостной анализы, содержал крайне незначительные количества альдегидов I-VI (см. табл. 4).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИПОАЛЛЕРГЕННОГО ЛИШАЙНИКОВОГО МАСЛА | 1991 |
|
RU2092168C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2003 |
|
RU2360903C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКОГО РАСТВОРА ДИАЛКИЛПЕРОКСИДИКАРБОНАТА | 2011 |
|
RU2606498C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ HMG-COA РЕДУКТАЗЫ | 2003 |
|
RU2299196C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ 2-АМИНО-1,3-ПРОПАНДИОЛА И ИХ СОЛЕЙ | 2014 |
|
RU2663833C2 |
| ТАКСОИДЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2139864C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ОКСАЗОЛИДИН-5-КАРБОНОВОЙ КИСЛОТЫ (ВАРИАНТЫ) | 1993 |
|
RU2114834C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ ГЕКСАГИДРОФУРО[2,3-b] ФУРАН-3-ОЛА | 2007 |
|
RU2464266C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТАКСАНА И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2116303C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЛОКАТОРА АНГИОТЕНЗИНОВОГО РЕЦЕПТОРА | 2003 |
|
RU2412173C2 |





Использование: изобретение относится к эфирно-масличной промышленности и касается получения гипоаллергенных моховых масел. Сущность: в способе получения гипоаллергенных моховых масел, предусмотрена реакция исходного мохового масла, конкрета или, предпочтительнее, его абсолюта с альдегидвосстанавливающим агентом в среде органического растворителя, в качестве агента используют гидриды щелочных металлов, в качестве органического растворителя - например, галоидированные алифатические или ароматические углеводороды, сложные эфиры или их смеси, обработку возможно вести при температуре 20-80oC. 6 з.п. ф-лы, 5 табл.
| EP, 0202647, кл.C 11B 9/02, 1987. |
Авторы
Даты
1997-11-10—Публикация
1994-01-19—Подача