Изобретение имеет отношение к новому производному триазола, используемому как инсектицид, также как и к инсектициду, содержащему его в качестве активного ингредиента.
Известно, что производные триазола, такие, как 3-хлорофенил-5-хлоропиридил-1-метил-1Н-1,2,4-триазол и ему подобные, эффективны для контроля численности клещей и кровососущих насекомых (описание исследования RD 278004).
В этой литературе нет описания того, какая концентрация выше названного производного является эффективной по отношению к какому виду вредных насекомых, а также не ясно происхождение этого производного. Более того описанные в названной литературе конкретные соединения обладают недостаточными характеристиками с точки зрения системного перемещения и системного проникновения и едва ли могут быть удовлетворительными инсектицидами.
Насекомые вредители продуктов сада и фермы относятся к тлям, таким, как хлопковая тля, тля зеленых персиков, тля наперстянки и т.п. Эти тли поедают растения в точках роста и сильно повреждают продукты садов и ферм, а также вносят вирусы. Поэтому необходимо контролировать размножение тлей. Нарастающая устойчивость вредных насекомых к существующим инсектицидам и акарицидам делает такой контроль еще более серьезным. В этой связи химикаты для контроля вредителей должны обладать негативными свойствами системного переноса и проникновения.
Изобретатели синтезировали различные производные триазола, чтобы предложить инсектицид, применимый для контролирования выше названных вредных насекомых, и провели исследование их физиологической активности.
В результате изобретатели нашли, что новые соединения с общей формулой (I), приведенной ниже, имеют прекрасные данные системного перемещения и по системному проникновению и обнаруживают превосходную инсектицидную активность по отношению к различным вредным насекомым и акаридам по сравнению с теми конкретными соединениями, которые описаны в вышеупомянутой литературе.
Согласно изобретению, предлагается триазольное производное с общей формулой (1)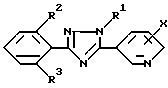
где R1 группа низшего алкила, а R2 и R3 - одинаковые или различные атомы галогенов; X атом хлора, находящийся в 2 - или 6-положении).
Согласно изобретению данные производные триазола имеют особенно улучшенную активность по активному перемещению и проникновению благодаря тому, что как R2, так и R3 заместители бензольного кольца, связанного с 3-им положением триазольного цикла, являются атомами галогена. Более того триазольные производные, имеющие два заместителя в бензольном кольце, связанном с 3-им положением триазольного кольца, и алкильный заместитель в 1-м положении триазольного кольца, могут быть синтезированы новыми методами.
В общей формуле (I) группа низшего алкила R1 включает метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, трет-бутильную группу, втор-бутильную группу и т.п. а атом галогена R2 и R3 это фтор, хлор, бром и иод. Среди соединений общей формулы (I) соединение, в котором R1 метильная или этильная группа, а X атом хлора, находящийся во 2- или 6-м положении, является предпочтительным.
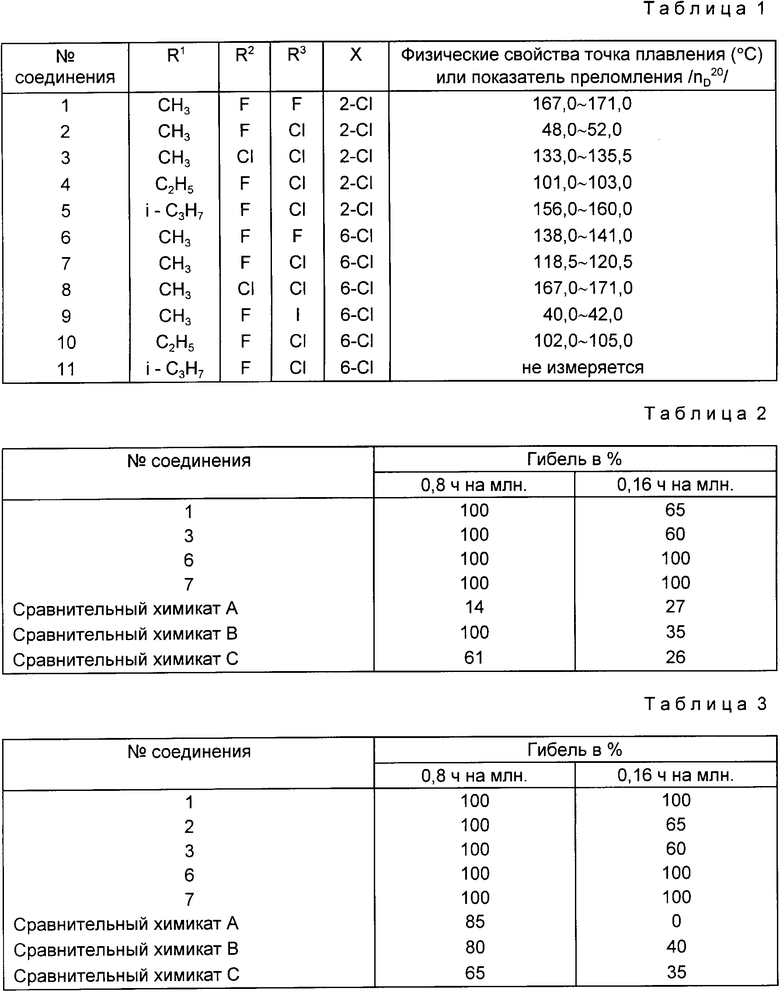
Соединения общей формулы (I), соответствующие изобретению, приведены в табл.1. Нумерация соединения соответствует их дальнейшему описанию.
Соединения, соответствующие изобретению, могут быть получены следующими методами, но не ограничиваются этими методами.
Способ получения 1-1
Соединение общей формулы (I) может быть получено при взаимодействии алкил-N-ациламидатного производного или алкил-N-ацилтиоамидатного производного, представленных общей формулой (II), с производным гидразина общей формулы (III) в инертном растворителе согласно следующей системе реакции: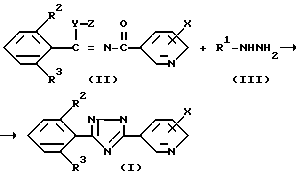
где Y атом серы или атом кислорода; Z группа низшего алкила; R1, R2, R3 и X то же, что указано выше.
В качестве инертного растворителя может использоваться любой, не препятствующий реакции, такой как спирт: метанол, этанол и т.п. эфир, напр. диэтиловый эфир, тетрагидрофуран, диоксан диглим и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. нитрил, такой как ацетонитрил и т.п. N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, вода и их смеси. Кроме того, производное гидразина (III) обычно используется в количестве 1-5 моль на 1 моль алкил-N-ациламидатного производного или алкил-N-ацилтиоимидатного производного или алкил-N-ацилтиоимидатного эфирного производного (II).
Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 0oC до 50oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах 1-72 ч.
Конкретный пример такой реакции приводится, например, в Synthesis 483 (1983).
Алкил-N-ацил/тио/имидатное производное (II) как исходное соединение может быть получено следующим методом.
Способ получения 1-2
Алкил-N-ацил/тио/имидатное производное, представленное общей формулой (II), может быть получено путем взаимодействия бензимидатного производного, представленного общей формулой (V) в инертном растворителе в присутствии основания согласно следующей схеме реакции: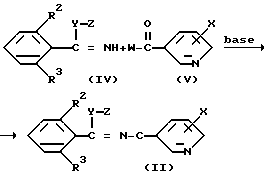
в которой W атом галогена, а R2, R3, X, Y и Z те же, что указаны выше).
Кроме того, бензимидатное производное общей формулы (IV) может использоваться в виде кислотно-аддитивной соли. В этом случае тетрафторид был хлористый водород, бромистый водород, йодистый водород и т.п. могут быть использованы.
В качестве основания могут быть использованы неорганические основания, такие как карбонат натрия, карбонат калия, бикарбонат иодид гидроксид натрия, гидроксид калия и т.п. они органические основания, такие как диэтиламин, триэтиламин, пиридин, 4-N,N-диметиламинопиридин и т.п. В качестве растворителя следует упомянуть кетон, такой как ацетон, метилэтилкетон и т.п. как эфир диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод или т.п. нитрил, такой как ацетонитрил или подобные ему; диметилформамид, диметилацетамид, диметилсульфоксид и их смеси.
В общем галогенангидрид никотиновой кислоты (V) используют в количестве 0,8-1,3 моль на 1 моль бензимидатного производного (IV). Количество применяемого основания равно 1,0- 2,0 моль-эквивалента на 1 моль бензимидатного производного (IV).
Время реакции зависит от используемых исходных соединений, но обычно в пределах 1-24 часа, температура реакции в пределах от 0oC до точки кипения используемого растворителя.
Способ получения 2
Соединение общей формулы (I) в соответствии с изобретением может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного, представленного общей формулой (VI) с 3-цианопиридиновым производным, представленным общей формулой (VII) в инертном растворителе в присутствии кислоты Льюиса в соответствии со следующей схемой реакции: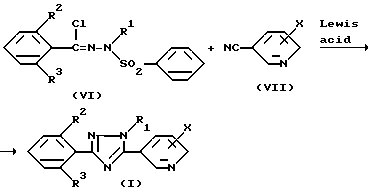
где R1, R2, R3 и X те же, что упомянуты выше.
В качестве инертного растворителя можно взять любой, не мешающий реакции, например эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, дихлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, 3-цианопиридиновое производное (VII) и кислота Льюиса используются в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI) соответственно.
Температуру реакции возможно поддерживать в диапазоне от 0oC до точки кипения используемого растворителя, лучше в пределах 50 -150oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч.
Конкретный пример этой реакции приводится, например, в Bulletin of Chemical society of Japan, vol.56 pages 545-548 (1983). 545-545 (1983).
Способ получения 3
Соединение общей формулы (I) в соответствии с изобретением может быть получено путем реакции N-/фенилсульфонил/бензамидразонового производного, представленного общей формулой (VIII) с галогенангидридом никотиновой кислоты производным общей формулы (V) в инертном растворителе согласно следующей реакции: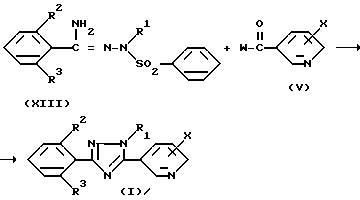
где R1, R2, R3 и X то же самое, что упомянуто выше.
В качестве инертного растворителя можно использовать любой из растворителей, не мешающих реакции, которые включают эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир, и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, никотиноилгалоидное производное (V) (галогенангидридное производное) используют в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфенил) бензамидгидразонового производного (VIII).
Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 50oC до 200oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч.
Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 545-548, 1983.
Кроме того, N-/фенилсульфонил/бензамидразоновое производное (VIII) как исходное соединение может быть получено следующим методом.
Способ получения 3-2
N-/фенилсульфонил/бензамидразоновое производное, представленное общей формулой (VIII) может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного общей формулы (VI) с газообразным аммиаком в инертном растворителе в соответствии со следующей реакцией: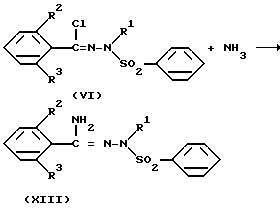
где R1, R2, R3- те же, как указано выше.
В качестве инертного растворителя можно использовать любой, не мешающий реакции, напр. эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т. п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т. п. и алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, аммиак и используют в количестве 5,0 10,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI).
Температура реакции возможна в пределах от 0oC до точки кипения используемого растворителя, но предпочтительно в пределах 50 150oC. Время реакции зависит от используемых исходных веществ, но обычно в пределах 5 20 ч. Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 547,1983.
Следующие примеры даются в качестве иллюстрации, но не для ограничения изобретения.
Пример получения 1. 5-/2-хлорпиридин-3-ил/-3-/2,6-дифторфенил/-1-метил-1Н-1,2,4-триазол (соединение 1)
В 100 мл толуола растворяли в 1,9 г этил-2,6-дифторбензимидата и 1,2 г триэтиламина, к которым добавляли по каплям 1,8 г 2-хлороникотиноилхлорида в диапазоне температур 5-10oC при перемешивании. Полученный раствор перемешивали при комнатной температуре в течение 6 ч. После завершения реакции раствор промывали водным раствором соли, затем водой и образующийся толуольный слой высушивали сульфатом натрия.
К толуольному слою добавляли 0,5 г монометилгидразина, который реагировал при комнатной температуре в течение 8 ч. После завершения реакции раствор промывали разбавленным раствором соляной кислоты, затем водой, а затем толуольный слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении.
Полученный концентрат хроматографировали на силикагеле /торговая марка: Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата, чтобы получить 0,8 г /выход 25,8%) целевых желтых гранулированных кристаллов/точка плавления: 167-171,0oC).
Данные ЯМР (60 МГц CDCl3 растворитель, величина)
3,95 (s, 3Н)
6,80 7,68 (m, 4Н)
7,05 (dd, 1Н)
8,55 (dd, 1Н)
Пример 2. 3-(2,6-дихлорфенил)-5-(2-хлорпиридил-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 3)
5,7 г N-метил-N- фецилсульфонил-2,6-дихлорбензогидразоноил хлорида и 2,3 г 2-хлор-З-цианопиридина растворили в 50 мл дихлорбензол и к полученному раствору добавили при перемешивании 2,2 г безводного хлорида алюминия при комнатной температуре.
Полученный раствор нагревали до 120-140oC на масляной бане при перемешивании в течение 4 ч. После завершения реакции реакционный раствор промывали разбавленным раствором щелочи, а затем разбавленным раствором соляной кислоты.
После промывки водой органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении.
Результирующий концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя для заявления смешанный раствор гексана и этилацетата с получением 1,9 г (выход 37,3%) целевых светлокоричневых кристаллов в виде гранул (т.п. 133,0-135,5oC)
ЯМР: 160 МГц, CDCl3, б): 3,93 (с, 3Н), 7,30-7,63 (м, 4Н), 7,95 (dd, 1Н), 8,55 (dd, 1Н)
Пример 3. 3-/2-хлор-6-фторфенил)-5- (6-хлорпиридин-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 7)
N-метил-N-фенилсульфонил-2-хлоро-6-фторбензамидразон и 4,5 г 6-хлорпикопитиноилхлорида растворили в 50 мл 1-метил-2-пирролидина (NMP).
Полученный раствор нагревали до 110-120oC на масляной бане и перемешивали 4 ч.
После завершения реакции добавили 200 мл хлороформа и промывали водой. Полученный органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении.
Результирующий концентрат хроматографировали на силикагеле (торговая марка Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата с получением 2,0 г (выход 35,5%) желтых кристаллических гранул (т.пл. 118,5-120,5oC).
ЯМР (60 МГц, CDCl3, δ ): 4,03 (С, 3Н), 6,83-7,80 (т, 4Н), 8,05 (дд. 1Н), 8,75 (дд. 1Н).
Пример 4. 3-/2-хлоро-6-фторфенил/-5-6-хлоропиридин-3-ил)-1-изопропил- 1Н-1,2,4-триазол (соединение 11)
В 20 мл дихлорбензола растворяли 5,8 г N-метил-N-фенилсульфонил-2-хлоро-6-фторбензогидразоноилхлорида и 2,3 г 6-хлоро-З-цианопиридина, к которым добавляли 2,2 г безводного алюминия хлорида при комнатной температуре при перемешивании. Образующийся раствор нагревали до 140o на масляной бане и перемешивали в течение 30 мин. После завершения реакции реакционный раствор растворяли в 200 мл хлороформа. Раствор в хлороформе промывали разбавленным щелочным раствором, а затем разбавленным раствором соляной кислоты, после промывания водой органический слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя смешанный раствор гексана и этилацетата в качестве элюирующего растворителя, и получили продукт в виде коричневой вязкой жидкости (показатель преломления ( n
Данные ЯМР (60 МГц, CDCl3 растворитель, величина δ )
1,60 (д, 6Н)
4,45-4,95 (м, 1Н)
6,95 7,55 (m, 4Н)
7,95 (дд, 1Н)
8,65 (д, 13)
Инсектицид в соответствии с изобретением содержит производное триазола, представленное общей формулой (I) в качестве активного ингредиента.
Когда триазольные соединения, соответствующие изобретению, используются как активный ингредиент инсектицидов, эти соединения могут применяться сами по себе отдельно или совместно с носителем, поверхностно-активным веществом, диспергирующим агентом или любой добавкой, чтобы получить порошки, смачиваемый порошок, эмульсию, тонкоразмельченный порошок, гранулы и т.п. В качестве носителя для получения сельскохозяйственных химикатов могут быть упомянуты такие твердые носители как зиклит, тальк, бентонит, глина, каолин, диамотовая земля, белый уголь, вермикулит, гидроксид кальция, кварцевый песок, сульфат аммония, мочевина и т.п. а жидкие носители изопропиловый спирт, ксилол, циклогексанон, метилнафталин, и т.п. Как поверхностно-активные и диспергирующие агенты могут быть упомянуты металлические соли алкилбензолсульфокислоты, динафтил метандисульфоновой кислоты, эфира спирта и серной кислоты, алкиларилсульфонат, лигносульфонат, полиоксиэтиленгликолевый эфир, полиоксиэтиленалкилариловый эфир, полиоксиэтиленсорбитанмоноалкилат и т.п. В качестве добавки следует упомянуть карбоксиметилцеллюлозу, полиэтиленгликоль, гуммиарабик и т.п.
При составлении композиций количество используемого активного ингредиента может быть выбрано соответственно составленной цели, но подходящим является вызов в пределах 0,05 20% по весу, преимущественно 0,1 10% по весу в случае порошков и гранул. В случае эмульсий и смачиваемых порошков количество активного ингредиента лучше выбирать в пределах 0,5-8,0% по весу, лучше 1-6% по весу.
Инсектицид, соответствующий изобретению, может применяться путем распыления на стебли и листья, внесения в почву, внесения в ящики для рассады, распыления над поверхностью воды и т.п. При употреблении инсектицид непосредственно наносится или распыляется после разведения до подходящей концентрации. Количество наносимого инсектицида зависит от вида соединения, используемого в качестве активного ингредиента, от вредного насекомого, против которого оно применяется, от направленности и степени вреда, наносимого насекомым, от условий окружающей среды, от вида используемой формы инсектицида и т. п. Когда инсектицид, соответствующий изобретению, непосредственно используется как порошок или гранулы, количество активного ингредиента обычно выбирается в пределах 0,05 г 5 кг, предпочтительно 0,1 1 кг на 10 ар. Более того, когда он используется в виде жидкой эмульсии или смачиваемого порошка, количество активного ингредиента стоит выбрать в пределах 0,1 5000 ч. на 1 млн. лучше 1-1000 ч. на 1 млн. Кроме того, инсектицид, соответствующий изобретению, можно использовать в смеси с другими инсектицидом, фунгицидом, удобрениями, регулятором роста растений и т.п.
Составление композиций будет далее описано на конкретных примерах. В этом случае вид соединений и добавок и их соотношения не ограничиваются этими примерами и могут изменяться в широких пределах. Кроме того, указаны весовые проценты, если специально не оговорено.
Пример получения состава 1.
Эмульсия
Эмульсия была приготовлена равномерным растворением 30% соединения 6, 20% циклогексанона, 11% полиоксиэтиленалкиларилового эфира, 4% алкилбензолсульфоната кальция и 35% метилнафталина.
Пример получения состава 2.
Смачиваемый порошок
Смачиваемый порошок готовили равномерным смешиванием и измельчением в порошок 40% соединения 3, 15% диатомовой земли, 15% глины, 5% белого угля, 2% натрийдинафтилметандисульфоната и 3% натрийлигнинсульфоната.
Пример получения состава 3.
Порошок
Порошок готовили равномерным смешиванием и измельчением 2% соединения 1,5% диатомовой земли и 93% глины.
Пример получения состава 4.
Гранулы
5% соединения 7, 2% натриевой соли эфира лаурилового спирта и серной кислоты, 5% натрий-лигнин-сульфоната, 2% карбоксиметилцеллюлоза и 86% глины, которые были равномерно смешаны и измельчены. Затем 100 ч. по весу полученной смеси добавили к 20 ч. воды (по весу) и месили и придавали форму гранул размером 14-24 меш, пропуская через гранулирующую машину путем выдавливания и высушивали, чтобы получить гранулы.
Триазольные производные, соответствующие изобретению, эффективны для контроля численности тлей, таких как хлопковая тля, тля зеленых персиков, капустная тля и т.п. цикадки, такие как коричневые цикадки и т.п. листовые цикады, такие как зеленая рисовая цикада, чайная зеленая цикада и т.п. белокрылки, такие как белокрылка тепличная и т.п. парнокрылые вредные насекомые, такие как тутовый шелкопряд, рисовый клоп и т.п. чешуекрылые вредные насекомые, такие как капустная моль, бобовая бабочка-совка, табачная бабочка-совка и т.п. двукрылые вредные насекомые, такие как домашняя муха, москиты и т.п. жесткокрылые вредные насекомые, такие как рисовый долгоносик, соевый долгоносик, тыквенный листоед и т.п. тараканы, такие как Американский таракан, паровая муха, и т.п. клещи, такие как двухпятнистый клещик паутинный, паутинный клещ канзава, красный лимонный клещ и т.п.
В особенности инсектицид, соответствующий изобретению, оказывает очень выраженное действие на контролирование численности тлей, таких как хлопковая тля, тля зеленых персиков, кукурузная тля и т.п. дельфацидов, таких как вьюнковая тля, капустная тля и т.п. белокрылок, таких как тепличная белокрылка, белокрылка сладкого картофеля и т.п. парнокрылых вредных насекомых, таких как тутовый шелкопряд и т.п. трипсов, таких как южный желтый трипс и т.п. клещей, таких как двухпятнистый клещик паутинный, паутинный клещ канзава, цитрусовый красный клещ и т.п.
Действие соединений, соответствующих изобретению, будет описано в соответствии со следующими примерами испытаний. Более того следующие соединения использовали как сравнительные агенты.
Сравнительные агенты от A до C это соединения, опубликованные в Research Disclosure RD 278004, и используются в такой же форме, которая описана выше, тогда как сравнительные химикаты D и E это коммерческие продукты, обычно применяемые для борьбы с тлями.
Сравнительный агент A: 3-/2/хлорофенил/-5-/2-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол,
Сравнительный агент B: 3-/2/хлорофенил/-5-/6-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол,
Сравнительный агент C:
3-/2-хлоро-4-фторфенил/-5-/6-хлоропиридиы-3-ил/-1-метил-1Н-1,2,4-триазол;
Сравнительный агент D: 45% смачиваемый порошок метомил
Сравнительный агент E: 50% эмульсия этиофенкарб
Пример испытаний 1. Проверка инсектицида методом погружения
Смачиваемый порошок, приготовленный в соответствии с примером получения состава 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. В полученный разбавленный увлажняемый порошок погружали проростки огурца, предварительно зараженные личинками хлопковой тли, и затем высушивали на воздухе. После высушивания проростки огурцов помещали в термостатированную камеру при 25oC на 3 дня и после этого подсчитывали число погибших личинок, чтобы определить процент их гибели. Тест проводили в двух сериях. Результаты приведены в табл.2.
Пример испытаний 2. Проверка инсектицида методом введения
Смачиваемый порошок, полученный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. Полученный разбавленный смачиваемый порошок вносили в горшок, содержащий проростки огурца, предварительно зараженные личинками хлопковой тли. После введения инсектицида проростки огурца помещали в термостат при 25oC на 3 дня и затем подсчитывали число погибших личинок, чтобы определить процент гибели. Тест проводили в двух сериях. Результаты приведены в табл.3.
Пример испытания 3. Тест на проверку системного перемещения в почве, улучшающий процесс обработки
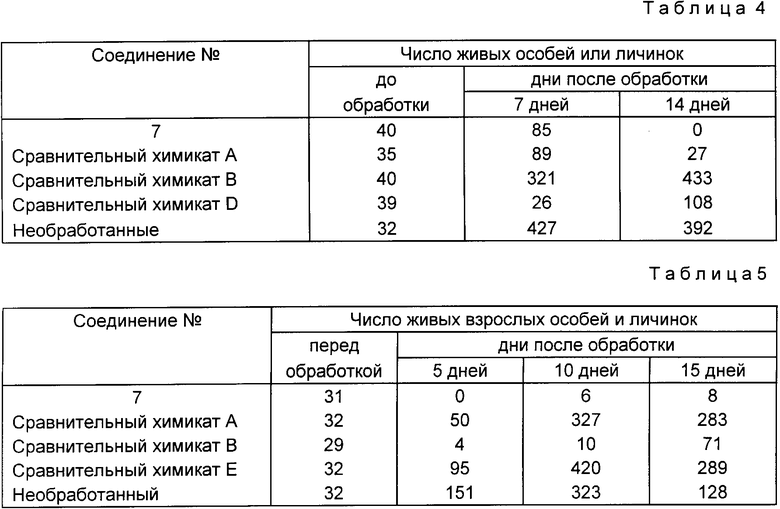
Гранулы, приготовленные в соответствии с примером приготовления 4/0,5 кг на 10 ар, наносили на стержневые корни проростков огурца, растущих в горшке и предварительно зараженных личинками тли. После такой обработки горшок помещали в теплицу, где число живых взрослых особей и личинок подсчитывали каждые 7 дней. Тест выполняли тремя параллельными сериями. Результаты показаны в табл.4.
Пример теста 4. Тест для контроля системного перемещения путем распыления на стебли и листья
Смачиваемый порошок, приготовленный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 100 ч. на 1 млн. Полученный разбавленный смачиваемый порошок распыляли только на верхнюю часть листьев сеянцев огурца, посаженных в горшок и предварительно зараженных с нижней стороны личинками тли, причем нижняя сторона не опрыскивалась. После обработки горшок помещали в теплицу и каждые 5 дней подсчитывали количество взрослых особей и живых личинок на нижней стороне. Тест проводили с тремя параллельными сериями. Результаты приведены в табл.5.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ТРИАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИНСЕКТОАКАРИЦИДНАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2114107C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ИНСЕКТИЦИДНОЕ И АКАРИЦИДНОЕ СРЕДСТВО | 1994 |
|
RU2131421C1 |
| ПРОИЗВОДНОЕ БЕНЗИЛСУЛЬФИДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПЕСТИЦИД | 1996 |
|
RU2170728C2 |
| КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ БОРЬБЫ С ГРИБКАМИ | 1993 |
|
RU2098408C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА | 1992 |
|
RU2049781C1 |
| ПРОИЗВОДНЫЕ ПИКОЛИНОВОЙ КИСЛОТЫ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, НЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1991 |
|
RU2091380C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНИЛОКСИАЛКАНАМИДОВ И ФУНГИЦИДЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА ИЛИ САДОВОДСТВА | 1997 |
|
RU2194040C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2315758C2 |
| ПРОИЗВОДНЫЕ АМИДА N-СУЛЬФОНИЛКАРБОНОВОЙ КИСЛОТЫ, ВКЛЮЧАЮЩИЕ N-СОДЕРЖАЩЕЕ 6-ЧЛЕННОЕ АРОМАТИЧЕСКОЕ КОЛЬЦО, ФУНГИЦИДНАЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С СОРНЯКАМИ И ФИТОПАТОГЕННЫМИ ГРИБКАМИ | 1993 |
|
RU2117662C1 |
Сущность изобретения: 1. Производное триазола общей формулы I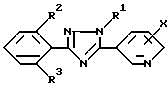
где R1 - низший алкил; R2 и R3- независимо галоид; X - хлор в 2- или 6-положении. 2. Афицидное средство на основе производного триазола общей формулы (I). 3. Способы получения производного триазола общей формулы (I) или: а/ путем взаимодействия соединения общей формулы II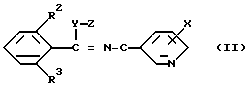
с гидразином R1-NHNH2; или б/ путем взаимодействия соединения общей формулы III: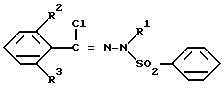
с производным бензонитрила формулы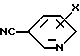
в присутствии кислоты Льюиса; или в/ путем взаимодействия соединения общей формулы IV: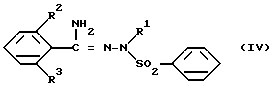
с соединением формулы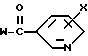
Использование - в сельском хозяйстве. 3 с. и 4 з.п.ф-лы, 5 табл.
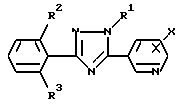
где R1 низшая алкильная группа;
R2 и R3 одинаковые или различные атомы галогенов;
X хлор, расположенный в 2-м или 6-м положении.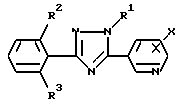
где R1 низшая алкильная группа;
R2 и R3 одинаковые или различные атомы галогенов;
X хлор, находящийся во 2-м или 6-м положении,
отличающийся тем, что включает взаимодействие соединения общей формулы II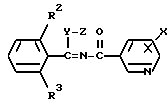
где Y сера или кислород;
Z низшая алкильная группа;
R2, R3 и X имеют указанные значения,
с производным гидразина общей формулы III
R1 NHNH2,
где R1 имеет указанное значение.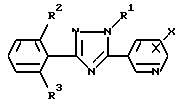
где R1 низшая алкильная группа;
R2 и R3 одинаковые или различные атомы галогенов;
X хлор, расположенный во 2-м или 6-м положении,
отличающийся тем, что включает взаимодействие соединения общей формулы VI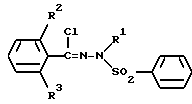
где R1, R2 и R3 имеют указанные значения,
с производным бензонитрила общей формулы VII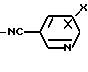
где X имеет указанное значение
в присутствии кислоты Льюиса.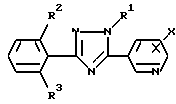
где R1 низшая алкильная группа;
R2 и R3 одинаковые или различные атомы галогена;
X хлор, находящийся во 2-м или 6-м положении,
отличающийся тем, что включает взаимодействие соединения общей формулы VIII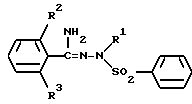
где R1, R2 и R3 имеют указанные значения,
с соединением общей формулы V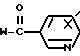
где W галоген;
X имеет указанное значение.
| EP, 0185256, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| EP, 0217552, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| 0 |
|
SU278004A1 | |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СПОСОБ СОСТАВЛЕНИЯ ЗВУКОВОЙ ЗАПИСИ | 1921 |
|
SU276A1 |
Авторы
Даты
1998-01-10—Публикация
1993-03-03—Подача