Изобретение относится к специфическим связывающим агентам, в частности к полипептидам, которые содержат аминокислотные последовательности, специфически связывающиеся с другими белковыми и небелковыми веществами. В наибольшей степени изобретение относится к получению указанных специфичных связывающих агентов методами генной инженерии.
Структура антител
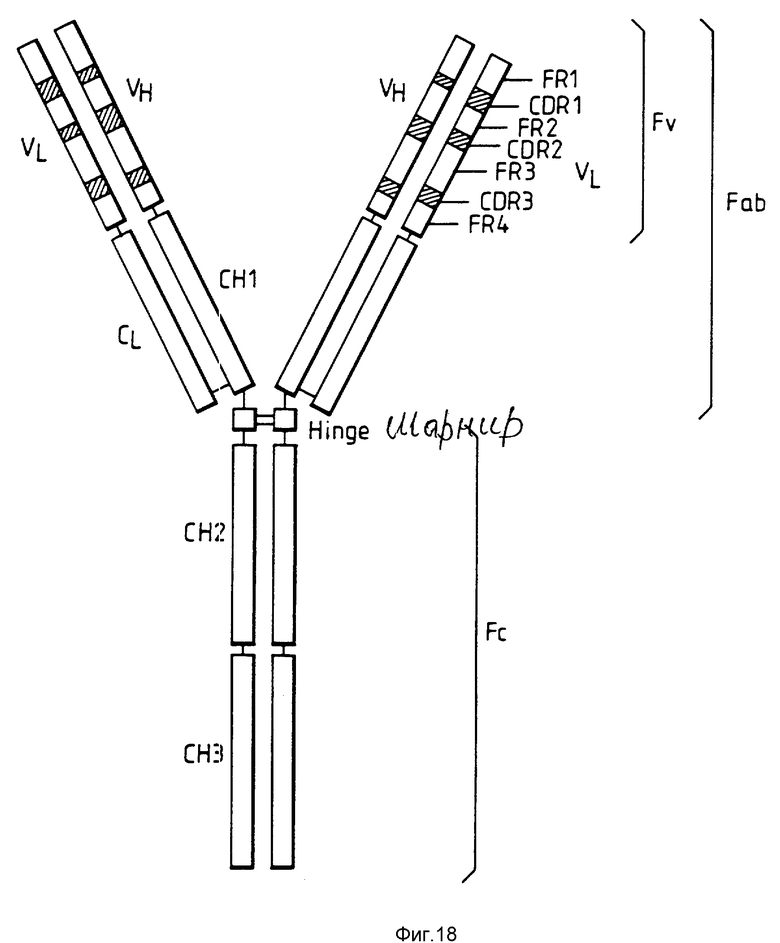
Природные молекулы антител состоят из двух идентичных полипептидов с тяжелой цепью и двух идентичных полипептидов с легкой цепью. На фиг. 18 схематически представлена типичная структура антитела, относящегося к классу IgG. N-концевые домены всех цепей отличаются составом аминокислотных последовательностей и потому именуются вариабельными участками (V-области). Эти участки тяжелых (VH) и легких (VL) цепей, ассоциируясь, образуют антиген-связывающие сайты. Модуль, возникающий в результате объединения VH и VL доменов, обозначают как FV (вариабельный фрагмент) антитела. С-концевые участки тяжелых и легких цепей более консервативны в отношении аминокислотной последовательности и потому называются константными областями. В тяжелых цепях константные области включают несколько доменов. Например, тяжелая цепь гамма-изотипа (IgG) имеет три домена (CH1, CH2 и CH3), а также шарнирный элемент, связывающий CH1 и CH2 домены. Шарнирные элементы двух тяжелых цепей ковалентно связаны дисульфидными мостиками. Легкие цепи содержат по одному константному участку, который расположен напротив домена CH1. В молекуле антитела константные области выполняют эффекторные функции, в частности обеспечивают лизис комплемента и определяемую антителом клеточную цитотоксичность (АДСС). Классическое переваривание антитела протеолитическим ферментом папаином приводит к образованию трех фрагментов. Один из них содержит CH2 и CH3 домены и легко кристаллизуется. Он получил обозначение Fc фрагмент. Два других фрагмента сокращенно обозначаются символом Fab (антиген-связывающие фрагменты). Они совершенно идентичны и содержат полную легкую цепь в комбинации с VH и CH1 доменом. При переваривании пепсином протеолитическое расщепление сопровождается образованием структуры, в которой два фрагмента Fab остаются связанными между собой через шарнирный элемент, давая начало фрагменту (Fab)2. На генетическом уровне каждый из доменов представлен отдельным экзоном.
Вариабельные участки, в свою очередь, содержат по три группы сверхизменчивых остатков в составе более консервативных последовательностей. Эти сверхизменчивые остатки взаимодействуют с антигеном и известны под названием определяющих комплементарность областей (CDR). Более консервативные последовательности, в свою очередь, называются структурными компонентами (FR) (см. Kabat et al, 1987). Рентгенографическое исследование антител показало, что CDR образуют петли, которые выступают из верхней части молекулы, тогда как FR образуют β- структурную основу.
Модифицированные антитела
Один из аспектов изобретения относится к так называемым "измененным" или "модифицированным" человеческим антителам, именно к иммуноглобулинам, которые характеризуются наличием свойственных человеку константных областей и структурных компонентов, но имеют обусловливающие комплементарность участки (CDR), которые свойственны иммуноглобулинам иного происхождения или соответствующим фрагментам модифицированных антител. Эта разновидность измененных антител может быть определена как "химерная" структура.
Общие принципы получения таких видоизмененных человеческих антител в настоящее время хорошо известны. Можно сослаться на работы Jones et al.(1986), Riechmann et al (1988), Verhoeyen et al (1989) и Европейскую патентную заявку N 239400 (Winter). К настоящему описанию прилагается исчерпывающий перечень литературы по этому вопросу.
Видоизмененные человеческие антитела типа "химер" и их фрагменты имеют особенно большое значение для диагностики in vivo и для лечения разнообразных расстройств у людей, поскольку человеческие иммуноглобулины менее других способны индуцировать нежелательные реакции при введении больным, а обусловливаемая CDR специфичность может быть усилена в животных-хозяевах, например в мышах, от которых антитела, обладающие избирательной специфичностью, получать легче. Гены вариабельных областей можно клонировать из иных, нежели человек, организмов, а CDR могут быть включены в структурные компоненты вариабельных областей человеческих антител методами генной инженерии. Для выполнения этой задачи необходимо идентифицировать и секвенировать хотя бы CDR в составе антител избранных организмов (желательно определить полную последовательность вариабельных участков), чтобы выявить потенциально значимые взаимодействия между структурными компонентами и участками, обусловливающими комплементарность.
Один из аспектов изобретения относится к получаемому методом рекомбинантных ДНК полипептиду со специфической связывающей активностью в отношении щелочной фосфатазы женской плаценты (PLAP).
Изобретение касается, в частности, модифицированных человеческих антител или фрагментов модифицированных человеческих антител, обладающих специфичностью в отношении щелочной фосфатазы женской плаценты и содержащих один или несколько CDR, как показано на фиг. 1 и 2. Химерные антитела или их фрагменты согласно изобретению содержат, в частности, все три CDR в составе структурных компонентов вариабельных участков тяжелых цепей (см. фиг. 1). В качестве альтернативного или дополнительного варианта модифицированные антитела или их фрагменты согласно изобретению содержат все три CDR, показанные на фиг. 2, в структурном компоненте вариабельных участков легкой цепи человеческих антител.
Еще один аспект изобретения относится к антителам человека или их фрагментам, имеющим в своем составе белковую последовательность, показанную на фиг. 15 и/или 16.
Важным аспектом изобретения является также последовательность ДНК, приведенная на фиг. 15 и/или 16 и вектор экспрессии, содержащий последовательность ДНК, которая кодирует одну или несколько белковых последовательностей, обозначенных на фиг. 1 и/или 2 символом CDR.
Изобретение раскрывает стабильную линию клеток-хозяев, содержащих инородный ген, который обеспечивает образование этими клетками специфического связывающего агента. Такая стабильная клеточная линия может содержать инородный ген, кодирующий по крайней мере одну из аминокислотных последовательностей, обозначенных символом CDR на фиг. 1 и/или фиг. 2, вместе с белковым структурным компонентом, который в случае экспрессии указанной аминокислотной последовательности обеспечивает ее функционирование в качестве CDR, специфичного по отношению к PLAP.
Кроме того, настоящее изобретение касается непрерывной клеточной линии млекопитающих или дрожжей, или других эукариот и прокариот (например, бактерий), продуцирующих модифицированные антитела или фрагменты модифицированных антител согласно данному изобретению.
Важный аспект изобретения составляют химерные антитела, специфичность которых эквивалентна специфичности гамма-1, каппа антител к PLAP, секретируемых клеточной линией Н17Е2 мышиной гибридомы.
Предметом изобретения являются также две новые плазмиды: prgptHu2VHPLAP-HulgG1 иprVreoHuVkPLAP-Huck, которые можно использовать для получения модифицированных человеческих антител.
Эти плазмиды локализованы в новых штаммах E.coli: соответственно NСТС 12389 и NCTC 12390.
Изобретение имеет также следующие аспекты.
а) Последовательность ДНК, кодирующая вариабельную область тяжелой цепи химерных человеческих антител, специфичную по отношению к щелочной фосфатазе женской плаценты, и содержащаяся в E.coli NСТС 12389.
б) Последовательность ДНК, кодирующая вариабельный участок легкой цепи, специфичный по отношению к щелочной фосфатазе женской плаценты, и содержащаяся в E.coli NСТС 12390.
в) Вариабельная область тяжелой цепи химерных антител, специфичная по отношению к щелочной фосфатазе женской плаценты, которая продуцируется в процессе экспрессии вектора, имеющегося в E.coli NCTC 12389.
г) Вариабельная область легкой цепи химерных антител, специфичная по отношению к щелочной фосфатазе женской плаценты, которая продуцируется вектором экспрессии, имеющимся в E.coli NСТС 12390.
Таким образом, характерным аспектом настоящего изобретения являются видоизмененные человеческие антитела, обладающие специфичностью по отношению к PLAP и содержащие комбинацию CDR (которая может быть, в частности, клонирована из мышиных анти-PLAP иммуноглобулинов) с аминокислотными последовательностями, обозначенными на фиг. 1 и 2 символами CDR1, CDR2 и CDR3. Эти последовательности соответствуют вариабельному участку тяжелой цепи (VН) и вариабельному участку легкой цепи (Vк) клонированных и секвенированных мышиных моноклональных антител к PLAP. В случае интактных антител или их фрагментов, содержащих по крайней мере один вариабельный участок легкой цепи и хотя бы один вариабельный участок тяжелой цепи, модифицированные антитела или их фрагменты должны предпочтительно включать все три CDR из других, нежели человеческий, источников. Для обеспечения максимальной эффективности связывания CDR должны предпочтительно размещаться по отношению один к другому так же, как в исходных антителах животных (например, VН CDR должен входить в состав структурного компонента человеческой VН), и в той последовательности, в которой они естественно находятся в антителах животных.
Как известно, последовательности CDR и окружающие их последовательности структурных компонентов могут претерпевать слабые изменения без существенной потери специфической связывающей активности. Такие небольшие изменения могут иметь место либо на генетическом уровне, либо на уровне аминокислотной последовательности, либо на обоих уровнях. В соответствии с этим изобретение охватывает и антитела, функционально эквивалентные описанным здесь антителам с точно определенной генетической или аминокислотной последовательностью.
Изобретение может использоваться также для получения биспецифичных антител, содержащих участки Fab с разной специфичностью, причем специфичность одного из этих участков обусловлена вариабельной частью модифицированного человеческого антитела с одним или несколькими CDR, как показано на фиг. 1 и 2.
В равной степени изобретение может быть полезным при получении так называемых одноцепочечных антител (например, описанных в Европейской патентной заявке Genex 281604); антител, сцепленных с полисахаридами (см. Европейскую патентную заявку Hubriech 315456) и других модифицированных антител.
Для этих целей пригодны любые константные участки человеческих антител, например типа гамма-1, 2, 3 или 4.
В качестве фрагментов антител, сохраняющих полезные связывающие свойства, можно назвать фрагменты (Fab)2, Fab, FV, Vк или VН. Их можно получать из интактных модифицированных антител, например посредством переваривания последних протеазами, или конструировать методами генной инженерии.
Практическое применение изобретения
Важным аспектом изобретения являются вышеописанные химерные антитела к PLAP, связанные с или включенные в состав агентов, которые замедляют или останавливают рост раковых клеток, а также связанные с или включенные в состав маркерных соединений, поддающихся идентификации после введения в человеческий организм. Изобретение может быть также использовано для создания композиций для инъекций, в состав которых входят такие комбинации вместе с фармацевтически приемлемыми носителями (физиологическим раствором, липосомами или наполнителями). Изобретение, кроме того, предусматривает применение вышеописанных антител к PLAP или при терапии злокачественных новообразований или диагностике с использованием контрастных веществ и радиоактивных изотопов. Изобретение также дает возможность применения таких антител при изготовлении лекарственных препаратов для клинического использования с целью снижения тяжести рака у человека или при изготовлении диагностических композиций, применяемых in vivo.
Участок Fc антител включается в процессы и механизмы, имеющие место в человеческом организме, вызывая, в частности, лизис комплемента или зависимую от антител цитотоксичность. Кроме того, его можно использовать для ингибирования злокачественного роста клеток. В этом случае не требуется связывания с антителами дополнительного реагента.
К числу агентов, подавляющих злокачественный рост клеток, относятся радиоизотопы (в частности иттрий-90 и йод-131); такие лекарственные средства, как метотрексат; токсины типа рицина или их фрагменты, а также ферменты, которые могут, например, превращать неактивное соединение в активное в местах связывания антител.
В качестве агентов, используемых в диагностических целях, можно назвать радиоизотопы, генерирующие гамма-излучение (например индий-III и технеций-99); радиоизотопы, излучающие позитроны (медь-64), а также такие нерадиоактивные препараты, как барий, которые используют в качестве контрастного материала при рентгенографических исследованиях, или гадолиний, применяемый при сканировании с использованием ядерного или электронного резонанса.
Для связывания металла (в частности, радиоактивного) со специфическим связывающим агентом согласно данному изобретению может потребоваться хелат или сопрягающий фактор. В настоящее время для этой цели предложено множество хелирующих агентов, среди которых можно, в частности, упомянуть соединения, описанные в патентах США NN 4824986, 4831175, 4923985 и 4622420. В свою очередь, способы применения этих агентов описаны в патентах США N 4454106 и N 4722892, а также в работах Hoi et al (1988), Me Call et al (1990), Peshpande et al (1990) и Meares et al (1990).
Европейский патент N 35265 описывает применение меченных радиоизотопами антител и их фрагментов при диагностике и лечении рака у людей. Может оказаться полезным использование обладающих специфическим действием на раковые клетки меченых антител или их фрагментов в сочетании с неспецифическими агентами, меченными различными радиоизотопами, для получения контрастного фона при так называемой дигитальной лучевой диагностике.
Реагенты на основе антител по изобретению могут найти применение для диагностики (например посредством анализа сывороток или лучевыми методами) и/или лечения PLAP продуцирующих форм рака, таких как рак легких, яичников и толстой кишки, или сопровождающихся выделением жидкостей (эксудат в плевральной полости).
Получение модифицированных антител
Фрагменты вариабельных участков VН и V1, которые согласно общепринятой практике (Kabat, 1987) обозначают как CDR, являются не единственными структурами, которые подлежат переносу из моноклональных антител животных. В некоторых случаях повышение эффективности антител, связанное с их специфичностью и/или сродством, может быть достигнуто посредством сохранения в модифицированных человеческих антителах структурных компонентов, принадлежащих антителам животных. Задача при этом состоит в сохранении трехмерной белковой структуры, ассоциированной с CDR, существование которой обеспечивается благодаря контактам с остатками структурных компонентов.
Отправной точкой для получения химерных антител согласно настоящему изобретению обычно служит клетка (предпочтительно принадлежащая к непрерывной клеточной линии), источником которой являются животные (например, мыши) и в которой возможна экспрессия антител, специфичных по отношению к человеческой PLAP. В качестве источника такой клеточной линии можно, в частности, использовать гибридому, получаемую технологией моноклональных антител. Желательно, чтобы подлежащие экспрессии антитела обладали высокими сродством и специфичностью к PLAP, поскольку во время переноса этих признаков в человеческие антитела посредством процедур согласно данному изобретению можно ожидать определенных потерь сродства и/или специфичности. Используя в качестве исходных антител антитела, обладающие высокими сродством и специфичностью, можно с большой долей вероятности ожидать, что конечные химерные антитела будут также обладать высокой связывающей активностью.
Следующей стадией является клонирование кДНК из клеток, в которых происходит экспрессия антител того или иного вида животных, секвенирование и идентификация генов, кодирующих вариабельные области, в том числе последовательностей, которые кодируют CDR. В настоящее время эти процедуры считаются рутинными, но тем не менее остаются достаточно трудоемкими.
Если планируется получение модифицированных полных человеческих антител или по крайней мере фрагментов таких антител, содержащих как тяжелые, так и легкие изменчивые домены, необходимо провести секвенирование кДНК, связанных с каждым из этих доменов.
После завершения анализа последовательности или последовательностей соответствующих ДНК требуется получить один или несколько реплицирующихся векторов экспрессии, которые содержат последовательность ДНК, кодирующую по крайней мере один вариабельный участок антитела. Этот домен должен включать участки структурных компонентов человеческих антител вместе с одним или несколькими CDR из антител к PLAP иного происхождения. Вектор должен включать соответствующие регуляторные последовательности, которые способны обеспечить эффективную транскрипцию и трансляцию гена, в частности промотор и лидирующую последовательность, функционально связанные с последовательностью, кодирующей вариабельный домен. Типичная процедура получения химерных антител согласно изобретению требует получения двух векторов экспрессии, один из которых содержит последовательность ДНК для модифицированной легкой цепи человеческого антитела, а другой последовательность ДНК для модифицированной тяжелой цепи. Векторы экспрессии должны обладать способностью трансформировать данную клеточную линию, в которой происходит образование модифицированных антител или их фрагментов. В качестве такой линии можно использовать, например, стабильную линию клеток непродуктивной миеломы (NSO или SP 2-0). Такие клеточные линии доступны по обычным коммерческим каналам. В качестве альтернативы допустимо использование бактериальной системы (в частности, Е. coli). Таким образом, на последних стадиях описанной процедуры осуществляется трансформация избранных клеточных линий или организмов с использованием вектора или векторов экспрессии, с последующим культивированием трансформированных клеток или организмов для получения модифицированных человеческих антител или их фрагментов.
Ниже подробно описан способ получения необходимых векторов экспрессии, однако это описание следует рассматривать исключительно как иллюстрацию предлагаемого изобретения. В настоящее время манипуляции с ДНК-содержащим материалом доступны любой хорошо оснащенной лаборатории, а необходимые процедуры могут быть легко выполнены квалифицированными специалистами. Большинство геномных и кДНК библиотек, плазмид, рестриктаз, разнообразных реагентов и сред, необходимых для этих манипуляций, поступает на рынок от поставщиков соответствующих лабораторных материалов. Например, геномные и кДНК библиотеки выпускаются компанией Клонтех Лабораториз. Описанные в нижеследующих примерах стадии работы следует рассматривать исключительно как возможные варианты. Реализация изобретения не зависит в сколько-нибудь существенной степени от доступности того или иного или нескольких исходных материалов. На практике имеется очень широкий выбор таких материалов, и описанные методики можно адаптировать, опираясь на имеющийся опыт и применяя наиболее доступные из имеющихся материалов. Это относится, в частности, к плазмидам, которые в настоящее время столь широко используются в лабораторной практике, что их можно считать самыми обычными объектами экспериментальной работы.
На фиг. 1 показана последовательность кДНК, кодирующая вариабельный участок тяжелой цепи мышиных антител, специфичных по отношению к PLAP. Показаны три классических участка CDR, а также аминокислотная последовательность, соответствующая кодирующей последовательности кДНК.
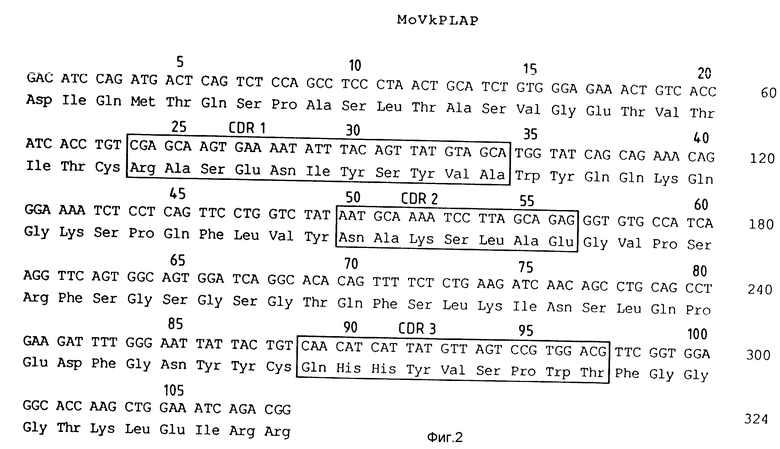
Фиг. 2 представляет последовательность кДНК, кодирующую вариабельный участок легкой цепи мышиных антител, специфичных по отношению к PLAP.
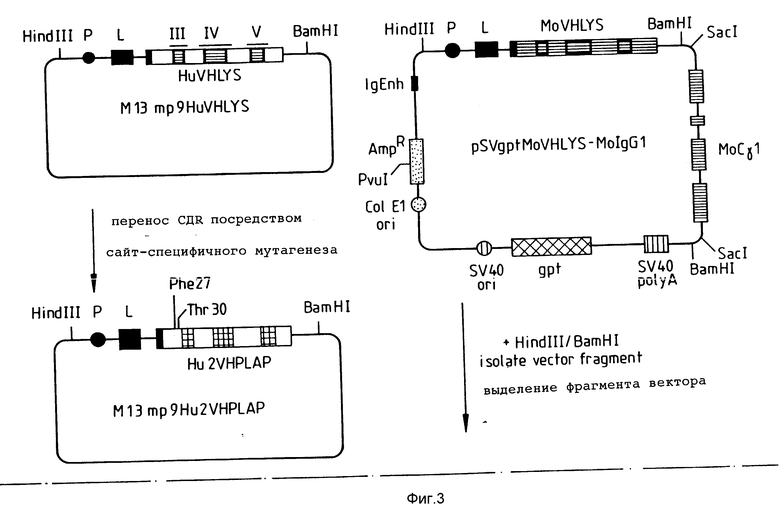
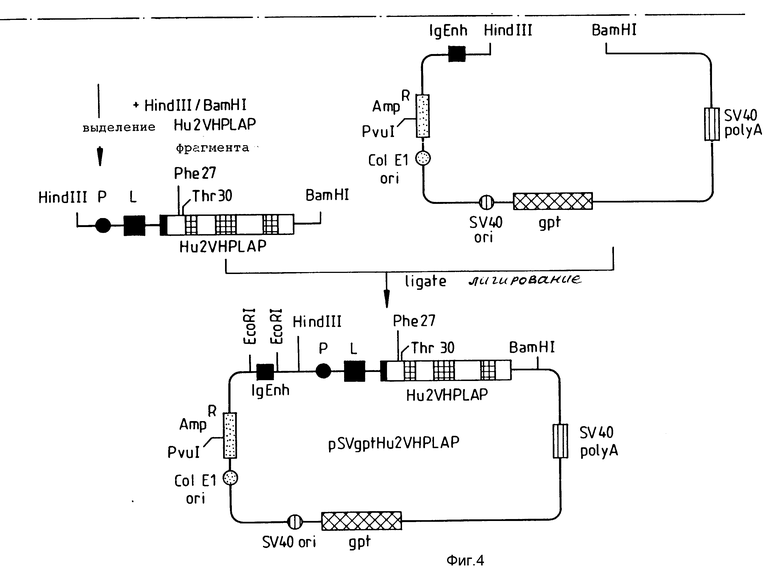
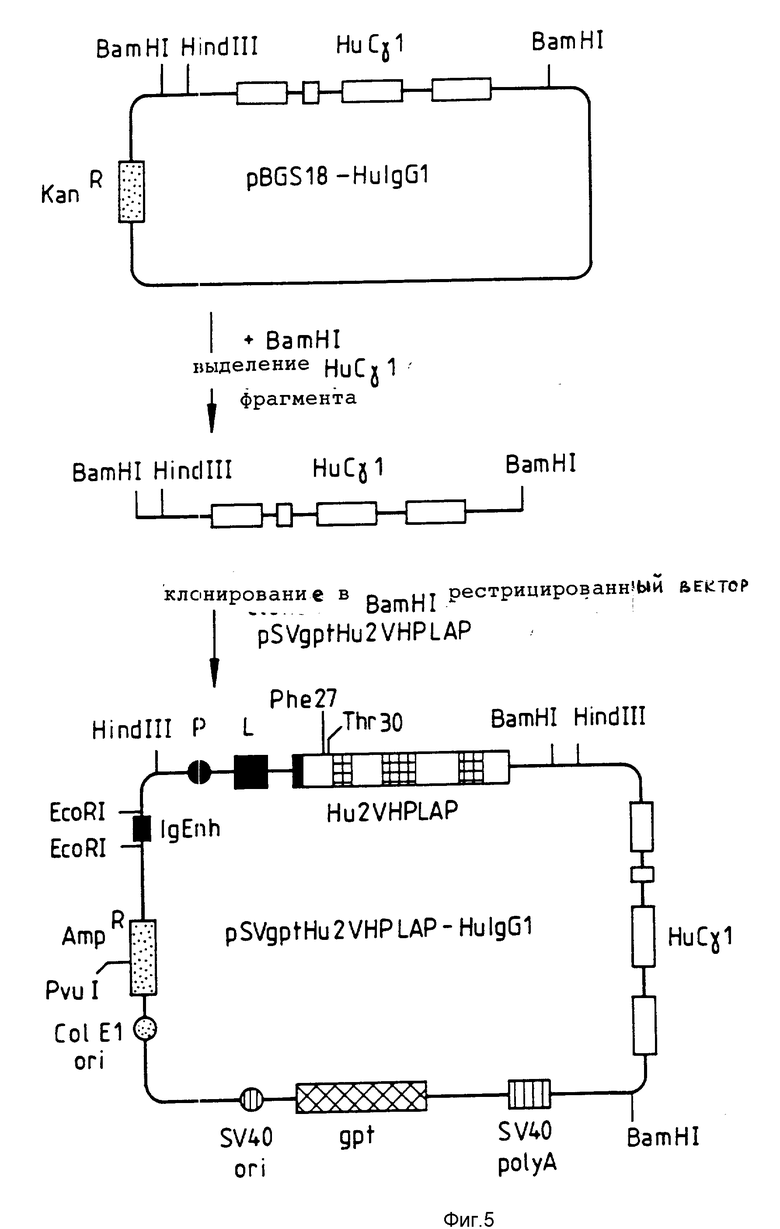
Фиг. 3 5 в совокупности иллюстрируют способ получения вектора экспрессии, кодирующего модифицированную тяжелую цепь человеческих антител, содержащую участки CDR, которые показаны на фиг. 1.
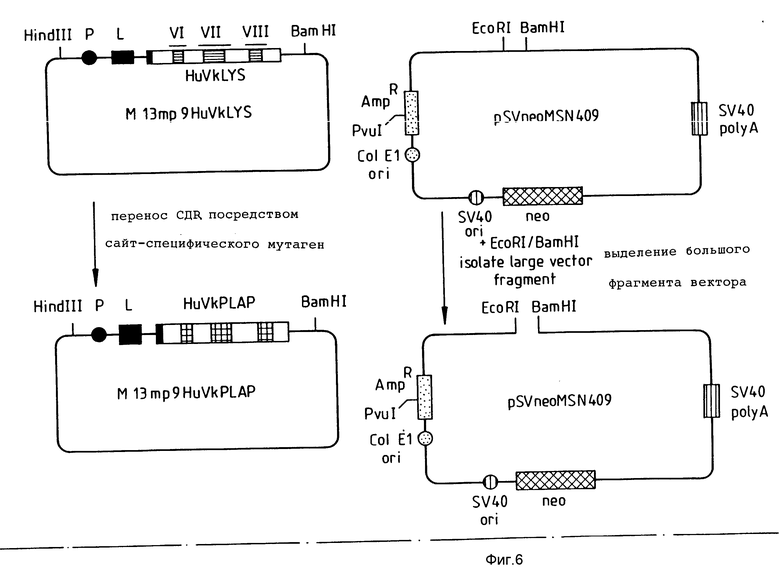
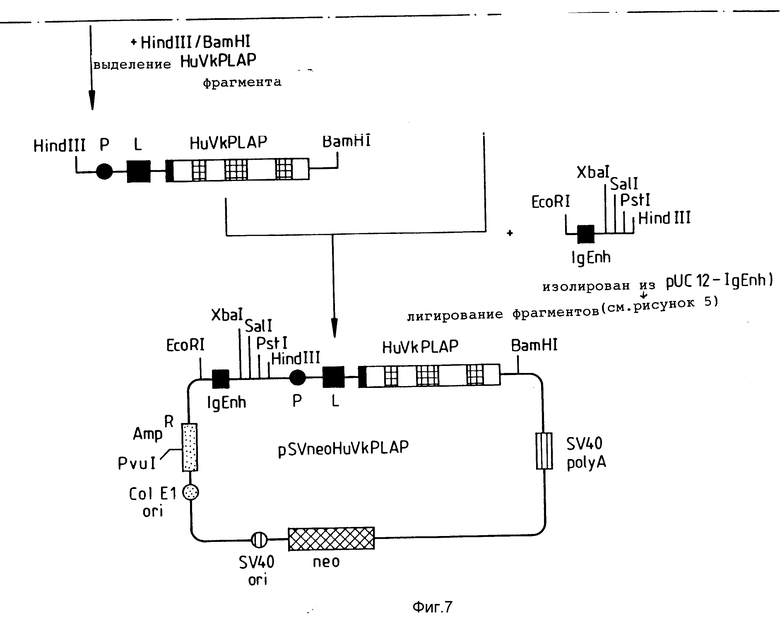
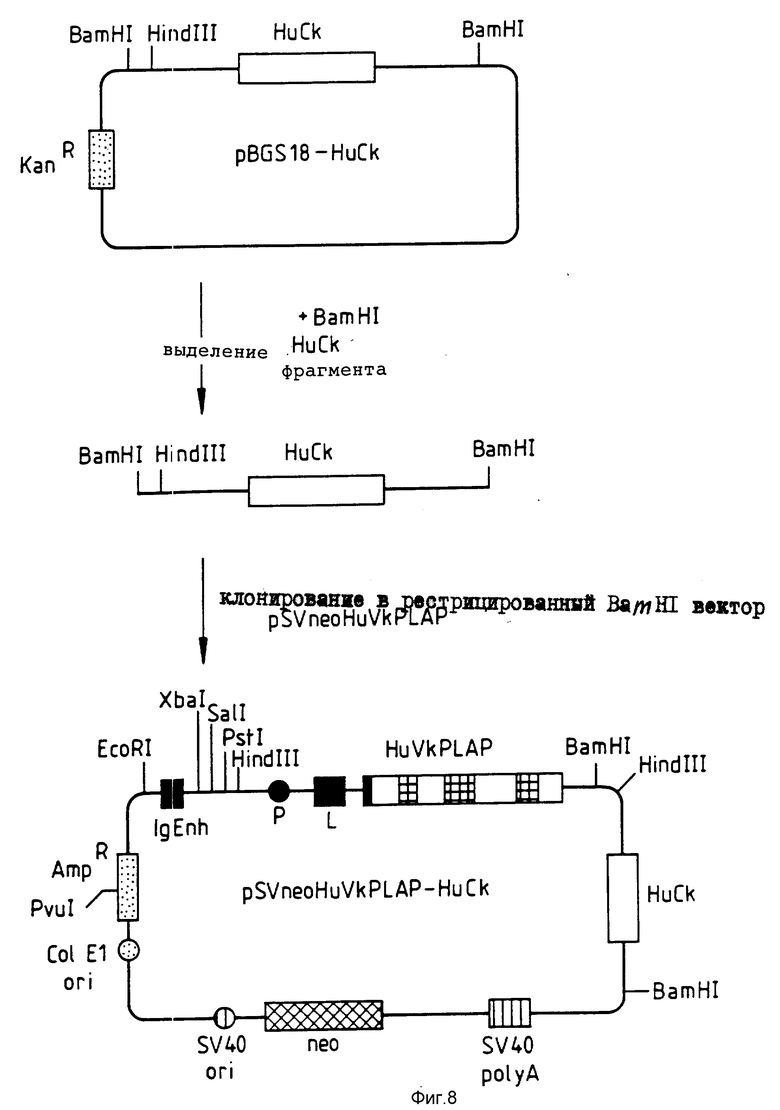
Фиг. 6 8 в совокупности иллюстрируют аналогичный способ трансформации с целью получения вектора экспрессии, кодирующего модифицированную легкую цепь человеческих антител, которая содержит CDR, показанные на фиг. 1.
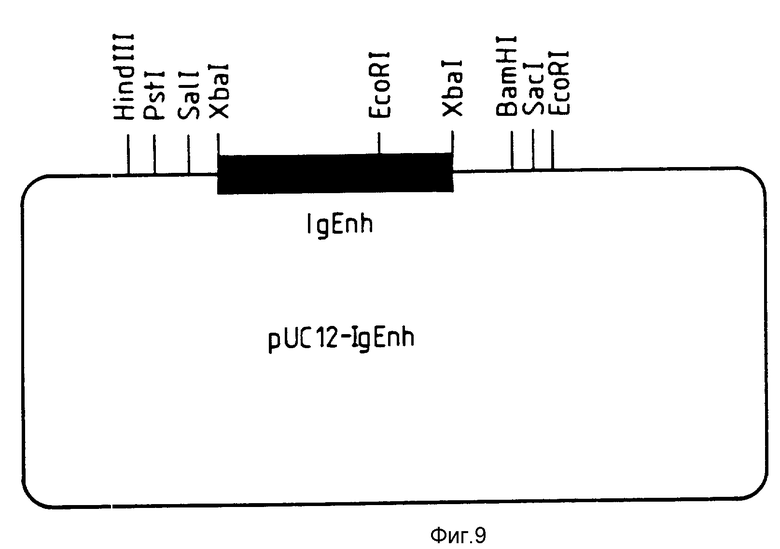
Фиг. 9 показывает плазмиду pU 12-IgFnh которая содержит ген-усилитель, используемый в процедуре согласно фиг. 6 -8.
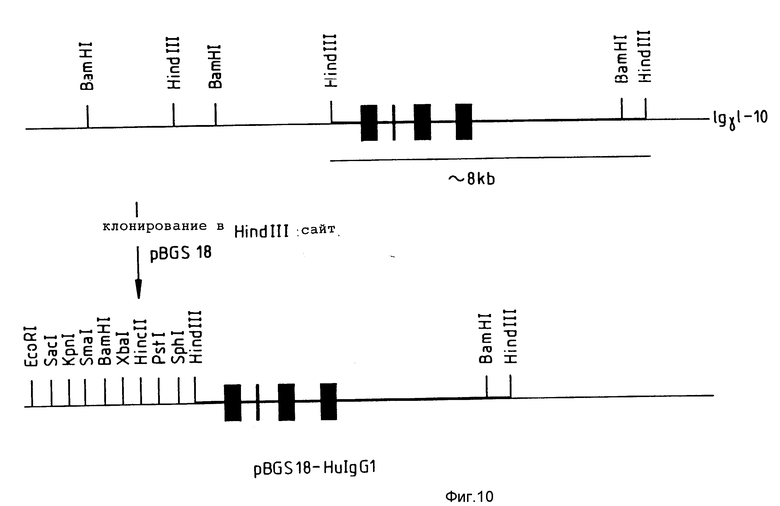
Фиг. 10 иллюстрирует источник плазмиды pBgS18-HulgGt, используемой при трансформации, как показано на фиг. 5.
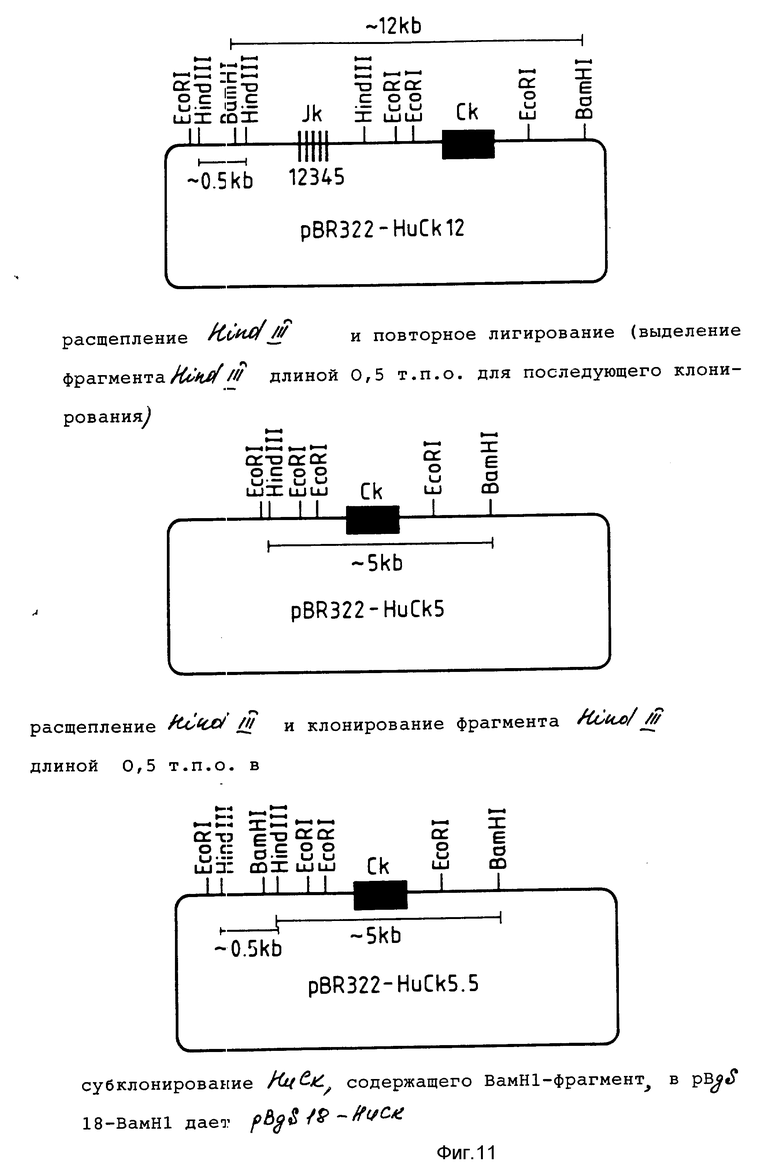
Фиг. 11 иллюстрирует источник плазмиды pBgS18-HucK, используемой при трансформации, как показано на фиг. 8.
На фиг. 12 представлены две синтетические нуклеотидные последовательности 1 и 11, используемые при клонировании последовательностей кДНК, которые показаны на фиг. 1 и 2.
На фиг. 13, 14 представлены шесть синтетических олигонуклеотидных последовательностей (с III по VIII), используемых при трансформации, как показано на фиг. 3 8.
На фиг. 15, 16 представлены последовательность кДНК и аминокислотная последовательность конечных вариабельных участков соответственно тяжелой и легкой цепи химерных антител.
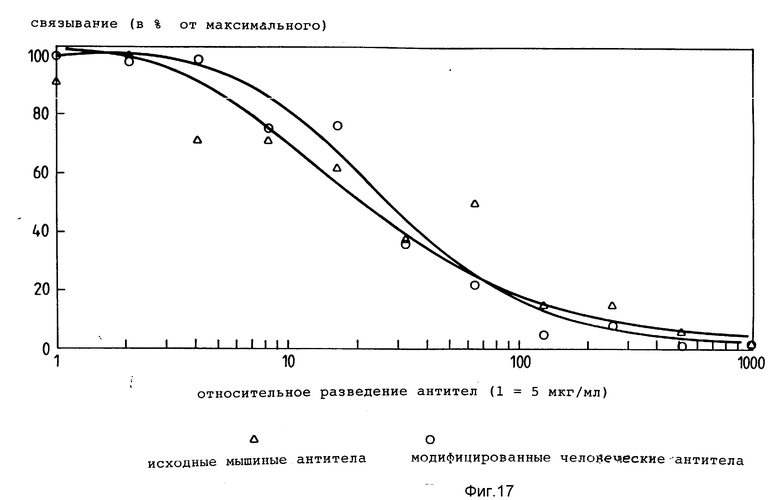
Фиг. 17 в графической форме иллюстрирует относительную удельную связывающую активность конечных модифицированных человеческих антител к PLAP.
На фиг. 18 представлена схематическая структура типичной молекулы антитела (иммуноглобулина).
Экспериментальные подходы к практической реализации изобретения сами по себе не представляют ничего необычного с методической точки зрения. Они предполагают применение обычных методов клонирования и мутагенеза, которые описаны, например, в работах Verhoeyen et al (1988), Riechmann et al (1988), или в Европейской патентной заявке N 239400 (Winter). С другой стороны, вариабельные области модифицированных человеческих антител могут быть синтезированы in virto (см. Jones et al 1986), при условии, что в деталях известна необходимая для этой цели последовательность ДНК (на прилагаемых к настоящему описанию чертежах показана последовательность, определяющая специфичность антител к PLAP). Лабораторное оборудование и реактивы для синтеза длинных олигонуклеотидных цепей легко доступны. Наряду с постоянным совершенствованием методических подходов, это позволяет в практических условиях синтезировать все более длинные последовательности.
Имеются также подробные руководства по использованию рекомбинантной технологии в лабораторных условиях (см. например, "Molecular cloning", "Sambrook" с соавторами, 1989).
С помощью данного изобретения в структурные компоненты человеческих антител были внедрены связывающие антиген участки мышиных антител к PLAP. Полученные в результате химерные антитела (обозначенные как Hu2 PLAP) обладали такими же связывающими свойствами, как и исходные мышиные антитела.
Такие модифицированные антитела можно использовать для диагностики in vivo) и лечения рака у людей (в частности, в случаях рака яичников или семиномы). Ожидается, что их применение по крайней мере частично снимет остроту проблемы иммунореактивности у больных, которая нередко возникает при введении им антител животных. Аналогичным преимуществом обладают модифицированные антитела САМРАТН-1, которые описаны Hale с соавторами (1988).
Методы.
а) Клонирование и секвенирование генов вариабельных участков у мышей.
Информационную РНК выделяли из линии Н17Е2 мышиной гибридомы, которая секретирует гамма-1, каппа антитела к PLAP (см. Travers et al 1984). Первую цепь кДНК синтезировали, используя в качестве затравки олигонуклеотиды I и II, комплементарные 5'-концам соответственно СН1 и Ск экзонов (см. фиг. 12). Вторую цепь кДНК получали, как описано Gubler и Hoffmann (1983).
Обработанные киназой линкеры EcoR 1 лигировали с двуцепочечной кДНК, которую предварительно подвергали воздействию метилазы EcoR I для защиты потенциальных внутренних сайтов EcoR I. После этого производили клонирование в ЕсоR I-сайте плазмиды (фиг. 13, 14) (Vicira et al 1982) и трансформацию штамма Тg2.Е.соli (Gibson 1984).
Колонии, содержавшие гены, кодирующие VН мышиных антител к PLAP (MoVH PLAP) и Vк мышиных антител к PLAP (MoVK PLAP), идентифицировали с помощью гибридизации с двумя зондами, которые представляли собой меченые P32 однонитевые к ДНК анти-PLAP VH и Vk. Положительные клоны характеризовали, получая плазмиды, с последующим перевариванием EcoR I и анализом в 1,5% агарозном геле. Полноразмерные вставки длиной примерно 450 п.о. субклонировали в сайте EcoR I М13мр18 (Norrander et al, 1983). Это приводило к формированию клонов со вставками обеих ориентаций, что облегчало определение нуклеотидной последовательности всей вставки методом дидезокси-"обрыва" цепи (Sanger et al 1977).
На фиг. 1 и 2 показаны нуклеотидные последовательности, кодирующие вариабельные участки полностью сформированных генов MoVH PLAP и MoVk PLAP и соответствующие им аминокислотные последовательности. Вставки длиной 450 п. о. включали сигнальную последовательность, нетранслируемую 5'-последовательность и линкеры (на чертежах не показаны).
б) Перенос СDR мышиных антител к PLAP на структурные компоненты человеческих антител.
Общие методические подходы к осуществлению такого переноса хорошо описаны в работах Jones et al (1986), Verhoeyen et al (1988), Ricchmann et al (1988) и в Европейской патентной заявке N 239400 (Winter).
В процедуре модификации использовали, в основном, М13мр9 HuVHLVS (Verhocyen et al, 1988) и М13мр9НuVKIVS (Ricchmann et al 1988), которые содержат соответственно структурные компоненты вариабельного участка тяжелой цепи человеческого "NEW" и вариабельного участка легкой цепи человеческого "RE1". Оба эти типа человеческих антител подробно охарактеризованы и соответствующие результаты опубликованы (Saul 1978, Epp et al 1974).
В этих структурах (фиг. З и 6) CDR были заменены посредством сайт-направленного мутагенеза на олигонуклеотиды, которые кодируют CDR антител к PLAP, фланкированные по меньшей мере 12 нуклеотидами на каждом конце, кодирующем соответствующие структурные компоненты человеческих антител. Эти олигонуклеотиды представлены на фиг. 13, 14 последовательности, соответствующие CDR подчеркнуты).
В данном случае мы сочли целесообразным сохранить аминокислотные остатки Phe 27 и Thr 30 мышиных VHPLAP в VH-домене модифицированных человеческих антител к PLAP. В олигонуклеотиде III с 24 нуклеотидами, фланкирующими 5'-конец CDR I, мышиные кодоны для Phe 27 и Thr 30 выделены курсивом (см. фиг. 13, 14).
Мутагенез осуществляли с помощью методики, описанной Ricchmann et al (1988). Полученные вариабельные участки обозначали как Hu2VHPLAP и HuVkPLAP (см. фиг. 15 и 16).
в) Сборка модифицированных генов человеческих антител в векторах экспрессии.
На следующей стадии работы использовали энхансер Jg Enh тяжелой цепи мышиных антител, описанный Neuberger et al (1983). При этом энхансер локализовался во фрагменте Хваl длиной 1 т.п.о. плазмиды pSV-VmI. Для сообщения активности энхансера оказалось достаточно субфрагмента Хbа1 длиной 700 пар оснований, обозначенного как Хbа1/ЕсоR I.
Модифицированные человеческие гены, полученные как описано в разделе в), вычленяли из векторов М13 в форме фрагментов Hindu-BAMHI. Гены вариабельных участков тяжелой цепи клонировали в векторе на основе pSV2gPt (Molligan et al 1981), а гены вариабельных участков легкой цепи в векторе на основе pSV2neo (Southern et al, 1981). Оба вектора содержали энхансер тяжелой цепи иммуноглобулина (Jg Enh). В векторе pSV2Pt для экспрессии антител (см. фиг. 3 5) фрагмент Хbа1/EcoR I, содержащий энхансер, клонировали в уникальном сайте EcoR I вектора pSV2gPt (после лигирования линкеров EcoR I с заполненным концом Хbа1-фрагмента). В качестве источника производного вектора pSV2Pt, содержащего энхансер Jg Enh, использовали вектор pSVgptMoVHLVS (Verhoeyen et al 1988).
В векторе pSV neo для экспрессии антител (см. фиг. 6 8) фрагмент, содержащий ген-усилитель Хbа1 длиной 1 т. п. о, сначала клонировали в pU С12 (Vicira et al, 1982), получая плазмиду pU С12-Ig Enh (см. фиг. 9). После этого из энхансера вырезали фрагмент EcoR I/Hind III длиной 700 пар оснований (ориентация энхансера не имела значения), который клонировали в векторе на основе pSV2 neo (показанный на фиг. 6 вектор pSV neo MSN 409). Последний получали удалением сайта Hind III из pSV neo. В качестве альтернативного вектора для экспрессии легкой цепи можно использовать pSV2 gpt, поскольку на практике нет необходимости в неоселекции.
Ген Hu2VHPLAP присоединяли к g1 -константной области (Takahashi et al 1982), после чего клонировали в сайте Hind III плазмиды pBgS 18 в форме фрагмента Hind III длиной 8 т.п.о. (Spratt et al 1986), а затем в векторе экспрессии pVS2gpt в виде фрагмента Bam HI (см. фиг. 3 и 10). Следует отметить ошибку в фиг. 1 работа Takahashi et al 1982): последние (3') два сайта BamH1 находятся перед Hind III, а не наоборот. Справедливость этого замечания подтверждает Flanagan et al (1982).
Ген Hu Vk PLAP присоединяли к Скаппа константной области человека (Hicter et al 1980) и клонировали в форме фрагмента Bam HI (см. фиг. 8 и 11). Источник человеческого Ск (см. фиг. 11) описан Hicter et al (1980). Фрагмент Bam HI длиной 12 т. п.о. из эмбриональной ДНК (клонированный в векторной системе гамма-С 28) субклонировали в сайте Bam HI плазмиды рВР322.
г) Экспрессия в клетках миеломы.
Контрансфекцию плазмид экспрессии pSVgptHu2VHPLAP и pSV neo HuVkPLAP-HuCk (фиг. 5 и 8) в клетки миеломы NS осуществляли методом электропорации после перевода в линейную форму с помощью Pvu I (Potter et al 1984). Трансфектомы отбирали в среде, содержащей микофеноловую кислоту, с целью получения клеток, в которых возможна экспрессия продуктов гена gpt. Скрининг клеток на продукцию антител и анти-PLAP активность осуществляли с помощью метода FLSA.
Положительные клоны подвергали субклонированию в условиях ограниченного разведения, чистые клоны снова испытывали на анти-PLAP активность и наиболее продуктивные из них культивировали в бессывороточной среде для получения антител.
д) Связывающая способность химерных антител.
Для целей практического использования модифицированные человеческие антитела должны обладать достаточно высокой связывающей способностью. В случае, если исходные антитела достаточно эффективны, можно мириться с потерей известной доли активности в процессе модификации. Связывающая способность зависит от многих факторов, в частности от сродства антител к антигену (в данном случае, к щелочной фосфатазе женской плаценты). Удобным способом демонстрации, связывающей способности модифицированных антител, является подтверждение сходства кривых разведения при связывании с антигеном, адсорбированным на поверхности пластмассовых ячеек. Ниже описан способ получения таких кривых с использованием в качестве исходных антител мышиных антител к PLAP, а также химерных антител, полученных вышеописанным способом.
Множественные ячейки пластмассовых плит (Costar 6595,PETg) покрывали щелочной фосфатазой плаценты (5 мкг/мл в фосфатном буфере рН 7,4 при 37oC в течение 2 ч). Перед фиксацией желатином платы промывали в фосфатном буферном растворе при комнатной температуре в течение часа, а затем 4 раза отмывали в фосфатном буферном растворе, содержавшем твин-20 (0,15%). Желатин использовали в виде 0,02%-ного раствора в фосфатном буферном растворе.
Связывание антител производили в содержащем твин-20 фосфатном буферном растворе при комнатной температуре на протяжении часа, после чего платы отмывали тем же буферным раствором. Для выявления связанных антител использовали конъюгаты пероксидазы хрена с антиглобулинами (человеческие IgG в случае модифицированных антител и мышиные IgG в случае исходных молекул). Конъюгаты (Сигма) в буферном растворе (1:1000) инкубировали при комнатной температуре на протяжении часа с последующей четырехкратной промывкой, как описано выше. Спустя 45 мин ставили цветную реакцию с тетраметилбензиденом (0,01% и перекисью водорода) 1:200 или 100 объемов в цитратном буфере рН 6,5. Реакцию останавливали добавлением 2М соляной кислоты.
В контроле наблюдали развитие слабой окраски вследствие неспецифического связывания конъюгата или связывания антител в ячейках, не содержащих щелочной фосфатазы плаценты. Результаты оценки, показанные на фиг. 17, выражали в процентах от максимальной интенсивности окраски (связывания). Обе кривые характеризуются значительным сходством и свидетельствуют о достаточно высокой и достоверной эффективности связывания химерных антител согласно изобретению.
е) Депонирование плазмид.
Штаммы E.coli, содержащие вышеописанные плазмиды, в соответствии с Будапештским соглашением депонировали в Национальной коллекции типовых культур 19 апреля 1990 г. Это относится к следующим плазмидам и штаммам:
NCT 12389: К12,TG1/Е.со1i, содержащие плазмиды pSVgPtHu2VHPLAP.
NCTC 12390: К12,TG1/Е.со1i, содержащие плазмиды PSV neo HuVkPLAP-Huck.
Литература
Deshpande et al (1990) J. Nucl. Med. 31, p.473 479.
Epp et al (1974) Eur. J. BiocheTn. 45, p.513 524.
Flanagan et al (1982) Nature, 300, p.709 713.
Gibson T (1984) PhD thesis, LMB-MRC Cambridge.
Gubler et al (1983) Gene. 25, p.263 269.
Hale et al (1988) Lancet. 2, p.1394.
Hietert al (1980) Cell. 22, p.197 207.
Jones et al (1986) Nature. 321, p.522 525.
Kabat et al (1987) in Sequences of Proteins of lmnunological Interest, p.ix -US Dept of Health and Human Services.
McCall et al (1990) Bioconlucfate Chemistry. I, p.222 226.
Meares et al (1990) Br. J. Cancer, 62, Suppi. X, p.21 26.
Moi et al (1988) J. Am. Chem. Soc. 110, p.6266 6269.
Mulligan et al (1981) Proc. natn. Acad. Sci. U.S.A. 78, p.2072 2076.
Neuberger et al (1983) EMBO Journal. 2, p.1373 1378.
Norrander et al (1983) Gene. 26, p.101 106.
Potter et al (1984) PNAS, 81, p.7161 7163.
Riechmann et al (1988) Nature, 332, p.323 327.
Sambrook et al (1989) Molecular Cloning, 2nd Edition, Cold Spring Harbour Laboratory Press, New York
Sanger et al (1977) PNAS USA. 74, p.5463 5467.
Saul et al (1978) J. biol. Chem. 253, p.585 597.
Southern et al (1981) J. molec, appl. Genetics. I, p.327 345.
Spratt et al (1986) Gene. 41, p.337 342.
Takahashi et al (1982) Cell. 29, p.671 679.
Travers et al (1984) Int. J. Cancer, 33, р.6ЗЗ.
Verhoeyen et al (1988) Science. 239, p.1534 2536.
Vieira et al (1982) Gene. 19, p.259 268.
Winter (1987) EP-A-239400





Использование: медицинская биотехнология, разработка агентов, препятствующих росту раковых клеток. Сущность: получение модифицированных антител и их фрагментов, взаимодействующих с плацентарной щелочной фосфатазой. При этом по крайней мере одна легкая и/или тяжелая цепь антитела содержит вариабельную область, в которую введены участки, определяющие комплементарность связывания с антигеном мышиного происхождения. Получены также фрагменты кДНК, кодирующие вариабельные области тяжелой и легкой цепи химерного антитела. 5 с. и 1 з.п.ф-лы, 18 ил.
CDR1(γ) Ser Tyr Gly Val Ser
CDR2(γ) Val Ile Trp Glu Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile Ser
CDR3(γ) Pro His Tyr Gly Ser Ser Tyr Val Gly Ala Met Glu Tyr
CDR1(k) Arg Ala Ser Glu Asn Ile Tyr Ser Tyr Val Ala
CDR2(k) Asn Ala Lys Ser Leu Ala Glu
CDR3(k) Gln His His Tyr Val Ser Pro Trp Thr.
Авторы
Даты
1998-01-20—Публикация
1990-11-14—Подача