Изобретение относится к имплантантам ткани, в особенности к нанесению имплантантов кожи для обработки всего или части пораженного слоя кожи, например, при ожогах или других ранах.
Поражения всего или части слоя кожи, например, при ожогах и других ранах, составляют значительные затраты в системе здравоохранения. Например, около двух миллионов людей в Северной Америке ежегодно страдают от ожогов. Из них около 200000 людей госпитализируют, 15000 из которых умирают по причине, связанной с ожогами. Общая стоимость лечения таких пациентов в госпитале составляет порядка 1000 долл. на 1% площади ожога (SU. S. 1992), так что на долю среднестатистического пациента с ожогами, составляющими от 20 до 30% общей площади кожного покрова тела, приходится около 25000 долл., не включая стоимость дальнейшего лечения и потенциальной потери производительности и дохода. Например, McMillan et. al (J.Burn Care Rehab, 6:444-446; 1985) показывает, что расходы на операции увеличиваются в логарифмической зависимости от процента площади ожога кожи. Ясно, что существует потребность в развитии технологии, которая позволила бы уменьшить эти затраты и облегчить страдания пациентов.
Кожа состоит из дермального слоя, который расположен под эпидермальным слоем. Дермальный слой состоит в основном из фибробластов и примерно в пять раз толще эпидермального слоя. Эпидермальный слой здоровой кожи, состоящий в основном из кератиноцитов и иммунных клеток, таких как дендритовые лангерансовые клетки, препятствует потере воды и проникновению микробов. Поэтому повреждения части или всего слоя кожного покрова может угрожать жизни человека. Таким образом, скорость заживления раны, предотвращающая потерю жизненно важных жидкостей организации и проникновение бактерий, является жизненно важным фактором выздоровления пациента. Соответственно разработан широкий спектр покрытий для ран с целью ускорения их заживления.
Существующий метод заживления ожогов и ран включает использование собственной кожи пациента или ткани, полученной от умершего или свиньи, для пересадки на рану пациента. Традиционная технология пересадки кожи, полученной от пациента, (аутопересадка) является обычно очень болезненной для пациента, и так уже страдающего от ожога или другой раны. Аутопересадка состоит из значительной толщины как эпидермального, так и дермального слоев кожи, взятой с другой части тела. С целью уменьшить количества кожи, взятой с другой части тела, а следовательно, и размер новой раны, аутопересаженную ткань обрабатывают таким образом, чтобы вдоль повреждения кожи образовать решетчатый образец. Однако решетчатый образец в слое дермы аутопересадки затем заполняется постоянной тканью шрама in vivo. Эти шрамы часто являются очень большими и могут быть сильно бесформенными или в зависимости от их месторасположения могут вызывать дисфункцию. Кроме того, у пациента может не оказаться достаточного количества необожженной поверхности для трансплантации достаточно большого количества пересаживаемой на другое место ткани.
Пересадку кожи, полученной от умершего (аллопересадку) или от свиньи (ксенопересадку), используют для уменьшения страданий пациента и с тем, чтобы способствовать заживлению раны. Основным недостатком аллопересадки является возможность передачи заболевания (например, HIV, гепатит B). Более того, эпидермальный слой проявляет заметный антагонизм, ввиду чего пересаженная ткань, включая аллопересадку, которая не получена непосредственно от пациента, обычно отторгается в течение двух недель с момента пересадки. Хотя ксенопересадка представляет собой такой вид пересадки, при которой экономится ткань человека-донора, однако ткань отторгается даже еще быстрее, чем при аллопересадке, и она должна быть удалена на третий день после нанесения до высыхания и образования струпа и прежде сильного прилипания к ране, вызывающего необходимость хирургического вмешательства.
Все эти виды пересадки кожи, а именно, аутопересадка, аллопересадка и ксенопересадка, обычно являются очень тонкими и непрочными, что очень затрудняет их транспортировку и обращение с ними. Помимо этого пересаженную ткань закрепляют на ране очень часто посредством обширных хирургических швов и/или скобок, что значительно повышает дискомфорт пациента. Кроме того, пациенты с серьезными ожогами или ранами уже подвергаются риску, что делает хирургическое вмешательство под наркозом еще более затруднительным и угрожающим жизни.
В более поздних разработках, например, в патенте США N 4996154 (опубл. 26 февраля 1991, на имя Millipore Corp. , США) и Beumar G.J. et. al. ("Biocompatibility and Characterization of a Polymeric Cell-Seeded Skin Substitute", 17th Ann Meeting Soc for Biomaterials; May 1-5, 1991, Scottsdale, Arizona, USA, p.263) предлагается выращивать клетки кожи на листах с ячейками для получения белкового имплантанта. Листы пришивают или прикрепляют скобками на область раны, и материал временной подложки-носителя обычно ресорбируется телом. Предварительные исследования показывают, что при этом может быть снижена степень роста ткани шрама. Кроме того, участок ячеистой матрицы более стабилен, чем пересаженная кожа.
Однако существует множество проблем с плоскостными ячеистыми пленками или листами из регенерированной кожи. Участки ячеистой матричной кожи обычно поставляют размером около 10 см ширины на 10 см длины и толщиной лишь в несколько клеток. Специалисту понятно, что ожоги часто имеют большую и редко однородную глубину или плоскостную структуру. Участки неадекватно соответствуют контурным изменениям в коже, ввиду чего все же существует в большей или меньшей степени проблема обезображивания. Являясь более стабильными, чем пересадки, тонкие участки все же очень хрупкие и во многих случаях тонкие листы укрепляют для хирургических процедур металлической тканью, пропитанной нефтяным желе. Кроме того, небольшие куски все же должны быть пришиты и/или прикреплены скобками друг к другу и к телу, что приводит к удлинению хирургической процедуры на неделю и создает риск для пациента.
Более того, нанесенные участки кожи имеют очень плохие характеристики газо- и массопередачи, что приводит к омертвлению ткани в результате недостаточного питания клеток. Это в свою очередь может привести к тому, что ткани образуют волдыри. Процессы газо- и массопередачи могут быть также ухудшены за счет остаточного слоя нефтяного желе после удаления металлической ткани с последующей хирургической процедурой. Остаточный слой нефтяного желе может даже привести к выделению различных факторов, таких как факторы роста, в этот слой, где они не будут затем в состоянии воздействовать на клетки.
Другой недостаток заключается в фактическом развитии полученных из кожи клеток in vitro. Обычно эти зафиксированные клетки размножаются в статических условиях в сосуде для тканевой культуры, содержащем ячеистую матрицу в относительно небольшом объеме культуральной среды и, таким образом, создаются условия для пассивной газопередачи с поверхности среды к клеткам, находящимся на дне сосуда. Большое внимание уделяется расходу питательных веществ из среды, что может сопровождаться образованием микросреды в непосредственной близости от клеток. Такая микросреда содержит даже еще меньше питательных веществ и имеет тенденцию к повышенной концентрации метаболических промежуточных продуктов, что отрицательно отражается на развитии клеток. Для преодоления этих проблем требуется множество трудоемких операций для изменения среды, причем каждая операция увеличивает возможность микробного заражения.
С целью увеличения газо- и массопередачи была предложена культуральная система, заключенная в газопроницаемом мешке с рециркуляционным наносом (Marrow-Tech lnc. , USA) для циркуляции среды по поверхности развивающейся культуры на содержащейся внутри мешка ячеистой ткани. Клетки обычно посеяны беспорядочно на ячейке, в результате чего создается множество центров развития клеток. Однако любая твердо не прикрепленная к поверхности клетка может быть подвергнута циркуляции через насос и испытать сдвиговые и другие разрушающие воздействия. Система все же является трудоемкой и громоздкой, что приводит к повышению вероятности заражения ввиду чрезмерных требований в обращении с ней. Если система не является статичной, то среда не является полностью гомогенной и закрепленные на ячейке клетки не находятся в одной фазе развития ввиду полустатичных условий культивирования и беспорядочного посева клеток на ячейке. Кроме проблемы гомогенности внутри одного участка существует также проблема гомогенности от участка к участку по обычно обширной зоне повреждения кожи. Более того, эффективная площадь жизнеспособных клеток может быть значительно уменьшена сшиванием и/или соединением скобками по краям участка, что может разрушить или нарушить размножение клеток.
Ни одна из известных ранее технологий не обеспечивает соответствие изменениям контура поврежденной кожи. Редко когда поврежденная кожа имеет форму в совершенном соответствии с известными плоскостными пересадками и участками, что приводит к возможному образованию неконтактных зон, в которых новая кожа не вполне соответствует им.
Более того, многие из этих разработок не отвечают крайней потребности упрочнения слоя эпидермы. Пары воды проходят через неповрежденную кожу со скоростью около 8,5 г/м2•ч, а в области без слоя эпидермы - со скоростью около 150 г/м2•ч. В идеале проницаемость имплантанта кожи должна приближаться к проницаемости здоровой кожи для предотвращения высыхания ткани и тромбоза в случае, когда проницаемость слишком высока, и для предотвращения скопления жидкости и низкой адгезии пересаженной ткани в случае низкой проницаемости.
Demetriou A. A. ("Replacement of liver function in rats by transplantation of microcarrier-attached hepatocytes" Science 233:1190-1192; September 12, 1986) описывает закрепления гепатоцитов на микроносителях из сшитого декстрана с колагеновым покрытием для последующей имплантации в область брюшины крыс. Микроносители используют как поверхность для закрепления, благодаря чему гепатоциты выживают и действуют in vivo. Имплантированные микроносители не ресорбируются и не разрушаются.
Международная заявка PCT/US90/02257 (Vacanti et. al., published November 1, 1990, WO 90/12604) относится к имплантанту большого объема клеток на полимерной матрице. Матрица представляет собой волокнистый биосовместимый способный разрушаться или неразрушающийся полотнообразный материал с промежутками 100-200 мкм. Vacanti et. al. описывает закрепление и развитие гепатоцитов на матрице для последующей имплантации в брыжейку тонкой кишки.
Задачей изобретения является создание заменителя здоровой кожи для лечения повреждений части или всего слоя кожи, таких как ожоги и ранения, который может приспосабливаться к изменениям контура, а также создание имплантанта, имеющего дермальный слой и функционирующий эпидермис и не требующего сшивания, закрепления скобками или другими методами.
Согласно одному аспекту изобретения предложен заменитель здоровой кожи для полностью или частично поврежденного слоя кожи, характеризующийся тем, что он содержит множество микросфер из биосовместимого и ресорбирующегося in vivo материала и культуры кожных клеток, покрывающей микросферы, при этом микросферы с покрытием из кожных клеток наносят на поврежденную кожу.
Согласно другому аспекту изобретения предложен способ получения заменителя здоровой кожи, заключающийся в культивировании клеток кожи, получении множества биосовместимых ресорбирующихся микросфер и размножении закрепленных клеток кожи в среде до их слияния или приблизительного слияния с последующим концентрированием покрытых клетками микросфер до суспензии путем удаления части или почти что всей среды и нанесением суспензии покрытых клетками микросфер на область повреждения кожи.
На фиг.1 изображена фотомикрография закрепленных дермальных фибробластов на микросферах через 1 ч после посева клеток; на фиг.2 - фотомикрография дермальных фибробластов, закрепленных на тех же микросферах, что и на фиг.1, через 22 ч после посева клеток; на фиг.3 - схематично повреждение всего слоя кожи; на фиг. 4 - схематично повреждение всего слоя кожи согласно фиг.3 с имплантацией заменителя здоровой кожи согласно изобретению; на фиг.5 - фотомикрография кератиноцитов, закрепленных на микросферах, через 24 ч после посева клеток; на фиг.6 - фотомикрография кератиноцитов, закрепленных на микросферах, через 24 ч после посева клеток, микросферы инкубированы в культуральной среде в течение 24 ч перед посевом клеток; на фиг.7 - гистограмма данных, полученных на цитофлуорометре; на фиг.8 - фотомикрография дермальных фибробластов, закрепленных на обработанных фактором закрепления микросферах, через 1 ч после посева клеток; на фиг.9 - фотомикрография дермальных фибробластов, закрепленных на микросферах, обработанных фактором закрепления, согласно фиг.8 через 22 ч после посева клеток; на фиг.10 - фотомикрография дермальных фибробластов, закрепленных на поверхности стекла (контрольный опыт); на фиг.11 - фотомикрография дермальных фибробластов, закрепленных на плоскостной поверхности PMB-PHV (сополимер полигидроксибутирата с полигидроксивалератом); на фиг.12 - фотомикрография дермальных фибробластов, закрепленных на плосткостной поверхности PMB-PHV, обработаннной фактором закрепления.
Согласно изобретению клетки закрепляют на микросферах для последующей имплантации in vivo. В особенности суспензию микросфер, покрытых клетками кожи, используют в качестве заменителя здоровой кожи в случае повреждения части или всего слоя кожи. Суспензию покрытых клетками кожи микросфер наносят непосредственно на поврежденную кожу таким же образом, как раствор или мазь.
Клетки кожи могут быть получены от пациента из относительно небольшого тканевого эксплантанта. Альтернативно дермальные фибробласты, проявляющие низкую аллергеничность в трансплантантах, могут быть получены от донора, включая умершего. Эпидермальный слой проявляет заметную антигеничность, поэтому имплантанты из этого слоя обычно необходимо получать непосредственно от пациента. Исследования показывают, однако, что лангерансовые клетки во многом ответственны за антигеничность эпидермального слоя (Bagot M. et. al., Clin Exp. Jmmunol. 71:138; 1988). Поэтому возможно получить чистую культуру кератиноцитов от донора, вследствие чего отторжение будет либо минимальным, либо вообще отсутствует.
Согласно изобретению небольшой тканевый эксплантант, обычно размером 4 см2, получают от пациента или донора с помощью дерматома или другого подходящего хирургического инструмента. Эксплантант может включать только эпидермальный слой или комбинацию эпидермального и дермального слоев. Ткань затем разрушают под действием подходящего энзима по известной технологии и производят посев клеток в тканевой культуральной колбе для последующего клеточного увеличения фибробластов и/или кератиноцитов. Клетки дермальных и эпидермальных слоев могут быть выделены посредством энзимов, таких как диспаза либо посредством пропитки культуральной средой или буферным фосфатным раствором, либо другими хорошо зарекомендовавшими себя методами. Для специалистов понятно, что может быть создан "банк" клеток, полученных от донора, включая умершего, для своевременной обработки повреждений кожи.
Микросферы имеют диаметр в пределах от около 50 до 500 мкм и преимущественно в пределах от около 80 до 250 мкм. Микросферы могут быть изготовлены из различных материалов, как это будет более детально рассмотрено ниже. Важную роль при выборе материала играет биосовместимость и способность к ресорбции в теле без образования токсичных побочных продуктов. Одним из таких подходящих материалов является полигидроксибутират (PHB), который обычно используют для изготовления ресорбирующихся хирургических скобок или шовных материалов. PHB ресорбируется in vivo с образованием в качестве конечных продуктов двуокиси углерода и воды. Другими подходящими материалами являются полилактидгликолиды, которые выпускаются в промышленности для систем доставки медикаментов. Полимеры абсорбируют нерегулярным гидролизом сложноэфирных связей и разлагают на лактоновую и гликолевую кислоты, являющиеся обычными побочными продуктами метаболизма.
Согласно одному варианту воплощения изобретения дермальные фибробласты, выделенные из тканевого эксплантанта, полученного от пациента или донора, культивируют в тканевой культуральной колбе до тех пор, пока не будет получено достаточное число клеток для достижения их жизнеспособной плотности в биореакторе от около или по меньшей мере 104 до 105 клеток/мл,
При типичной загрузке микросфер от 3 до 5 мг/л, что соответствует количеству примерно 5•106 микросфер/г сухого веса, плотность клеток соответствует примерно 5 клеткам/микросферу.
После получения достаточного количества клеток их отделяют со дна тканевой культуральной колбы посредством, например, трипсина. Специалисту очевидно, что для получения необходимого количества клеток требуется некоторое число пассажей в различных по величине тканевых культуральных колбах. После этого производят посев клеток в биореакторе, содержащем подходящую культуральную среду и микросферы при плотности от 1 до 25 г/л, оптимально 2-5 г/л. Микросферы могут быть добавлены в культуральную среду либо непосредственно перед посевом клеток, либо микросферы предварительно перед посевом клеток пропитывают в этой среде некоторое время. Затем клетки закрепляют на микросферах в течение некоторого времени в статических или полустатических условиях, например, в течение 3-6 ч.
Стадия закрепления может быть осуществлена в сокращенном объеме среды с прерывающимся перемешиванием несколько минут каждые полчаса в течение 3-6 ч.
На фиг. 1 представлена фотомикрография, на которой показаны дермальные фибробласты, полученные из плаценты новорожденного (neo-natal foreskin), закрепленные на микросферах из PHB-PHV (сополимер полигидроксибутирата с полигидроксивалериатом), через 1 ч после посева клеток. Дермальные фибробласты начинают закрепляться на микросферах.
Спустя некоторое время, достаточное для дальнейшего закрепления клеток на микросферах, добавляют оставшееся количество среды для создания желаемого рабочего объема при последующем непрерывном перемешивании. На фиг.2 представлена фотомикрография, на которой показаны дермальные фибробласты, закрепленные на микросферах из PHB-PHV, согласно фиг.1 через 22 ч после посева. Большинство дермальных фибробластов, закрепленных на микросферах, из сферических превратились в плоские.
Альтернативно клетки, выделенные из тканевого эксплантанта, могут быть посеяны непосредственно в биореакторе. Например, из тканевого эксплантанта размером 4 см2 получают (2-5)•107 клеток, что достаточно для достижения плотности посева от 3 до 5 клеток/микросферу в 1 л среды.
Клетки дермального фибробласта, закрепленные на микросферах, затем выращивают в культуральной суспензии в биореакторе, имеющем обычно рабочий обьем от 250 мл до нескольких литров. Возможно получить реальный имплантант кожи с использованием клеток, культивированных в биореакторе объемом 1 л. При средней площади поверхности 5000 см2/г сухого веса микросфер и плотности микросфер от 3 до 5 мг/мл получают эффективную площадь поверхности от 2 до 2,5 м2 на 1 л рабочего объема. Клетки в конце концов покрывают всю эту поверхность, создавая сравнимый слой кожи для дальнейшей миграции и размножения in vivo.
Ожоги меньшей площади могут быть обработаны культурой из сосуда меньшего объема, включая 250-мм прядильную колбу. Может быть использован усложненный биореактор с тщательным контролем и регулированием параметров. Например, такой как описан в патенте US N 4906577 (Armstrong, Fleming & Grenzowski), опубликованном 6 марта 1990. Альтернативно может быть использован простой контейнер с перемешиванием в CO2 инкубаторе. От начала посева клеток до конечной стадии выгрузки покрытых клетками микросфер из биореактора внутри сосуда поддерживают стерильность известным образом.
Подобно статичной или полустатичной технологии культивирования клеток, практикуемой для участков с ячеистой матрицей, описанной выше, выращивание клеток в суспензии в биореакторе дает более высокую продуктивность ячейки. Это было доказано развитием в суспензии культуры клеток, закрепленных на микросферах, представляющих небольшие шарики диаметром от 100 до 200 мкм с площадью поверхности около 5000 см2/г, обычно из сшитого декстрана. Некие ряды клеток были выращены на микроносителях для доказательства продуктивности элемента при выращивании клеток и/или образовании продукта, превышающей продуктивность, достигаемую в статическом культивировании в тканевой культуральной колбе (van Wezel, A. L. "Growth of Cell Strains and Primary Cells in Microcarriers in Homogeneous Culture" Nature 216:64-65; October 7, 1967).
Статичные культураторы для получения пересадок кожи на подложках в виде ячеистых листов в тканевых культуральных контейнерах имеют отношение эффективная поверхность/объем (S/V) около 2-5 см-1 в сравнении с отношением S/V около 150 см-1 для микросфер, суспендированных при концентрации 25 г/л. Более того, суспензионное культивирование менее трудоемко, а культура является более гомогенной, ввиду чего проблемы газопередачи, истощения питательной среды и накопления питательной среды не являются столь ограничивающими. Например, для получения 2 м2 новой ткани с использованием ячеистой матрицы потребуется приблизительно 250 тканевых культуральных колб из расчета обычно 80 см2 площади свободной поверхности на одну колбу.
Предпочтительно дермальные фибробластовые клетки выращивают в биореакторе до тех пор, пока они не достигнут стадии слияния или приблизительного слияния друг с другом, при которой клетки почти целиком покрывают микросферу. Слияние клеток обычно достигается в течение 7 дней. Однако возможно использовать покрытые клетками микросферы терапевтически и до этого времени в стадии приближения к слиянию, когда популяция клеток находится еще в состоянии высокой миграции и быстрого размножения. Затем клетки концентрируют удалением избытка культуральной жидкости и промывают in situ соответствующим буфером или раствором для получения суспензии микросфера/клетка. В противоположность обычной практике культивирования с микроносителем, согласно которой затем используют такой фактор, как трипсин для удаления клеток с микроносителем, согласно настоящему изобретению дермальные фибробластовые клетки не удаляют с микросфер. Суспензию микросфер с клетками затем наносят непосредственно на рану таким же образом, как раствор или мазь. Благодаря однородности суспензии микросфер каждая микросфера имеет одинаковое число закрепленных на ней клеток, что приводит к гомогенному распределению при дальнейшем нанесении на поврежденную кожу. Более того, существует гомогенность фазы роста клеток в области повреждения кожи даже в случае обширной области повреждения,
В противоположность участку ячеистой матрицы, описанному выше, изобретение позволяет снизить количество манипуляций с клетками. Это в свою очередь снижает вероятность повреждения самих клеток и сводит к минимуму вероятность загрязнения, приводящего к инфицированию раны.
Нанесенные на рану клетки в соответствии с изобретением могут быть легко распределены по всей поверхности раны. Это является очень важным преимуществом, поскольку клетки, выращенные на ячеистой матрице, и даже кожа для пересадки, полученная от пациента, часто имеют множество неконтактных зон, в которых не могут быть полностью восстановлены. Консистенция суспензии позволяет скорректировать контурные изменения раны. Это является большим преимуществом перед плоскостными имплантантами согласно известному ранее уровню техники. Во-первых, рана редко имеет равномерную глубину с гладким плоским основанием. Во-вторых, может распространяться на значительную площадь. Например, специалисту ясно, что при обработке ожога, образованного вдоль всей длины руки на тыльной ее стороне, встречается много естественных изгибов вдоль всей длины руки. Изобретение предлагает имплантант, который может заполнить даже самую глубокую рану для ее эффективного лечения и более естественной трехразмерной регенерации ткани в месте повреждения.
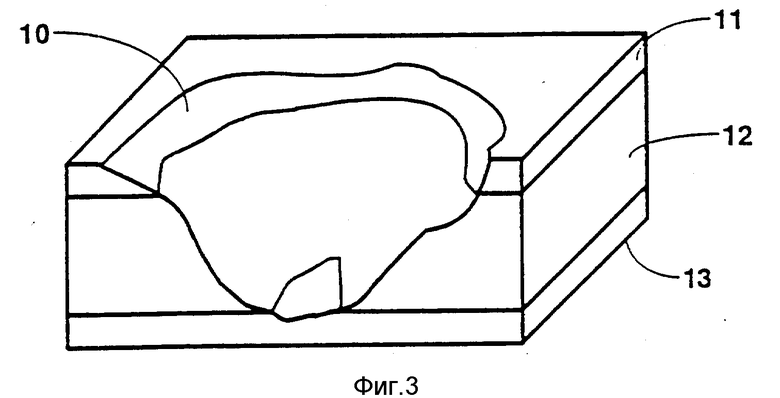
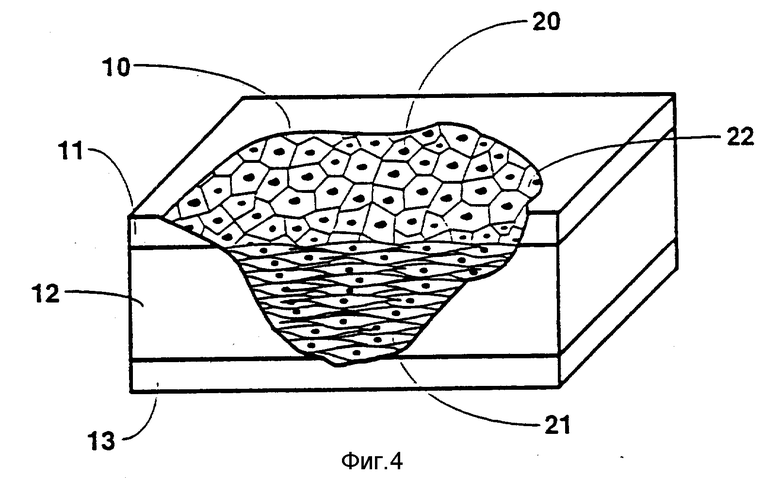
Пример неравномерного повреждения слоя кожи по всей его толщине показан на фиг.3. Повреждение кожи 10 распространяется сквозь эпидерму 11 и дерму 12 к находящемуся под ней мускулу 13. Специалисту понятно, что плоскостная пересадка кожи не обеспечит адекватного имплантанта кожи для повреждения такого типа. На фиг.4 схематично показано то же самое повреждение кожи 10 с имплантантом заменителя здоровой кожи 20 согласно изобретению.
Заменитель здоровой кожи 20 создает имплантант дермальных фибробластов 21 и кератиноцитов 22. Последовательные слои дермальных фибробластов могут быть нанесены на рану поверх слоя дермальных фибробластов, например, с целью корректировки любых дальнейших изменений контура. Также возможно нанесение на рану суспензии, полученных от донора дермальных фибробластов с микросферами, с последующим нанесением на нее суспензии, полученных от пациента дермальных фибробластов с микросферами.
Использование клеток в условиях слияния или близких к слиянию на микросферах не только обеспечивает высокую концентрацию клеток на месте повреждения кожи, но и увеличивает эффективность клеток. Клетки животных имеют тенденцию лучше функционировать, если они находятся в микрокосме, таком как обнаруживается в условиях слияния иди близких к слиянию популяции клеток на микросфере. Достигается также улучшении производства факторов роста и распределения особенно, у клеток, находящихся в тесном контакте друг с другом в результате межклеточной регуляции, включая аутокринное и паракринное взаимодействие, уменьшения диффузиональных ограничений и так далее. Нанесение дермального слоя позволяет быстрее получать структурный протеиновый коллаген и другие факторы роста и закрепления. Ранее нанесение дермальных фибробластов может снизить или предотвратить сжатие кожи, что является главной причиной образования шрамов и потери избытка жидкости. Дермальные фибробласты могут дифференцироваться и объединяться по оси в ране для эффективного соединения раны, особенно, если повреждением кожи является продольный разрез. Ранее нанесение микросфер, покрытых фибробластами, приводит к лучшему залечиванию раны и уменьшает страдания пациента.
После нанесения суспензии на рану область раны может быть покрыта газопроницаемым перевязочным средством. Дермальные фибробласты, находящиеся в суспензии микросфер с клетками, затем мигрируют и разрастаются в направлении от микросфер в окружающую ткань и создают непрерывную поверхность в месте повреждения кожи. По прошествии некоторого времени, когда клетки растут, микросферы начинают ресорбировать in vivo.
Предпочтительно кожный имплантант включает также регенерацию эпидермального слоя. В то время как in vivo создается дермальный фибробластовый слой, клетки эпидермального слоя пациента могут быть культивированы в тканевой культуральной колбе. После получения достаточного количества клеток клетки удаляют со дна тканевой культуральной колбы посредством, например, трипсина. Затем производят посев клеток в биореакторе, содержащем подходящую культуральную среду и микросферы. Как описано выше, другим оптимальным вариантом является использование эпидермальных клеток полученного от пациента тканевого эксплантанта для непосредственного инокулирования микросфер, клетки закрепляют на микросферах и культивируют в суспензии в биореакторе так же, как описано ранее в случае дермальных фибробластов. Специалисту понятно, что может потребоваться использование широкого спектра антибиотиков в начальной фазе размножения клеток ввиду возможности заражения области раны флорой от здоровой кожи и из других источников.
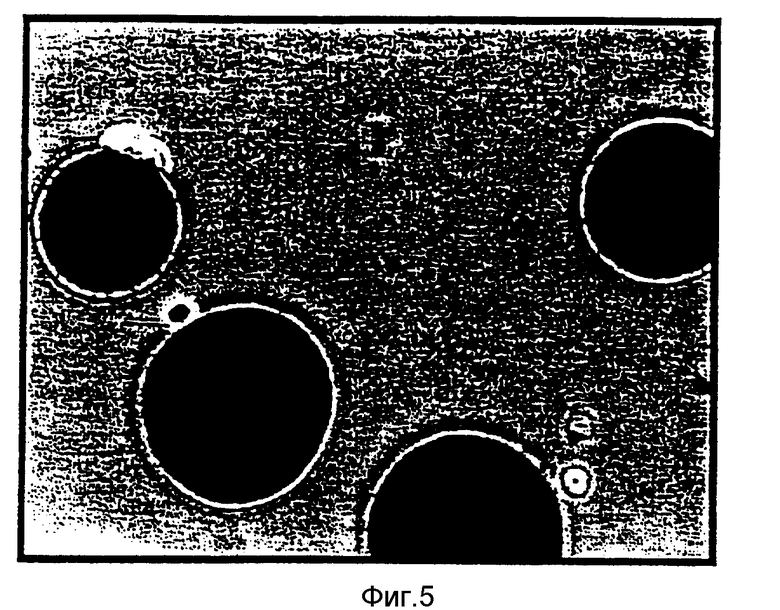
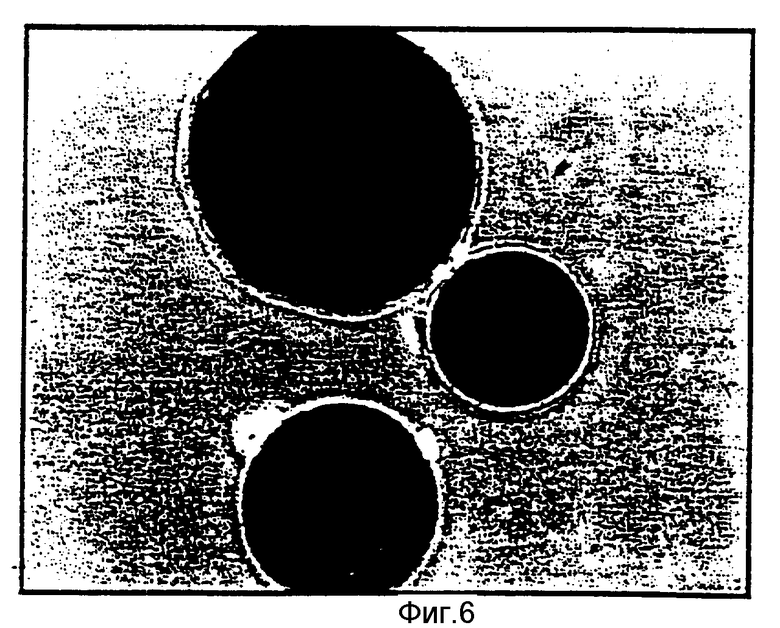
На фиг.5 изображена фотомикрография полученных из плаценты новорожденных кератиноцитов, закрепленных на PHB-PHV микросферах, через 24 ч после посева клеток. Большинство кератиноцитов, закрепившихся на микросферах стали плоскими и потеряли сферическую форму. Как упоминалось выше, микросферы могут быть добавлены в культуральную среду непосредственно перед посевом клеток иди они могут быть предварительно пропитаны в этой среде в течение некоторого времени перед посевом клеток. На фиг.5 изображена микрофотография кератиноцитов, полученных из плаценты новорожденного (neo-natal foreskin) и закрепленных на PHB-PHV микросферах, через 24 ч после посева клеток. Микросферы инкубировали в культуральной среде в течение 24 ч перед посевом клеток. Большинство кератиноцитов, закрепленных на микросферах, приняло плоскую форму.
После того как эпидермальные клетки, включая кератиноциты, достигнут слияния или приблизительного слияния на микросферах, часть или всю культуральную среду удаляют и получают суспензию покрытых клетками микросфер. Перевязочные средства, если они имеются, удаляют с раны и наносят суспензию поверх слоя дермальных фибробластов для регенерации наружного слоя кожи, благодаря чему создается защитный барьер неповрежденной кожи.
После нанесения на рану суспензии эпидермальных клеток место повреждения может быть покрыто газопроницаемым перевязочным средством. Затем клетки эпидермы мигрируют и растут в направлении от микросфер в окружающую ткань для создания непрерывной поверхности заменителя повреждения кожи. По мере роста клеток происходит ресорбция микросфер in vivo. Некоторый процент эпидермальных клеток может быть обработан либо in vivo, либо in vivo специфичным фактором, таким как кальций и/или CAMP для ускорения получения stratum corneum, самого верхнего слоя мертвых высококератинизированных клеток. Stratum corneum помогает регулировать количество потерянной телом воды, а также предотвращать вторжение микробов в область раны. При контролируемом ускорении дифференциации этого слоя заживленное место раны будет функционировать подобно неповрежденной здоровой кожи.
Согласно другому варианту воплощения изобретения в тканевой культуральной колбе культивируют клетки как дермального, так и эпидермального слоев. Этот вариант воплощения изобретения создает возможность развития усиленного паракринного и аутокринного функционирования. При использовании той же самой технологии, которая описана раньше, клетки затем удаляют из тканевой культуральной колбы и производят посев их в биореакторе, содержащем культуральную среду и микросферы. Закрепляют клетки на микросферах в статичных или полустатичных условиях для последующего сокультивирования в суспензии в биореакторе. Индивидуальная микросфера может затем иметь закрепленные на ней клетки обоих как дермального, так и эпидермального слоев. Полученную суспензию микросфер с клетками наносят непосредственно на рану тем же самым образом, как мазь или пасту наносят на рану для восстановления одновременно дермального и эпидермального слоев.
Как это случается in vivo, дифференцирующиеся кератиноциты стремятся мигрировать в самые верхние места раны, что приводит к естественному образованию stratum corneum. Затем рана может быть покрыта газопроницаемым перевязочным средством до эффективного ее заживления в результате естественного преобразования дермального и эпидермального компонентов.
Согласно еще одному варианту воплощения изобретения дермальные фибробласты и клетки, полученные из эпидермального слоя культивируют независимо друг от друга в отдельных тканевых культуральных колбах. Дермальные фибробласты удаляют из соответствующей тканевой культуральной колбы посредством, например, трипсина и производят их посев в сосуде, содержащем соответствующую клеточную культуральную среду и микросферы. Затем закрепляют дермальные фибробласты на микросферах в статичных или полустатичных условиях.
Аналогичным образом эпидермальные клетки, включая кератиноциты, удаляют из соответствующей тканевой культуральной колбы посредством, например, трипсина и производят их посев в другом сосуде, содержащем подходящую клеточную культуральную среду и микросферы. Затем эпидермальные клетки закрепляют на микросферах в статичных или полустатичных условиях. Микросферы, покрытые дермальными фибробластами, и микросферы, покрытые эпидермальными клетками, затем вводят в один и тот же биореактор для последующего сокультивирования их.
Полученную суспензию покрытых клетками микросфер затем наносят на рану для одновременного восстановления дермального и эпидермального слоев. Затем рана может быть покрыта газопроницаемым перевязочным средством.
Согласно еще одному варианту воплощения изобретения дермальные фибробласты закрепляют на микросферах и подвергают быстрому размножению в биореакторе. По истечении некоторого времени производят посев клеток из эпидермального слоя в биореакторе для последующего закрепления на микросферах, ранее покрытых в некоторой степени дермальными фибробластами. В результате кератиноциты могут извлечь пользу из паракриновых эффектов фибробластов.
Изобретение может быть также использовано для имплантации in vivo меланоцитов с целью придания коже естественной пигментации и для защиты от УФ.
В области косметической медицины, например, для залечивания шрамов при ранениях, прыщах и т. д. , эпидермальный слой и преимущественно небольшой процент расположенного под ним дермального слоя может быть удален хирургическим путем посредством дерматома или другого подходящего хирургического инструмента. После этого на предварительно обработанную область непосредственно наносят суспензию покрытых клетками микросфер в один иди более слоев для корректировки контурных изменений.
Используемые по изобретению микросферы могут быть изготовлены из различных материалов, которые являются биосовмастимыми и способны к ресорбции в тело пол воздействием in vivo естественных энзимов без образования токсичных побочных продуктов.
Подходящими материалами для микросфер являются натуральные или синтетические биоресорбирующиеся материалы, такие как полигидроксибутират (PHB), сополимер PHB - полигидроксивалериат (PHB-PHV), PHB с полиэфирными связями, полилактидогликолиды, липиды, фосфолипиды, полилактоны, полиэфиры, полилактиды, полигликолиды, полиангидриды, коллаген, желатин или другие ресорбирующиеся материалы, не оказывающие отрицательного действия на ткань во время лечения (т.е. нетоксичные по отношению к клеткам изначально или через конечные продукты ресорбции). Эти материалы могут быть использованы в чистом виде или в виде смеси материя лов для улучшения физико-химических свойств или с целью контроля скорости их разложения.
Предпочтительно микросферы имеют плотность от 1,01 до 1,04 г/мл для облегчения смешения и суспендирования их в культуральной среде. Микросферы могут быть относительно равными или с изменяющейся поверхностью и иметь микропористость от 30 до 80% с размером пор от 30 до 80 мкм.
Микросферы имеют относительно большую площадь поверхности, например, около 5000 см2/г сухого веса. Для сравнения ячеистые матрицы согласно известной ранее плоскостной технологии имеют обычно площадь поверхности от 200 до 700 см2/г. Более того, для достижения адекватной прочности необходимо больший расход материала для изготовления ячеистой матрицы. Соответственно значительно больше потребуется материала для получения имплантанты с такой же поверхностной площадью, и, следовательно, больше материала должно быть ресорбировано in vivo при использовании ячеистой матрицы.
Специалисту ясно, что в заменителе живой кожи по изобретению могут быть использованы и другие структуры, такие как цилиндрические, яйцевидные, вафлеобразные.
Микросферы могут состоять из ядра из одного вида материала с оболочкой в виде наружного слоя или покрытия из другого материала для улучшения ресорбционных и функциональных свойств, включая плотность заряда, способность к закреплению других химикатов или компонентов, улучшение закрепления клеток и распределения. Например, покрытие фосфолипидом способствует образованию полярной поверхности с функциональными фосфатными группами. Ацильные группы фосфолипидов создают более гидрофобную поверхность микросфер. На эту часть фосфолипидов затем могут быть закреплены различные химикаты и биомолекулы. Кроме того, микросферы могут быть покрыты некоторыми stratum corneum липидами, включая фосфолипиды и сфингозины для улучшения антимикробной активности. Сфингозины особенно хороши для ингибирования размножения микробов на мкг уровнях (Antimicrobial activity of sphingosines, J. Invest Dermatol, 98: 269-273, 1992).
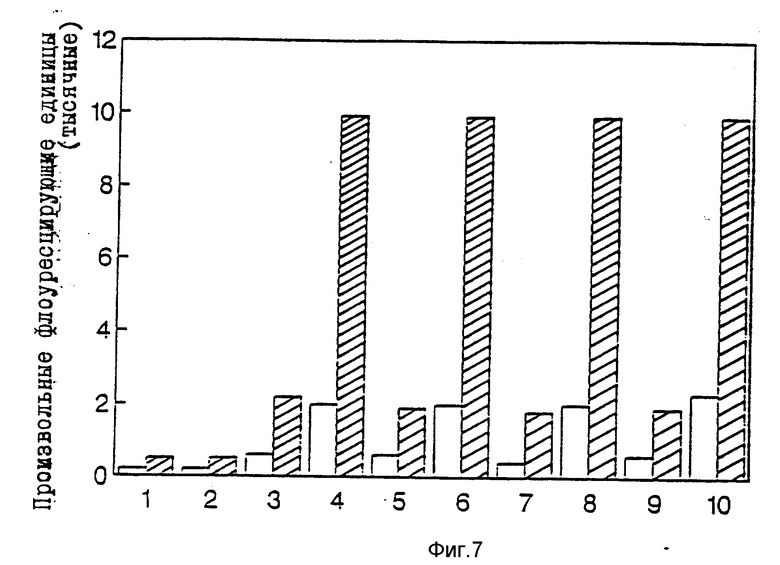
На фиг. 7 изображена гистограмма данных, полученных на цитофлуорометре для измерения жизнеспособности клеток. Жизнеспособность клеток измеряют с помощью флуорохрома специально для живых клеток и флуорохрома специально для мертвых клеток.
Результаты измерений выражают как "Условия флуоресцирующие элементы" и наносят на гистрограмму в виде крестиков, обозначающих живые клетки, и в виде черточек, обозначающих мертвне клетки. Интерпретация данных скорректирована набором данных 1 и 2 соответственно для фосфатного буферного раствора и для контрольного. Кератиноциты из одной и той же колонии клеток были посеяны на PHB и PHB с покрытием фосфолипидом и в каждом случае инкубированы в течение 24 ч. Измеряли жизнеспособность закрепленных клеток на соответствующих образцах посредством флуорохромов, описанных выше. Образцы без закрепленных на них клеток также измеряли на флуорохромах для дополнительной коррекции с учетом специфичности ресорбируемого материала. Образцы свободные от клеток представлены набором данных 3,5,7 и 9 как корректирующие факторы для набора данных 4,6,8 и 10, соответственно.
Набор данных 4 и 8 представляет собой жизнеспособность кератиноцитов, закрепленных на PHB, в то время как набор данных 6 и 10 показывает PHB с покрытием фосфолипидами. Ресорбирующиеся материалы, соответствующие набору данных 3,4,5 и 6, подвергали стерилизации в автоклаве перед посевом клеток, в то время как ресорбирующиеся материалы, соответствующие набору данных 7,8,9 и 10 стерилизовали без термообработки окисью этилена. Данные свидетельствуют о высокой жизнеспособности клеток на этих ресорбирующихся материалах. Более того, метод предварительной стерилизации (паром или окисью этилена) не влияет на эффективность закрепления или жизнеспособность популяции клеток. Согласно другому варианту воплощения изобретения микросферы получают из смеси полисахарида и ресорбирующегося материала, так что ресорбирующийся материал неравномерно распределен по массе ядра. Полисахарид (такой как, декстран или крахмал) может быть разрушен или удален химическими или энзиматическими средствами перед нанесением на микросферы покрытия из клеток кожи, оставляя открытой структуру для гидролиза ресорбирующегося материала in vivo. Этот вид микросфер снижает диффузионные ограничения питательных веществ или промежуточных продуктов метаболизма, благодаря чему дополнительно ускоряется рост клеток. Кроме того, различные факторы, например, факторы роста и другие, введенные внутрь или на поверхность микросфер, удаляются более быстро, благодаря чему облегчается доступ к этим факторам в определенное время в период лечения.
Альтернативно микросферы могут быть использованы с неповрежденным полисахаридным компонентом для ресорбции во время быстрого размножения клеток in vitro и in vivo.
В предпочтительном варианте осуществления изобретения микросферы ресорбируют со скоростью, сравнимой с распространением популяции клеток. Таким образом, по мере ресорбции микросфер клетки растут внутрь небольших пустот, образуемых при частичном удалении ресорбирующихся микросфер, благодаря чему сводится к минимуму образования шрама и изменение контура.
Один из подходов к выбору материалов и/или факторов или материала покрытий заключается в выборе одной комбинации для дермального слоя и другой для эпидермального слоя. Предпочтительно микросферы в эпидермальном слое ресорбируются гораздо быстрее, чем ниже расположенный материал для дермального слоя. Это способствует более естественной миграции и распространению кератиноцитов на расположенный ниже дермальный слой. Возможно также использование разных покрытий для разных видов клеток, хотя может быть пригодным один тип покрытия. Микросферы могут иметь и другие свойства, которые им придают введением добавок внутрь или на поверхность микросфер, например, иммобилизацией, инкапсулированием, ковалентным присоединением или простой адсорбцией. Эти добавки используют для ускорения размножения клеток, для улучшения локальной окружающей среды in vivo с последующей имплантацией и/или для контроля удаления определенного фактора. Такие добавки могут быть введены внутрь или на поверхность почти всех микросфер имплантанта либо только на их часть.
Например, особенно важным является контролируемое поступление антимикробных факторов, так как многие из них цитотоксичны как по отношению к дермальным фибробластам, так и по отношению к кератиноцитам, что создает отрицательный эффект при заживлении раны. Улучшения контролируемого поступления антимикробного фактора достигают предварительной обработкой микросфер антимикробным фактором, что приводит к меньшему отрицательному влиянию на заживление раны в случае содержания асептика.
Альтернативно поверхность микросфер может быть предварительно обработана для облегчения закрепления на них клеток, например, закрепляющим фактором таким, как трипептид аргиноглициноаспарагиновой кислоты (RGD) или поли-L-лизин. На фиг.8 изображена фотомикрография, на которой показаны дермальные фибробласты, полученные из плаценты новорожденного (neo-natal foreskin) и закрепленные на PHB-RHV микросферах, обработанных RGD в качестве закрепляющего фактора через 1 ч после посева клеток. На фиг.9 изображена фотомикрография, на которой показаны те же дермальные фибробласты, закрепленные на PHB-PHV микросферах, обработанных RGD, что и на фиг.8, но через 22 ч после посева клеток. Большинство клеток, которые закрепились на микросфере, превратились из сферических в плоские.
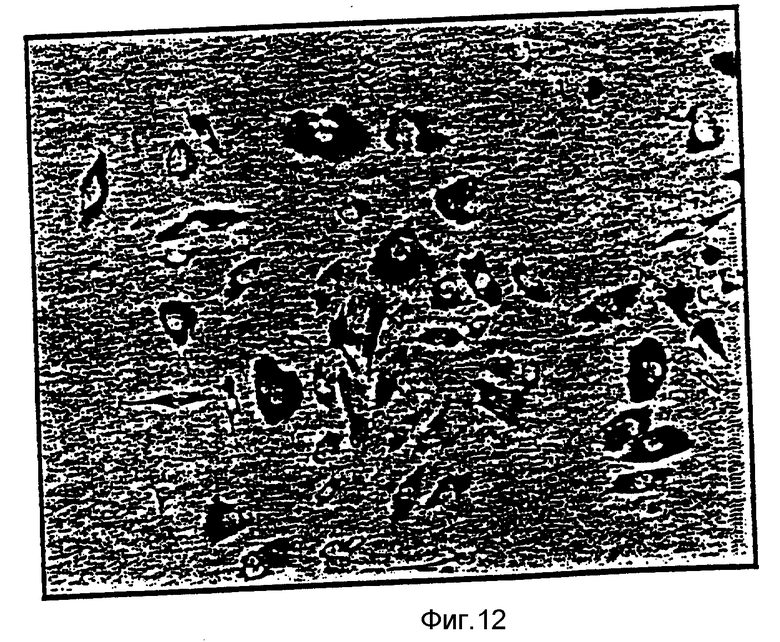
На фиг.10 изображена фотомикрография дермальных фибробластов, полученных из плаценты новорожденных (neo-natal foreskin) и закрепленных на стеклянной поверхности (контрольный опыт) после 26 ч инкубации. На фиг.11 изображена фотомикрография дермальных фибробластов, полученных из плаценты новорожденных (neo-natal foreskin) и закрепленных на плоскостной поверхности PHB-PHV после 26 ч инкубации. На фиг.12 изображены дермальные фибробласты, полученные из плаценты новорожденных (neo-natal foreskin) и закрепленные на плоскостной поверхности из PHB-PHV, обработанной RGD, и инкубированных в течение 26 ч.
Живые клетки на фиг. 10-12 помечены красителем нейтрально красным (Neutral Red). Краситель активно выбирается клетками, чтобы проиллюстрировать на фиг.11 и 12, что клетки на используемых биоресорбирующихся материалах являются высокожизнеспособными.
Другие факторы, которые могут быть введены в микросферы, включают факторы роста, такие как фактор эпидермального роста (EGF), трансформирующий фактор роста-альфа (TGA), трансформирующий фактор роста-бета (TGF-бета), фактор роста кератиноцитов (KGF), фактор роста основных фибробластов (bFGF) и фактор-I инсулиноподобного роста (TGF-1). Контролируемое поступление этих факторов может быть достигнуто использованием микросфер для лучшего регулирования заживления раны, поскольку в случае слишком быстрого поступления митогенного фактора (фактора роста) или ангиогенного фактора (вызывающего рекапилляризацию раны) на месте раны может образовываться шрам. На поверхности микросфер могут быть иммобилизованы также факторы роста с образованием постоянной ковалентной связи, так что клетки контактируют с иммобилизованным фактором роста.
На микросферы могут быть закреплены моноклональные антитела для регулирования локального in vivo уровня TGF-бета, например, во избежание излишнего поступления этого фактора в определенном месте в процессе заживления раны. Поступление обычного количества TGF-бета может привести к диспропорциональному избыточному воспроизводству коллагена фибробластами и клетками макрофагами.
Ресорбции микросфер способствует введение в микросферы энзимов, таких как липаза, деполимераза и дегидрогеназа. Эти энзимы способствуют ресорбции под действием других эндогенных энзимов in vivo или свободных радикалов, генерированных телом (например, клетками макрофагами), которые могут атаковать структуральные связи, что приводит к деполимеризации биоресорбирующегося материала.
Возможно также, что некоторые присоединенные к микросферам или введенные в них вещества могут быть получены непосредственно от пациента. Например, фактор роста, полученный из пластинок крови (PDGF) (известный как способствующий заживлению раны), может быть получен из пластинок крови пациента и присоединен внутри микросфер или на их поверхности. Для этого необходим относительно небольшой образец крови, например, 100-200 мл.
Другие добавки включают: полиамины, уменьшающие гипертрофированные шрамы; вещества, придающие биостатичные, микробицидальные и антиотторгающие свойства, и протеиноиды, повышающие активность и/или стабильность.
Кроме того, факторы роста, миграции, ангиогенезиза и другие факторы могут быть введены внутрь или на поверхность дополнительных микросфер, на которые не предусматривается нанесения клеток. С этой целью можно использовать ультрамалые микросферы, так как не требуется использовать их в большом количестве, благодаря чему снижается количество материала, подлежащего ресорбции. Эти ультрамалые микросферы с диаметром от 10 до 50 мкн могут быть распределены вместе с большими покрытыми клетками микросферами в области раны либо введены дополнительно в нужный момент времени,
Окружающие ткани могут быть обработаны хемотактичными, ангиогенными и митогенными факторами, которыми покрывают поверхность таких не содержащих клеток микросфер, чтобы улучшить среду для миграции клеток, доставку питательных веществ, миграцию и рост. Другим преимуществом изобретения является то, что несмотря на относительно низкую стабильность этих факторов в растворе, они могут быть приготовлены в свежем виде непосредственно перед обработкой раны покрытыми клетками микросферами. Эти микросферы могут быть распределены и поданы одновременно с клетками или до них с тем, чтобы способствовать клеточной миграции, ангиогенезизу и/или быстрому размножению. Таким образом, может быть создана программируемая среда для ускоренной регенерации ткани и миграции в область раны, В результате может быть увеличена расположенная ниже капиллярная сеть для "нормального" питания нанесенных клеток.
Значительные успехи были достигнуты в последние несколько лет в создании культуральной среды, не содержащей полученной от животных сыворотки. Это особенно важно для технологий, предназначенных для применения в клиниках для людей. Сыворотка, обычно получаемая из бычачьих источников, не только является совершенно неопределенной, но может также служить источником загрязнений конечного продукта и привести к изменяющимся результатам. Определенная, не содержащая сыворотку среда является подходящей для культивирования дермальных фибробластов и кератиноцитов. В промышленности выпускается множество не содержащих сыворотки культуральных сред, например, Clonetics, Corporation KGM, FGM и GIBCO KGM.
В процессе сокультивирования кератиноцитов и дермальных фибробластов, кератиноциты требуют меньшего содержания кальция в среде для быстрого роста и предотвращения конечной дифференциации. При высоком содержании кальция (>0,1 мМ), кератиноциты имеют тенденцию к медленному росту и претерпевают конечную дифференциацию, приводящую к апоптозису (запрограммированной смерти клеток).
Дермальные фибробласты обычно выращивают в среде с содержанием кальция от 1 до 3 мМ, что обеспечивает их нормальный рост и функционирование соответственно, согласно одному из вариантов дермальные фибробласты сначала культивируют в среде с концентрацией кальция более 0,1 мМ. Через некоторое время клетки промывают раствором фосфатного буфера (PBS) in situ для удаления среды роста. Затем в тканевую культуральную колбу, содержащую культивированные дермальные фибробласты, добавляют кератиноциты и другую среду с пониженной концентрацией кальция. Результатом дальнейшего культивирования является снижение роста фибробластов и хороший рост кератиноцитов. Такие условия являются идеальными, так как они способствуют росту слоя кератиноцитов в присутствии фибробластов без роста фибробластов поверх кератиноцитов. Хотя фибробласты и не размножаются быстро, они могут произвести требующиеся кератиноцитам факторы для оптимального роста и построения дермальной поверхности. Факторы, произведенные фибробластами, которые способствуют оптимальному росту/организации кератиноцитов, включают фибронектин и TGF-бета.
Изобретение создает потенциал для географической централизации средств для обработки ран или ожогов в случаях действенной манипуляции клетками. Нанесение дермальных фибробластов при повреждениях всего или части кожного слоя может быть произведено более быстро при создании местного "банка" полученных от донора, включая умерших, дермальных фибробластов, проявляющих низкую аллергенность в трансплантатах.
Тканевый эксплантант, полученный от пациента, может затем транспортироваться в соответствующей транспортирующей среде, подобной используемой при транспортировании органов для трансплантации (такой как, ViaSpan (торговая марка) UW Solution, Dupont или другая сохраняющая среда) в центр разведения клеток для культивирования кератиноцитов, в то время как пациент уже будет обработан суспензией дермальных фибробластов с микросферами. Обычно тканевый эксплантант размером 4 см2 может быть быстро транспортирован и увеличен, если потребуется до размеров, достаточных для обработки эквивалентной тканевой площади размером несколько квадратных метров в течение от одной до трех недель.
Рост достаточного количества клеток для обработки происходит значительно скорее и более эффективно, чем при обычном описанном выше подходе.
После достижения необходимого размера клеток популяции, покрытые клетками микросферы, могут быть собраны, концентрированы и помещены в сохраняющую среду для доставки в удаленный центр обработки. В относительно небольшом объеме может быть на микросферах транспортировано большое число клеток, порядка 107 клеток/мл. В этом состоит преимущество перед плоскостной технологией, требующей большого числа контейнеров для эквивалентного количества клеток. Кроме того, транспортирование ячеистой матрицы затруднено хрупкой природой приготовления ткани. Суспензия микросфер с клетками согласно изобретению менее хрупка и все же может удовлетворительно переносить перевозки в далеко не идеальных условиях.
Покрытые клетками микросферы можно транспортировать в среде подобно используемой для транспортировки трансплантатов органов, таких как сердце. Более того, среда может быть адаптирована к включению перфторуглеводородов для лучшего переноса кислорода. Суспензия микросфер с клетками либо совсем не требует, либо требует небольшой дополнительной обработки перед нанесением на поврежденную кожу. Для их транспортирования могут быть также использованы известные технологии, такие как тангенциальные мембраны или мембраны из полого волокна, сохраняющие микросферы с клетками во время манипуляции со средой, в которой они находятся.
Ранее описанные имплантанты с ячеистой матрицей обычно крио-консервируют перед транспортировкой. Однако специалисту ясно, что крио-консервирующая среда может содержать диметилсульфоксид (DMSO), который требует сложной техники, включая стерильную среду, и множество операций, для чего необходима лаборатория тканевой культуры при получении и для удаления его перед имплантацией. Этот вид услуг не всегда имеется на месте, когда или где необходима обработка.
Изобретение позволяет производить быструю и эффективную обработку повреждений всего или части слоя поврежденной кожи, например, при ожогах и других ранах. В противоположность обычным методам изобретение не требует наложения швов или скобок или других методов закрепления при нанесении пациенту. Оно не сопряжено с проблемами, связанными с конфигурацией и изгибами тела. Более того, нанесение суспензии микросфер с клетками может быть осуществлено как в идеальных, так и далеко не идеальных условиях.
Заменитель живой кожи согласно изобретению может быть также использован как "модель кожи" при опасных и безопасных оценочных испытаниях веществ для фармацевтической, косметической промышленности и бытовой сферы. Эта область расширяется благодаря требованиям к хитрым испытаниям на животных.
Изобретение может быть также использовано в косметике для исправления дефектов кожи.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИОННЫЙ ЭКВИВАЛЕНТ ЖИВОЙ КОЖИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ТЕСТ-НАБОР | 1991 |
|
RU2135191C1 |
| ЭКВИВАЛЕНТ КОЖИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2342164C2 |
| СКОНСТРУИРОВАННЫЙ ЭКВИВАЛЕНТ КОЖИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРОДУКТЫ, ПОЛУЧАЕМЫЕ ИЗ НЕГО | 2017 |
|
RU2820590C2 |
| ОККЛЮДЕР ДЛЯ ЧРЕЗКОЖНОЙ ТРАНСЛЮМИНАЛЬНОЙ ПРОЦЕДУРЫ (ВАРИАНТЫ), СПОСОБ ЧРЕЗКОЖНОГО ТРАНСЛЮМИНАЛЬНОГО ЗАКРЫТИЯ ОТВЕРСТИЯ В СЕРДЦЕ, СПОСОБ АКТИВИЗАЦИИ ВАСКУЛЯРИЗАЦИИ ТКАНИ МЛЕКОПИТАЮЩЕГО IN VIVO И СПОСОБ АКТИВИЗАЦИИ ЗАЖИВЛЕНИЯ МЕСТА АНАСТОМОЗА | 2007 |
|
RU2470611C2 |
| СПОСОБ ЛЕЧЕНИЯ СОСТОЯНИЯ РОТОВОЙ ПОЛОСТИ БОЛЬНОГО (ВАРИАНТЫ) | 2007 |
|
RU2498808C9 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОЖНОГО ПОКРОВА | 2016 |
|
RU2658707C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОЖНОГО ПОКРОВА | 2016 |
|
RU2644633C1 |
| СПОСОБ ТЕРАПИИ КОСМЕТИЧЕСКИХ ДЕФЕКТОВ КОЖИ | 2024 |
|
RU2831472C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ВРОЖДЕННЫМ БУЛЛЕЗНЫМ ЭПИДЕРМОЛИЗОМ ПУТЕМ КОМБИНИРОВАННОГО ПРИМЕНЕНИЯ АЛЛОГЕННЫХ ФИБРОБЛАСТОВ ЧЕЛОВЕКА И ЖИВОГО ЭКВИВАЛЕНТА КОЖИ | 2020 |
|
RU2779997C2 |
| БИОЛОГИЧЕСКИЙ АКТИВНЫЙ КОМПЛЕКС ДЛЯ ОРГАНОГЕНЕЗА | 2003 |
|
RU2254146C2 |





Изобретение относится к медицине, в частности к имплантологии. Предложен заменитель живой кожи для обработки части или всего слоя поврежденной кожи, например при ожогах и ранах, состоящий из суспензии покрытых клетками микросфер, который может быть нанесен на поврежденную кожу аналогично пасте или мази. Имплантант кожи может приспосабливаться к контурным изменениям повреждений кожи обширной площади и не требует наложения швов, скобок или других методов закрепления. Микросферы могут быть выполнены из различных биосовместимых и ресорбирующихся in vivo материалов. 3 с. и 23 з.п. ф-лы, 12 ил.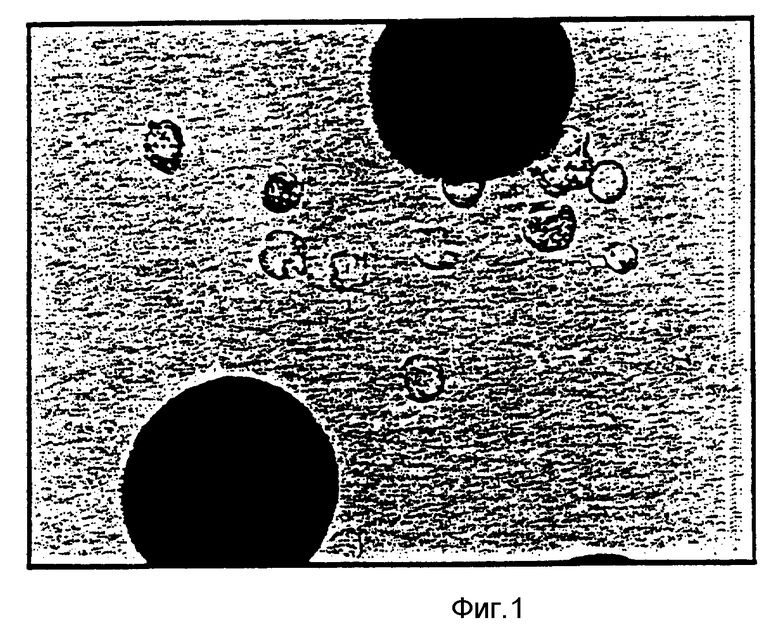
| US, патент 4996154, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1998-02-10—Публикация
1993-04-23—Подача