Изобретение относится к медицине, а именно к методам эфферентной медицины в хирургии.
Известен метод экстракорпорального лазерного облучения крови, применяемый с целью продления сроков ремиссии в процессе обменного плазмафереза при возвращении больному эритроцитарной массы и введении донорских плазмозамещающих препаратов, при аутоимунных заболеваниях. При этом у больного производят эксфузию крови в количестве 500 мл в полимерный контейнер "Гемакон-500". Затем контейнер с кровью центрифугируют таким образом, что эритроциты оседают, а плазма крови и взвешенные в ней ферментные элементы остаются над осадком. Плазму, содержащую иммунокомпетентные клетки, патологические иммуноглобулины, компонент,сливают. Эритроциты ресуспензируют в 50 мл физраствора и реинфундируют больному, облучая их монохроматическим лазерным излучением. Процедура повторяется последовательно несколько раз (3-5). В результате за один сеанс удаляется в среднем 1000 мл плазмы больного и 3 х 10 - 4 х 10 лейкоцитов. В конце процедуры плазмопотеря компенсируется белковыми и солевыми растворами: свежезамороженной донорской плазмой, альбумином и т.д. [1]. Данный способ принят нами за прототип.
Недостатком этого метода является то, что отсутствует точный метрологический контроль, отсутствует точный учет энергии,потерянной в результате рассеяния, отсутствует непосредственное воздействие лазерного излучения на иммунокомпетентные клетки, т.к. облучаются отдельно аутоэритроциты и отдельно донорская плазма (если плазмопотеря компенсируется ею). Кроме того, условия замораживания и хранения донорской плазмы, содержащей определенное число иммунокомпетентных клеток, не позволяют сохранить их в живом виде. Применение лазерного излучения с целью стимуляции иммунокомпетентных клеток после размораживания плазмы вряд ли можно считать целесообразным и методологически оправданным способом иммуностимуляции, т. к. для сохранения жизнеспособных клеток крови требуются иные условия замораживания и хранения, отличные от условий заготовки и хранения донорской плазмы.
Цель изобретения - повышение эффективности лечения больных с гнойно-септическими осложнениями заболеваний органов брюшной полости путем сокращения сроков иммунореабилитации и снижения клинико-лабораторных проявлений синдрома эндогенной интоксикации.
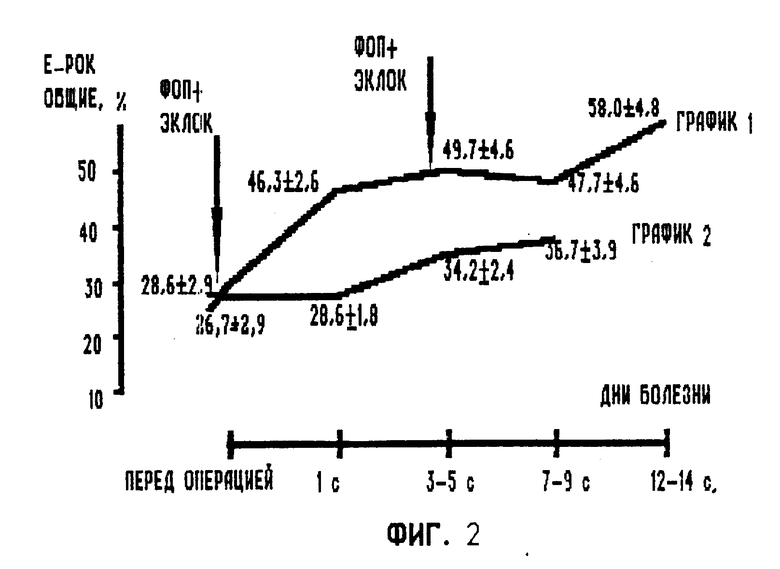
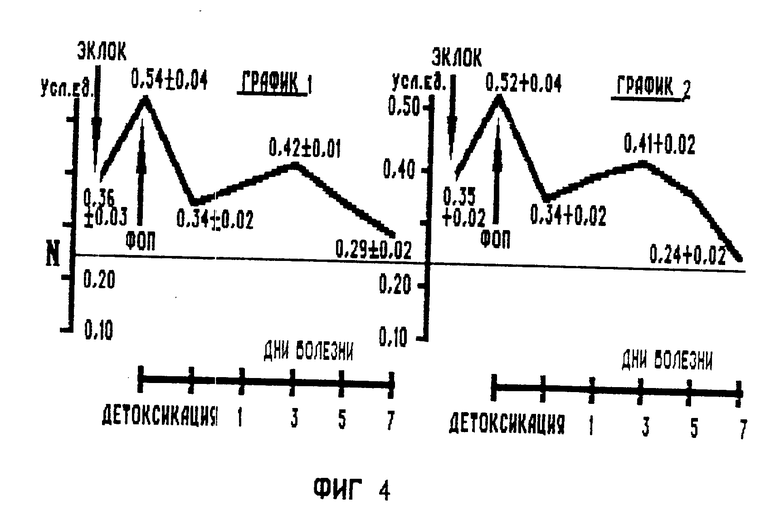
На фиг. 1 изображена схема экстракорпорального лазерного облучения крови в сочетании с фильтрационным обменным плазмаферезом: роликовый насос 1, лазерный излучатель 2 "Узор", насадка на коммутирующую магистраль 3, плазмофильтр 4, воздушная ловушка 5; на фиг.2 - динамика лимфоцитов (E-POK активные) при проведении ЭКЛОК в сочетании с ФОП (график 1) и в группе сравнения (график 2); на фиг. 3 - динамика средних молекул Е254 (график 1) и Е280 (график 2) в процессе проведения ЭКЛОК в сочетании с ФОП; на фиг. 4 - динамика средних молекул Е254 (график 1) и Е280 (график 2) в процессе проведения ЭКЛОК в сочетании с ФОП.
Поставленная цель достигается тем, что облучение проводят в непрерывном экстракорпоральном контуре, рассчитывая дозу поглощения по формуле Wпогл. = I • K осл. • ft, где I -мощность излучения;T - время экспозиции,с;Rосл. - коэффициент ослабления (учитывает ослабление сферы и ослабление стенки трубки, равен 0,24); f - частота импульсов;t - длительность лазерного импульса (для аппарата "Узор" 7•10-9 с); фильтрационный обменный плазмаферез (ФОП) осуществляется в течении 20-30 мин при скорости экстракорпорального кровотока от 75 до 100 мл/мин, объемом плазмафереза 1200-1500 мл и адекватном восполнении плазмопотери донорской плазмой (фиг. 1).
Экстракорпоральное лазерное облучение крови осуществляют с помощью лазерного излучателя "Узор" и специально сконструированного разъемного сферического устройства, которое представляет собой замкнутую металлическую сферу (шар), обработанную изнутри специальным покрытием. Через нее проходит стандартная кровопроводящая магистраль от аппарата для фильтрационного плазмафереза, облучаемая лазерным излучением, которое подается от излучателя "Узор" по световоду. Такое подключение обеспечивает равномерное облучение протекающей массы крови, минимальные потери энергии и точный количественный учет поглощенной дозы (как суммарный, так и в пересчете на единицу объема крови).
Экстракорпоральное лазерное облучение предполагает воздействие на кровь через стенку прозрачных кровопроводящих магистралей. При этом отсутствует необходимость введения световода в сосудистое русло, облучение крови происходит без воздействия на сосудистую стенку и паренхиму окружающих сосуд органов. Кроме того, ЭКЛОК можно применять одновременно с различными методами экстракорпоральной детоксикации, в данном случае с фильтрационным обменным плазмаферезом (ФОП).
Плазмаферез осуществляется с помощью мембранного плазмафильтра в едином с ЭКЛОК замкнутом экстракорпоральном контуре. Длительность ЭКЛОК составляет 20-30 мин при скорости экстракорпорального кровотока 75-200 мл/мин, мощность излучения - 40 Вт, частота - 1500 Гц, количество крови, подвергнутой облучению,1500-3000 мл. После проведения ЭКЛОК начинают процесс плазмофильтрации в следующем режиме:
Скорость кровотока - 75-100 мл/мин
Трансмембранное давление - Менее 100 mm Hg
Давление в венозной магистрали аппарата - Менее 150 mm Hg
Объем плазмафереза - 1200-1500 мл
Для оценки эффективности применения экстракорпорального лазерного облучения крови (ЭКЛОК) в сочетании с ФОП учитывалось исходное состояние показателей клеточного и гуморального иммунитета больных. Иммунологические исследования, проводимые до сеансов ЭКЛОК в сочетании с ФОП, позволяют разделить больных на три группы в зависимости от показателей клеточного звена иммунитета (Е-РОК общие, Е-РОК активные): больные со сниженным количеством розеткообразующих Т лимфоцитов, больные с количеством Е-РОК общих и Е-РОК активных в пределах нормы, больные с повышенными значениями Е-РОК общих и Е-РОК активных. Иммунологический контроль осуществляли в динамике:при поступлении в клинику, до и после сеансов ЭКЛОК в сочетании с ФОП, на 3-5- и 7-9-е сутки. Сеансы ЭКЛОК в сочетании с ФОП проводили на 1-2-е сутки после операции с интервалом в 1-2 дня, в зависимости от клинических проявлений, степени интоксикации и уровня иммунологических показателей.
Детоксикационный эффект учитывали по динамике изменения лейкоцитарного индекса интоксикации, токсичности крови, количеству среднемолекулярных пептидов (СМ).
Изучая влияние ЭКЛОК на организм больного, мы установили, что помимо положительного влияния экстракорпорального лазерного облучения на клеточное звено иммунитета (фиг. 2, 3) в ряде случаев наблюдается увеличение концентрации в крови СМ (фиг. 4). Последовательное проведение лазерного облучения крови больного и ФОП позволяет устранить нежелательное побочное действие низкоинтенсивного лазерного излучения (НИЛИ) и является оптимальным решением проблемы.
Пример 1. Больная Б. (Беляева Н.А., и/б N 8935), 27 лет, оперирована в районной больнице по поводу о. гангренозно-перфоративного аппендицита, диффузного перитонита на вторые сутки от начала заболевания. Выполнена аппендэктомия, произведена санация и дренирование брюшной полости. В послеоперационном периоде лихорадка до 38,5, нарастающая интоксикация. На седьмые сутки после операции произведена релапаротомия, санация и дренирование брюшной полости по поводу разлитого гнойного перитонита. В дальнейшем состояние больной прогрессивно ухудшалось, прогрессировал перитонит, нарастали явления интоксикации и больная переведена в МОНИКИ 06.07.94 г.При поступлении состояние больной очень тяжелое. Картина токсической энцефалопатии, больная вялая, заторможена. При осмотре диагностирован разлитой перитонит и больная срочно оперирована. Произведена релапоротомия. В брюшной полости большое количество гнойного выпота с колибациллярным запахом (при бактериологическом исследовании обнаружен рост кишечной палочки), выявлены множественные абсцессы. Петли тонкой кишки отечны, гиперемированны, покрыты фибрином. Произведена назоитестинальная интубация тонкой кишки, санация и дренирование брюшной полости. Через сутки произведен этапный лаваж брюшной полости. Несмотря на проводимую массивную детоксикационную, антибактериальную терапию в послеоперационном периоде состояние больной оставалось крайне тяжелым - нарастали явления токсической энцефалопатии, гепатопатии. Возникло угрожающее жизни состояние. Учитывая явления перитонита в фазе полиорганной недостаточности, а также состояние вторичного иммунодефицита (количество Е-РОК общих и Е-РОК активных было снижено более чем в 2 раза), проведен сеанс ЭКЛОК в течении 30 мин с последующим фильтрационным плазмаферезом (с заменой 1,2 л плазмы). Процедура повторена через двое суток. В результате комплексной терапии состояние больной значительно улучшилось, уменьшились явления интоксикации, купированы явления перитонита, полиорганной недостаточности. Постепенное выздоровление. Показатели клеточного звена иммунитета в динамике также улучшились, и на 7-9-е сутки болезни практически приближалось к норме. Отмечена выраженная положительная динамика ЛИИ (до процедуры 2,8, через сутки 1,7, через семь суток 1,5), средние молекулы до ЭКЛОК 0,38, после ЭКЛОК0,48, после ФОП 0,32. Исследование токсичности плазмы крови, проведенное методом гемокультуры,выявило исходное увеличение токсичности плазмы до 56,1 у. е. и снижение ее до 33,5 у. е., после проведения комбинированной процедуры детоксикации.
Пример 2. Больной К. (Комаров М.А. и/б N 10774), 54 года, находился в районной больнице в течение семи суток после тупой травмы живота, не оперирован. 24.08.90 года, в крайне тяжелом состоянии переведен в абдоминальное отделение МОНИКИ. При осмотре состояние крайне тяжелое, диагностирован разлитой перитонит в фазе полиорганной недостаточности. Произведена срединная лапоротомия, выявлен каловый перитонит, вследствие разрыва сигмовидной кишки. Выполнена резекция участка сигмовидной кишки, наложена трансверзостома, НИИ, санация и дренирование брюшной полости. С интервалом в сутки дважды проводился програмный лаваж брюшной полости. В комплексное лечение были включены два сеанса сочетанного применения ЭКЛОК и ФОП. Непосредственно после второго сеанса наступило улучшение общего состояния, уменьшились явления токсической энцефалопатии, гепатопатии, купировались явления перитонита. Одновременно улучшились и биохимические показатели гомеостаза. Токсичность сыворотки снизилась с 34 до 16%. Уровень средних молекул с 0,37 (Е254) и 0,32 (Е280) до 0,21 и 0,17 соответственно. Е-РОК общие с 30 до 58%, Е-РОК активные - с 15 до 39%.
Пример 3. Больная П. (Пройдакова Е.Б. и/б N 1934), 40 лет, оперирована в районной больнице по поводу о. деструктивного аппендицита, местного перитонита. На десятые сутки с момента заболевания в связи с ухудшением состояния переведена в абдоминальное отделение МОНИКИ. При поступлении состояние больной очень тяжелое, выраженные явления эндотоксикоза вследствие прогрессирующего п/операционного перитонита. Больная срочно оперирована, во время операции обнаружена несостоятельность культи ч/образного отростка, поддиафрагмальный, подпеченочный абсцессы справа, гнилостная забрюшинная флегмона справа. В послеоперационном периоде больной дважды выполнены сеансы ЭКЛОК в сочетании с ФОП. В результате комплексной терапии значительно уменьшились явления интоксикации, купировались явления перитонита. Отмечено улучшение ряда показателей (снижение токсичности сыворотки, уровня средних молекул, ЛИИ, нормализовались показатели клеточного звена иммунитета). Постепенное выздоровление.
Таким образом, применение ЭКЛОК в сочетании с ФОП способствует повышению эффективности лечения больных с гнойно-септическими осложнениями заболеваний органов брюшной полости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения гнойно-септических заболеваний | 1985 |
|
SU1298281A1 |
| СПОСОБ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 1991 |
|
RU2005513C1 |
| СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ РАЗЛИТЫМ ГНОЙНЫМ ПЕРИТОНИТОМ | 1992 |
|
RU2038097C1 |
| СПОСОБ ДЕТОКСИКАЦИИ ПРИ СИНДРОМЕ ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ С ГНОЙНО-СЕПТИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ | 1999 |
|
RU2161509C1 |
| Способ детоксикации организма | 1989 |
|
SU1811858A1 |
| Способ лечения разлитого гнойного перитонита | 1986 |
|
SU1521459A1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ АУТОИММУННЫМИ ЗАБОЛЕВАНИЯМИ | 1999 |
|
RU2159635C2 |
| СПОСОБ ЛЕЧЕНИЯ СЕПСИСА У ДЕТЕЙ | 2001 |
|
RU2209071C2 |
| Способ детоксикации организма | 1988 |
|
SU1659058A1 |
| СПОСОБ ЛЕЧЕНИЯ ДЫХАТЕЛЬНОГО КРИЗА ПРИ МИАСТЕНИИ | 1995 |
|
RU2119355C1 |

Предлагается способ лечения иммунодефецита при гнойно-септических осложнениях заболеваний органов брюшной полости, включает лазерное облучение крови и фильтрационный обменный плазмаферез в непрерывном экстракорпоральном контуре. Облучение проводят в течение 20-30 мин при мощности излучения 3,5 - 4,0 Вт, частоте импульсов 1450 - 1500 Гц, длительности импульса 7 х 10 с и скорости экстракорпорального кровотока 75 -1000 мл/мин с одновременным фильтрационным обменным плазмаферезом в объеме 1200 - 1500 мл и адекватным возмещением плазмопотери донорской плазмой. 4 ил.
Способ лечения вторичного иммунодефицита при гнойно-септических осложнениях заболеваний органов брюшной полости, включающий лазерное облучение крови и фильтрационный обменный плазмаферез в непрерывном экстракорпоральном контуре, отличающийся тем, что облучение проводят в течение 20 30 мин при мощности излучения 3,5 4,0 Вт, частоте импульсов 1450 1500 Гц, длительности импульса 7 х 10 с и скорости экстракорпорального кровотока 75 - 100 мл/мин с одновременным фильтрационным обменным плазмаферезом в объеме 1200 1500 мл и адекватным возмещением плазмопотери донорской плазмой.
| RU, патент, 2005513, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1998-02-10—Публикация
1995-11-10—Подача