Изобретение относится к медицине, конкретно, к лекарственным средствам применяемым при лечении ишемической болезни сердца, и аритмий, ее осложняющих.
Проблема профилактики и лечения ишемической болезни сердца весьма актуальна, поскольку смерть больных, страдающих заболеваниями сердечно-сосудистой системы, занимает первое место в мире среди летальных исходов от других болезней.
Кроме того, ишемическая болезнь сердца подчас осложняется тяжелой аритмией, и при лечении данного заболевания приходится применять комбинацию препаратов с противоишемическим и антиаритмическим действием, что далеко не всегда дает положительный результат.
Целью изобретения является создание лекарственного средства для лечения ишемической болезни сердца и аритмии ее осложняющей, и разработка способа его получения с высоким выходом.
Поставленная цель достигается N-(2,4,6-триметилфенилкарбамоилметил)-N-аллилморфолиний бромидом формулы (1):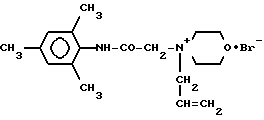
Исследование фармакологической активности 1.
1. Противоишемическая активность 1.
Указанный эффект 1 изучали на белых нелинейных крысах массой 250-300 г по известной методике, которая позволяет оценить влияние испытуемого вещества на размеры зон ишемии и некроза в остром периоде инфаркта миокарда. В качестве препарата сравнения использовали обзидан, антиишемическое действие которого известно (Машковский М. Д. Лекарственные средства. М. Медицина, 1993, ч.1, с.330-332).
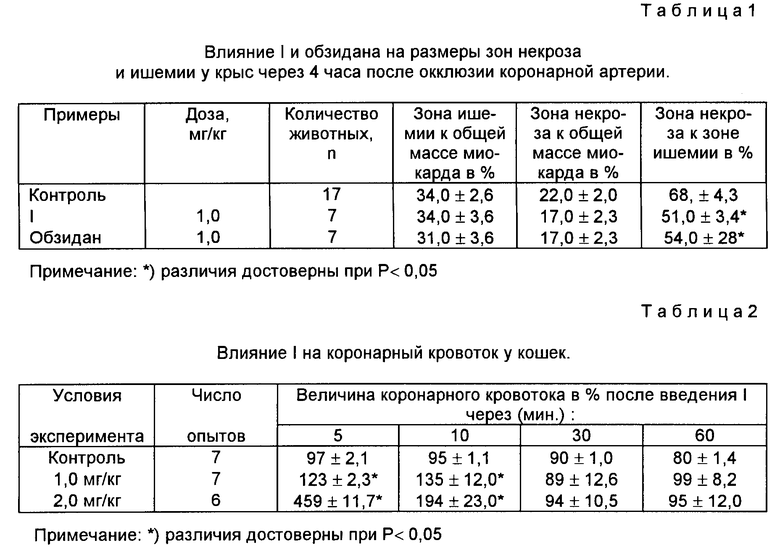
Результаты проведенных исследований представлены в табл.1.
Из представленных данных следует, что 1 уменьшает размер зоны некрозы по отношению к зоне ишемии и этот эффект препарата соответствует препарату сравнения-обзидану.
2. Влияние 1 на коронарный кровоток.
Определение влияния 1 на коронарный кровоток проводили по известной методике Н. В.Кавериной на наркотизированных этаминал-натрием (50 мг/кг внутрибрюшинно) кошках, переведенных на управляемое дыхание. После вскрытия грудной клетки и канюлирования коронарного синуса кровоток из него направляли в яремную вену таким образом, чтобы с помощью тройника в нужный отрезок времени можно было проводить забор венозной крови из коронарных сосудов в мерную емкость. Каждый раз забор оттекающей крови продолжали на протяжении 15 с. Собранное количество крови умножали на 4 и получали объемную скорость кровотока за 1 мин. После введения 1 исследование коронарного кровотока производили через 5, 15, 30 и 60 мин.
Результаты представлены в табл.2.
Из приведенных данных видно, что 1 в дозе 1 мг/кг и еще более в дозе 2 мг/кг повышает объемную скорость коронарного кровотока в первые 10 мин наблюдения.
3. Противоаритмическая активность 1 в острую фазу экспериментального инфаркта миокарда.
Исследования проведены на беспородных собаках массой 8-25 кг и кошках массой 2-4 кг. Нарушение коронарного кровообращения вызывали у наркотизированных гексеналом (50 мг/кг внутрибрюшинно) животных путем наложения лигатуры на верхнюю треть нисходящей ветви левой коронарной артерии.
В качестве препарата сравнения использован лидокаин, который считается препаратом выбора при лечении аритмий в острую фазу инфаркта миокарда.
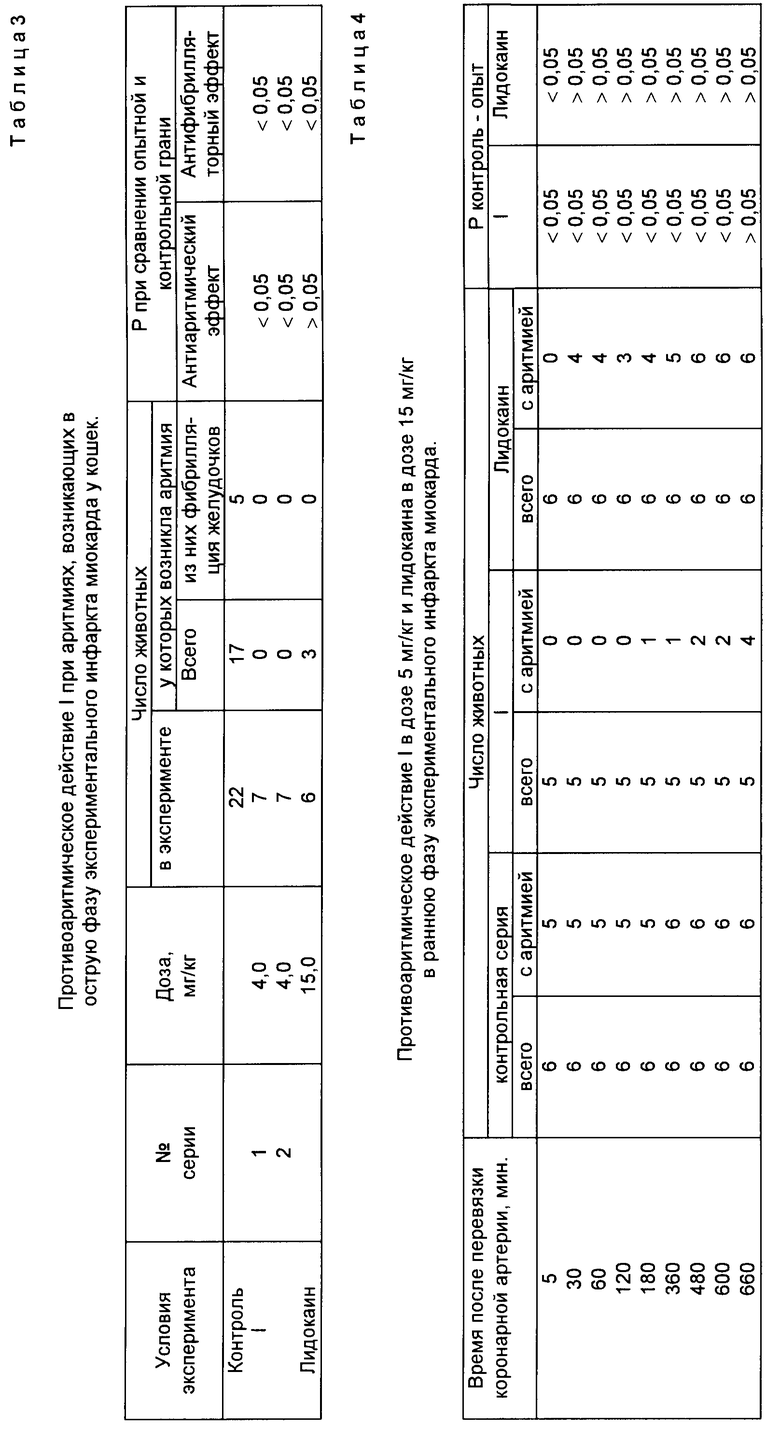
Результаты исследования 1 на кошках представлены в табл.3, на собаках в табл.4.
Результаты, приведенные в табл.3, свидетельствуют, что 1 превосходит лидокаин по противоаритмической активности на модели желудочковой аритмии у кошек, вызванной перевязкой коронарной артерии, а по противофибрилляторному действию 1 не отличается от препарата сравнения.
Важно отметить, что 1 не только предупреждает наступление желудочковой аритмии и фибрилляции желудочков, но способен купировать уже возникшую аритмию. Об этом свидетельствует вторая серия экспериментов, проведенная с препаратом, который вводился на фоне уже возникшей аритмии (табл.3,серия 2).
Такие же данные получены при исследовании противоаритмической активности 1 в острый период нарушения коронарного кровообращения у собак (табл.4). Внутривенное введение 1 после наложения лигатуры на коронарный сосуд позволяет предупредить наступление аритмии у большинства животных на протяжении 10 ч.
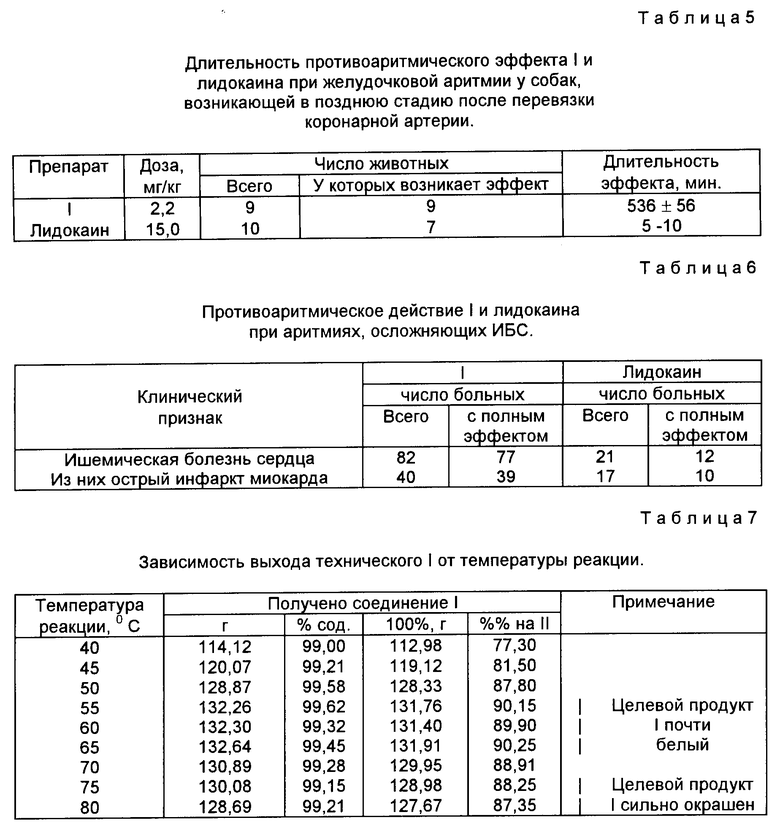
Противоаритмический эффект лидокаина в дозе 15 мг/кг в аналогичных условиях эксперимента сохраняется менее 30 мин. 1 также оказывает выраженное противоаритмическое действие и в поздние сроки после нарушения коронарного кровообращения у собак, восстанавливая синусовый ритм у всех животных на 536±56 мин (табл. 5). В аналогичных условиях эксперимента антиаритмический эффект лидокаина продолжается 5-10 мин.
Таким образом, 1 обладает выраженной противоаритмической активностью при нарушениях сердечного ритма, возникающих в результате ишемии миокарда. 1 выгодно отличается от лидокаина большей активностью и более длительным противоаритмическим эффектом.
Важной особенностью 1 является сочетание антиаритмического и противоишемического действия, что делает это средство препаратом выбора при лечении аритмии в острую фазу инфаркта миокарда.
4. Противоаритмическая активность 1 у больных с ишемической болезнью сердца.
Противоаритмическую активность 1 исследовали в виде острого лекарственного теста. Оценку противоаритмического действия 1 производили с помощью аппарата "Лента-МТ", который позволял проводить динамическую электрокардиографию с последующим анализом записи. Фоновый холтеровский контроль ЭКГ проводили больным, у которых отсутствовали показания для экстренного купирования аритмии, а при наличии таковых тип и класс аритмии определяли путем кардиомониторирования на протяжении 30-120 мин или записи ЭКГ-12.
В табл. 6 приведены сравнительные данные противоаритмического действия 1 и лидокаина при аритмиях, осложняющих ИБС.
1 использован для купирования желудочковой аритмии 82 больным, страдающим ишемической болезнью сердца, среди них у 40 больных имел место острый инфаркт миокарда.
Внутривенное введение 1 вызвало полное и стабильное подавление желудочковой аритмии у 39 больных с острым инфарктом миокарда, а у одного больного имело место заметное (более чем на 50%) снижение частоты желудочковой экстрасистолии. У других 42 больных с ишемической болезнью сердца противоаритмический эффект 1 проявился у 38 больных. Приведенные данные свидетельствуют о высокой противоаритмической активности 1 при желудочковых аритмиях ишемического генеза.
Лидокаин, являющийся антиаритмиком выбора при лечении аритмий ишемического происхождения, особенно в острую фазу инфаркта миокарда, проявил полный противоаритмический эффект при аритмиях, осложняющих острый период инфаркта миокарда у 10 больных из 17, что достоверно ниже при сравнении с 1 (Р < 0,05).
У 73% больных с ИБС, имевших загрудинные боли, введение 1 сопровождалось либо полным исчезновением болевого синдрома, либо его заметным уменьшением.
5. Антиангинальная активность (ААА) 1.
Обследовано 11 мужчин в возрасте от 30 до 60 лет со стенокардией напряжения II и III функционального классов.
Для выявления и объективизации ААА 1 использовали метод парных велоэргометрий (ВЭМ). Каждому больному проводилась диагностическая стандартная непрерывная ступенчатовозрастающая ВЭМ. За 1 ч до проведения второй ВЭМ внутривенно вводили 1 в дозе 1,5 мг/кг. Нагрузку прекращали при депрессии сегмента ST на 1 мм и более на расстоянии 0,08 с от точки j в сочетании с приступом стенокардии. Критерием ААА считали увеличение продолжительности нагрузки на фоне применения препарата не менее чем на 2 мин.
У 7 (64%) больных зарегистрировано антиишемическое действие 1. И хотя у остальных пациентов 1 был неэффективен по принятым критериям, у всех отмечено повышение толерантности к физической нагрузке: увеличение времени или мощности нагрузки и общего объема выполненной работы от 8 до 125% (в среднем на 40%).
Нитросорбид, являющийся эталонным препаратом этих исследований, в дозе 10 мг не уступает по выраженности антиангинального действия 1. Лишь в одном случае 1 был эффективнее нитросорбида. Следует отметить, что у двух больных оба препарата в исследуемых дозах оказались неэффективными.
Из полученных результатов следует, что 1 обладает антиишемическим действием, примерно соответствующим нитросорбиду.
Представленные результаты убедительно свидетельствуют, что 1 обладает антиишемической и антиангинальной активностью. Эти эффекты 1, нашедшие экспериментальное и клиническое подтверждение, сочетаются с выраженной противоаритмической активностью, которая, в отличие от лидокаина, сохраняется до 10 ч. Наиболее ярко противоаритмическое действие 1 проявляется, как в эксперименте, так и в клинике, в острую фазу инфаркта миокарда.
Совокупность перечисленных фармакологических свойств 1 делает препарат весьма перспективным для совершенствования фармакотерапии острого периода инфаркта миокарда.
Способ получения 1 заключается во взаимодействии N-(2,4,6-триметилфенилкарбамоилметил)морфолина (II) с бромистым аллилом (III) в среде изопропилового спирта при мольном соотношении II:III как 1:1,4-1,6, соответственно, при температуре 55-65o С. Целевой продукт выделяют фильтрацией выпавшего 1 после охлаждения реакционной массы до комнатной температуры. Получают 1 в виде почти белого кристаллического порошка с выходом 90% считая на II, т.пл. 172-176oС (в интервале двух градусов). После перекристаллизации из изопропилового спирта получают фармакопейный 1.
Способ по изобретению иллюстрируется следующим примером.
Пример. Смешивают 400 мл изопропилового спирта, 100,3 г 99,7%-ного, 100 г (0,38 моль) 100%-ного II и 50 мл (0.58 моль) III. Смесь выдерживают при 55-65oС в течение 7 ч, затем охлаждают до комнатной температуры. Выпавший осадок 1 отфильтровывают, промывают изопропиловым спиртом. Получают 132,3 г 99,4%-ного или 131,5 г 100%-ного 1, что составляет 90,0 от теории, считая на II, т.пл. 172-173,5oС. После перекристаллизации из изопропилового спирта получают фармакопейный 1.
Соединение I легко растворимо в воде, нерастворимо в эфире, хлороформе.
Найдено, N 7,6; Br 20,6.
С18Н27N2O2Br.
Вычислено, N 7,31; Вr 20,84.
Чистоту и индивидуальность продуктов реакции проверяют тонкослойной хроматографией на пластинках "Silufol UV-254" в системе растворителей хлороформ этанол 95% кислота уксусная 95 4,5 0,5 с проявлением в камере для хлорирования над смесью 3%-ный раствор калия перманганата 15%-ный раствор кислоты хлористоводородной. Пластинку после подсушивания опрыскивают раствором о-толидина.
ПМР спектр снят на приборе Hitachl Perkin elmer, рабочая частота 90 МГц, внутренний стандарт гексаметилдисилоксан, температура 35oС. Растворитель дейтерированный диметилсульфоксид и ацетон. Химические сдвиги протонов (м.д. ) приведены по шкале δ. Сигналы протонов: 3,75-4,10 м.д. М(СН2)4 8Н морфолина; 4,52 м.д. (СН2) 2Н аллила; 4,81 м.д. с (СН2)-2Н уксусной кислоты; 5,56 5,91 м.д. М(СН2)-2Н аллила; 5,91 6,5 м.д. М(СН)-1Н аллила; 6,81 м.д. с (2Н)- 3,5Н ароматика; 10,38 м.д. с (NH).
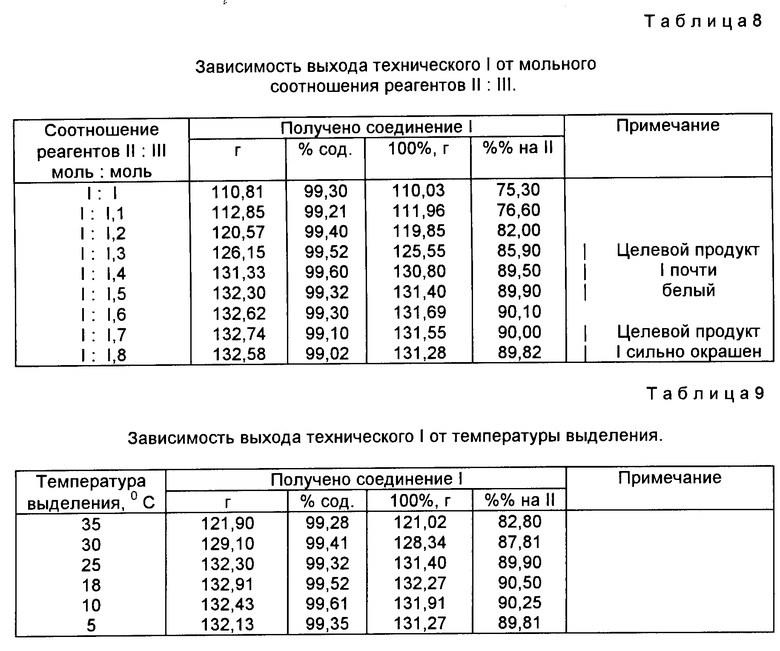
Указанные в примере параметры процесса получения 1 найдены экспериментальным путем и являются оптимальными, подтверждением чего являются результаты экспериментов, приведенные в табл. 7-9.
Важным параметром проведения процесса является температура реакции. Как показал эксперимент, оптимальный интервал температур 55-65oС. При более низких температурах реакция до конца не доходит, снижается выход целевого продукта 1. При более высоких температурах наблюдается осмоление реакционной массы, целевой продукт 1 подвергается деструкции с образованием исходного продукта II, в результате получают целевой продукт 1, не удовлетворяющий требованиям по цветности, посторонним примесям.
Как следует из табл.8, оптимальное мольное соотношение реагентов II:III при проведении реакции 1:1,4-1,6, соответственно. Уменьшение количества III приводит к существенному снижению выхода, а увеличение количества его недопустимо из-за ухудшения качества целевого продукта 1.
Как видно из табл.9, оптимальной температурой выделения соединения 1 является комнатная температура 18-25oС. Снижение температуры не приводит к сколько-нибудь существенному увеличению выхода, при повышенных температурах наблюдаются потери в выходе.
Кроме того, в процессе получения 1 было проверено использование других растворителей. При этом выход 1 был ниже. чем в предлагаемом способе, а в отдельных случаях и более низкое качество 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОЛОНГИРОВАННОЙ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2538674C2 |
| ГАММА-ГИДРОКСИПРОПИЛАМИНИЙ-5-ГИДРОКСИНИКОТИНАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2245329C1 |
| СОЛИ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ ПРОИЗВОДНЫХ И 5-ГИДРОКСИНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНТИАНГИНАЛЬНЫМИ И ПРОТИВОАРИТМИЧЕСКИМИ СВОЙСТВАМИ | 1993 |
|
RU2067577C1 |
| 2-(Диэтиламино)-N-(2,6-диметилфенил)ацетамида L-глутаминат, обладающий пролонгированной противоаритмической активностью, фармацевтическая композиция | 2018 |
|
RU2697717C1 |
| Фармацевтическая композиция, обладающая антиаритмической активностью различной этиологии | 2021 |
|
RU2783944C1 |
| ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, ПРОЯВЛЯЮЩИЕ АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 1999 |
|
RU2164512C1 |
| ПРОТИВОИШЕМИЧЕСКОЕ И АНТИАТЕРОСКЛЕРОТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1998 |
|
RU2144822C1 |
| ЩЕЛОЧНЫЕ СОЛИ АМИДОВ ОРОТОВОЙ КИСЛОТЫ И АМИНОКИСЛОТ, ОБЛАДАЮЩИЕ ГИПЕРТЕНЗИВНЫМ ЭФФЕКТОМ | 1995 |
|
RU2086543C1 |
| ПРИМЕНЕНИЕ 2-МЕТИЛЕН-1,3-ДИНИТРОКСИПРОПАНА В КАЧЕСТВЕ ПРОТИВОИШЕМИЧЕСКОГО СРЕДСТВА | 2015 |
|
RU2580929C1 |
| ЧЕТВЕРТИЧНОЕ АММОНИЕВОЕ ПРОИЗВОДНОЕ ЛИДОКАИНА, ОБЛАДАЮЩЕЕ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2258700C1 |
Новое химическое соединение - N-(2,4,6-триметилфенилкарбамоилметил)-N-аллилморфолиний бромид формулы 1 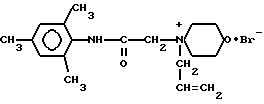 проявляет в эксперименте на животных, а также в клинических условиях противоишемическое и антиаритмическое действие при ишемической болезни сердца и может быть использовано для создания перспективного лекарственного средства для лечения ишемической болезни сердца. Способ получения соединения 1, заключающийся во взаимодействии N-(2,4,6-триметилфенилкарбамоилметил) морфолина с бромистым аллилом при мольном соотношении 1:1,4-1,6, соответственно, в среде изопропилового спирта при температуре 55-65oС с последующим отделением целевого продукта после охлаждения реакционной массы до комнатной температуры. Выход 90%, содержание основного вещества не менее 99%. 2 с.п.ф-лы, 9 табл.
проявляет в эксперименте на животных, а также в клинических условиях противоишемическое и антиаритмическое действие при ишемической болезни сердца и может быть использовано для создания перспективного лекарственного средства для лечения ишемической болезни сердца. Способ получения соединения 1, заключающийся во взаимодействии N-(2,4,6-триметилфенилкарбамоилметил) морфолина с бромистым аллилом при мольном соотношении 1:1,4-1,6, соответственно, в среде изопропилового спирта при температуре 55-65oС с последующим отделением целевого продукта после охлаждения реакционной массы до комнатной температуры. Выход 90%, содержание основного вещества не менее 99%. 2 с.п.ф-лы, 9 табл.
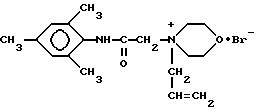
проявляющий противоишемическое и антиаритмическое действие при ишемической болезни сердца.
Авторы
Даты
1998-02-27—Публикация
1997-06-24—Подача