Изобретение относится к медицине и может найти применение в медицинской практике для коррекции нарушений ритма сердечной деятельности.
Известно соединение N-(2,4,6-триметилфенилкарбамоилметил)-N-аллилморфолиний бромид под названием кватернидин, проявляющий противоишемическое и антиаритмическое действие при ишемической болезни сердца (RU 2105554, МПК 6 А 61 К 31/535, С 07 D 29/037, опубл. 1997).
Недостатком известного решения является его высокая токсичность и малая широта терапевтического действия.
Технический результат заключается в уменьшении острой токсичности, увеличении широты терапевтического действия и снижении смертности лабораторных животных при хроническом стрессе.
Технический результат достигается четвертичным аммониевым производным лидокаина - N-аллил-(2,6-диметилфениламинокарбонилметил) морфолиний бромидом формулы (1):

обладающим противоаритмической активностью.
Способ получения соединения формулы (1) заключается в том, что N-(2,6-диметилфениламинокарбонилметил)морфолин подвергают взаимодействию с аллилом бромистым в среде изопропилового спирта при температуре 58-62°С с последующим охлаждением реакционной смеси до комнатной температуры и выделением N-аллил-(2,6-диметилфениламинокарбонил-метил)морфолиния бромида.
Способ по изобретению иллюстрируется следующим примером.
Пример. Синтез N-аллил-N-(2,6-диметилфениламинокарбонилметил)морфолиний бромида
К 100 г N-(2,6-диметилфениламинокарбонилметил)морфолина приливают 130 мл спирта изопропилового, к раствору постепенно добавляют 49 мл аллила бромистого. Смесь нагревают до температуры 60°С, перемешивают в течение 5-6 часов, после чего охлаждают, выделившийся продукт отфильтровывают. Получают 133,5 г технического вещества (89,72%), которое очищают перекристаллизацией из изопропилового спирта с добавлением активированного угля. Получают 109,5 г белого кристаллического порошка легкорастворимого в спирте, растворимого в воде, практически нерастворимого в эфире и хлороформе. Т пл. 195-197°С.
Найдено %: С 55,12 Н 6,71 N 7,42 О 8,53, Br 21,52
Вычислено, %: С 55,29 Н 6,82 N 7,59 О 8,66, Br 21,64
C17H25N2O2Br, м.м. 369,29
ИК-спектр, γ см-1: 1550 (NHCO), 1670 (C=O), 3280 (NH)
Исследование фармакологической активности 1
В отличие от кватернидина 1 выгодно отличается меньшей токсичностью при внутрибрюшинном, оральном и внутривенном способах введения, а также большей безопасностью, что иллюстрируется примером 1.
Пример 1. Острая токсичность 1 и ближайших аналогов
Острая токсичность 1 изучена в опытах на мышах (n=440, m=18-20 г) при внутрибрюшинном и оральном способах введения, на кошках (n=15, m=1,5-4,8 кг) при внутривенном введении.
Показатель LD50 рассчитывали методом Миллера и Тейнтера (кн. Беленький М.Л. Элементы количественной оценки фармакологического эффекта. - Рига: Изд-во АН ЛССР, 1963. - 130 с.). Для определения острой токсичности при внутривенном введении (LD100) растворы в изотоническом растворе хлористого натрия вводили животным до остановки сердечной деятельности. Результаты исследования структурного предшественника лидокаина, кватернидина, а также 1 представлены в табл.1.
Из предлагаемых в таблице данных хорошо видно, что заявляемое соединение более токсично, нежели структурный предшественник лидокаин при внутрибрюшинном введении и менее токсично, чем четвертичный дериват тримекаина - кватернидин. При пероральном введении острая токсичность 1 была меньше аналогичного показателя лидокаина и кватернидина. Летальная внутривенная доза 1 для кошек также ниже таковой кватернидина и лидокаина.
Пример 2. Антиаритмическая активность 1 и ближайших аналогов при желудочковой аритмии в позднюю стадию экспериментального инфаркта миокарда у собак
Желудочковая аритмия в поздней стадии экспериментального инфаркта миокарда воспроизводилась у половозрелых собак обоего пола массой 7,0-15,0 кг. Нарушение коронарного кровотока у животных вызывали по методу, описанному в источниках: Harris A.S. Delayed development of ventricular ectopic rhythm following experimental coronary occlusion. // Circulation Res. - 1950. - Vol.1. - N6. - P.1318-1328 и Генденштейн Э.И., Костин Я.В. Противоаритмическое действие тримекаина при желудочковых аритмиях // Кардиология. - 1976. - №1. - С.128-131.
Результаты тестирования заявляемого соединения и аналогов приведены в табл.2.
Исследование 1. Введение 1 в дозе 4 мг/кг позволило подавить аритмию в 100% опытов. Длительность антиаритмического эффекта составила не менее 500 минут наблюдения. Полный противоаритмический эффект развивался в среднем через 15 минут после введения.
Таким образом, по силе и длительности противоаритмического эффекта 1 не уступает кватернидину и лидокаину. Так же как и четвертичным производным тримекаина (кватернидину) 1 свойственна двухфазность возникновения антиаритмического действия.
Пример 3. Активность 1 и кватернидина на модели аконитиновой аритмии у крыс и мышей
Аритмию воспроизводили по методу Ю.И.Вихляева и Н.В.Кавериной (1958) (кн. Каверина Н.В., Бердяев С.Ю., Кущук Е.П., Пасхина О.Е. Методические указания по изучению антиаритмической активности новых фармакологических веществ // Руководство по экспериментальному (доклиническому) исследованию новых фармакологических веществ / Под ред. В.П.Фисенко. - М., 2000. - С.210). Нитрат аконитина вводили животным в дозе 50 мкг/кг. Результаты исследований представлены в таблице 3.
Данная модель позволяет судить о широте терапевтического действия представляемого соединения, его ближайших аналогов и структурного предшественника. О широте терапевтического действия судили по величине антиаритмического индекса, определяемого как отношение LD50 при внутрибрюшинном способе введения к ЭД50 на аконитиновой модели аритмий.
Проведенный эксперимент показывает, что 1 эффективно купирует предсердную аритмию, вызванную внутривенным введением нитрата аконитина. При этом значение антиаритмического индекса, рассчитанного для 1, намного превосходит таковые кватернидина и лидокаина, следовательно, 1 обладает большей широтой терапевтического действия, чем сравниваемые аналоги, что свидетельствует о большей его безопасности при эквивалентной активности.
Пример 4. Изучение влияния 1, лидокаина и кватернидина на экспериментальную летальность при длительном введении животным, находящимся в условиях стресса
В настоящее время для оценки безопасности проведения длительной антиаритмической терапии используется метод (Балашов В.П., Балыкова Л.А., Шувалова Е.Н. и др. Новый метод оценки безопасности потенциальных противоаритмических средств // Бюлл. Эксп. биол. и мед. - 2002. - Т.133. - №5. - С.598-600) моделирования 6-часового иммобилизационного стресса у белых мышей ежедневно на протяжении 6 недель.
Результаты изучения 1, лидокаина и кватернидина представлены в табл.4. Все соединения вводили в дозе, составляющей 5% от LD50 при внутрибрюшинном введении для мышей. 1 - в дозе 4 мг/кг внутрибрюшинно, лидокаин - 10 мг/кг, кватернидин - 2 мг/кг.
В контроле иммобилизация приводила к гибели части животных, и летальность по истечении 6 недель составила 30%. Лидокаин достоверно повышал летальность мышей при стрессе. Кватернидин обнаруживал тенденцию к ее повышению, а процент гибели животных при введении 1 был наименьшим из всех рассмотренных веществ.
Представленные данные свидетельствуют, что N-аллил-N-(2,6-диметилфениламинокарбонилметил) морфолиний бромид (1) проявляет выраженные противоаритмические свойства на моделях желудочковых и предсердно-желудочковых (аконитиновых) аритмий, сопоставимые со свойствами ближайшего аналога (кватернидина) и превосходящие противоаритмические свойства структурного предшественника (лидокаина).
Длительность эффекта 1 соответствует аналогичному показателю кватернидина и существенно превышает длительность эффекта лидокаина. Важным достоинством заявляемого соединения является его большая широта терапевтического действия по сравнению с аналогичным показателем у лидокаина и кватернидина. Кроме того, в условиях длительного иммобилизационного стресса при 6-недельном введении, 1 в отличие от лидокаина не повышает смертность подопытных животных.
Таким образом, модификация морфолинового аналога лидокаина путем присоединения к атому азота аллильной группировки (синтез N-аллил-N-(2,6-диметилфениламинокарбонилметил) морфолиния бромида) позволяет получить более эффективное и безопасное соединение для терапии нарушений сердечного ритма, чем его структурный предшественник и ближайший аналог.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЧЕТВЕРТИЧНОЕ АММОНИЕВОЕ ПРОИЗВОДНОЕ НОВОКАИНА, ОБЛАДАЮЩЕЕ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2414893C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОЛОНГИРОВАННОЙ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2538674C2 |
| 10-BR-N(4)-ПРОПИЛАЙМАЛИНИЯ БЕНЗОЛСУЛЬФОНАТ, ОБЛАДАЮЩИЙ АНТИАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2083578C1 |
| N-(2,4,6-ТРИМЕТИЛФЕНИЛКАРБАМОИЛМЕТИЛ)-N-АЛЛИЛМОРФОЛИНИЙ БРОМИД, ПРОЯВЛЯЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЕ И АНТИАРИТМИЧЕСКОЕ ДЕЙСТВИЕ ПРИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2105554C1 |
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| СОЕДИНЕНИЕ НИБЕНТАНА С АМИНОКИСЛОТОЙ, ОБЛАДАЮЩЕЕ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2572710C1 |
| ДИЦИКЛОГЕКСИЛАМИДЫ N-ЗАМЕЩЕННЫХ α-АМИНОКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ И АНТИФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2114821C1 |
| КОМПОЗИЦИЯ АМИНОКИСЛОТ С МИКРОЭЛЕМЕНТАМИ, ОБЛАДАЮЩАЯ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2173553C2 |
| Четвертичные аммониевые производные анилидов аминоуксусной кислоты,обладающие противоаритмической активностью | 1981 |
|
SU956463A1 |
Изобретение относится к новому биологически активному соединению. Описывается четвертичное аммониевое производное лидокаина формулы (1):
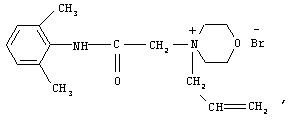
обладающее противоаритмической активностью. Также описывается способ получения четвертичного аммониевого производного лидокаина формулы 1, заключающийся в том, что N-(2,6-диметилфениламинокарбонилметил) морфолин подвергают взаимодействию с аллилом бромистым в среде изопропилового спирта при температуре 58-62°С с последующим охлаждением реакционной смеси до комнатной температуры и выделением N-аллил-(2,6-диметилфениламинокарбонилметил) морфолиния бромида. Технический результат - получено новое соединение, обладающее полезными биологическими свойствами. 2 н.п. ф-лы, 4 табл.
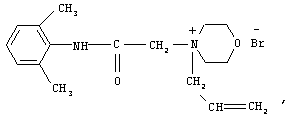
обладающее противоаритмической активностью.
| N-(2,4,6-ТРИМЕТИЛФЕНИЛКАРБАМОИЛМЕТИЛ)-N-АЛЛИЛМОРФОЛИНИЙ БРОМИД, ПРОЯВЛЯЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЕ И АНТИАРИТМИЧЕСКОЕ ДЕЙСТВИЕ ПРИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2105554C1 |
Авторы
Даты
2005-08-20—Публикация
2004-06-28—Подача