Изобретение относится к способу стимулирования адаптации организма к экстремальным и стрессовым воздействиям биологически активными водорастворимыми полимерными композициями, содержащими высокодисперсное металлическое серебро, стабилизированное поли-N- винилпирролидоном; обладающими адаптогенными свойствами.
Изобретение может найти широкое использование в медицине и ветеринарии в качестве потенциального лекарственного средства с антигипоксической, противошоковой, анальгезирующей, антидепрессивной и противострессовой активностью.
Термины, используемые в описании и их разъяснении.
Колларгол-коммерческий лекарственный препарат, включающий в свой состав коллоидное металлическое серебро (70%) и продукты гидролиза казеина. Используется как антимикробное средство /БСЭ, 3 изд., т.12, М.: изд. СЭ, 1973/.
ПВП - поли-N-винилпирролидон - синтетический водорастворимый полимер общей формулы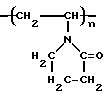 .
.
Используется в медицине в качестве плазмозаменителя крови и детоксиканта. Выпускается для медицинских целей с различными молекулярными массами (мол.м. 12600 ± 2700 - плазмозаменитель "Гемодез", мол.м. 8000 ± 2000 - плазмозаменитель "Гемодез-Н", мол.м. 35000 ± 5000 - для покрытия таблеток и в качестве связующего в готовых лекарственных формах.
АТФ - аденозин-5' -трифосфат динариевая соль, гидрат /99%, мол.м. 551,15, т. пл. 176oC, стоимость 10 г 51,75 долл. США, Aldrich, 1992-93, N A 2.690-9/. Природный адаптоген.
По достигаемому положительному эффекту аналогами предложенного способа являются способы стимулирования адаптации организма к экстремальным и стрессовым факторам с использованием в качестве активного начала природных адаптогенов, в первую очередь аденозина и его производных.
Описан способ с введением внутримышечно (в/м) или внутрибрюшинно (в/бр) АТФ в дозах 10 - 50 мг/кг /I/, обеспечивающий адаптацию организма к экстремальным факторам, таким как недостаток кислорода, шок, боль, стрессовые воздействия. При пероральном или внутрижелудочном (в/ж) введении в тех же дозах аденозин и его производные неэффективны как адаптогены.
Главным недостатком известного способа является то, что в указанных терапевтических дозах АТФ и аденозин оказывают побочное физиологическое действие: существенно снижают артериальное давление, угнетают сердечную деятельность, а при дозах более 50 мг/кг угнетают функции центральной нервной системы и вызывают острую сердечно-сосудистую и дыхательную недостаточность /3/.
Задачей изобретения являлось преодоление недостатков известного решения, т. е. создание способа стимулирования адаптации организма к экстремальным и стрессовым факторам с использованием в качестве активного начала малотоксичных средств с минимальным побочным действием.
Эта задача была решена заявленным способом с введением в качестве активного начала водорастворимой полимерной композиции, содержащей высокодисперсное металлическое серебро, стабилизированное поли-N-винилпирролидоном при соотношении компонентов, мас.ч.:
ПВП мол.м. (6 - 40)•103 - 1
Высокодисперсное металлическое серебро - 0,01 - 2,33
Эта композиции вводится внутрижелудочно (в/ж) или внутримышечно (в/м) в дозах 1,0 - 300 мг/кг живой массы тела.
Анализ известного уровня науки и техники не позволил обнаружить какую-либо информацию о способах, в которых активным началом были бы серебросодержащие композиции с адаптогенными свойствами. Ближайший аналог активного начала по составу - препарат колларгол, используется только как антимикробное и противовирусное средство.
Т.о., заявленное решение соответствует требованию "новизна".
Заявляемый способ основан на впервые обнаруженном свойстве полимерной композиции, содержащей высокодисперсное металлическое серебро, стимулировать адаптацию организма к экстремальным и стрессовым факторам при в/ж или в/м введении в организм в субтоксических дозах.
Нахождение неочевидной зависимости между структурой и свойствами серебросодержащей композиции позволяет утверждать о соответствии изобретения требованию "изобретательский уровень".
Адаптогенные свойства заявленной композиции оценивались по ряду специальных тестов:
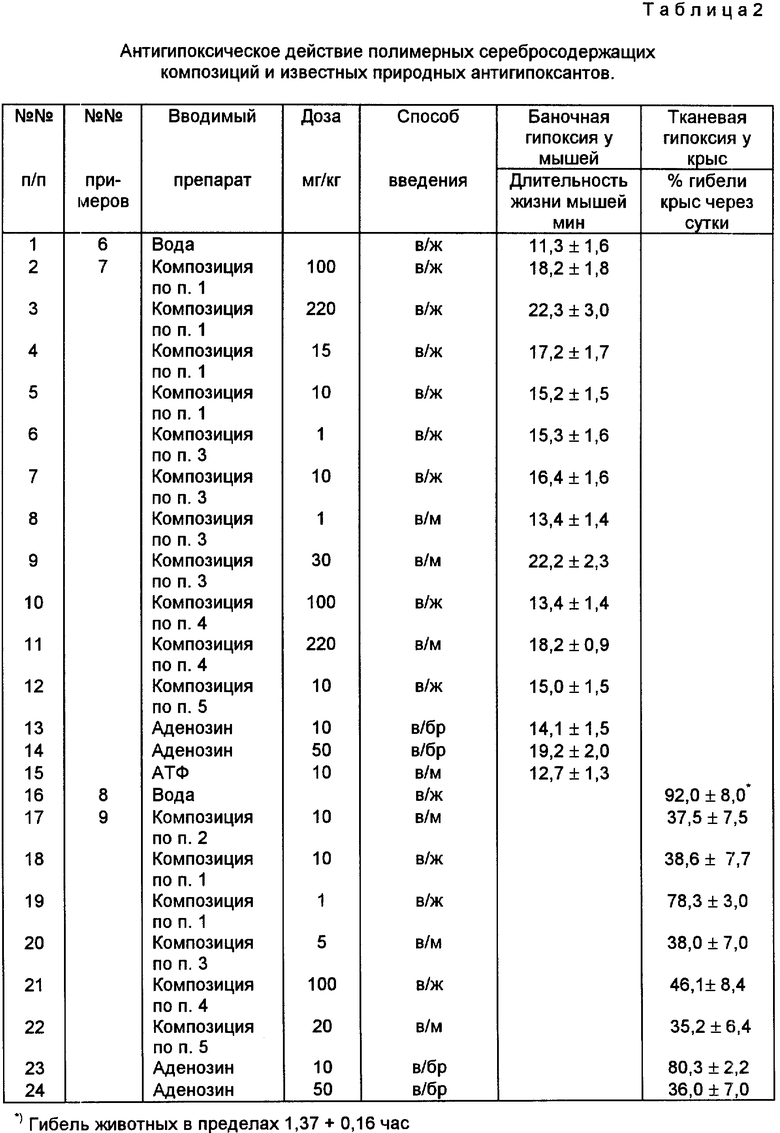
1. Антигипоксическая активность оценивалась на двух моделях гипоксии - баночной гипоксии с гиперкапнией у мышей и тканевой гемической гипоксии у крыс, вызванной инъекцией нитрита натрия.
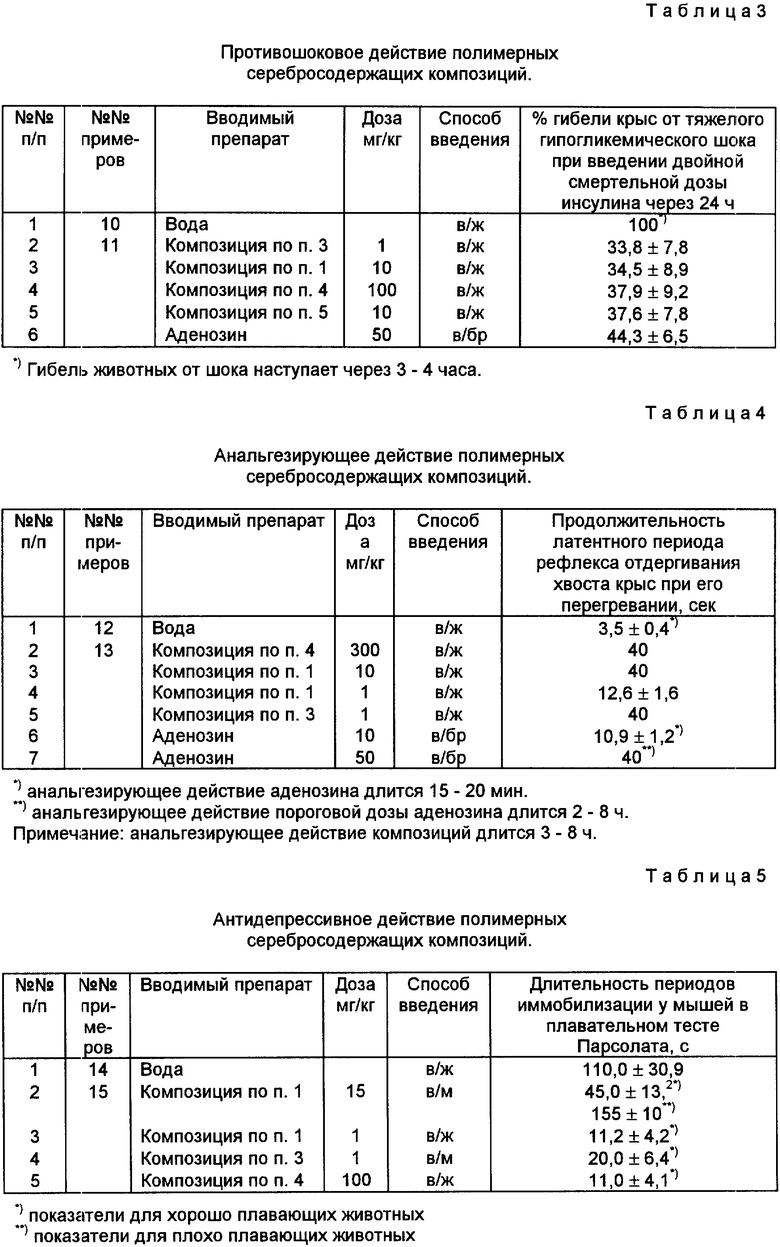
2. Противошоковое действие композиции оценивалось на модели тяжелого инсулинового шока, вызываемого в/м введением двойной смертельной дозы инсулина.
3. Анальгезирующее действие веществ оценивалось по их способности удлинять продолжительность латентного периода отдергивания хвоста крыс при его погружении в горячую воду (56oC).
4. Антидепрессивный эффект веществ оценивался в плавательном тесте Порсолта на белых мышах по длительности времени иммобилизации животных.
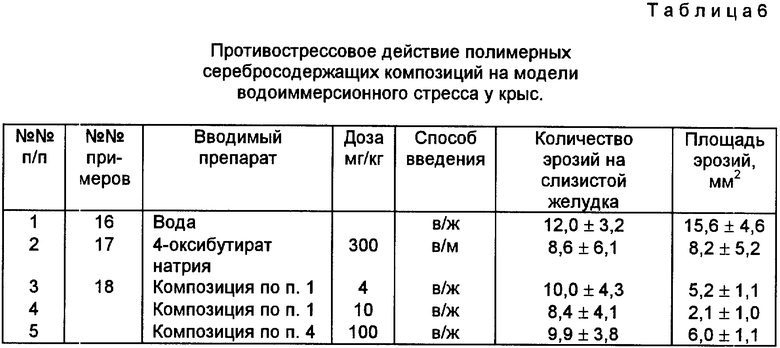
5. Противострессовое действие вещества оценивалось на модели водоиммерсионного стресса на крысах в сравнении с эталонным препаратом - оксибутиратом натрия, причем регистрировалось количество и площадь эрозий на слизистой желудка, образующихся в результате стресса.
Пример 1. В защищенный от света стеклянный реактор, снабженный мешалкой, капельной воронкой и барботером для продувки инертным газом (азот, аргон), загружают 1172,6 мл дистиллированной воды, 100 г этилового спирта и 200 г ПВП мол. м. 126000 ± 2700. Раствор нагревают при перемешивании в течение 10 мин до 75oC и при этой температуре добавляют к нему 27,39 г нитрата серебра (хч, 99,999%), растворенного в 500 мл воды. Реакционную массу, содержащую 10% ПВП, 1,37% нитрата серебра и 5% этилового спирта, перемешивают при той же температуре до полного исчерпания ионного серебра (контроль по пробе с 1%-ным водным раствором хлорида натрия). Полученный голубовато-зеленый раствор сушат на распылительной сушилке и получают целевую водорастворимую композицию высокодисперсного металлического серебра и ПВП в виде порошка зеленовато-серого цвета. Выход целевого продукта 217,2 г (99,9%); содержание металла 7,94%.
Условия получения композиций других составов по примерам NN2-5 приведены в табл.1. Там же указаны показатели острой токсичности композиций при внутрибрюшинном введении белым мышам.
Пример 6 (контроль - баночная гипоксия у мышей).
Мышам (n=20) массой 20 г вводили в/ж с помощью металлического зонда 0,3 мл дистиллированной воды и через 30 мин животных помещали в замкнутую герметичную баночку вместимостью 100 см3. Через 11,3 ± 1,6 мин все животные погибли от кислородного голодания.
Пример 7. В условиях примера 6 за 30 мин до гипоксии мышам (n=20) вместо дистиллированной воды вводили в/ж 0,3 мл 1%-ного водного раствора композиции состава, указанного в примере 1, что соответствовало дозе 100 мг/кг массы тела. Через 18,2 ± 1,8 мин все животные погибли от кислородного голодания, т.е. по сравнению с контролем длительность их жизни в условиях гипоксии возросла в 1,61 раза.
Пример 8 (контроль - гемическая гипоксия у крыс).
Белым беспородным крысам (n=100) массой 160-200 г вводили внутрижелудочно 0,3-0,5 мл дистиллированной воды и через 30 мин делали внутримышечную инъекцию нитрата натрия в дозе 85 мг/кг массы тела. Через 1,37 ± 0,16 ч. на фоне ярко выраженной гипоксии погибло 92 ± 8% животных.
Пример 9. В условиях примера 8 за 30 мин до инъекции нитрита натрия крысам (n=100) вводили внутримышечно 0,1%-ный водный раствор композиции, полученной в условиях примера 2. Доза композиции составляла 10 мг/кг массы тела. Через сутки после гипоксии погибло 37,5 ± 7,5% животных.
Пример 10 (контроль - смертельный инсулиновый шок у крыс).
Белым беспородным крысам (n=100) массой 170-190 г вводили в/м двойную смертельную дозу инсулина (2,5 МЕ инсулина на 100 г массы крысы). Через 3-4 ч. тяжелый гипогликемический шок вызывал смерть 100% животных.
Пример 11. В условиях примера 10 за 30 мин до инъекции инсулина животным вводили внутримышечно 0,01%-ный водный раствор композиции, полученной в условиях примера 3. В пределах 8 ч. после шока гибели крыс от шока не наблюдалось. Через сутки после инъекции инсулина погибло 38 ± 7% животных.
Пример 12 (контроль - анальгезирующий эффект, оцениваемый по рефлексу отдергивания хвоста крыс при его перегревании)
Белым беспородным крысам (n=20) массой 160-180 г вводили в/ж 0,3 мл дистиллированной воды и через 30 мин регистрировали латентный период рефлекса отдергивания хвоста крыс при его погружении в горячую воду с температурой 56oC, который составил 3,5±0,42 с.
Пример 13. В условиях примера 12 внутрижелудочное введение композиции, полученной в условиях примера 4, в дозе 300 мг/кг тела, полностью угнетало рефлекс отдергивания хвоста у крыс при его перегревании (латентный период рефлекса более 40 с), причем анальгезирующее действие сохранялось в течение 3-8 ч.
Пример 14 (контроль - депрессия мышей в тесте Порсолта).
Белым мышам-самцам (n= 20) массой 18-20 г, голодавшим 12 и более часов перед опытом, вводили в/ж 0,2 мл дистиллированной воды и через 30 мин мышей опускали плавать в стеклянной банке диаметром 40 мм и высотой 700 мм в воде с температурой 28-30oC. Регистрировали у мышей продолжительность всех остановок в плавании (иммобилизации) за период наблюдения в течение 5 мин (с 1-ой по 6-ую минуту после погружения), которая составила 110,0±30,9 с.
Пример 15. Внутримышечное введение мышам водного раствора композиции, полученной в условиях примера 1, в дозе 15 мг/кг за 60 мин до теста по примеру 14, вызывало у животных два противоположных физиологических эффекта в зависимости от врожденной способности животных к плаванию. У 80% хорошо плавающих особей наблюдался сильный антидепрессивный эффект, так как время иммобилизации мышей снижалось до 45,0±134,2 с. У 20% плохо плавающих животных депрессия усугублялась и время их иммобилизации в тесте Порсолта возрастало до 155,0±10,0 с.
Пример 16 (контроль - водоиммерсионный стресс у крыс)
Беспородным крысам-самцам (n=20) массой 210-260 г вводили в/ж 0,8 - 1,2 дистиллированной воды и через 30 мин животных помещали в тесные пеналы. Животных фиксировали в вынужденном положении: они не могли повернуться на бок и развернуться. Пеналы с животными помещали с температурой 21-24oC. Уровень воды соответствовал мечевидному отростку крысы. Длительность пребывания в воде составляла 7 ч. У животных регистрировалось количество и площадь эрозий на слизистой желудка, образовавшихся в результате стресса. Среднее количество эрозий составило 12,0±3,2, а их площадь 15,6 ±4,6 мм2.
Пример 17. В условиях примера 16 в качестве противострессового препарата сравнения использования натриевую соль 4-гидроксимасляной кислоты /Aldrich, 1992/93, с.695, стоимость 100 г 75,85 долл. США/, которую вводили крысам в/м в дозе 300 мг/кг массы тела за 30 мин до стресса. Среднее количество эрозий у животных составило 8,6± 6,1, а их площадь 8,2±5,2 мм2, т.е. в 2 раза меньше, чем в контроле.
Пример 18. В условиях примера 16 за 30 мин до стресса животным вместо воды вводили в/ж 0,1%-ный водный раствор композиции, полученной в условиях примера 1. Доза препарата составляла 4 мг/кг массы тела. Среднее количество эрозий у крыс составило 10,0± 4,3, а их площадь 5,2±1,1 мм2, т.е. в 3 раза меньше, чем в контроле.
Адаптогенные свойства серебросодержащих композиций различного состава при их в/ж и в/м введении в организм, а также некоторых природных адаптогенов приведены в табл. 2-6.
Анализ этих данных показывает, что заявленный способ стимулирования адаптации организма к экстремальным воздействиям по своей эффективности сопоставим или превышает эффективность известных способов и более физиологичен, т. к. положительный эффект достигается не только при системном, но и внутрижелудочном введении активного начала.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОРАЛЬНЫЕ АДАПТОГЕНЫ С АНТИГИПОКСИЧЕСКОЙ, ПРОТИВОШОКОВОЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2120287C1 |
| СПОСОБ ПОТЕНЦИИРОВАНИЯ ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1994 |
|
RU2088233C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2094056C1 |
| Средство для стимулирования адаптации организма к экстремальным и стрессовым факторам и способ стимулирования адаптации организма к экстремальным и стрессовым факторам | 2018 |
|
RU2683311C1 |
| ВОДОРАСТВОРИМЫЕ СОПОЛИМЕРЫ N-ВИНИЛ-2-ПИРРОЛИДОНА С ПРОИЗВОДНЫМИ КРОТОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ГЛЮКОКОРТИКОИДНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2081124C1 |
| АДАПТОГЕННОЕ СРЕДСТВО | 2007 |
|
RU2438687C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РЕПАРАТИВНОЙ АКТИВНОСТЬЮ | 1987 |
|
RU2080859C1 |
| ВОДОРАСТВОРИМАЯ БАКТЕРИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2088234C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ СЕДАТИВНОЙ И АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2171681C1 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИСТРЕССОРНЫМ, ПРОТИВОСУДОРОЖНЫМ И НЕЙРОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1997 |
|
RU2115660C1 |

Использование: изобретение относится к способам повышения устойчивости организма к экстремальным воздействиям с использованием биологически активных веществ. Решение может быть использовано в медицине и ветеринарии в терапии острых гипоксических состояний, ишемии мозга, сердца, шока, стресса, а также в качестве анальгетического и антидепрессивного средства. Задача: создание физиологического способа стимулирования адаптации организма к воздействию неблагоприятных экстремальных факторов с использованием малотоксичных биологически активных веществ. Сущность изобретения: предложен способ защиты организма от экстремальных и стрессовых воздействий путем внутримышечного или внутрижелудочного введения в субтоксических дозах (1 - 300 мг/кг) водных растворов композиции, содержащей высокодисперсное металлическое серебро и поли-N-винилпирролидон (ПВП) с ММ (6 - 40) • 103 при соотношении ингредиентов, мас.ч.:
ПВП - 1
Серебро - 0,01 - 2,33
Положительный эффект: при внутрижелудочном введении указанных композиций в организм достигается высокая эффективность защиты от гипоксии, шока, боли, депрессии и стресса, при отсутствии побочного действия, характерного для природных адаптогенов. 6 табл.
Способ стимулирования адаптации организма к экстремальным и стрессовым факторам путем введения водного раствора активного начала, отличающийся тем, что в качестве активного начала используют композицию, содержащую высокодисперсное металлическое серебро и поли-N-винилпирролидон при соотношении компонентов, мас.ч.:
Поли-N-винилпирролидон - 1
Серебро - 0,01 - 2,33
при этом поли-N-винилпирролидон берут с ММ от 6000 до 40000, активное начало вводят внутрижелудочно или внутримышечно в дозах от 1 до 300 мг/кг массы тела.
| Елисеев В.В | |||
| Роль аденозина в регуляции физиологических функций организма | |||
| - М.: Наука, 1991, с | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
Авторы
Даты
1998-04-20—Публикация
1994-11-25—Подача