Изобретение относится к способу получения 1, 2, 3, 9-тетрагидро-9-метил-3- [(2-метил-1H-имидазол-1-ил)метил] -4H- карбазол-4-он с формулой 1;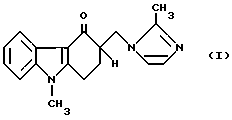 , которое является селективным антагонистом 5-HT3 рецепторов и проявляет интересные свойства как противорвотное в химиотерапии, так же как при лечении головной боли, шизофрении, боязни, ожирения, и маниакального синдрома.
, которое является селективным антагонистом 5-HT3 рецепторов и проявляет интересные свойства как противорвотное в химиотерапии, так же как при лечении головной боли, шизофрении, боязни, ожирения, и маниакального синдрома.
Известен способ получения 1, 2, 3, 9-тетрагидро-9-метил-3-[(2-метил-1H-имидазол-1-ил)метил] -4H-карбазол-4-она реакцией карбозолона с формулой III с 2-метилимидазолом.
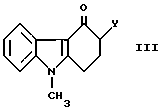 ,
,
где
V является метиленовым радикалом или галогенметильным радикалом (Патент EP 548430)
Также известен способ получения 1, 2, 3, 9-тетрагидро-9-метил-3- (2-метил-1H-имидазол-1-ил)метил -4H-карбазол-4-она окислением карбозола формулы IV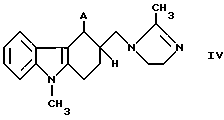 ,
,
где
A является атомом водорода или гидроксильным радикалом [EP N 556101]
Патент ES 539852 описывает получение 1,2, 3, 9-тетрагидро-9-метил-3-[(2-метил-1H-имидазол-1-ил)метил] -4H-карбазол-4-она алкилированием карбазолона формулы V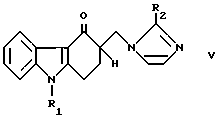 ,
,
где
R1 и/или R2 являются атомами водорода.
Патент ES 2000935 описывает получение 1, 2, 3, 9-тетрагидро-9-метил-3- [(2-метил-1H-ил)метил] -4H-карбазол-4-она циклизацией фенилгидразинового производного формулы VI.
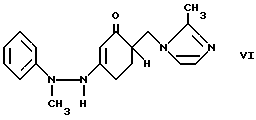 ,
,
Известно получение 1, 2, 3, 9-тетрагидро-9-метил-3-[(2-метил-1H-имидазол-1-ил)метил] -4H-карбазол-4- она циклизацией производного анилина с формулой VII [1]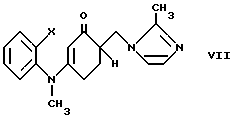 ,
,
где
X является атомом водорода или галогена.
Изобретение относится к способу получения 1, 2, 3, 9-тетрагидро-9-метил-3-[(2-метил-1H-имидазол-1-ил)метил] -4H-карбазол-4-она формулы I.
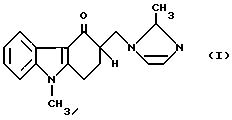 ,
,
который включает циклизацию 2-[(2-метил-1H-имидазол-1-ил)-метил]-4-(1-метилиндол-2-ил)бутировой кислоты с формулой II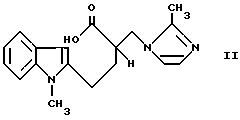 ,
,
в условиях реакции ацилирования по Фриделю-Крафтсу, через активацию карбоксильной группы в присутствии кислого катализатора, в проходящей среде растворителя и дальнейшим выделением необходимого продукта общепринятым методами.
Активация карбоксильной кислоты проводится превращением ее в ацилгалоид или в смешанный трифторуксусный, метансульфоновый или triflic ангидрид. предпочтительно в смешанный трифторуксусный ангидрид.
Кислым катализатором могут быть неорганические кислоты, такие, как соляная, серная или фосфорная, или кислоты Льюиса, такие, как трифторид бора, хлорид цинка или трихлорид алюминия, предпочтительно фосфорная кислота.
Реакция проводится в апротонных органических растворителях, таких, как хлороформ, дихлорметан, дихлорэтан, эфир, тетрагидрофуран, ацетонитрил, предпочтительно ацетонитрил.
Реакция циклизации может проходить достаточно эффективно в температурной области от -60 до 50oC, предпочтительно при 0oC.
После завершения реакции требуемый продукт выделяется общепринятыми способами, предпочтительно из метанола, до получения химически чистого 1,2,3,9-тетрагидро-9-метил-3- [(2-метил-1H-имидазол-1-ил)метил] -4H-карбазол-4-она.
Соединение формулы II может быть приготовлено реакцией 2-метилен-4-(3-карбоксил-1-метилиндол-2-ил)масляной кислоты формулы VIII c 2-метилимидазолом.
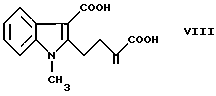 .
.
Общепринято проводить реакцию в температурной области 100 - 200oC, предпочтительно при 150oC.
Реакция проводится в высококипящих растворителях, таких как толуол, ксилол или бромбензол, или их смесь, или без растворителя, что предпочтительно.
После завершения реакции требуемый продукт выделяют общепринятыми способами и перекристаллизовывают из органического растворителя, такого, как метанол, толуол, диметиксиэтан, метоксиэтанол, предпочтительно из диметоксиэтана.
Дикислоту формулы III получают гидролизом 2-метилен-4-(3-этоксикарбонил-1-метилиндол-2-ил) масляной кислоты с формулой IX.
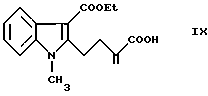 ,
,
которая в свою очередь может быть приготовлена реакцией этил 1,2-деметилиндол-3-карбоксилат аниона с формулой X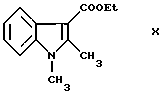 ,
,
(приготовлен в соответствии с John E. Macor, Kewin Ryan, Michael E. Newman in J. Org. Chem. 54, 4785 (1989)) из α -(бромметилакриловой) кислоты с фомрулой XI.
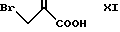 .
.
Нижеследующие примеры иллюстрируют, но не ограничивают область изобретения.
Пример 1. 2-Метилен-4-(3-этоксикарбонил-1-метилиндол-2-ил) масляная кислота.
К раствору литиевой соли, приготовленной из 4,34 г (20 ммоль) этил 1,2-диметилиндол-3-карбоксилата в 150 мл тетрагидрофурана, выдержанного при -60oC, добавляют в течение 10 с раствор 4,98 г (30 ммоль) α -(бромметилакриловой) кислоты в 20 мл тетрагидрофурана. Температура не должна превышать -50oC. После 2 ч встряхивания при -60oC раствор выливают в смесь, содержащую 400 г льда, 15 мл концентрированной соляной кислоты и 200 мл этилацетата. После расслоения фазы разделяют и водный слой экстрагируют этилацетатом (2•200 мл). Собранные органические экстракты сушат над MgSO4 и затем упаривают. Образующееся твердое вещество перекристаллизовывают из толуола и затем из метанола, при этом получают 3,0 г (50%) аналитически чистого названного соединения в форме белых кристаллов.
Т. пл. 138 - 140oC.
1H - NMR δ (CDCl3): 1,46 (т, J=7,1, 3H, -CH2-CH3), 2,62 - 2,71 (м, 2H, -CH2-C=C), 3,36 - 3,48 (м, 2H, индол-CH2), 3,76 (с, 3H, N-CH3), 4,41 (к, J = 2,1, 2H, -CH2-CH3), 5,81 (д, J=1,2, 1H, -C=CH), 6,37 (d, J=1,2, 1H, -C=CH), 7,15 - 4,40 (м, 3H, ароматика), 8,1 - 8,2 (м, 1H, ароматика).
Пример 2. 2-Метилен-4-(3-карбоксил-1-метидиндол-2-ил) масляная кислота. К суспензии 5,7 г (18,9 ммоль) соединения 1 в 15 мл метанола и 15 мл воды добавляют 19 г гидроксида калия и получившуюся смесь нагревают до закипания в течение 30 мин. Затем выливают ее в смесь 200 г льда и 200 мл воды, подкисляют 30 мл концентрированной соляной кислоты. Продукт выделяют фильтрацией и суспендируют его в 250 мл толуола, отбирают 10 мл и затем перегоняют и после охлаждения до 20oC и дальнейшей фильтрации получают 4,5 г (87%) аналитически чистого названного продукта в виде белых кристаллов.
Т. пл. 194 - 196oC
1H-NMR δ (CDCl3): 2,40 - 2,60 (м, 2H, индол-CH2-CH2-),3,20 - 3,50 (м, 2H, индол-CH2-CH2-), 3,77 (с, 3H, N-CH3), 5,59 (д, J=1,5, 1H, -C=C-H), 6,07 (д, J=1,5, 1H, -C=C-H), 7,10 - 7,25 (м, 2H, ароматика), 7,46 - 7,54 (м, 1H, ароматика), 7,96 - 8,05 (м, 1H, ароматика).
Пример 3. 2[(2-метил-1H-имидазол-1-ил] -4-(1-метилиндол-2-ил) масляная кислота Смесь 2,73 г (10 ммоль) соединения по примеру 2 и 2,46 г (30 ммоль) 2-метилимидазола нагревают при 160oC в течение 2 мин. После охлаждения до комнатной температуры смесь растворяют в хлороформе, пропускают через хроматографическую колонку с силикагелем, элюируют системой метиленхлорид/метанол в соотношении 70:30. Таким образом, получают 2,21 г (71%) целевого соединения в виде желтоватых кристаллов, аналитически чистое.
Т. пл. 198 - 199oC
1H-NMR δ (DMCO): 1,65 - 2,05 (м, 2H, индол-CH2-CH2-), 2,27(с, 3H, C-CH3), 2,65 - 2,95 (м, 3H, индол-CH и -CH-COOH), 3,63 (с, 3H, N-CH3), 3,95 - 4,25 (м, 2H, имидазол-CH2-), 6,15 (с, 1H, индол-H), 6,79 (д, J=1,6, 1H, имидазол-H), 6,90 - 7,10 (м, 3H), включая 7,06 (д, J=1,6, 1H, имидазол-H), 7,30 - 7,45 (м, 2H, ароматика).
Пример 4. 1,2,3,9-Тетрагидро-9-метил-3[(2-метил-1H-имидазол-1- ил)-метил]-4H-карбозол-4-он.
К суспензии 311 мл (1 ммоль) соединения примера 3 в 10 мл ацетонитрила добавляют 28 мкл (0,28 ммоль) 85% фосфорной кислоты. Реакционную смесь охлаждают до 0oC, и по каплям добавляют 353 мкл (2,5 ммоль) трифторуксусного ангидрида. Через 15 мин реакционную смесь пропускают через смесь из 50 г льда и 50 мл насыщенного раствора монокарбоната натрия и экстрагируют метиленхлоридом (3•10). Объединенные органические экстракты сушат (MgSO4) и упаривают. Твердый осадок перектристаллизовывают из метанола с получением 160 мг (55%) названного соединения в виде аналитически чистых белых кристаллов.
Т. пл. 227 - 228oC.
1H - NMR δ (CDCl3): 1,70 - 2,05 (м, 1H, H-C(2)), 2,10 - 2,30 (м, 1H, H-C (2 ν , 2,45 (с, 3H, CH3), 2,75 - 3,15 (м, 3H, H-C(1) и H-C(3)), 3,72 (s, 3H, N-CH3), 4,10 (дд, J=8,15, 1H, N-CH2), 4,70 (дд, J=4,15, 1H, N-CH2), 6,85 - 7,05 (м, 2H, ароматика), 7,20 - 7,40 (м, 3H, имидазол-H и ароматика), 8,20 - 8,30 (м, 1H, ароматика). gт
Способ получения 1,2,3,9-тетрагидро-9-метил-3- [(2-метил-1Н-имидазол-1-ил)метил] -4Н-карбазол-4-она формулы I, который заключается в циклизации соединения формулы II при условиях ацилирования по Фриделю-Крафтсу через активацию карбоксильной группы кислотным катализатором в среде подходящего растворителя и конечным выделением требуемого продукта общепринятыми способами. 4 з.п. ф-лы.
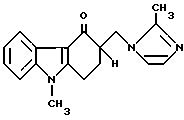
циклизацией производного имидазола, отличающийся тем, что циклизации подвергают 2-[2-(метил-1Н- имидазол-1-ил)метил] - 4-(1-метилиндол-2-ил) масляной кислоты II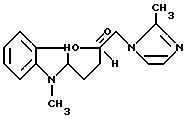
и процесс ведут в присутствии кислотного катализатора в среде растворителя.
| ES, 2000936, Кимика Синтетика, 20.01.90, C 07 D 233/58. |
Авторы
Даты
1998-04-27—Публикация
1993-03-12—Подача