Изобретение относится к гидролитическому способу извлечения кобальта и может быть использовано для отмывки осажденного гидроксида кобальта (III) от примесей.
Известен способ промывания осадка (В.Ф.Гиллебранд и другие. Практическое руководство по неорганическому анализу. Из-во "Химия", М, 1966, с. 129), используемый при выполнении различных разделений, раствором такого же состава, каким было сделано осаждение.
Недостатком способа является то, что он в ряде случаев является громоздким и дорогостоящим, к тому же часть составляющих можно исключить без ущерба для результатов промывки.
Так, выделение кобальта из раствора в виде гидроксида кобальта (III) осуществляют при pH = 1,9-2,1, используя в качестве окислителя гипохлорит или хлор, в последнем случае постоянство pH раствора во время процесса осаждения обеспечивается подачей содового раствора. К концу операции pH раствора повышается до pH= 2,3-2,5. После осаждения гидроксида кобальта (III) пульпу подогревают паром и перемешивают воздухом для удаления хлора, после чего отфильтрованный гидроксид промывают. Таким образом хлор, используемый при осаждении гидроксида, не используется в последующей операции промывки осадка.
Наиболее близким техническим решением является (И.Ф.Худяков, С.Э. Кляйн, Н.Г.Агеев, Металлургия меди, никеля, сопутствующих элементов и проектирование цехов. М, "Металлургия", 1993, стр. 169-170) способ промывки гидроксида кобальта (III), включающий промывку горячей водой на фильтрпрессе для удаления адсорбированного никельсодержащего раствора и обработку содовым раствором, содержащим 150-200 г/дм3 Na2CO3.
Гидроксид, снятый с фильтра-пресса содержит 25% кобальта и примеси в количестве, %: Ni=0,3; Fe=0,1; Mn=0,05; Cu-0,04 от содержания в осадке кобальта.
Недостатком способа является то, что промывка горячей водой (pH=7) не способствует отмывке гидроксида кобальта (III) от примесей никеля, железа, марганца и меди, которые при этом значении pH будут находится в осадке в виде гидроксидов или гидроксосолей, к тому же из маточника, захваченного осажденным гидроксидом кобальта, при промывке горячей водой дополнительно выпадут вышеперечисленные примеси в виде гидроксидов за счет повышения pH, разбавления и нагрева раствора.
Последующая обработка гидроксида кобальта содовым раствором закрепляет вышеперечисленные нежелательные процессы, не способствуя удалению примесей, захваченных при осаждении гидроксида кобальта (III).
К тому же использование соды приводит к загрязнению гидроксида кобальта серой, содержащейся в соде, что приводит к необходимости прокаливания отмытого осадка с добавкой соды для перевода содержащейся в соде серы в форму легко растворимого в воде сульфата натрия.
Задачей изобретения является более глубокая отмывка гидроксида кобальта (III) от примесей при одновременной простоте и экономичности процесса.
Техническим результатом является получение более чистого по примесям кобальта при сокращении расхода реагентов на стадии промывки.
Этот технический результат достигается тем, что в известном способе промывки осажденного гидроксида кобальта (III), включающем промывку водным раствором, промывку осуществляют порционной подачей кислого раствора при pH= 2,0-3,5.
Промывка горячим кислым раствором при pH=2,0-3,5 способствует более глубокой отмывке от примесей, однако при этом повышаются потери кобальта за счет его перехода в раствор в зажимной форме.
Сущность способа поясняется экспериментальными данными, представленными в табл. 1-5.
Пример конкретного выполнения способа.
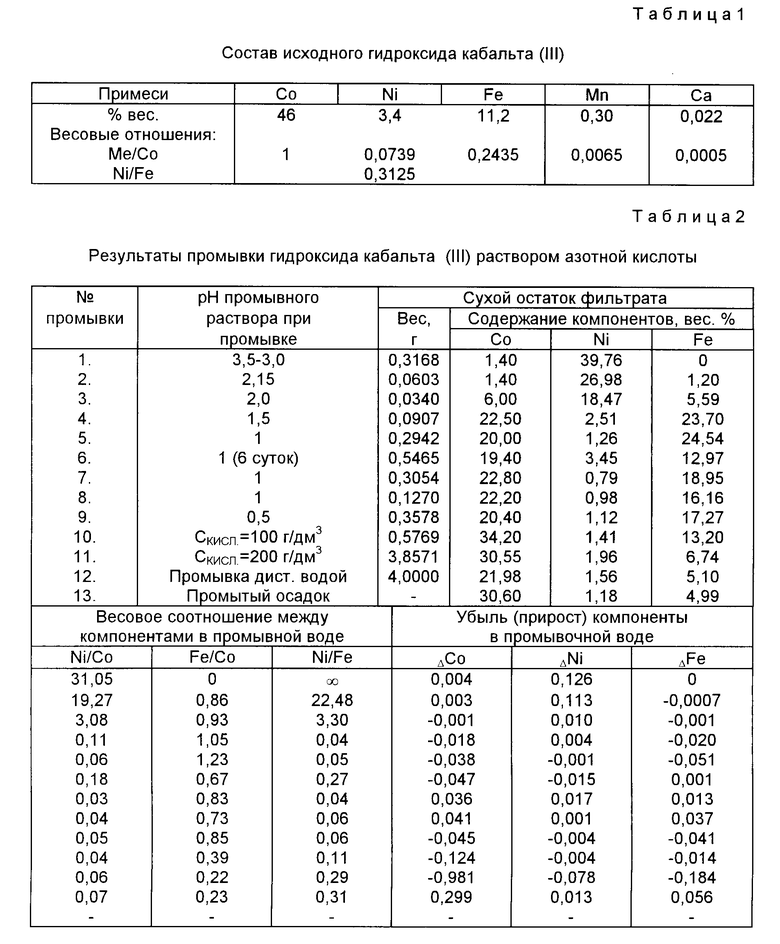
Для промывки использовали гидроксид кобальта (III), состав которого приведен в табл. 1, полученного при осаждении кобальта (III) при pH=1,9-2,1. В качестве окислителя использовали гипохлорит, промывку осуществляли способом, описанном в прототипе.
Промывку 30 г гидроксида кобальта (III) осуществляли порционно (до 100 мл) кислым раствором при перемешивании.
Пример 1 (табл.2). Для поддержания заданной кислотности в промывном растворе использовали азотную кислоту, температура комнатная.
В каждой последующей порции промывного раствора повышали кислотность, в табл.2 указана соответствующая величина pH промывного раствора.
Промывки 5-8 осуществляли при pH=1, причем промывку 6 осуществляли при длительном контакте промывной воды и осадка в течение 6 суток; промывки 10 и 11 осуществляли кислыми растворами с концентрацией кислоты соответственно, в г/дм3:700 м 1500; промывку 12 осуществляли дистиллированной водой.
Сухой остаток фильтрата после каждой промывки взвешивали и определяли в нем содержание кобальта, никеля и железа.
В промытом осадке гидроксида кобальта (III) также определяли содержание вышеперечисленных компонентов.
По полученным данным рассчитывали изменение Δ концентраций компонентов, а также их отношение после каждой промывки в фильтрате и в осадке.
В табл. 2 убыль компонента дана со знаком плюс, прирост = со знаком минус.
Из данных табл. 2 можно сделать следующие выводы:
1. Переход кобальта в раствор происходит при pH < 2,0, никеля - при pH < 1,5, железа - при pH < 3,0.
2. Длительный контакт осадка и раствора (см. промывку 6, время 6 суток) при pH - 1 приводит к повышенной растворимости никеля и снижению растворимости железа.
3. В интервале pH = 2,0 - 0,5 кобальт и железо переходит в фильтрат примерно в одинаковых количествах, в более кислой среде преобладает растворимость кобальта.
4. В интервале pH = 3,5 - 2,0 преобладает переход никеля в фильтрат по сравнению с кобальтом и железом.
5. Наиболее чистый по никелю фильтрат получен при pH=3,5-3,0, в этом фильтрате не содержится железо, содержание кобальта незначительно.
6. Осадок после 12 промывок содержит в 1,92 раза меньше никеля и в 1,49 раз меньше железа по сравнению с исходным гидроксидом.
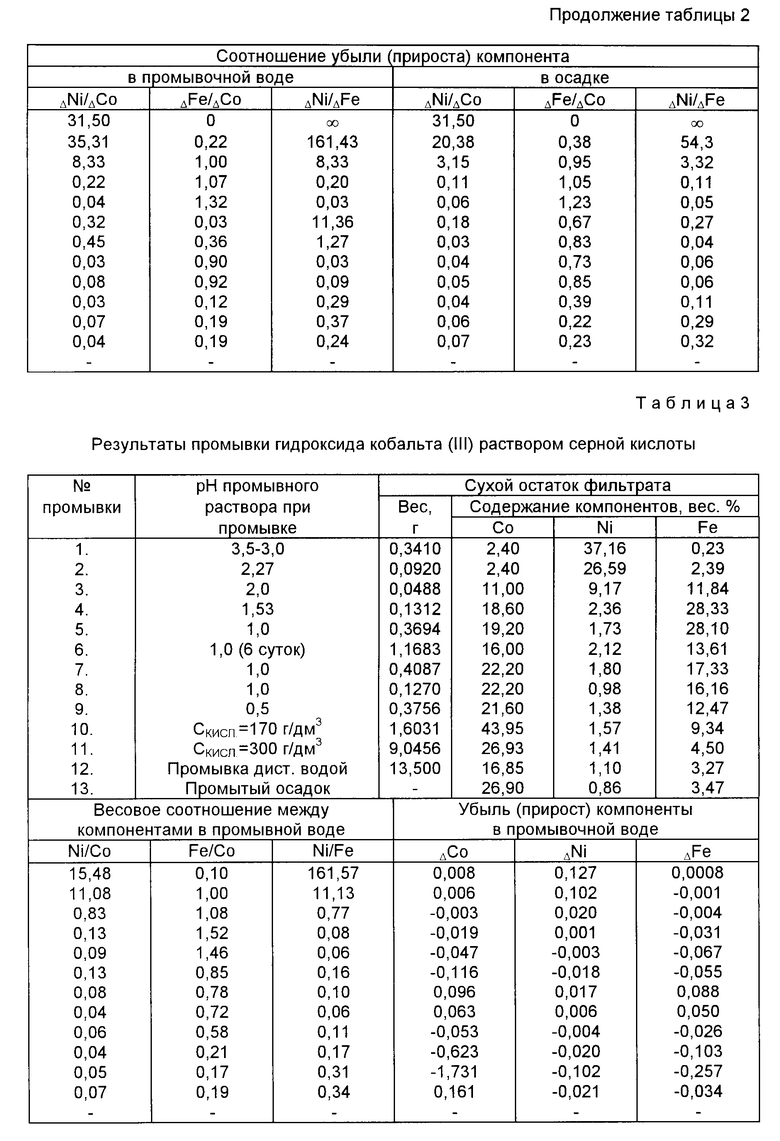
Пример 2 (табл. 3). Для поддержания заданной кислотности использовали серную кислоту, температура комнатная.
Условия проведения экспериментов аналогичны примеру 1.
Экспериментальные данные представлены в табл. 3.
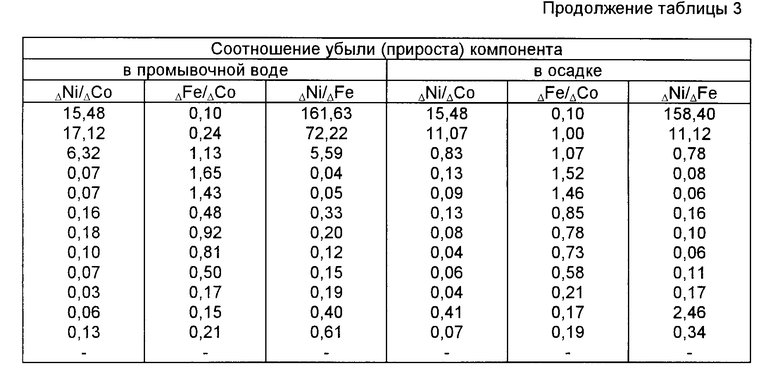
Из табл. 3 можно сделать следующие выводы:
1. Переход кобальта в раствор происходит при pH < 2,3, никеля - при pH < 1,5, железа - при pH < 3,0.
2. Длительный контакт осадка и раствора (см. промывку 6, время 6 суток) при pH = 1 приводит к повышенной растворимости железа и кобальта.
3. В интервале pH = 2,0 - 0,5 кобальт и железо переходят в фильтрат примерно в одинаковых количествах, в более кислой среде преобладает растворимость кобальта.
4. В интервале pH = 3,5 - 2,5 преобладает переход никеля в фильтрат по сравнению с кобальтом и железом.
5. Наиболее чистый по никелю фильтрат получен при pH = 3,5 - 3,0; в этом фильтрате содержатся в незначительном количестве железо и кобальт.
6. Осадок после 12 промывок содержит в 2,3 раза меньше никеля и в 1,9 раза меньше железа по сравнению с исходным гидроксидом.
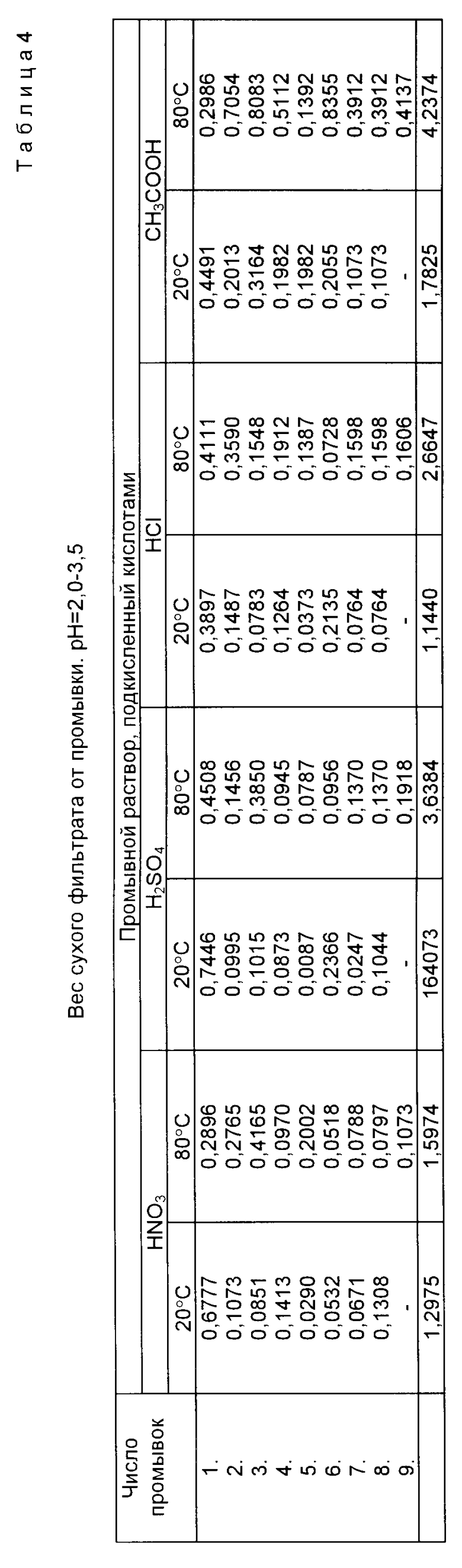
Пример 3 (табл.4 и 5) Промывку исходного гидроксида кобальта (III) осуществляли кислыми растворами азотной, серной, соляной и уксусной кислот при pH = 2,0 - 3,5 и температурах комнатной (20 o C) и при нагревании (80 o C).
В табл. 4 дан вес сухого фильтрата, полученного от промывки исходного гидроксида кобальта (III), в зависимости от числа промывок, температуры и вида использованной кислоты.
Из данных табл. 4 можно сделать следующие выводы:
1. Потери кобальта возрастают с увеличением числа промывок.
2. Потери кобальта возрастают при нагревании.
3. При комнатной температуре потери кобальта возрастают в ряду
HCl < HNO 3< H 2 SO 4< CH 3 COOH
4. Потери кобальта при нагревании возрастают в ряду
HNO 3< HCl < H 2 SO 4< CH 3 COOH
5. Приведенные ряды потери кобальта при промывке соответствуют рядам растворимости соответствующих солей кобальта при указанных условиях.
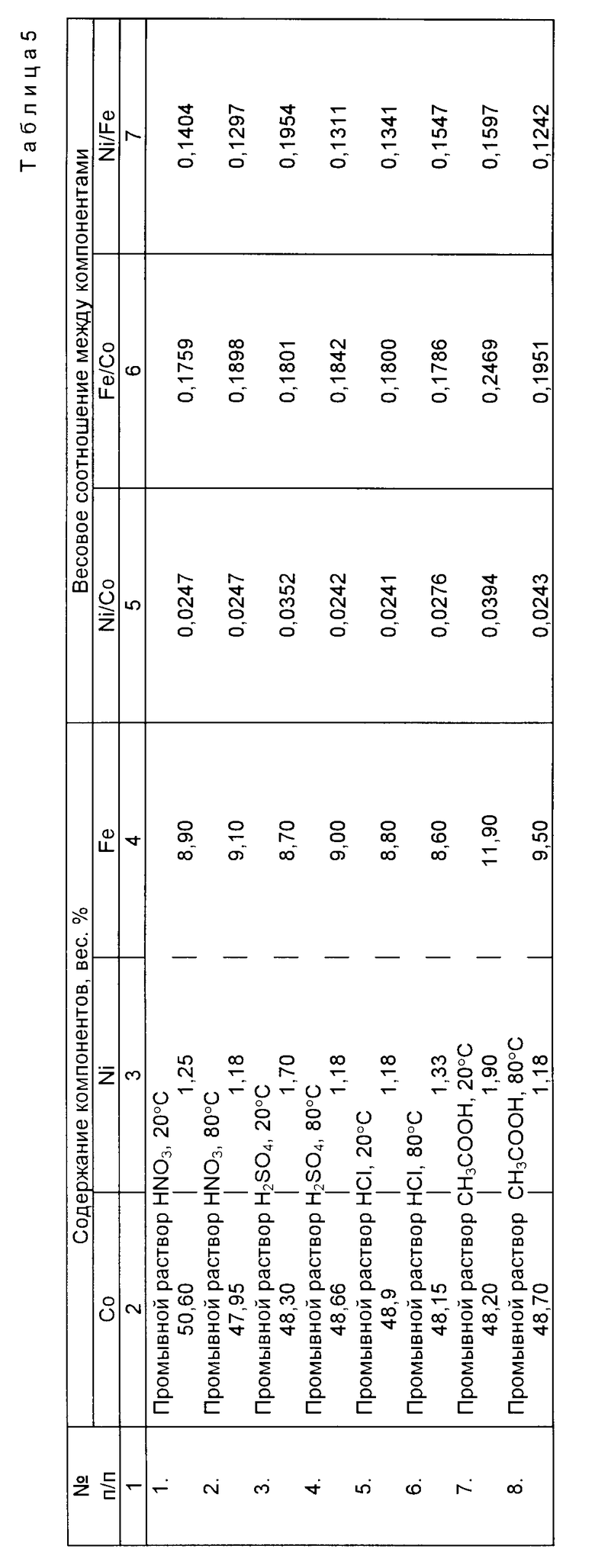
В табл. 5 даны результаты промывки осадка в зависимости от температуры и вида используемой кислоты.
Из данных табл. 5 можно сделать следующие выводы:
1. Нагрев способствует более глубокой промывке осадка от примесей.
2. При комнатной температуре убыль примесей в промытом осадке возрастает в ряду: по никелю CH 3 COOH < H 2 SO 4< HNO 3< HCl; по железу CH 2 COOH < H 2 SO 4< HCl < HNO 3.
3. При промывке осадка горячим промывным раствором убыль примесей в промытом осадке возрастает в ряду: по никелю HCl < HNO 3<C H 3 COOH < H 2 SO 4; по железу CH 3 COOH < HNO 3< H 2 SO 4< HCl
4. Условия наибольшего удаления примесей при промывании гидроксида кобальта (III) при pH 2,0 - 3,5:
по никелю раствор HCl при комнатной температуре или горячий раствор H 2 SO 4; по железу раствор HNO 3 или HCl при комнатной температуре или горячий раствор HCl.
Из экспериментальных данных, представленных в табл. 1-5, можно сделать следующие выводы:
1. Оптимальным интервалом величины pH для промывки является pH 2,0 - 3,5.
При pH > 3,5 примеси отмываются хуже, при pH < 2,0 возрастают потери кобальта.
2. Промывка горячим раствором лучше удаляет примеси, но увеличивает потери кобальта
3. При промывке кислым раствором кобальт переходит в раствор в восстановленной форме Co(II) за счет протекания в этих условиях окислительно-восстановительных реакций.
4. Наиболее чистый по никелю раствор получается в первых порциях промывной воды при pH 3,0 - 3,5.
5. По сравнению с исходным гидроксидом в промытом гидроксиде на единицу массы кобальта количество примесей уменьшается по никелю в 1,8 -3,1 раза; по железу в 1,0 - 1,4 раза.
Экспериментами установлено, что в промытом гидроксиде по сравнению с исходным на единицу массы кобальта количество примесей уменьшается по марганцу в 2 раза; по кальцию в 2 раза.
В примерах практического использования предлагаемого способа в качестве исходного использования уже промытый гидроксид, его промывка осуществлялась способом, описанном в прототипе.
Промывка такого гидроксида предлагаемым способом позволяет при незначительных потерях кобальта получить более чистый кобальт в осадке и получить в промывных водах никель высокой чистоты.
При больших содержаниях примесей в исходном гидроксиде вышеперечисленные преимущества предлагаемого способа соответственно возрастут.
По сравнению с прототипом предлагаемый способ промывки осажденного гидроксида кобальта (III) способствует более глубокому удалению примесей. Способ экономичен, т.к. расход кислот для поддержания заданного pH при промывке незначителен. Кроме того, в первых порциях фильтрата содержится никель высокой чистоты, извлечение которого дает дополнительный экономический эффект.
По сравнению с прототипом предлагаемый способ не вносит дополнительно сколько-нибудь значительного количества вредных примесей и не требует сложной аппаратуры для реализации.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ КОБАЛЬТА ОТ МАРГАНЦА | 2001 |
|
RU2214468C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ЖЕЛЕЗА, ЦИНКА, МЕДИ И МАРГАНЦА | 2006 |
|
RU2338801C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2106415C1 |
| СПОСОБ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ КОБАЛЬТА ОТ МАРГАНЦА | 2001 |
|
RU2214469C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ НИКЕЛЯ ИЗ ВОДНЫХ РАСТВОРОВ С ВЫСОКИМ СОДЕРЖАНИЕМ СОЛЕЙ СУЛЬФАТА НАТРИЯ | 2001 |
|
RU2221883C2 |
| СПОСОБ ОЧИСТКИ КОБАЛЬТА И НИКЕЛЯ ОТ ПРИМЕСЕЙ | 1997 |
|
RU2114198C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ КОБАЛЬТА ОТ МАРГАНЦА | 2001 |
|
RU2212460C2 |
| СПОСОБ ОЧИСТКИ НИКЕЛЕВОГО ЭЛЕКТРОЛИТА ОТ ПРИМЕСЕЙ ЖЕЛЕЗА (III), КОБАЛЬТА (III) И МЕДИ (II) ЭКСТРАКЦИЕЙ | 2015 |
|
RU2604289C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД, СОДЕРЖАЩИХ КРЕМНЕЗЕМ, ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1997 |
|
RU2140397C1 |
| КАТАЛИЗАТОР ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА | 2000 |
|
RU2180610C1 |
Способ может быть использован для отливки осажденного гидроксида кобальта от примесей. Промывку гидроксида кобальта (III) от примесей осуществляют порционной подачей водного раствора кислоты рН 2,0 - 3,5. Промывку можно осуществлять горячим раствором. Способ позволяет более глубоко отмыть гидроксид кобальта (III) от примесей при одновременной простоте и экономичности процесса. 1 з.п.ф-лы, 5 табл.
| Гиллебранд В.Ф | |||
| и др | |||
| Практическое руководство по неорганическому анализу | |||
| - М.: Химия, 1966, с | |||
| Способ применения резонанс конденсатора, подключенного известным уже образом параллельно к обмотке трансформатора, дающего напряжение на анод генераторных ламп | 1922 |
|
SU129A1 |
| Худяков И.Ф., Клейн С.Э., Агеев Н.Г | |||
| Металлургия меди, никеля, сопутствующих элементов и проектирование цехов | |||
| - М.: Металлургия, 1993, с | |||
| Универсальный двойной гаечный ключ | 1920 |
|
SU169A1 |
Авторы
Даты
1998-04-27—Публикация
1996-12-25—Подача