Изобретение относится к новым гетероциклическим алкилен-хиноксалинилоксифеноксипропаноатным соединениям, которые обнаруживают неожиданно высокую селективную гербицидную активность.
Хотя многие известные соединения, показанные в приведенных выше публикациях, проявляют желательную гербицидную активность, тем не менее существует потребность в селективных гербицидах.
Согласно изобретению предлагается новый класс соединений, имеющих структурную формулу:
где
n представляет собой 1, 2 или 3;
R1 и R2 каждый независимо выбран из группы, состоящей из галогена, водорода, C 1 - 3 алкокси, C 1 - 3 галоидалкокси, моногалоидметила, дигалоидметила, тригалоидметила, цианато и нитро;
R3 представляет собой 5- или 6-членное насыщенное, ненасыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1 или 2 атома кислорода, причем указанное кольцо необязательно замещено 1 - 3 заместителями, каждый из которых выбран независимо из группы, состоящей из оксо, C 1 - 3 алкила и C 1 - 3 алкокси.
Особенно предпочтительные соединения включают:
2-тетрагидрофуранилметил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]-7-пропаноат.
2-фуранилметил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]пропаноат;
2-тетрагидропиранилметил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]-пропаноат;
2-[2-/2-метил-1,3-диоксоланид/] этил 2-[4-/6-хлор-2-хиноксалинилокси/-фенокси]-пропаноат,
4-/3,3-деметил-2-бутиролактонил/метил 2-[4-/6-хлор-2-хиноксалинилокси/-фенокси]-пропаноат,
4-/2,2-диметил-1,3-диоксоланил/метил 2-[4-/6-хлор-2-хиноксалинилокси/-фенокси]-пропаноат.
Соединения данного изобретения могут быть получены по реакции хиноксалинилоксифенольного соединения формулы:
где
R1, R2 имеют значения, определенные для структуры (1), приведенной выше, с гетероциклическим алкилпропаноатгалогенидом формулы:
где
X представляет собой галоген, мезилат (метилсульфонилат) или тозилат (толилсульфонилат), а n и R3 имеют значения, определенные для структуры (1), приведенной выше. Данная реакция в типичном случае проводится в органическом растворителе (таком как диметилформамид, диметилсульфоксид, акрилонитрил или аналогичные) в присутствии неорганического или органического основания (такого как карбонат натрия, гидроокись калия или карбонат калия) при подходящей температуре.
Хиноксалинилоксифенокси исходные соединения могут быть получены с помощью взаимодействия 2-галоидхиноксалинового соединения, имеющего формулу:
где
X представляет собой галоген, и R1 и R2 имеют значения, определенные для структуры (1) выше, с фенилбензиловым эфиром формулы:
в присутствии неорганического или органического основания с получением промежуточного соединения формулы: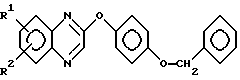
и гидрирования такого промежуточного соединения (с применением катализатора гидрирования, такого как палладий) с получением продукта дебензилирования и образования тем самым хиноксалинилоксифенольного исходного материала.
Гетероциклическое алкилпропаноат-галогенидное исходное соединение может быть получено с помощью взаимодействия галоидангидрида галоидированной пропионовой кислоты с соответствующим гетероциклическим алкиловым спиртом.
Альтернативно этил 2-галоидпропаноат может подвергаться реакции с соответствующим гетероциклическим алкиловым спиртом в присутствии соответствующего катализатора (такого, как тетра-изопропоксититан) с получением гетероциклического алкилпропаноатгалогенида реакций переэтерификации.
Композиции данного изобретения состоят из (A) по крайней мере одного из хиноксалинилоксифеноксипропаноатных соединений данного изобретения и (B) подходящего носителя.
Для получения гербицидных композиций хиноксалинилоксифеноксипропаноатное соединение может смешиваться с инертными ингредиентами, давая композиции в форме твердых, тонко измельченных веществ в виде частиц, гранул, таблеток, смачиваемых порошков, текучих жидкостей, растворимых порошков, растворов и дисперсий или эмульсий в водном или органическом растворителе. Такие готовые препаративные формы могут быть нескольких различных физических и химических типов, любой из которых может быть получен лицом, знакомым с данной областью техники.
Концентрация активного химического соединения в композиции может варьировать в широких пределах, обычно в интервале примерно от 1 до 95 мас.%. Концентрация активного химического агента в дисперсиях, применяемых по отношению к почве, семенам или листве, в типичном случае составляет примерно между 0,002 и 80 мас.%.
Для использования в качестве предвсходового гербицида соединение данного изобретения обычно применяется в количестве примерно от 0,01 до 10 фунтов на акр (примерно 0,01 - 11,2 кг/га) по отношению к почве, которая содержит семена сорняков и культурных растений. Такое применение производится или по отношению к поверхности почвы или в верхний слой почвы на глубину от одного до трех дюймов (2,5 - 7,5 см). При применении в качестве послевсходового гербицида соединение обычно наносится в количестве примерно от 0,01 до 10 фунтов на акр (примерно 0,01 - 11,2 кг/га) на воздушные части сорняков (наземные части).
Соединения настоящего изобретения включают изомерные формы и их смеси, т. е. как оптически-активные изомеры, так и рацемические смеси. Если не указано иное, соединения, описываемые в примерах, представляют собой рацемат.
Пример 1.
Получение 2-тетрагидрофуранилметил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]пропаноата (соединение 4).
A. Получение 2-тетрагидрофуранилметил 2-бромпропаноата.
В 250-миллилитровую трехгорлую колбу добавляют 0,15 моль 2-/гидроксиметил/тетрагидрофурана, 0,15 моль триэтиламина и 100 мл диэтилового эфира. Колбу погружают в лед и по каплям вводят 0,15 моль 2-бромпропаноилхлорида. Ледяную баню удаляют и реакционную смесь перемешивают при температуре окружающей среды в течение двух часов. Смесь экстрагируют равным объемом воды и органическую фазу сушат над сульфатом натрия. Декантируют и удаляют растворитель, получая в результате 2-тетрагидрофуранилметил 2-бромпропаноат с выходом 94%.
B. Получение 2-тетрагидрофуранилметил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]пропаноата.
В 500-миллилитровую круглодонную колбу добавляют 0,055 моль 2-/4-гидроксифенокси/-6-хлорхиноксалина, 0,055 моль 2-тетрагидрофуранилметил 2-бромпропаноата, 0,110 моль безводного карбоната калия и 250 мл ацетонитрила. Смесь нагревают с обратным холодильником в течение 5,5 ч и растворитель удаляют. Остаток фильтруют через колонку из окиси алюминия с дихлорметаном. Удаление растворителя и перекристаллизация из кипящего гексана дает в результате (с выходом 85%) 2-тетрагидрофуранилметил 2-[4-/6-хлор-2- хиноксалинилокси/фенокси] пропаноат. Вещество плавится в интервале 52 - 55oC.
Пример 2.
С использованием методики, описанной выше, получают другие соединения. Структуры и точки плавления и/или спектры ЯМР этих соединений представлены в табл. 1. (Примечание: в приведенных данных ЯМР спектров: s - синглет, d - дуплет, т. -триплет, q - квартет и м. - мультиплет).
Пример 3.
Довсходовая обработка.
Для иллюстрации эффективности соединений данного изобретения в качестве предвсходовых гербицидов 300 мг каждого из перечисленных ниже соединений растворяют в 10 мл ацетона, добавляют 30 мг эмульгирующего агента - этоксилированного сорбитанмонолаурата. Раствор разбавляют до 100 мл дистиллированной водой. Десять миллилитров данного раствора 3000 ч./млн разбавляют до концентрации 250 ч./млн дистиллированной водой. Соединения применяют в количестве 10 фунт/акр (11,2 кг/га), смачивая поверхность почвы в пластиковых горшках размером 4-1/2 дюйма (11,25 см), в которые высажены семена следующих сорняков: канатника Теофраста (Abutilon theophrasti Medic) VL, дурмана вонючего (Datura stramonium L) JW, ипомеи пурпурной (Ipomea purpurea L. Roth) TM, проса прутьевидного (Panicum virgatum L) SG, ежовника (Echinochloa crusgalli) L Beauv. BG и щетинника зеленого (Setaria viridis L. Beauv GF 46 мл 250 ч./млн раствора.
Спустя две недели после обработки определяют процент подавления роста сорняков в сравнении с необработанными контрольными растениями. Результаты испытаний приведены в табл. 2.
Приведенные выше данные показывают превосходное селективное предвсходовое уничтожение сорняков, проявляемое соединениями данного изобретения.
Пример 4.
Послевсходовая обработка.
Для иллюстрации эффективности соединений данного изобретения в качестве послевсходовых гербицидов 3000 ч. /млн растворы, описанные в примере 3, распыляют с помощью обычного распылителя Devilbis (торговая марка), смачивая листву до момента стекания капель. В остальном процедуру повторяют также, как описано в примере 3. Сорняки обрабатывают через 6 дней после появления всходов.
Процент подавления или уничтожения сорняков оценивают через две недели после обработки. Результаты данного испытания суммированы в табл. 3.
Приведенные данные показывают селективное послевсходовое гербицидное уничтожение сорняков, обнаруживаемое соединениями данного изобретения.
Пример 5.
Для иллюстрации эффективности соединений данного изобретения по предвсходовому уничтожению трав по сравнению с соединениями предшествующего уровня техники растворы нескольких соединений приготавливались по методике, аналогичной описанной в примере 1. Растворы концентраций 250 ч./млн разбавляют до 3,1 ч. /млн дистиллированной водой для проведения испытания и применяют при норме расхода 0,14 кг/га, в количестве 46 мл для пропитки почвы в горшках диаметром 11,25 см. Аналогичным образом приготавливают и испытывают растворы соединения A - бензил 2-[4-/6-хлор-2-хиноксалинилокси/фенокси]пропаноата, соединения, описанного в патенте США 4629493 (соединение 55).
Структуры испытываемых соединений являются следующими:
Соединение 2: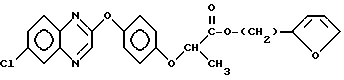
Соединение 4:
Соединение 6:
Соединение A:
Результаты испытания приведены в табл. 4.
Приведенные выше данные ясно показывают неожиданную активность соединений настоящего изобретения по сравнению с известными гомоциклическими производными.
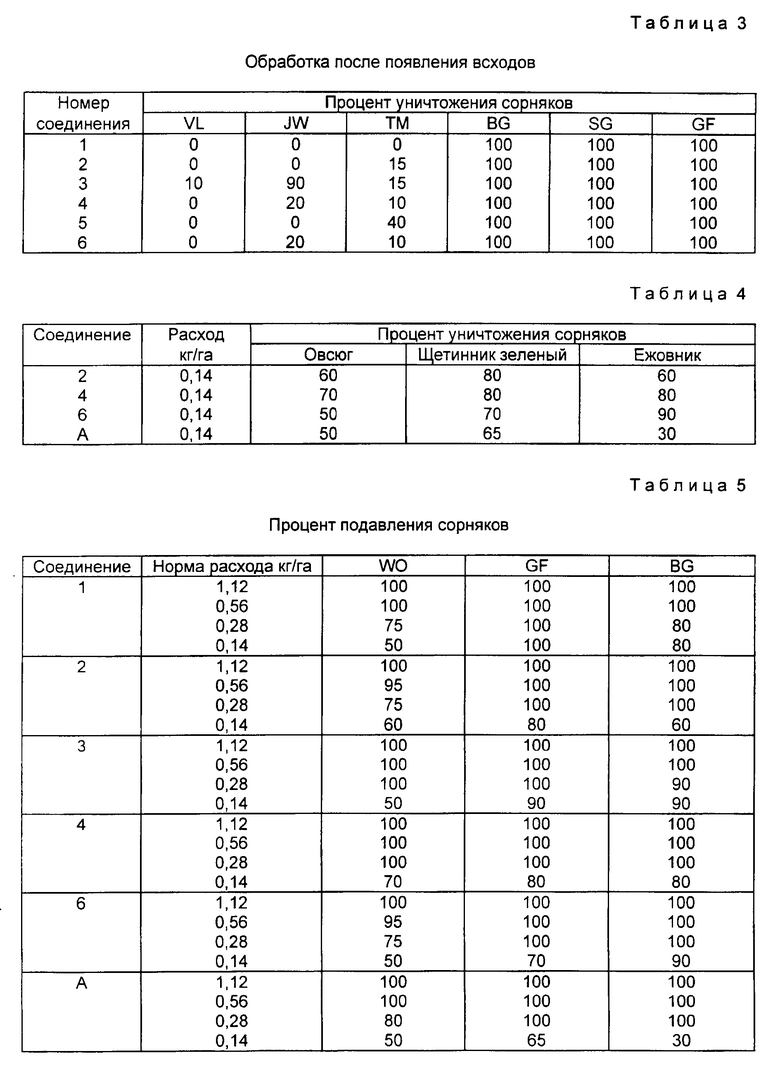
Кроме того, проводят дополнительные испытания, аналогичные описанным в примере 3 и табл. 2, в которых соединения 1-4 и 6 испытывают на действие против овсюга (WО), щетинника зеленого (GF) и ежовника (BG) при различных нормах расхода. Испытывают также известное соединение A (из примера 5). Результаты представлены в табл. 5.
Эти результаты показывают превосходное предвсходовое гирбицидное действие этих соединений при таких низких нормах расхода, как 0,14 кг/га и по крайней мере до 1,12 кг/га. Поскольку все испытанные соединения дают 100%-ное уничтожение при дозе 1,12 кг/га, правомерно ожидать, что тот же результат будет получен при любой более высокой норме расхода применяемого соединения.
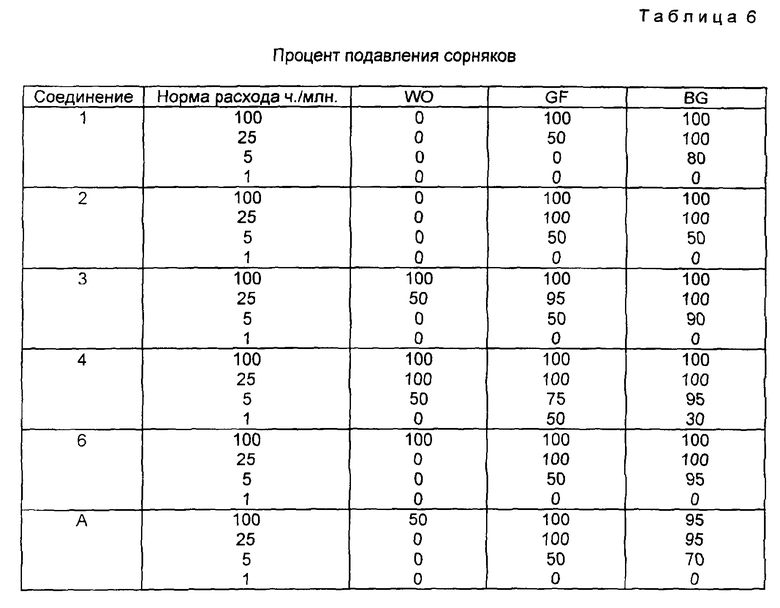
Также проводят дополнительные испытания в соответствии с описанными в примере 4 и табл. 3. Полученные результаты представлены в табл. 6.
Приведенные результаты демонстрируют превосходный послевсходовый селективный гербицидный эффект настоящего изобретения в широком диапазоне доз.

Изобретение относится к новым производным хиноксалинилоксифеноксипропаноата общей формулы, где n целое число 1, 2, 3, R1-галоген или тригалометил, R2-водород, R3-фуранил, тетрагидрофуранил, диоксаланил, пиранил, тетрагидропиранил, необязательно замещенный 1, 2 или 3 заместителями, выбранными из группы, включающей оксогруппу и C1-C3-алкил. Соединения проявляют высокую селективную гербицидную активность. Формула соединений:  3 з.п. ф-лы, 6 табл.
3 з.п. ф-лы, 6 табл.

где n = 1, 2, 3;
R1 - галоген или тригалометил;
R2 - водород;
R3 - фуранил, тетрагидрофуранил, диоксаланил, пиранил или тетрагидропиранил, необязательно замещенный 1, 2 или 3 заместителями, выбранными из группы, включающей оксогруппу и С1 - С3-алкил.
| US, 4629493, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ЕР, 0023785 А1, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕР, 0042750 А1, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕР,0046467 А1, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕР, 0046468 А1, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕР, 0058639 А1, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1998-05-20—Публикация
1989-01-05—Подача