Изобретение относится к комплексам включения N-этоксикарбонил-3-морфолинсиднонимина (молзидомин) или его соли с циклодекстрином или производным циклодекстрина или его производным, преимущественно, с гептакис-2,6-O-диметил-(β -циклодекстрином (димеб), гидроксипропил- β -циклодекстрином или с β- или γ-циклодекстрином, к способу их получения, а также к содержащим их фармацевтическим композициям и способам получения их, а также способу лечения стенокардии или ишемической болезни сердца.
Молзидомин является соединением, обладающим антиангинальным и антиишемическим действием, которое широко применяется для предупреждения и лечения стенокардии. Его преимущество по сравнению с органическими нитратами заключается в большей продолжительности действия и в меньших побочных эффектах, вследствие чего он не вызывает привыкания и редко - головные боли, причем менее сильные. Явно выражено также его действие против аритмии, фибринолиза, агрегирования тромбоцитов, а также способность понижать кровяное давление.
Молзидомин поступает на рынок в виде таблеток, содержащих 2 мг, 4 мг (препарат обычный) и 8 мг (препарат замедленного действия) активного ингредиента под названием корватон (Casella, Riedel), мориал (Takeda Ltd.). Композиция замедленного действия - это композиция, в которой активный ингредиент содержится в микрокапсулах, с особым воском в отношении 1:4, которые обеспечивают эффективную концентрацию в плазме крови в продолжение 12 ч.
Молзидомин относительно хорошо растворяется в воде (18 мг/мл при 25oC), устойчив в воде при pH 5-7. Очевидно, что лимитирующей стадией ресорбции его из желудка и кишечного тракта не является растворимость. Препараты для перорального применения, в которых содержится 2 мг активного ингредиента, эффективны в течение 3-5 ч. Максимальный уровень содержания в крови может быть достигнут в течение 1/2-1 ч. Он прекрасно поглощается вдоль всего Gi- тракта, его биодоступность удовлетворительна. Наибольшие преимущества обеспечивают в случае препаратов, предупреждающих стенокардию, формы с контролируемым выделением активного ингредиента. Это обеспечивает длительную и контролируемую ресорбцию медикамента и поддержание в течение длительного периода времени терапевтически эффективного содержания в плазме крови. Побочные эффекты можно в значительной степени снизить за счет исключения слишком высокого, токсичного, уровня содержания в плазме крови.
Особенно перспективны трансдермальные формы с контролируемым выделением активного агента.
Ресорбция активного ингредиента через кожу зависит от его физико-химических свойств и от растворимости липоидов и главным образом - от используемой формы.
Сам молзидомин ресорбируется через кожу медленно и в малой степени, его биоусвояемость всего 4%, в связи с чем применяются добавки, способствующие ресорбции.
В описании к Европатенту N 127 468, Takeda Company, описан препарат для введения через кожу, обладающий прекрасной ресорбцией молзидомина, в состав которого входит специальная способствующая проникновению добавка, состоящая из двух компонентов - смесь пропиленгликоля, содержащая 10% олеиновой кислоты.
Возможен следующий механизм такой высокой биоусвояемости, равной 95%; компонент олеиновой кислоты изменяет проницаемость защитного слоя кожи (Stratum corneum) за счет растворения его барьерных липоидных компонентов. Таким образом, молзидомин отлично ресорбируется через видоизмененный слой кожи.
Известно, что ресорбция молзидомина и пропиленгликоля происходит в одинаковой степени и соответственно в аналогичных количествах, что означает, что может ресорбироваться только молзидомин, растворенный в пропиленгликоле.
Обнаружено, что эффект молзидомина или его солей можно замедлить за счет образования его комплекса с гептакис-2,6-О-диметил- β -циклодекстрином, гидроксипропил- β -циклодекстрином или с β - или γ -циклодекстрином.
Целью настоящего изобретения является создание нового комплекса включения N-этоксикарбонил-3-морфолинсиднонимина или его соли с циклодекстрином или его производным, с замедленным высвобождением последнего из комплекса, а также создание фармацевтических композиций, содержащих указанный комплекс включения или N-этоксикарбонил-3-морфолинсиднонимин или его соли в смеси с циклодекстриновой компонентой и способа лечения стенокардии или ишемической болезни сердца, используя препарат на основе комплекса включения N-этоксикарбонил-3- морфолиносиднонимина, а также разработка способов получения комплекса и фармацевтических композиций.
Поставленная цель достигается новым комплексом включения N- этоксикарбонил-3-морфолино-сиднонимина или его соли с циклодекстрином или производным циклодекстрина, преимущественно β - или γ -циклодекстрином, гептакис-2,6-O- диметил- β -циклодекстрином или гидроксипропил-циклодекстрином при молярном соотношении N-этоксикарбонил-3-морфолиносиднонимина или его соли к циклодекстрину или производному циклодекстрина, равном 1:1-40 соответственно.
Комплекс получают взаимодействием N-этоксикарбонил-3-морфолинсиднонимина или его соли с циклодекстрином или производным циклодекстрина, преимущественно β - или γ -циклодекстрином, гептакис-2,6,O-диметил- β -циклодекстрином или гидроксипропил-β-циклодекстрином, взятыми в молярном соотношении 1:1-40 соответственно, в водной среде или в среде смешивающегося с водой органического растворителя или при механическом измельчении смеси исходных реагентов. В качестве смешивающегося с водой органического растворителя предпочтителен алканол.
Предпочтительно комплекс включения выделяют из раствора путем лиофилизации, сушки с распылением или вакуумной сушки.
Поставленная цель достигается также фармацевтическими композициями, включающими комплекс включения или N-этоксикарбонил-3-морфолинсиднонимин в смеси циклодекстриновым компонентом при соотношении N-этоксикарбонил-3-морфолинсиднонимина или его соли к циклодекстриновой компоненте, равной 1: 1-40.
Фармацевтические композиции получают путем смешения активного ингредиента с фармацевтически приемлемыми целевыми добавками.
Таким образом образованный циклодекстриновый комплекс или смесь предназначены для задерживания высвобождения молзидомина в поток крови, что снижает отрицательное воздействие на пациента токсичности вводимого лекарства.
Комплексы согласно данному изобретению могут быть использованы в терапии в виде, например, таблеток, пилюль, микрокапсул, мазей, инъекций, капель, вливаний, предпочтительно в виде таблеток или микрокапсул, предназначенных для приема один раз в день.
Дозы, в которых употребляются комплексы согласно данному изобретению, могут меняться в зависимости от возраста, веса тела и состояния субъекта, способа употребления, количества приемов и т.п., но составляют от 6 до 800 мг в день, предпочтительно 10-400 мг в день.
Эффект замедленного выделения преобладает, в частности, в случае применения фармацевтической композиции в виде таблеток, по одной в день, микрокапсул и мазей, особенно подходящих соответственно для введения через кожу. Фармацевтические композиции согласно данному изобретению изготовляют обычным способом. В качестве адьювантов и носителей используют вещества, обычно применяемые в области фармакологии.
Иллюстрацией взаимодействия комплекса в растворе может служить тест на проникновение через мембрану.
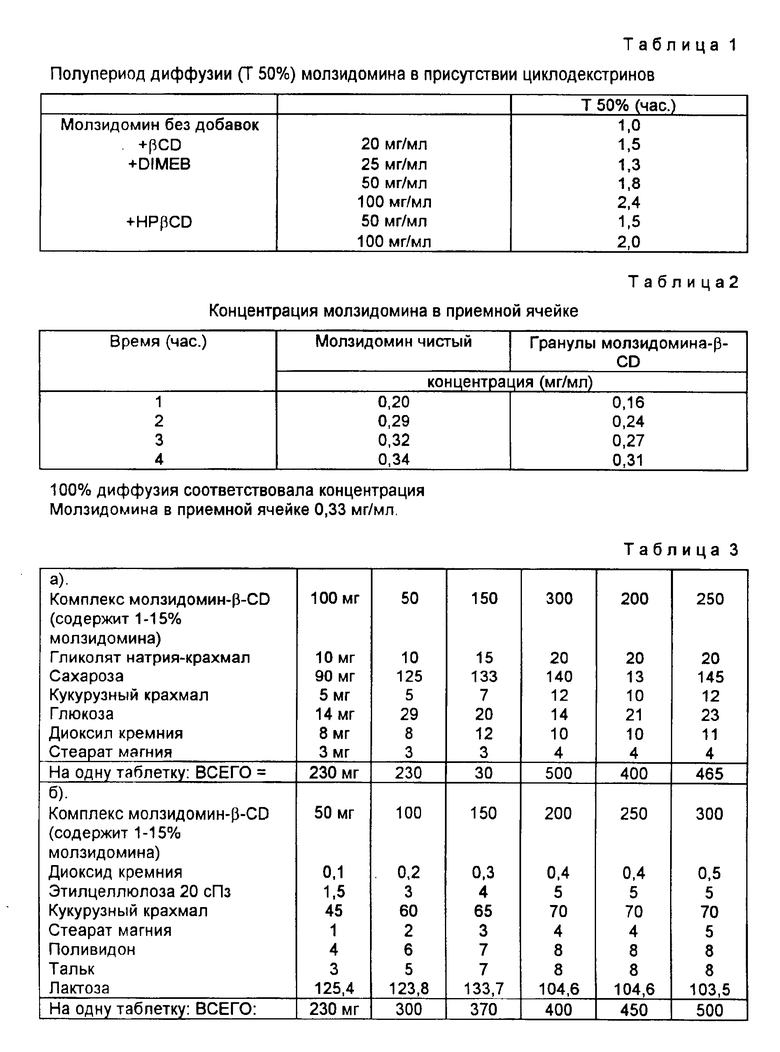
Использовали целлофановую мембрану visking-типа (средний диаметр пор  ). Водные растворы молзидомина концентрацией 1 и 2 мг/мл поместили в донорскую ячейку, тогда как в приемном отделении ячейки с проницаемой мембраной находилась дистиллированная вода. Растворы перемешивали с помощью магнитной мешалки, температура их поддерживалась на уровне 37 + 1oC. Через соответствующие интервалы времени из растворов в приемнике пипеткой отбирали пробы и измеряли концентрацию растворов в приемнике с помощью УФ-спектрофотометрии. Тест повторили в присутствии различных циклодекстринов, при различных концентрациях в донорском отделении.
). Водные растворы молзидомина концентрацией 1 и 2 мг/мл поместили в донорскую ячейку, тогда как в приемном отделении ячейки с проницаемой мембраной находилась дистиллированная вода. Растворы перемешивали с помощью магнитной мешалки, температура их поддерживалась на уровне 37 + 1oC. Через соответствующие интервалы времени из растворов в приемнике пипеткой отбирали пробы и измеряли концентрацию растворов в приемнике с помощью УФ-спектрофотометрии. Тест повторили в присутствии различных циклодекстринов, при различных концентрациях в донорском отделении.
В табл.1 перечислены периоды времени, необходимые для диффузии 50% молзидомина (Т 50 %).
Скорость проникновения молзидомина может быть в значительной степени снижена, что указывает на наличие значительного взаимодействия между молзидомином и исследуемыми циклодекстринами.
Только свободное (не в виде комплексов) лекарство может свободно проникать через использованную мембрану. Концентрация свободного лекарства зависит от величины константы устойчивости комплекса.
Чем меньше константа устойчивости, тем выше концентрация свободного лекарства, при которой возможно проникновение через мембрану. Напротив, в случае, когда комплекс очень устойчив или концентрация циклодекстрина достаточно высока (он присутствует в большом избытке), равновесие диссоциации комплекса сдвигается в сторону комплексообразования, и диффузия в значительной степени затрудняется.
Полученные результаты обеспечивают принцип контроля (поддержания, изменения) профиля высвобождения молзидомина через полимер, образующий полупроницаемую мембрану, через образование комплексов с декстрином, согласно данному изобретению.
Пример 1. Комплекс молзидомин-димеб, полученный в результате лиофилизации. Растворили в 100 мл дистиллированной воды 7 г димеба (5 ммолей, содержание влаги 2 %), а затем в полученном растворе растворили 0,4 г молзидомина. Заморозили полученный гомогенный раствор и подвергли его дегидратации путем лиофилизации, след, чтобы по ходу процесса раствор - подвергался как можно более слабому воздействию света. Целесообразно заворачивать реактор в черную бумагу, пока продолжается растворение. Полученный продукт представляет собой светлый рыхлый порошок, содержание активного ингредиента, по данным спектрофотометрии, составляет 5±0,4%. Это соответствует молярному соотношению молзидомин: димеб около 1:3. Тест, показывающий факт комплексообразования. Кривые дифференциальной сканирующей калориметрии (ДСК) показали характерные различия между физической смесью и лиофилизированным комплексом с димебом. Ход кривых ДСК механической смеси и комплекса различен: в случае смеси острый эндотермический пик при 140-142oC отвечает плавлению молзидомина, тогда как на кривой комплекса в этом температурном интервале имеется острый экзотермический пик. Этот последний можно объяснить химическим разложением комплекса при нагревании. Рентгеновская дифрактометрия. Дифрактограмма комплекса выявила аморфную структуру комплекса, несмотря на то, что оба исходных вещества обладают кристаллической структурой. Следовательно, результатом образования комплекса включения может быть новый тип структуры твердого состояния. Исследования C13-ЯМР доказали, что этоксикарбонильная часть молекулы молзидомина располагается внутри пустоты молекулы димеба. Этот факт иллюстрируется значениями химических сдвигов (Δδ) , поскольку величина химического сдвига указывает на то, каким образом происходит внедрение в растворе. Наибольшие сдвиги относятся к части молекулы-"гостя", которая входит в пустоту молекулы циклодекстрина. Для этоксикарбонильной части можно измерить величину Δδ= -2,2±1,3 ppm, тогда как для морфолиновой части молекулы-"гостя" химические сдвиги практически нельзя зарегистрировать.
Пример 2. Получение комплекса молзидомин-димеб путем сушки с распылением. Растворили 14 г димеба (10 ммолей, влажность 2%) и 1,2 г молзидомина (5 ммолей) в 180 мл дистиллированной воды при ультразвуковом перемешивании. Полученный гомогенный раствор подвергли сушке с распылением, температура подаваемого воздуха составляла 125oC, а выходящего 92oC. В процессе обработки и раствор, и сосуд, в котором содержался продукт, соответственно, защищали от света и непрерывно перемешивали. Выход: 10 г. Полученный продукт представлял собой рыхлый белый порошок с содержанием активного ингредиента, по данным спектрофотометрии, около 7,8 ± 0,2 %, что соответствует молярному отношению приблизительно 1: 2. Кривые термического анализа (ДСК) продукта, полученного сушкой с распылением, и его дифрактограммы идентичны снятым с комплекса, полученного в результате лиофилизации.
Пример 3. Получение комплекса молзидомин- β -CD смешиванием. Гомогенизировали 6,6 г β -циклодекстрина (5 ммолей, содержание влаги 14%) и 0,6 г (2,5 ммоля) молзидомина во фрикционной мельнице, защищенной по возможности от света. Добавили 3 мл 50%-ного этилового спирта и перемешивали тяжелую суспензию еще в течение 30 мин; после того как распределили продукт, отличающийся тяжелой маслянистостью и пастообразной консистенцией, на предметном стекле, его высушили до постоянного веса в эксикаторе в присутствии пятиокиси фосфора. Полученный продукт превратили в порошок, содержание в нем активного ингредиента составляло 9±0,5% (по данным спектрофотометрии), что соответствует молярному отношению около 1:2. Кривые ДСК молзидомина, его механической смеси и комплекса, образуемого им с β -CD, значительно различались. Эндотермический пик при 140-142oC на кривой ДСК полностью исчезал в случае комплексов с β -CD, полученных как смешиванием, так и лиофилизацией. Это указывает на то, что молзидомин связан в комплекс, и в интервале температур 130-160oC даже при 50-кратном увеличении на кривой не обнаруживался эндотермический пик плавления - в случае комплекса, полученного в результате лиофилизации. При снятии кривой ДСК в атмосфере аргона разложение молзидомина при нагревании заметно подавляется, что позволяет количественно оценить содержание молзидомина в свободном виде и в составе комплекса на основании сравнения областей кривых вблизи пика плавления. Плавление чистого молзидомина соответствует изменению энтальпии ΔH = 140 мДж/мг. В случае замороженного и высушенного комплекса оказалось, что комплексуется полностью весь молзидомин, а в случае комплекса, полученного смешиванием, - менее 10%.
Пример 4. Получение комплекса молзидомин HP-β CD в результате лиофилизации. Растворили 13 г HP- β -CD (0,01 моль) (C3 = 2,7, где C3 означает среднюю степень замещения в расчете на молекулу циклодекстрина) в 100 мл дистиллированной воды. Добавили 0,7 г молзидомина, растворение интенсифицировали перемешиванием, раствор был защищен от воздействия света. Из полученного гомогенного раствора удалили воду теми же методами, что и в предыдущих примерах. Продукт представлял собой белый рыхлый порошок, содержание молзидомина, определенное методом спектрофотометрии, составляло 5±0,2%, что соответствует молярному отношению молзидомин:HP- β CD приблизительно 1:3.
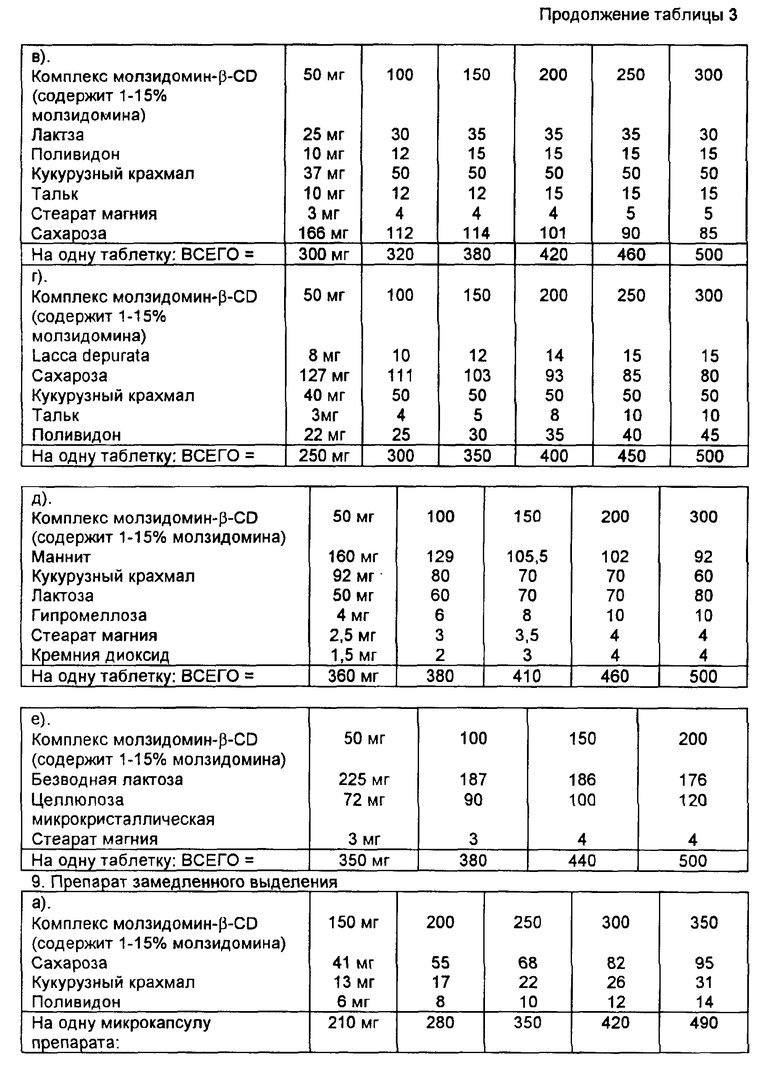
Пример 5. Получение гранул комплекса молзидомин- β CD смешиванием. Смешали в ступке 1 г (4,1 ммоля) молзидомина и 11 г β -CD (8,3 ммоля, влажность 14%), добавили 4 мл 30 %-ного этилового спирта, растирали плотную суспензию в течение 30 мин. Полученный продукт, имевший пастообразную консистенцию, размазали на подносе и сушили при 40oC в течение двух часов. Затем полусухой продукт протерли через сито (размер пор 1 мм). Полученные гранулы высушили при 60oC до постоянного веса и повторно просеяли через сито, получив в результате гранулы желаемого размера. Содержание активного ингредиента составило 10 ± 0,5%, по данным УФ-спектрофотометрии, что приближенно соответствует величине молярного отношения молзидомин: β -CD 1:2. Полученные гранулы отличались соответствующей текучестью, низким содержанием порошка, и их можно применять для изготовления сердцевины таблеток, в котором содержится медикамент в желаемой дозировке, способом прямого прессования, или для изготовления форм постоянного высвобождения путем прямого прессования с полимерными компонентами, из которых образуется матрица, или для получения пилюль с пленочным покрытием в псевдоожиженном слое, где покрытие играет роль полупроницаемой мембраны в процессе растворения. Сердцевины таблеток, полученные простейшей технологией прямого прессования, можно использовать для изготовления дозированных форм контролируемого замедленного выделения путем нанесения на них покрытия из полимера или из смеси полимеров, известных в данной области. Тест на проникновение через мембрану. С использованием описанной выше ячейки с полупроницаемой мембраной исследовали профиль диализа гранул молзидомин- β -CD. В эксперименте использовали молзидомин с концентрацией 1 мг/мл и эквивалентное количество гранул комплекса. В табл.2 приведены измеренные концентрации молзидомина в приемной ячейке через различные интервалы времени.
Пример 6. Таблетки молзидомина с содержанием активного ингредита 2 мг на таблетку.
Композиция:
40 мг комплекса молзидомин-димеб с содержанием активного ингредиента 5%, полученного по методике примера 1;
40 мг кукурузного крахмала;
78 мг молочного сахара;
2 мг стеарата магния.
Общий вес таблетки 160 мг.
Пример 7. Приготовление мази для использования через кожу, в состав которой входит в качестве агента 10 мг комплекса молзидомина и 2 г геля. Растворили 2 г комплекса молзидомин-димеб (содержание активного ингредиента 5%) в 20 мл дистиллированной воды. К раствору при интенсивном перемешивании добавили 50 мг KLUCEL-HF (гидрокси-пропилцеллюлоза). При этом получается вязкий раствор, с трудом перемешиваемый, который выдерживают при комнатной температуре в течение 1 дня, защищая от действия света. В результате прозрачная мазь, в 2 мг которой содержится 10 мг молзидомина.
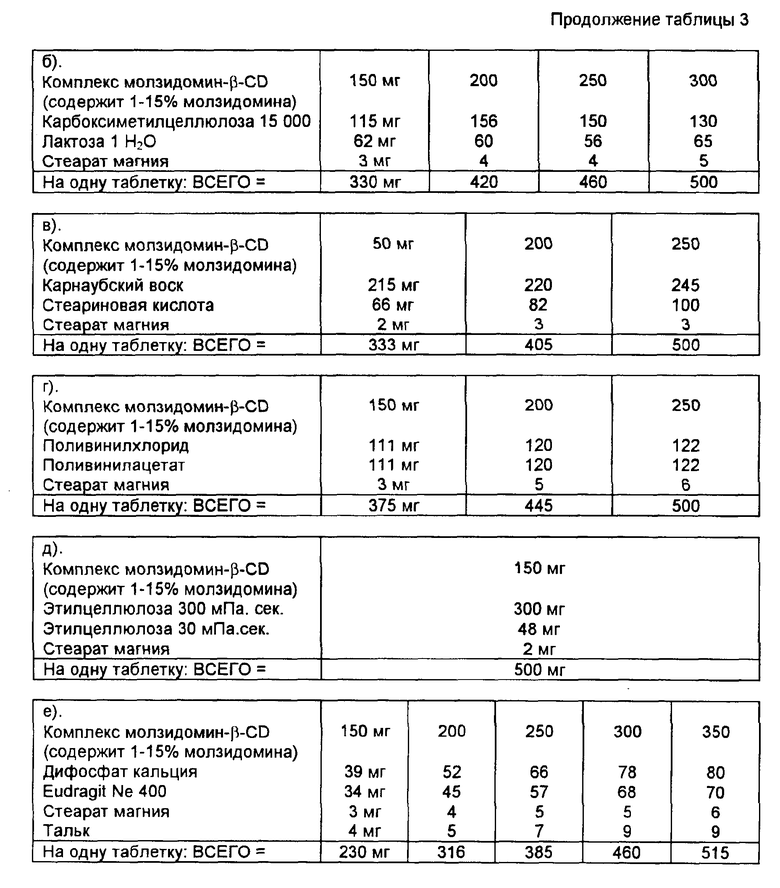
Пример 8. Фоpмы незамедленного высвобождения (см. табл. 3).
Использование: изобретение относится к комплексам включения N-этоксикарбонил-3-морфолинсиднонимина или его солей с циклодекстрином или его производными, к их получению и к содержащим их фармацевтическим композициям. Сущность изобретения: комплекс включения N-этоксикарбонил-3-морфолинсиднонимина или его соли с производным циклодекстрина получают: а) взаимодействием N-этоксикарбонил-3-морфолинсиднонимина или его соли и производного циклокстрина в среде растворителя и при желании выделением комплекса из раствора путем удаления воды или б) очень энергичным размалыванием смеси N-этоксикарбонил-3-морфолинсиднонимина или его соли с производным циклодекстрина. 7 с. и 5 з. п. ф - лы, 3 табл.
Приоритет по пунктам:
28.03.90 - признаки, касающиеся комплексов включения N-этоксикарбонил-3- морфолинсиднонимина или его солей и гептакис-2,6-О-диметил -β- циклодекстрина, способа получения этого комплекса включения, фармацевтических композиций, содержащих указанные соединения, способов получения этих фармацевтических композиций и способов лечения с использованием указанных соединений;
27.06.90 - признаки, касающиеся комплексов включения N-этоксикарбонил-3- морфолинсиднонимина или его солей с циклодекстрином, способа получения этого комплекса включения, фармацевтических композиций, содержащих указанные соединения, способа их получения и способа лечения с использованием указанных соединений.
| EP, заявка, 0153999, кл | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| EP, заявка, 0127468, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1998-05-20—Публикация
1991-03-28—Подача