Изобретение относится к гидрометаллургии благородных металлов, в частности к аффинажу золота, и может быть использовано для получения золота высокой степени чистоты (99,99%).
Известен электролитический способ получения золота высокой степени чистоты (99,99%), заключающийся в проведении электролиза золотохлористоводородной кислоты, при котором анод представляет сплав золота с примесями металлов (Ag, Cu, Fe, Pt, Pd и др.), катод - чистую золотую пластину. В процессе электролиза чистое золото осаждается на катоде, а примеси концентрируются в электролите [1]. Недостатками способа являются очень большая его энергоемкость, необходимость частой смены золотосодержащего электролита, накопление примесей в котором может вызывать осаждение их на катоде и тем самым приводить к снижению чистоты целевого продукта, необходимость удержания в процессе аффинажа большого количества чистого золота для возобновления электролита.
Более эффективными являются способы получения золота с использованием жидкостной экстракции. Для извлечения золота известен широкий класс экстрагентов. Большинство из них неизбирательны и используются не для глубокой очистки золота от примесей, а для извлечения золота и отделения его от ряда элементов [2]. Число экстрагентов, используемых для отделения макроколичеств золота от сопутствующих ему элементов, довольно ограничено.
Известен способ получения золота из концентратов, основанный на экстракции его из солянокислых растворов метилизобутилкетоном [3, с. 360]. По данному способу проводят двухступенчатые экстракцию и реэкстракцию с последующим восстановлением золота из органической фазы железным порошком и получением металлического золота, требующего дальнейшей очистки. Недостатками способа являются высокая растворимость экстрагента в воде (17 г/л), неудовлетворительное отделение золота от ряда элементов (вместе с золотом экстрагируются железо и теллур), что не приводит к получению золота высокой степени чистоты.
Известен способ извлечения золота из солянокислых растворов экстракцией диэтиловым эфиром [4].
Недостатками его являются использование токсичного взрывоопасного летучего экстрагента (Tкип. = 35oC, Tвспышки = -45oC), а также сравнительно высокая растворимость эфира в воде (66 г/л).
Известен способ извлечения золота из раствора эксракцией β,β′ -дихлорэтиловым эфиром [5].
Недостатком этого способа является относительно высокая растворимость дихлорэтилового эфира в воде (10 г/л), что приводит к потере экстрагента и необходимости его извлечения из сбросных вод.
Известен способ получения высокочистого золота (выбран нами в качестве прототипа), основанный на его экстракции из солянокислых растворов дибутиловым эфиром диэтиленгликоля (дибутилкарбитол, ДБК) [3, с. 358; 6]. Для удаления соэкстрагированных примесей экстракт трижды отмывают раствором соляной кислоты концентрации 1,5 моль/л, после чего золото восстанавливают из органической фазы до металла горячим раствором щавелевой кислоты в течение трех ч. В результате последующих операций - фильтрации, промывки порошка золота и плавки - получают золото чистотой 99,99%. Из щавелевокислого реэкстракта и солянокислых промывных растворов извлекают другие благородные металлы. Очистка золота от примесей происходит на стадиях экстракции, отмывки экстракта и реэкстракции (восстановления) щавелевой кислотой. Недостатком способа является использование в качестве экстрагента дибутилкарбитола, который не является широкодоступным реагентом, относительно дорог, имеет заметную растворимость в воде (3,0 г/л). Кроме того, поскольку ДБК не является высокоселективным реагентом, то после экстракции требуются дополнительные стадии (три) отмывки экстракта от соэкстрагированных примесей.
Задачей изобретения - получения высокочистого золота (степень чистоты - 99,99%) - является упрощение и удешевление процесса, осуществляемые на стадиях экстракции и отмывки экстракта.
Это достигается тем, что в отличие от способа получения высокочистого золота с использованием ДБК, включающем перевод металла в раствор, содержащий соляную кислоту, экстракцию золота из раствора, промывку экстракта, выделение золота, по данному изобретению процесс получения высокочистого золота из чернового золота, содержащего примеси серебра, меди, железа, палладия и другие, проводят путем экстракции золота из солянокислого или азотно-солянокислого раствора трибутилфосфатом при мольном соотношении экстрагента к золоту (3,0-4,0) : 1,0, промывки раствором серной кислоты, при этом выделение золота ведут последовательно реэкстракцией и восстановлением известными методами.
Отличительными от прототипа признаками являются условия осуществления действий:
экстракцию проводят трибутилфосфатом при мольном отношении экстрагента (ТБФ) к металлу (3,0-4,0) : 1,0;
отмывку экстракта осуществляют раствором серной кислоты в одну стадию.
Упрощение и удешевление процесса достигается за счет:
применения широкодоступного дешевого экстрагента - трибутилфосфата;
сокращения количества стадий отмывки экстракта;
уменьшения потерь экстрагента вследствие меньшей его растворимости.
Сущность предлагаемого способа заключается в следующем.
Известно, что 100% ТБФ (концентрация 3,67 моль/л) является неселективным реагентом [7] и поэтому он не был применен для очистки золота. Экстракция золота ТБФ характеризуется высоким коэффициентом распределения : DAu = 30000 для 1 моль/л HCl при CТБФ >> CAu и VВОД : VТБФ = 1 : 1, т.е. когда количество трибутилфосфата (в молях) в органической фазе превышает количество золота (в молях) в водной фазе. С уменьшение концентрации ТБФ коэффициент распределения золота падает. Экстракция золота (III), железа (III),серебра (I) и ряда других металлов протекает по одинаковому (гидратно-сольватному) механизму. Показано, что для золота (в широкой области его концентраций) происходит образование сольвата с ТБФ, равновесие которого имеет вид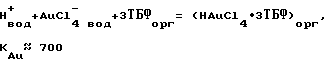
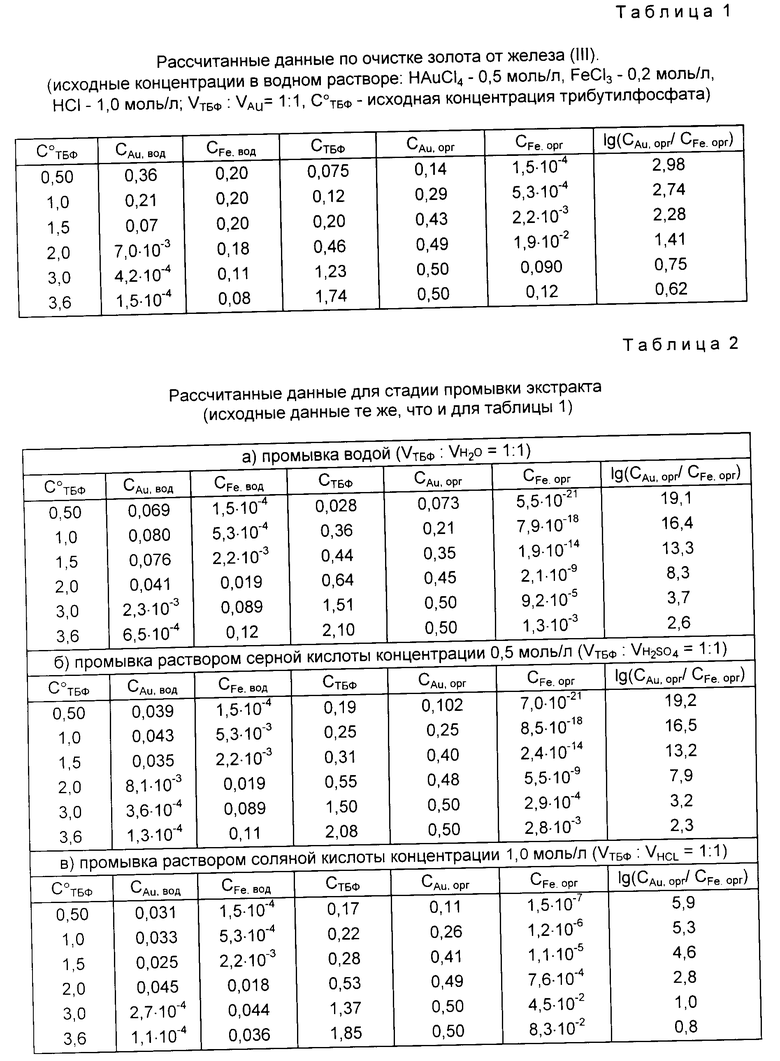
По такой же схеме (экстракция в форме металлокислот), но с гораздо меньшими значениями констант трибутилфосфат извлекает и другие металлы, образующие в солянокислых растворах комплексные анионы (De, Ag, Cu, Pd и др. ). При экстракции ТБФ коэффициент распределения золота намного выше, чем у всех основных примесей. За счет связывания ТБФ золотом в сольват концентрация свободных молекул ТБФ в органической фазе снижается, что приводит к уменьшению коэффициентов распределения примесей. Это уменьшение тем больше, чем ниже молярное соотношение ТБФ к золоту. Особенно сильно коэффициенты распределения примесей снижаются, когда соотношение ТБФ к Au становится меньше, чем требуется по стехиометрии для образования сольвата золота, т.е. трех. Другими словами, очистка золота от примесей при экстракции ТБФ (выражающаяся соотношением концентраций золота и примесей в органической фазе) будет тем эффективней, чем ниже будет исходное мольное соотношение количеств ТБФ и золота. В табл. 1 в качестве примера представлены расчетные данные по очистке золота от железа (III) как от металла-примеси (соотношение концентраций в органической фазе) в зависимости от концентраций ТБФ. Железо (III) в условиях, близких к условиям экстракции золота (1,0 моль/л HCl), имеет коэффициент распределения один из самых высоких среди основных примесей. Равновесие для железа (III) имеет вид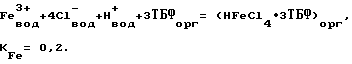
Расчет равновесных концентраций железа (III), золота (III), ТБФ в органической и водной фазах проведен с использованием вышеприведенных значений констант равновесий экстракции железа и золота (KAu и KFe) при условиях, заданных в табл. 1.
Как видно из полученных данных табл. 1, при проведении экстракции золота трибутилфосфатом при любом соотношении в молях экстрагента к золоту очистка золота от железа не происходит до желаемой чистоты (логарифм отношения концентраций золота к железу в органике должен быть больше четырех для получения высокочистого золота).
Обязательной стадией является промывка органической фазы. Во-первых, на стадии промывки происходит дополнительное более полное удаление из органической фазы соэкстрагированных примесей. Во-вторых, что очень важно, удаляются микрокапли эмульсии водной фазы, захваченные органической фазой при экстракции. Их попадание в реэкстракт приводит к загрязнению конечного продукта.
Промывка органической фазы ведет к тому, что часть золота может перейти в промывные воды. Поэтому предпочтительнее применять экстрагент с высоким коэффициентом распределения для золота, что также свидетельствует в пользу ТБФ. Промывка только водой нежелательна, так как при этом заметная часть золота переходит в промывные воды и, кроме того, некоторые примеси в этих условиях способны давать осадки нерастворимых гидроокисей, и поэтому желательно промывку экстракта проводить кислым раствором. Промывка раствором соляной кислоты снижает количество золота, перешедшее в промывной раствор, но при этом удаление соэкстрагированных примесей происходит значительно хуже вследствие образования способных экстрагироваться хлоридных комплексов. Поэтому может потребоваться несколько стадий отмывки, как это проводится, например, в прототипе. В табл. 2 для сравнения приведены рассчитанные величины логарифма отношения концентраций золота и железа при проведении стадии промывки экстракта водой, растворами соляной и серной кислот.
Наиболее приемлемой (с точки зрения удаления примесей и удержания экстрагированного золота в органической фазе) является промывка раствором серной кислоты. Дополнительно к рассмотренным выше факторам следует добавить, что при промывке серной кислотой происходит срабатывание плохо экстрагируемых сульфатных комплексов со многими примесными ионами неблагородных металлов. Использование в наших опытах серной кислоты концентрации 0,5 моль/л обусловлено тем, что дальнейшее ее повышение не имеет смысла, так как равновесная концентрация сульфат-иона при этом не изменяется и, следовательно, извлечение примесей за счет образования сульфатных комплексов не увеличивается. Кроме того, дальнейшее увеличение концентрации серной кислоты ведет к увеличению активности всех комплексных форм и, следовательно, худшему извлечению примесей из органической фазы в водную. Снижение концентрации H2SO4 ниже 0,5 моль/л возможно, но это ведет к общему снижению кислотности и, следовательно, к увеличению перехода золота в водную фазу. Поэтому нижний порог концентрации H2SO4 определяется предельно допустимым по требованиям производства содержанием золота в промывных водах с учетом затрат на его извлечение.
Из отмытого очищенного от примесей экстракта золото извлекается известными методами, например по [8].
Указанные отличительные признаки являются существенными и создают новый положительный эффект по сравнению с прототипом.
Высказанное выше подтверждается следующими примерами.
Способ очистки золота проверяли на солянокислом (раствор I) и азотно-солянокислом (раствор II) растворах. Раствор золотохлористоводородной кислоты был получен растворением чернового металла, полученного из электронного лома (чистота около 95%, основные примеси Cu, Fe, Sn, Ag) в царской водке с последующим трехкратным выпариванием с концентрированной соляной кислотой. Затем в золотосодержащий раствор были дополнительно введены примеси металлов, а именно соли железа (FeCl3), серебра (AgCl), меди (CuCl2), палладия (H2PdCl4). Состав исходного раствора I: CAu = 0,544 моль/л, CFe = 0,1 моль/л, CCu=0,1 моль/л, CPd = 0,04 моль/л, CAg до насыщения по AgCl, CHCl = 1моль/л. Раствор II содержал те же компоненты, что и раствор I, но дополнительно ввели азотную кислоту до концентрации 1,0 моль/л. Экстракцию золота из раствора I и раствора II проводили 50% ТБФ (1,83 моль/л, разбавитель четыреххлористый углерод) при одном контакте, продолжительности контакта 0,5 мин при комнатной температуре и при различном соотношении экстрагента к золоту (в молях), достигнутом варьированием объема органической фазы. Промывку экстракта проводили раствором серной кислоты концентрации 0,5 моль/л при соотношении Vорг : Vвод = 1 : 1, реэкстракцию золота из органической фазы проводили щелочью с последующим восстановлением его из экстракта сульфитом натрия в кислой среде. Промытый водой порошок золота спекали в королек при 900oC в фарфоровом тигле. Содержание примесей в корольке определяли атомноэмиссионным спектральным методом. Содержание примесей (мас.%) приведено в табл. 3.
Как видно из полученных данных, при проведении очистки золота экстракцией ТБФ и промывкой экстракта в найденных нами условиях с последующими стадиями реэкстракции и выделения золота известными методами происходит глубокая очистка золота от таких трудноотделяемых примесей как серебро, палладий и др. Содержание примесей составляет (56-59) • 10-4%, содержание металла 99,994%.
Интервал соотношения концентрации ТБФ к золоту (III) (3,0-4,0) : 1,0 найден нами как оптимальный как для отделения золота от примесей, так и для наиболее полного извлечения золота из раствора при обязательном проведении однократной отмывки экстракта серной кислотой. С увеличением мольного отношения ТБФ к золоту больше четырех сохраняется высокая степень извлечения золота, но при этом не достигается необходимая чистота целевого продукта. С уменьшением соотношения концентраций ТБФ к золоту меньше трех достигается необходимая чистота золота (99,99%), но при этом полнота извлечения золота в органическую фазу снижается, что нежелательно.
Попытки исключить стадию промывки показывают, что она является обязательной, особенно из-за необходимости удаления следов эмульсии водной фазы, захваченной при экстракции. Так, эксперименты по экстракции 50% ТБФ из растворов, содержащих вначале 0,5 моль/л HAuCl4 и 0,2 моль/л FeCl3 в 1 моль/л HCl, при мольном соотношении ТБФ к золоту 2,4 : 1 (Vорг : Vвод) = 0,60 показали, что содержание железа (III) в органической фазе может достигать величины 2,5 • 10-3 моль/л. При этом воспроизводимость результатов была очень плохой - содержание железа в параллельных опытах различалось в несколько раз. Содержание золота в органической фазе в этих опытах соответствовало ожидаемому (0,6 моль/л).
Использование ТБФ в качестве экстрагента предпочтительнее, так как ТБФ является более доступным и более дешевым реагентом, имеет лучшие физико-химические свойства (см. табл. 4) среди перечисленных выше используемых для отделения золота экстрагентов и, в частности, по отношению к ДБК, а именно мало летуч, малотоксичен, взрыво- и пожаробезопасен, очень мало растворим в воде. Кроме того, ТБФ устойчив к действию окислителей, например к действию концентрированной азотной кислоты, кислороду воздуха. ТБФ отвечает большинству требований промышленной технологии.
Использование предлагаемого способа очистки золота позволяет удешевить процесс, так как затраты на экстрагент оказываются значительно меньше. Данное положение подтверждается следующим сравнением затрат на экстрагент в сопоставимых ценах одного года. Согласно прототипу концентрация золота в органической фазе равна 30 г/л, то есть в 1 л дибутилкарбитола находится 30 г золота. Для очистки 30 г золота по прототипу требуется 1 л ДБК стоимостью 1760 руб. (цена 1 кг ДБК марки "ч" или 1,136 л 2000 руб. [9, с. 165]). Для очистки 30 г золота по предлагаемому способу требуется 0,125-0,167 л ТБФ (это 0,456-0,608 моль 100% ТБФ) стоимостью 0,61-0,81 руб. (цена 1 кг ТБФ марки "ч." или 1,031 или 3,759 моль 5 руб. [9, с. 491]). Поскольку использовали 50%-ный ТБФ, то стоимость разбавителя должна быть учтена. Цена 1 кг четыреххлористого углерода (0,6 л) равна 0,45 руб. [9]). Итого по предлагаемому способу затраты на стадии экстракции в 2170 раз меньше, чем по прототипу. Кроме того, сокращение числа стадий отмывки, использование более дешевой серной кислоты для промывки, уменьшение объема используемой органической фазы на стадии экстракции также ведет к удешевлению и упрощению процесса очистки золота.
Таким образом, предлагаемый способ очистки золота по сравнению с известным позволяет получать золото высокой степени чистоты (99,99%) с использованием широкодоступного экстрагента и с меньшими затратами. Использование ТБФ позволит отказаться от дефицитного реагента, сократить число стадий отмывки экстракта, снизить потери экстрагента.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ЗОЛОТА ИЗ ЧЕРНОВОГО МЕТАЛЛА | 1998 |
|
RU2150522C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ТРИБУТИЛФОСФАТА | 1996 |
|
RU2117010C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ТРИБУТИЛФОСФАТА ИЗ ВОДНЫХ РАСТВОРОВ | 1997 |
|
RU2123976C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА И СЕРЕБРА ИЗ КОНЦЕНТРАТОВ | 2007 |
|
RU2351666C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА ИЗ СОЛЯНОКИСЛОГО РАСТВОРА | 2013 |
|
RU2542181C1 |
| СПОСОБ РАЗДЕЛЬНОГО ИЗВЛЕЧЕНИЯ ЗОЛОТА И СЕРЕБРА ИЗ ТИОЦИАНАТНЫХ РАСТВОРОВ | 2008 |
|
RU2385958C1 |
| СПОСОБ РАЗДЕЛЕНИЯ МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ | 1991 |
|
RU2033442C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА ИЗ ЦАРСКОВОДОЧНЫХ И СОЛЯНОКИСЛЫХ РАСТВОРОВ | 1990 |
|
RU1741436C |
| СПОСОБ ИЗВЛЕЧЕНИЯ СКАНДИЯ ИЗ РАСТВОРОВ ХЛОРИДА АЛЮМИНИЯ | 1993 |
|
RU2081831C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗОЛОТА ВЫСОКОЙ ЧИСТОТЫ | 1997 |
|
RU2110592C1 |

Способ может быть использован в гидрометаллургии благородных металлов, в частности в аффинаже золота при получении золота высокой степени чистоты 99,99%. Проводят экстракцию золота из раствора трибутилфосфатом при мольном соотношении экстрагента к золоту (3,0-4,0) : 1,0, а промывку экстракта проводят раствором серной кислоты. Последующее выделение металла проводят известными методами. Использование изобретения позволяет удешевить процесс, так как затраты на экстрагент оказываются значительно меньше. 1 табл.
Способ получения высокочистого золота из чернового золота, содержащего примеси серебра, меди, железа, палладия и другие, включающий перевод металла в раствор, содержащий соляную кислоту, экстракцию золота из раствора, промывку экстракта, выделение золота, отличающийся тем, что экстракцию золота проводят из солянокислого или азотно-солянокислого раствора трибутилфосфатом при мольном соотношении экстрагента к золоту 3,0 - 4,0 : 1,0, промывку проводят раствором серной кислоты, а выделение золота ведут последовательно реэкстракцией и восстановлением известными методами.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Металлургия благородных металлов | |||
| /Под ред | |||
| Л.В.Чугаева | |||
| - М.: Металлу ргия, 1987, с | |||
| Способ переработки сплавов меди и цинка (латуни) | 1922 |
|
SU328A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Бусев А.И., Иванов В.М | |||
| Аналитическая химия золота | |||
| - М.: Наука, 1973 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Меретуков М.А., Орлов А.М | |||
| Металлургия благородных металлов (зарубежный опыт) | |||
| - М.: Металлургия, 1991 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| A.Zelle, I.Fijalko wski Chem | |||
| Analit (Polska) | |||
| Водоотводчик | 1925 |
|
SU1962A1 |
| Обогреваемый отработавшими газами карбюратор для двигателей внутреннего горения | 1921 |
|
SU321A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Николаев А.В., Юделевич И | |||
| Г., Буянова Л.М | |||
| и др | |||
| Изв | |||
| СО РАН Сер | |||
| хим.наук | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| D.F.C.Morris, M.Ali Khan Talanta, 1968, 15, p | |||
| Турбина, работающая угольной кислотой | 1924 |
|
SU1301A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Золотов Ю.А | |||
| , Иофа Б.З., Чучалин Л.К | |||
| Экстракция галогенидных комплексов металлов | |||
| - М .: Наука, 1973 | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| RU, 263578, C 22 B 1/00, 1979 | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Химические реактивы и высокочистые химические вещества: Каталог | |||
| - М.: Химия, 1983. | |||
Авторы
Даты
1998-06-20—Публикация
1996-10-22—Подача