Изобретение относится к биоразлагаемым полимерам, более конкретно к липофильным полимерам, которые являются биоразлагаемыми с образованием водно-растворимых полимеров.
Биоразлагаемые полимеры в течение длительного времени использовались в медицине, например, для получения биоразлагаемых материалов имплантатов и систем поставки лекарств с замедленным высвобождением.
В настоящее время они представляют широкий интерес в преодолении проблем загрязнения материалами упаковок (с длительным сроком существования) домашней утвари, детергентов и т.д.
Существует также необходимость в полимерах, которые, если их полностью или частично разрушить химическими или биологическими средствами, дают нетоксичные и легко устранимые продукты.
Биоразложение обычно включает ферментативный гидролиз конкретных химических связей в полимере, особенно сложноэфирных, уретановых или амидных групп, которые в других случаях являются стабильными при отсутствии ферментов; такой гидролиз можно дополнительно или альтернативно вести в присутствии кислот или оснований.
Для упаковочных материалов такие алифатические полиэфиры, как поликапролактон, полиэтиленадипат и полигликолевая кислота, являются материалами-кандидатами для биоразложения, хотя полиэтилентерефталаты, которые широко используют в текстиле и волокнах, устойчивы к биоразложению.
В области медицины рассасывающиеся полимеры представляют особый интерес для шовного материала и скобок для ран, рассасываемых имплантатов при лечении остеомиелитов и других костных поражений, тканевых швов и сетчатых тампонов, анастомоза, а также систем введения лекарств и диагностики.
В этих областях были предложены полиакриловая кислота, полигликолевая кислота, поли(L-лактид-со-гликолид), полидиоксанон, поли(гликолид- со-триметиленкарбонат), поли(этиленкарбонат), поли(иминокарбонаты), полигидроксибутират, поли(аминокислоты), поли(эфир-амиды), поли(ортоэфиры) и поли(ангидриды) (T.H. Barrows, Clinical Materials 1/1986/, с. 233-257), так же как и такие природные продукты, как полисахариды.
В частности, в патенте США A-4180646 описаны новые поли(органоэфиры) для использования в широком интервале продуктов.
В нашей находящейся на одновременном рассмотрении международной патентной заявке N WO92/04392, содержание которой включено сюда по ссылке, мы описываем широкий круг полимеров, отличающихся тем, что они содержат необязательно замещенные метиленовые диэфирные фрагменты формулы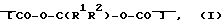
где
R 1 и R 2 каждый представляет атом водорода или присоединенную к углероду одновалентную органическую группу, или R 1 и R2 вместе образуют связанную углеродом двухвалентную группу.
Такие фрагменты особенно быстро разлагаются под действием обычных эстеразных ферментов, но являются стабильными при отсутствии ферментов.
Их можно присоединить не только к углерод-соединенным органическим группам, как в простых карбоксилатных сложных эфирах, но также к -O- атомам, как в карбонатных сложных эфирах.
Указанные фрагменты формулы (I) обычно присутствуют в полимерной цепи либо как повторяющиеся единицы, либо как связки между участками полимера, или присутствуют в группах сшивок между полимерными цепями.
В этом последнем контексте можно, например, превратить водно-растворимое длинноцепочечное природное или синтетическое небиоразлагаемое или медленно разлагаемое вещество, например, такие протеины, как желатин или альбумин, полисахариды или олигосахариды, или короткоцепные полисахариды, в водно-нерастворимую, но биоразлагаемую форму за счет сшивки с использованием сшивающих групп, содержащих фрагменты формулы (I); это может снизить стоимость продукта по сравнению с полимерами, которые содержат фрагменты формулы (I) в полимерной цепи за счет снижения относительного содержания сравнительно дорогостоящих фрагментов формулы (I).
Хотя такие сшитые полимеры имеют широкое применение, как указано в заявке N WO92/04392, их структура неизбежно накладывает некоторые ограничения на обрабатываемость полимеров, так как за счет их сшитого характера они обычно не растворимы в органических растворителях, а также и в водных растворителях и не обладают термопластическими свойствами.
Соответственно, их нельзя обрабатывать такими обычными способами, как отливка из растворителя или обработка в расплаве.
Изобретение основано на открытии того факта, что имеется возможность получать практически несшитые /например, линейные/ полимеры, содержащие биоразлагаемые липофильные боковые цепи, включающие метиленовые диэфирные фрагменты формулы (I), таким образом, что полимер объединяет преимущества практической нерастворимости в воде /или существенно пониженной растворимости в воде/ с термопластичностью и растворимостью в различных органических растворителях, и со свойством биоразлагаемости до получения водно- растворимых /и поэтому легко диспергируемых и/или устраняемых/ продуктов разложения, в частности водно-растворимых полимеров, получаемых за счет биоразлагаемого отщепления липофильных боковых цепей.
В EP-A-0130935 описаны биоразлагаемые этерифицированные полипептиды формулы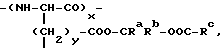
где
Ra и Rb являются алкильными группами или атомами водорода и Rc является необязательно замещенной алифатической или ароматической группой, или Rb является атомом водорода или алкильной группой, a Ra и Rb вместе образуют двухвалентную группу, такую как диметиленовую, виниленовую или финиленовую группу, y равно 1 или 2, а x таково, что молекулярная масса полимера составляет по крайней мере 5000 (и их сополимеры с другими поли/аминокислотами) в качестве носителей с замедленным высвобождением лекарств, которые могут быть смешаны с другим полимером или заключены в него.
Известно, что первой стадией в биоразложении таких полимеров является отщепление метиленовых диэфирных групп боковой метиленовой цепи до получения полимеров, содержащих фрагменты формулы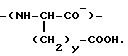
Указывается, что такие полимеры будут затем подвергнуты разложению под действием пептидаз на их компоненты - аминокислоты, которые могут быть абсорбированы хозяином, которому эта комбинация полимер/лекарство вводится.
Такой ход разложения может быть противоположен тому, который существует для полимеров настоящего изобретения, где полимеры, полученные при биоразложении липофильных - содержащих метиленовые диэфирные боковые цепи, специально выбирают так, чтобы они были водно- растворимы с тем, чтобы их можно было диспергировать и/или удалить без необходимого дальнейшего разложения.
Потенциальным недостатком полимеров, описанных в EP-A-0130935, является то, что высокое содержание водородных связей, которое существует в полипептидах, будет иметь тенденцию придать им относительно высокие температуры плавления, так что может быть их не удастся обрабатывать в расплаве без ненужного процесса деградации. Кроме того, пептидные структуры могут вызывать аллергические реакции, если их применять in vivo.
В соответствии с одним аспектом изобретения мы получили биоразлагаемые несшитые полимеры с низкой растворимостью в воде или вовсе не растворяющиеся в ней, содержащие не полипептидную полимерную цепь с боковыми цепочками, по крайней мере часть указанных боковых цепей, содержащих липофильные фрагменты, связанные с полимерной цепью метиленовыми диэфирными фрагментами формулы (I), как было указано ранее, за счет чего указанные липофильные фрагменты являются биоразлагаемо расщепляемыми до получения водно-растворимого полимера.
Как указано ранее, каждая из сложноэфирных группировок, метиленовых диэфирных фрагментов формулы (I) может быть либо карбоксилатной, либо карбонатной группировкой. Полимеры по предложенному способу могут быть представлены как содержащие фрагменты формулы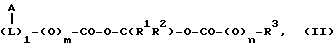
где
A является повторяющимся фрагментом неполипептидной полимерной основной цепи; L не является необязательно связывающей группой /например, l является 0 или 1/; m и n, которые могут быть одинаковы или различны, каждый является нулем или 1; R1 и R2 имеют указанные ранее значения; а R3 является липофильной органической группой.
Биоразложение метиленовых диэфирных группировок в полимерах, содержащих фрагменты формулы (II), будет обычно идти за счет ферментативного гидролитического расщепления связей, соединяющих группу O-C/R1R2/-О- с соседними карбонильными группами, и обычно приводит к получению альдегида или кетона формулы R1-CO-R2.
Характер других продуктов разложения будет меняться в зависимости от того, имеют ли каждый m и n значения 0 или 1; если m = 0, обычно образуются водно-растворимые полимеры, содержащие карбоксигруппы с фрагментами формулы (III):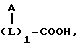
где
A, L и l имеют указанные ранее значения,
если m = 1, предположительно образующаяся группа карбоновой кислоты обычно исключает диоксид углерода до получения водно-растворимого полимера, содержащего гидроксильные группы с фрагментами формулы: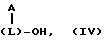
где
A, L и l имеют указанные ранее значения,
хотя продукты R3-COOH и R3-ОН аналогично будут образовываться в зависимости от того, будет ли n = 0 или 1.
Факторы, влияющие на растворимость в воде продуктов разложения полимеров, содержащих фрагменты формулы (III) или (IV), включают природу повторяющихся фрагментов A и любых сомономерных фрагментов, которые могут присутствовать, длину любой из связующих групп l и полную длину цепи полимера, которая обычно предпочтительно такова, что молекулярная масса биоразлагаемого полимера не превышает величины около 2000000. Полимеры с более низким молекулярным весом могут быть с успехом использованы, например, в таких применениях, которые требуют высокую степень биоразложения.
Так, например, может оказаться предпочтительным, чтобы полимерные системы, предназначенные для использования in vivo, например, в виде систем для введения лекарств или для диагностических целей для парентерального введения, имели молекулярную массу, не превышающую около 40000.
Повторяющиеся фрагменты A и любые сомономерные фрагменты в полимере по предложенному способу предпочтительно относительно коротки, например, содержат вплоть до 10, например 1-6 атомов углерода и необязательно кислорода, азота и серы и/или замещенных одним или более заместителей, содержащих такие гетероатомы /например такие, как оксо, гидрокси и аминогруппы/.
Там, где гидрофильные группы включены в повторяющиеся A и/или любые сомономерные фрагменты, размер этих фрагментов нет необходимости ограничивать, а возможные фрагменты таким образом включают полиоксиэтилен (например, как полиоксиэтиленовых сложных эфиров метакриловой кислоты).
Любые связующие группы L представляют собой короткие группы и включают, например, C1-3 алкиленовые группы, такие как метилен, этилен или пропилен, необязательно оканчивающиеся и/или (там, где необходимо) прерванные, например, окси, карбонил, оксикарбонил, имино или имино-карбонильными группами.
Если в связующей группе присутствуют такие полярные группировки, как атомы кислорода или иминогруппы, такие группы могут быть более длинными, например, могут содержать вплоть до 10 атомов углерода без ненужного ингибирования растворимости в воде.
Подходящие продукты разложения полимеров включают таким образом, например, поливиниловый спирт, полиакриловую кислоту, полиметактиловую кислоту, полигидроксиалкилакрилаты и метакрилаты, такие как поли(2- гидроксиэтилакрилат), полисахариды, сложные полиэфиры, простые полиэфиры, такие как полиоксиэтилены и полиоксипропилены, полиакриламиды и полиметакриламиды, такие как поли/N-гидроксиалкил/ акриламиды и метакриламиды, например, поли-N-/2-гидроксипропил/метакриламид, полиамиды, полиуретаны и эпоксиполимеры.
Вообще, продукты разложения биоразлагаемых полимеров по предложенному способу за счет их растворимости в воде сами не должны быть биоразлагаемыми; таким образом, они могут быть, например, полиолефинами.
Поэтому изобретение включает полимеры, содержащие фрагменты формулы (II), в которых A является повторяющимся фрагментом полиолефина, например этиленом или пропиленом.
Следует учитывать, что полимеры такого типа можно получить при свободнорадикальной полимеризации относительно легко и экономично, и в противоположность более сложному полипептидному синтезу нет необходимости получать такие полимеры, которые описаны в EP-A- 0130935.
В биоразлагаемых полимерах по предложенному способу по крайней мере часть повторяющихся фрагментов должна иметь звенья боковой цепи формулы;
-/L/l-/O/m-CO-O-C/R1R2/-O-CO- /O/n-R3,
как указано для формулы (II), присоединенной к полимерной цепи; следует учитывать, что точный уровень замещения может меняться, например, за счет использования методики частичной этерификации, что более подробно описано далее для модификации при желании параметров растворимости как для биоразлагаемого полимера, так и для продукта разложения полимера.
R1 и R2 /если они отличны от водорода/ и R3 в звеньях боковой цепи вышеуказанной формулы могут, например, каждый быть углеводородной или гетероциклической группой, присоединенной к атому углерода, например, содержащей 1 - 20 атомов углерода, например, такой алифатической группой, как алкильная или алкенильная группа /предпочтительно, содержащей вплоть до 10 атомов углерода/, циклоалкильной группой /предпочтительно содержащей вплоть до 10 атомов углерода/, аралифатической группой, такой как аралкильная группа /предпочтительно, содержащей вплоть до 20 атомов углерода/, арильной группой /предпочтительно содержащей вплоть до 20 атомов углерода/ или гетероциклической группой, содержащей вплоть до 20 атомов углерода, и один или более из гетероатомов, выбранных из О, S и N.
Такие углеводородные или гетероциклические группировки могут содержать одну или более из функциональных групп, таких как атомы галоидов или группы формулы -NR4R5, -CONR4R5, -OR6, -SR6 и -COOR7, где R4 и R5, которые могут быть одинаковы или различны, являются атомами водорода, ацильными группами или углеводородными группами, как указано для R1 и R2; R6 является атомом водорода или ацильной группой, или группой, как определено для R1, или R2 и R7 является атомом водорода или группой, определенной для R1 или R2.
Если R1 и R2 представляют двухвалентную группировку, они могут быть, например, алкилиденом, алкенилиденом, алкиленом или алкениленовой группой (предпочтительно, содержащей вплоть до 10 атомов углерода), которая может содержать одну или более из функциональных групп, как определено ранее. Углеродные цепи R3 групп могут быть, например, прерваны и/или заканчиваться гетероатомами такими, как О, N или S.
Алифатические группы, представленные, например, R1, R2 или R3, могут быть разветвленной или неразветвленной, насыщенной или ненасыщенной группой, включая, например, алкильные и алкенильные группы, например, метил, этил, пропил, изопропил, бутил, децил или аллил. Аралифатические группы включают /монокарбоциклический арил/- алкильные группы, например, бензильные группы. Арильные группы включают моно- или би-циклические арильные группы, например фенильные, толильные или нафтильные группы. Гетероциклические группы включают 5- или 6-членные гетероциклические группы, предпочтительно, содержащие один гетероатом, например, фурильные, тиенильные или пиридильные группы. Заместители - атомы галоидов - могут, например, быть хлором, бромом или иодом.
Природа или размер R1, R2 и R3 будут влиять как на уровень содержания в полимере фрагментов формулы (II), которые придают липофильность и тем самым нерастворимость в воде, так и на скорость, с которой боковая цепь биоразлагаемо отщепляется.
Крупные и/или объемные группы будут иметь тенденцию снижать скорость биоразложения за счет стерических затруднений, повышая тем самым липофильность полимера.
В одной подходящей категории боковые цепи R1 и R2 каждый выбирают из атомов водорода C1-4 алкильных групп, таких как метил, и R3, представляющий низшую алкильную группу, например, предпочтительно, содержащую 1-20 атомов углерода; такие боковые цепи объединяют в основном степени липофильности и биоразлагаемости.
Следует учитывать, что как основная цепь, так и боковые цепи полимеров по предложенному способу должны выбираться таким образом, чтобы их продукты разложения были биоприменимы, в частности, чтобы они не были токсичными. В том случае, когда полимеры предназначаются для использования в медицине, продукты разложения должны быть физиологически приемлемы; так R1, R2, R3, A и любая группа - связка L должны быть такими, чтобы соединение R1- CO-R2, полимеры, содержащие фрагменты формулы (III) или (IV) и продукты формулы R3-COOH или R3-ОН, должны быть физиологически приемлемы и легко диспергируемы и устранимы, были предпочтительно растворимы в воде. Двуокись углерода, которая высвобождается при отщеплении присутствующих карбонатных группировок, обычно физиологически приемлема; их образование может быть функционально желательным в некоторых применениях полимеров по способу настоящего изобретения.
Полимеры по изобретению могут быть получены любым обычным способом, например, либо при взаимодействии /A/ предварительно полученного водно-растворимого полимера с реагентом, который служит для введения целевой липофильной метиленовой диэфирной боковой цепи, /В/ либо за счет полимеризации функционального мономера, который несет целевую липофильную метиленовую диэфирную боковую цепь.
Способ /A/ можно осуществить, например, при взаимодействии полимера с подвешенными спиртовыми гидроксильными группами /например, поливиниловый спирт, полигидроксиалкилакрилат или полисахариды/ с соединением формулы
X-CO-O-C/R1R2/-O-CO-/O/n-R3, (V)
где R1, R2, R3 и n имеют указанные ранее значения, а X является отщепляемой группой, например атомом галоида, например фтором, хлором, бромом или иодом. Реагенты формулы (V) могут быть, например, получены, как описано Folkman and Iund, Sunthesis, 1990, 1159.
Такие реакции, которые приведут к получению полимеров, содержащих фрагменты формулы (II), где m = 1, удобно вести в растворе, например в таком растворителе, как тетрагидрофуран, в присутствии слабонуклеофильных оснований, таких как пиридин.
Каталитическое количество третичного амина, такого как 4-диметиламинопиридин, можно также использовать. Количество полимерных гидроксильных групп, которые вступают в реакцию с образованием целевых липофильных метиленовых диэфирных групп, можно контролировать за счет соответствующего выбора таких факторов, как количества реагентов и времена реакций и температур, для достижения конечного баланса гидрофильности-липофильности липофилизованных полимеров.
Полученный продукт можно очистить такими стандартными способами, как экстракция растворителем и/или повторным растворением/переосаждением.
В другом варианте способ /A/ можно осуществить при взаимодействии полимера, содержащего подвешенные карбоксильные группы (например, полиакриловую кислоту или полиметакриловую кислоту), с соединением формулы:
X-CR1R2-O-CO-/O/n-R3, (VI)
где
R1, R2, R3, X и n имеют указанные ранее значения. Такие реакции, которые приведут к получению полимеров, содержащих фрагменты формулы (II), в которых m = 0, удобно осуществлять в растворе, например в таком растворителе, как N, N- диметилформамид, в присутствии сильного основания, например такого алкоксида щелочного металла, как трет.- бутоксид калия. Каталитические количества краун-эфира такие, как 18- краун-6, также можно использовать.
Гидрофильный липофильный баланс полимерного продукта можно контролировать соответствующим выбором реакционных параметров для определения числа карбоксильных групп, которые вступают в реакцию, и этот продукт можно очистить обычными способами.
Реагенты формулы (VI) можно получить, например, в реакции альдегида или кетона формулы R1-CO-R2 с галоидангидридом или сложным эфиром галоидформата формулы R3-/O/-CO-X, например, в присутствии такого катализатора, как хлорид цинка или пиридин.
Способ /A/ можно также осуществить, например, в реакции полимера, содержащего функциональные группы, такие как эпоксигруппы, с реагентом, содержащим целевые липофильные метиленовые диэфирные группировки и содержащим концевые реакционноспособные группы с такими функциональными группами; концевыми группами, реагирующими с эпоксигруппами, включая амино, гидроксильные и карбокси-группы.
Аналогично последние группы могут присутствовать в исходном полимере, и реагент может содержать концевые эпоксигруппы.
Обычно предпочтительно, чтобы полимерный исходный материал, используемый в способе /A/, имел молекулярную массу не более чем около 2000000.
Способ /B/ можно осуществить, используя любые мономеры, которые можно полимеризовать или сополимеризовать до получения несшитых полимеров, которые могут иметь один или более из заместителей, которые не участвуют в полимеризации и которые могут быть превращены в производное до процесса полимеризации для введения целевых липофильных метиленовых диэфирных группировок.
Можно использовать свободнорадикальную, конденсационную и ионную полимеризацию. Свободнорадикальную полимеризацию можно, например, осуществить, используя мономеры, содержащие карбоксигруппы, такие как производные акриловой кислоты или метакриловой кислоты при взаимодействии с соединением формулы (VI), или используя мономеры, содержащие гидроксильные группы, такие, как производные 2- гидроксиэтилакрилата или N-/2-гидроксипропил/метакриламида, полученные за счет взаимодействия с соединением формулы (V).
В другом варианте мономеры, содержащие гидроксильные группы, можно подвергнуть взаимодействию с соединением формулы
X-CO-O-O-C/R1R2/-X, (VII)
где
R1, R2 и X имеют указанные ранее значения,
и полученный продукт подвергают взаимодействию с соответствующей солью карбоновой кислоты R3-COOH. Свободнорадикальную полимеризацию можно также осуществить, используя сложные эфиры винилкарбоната формулы:
CH2-CH-O-CO-O-O-C/R1R2/-O-CO-/O/n- R3, (VIII)
где
n, R1, R2 и R3 имеют указанные ранее значения.
Такие мономеры, например, имеющие n = 0, можно получить при взаимодействии винилхлорформата с альдегидом или кетоном R1R2C = 0 в присутствии каталитического количества, например, пиридина или кислоты Льюиса до получения необязательно замещенного хлорметилфинилкарбоната формулы
CH2 = CH-O-CO-O-C/R1R2/-Cl, (IX)
где
R1 и R2 имеют указанные ранее значения,
с последующим взаимодействием, например, с соответствующей солью карбоновой кислоты R3-COOH предпочтительно в присутствии каталитического количества подходящего краунэфира.
Следует учитывать, что соединения (VIII) формально можно называть "виниловыми спиртами", модифицированными соединением формулы (VII).
Полученные из них полимеры должны быть соответственно ферментативно биоразлагаемыми до поливинилового спирта.
Можно использовать обычные способы полимеризации в массе, в растворе, в эмульсии и в суспензии. Молекулярную массу полимерного продукта, которая предпочтительно не должна превышать около 2000000, можно регулировать, используя такие агенты переноса цепи, как меркаптаны, из которых растущая полимерная цепь может получить протон, ведущий к обрыву цепи и образованию сернистого радикала, который будет инициировать новую полимерную цепь; таким образом, молекулярная масса полимера будет зависеть от типа и концентрации агента переноса.
Соответственно виниловые мономеры, например, содержащие карбонильную группу, соседнюю с винильной группой, как в акриловых или метакриловых сложных эфирах, например, полученных, как указано ранее, могут также быть подвергнуты ионной полимеризации (как анионной, так и катионной); такие методики особенно подходят для получения полимеров со строго определенной молекулярной массой, особенно сравнительно низкомолекулярных материалов.
Конденсационную полимеризацию можно вести, используя широкий круг соответствующим образом функционализированных мономеров, примеры которых могут быть представлены формулами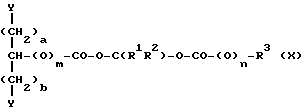
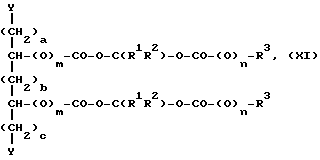
где
R1, R2, R3, m и n имеют указанные ранее значения, Y является реакционноспособной группой, например карбокси, гидроксильной или эпоксигруппой, такой как 2,3-эпоксипропилокси, а, b и с каждый могут быть нулем или небольшим целым числом, например, 1, 2 или 3.
В формуле (XI) группы R1, R2 и R3, а также m и n могут быть одинаковы или различны в двух боковых цепях. Такие мономеры можно использовать в обычных реакциях конденсации с соответствующими реагентами, такими как дикарбоновые кислоты, диспирты, диамины, ди/хлорангидриды/, диизоцианаты и бисэпокси-соединения до получения таких полимеров, как полиэфиры, полиамиды, полиуретаны и эпоксиполимеры.
Молекулярную массу полимерного продукта можно регулировать за счет выбора соответствующего времени реакции, температуры и т.д. и/или за счет использования монофункциональных агентов обрыва цепи.
В соответствующих случаях полимеры по изобретению можно получить, используя методику эмульсионной полимеризации; это может представлять особую ценность, если, например, нужно получить полимеры в форме монодисперсных частиц.
Способы эмульсионной полимеризации получения частиц, особенно монодисперсных частиц, описаны в EP-A- 0003905, EP-A-0091453, EP-A- 0010986 и EP-A-0106873.
Полимеры по предложенному способу находят применение, например, в таких хирургических имплантатах, как сшивающий материал, мягкие тканевые протезы, тампоны, пленки (например, искусственная кожа), материалы для покрытия ран (например, пластины гидрогелей), гибкие листовые материалы и изделия, такие как изготовленные из них контейнеры, изделия из композиций с замедленным высвобождением для лекарств или сельскохозяйственных химикалий; садоводческие агенты, такие как листы сохраняющей влагу "мульчи" и контейнеры для растений из биоразлагаемого материала.
Для использования при протезировании отформованные полимеры могут выгодно содержать гепарин, по крайней мере на их поверхности.
Как было указано ранее, линейный характер полимеров по изобретению улучшает их технологические свойства. За счет термопластичности их можно плавить и обрабатывать в расплаве в соответствии со стандартными способами, такими как литье под давлением, экструзия и раздув пленки. Растворы полимеров в соответствующих органических растворителях можно использовать, например, при нанесении оболочек на таблетки, отливке пленок и прядении волокон.
Если полимер по изобретению хотят использовать в качестве биоразлагаемого агента с замедленным высвобождением, активный материал можно заключить в оболочку из биоразлагаемого полимера, например в капсулы или микросферы, или его можно физически внедрить в процессе полимеризации так, чтобы он был равномерно распределен внутри полимера и мог высвободиться в процессе биоразложения.
В другом варианте активный материал может состоять весь или частично из любых групп R1, R2 или R3 и таким образом высвобождаться при ферментативном расщеплении. Типичные лекарства, которые включают в композиции с замедленным высвобождением, включают стероиды, контрацептивы, антибактериальные агенты, антагонисты наркотиков и противоопухолевые препараты.
Полимеры по изобретению, если они имеют достаточно короткую цепь, можно использовать в качестве пластификаторов для других полимеров.
Если полимеры являются биоразлагаемыми, разложение пластификатора таким образом либо нарушит целостность материала, либо раскроет его для атаки ферментами.
Биоразлагаемые полимерные частицы по предложенному способу можно также с выгодой использовать для диагностических целей.
Контрастный агент для рентгеновских исследований, который обычно является полииодоароматическим соединением, могут образовывать все или часть групп R3 или - C/R1R2/-, так что он высвобождается и безопасно удаляется из организма при биоразложении.
Такие частицы можно использовать для визуализации печени и селезенки, так как они включаются в ретикулоэндотелиальные системы этих органов. Рентгеновские контрастирующие агенты могут также просто физически удерживаться в полимерах за счет внедрения в них в процессе полимеризации.
Полимерные частицы по изобретению могут также содержать парамагнитные, суперпарамагнитные или ферромагнитные вещества, которые используют в диагностике при получении магнитно- резонансного изображения (MRI).
Субмикронные частицы железа или магнитной окиси железа можно физически включить в полимеры в процессе полимеризации до получения ферромагнитных или суперферромагнитных частиц. Парамагнитные MRI контрастные агенты принципиально содержат ионы парамагнитных металлов, таких как ионы гадолиния, удерживаемые хелатирующим агентом, который предотвращает их высвобождение (и таким образом практически исключает их токсичность).
Такие хелатирующие агенты с закомплексованными ионами металлов могут физически удерживаться в полимерах, за счет присутствия в процессе полимеризации, или группы R1, R2 и R3 могут содержать подходящие хелатирующие группы.
Вообще многие такие хелатирующие агенты являются полиаминополикарбоновыми кислотами, такими как диэтилентриаминпентауксусная кислота (R.B. Laufferchen Rev. 87, 1987, c. 901-927).
Полимерные частицы по изобретению могут также содержать контрастирующие агенты для ультразвуковых исследований, такие как тяжелые материалы, например барий-сульфат, или иодинированные соединения, такие как контрастирующие агенты для рентгеноскопии, указанные ранее, для создания контрастирующей среды для ультразвуковых исследований.
Полимеры по предложенному способу можно также использовать для получения микрочастиц пористого полимера, содержащего газ, и газ микропузырьков, заключенных в полимерное покрытие, оба из них могут быть пригодны в качестве контрастирующих агентов при ультразвуковых исследованиях.
Метакриловую кислоту перегоняют в вакууме для удаления стабилизатора. 2,2'-Азобисизобутиронитрил /AIBN/ термоинициатор очищают перекристаллизацией из метанола.
Все реакции ведут в атмосфере азота.
Эксклюзионная по размерам хроматография /SEC/:
Насос: Knauer HRLE насос 64.
Детектор: дифференциальный рефрактометр Кнауэра.
Колонки: колонки с гелем Полимер Лабораториз PL, соединенные последовательно. Размер пор 104, 500 и 100 ангстрем, размер частиц 5 мкм, длина 30, 30 и 60 см соответственно.
Растворитель: ТГФ.
Калибровка: Полистирол-стандарт /Полимер Лабораториз/.
Маркер скорости потока: толуол.
Программное обеспечение: вариант программ Полимер Лабораториз GPC/SEC 5.10.
Mw: средневесовой молекулярный вес /Mb/.
Mn: среднечисловой молекулярный вес /Mr/.
Mw/Mn: полидисперсность /Mb/Mr/.
Mp: молекулярный вес при максимальной реакции детектора.
Список сокращений:
Tg: температура стеклования.
TBA-OH: тетрабутиламмонийгидроксид.
TBA: тетрабутиламмоний.
AIBN: 2,2'-азобисизобутиронитрил.
SO2Cl2: сульфурилхлорид.
EтSCl: этансульфенилхлорид.
DBU: 1,8-диазабицикло[5.4.0]ундец-7-ен/1,5-5/
MgSO4: сульфат магния.
THF: тетрагидрофуран.
DMF: N,N-диметилформамид.
Пример 1. Бутилметакрилоилоксиметилкарбонат.
K раствору хлорметилхлорформата /2,84 г, 22,0 ммоль/ и пиридина /1,78 мл, 22,0 ммоль/ в метиленхлориде /24 мл/ н-бутанол /1,84 г, 20,0 ммоль/ добавляют при 0oC. Спустя 30 мин при 0oC и 21 ч при 25oС реакционную смесь промывают водной соляной кислотой /1М, 10 мл/, водным насыщенным бикарбонатом натрия /10 мл/ и водой /10 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния, в результате чего получают 2,66 г /80%/ интермедиата - н-бутилхлорметилкарбоната в виде неочищенного продукта.
1H ЯМР /60 МГц, CDCl3/ δ : 0,86 /CH3- CH2, м/, 1,40 /CH2-CH2, м/, 4,15 /CH2-O, т/, 5,63 /CH2Cl, c/.
Полученный интермедиат - н-бутилхлорметилкарбонат /2,5 г, 15 ммоль/ растворяют в диметилформамиде /80 мл/ и добавляют метакрилат калия /1,77 г, 15,0 ммоль/ вместе с каталитическим количеством 18- краун-6 /0,2 г, 7,5 ммоль/. Спустя 3 дня при 25o С растворитель удаляют при пониженном давлении, добавляют 30 мл хлороформа и 20 мл воды, и полученный продукт экстрагируют хлороформом. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния. В результате обработки на хроматографе с мгновенным испарением получают 1,96 г /61%/ бутилметакрилоилоксиметилкарбоната.
1H ЯМР /100 МГц, CHCl3/ δ : 0,99 /CH3-CH2, т/, 1,47 /CH2-CH2, м/, 1,72 /CH2-CH2, м/, 2,01 /CH3, c/, 4,25 /CH2-O, т/, 5,74 /H-C=, м/, 5,89 /OCH2O/, 6,27 /H-C=, м/.
13C ЯМР /75 МГц, CDCl3/ δ : 13,47 /CH3/, 17,97 18,71, 30,36 /CH3 и CH2 х 2/, 68,46 /CH2O/, 82,07 /O-CH2-OO/, 127,46 /CH2=/, 135,05 /C=/, 153,98 /C= O/, 165,50 /C=O/.
Пример 2.
a/ Полимер, полученный из бутилметакрилоилоксиметилкарбоната.
Мономер бутилметакрилоилоксиметилкарбоната /350 мг/ растворяют в ТГФ /2 мл/. Добавляют 1 мг AIBN в качестве инициатора свободнорадикальной полимеризации. Полученный раствор полимеризуют при 50o С в течение 5 ч. Продукт выделяют, осаждая в воду. Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 165000, Мч = 70000, Мв/Мч = 2,3.
b/ Полимер из метакрилоилоксиметилкарбоната
Раствор бутилметакрилоилоксиметилкарбоната /1,0 г/ в ДМФ нагревают до 60oC и добавляют AIBN (2,2'-азобисизобутиронитрил)/0,005 г, 0,03 моль/. Спустя 24 ч реакционную смесь охлаждают и прикапывают раствор полимера к перемешиваемому избытку метанола. Полимер отфильтровывают и промывают метанолом и водой, сушат при пониженном давлении. ИК /KBr/: 1763 /C=O/ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 0,90 /т, 3H, CH3/, 1,00 /м, 2H, CH2/, 1,39 /м, 2H, CH2/, 1,70 /м, 2H, CH2/, 1,90 /м, 3H, CH3/, 4,20 /т, 2H, CH2O/, 5,68 с, 2H, OCH2O/.
13C ЯМР /75 МГц, CDCl3/: δ 13,54 /CH3CH2/, 18,73 /CH2/, 30,39 /CH2/, 46,26 /C-CH3/, 69,72 /CH2O/, 83,67 /-OCH2O-/,153,86 /C-O/, 175,80 /C=O/.
По данным дифференциального сканирующего калориметра /DSC/ температура начала разложения 239,9oC / Tg не наблюдается/. По данным термомеханического анализа температура стеклования 24,7oC. Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 60000, Мч = 29000, Мв/Мч = 2,1.
Пример 3. Сополимер бутилметакрилоилоксиметилкарбоната и акриламида.
Мономеры бутилметакрилоилоксиметилкарбоната /250 мг/ и акриламид /250 мг/ растворяют в ТГФ /5 мл/. AIBN /1 мг/ добавляют в виде инициатора свободных радикалов. Полученный раствор полимеризуют при 60oC в течение 2 ч. Полученный продукт выделяют осаждением в холодную воду.
Пример 4. Общая процедура для хлорметилкарбонатов.
К раствору хлорметилкарбоната и указанного спирта в метиленхлориде /200 мл/ добавляют при 0oC пиридин. Спустя 20 мин при 0oC и 21 ч при 25oC реакционную смесь промывают водной соляной кислотой /1М, 10 мл/, водным насыщенным бикарбонатом натрия /10 мл/ и водой /10 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом натрия, получая в результате неочищенный хлорметилкарбонат.
Примеры 4a - 4d см. в табл. 1.
a/ Метилхлорметилкарбонат.
Соединение получают из хлорметилхлорформата и метанола.
1H ЯМР /60 МГц, CDCl3/: δ 3,98 /с, OCH3/, 5,85 /с, 2H,CH2Cl/.
b/ Этилхлорметилкарбонат.
Соединение получают из хлорметилхлорформата и этанола.
1H ЯМР /60 МГц, CDCl3/: δ 1,25 /т, 3H, CH3/, 4,25 /кв, 2H, CH2/, 5,70 /с, 2H, OCH2Cl/.
c/ Децилхлорметилкарбонат.
Соединение получают из хлорметилхлорформата и децилового спирта.
1H ЯМР /60 МГц, CDCl3/: δ 0,90-1,50 /м, 19H, CH3 и CH2/, 4,20 /м, 2H, CH2O/, 5,75 /с, OCH2Cl/.
d/ Бензилхлорметилкарбонат.
Соединение получают из хлорметилхлорформата и бензилового спирта.
1H ЯМР /60 МГц, CDCl3/: δ 5,20 /с, 2H, PhCH2O/, 5,70 /c, 2H, ClCH2O/, 7,32 /c, 5H, Ph/.
Пример 5. Общая процедура для метакрилоилметилкарбонатов.
Трет. -бутоксид калия добавляют к раствору метакриловой кислоты в ДМФ /200 мл/. Хлорметилкарбонат из примера 4 добавляют к полученной суспензии. Затем добавляют 18-краун-6, и реакционную смесь оставляют при перемешивании при комнатной температуре в течение 24 ч. Реакционную смесь фильтруют, а растворитель удаляют при пониженном давлении. Остаток растворяют в хлороформе /30 мл/ и промывают насыщенным водным бикарбонатом натрия /10 мл/ и водой /20 мл/. Органическую фазу сушат над сульфатом магния, и растворитель удаляют при пониженном давлении.
Примеры 5a - 5d см. в табл. 2.
a/ Метилметакрилоилоксиметилкарбонат.
Соединение получают из метилхлорметилкарбоната и метакрилата калия.
ИК /KBr/: 1772 /C=O, вал./, 1737 /C=O, вал./, 1635 /C = C, вал./см-1.
1H ЯМР /300 МГц, CDCl3/: δ 1,91 /с, 3H, CH3C=/, 3,79 /c, 3H, CH3O/, 5,64 /м, 1H, CH2=/, 5,80 c, 2H, -OCH2O-/, 6,16 /м, 1H, CH2- /.
13C ЯМР /75 МГц, CDCl3/: δ 17,95 /CH3C= /, 55,13 /CH3O/, 82,18 /- OCH2O-/, 127,52 /CH2=/, 135,02 /C=/, 154,44 /C=0/, 165,46 /C=O/.
b/Этилметакрилоилоксиметилкарбонат.
Соединение получают из этилхлорметилкарбоната и метакрилата калия.
ИК /KBr/: 1772 /C=O, вал./, 1736 /C=O, вал./, 1635 /C=C, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 1,27 /т, 3H, CH3/, 1,92 /с, 3H, CH3C-/, 4,23 /кв, 2H, CH2/, 5,66 /м, 1H, CH2-/, 5,80 /с, 2H, - OCH2O-/, 6,20 /м, 1H, CH2= /.
13С ЯМР /300 МГц, CDCl3/: δ 15,70 /CH3CH2/, 19,60 /CH3C/, 65,72 /CH2O/, 83,05 /-OCH2O-/, 127,76 /CH2=/, 135,40 /C=/, 153,82 /C=O/, 165,42 /C=O/.
c/ Децилметакрилоилоксиметилкарбонат.
Соединение получают из децилхлорметилкарбоната и метакрилата калия.
ИК /KBr/: 1772 /C-O, вал./, 1763 /C=O, вал./, 1635 /C-C, вал./см-1.
1ЯМР /300 МГц, CDCl3/: δ 0,90 /т, 3H, CH3/, 1,28 /м, 14H, CH2/, 1,72 /м, 2H, CH2/, 1,99 /с, 3H, CH3C-/, 4,21/т, 2H, CH2O/, 5,70 /м, 1H, CH2=/ 5,86/с, 3H, -OCH2O-/, 6,24 /м, 1H, CH2=/.
13C ЯМР /75 МГц, CDCl3/: δ 13,78 CH3/, 17,76 /CH3C=/, 22,76-31,55 /CH2/, 68,60 /CH2O/, 81,90 /-OCH2O-/, 127,28 /CH2=/, 134,86 /C=/, 153/73 /C=O/, 165,33 /C=O/.
d/ Бензилметакрилоилоксиметилкарбонат.
Соединение получают из бензилхлорметилкарбоната и метакрилата калия.
ИК /KBr/: 3077 /Ph/, 1772 /C=O, вал./, 1763 C=O, вал./, 1635 /C=C, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 1,96 /с, 3H, CH3C- /, 5,22 /c, 2H, CH2O/, 5,70 /м, 1H, CH2=/, 5,87 /c, 3H, -OCH2O-/, 6.22 /м, 1H, CH2=/, 7,39 /c, 5H, Ph/.
13C ЯМР /75 МГц, CDCl3/: δ 17,96 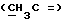 , 69,91 /CH2O/, 82,03 /-OCH2O-/, 127,41 /CH2=/, 128,32 /Ph/, 134,78 /C=/, 153,58 /C=O/, 165,28 /C= O/.
, 69,91 /CH2O/, 82,03 /-OCH2O-/, 127,41 /CH2=/, 128,32 /Ph/, 134,78 /C=/, 153,58 /C=O/, 165,28 /C= O/.
Пример 6. Общая процедура для полимеризации метакрилоилоксиметил карбонатов.
Раствор метакрилоилоксиметилкарбоната /1,0 г/ из примера 5 в ДМФ /8,0 г/ нагревают до 60oC и добавляют AIBN /0,005 г, 0,03 ммоль/.
Спустя 24 ч реакционную смесь охлаждают и раствор полимера прикапывают к перемешиваемому избытку метанола /не растворитель/. Полученный полимер фильтруют и промывают метанолом и водой и сушат при пониженном давлении.
a/ Полимер из метилметакрилоилоксиметилкарбоната
ИК /KBr/: 1763 /C - О, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 1,00 /м, 2H, CH2/, 1,90 /м, 3H/, 3,85 /с, 3H, /CH3O/, 5,70 /с, 2Н, OCH2O/.
13C ЯМР /75 МГц, CDCl3/: δ 46,35 /C-CH3/, 56,55 /CH3O/, 83,59 /- OCH2O-/, 154,41 /C=O/, 175,50 /C-O/.
По данным дифференциальной сканирующей калориметрии /DSC/ Tg = 59,8oC, а температура начала разложения составляет 242,2oC. По данным термомеханического анализа температура стеклования 59,9oC.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 100000, Мч = 59000, Мв/Мч = 1,7.
b/ Полимер из этилметакрилоилоксиметилкарбоната.
ИК /KBr/: 1763/C=O, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/ : δ 1,00 /м, 2H, CH2/, 1,32 /т, 3H, CH3/, 1,90/м, 3H, CH3/, 4,25 /м, 2H, CH2O/, 5,70 /с, 2H, OCH2O/.
13C ЯМР /75 МГц, CDCl3/: δ 15,77 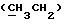 , 46,35 /C-CH3/, 65,90 /CH2O/, 83,50 /-OCH3O-/, 153,69 /C=O/, 175,80 /C=O/.
, 46,35 /C-CH3/, 65,90 /CH2O/, 83,50 /-OCH3O-/, 153,69 /C=O/, 175,80 /C=O/.
По данным дифференциальной сканирующей калориметрии, /DSC/ Tg = 35,9oC, а температура начала разложения составляет 260,9oC. По данным термомеханического анализа температура стеклования составляет 31,2oC.
Размеры по данным эксклюзионной хроматографии: Мв = 34000, Мч = 20000, Мв/Мч = 1,7.
c/ Полимер из децилметакрилоилметилкарбоната
ИК /KBr/: 1763 /C = О, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 0,90 /т, 3H, CH3/, 0,90 /м, 3H, CH2/, 1,30 /м, 14H, CH2/, 1,70 /м, 2H, CH2/, 1,90 /м, 2H/, 4,19 /т, 2H, CH2O/, 5,66 /с, 2H, OCH2O/.
13C ЯМР /75 МГц, CDCl3/: δ 13,78 /CH3/, 22,34 - 31,47 /CH2/, 46,26 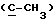 , 68,70 CH2O/, 83,67 /-OCH2O-/, 153,55 /C=O/, 175,80 /C=0/.
, 68,70 CH2O/, 83,67 /-OCH2O-/, 153,55 /C=O/, 175,80 /C=0/.
По данным дифференциальной сканирующей калориметрии /DSC/, температура начала разложения составляет 232,9oC /То не наблюдается/. По данным термомеханического анализа, температура стеклования составляет -3,3oC.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 160000, Мч = 90000, Мв/Мч = 1,7.
d/ Полимер из бензилметакрилоилоксиметилкарбоната
ИК /KBr/: 3077 /Ph/, 1763 /C=O, вал./ см-1.
1H ЯМР /300 МГц, CDCl3/: δ 0,95 /м, 3H, CH3/, 1,90 /м, 2H/, 5,25 /с, 2H, CH2O/, 5,75 /с, 2H, OCH2O/, 6,70 /с, 2H, Ph/.
13C ЯМР /75 МГц, CDCl3/: δ 47,26 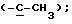 68,03 /-OCH2Ph/, 82,02 /-OCH2O-/, 129,45 /Ph/, 153,67 /C=O/, 175,80 /C=O/.
68,03 /-OCH2Ph/, 82,02 /-OCH2O-/, 129,45 /Ph/, 153,67 /C=O/, 175,80 /C=O/.
По данным дифференциальной сканирующей калориметрии /DSC/ Tg = 31,6oC, а температура начала разложения 197,1oC. По данным термомеханического анализа температура стеклования 32,8oC.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 92000, Мч = 44000, Мв/Мч = 2,1.
Пример 7. Свободнорадикальная полимеризация в растворе бензилметакрилоилоксиметилкарбоната с получением низкомолекулярного полимера.
Раствор бензилметакрилоилоксиметилкарбоната /0,5 г, 2,0 ммоль/ примера 5 в ДМФ /7,5 г/ нагревают до 60oC и добавляют аллилмеркаптан /0,0015 г, 0,02 ммоль/ вместе с AIBN /0,0025 г, 0,015 ммоль/.
Спустя 24 ч реакционную смесь охлаждают, и раствор полимера прикапывают к перемешиваемому избытку метанола /не растворитель/. Полимер отфильтровывают и промывают водой, а затем сушат при пониженном давлении.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 22000, Мч = 14000, Мв/Мч = 1,6.
Пример 8. Свободнорадикальная полимеризация этилметакрилоилоксиметилкарбонат примера 5b и метакриловой кислоты в ДМФ.
8,0 г нагревают до 60oC и добавляют AIBN /0,005 г, 0,03 ммоль/. Спустя 24 ч полимерный раствор прикапывают к перемешиваемому избытку хлороформа /не растворитель/, фильтруют и промывают дополнительным количеством хлороформа и сушат при пониженном давлении. Примеры 8a - 8d приведены в табл. 3.
1H ЯМР /200 МГц, CDCl3/: δ 1,10 /с, 6H, 2 х CH3/, 1,27 /т, 3H,  , 1,90 /с, 4H, 2 х CH2/, 3,52 /мс, 1H, OH/, 4,2 /м, 2H,
, 1,90 /с, 4H, 2 х CH2/, 3,52 /мс, 1H, OH/, 4,2 /м, 2H, 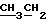 , 5,72 /с, -OCH2O-/. В табл. 4 показана растворимость каждого из сополимеров в горячей и холодной воде.
, 5,72 /с, -OCH2O-/. В табл. 4 показана растворимость каждого из сополимеров в горячей и холодной воде.
Пример 9. Этил-1-хлорэтилкарбонат.
K раствору 1-хлорэтилхлорформата /23,16 г, 0,162 моль/ и этанола /7,45 г, 0,162 моль/ в метиленхлориде /200 мл/ добавляют пиридин /12,82 г, 0,162 моля/ при 0oC.
Спустя 10 мин при 0oC и 21 ч. при 25oC, реакционную смесь промывают водной соляной кислотой /100 мл/, водным насыщенным бикарбонатом натрия /100 мл/ и водой /100 мл/. Растворитель удаляют при пониженном давлении, после сушки над сульфатом магния, получая 18,5 г /74%/ промежуточного соединения этилхлорэтилкарбоната в качестве неочищенного продукта.
1H ЯМР /60 МГц, CDCl3/: δ 1,30 /т, 3H, CH3/, 1,85 /д, 3H, CH3CH/, 4,25 /кв., 2H, CH2/, 0,45 /кв., 1H, CH/.
Пример 10. Этил-1-метакрилоилоксиэтилкарбонат.
Трет. -бутоксид калия /3,70 г, 0,033 моль/ добавляют к раствору метакриловой кислоты /2,84 г, 0,033 моль/ в ДМФ /100 мл/. Этил-1-хлорэтилкарбонат /5,08 г, 0,033 мл/ примера 9 добавляют к полученной суспензии.
Затем добавляют 18-краун-6 /0,61 г, 2,3 ммоль/, и полученную реакционную смесь оставляют при перемешивании при комнатной температуре на 3 дня. Реакционную смесь отфильтровывают, а растворитель удаляют при пониженном давлении. Остаток растворяют в 100 мл хлороформа и промывают насыщенным водным бикарбонатом натрия /50 мл/ и водой /50 мл/. Органическую фазу сушат над сульфатом магния, а растворитель удаляют при пониженном давлении.
При хроматографической обработке с мгновенным испарением получают 2,5 г /38%/ указанного в заглавии продукта (при регенерации исходного материала выход составляет 75%).
1H ЯМР /60 МГц, CDCl3/: δ 1,30 /т, 3H, CH3/, 1,60 /д, 3H, CH3CH/, 2,00 /с, 3H, CH3C=/, 4,20 /кв., 2H, CH2/, 5,70 /м, 1H, CH2=/, 6.25 /кв., 1H, -OCH/CH3/O-/, 6,90 /м, 1H, CH2=/.
Пример 11. Свободнорадикальная полимеризация этил- 1- метакрилоилоксиэтилкарбоната.
AIBN /0,033 г, 0,02 ммоль/ добавляют к раствору этил- 1- метакрилоилоксиэтилкарбоната /0,504 г, 2,49 ммоль/ из примера 10 в сухом ТГФ /8 мл/ при 50oC в атмосфере сухого азота.
Спустя 7 ч реакционную смесь охлаждают до З0oC, и полимер осаждают в метанол /50 мл/, и полученный раствор фильтруют. Полученный полимер растворяют в ТГФ, повторно осаждают в метанол /70 мл/ и фильтруют, получая 0,138 г белого порошка.
1H ЯМР /300 МГц, CDCl3/: δ 0,90 /м, 3H, CH3/, 1,25 /с, 3H, CH3/, 1,45 /с, 3H, CH3/, 1,87 /м, 2H, CH2/, 4,15/шир.с, 2H, CH2O/, 6,62 /шир.с, 1H, -CHCH3/.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 26500, Мч = 18600, Мр = 22000, Мв/Мч = 1,43.
Пример 12. Полимер, полученный эмульсионной полимеризацией этилметакрилоилоксиметилкарбоната.
Раствор натрийдодецилсульфата /0,056 г, 0,1% ммоль/ в воде /20, 5 мл/ нагревают до 60oC в атмосфере азота перед добавлением этилметакрилоилоксиметилкарбоната /5,266 г, 28,00 ммоль/ примера 6b. Полимеризацию инициируют смесью метабисульфита калия /53,4 мг, 0,25 ммоль/ и персульфата калия /4,38 мг, 0,02 ммоль/ -окислительно-восстановительной системой.
Спустя 16 ч при 60oC добавляют персульфат калия /4,38 мг, 0,02 ммоль/ и полимеризации дают возможность протекать еще 3 ч при 60oC в атмосфере азота перед охлаждением до 20oC.
Пример 13. O-ацетоксиметил-S-этилкарбонотиоат.
O- хлорметил- S-этилкарбонотиоат /4,50 г, 0,028 моль/ в ДМФ /20 мл/ добавляют к раствору ацетата калия /2,74 г, 0,028 моль/ в ТГФ /100 мл/.
Затем добавляют 18- краун-6/0,22 г, 0,84 ммоль/, и реакционную смесь оставляют при перемешивании при комнатной температуре в течение 3 дней. Затем реакционную смесь фильтруют, и растворитель удаляют при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением /силикагель, хлороформ/ до получения 4,23 г /85%/ указанного в заглавии продукта.
1H ЯМР /60 МГц, CDCl3/: δ 1,30 /т, 3H, CH3CH2/, 2,20 /с, 3H, CH3C = O/, 2,95 /кв, 2H, CH2CH3/, 5,80 /с, 2H, OCH2O/.
Пример 14. Ацетоксиметилхлорформат.
SO2Cl2 /2,43 г, 0,018 моль/ добавляют к О- ацетоксиметил-S-этилкарбонотиоату /3,15 г, 0,018 мл/ примера 13 при температуре 0-5oC при перемешивании в течение 15 мин с последующим перемешиванием при комнатной температуре в течение 45 мин.
После испарения EтSCl при комнатной температуре и 11 мм рт. ст. получают бесцветную жидкость. Выход: 2,44 г /89%/.
1H ЯМР /60 МГц, CDCl3/: δ 2,20 с, 3H, CH3C=O/, 5,76 /с, 2H, OCH2O/.
Пример 15. Ацетоксиметил- 2-метакрилоилоксиэтилкарбонат.
К раствору ацетоксиметилхлорформата /1,00 г, 0,0066 моль/ и 2- гидроксиэтилметакрилата /0,85 г, 0,0066 моль/ добавляют при 0oC.
Спустя 10 мин при 0oC и 18 ч при 25oC реакционную смесь промывают водной соляной кислотой /100 мл/, водным насыщенным бикарбонатом натрия /100 мл/ и водой /100 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния.
После хроматографической обработки с мгновенным испарением /силикагель, гексан/этилацетат 3: 2/ получают 1,05 г /65% / указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 1,95 /д, 3H, CH3C=/, 2,10 /с, 3H, CH3C=O/, 4,45 /с, 4H, CH2O/, 5,55 /м, 1H, CH2=/, 5,75 /с, 2H,- OCH2O-/, 6,05 /м, 1H, CH2=/.
Пример 16. N-/2-хлорметоксикарбонилоксипропил /метакриламид.
К раствору N-/2-гидроксипропил/метакриламида2 /2,85 г, 20 ммоль/ и пиридина /1,90 г, 24 ммоль/ в метиленхлориде /100 мл/ добавляют при 0oC хлорметилхлорформат /3,87 г, З0 ммоль/ в 120 мл метиленхлорида.
Спустя 15 мин при 0oC и 24 ч при 25oC реакционную смесь промывают водой /5 • 25 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния.
В результате хроматографической обработки с мгновенным испарением /силикагель, хлороформ /получают 3,30 г /70%/ указанного в заглавии соединения.
1ЯМР /60 МГц, CDCl3/: δ 1,42 /д, 3H, CH3-CH-O/, 2,0 /м, 3H, CH3C=/, 3,2 - 4,0 /м 2H, H-CH2-CH/, 4,8 - 5,3 /м, 1H, CH3-CH-O/, 5,6 /д, 2H, CH2=/, 5,7 /с, 2H, CH2Cl/, 6,1 -6,7 /шир. с, 1H, H/.
Пример 17. a/ N-/2-ацетоксиметоксикарбонилоксипропил/метакриламид.
Раствор ацетата ТВА /1,21 г, 4 ммоль/ в ТГФ /30 мл/, полученный вымораживанием водного раствора эквимолярного количества ТВА-ОН и уксусной кислоты, добавляют к перемешиваемому раствору N-/2- хлорметоксикарбонилоксипропил/метакриламида /0,943 г, 4 ммоль/ примера 16 в 10 ТГФ при комнатной температуре.
После перемешивания в течение 5 дней растворитель удаляют при пониженном давлении, а остаток растворяют в хлороформе /50 мл/ и промывают водой /5•10 мл/. Органическую фазу сушат над сульфатом магния, а растворитель удаляют при пониженном давлении.
После хроматографической обработки с мгновенным испарением /силикагель, гексан/этилацетат 3:4 /получают 0,486 г /47%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 1,4 /д, 3H, CH3-CH-O/, 2,0 /м, 3H, CH3C =/, 2,2 /с, 3H, CH3C-O/, 3,2 - 4,0 /м, 2H, NH-CH2-CH/, 4,8 - 5,3 /м, 1H, CH3-CH-O/, 5,6 /д, 2H, CH2=/, 5,8 /с, 2H, OCH2O/, 6,1 - 6,7 /шир. с, 1H, NH/.
b / N- /2-ацетоксиметоксикарбонилоксипропил/метакриламид.
К раствору N-/2-гидроксипропил/метакриламида2 /0,430 г, 3,0 ммоль / и пиридина /0,285 г, 3,6 ммоль/ в метиленхлориде /30 мл/ при 0oC добавляют ацетоксиметилхлорформат примера 14 /0,500 г, 3,3 ммоль/ в метиленхлориде /6 мл/.
Спустя 10 минут при 0oC и 3 дня при 25oC реакционную смесь промывают 100 мл воды. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния. После обработки хроматографической с мгновенным испарением /силикагель, гексан/этилацетат 3: 4 /получают 0,40 г /51%/ указанного в заглавии соединения.
Данные ЯМР находятся в хорошем соответствии с данными, приведенными в /a/ ранее.
Пример 18. Свободнорадикальная полимеризация N-/2- ацетоксиметоксикарбонилоксипропил/метакриламид.
AIBN /0,0138 г, 0,084 ммоль/ добавляют к раствору N- /2- ацетоксиметоксикарбонилоксипропил/метакриламида /0,519 г, 2 ммоль/ примера 17 в сухом ТГФ /8 мл/ при 50oC в атмосфере сухого азота. Спустя 3 дня растворитель удаляют при пониженном давлении до получения 0,439 г белого порошка.
1ЯМР /200 МГц, CDCl3/: δ 0,8 - 1,2 /м, 3H, CH3/, 1,2 -1,4 /м, 3H, CH2-CH/CH3/O/, 1,6 - 2,0 /м, 2H, CH2/, 2,1 /с, 3H, CH3CO/, 2,9 -3,9 /м, 2H, NH-CH2/, 4,7 - 5,0 /м, 1H, CH2CH/CH3/-O/, 5,8 /c, 2H, O-CH2-O/, 6,2 - 7,0 /м, 1H, NH/.
Размер по данным эксклюзионной хроматографии /SEC/: Мв = 5411, Мч = 2857, Мв/Мч - 1,894.
По данным дифференциального сканирующего калориметра /DSC/ Tg = 52,91oC.
Пример 19. N-/2- /1-хлорэтоксикарбонилокси/пропил/метакриламид.
К раствору N-/2-гидроксипропил/метакриламида2/3,15 г, 22 ммоль/ и пиридина/2,088 г, 26,4 ммоль/ в 100 мл метиленхлорида 1-хлорэтилхлорформат /4,718 г, 33 моль/ в 20 мл метиленхлорида добавляют при 0oC.
Спустя 10 мин при 0oC и 5,5 ч при 25oC реакционную смесь промывают водой /5•40 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния до получения 4,84 г /88%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 1,37 /д, 3H, CH3-CH-O/, 1,83 /д, 3H, CH3-CH-Cl/, 1,97 /м, 3H, CH3C=/, 3,3 - 3,6 /м, 2H, NH-CH2-CH/, 4,7 - 5,3 /м, 1H, CH2-CH/CH3/-O/, 5,3 /м, 1H, CH2= /, 5,70 /м, 1H, CH2=/, 6,0-6,6 /м, 2H, NH/-CH-CH-CH3/.
Пример 20. N-/2-/1-ацетоксиэтоксикарбонилокси /пропил/ метакриламид.
Раствор ацетата ТВА /6,93 г, 23 ммоль/ в ТГФ /100 мл/, полученный вымораживанием водного раствора эквимолярных количеств ТВА- ОН и уксусной кислоты, добавляют к перемешиваемому раствору N-/2-/l- хлорэтоксикарбонилокси/пропил/метакриламида /4,736 г, 19 ммоль/ в ТГФ /100 мл/ при комнатной температуре.
После перемешивания в течение 4 дней растворитель удаляют при пониженном давлении, а остаток растворяют в хлороформе /100 мл/ и промывают водой /5 • 20 мл/. Органическую фазу сушат над сульфатом магния, и растворитель удаляют при пониженном давлении.
В результате хроматографической обработки с мгновенным испарением /силикагель, гексан/ этилацетат 3:4 /получают 1,29 г /25%/ указанного в заглавии продукта.
1H ЯМР /60 МГц, CDCl3/: δ 1,3 /д, 3H, CH2-CH/CH3/ -О/, 1,5 /д, 3H, O-CH/CH3/-O/, 2,0 /м, 3H, CH3C=/, 2,1 /C, 3H, CH3C-O/, 3,3 - 3,6 /м, 2H, NH-CH2- CH/, 4,7 - 5,3 /м, 1H, CH2-CH/CH3/-O/, 5,4 /м, 1H, CH2-/, 5,7 /м, 1H, CH2=/, 6,1-6,6 /шир.с, 1H, NH/, 6,6 - 6,9 /м, 1H, O-CH/CH3/O/.
Пример 21. Свободнорадикальная полимеризация N-/2-/1-ацетоксиэтоксикарбонилокси/пропил/метакриламида.
AIBN /0,0031 г, 0,189 ммоль/ добавляют к раствору N- /2-/1- ацетоксиэтоксикарбонилоксипропил/метакриламида /1,23 г, 4,5 ммоль/ примера 20 в сухом ТГФ /18 мл/ при 50oC в атмосфере сухого азота.
Спустя 3 дня растворитель удаляют при пониженном давлении. В результате хроматографической обработки с мгновенным испарением /с поэтапным градиентом гексан/этилацетат 3:4 до метанола/ получают 0,95 г белого порошка.
1H ЯМР /200 МГц, CDCl3/: δ 0,8 - 1,2 /м, 3H, CH3/, 1,2 - 1,4 /м, 3H, CH2-CH/CH3/-O/, 1,5 /д, 3H, O-CH/CH3/-O/, 1,6 - 2,0 /м, 2H, CH2/, 2,0 - 2,2 /c, 3H, CH3CO/, 2,9 -3,9 /м, 2H, NH- CH2/, 4,7 -5,0 /м, 1H, CH2CH/CH3/-O/, 6,2 - 7,0 /м, 2H, NH-O-CH/CH3/-O/.
Размеры по данным эксклюзионной хроматографии SEC: Мв = 1991, Мч = 1268, Мр = 2105, Мв/Мч = 1,548.
По данным дифференциальной сканирующей калориметрии /DSC/ Tg = 51,53oC.
Пример 22. Метакрилоилоксиметилбензоат.
Трет.-бутокси калия /10,0 г, 0,090 моль/ добавляют к раствору метакриловой кислоты /7,75 г, 0,090 моль/ в ДМФ /300 мл/. Хлорметилбензоат3/15,0 г, 0,088 моль/ добавляют к полученной суспензии; 18-краун-6/1,8 г, 6,9 ммоль/ добавляют затем, и реакционную смесь оставляют при перемешивании при комнатной температуре на 2 дня. Реакционную смесь отфильтровывают, и растворитель удаляют при пониженном давлении. Остаток растворяют в хлороформе /100 мл/ и промывают насыщенным водным раствором бикарбоната натрия /50 мл/ и водой /50 мл/. Органическую фазу сушат над сульфатом магния, и растворитель удаляют при пониженном давлении.
В результате хроматографической обработки с мгновенным испарением получают 15,9 г /82%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 2,00 /с, 3H, CH3C=/, 5,65 /м, 1H, CH2=/, 6,15 /с, 2H, -OCH2O/, 6,35 /м, 1H, CH=/, 7,50 /м, 3H, Ph/, 8,05 /м, 2H, Ph/.
Пример 23. Полимер из метакрилоилоксиметилбензоата.
AIBN /0,005 г, 0,03 ммоль/ добавляют к раствору метакрилоилоксиметилбензоата /1,00 г, 4,55 ммоль/ примера 22 в сухом ТГФ /8 г/ при 60oC в атмосфере сухого азота. Спустя 24 ч реакционную смесь охлаждают до 20oC, растворитель удаляют при пониженном давлении.
Полученный полимер растворяют в CH2Cl2 и осаждают в метанол. Метанол удаляют из полимера фильтрованием, получая белый порошок.
1H ЯМР /200 МГц, CDCl3/: δ 0,85 /м, 3H, CH3/, 1,87 /м, 1H, CH2/, 5,70 /м, 2H, -OCH2O-/, 7,45 /м, 3H, Ph/, 8,05 /м, 2H, Ph/.
По данным дифференциальной сканирующей калориметрии /DSC/ Tg = 60,98oC.
По данным эксклюзионной хроматографии размеры/SEC/: Мв = 30281, Мч = 11580, Мр = 32286, Мв/Мч = 2,615.
Пример 24. Метилхлорэтилкарбонат.
К раствору хлорэтилформата /35,74 г, 0,25 моль/ и метанола/8,00 г, 0,25 моль/ в метиленхлориде /300 мл/ добавляют пиридин /19,78 г, 0,25 моль/ при 0oC.
Спустя 10 мин при 0oC и 2 дня при 25oC реакционную смесь промывают водной соляной кислотой /100 мл/, водным насыщенным бикарбонатом натрия /100 мл/ и водой /100 мл/. Растворитель удаляют при пониженном давлении после сушки над сульфатом магния, получают 25,6 г /74%/ интермедиата-метилхлорэтилкарбоната в виде неочищенного продукта.
1H ЯМР /60 МГц, CDCl3/: δ 1,85 /д, 3H, CH3CH/, 3,80 /с, 3H, CH3O/, 6,50 /кв, 1H, CH/.
Пример 25. Метил-1-метакрилоилоксиэтилкарбонат.
Трет. - бутилат калия /3,70 г, 0,033 моль/ добавляют к раствору метакриловой кислоты /2,84 г, 0,033 моль/ в 100 мл ДМФ. Метилхлорэтилкарбонат /4,55 г, 0,033 моль/ примера 24 добавляют к полученной суспензии; 18-краун-6/ 0,61 г, 2,3 ммоль/ добавляют затем к реакционной смеси, и все это оставляют при перемешивании при комнатной температуре на 3 дня. Реакционную смесь фильтруют, и растворитель удаляют при пониженном давлении. Остаток растворяют в 100 мл хлороформа и промывают насыщенным водным бикарбонатом натрия /50 мл/ и водой /50 мл/. Органическую фазу сушат над сульфатом магния, а растворитель удаляют при пониженном давлении.
В результате хроматографической обработки с мгновенным испарением получают 4,46 г /72%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 1,65 /д, 3H, CH3CH/, 2,00 /с, 3H, CH3C -/, 3,90 /с, 3H, CH3O/, 5,65 /м, 3H, CH2=/, 6,25 /м, 1H, CH2 =/, 6,90 /кв, 1H, CHCH3/.
Пример 26. Свободнорадикальная полимеризация метил-1-метакрилоилоксиэтилкарбоната.
AIBN /0,005 г, 0,03 ммоль/ добавляют к раствору метил- 1- метакрилоилоксиэтилкарбоната /1,0 г, 5,0 ммоль/ в сухом ТГФ /8 г/ при 60oC в атмосфере сухого азота. Спустя 24 ч реакционную смесь охлаждают до 20oC, а растворитель удаляют при пониженном давлении. Полученный полимер растворяют в CH2Cl2 и повторно осаждают в метанол. Метанол удаляют из полимера фильтрованием, получая белый порошок.
1H ЯМР /200 МГц, CDCl3/: δ 0,90 /м, 3H, CH3/, 1,45 /с, 3H, CH3CH/, 1,87 /м, 2H, CH2/, 3,80 /с, 3H, CH3O/, 6,65 /шир.с, 1H, CHCH3/.
Размеры по данным эксклюзионной хроматографии /SEC/: Мв = 16033, Мч = 6641, Мр = 16192, Мв/Мч = 2,41.
По данным дифференциальной сканирующей калориметрии /DSC/ Tg = 57,65oC.
Пример 27. Свободнорадикальная эмульсионная гомополимеризация бензилметакрилоилоксиметилкарбоната.
Раствор натрийдодецилсульфата /1,6 • 10-2 моль/ в дезоксигенированной воде /6,0 мл/ добавляют к 50 мл в двугорлой круглодонной колбе с магнитной мешалкой и холодильником.
К этому раствору добавляют метабисульфит калия /0,015 г, 6,7 • 10-2 ммоль/, растворенный в дезоксигенированной воде /1,0 мл/ и бензилметакрилоилоксиметилкарбонат /2,0 г, 8,0 ммоль/. Реакционную смесь нагревают до температуры 60oC.
К нагретой реакционной смеси добавляют персульфат калия /1,25 • 103 г, 4,6•103 ммоль/, и реакции дают возможность протекать. Спустя приблизительно 5 ч полимеризацию останавливают, и полимерную эмульсию прикапывают к значительному избытку метанола /не растворитель/.
Затем полимер отфильтровывают и промывают метанолом и водой. Эту процедуру повторяют трижды с целью очистки полимера. Затем полимер собирают и сушат в вакууме для удаления любых примесей растворителя.
Некоторое количество стабильной эмульсии не экстрагируют вышеуказанным способом, но сохраняют для определения размера частиц оптическим микроскопом. Размер частиц эмульсии по оценкам оптического микроскопа составляет менее 1 мкм диаметром.
Пример 28. Метакрилоилоксиметилацетат.
Трет.-бутоксид калия /5,0 г, 0,045 моль/ добавляют к раствору метакриловой кислоты /3,87 г, 0,045 моль/ в 150 мл ДМФ. К получению суспензии добавляют хлорметилацетат3/4,86 г, 0,045 моль/; 18-краун-6 /0,9 г, 3,46 ммоль/ добавляют при перемешивании к реакционной смеси, и оставляют при перемешивании при комнатной температуре в течение 4 дней.
Затем реакционную смесь фильтруют, и растворитель удаляют при пониженном давлении. Остаток растворяют в хлороформе /100 мл/ и промывают насыщенным водным карбонатом натрия /50 мл/ и водой /50 мл/. Органическую фазу сушат над сульфатом магния, и растворитель удаляют при пониженном давлении.
После хроматографической обработки с мгновенным испарением получают 5,19 г /75%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 2,00 /с, 3H, CH3C-/, 2,18 /с, 3H, CH3C = O/, 5,70 /м, 1H, CH2=/, 5,85 /c, 2H, -OCH2O-/, 6,25 /м, 1H, CH2=/.
Пример 29. Бутилакрилоилоксиметилкарбонат.
Трет. -бутилат калия /5,84 г, 0,052 моль/ добавляют к раствору акриловой кислоты /4,47 г, 0,045 моль/ в 220 мл ДМФ. Бутилхлорметилкарбонат /6,5 г, 0,052 моль/ в 150 мл ДМФ добавляют к полученной суспензии; 18-краун-6 /0,6 г/ добавляют затем, и реакционную смесь оставляют при перемешивании при комнатной температуре на 2 дня.
Реакционную смесь фильтруют, и растворитель удаляют при пониженном давлении. Остаток растворяют в хлороформе /100 мл/ и промывают насыщенным водным бикарбонатом натрия /50 мл/ и водой /50 мл/. Органическую фазу сушат над сульфатом натрия, и растворитель удаляют при пониженном давлении.
После хроматографической обработки с мгновенным испарением получают 4,57 г указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 0,80 /т, 3H, CH3CH2/, 1,28 /м, 2H, CH2/, 1,60 /м, 2H, CH2/, 4,15 /т, CH2O/, 5,78 /с, 2H, OCH2O/, 5,88 /дд, CH2=/, 6,1 /дд, 1H, CH2-/, 6,45 /дд, 1H, CH2= CH-/.
Пример 30. Полимер из метакрилоилоксиметилацетата.
AIBN /0,005 г, 0,03 ммоль/ добавляют к раствору метакрилоксиметилацетата /пример 28, 1,00 г, 4,55 ммоль/ в сухом ТГФ /8 г/ при 60oC в атмосфере сухого азота.
Спустя 24 ч реакционную смесь охлаждают до 20oC, и растворитель удаляют при пониженном давлении. Полученный полимер растворяют в CH2Cl2 и осаждают в метанол. Полимер выделяют из метанола фильтрованием, в результате чего получают белый порошок.
По данным дифференциальной сканирующей калориметрии /DSC/: Tg = 54,99oC.
Размеры по данным эксклюзионной хроматографии /SEC/ Мв = 184678, Мч = 2446, Мр = 54732, Мв/Мч = 7,56.
Пример 31. Полимер, полученный при эмульсионной полимеризации этил- 1-метакрилоилоксиэтилкарбоната.
Смесь натрийдодецилсульфата /6,5 мг, 0,023 ммоль/ в воде /2,40 мл/ и метабисульфита калия /6,3 мг, 0,028 ммоль/ в 0,82 мл воды нагревают до 60oC в атмосфере азота, до того как добавляют этил-1- метакрилоилоксиэтилкарбонат /пример 10, 0,617 г, 3,10 ммоль/.
Полимеризацию инициируют, добавляя персульфат калия /0,54 мг, 0,002 ммоль/ в 0,25 воды. Полимеризации дают протекать в течение 20 ч при 60oC в атмосфере азота, прежде чем реакционную смесь охлаждают до 20oC.
Пример 32. 1-Хлор-1- фенилметилвинилкарбонат.
Винилхлорформат /3,0 г, 0,025 моль/ и бензальдегид /4,14 г, 0,039 моль/ растворяют в 1,2-дихлорметане /30 мл/ и прикапывают пиридин /0,1 г, 1,28 моль/ к перемешиваемому раствору.
Этот раствор перемешивают в течение 1 дня при 80oC, промывают водой /25 мл/, и водную фазу снова экстрагируют 25 мл метиленхлорида. Объединенную органическую фазу сушат над сульфатом магния и концентрируют до получения 3,0 г /50%/ указанного в заглавии продукта.
1H ЯМР /60 МГц, CDCl3/: δ 4,55 /дд, 1H, CH2=/, 4,95 /дд, 1H, CH2/, 7,05 /дд, 1H, CH2 = CH-/, 7,25 /с, 1H, CH-Ph/, 7,40 /м, 5H, Ph/.
Пример 33. 1- Ацетокси-1- фенилметил-винилкарбонат.
Ацетат серебра /2,0 г, 0,012 моль/ добавляют к раствору 1- хлор-1-фенилметилвинилкарбоната примера 32 /2,50 г, 0,012 моль/ в 60 мл ДМФ. Реакционную смесь оставляют при перемешивании при комнатной температуре на 12 ч. Реакционную смесь фильтруют, и растворитель удаляют при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением /силикагель, метиленхлорид/ до получения 0,56 г /20%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDCl3/: δ 2,24 /с, 3H, CH3C=O/, 4,60 /дд, 1H, CH2=/, 4,95 /дд, 1H, CH2 =/, 7,00 /дд, 1H, CH=/, 7.50 /м, 5H, Ph/, 8,00 /c, 1H, -CH-Ph/.
Пример 34. Свободнорадикальная полимеризация 1-ацетокси-1- фенилметилвинилкарбоната.
AIBN /0,005 г, 0,03 моль/ добавляют к раствору 1-ацетокси-1-фенилметилвинилкарбоната примера 33 /1,0 г/ в сухом ТГФ /8 мл/ при 60oC в атмосфере сухого азота.
Спустя 12 ч растворитель удаляют при пониженном давлении. Полученный полимер растворяют в CH2Cl2 и повторно осаждают в подходящий растворитель. Полимер выделяют из растворителя фильтрованием, в результате чего получают белый порошок.
Пример 35. O-бензоилоксиметил-S-этилкарбонотиоат.
О-хлорметил-S-этилкарбонотиоат1 /5,73 г, 0,037 моль/ в 20 мл ДМФ добавляют к раствору бензоата калия /5,94 г, 0,037 моль/, и 18-краун-6 /0,485 г, 1,85 ммоль/ в 130 мл ДМФ добавляют затем к реакционной смеси и оставляют при комнатной температуре на 24 ч. Растворитель удаляют при пониженном давлении.
Остаток растворяют в 150 мл хлороформа, промывают водой /5 • 20 мл/ и сушат над сульфатом магния. Растворитель удаляют при пониженном давлении, очищают с помощью хроматографической обработки с мгновенным испарением /силикагель, хлороформ/ до получения 7,16 г /81%/ указанного в заглавии продукта.
1H ЯМР /60 МГц, CDCl3/: δ 1,3 /т, 3H, CH3/, 2,9 /кв, 2H, CH2CH3/, 6,1 /с, 2H, OCH2O/,7,3 - 7,7 /м, 3H, Ph/, 8,0 -8,2 /м, 2H, Ph/.
Пример 36. Бензоилоксиметилхлорформат.
SO2Cl2 /4,03 г, 0,030 моль/ добавляют к О-бензоилоксиметил-S-этилкарбонотиоату примера 35 /7,16 г, 0,030 моль/ при -5oC при перемешивании в течение 15 мин, с последующим перемешиванием при комнатной температуре в течение 2 ч.
После выпаривания EтSCl при комнатной температуре и 11 мм рт. ст. получают жидкость желтого цвета. Выход: 5,30 г /83%/.
1H ЯМР /60 МГц, CDCl3/: δ 6,1 /с, 2H, OCH2O/, 7,3-7,7 /м, 3H, Ph/, 8,0- 8,2 /м, 2H, Ph/.
Пример 37. N-/3-аминопропил /метакриламид.
Метакрилоилхлорид /8,0 г, 0,78 ммоль/ в метиленхлориде /10 мл/ добавляют к раствору 1,3- диаминопропана /35 мл/ в метиленхлориде /200 мл/ при 0oC.
Спустя 15 мин перемешивания при 0oC и 16 ч при 25oC реакционную смесь фильтруют и концентрируют при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением /силикагель, хлороформ/ метанол 8:2 /до получения /72%/ указанного в заглавии соединения.
1H ЯМР /60 МГц, CDClD/ацетон-d6/: δ 1,70 /м, 2H, CH2CH2CH2/, 2,0 /с, 3H, CH3C/, 2,30 /с, 2H, NH2/, 2,98 /м, 2H, CH2NH2/, 3,35 /м, 2H, NHCH2/, 5,35 /м, 1H, CH2=/, 5,80 /м, 1H, CH2=/, 7,45 /м, 1H, NH/.
Пример 38. N-/3-метакриламидоилпропил/O-/бензоилоксиметил/карбамат.
Бензоилоксиметилхлорформат /1 экв./ добавляют к 0,1 М раствору N- /3-аминопропил/метакриламида /2 экв./ в метиленхлориде при 0oC.
Спустя 15 мин при 0oC и подходящем времени при 25oC реакционную смесь фильтруют и концентрируют досуха при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением, получая целевой N-/3-метакриламидоилпропил/O- /бензоилоксиметил/карбамат.
Пример 39. Свободнорадикальная полимеризация в растворе N-/3- метакриламидоилпропил/-O-/бензоилоксиметил/карбамата.
AIBN /3/100 экв./ добавляют к 0,5 М раствору N-/3- метакриламидоилпропил/-O-/бензоилоксиметил/карбамата /1 экв./ в ТГФ при 60oC. Спустя 24 ч при 60oC реакционную смесь охлаждают до 25oC и концентрируют досуха при пониженном давлении. SEC анализ неочищенного продукта свидетельствует об образовании полимера.
Пример 40. Хлорметилморфолин-4-карбоксилат.
Морфолин /1 экв./ медленно добавляют к 0,1М раствору хлорметилхлорформата /10 экв./ в метиленхлориде при низкой температуре.
Спустя 15 мин при низкой температуре и подходящее время при 25oC реакционную смесь фильтруют и концентрируют досуха при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением, получая морфолин- 4-карбоксилат.
Пример 41. Метакрилоилоксиметилморфолин-4-карбоксилат.
Хлорметилморфолин-4-карбоксилат /1 экв./ добавляют к 0,1М раствору калиевой соли метакриловой кислоты /1,1 экв./ и 18-краун-6 /0,02 экв./ в ДМФ при 0oC.
Спустя 15 мин при 0oC и подходящее время при повышенной температуре реакционную смесь фильтруют и концентрируют досуха при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением, получая целевой метакрилоилоксиметилморфолин-4- карбоксилат.
Пример 42. Свободнорадикальная полимеризация метакрилоилоксиметил-морфолин-4-карбоксилата.
AIBN /0,03 экв./ добавляют к 0,5 M раствору метакрилоилоксиметилформолин-4-карбоксилата /1 экв./ в ТГФ при 60oC.
Спустя 24 ч при 60oC реакционную смесь охлаждают до 25oC и концентрируют досуха при пониженном давлении. По данным эксклюзионной по размерам хроматографии /SEC/ происходит образование полимера.
Пример 43. O-метакрилоилоксиметил-S-этилкарбонотиоат.
O- хлорметил- S-этилкарбонотиоат1 /1 экв./ добавляют к 0,1 M раствору калийной соли метакриловой кислоты /1 экв./ и 18-краун-6 /0,02 экв./ в ДМФ при 0oC.
Спустя 15 мин при 0oC и подходящее время при повышенной температуре реакционную смесь фильтруют и концентрируют досуха при пониженном давлении. Остаток очищают хроматографически с мгновенным испарением, получая O-метакрилоилоксиметил-S-этилкарбонотиоат.
Пример 44. Свободнорадикальная полимеризация O- метакрилоилоксиметил-S-этилкарбонотиоата.
AIBN /0,03 экв./ добавляют к 0,5 М раствору O-метакрилоилоксиметил- S- этилкарбонотиоата /1 экв./ в ТГФ при 60oC.
Спустя 24 ч при 60oC реакционную смесь охлаждают до 25oC и концентрируют досуха при пониженном давлении. По данным эксклюзионной по размерам хроматографии /SEC/ происходит образование полимера.
Пример 45. Свободнорадикальная сополимеризация в растворе N-/2-гидроксипропил/метакриламида с N-/2-ацетокси/- метоксикарбонилоксипропил/метакриламидом.
N-/2-гидроксипропил/метакриламид2 /0,430 г, 3,0 ммоль/ и N-/2- ацетокси/метоксикарбонилоксипропил/метакриламид /пример 17, 0,778 г, 3,0 ммоль/ растворяют в 10 мл тетрагидрофурана и нагревают до 50oC.
Добавляют AIBN /0,0207 г, 0,126 ммоль/, и полученную смесь перемешивают при 55oC в течение 3 дней до получения прозрачного геля.
Его растворяют в тетрагидрофуране, и растворитель выпаривают при пониженном давлении до получения белого порошка /1,33 г/. По данным эксклюзионной хроматографии по размерам /SEC/ происходит образование полимера.
Пример 46. Катализированный ферментами гидролиз полиметакрилоилоксиметилбензоата.
По 50 мл образца полимера /пример 23/ в виде тонкоизмельченного порошка и 20 мл 0,9%-ного водного NaCl помещают в три реакционные ампулы.
В одну из ампул добавляют также 0,1 мл эстеразы из свиной печени в 3,2 М /NH4/2SO4/Сигма, Е-3128, 250U-. В другую ампулу добавляют 0,1 мл 3,2 M /NH4/2SO4. Используя pH-stat /радиометр/, pH в каждой из ампул поддерживают постоянным 8,0, добавляя 0,1 М NaOH. Записывая расход NaOH, рассчитывают скорость гидролиза.
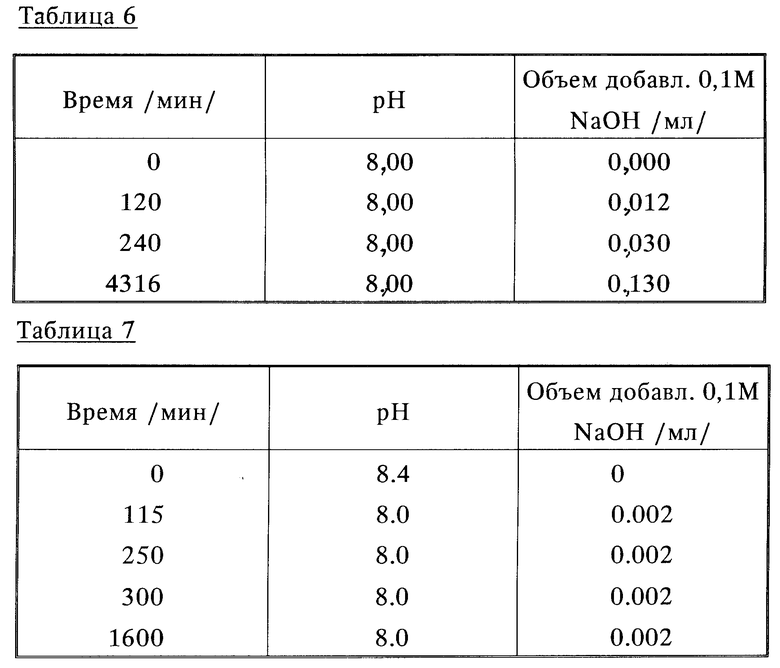
Более чем за 45 ч при 37oC выясняют, что гидролиз полимера с помощью эстеразы оказывается в 11 раз более быстрым, нежели контрольный с /NH4/2SO4 без эстеразы. В контрольном реакторе, содержащем полимер в 0,9%-ного NaCl, гидролиза не обнаруживают /см. чертеж/.
Расход 0,1 М NaOH в ампуле, содержащей полимер и эстеразу с 0,1 мл 3,2 М /NH4/2SO4 в 20 мл 0,9%-ного раствора NaCl приведен в табл. 5. Расход 0,1 М NaOH в контрольной ампуле, содержащей 0,1 мл 3,2 М /NH4/2SO4 в 20 мл 0,9%-ном растворе NaCl приведен в табл. 6.
Расход 0,1М NaOH в контрольной ампуле, содержащей полимер в 20 мл 0,9%-ного раствора NaOH приведен в табл. 7.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНТРАСТНЫЕ АГЕНТЫ И ИХ ПРИМЕНЕНИЕ | 1993 |
|
RU2122432C1 |
| ИОДИРОВАННЫЕ АРИЛЬНЫЕ СОЕДИНЕНИЯ И ДИАГНОСТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1995 |
|
RU2145955C1 |
| ПРОИЗВОДНЫЕ БЕНЗОПИПЕРИДИНА, БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2142945C1 |
| КОНЪЮГАТ ФОТОСЕНСИБИЛИЗАТОРА И ХИТОЗАНА И ЕГО ПРИМЕНЕНИЕ | 2013 |
|
RU2675830C2 |
| ПРОЛЕКАРСТВА ИНГИБИТОРОВ ТРОМБИНА | 1996 |
|
RU2176644C2 |
| Соединения фторхинолонового ряда на основе производных пиридоксина, обладающие антибактериальными свойствами | 2019 |
|
RU2713932C1 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2654336C2 |
| КОНЪЮГИРОВАННЫЕ ЛИПИДНЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2480447C2 |
| ИНГИБИТОРЫ ТРОМБИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ЗАЩИЩЕННОЕ ПРОИЗВОДНОЕ | 1996 |
|
RU2176645C2 |
| Четвертичные аммониевые соединения на основе производных пентаэритрита и пиридоксина, обладающие антибактериальной активностью | 2023 |
|
RU2811203C1 |


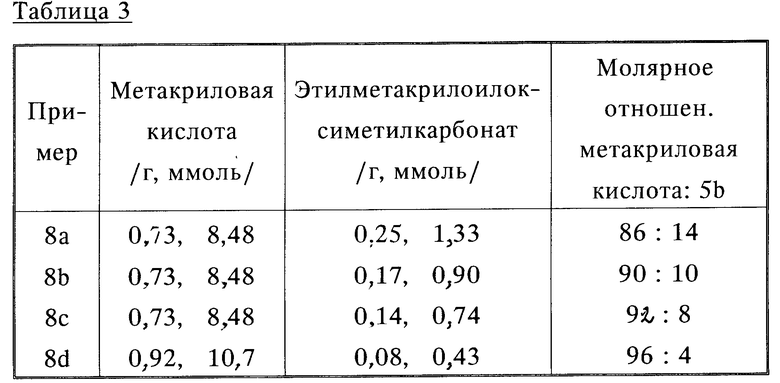
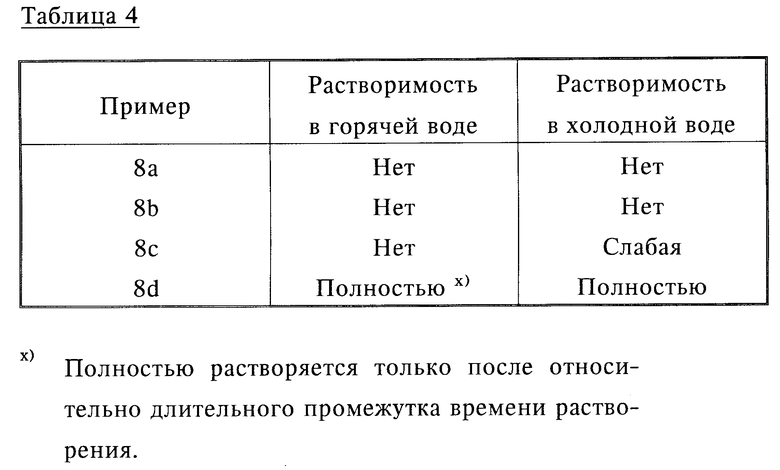
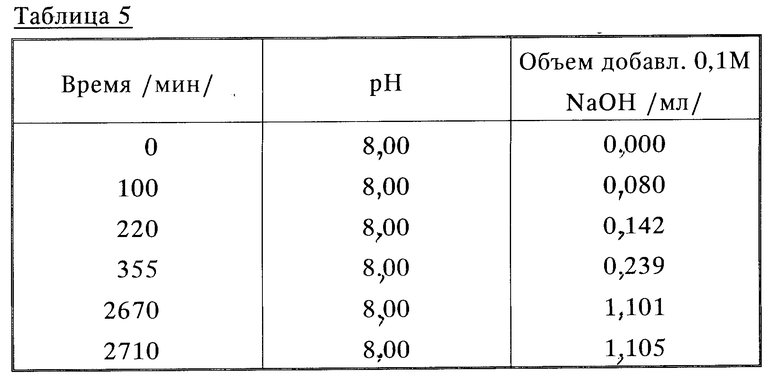
Использование: в медицине для получения биоразлагаемых материалов имплантатов и лекарств пролонгированного действия и при изготовлении упаковочных материалов. Сущность изобретения: биоразлагаемые несшитые полимеры с низкой или нулевой растворимостью в воде, с мол.м. 500-2000000 и содержащие звенья формулы II
в которой A - повторяющееся звено неполипептидной полимерной главной цепи, содержащей C1-C6 и, возможно, цепь прервана одним или более гетероатомами, выбранными из кислорода, азота и серы, и/или замещена одним (или более) заместителем, включающим такие гетероатомы; L = (C1-C3) алкиленовая группа, возможно заканчивающаяся и/или прерванная одной или более окси-, карбонил-, оксикарбонил-, имино- или иминокарбонилгруппами; l, m, n-одинаковые или различные и каждый 0 или 1; R1 и R2 - одинаковые или различные и каждый представляет собой водород, алифатические группы (до C10), циклоалкил (до C10), аралифатические группы (до C20), арил (до C20), гетероциклические группы (до C20) и один или более гетероатомов (O, S и N), и любая из упомянутых групп несет один или более функциональных заместителей, выбранных из галогена, NR4R5, CONR4R5, OR6, SP6 и COOR7(R4, R5, R6 - каждый выбран из ацильных групп, и атомы или группы, как определено для R1, R2, R7, являются атомом или группой, как определено для R1 и R2), или R1 и R2 вместе образуют алкилиден, алкилен или алкенилен (до C10), которые могут нести один или более функциональных заместителей, выбранных из галогена и групп формулы NR4R5, CONR4R5, OR6, SR6 и COOR7 (R4 - R7 - определены выше); и R3 - алифатическая группа (до C10); циклоалкил (до C10); аралифатическая группа (до C20); арил (до C20); гетероцикл (до C20), имеющий один или более гетероатомов из O, S, N; любые из указанных групп несут один или более функциональных заместителей, выбранных из галогена или групп: NR4R5, CONR4R5, OR6, SR6, COOR7 (R4 - R7 указаны выше), и/или прерваны, и/или оканчиваются гетероатомом (O, S или N), возможно вместе с сомономерными звеньями, включающими повторяющиеся звенья неполипептидных полимерных цепей и содержащие от 1 до 6 атомов углерода, возможно, прерывающихся одним или более гетероатомом (O, S или N) и/или замещенных одним или более заместителями, включающими такие гетероатомы. 4 з. п. ф-лы, 7 табл., 1 ил.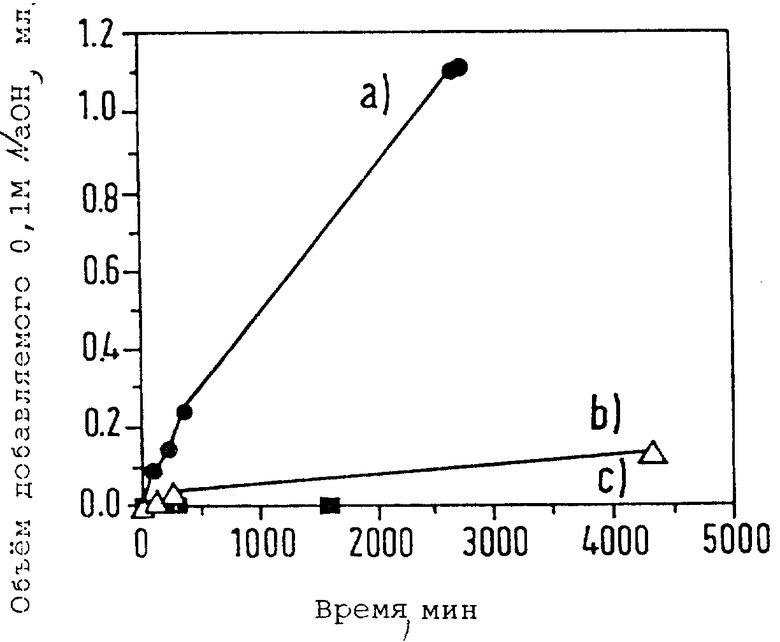

где A - повторяющееся звено неполипептидной полимерной главной цепи, содержащей C1-6 и, возможно, цепь прервана одним или более гетероатомами, выбранными из кислорода, азота и серы, и/или замещена одним или более заместителем, включающим такие гетероатомы;
L - C1-C3-алкиленовая группа, возможно заканчивающаяся и/или прерванная одной или более окси-, карбонил-, оксикарбонил-, имино- или иминокарбонилгруппами;
l, m, n - одинаковые или различные, каждый 0 или 1;
R1 и R2 - одинаковые или различные, каждый водород, алифатические группы, имеющие до 10 атомов углерода, циклоалкил, имеющий до 10 атомов углерода, алифатические группы, имеющие до 20 атомов углерода, арил, имеющий до 20 атомов углерода, гетероциклические группы, имеющие до 20 атомов углерода, и один или более гетероатомов, выбранных из кислорода, серы и азота, и любая из упомянутых групп несет один или более функциональных заместителей, выбранных из галогена, групп формулы - NR4R5, -CONR4R5, -OR6, -SR6 и -COOR7, где R4, R5 и R6 каждый выбран из ацильных групп и атомов или групп, как определено для R1 и R2, R7 является атомом или группой, как определено для R1 и R2, или R1 и R2 вместе образуют алкилиден, алкенилиден, алкилен или алкинилен, имеющий до 10 атомов углерода, которые могут нести один или более функциональных заместителей, выбранных из галогена, и групп формулы -NR4R5, -CONR4R5, -OR6, -SR6 и -COOR7, где R4, R5, R6, R7 определены выше;
- липофильная органическая группа, выбранная из алифатической группы, имеющей до 10 атомов углерода, циклоалкил, имеющий до 10 атомов углерода, алифатическая группа, имеющая до 20 атомов углерода, арил, имеющий до 20 атомов углерода, гетероцикл, имеющий до 20 атомов углерода, и один или более гетероатомов, выбранных из кислорода, серы, азота, и любые из указанных групп несут один или более функциональных заместителей, выбранных из галогена или групп формулы -NR4R5, -CONR4R5, -OR6, -SR6 и -COOR7, где R4, R5, R6, R7,
указанные выше, и/или прерваны и/или оканчиваются гетероатомом, выбранным из кислорода, азота, серы,
возможно вместе с сомономерными звеньями, включающими повторяющиеся звенья неполипептидных полимерных главных цепей и содержащие C1-6 атомов углерода, возможно прерывающихся одним или более гетероатомом, выбранным из кислорода, азота и серы и/или замещенных одним или более заместителями, включающими такие гетероатомы, указанные полимеры, являясь биоразлагаемыми, служат для получения водорастворимых полимеров путем биорасщепления указанных липофильных групп R3.
| US, патент, 4180646, C 08 G 65/28, 1979 | |||
| РСТ, заявка WO, 92/04392, C 08 G 63/00, 1992 | |||
| EP, заявка, 0130935, C 08 G 69/08, 1985. |
Авторы
Даты
1998-07-10—Публикация
1993-03-05—Подача