Изобретение относится к способам исследования биологических материалов с использованием соединений или составов для колориметрического, спектрофотометрического или флуорометрического анализа, в частности к способам определения количества бактерий в биопрепаратах, и может быть использовано в медицинской микробиологии и микробиологической промышленности.
Известен способ определения общего (живых и мертвых) количества бактерий подсчетом клеток под микроскопом с помощью камеры Тома-Горяева. Общим с предлагаемым изобретением является этап подготовки пробы к анализу, включающий в себя разведение биопрепарата в разводящей жидкости.
К недостаткам данного способа следует отнести то, что, позволяя определять общее количество бактерий, способ не дает информацию о содержании живых микроорганизмов в исследуемой пробе. Это обусловлено отсутствием микроскопического различия живых и мертвых бактерий в счетной камере.
Также известен культуральный способ определения количества живых микроорганизмов (метод Коха), заключающийся в высеве микробных суспензий на плотную питательную среду. Данный способ включает в себя последовательные десятикратные разведения микробной суспензии, высев конечного разведения на плотную питательную среду, инкубацию в условиях, определяемых видом микроорганизма, подсчет выросших колоний и определение количества живых клеток в единице объема исследуемой микробной суспензии (Луста К.А., Фихте Б.А. Методы определения жизнеспособности микроорганизмов. Пущино, 1990).
Общим с предлагаемым изобретением является этап разведения биопрепарата в разводящей жидкости.
К недостаткам данного способа следует отнести то, что, позволяя определять количество живых микроорганизмов, метод Коха не дает информацию об общем содержании микробных клеток. Это обусловлено тем, что мертвые бактерии не образуют колонии на плотной питательной среде.
В качестве прототипа выбран способ определения концентрации бактерий в суспензии (авторское свидетельство N 1231077 (СССР). Способ определения концентрации бактерий в суспензии. Н.В.Косарев и Е.О.Пучков. Опубл. в Б.И. 1986 г. N 18). Данный способ включает в себя следующие этапы: приготовление микробной суспензии и регистрацию интенсивности флуоресценции. Для проведения анализа готовят микробную суспензию в дистиллированной воде и вносят ее в раствор буфера (трис-HCl, 100 ммоль, pH 7,2 - 7,5). Затем с целью обеспечения проницаемости клеточной оболочки к смеси микробной суспензии с буферным раствором добавляют растворы тритона X-100 (до концентрации 0,03 - 0,05%), этилендиамин-тетраацетата-триса (ЭДТАТ), pH 7,2 - 7,5 (до концентрации 0,3 - 3,0 мМ) и этидиум бромид (до концентрации 4 - 7 мкмоль). После пятиминутной инкубации измеряют интенсивность флуоресценции этидиум бромида в микробной суспензии и в буферном растворе. Разность между первой и второй величинами характеризует концентрацию бактерий в суспензии.
Общими с предлагаемым изобретением являются следующие этапы:
подготовка пробы к анализу, включающая в себя разведение биопрепарата в буферном растворе и приготовление суспензии;
обработка микробной суспензии для проникновения флуоресцентного красителя через клеточную оболочку бактерии;
определение разницы в интенсивности флуоресценции этидиум бромида в буферном растворе и в микробной суспензии, подвергнутой обработке.
К недостаткам рассматриваемого способа следует отнести то, что он не позволяет определять количество живых микроорганизмов. Это обусловлено тем, что регистрация интенсивности флуоресценции этидиум бромида в микробной суспензии осуществляется после химической обработки, приводящей к гибели всех клеток в биопрепарате.
Задачей изобретения является определение содержания живых клеток в биопрепарате и общего их количества.
Поставленная задача решается благодаря тому, что в способе определения количества бактерий в биопрепарате, включающем разведение препарата в буферном растворе, обработку микробной суспензии для обеспечения проникновения флуоресцентного красителя через клеточную оболочку микробной клетки, определение разницы в интенсивности флуоресценции этидиум бромида в буферном растворе и в микробной суспензии, предусмотрено различие: измерение интенсивности флуоресценции этидиум бромида в микробной суспензии проводят до и после ее обработки.
Кроме того, предложенный способ отличается тем, что повышение проницаемости клеточной оболочки для флуоресцентного красителя достигается путем термической обработки микробной суспензии.
Сущность предложенного способа заключается в следующем. Готовят микробную суспензию в физиологическом растворе. Затем пробу делят на две части. Первую часть микробной суспензии вносят в буферный раствор трис-HCl (0,5 М), pH 7,0 - 7,2, добавляют флуоресцентный краситель этидиум бромид (до конечной концентрации 20 мкМ) и через 10 мин измеряют интенсивность флуоресценции этидиум бромида в микробной суспензии. Вторую часть пробы с целью обеспечения проницаемости клеточной оболочки подвергают температурному воздействию при температуре кипящей водяной бани в течение 5 мин. Затем пробу охлаждают до комнатной температуры, вносят в буферный раствор, добавляют этидиум бромид (до конечной концентрации 20 мкМ) и измеряют интенсивность флуоресценции приготовленной пробы. Параллельно измеряют интенсивность флуоресценции этидиум бромида в буферном растворе.
Полученные флуоресцентные показатели используют для определения количества бактерий в суспензии по формулам, полученным авторами эмпирическим путем.
Длительность методики составляет 30 мин с момента поступления пробы. Трудозатраты на анализ одной пробы составляют 0,5 чел/ч.
Наличие причинно-следственной связи между совокупностью существенных признаков заявляемого объекта и достигаемым техническим результатом показано в табл. 1.
Изобретение позволяет определить как общее количество микроорганизмов, так и содержание живых клеток в микробной суспензии.
Возможность осуществления заявляемого изобретения показана следующими примерами.
Пример 1.
Определение количества бактерий в биопрепарате.
Готовят микробную суспензию путем разведения биопрепарата в физиологическом растворе до концентрации 4 млрд.кл•см-3 по ОСО мутности 10 ед., учитывая кратность разведения (n). Затем пробу делят на две части. Первую часть суспензии в количестве 1,0 см3 вносят в измерительную кювету, к ней добавляют 2,9 см3 буферного раствора и 0,1 см3 0,8 мМ раствора этидиум бромида. Через 10 мин измеряют интенсивность флуоресценции полученной пробы (Iн).
Вторую часть микробной суспензии подвергают температурному воздействию при температуре кипящей водяной бани в течение 5 мин. После охлаждения до комнатной температуры 1,0 см3 подготовленной суспензии вносят в измерительную кювету, к ней добавляют 2,9 см3 буферного раствора и 0,1 см3 0,8 мМ раствора этидиум бромида и измеряют интенсивность приготовленной пробы (It).
Параллельно готовят пробу, содержащую этидиум бромид (до конечной концентрации 20 мкМ) в буферном растворе (Iф).
Измерение флуоресцентных показателей проводят на спектрофлуориметре типа "Квант" при длине волны возбуждающего света 475 нм и длине волны флуоресценции 600 нм с использованием измерительной кюветы с длиной оптического пути 1 см и рабочим объемом 4,0 см3.
Определение общего количества бактерий в биопрепарате проводят по формуле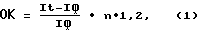
где
ОК - общая концентрация бактерий в биопрепарате, млрд.кл.•см-3;
It - интенсивность флуоресценции этидиум бромида в микробной суспензии, подвергнутой термическому воздействию, усл.ед.;
Iф - интенсивность флуоресценции этидиум бромида в буферном растворе, усл.ед.;
n - кратность разведения.
Определение количества живых бактерий в биопрепарате проводят по формуле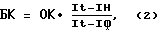
где
БК - количество живых бактерий в биопрепарате, млрд.кл.•см-3;
It - интенсивность флуоресценции этидиум бромида в микробной суспензии, подвергнутой термическому воздействию, усл.ед.;
Iн - интенсивность флуоресценции этидиум бромида в микробной суспензии, усл.ед.;
Iф - интенсивность флуоресценции этидиум бромида в буферном растворе, усл.ед.
Пример 2.
Определение количества бактерий Y. pestis шт. EV в культуральной жидкости.
Культуральную жидкость микробов Y. pestis шт. EV готовят к анализу, как описано в примере 1. Определение количества бактерий проводят по формулам (1, 2). Результаты представлены в табл. 2.
Пример 3.
Определение количества бактерий Y.pestis шт. EV в концентрированной суспензии.
Концентрированную суспензию микробов Y.pestis шт. EV разводят физиологическим раствором. Дальнейшую подготовку проб и измерение флуоресцентных показателей проводят, как описано в примере 1. Количество бактерий определяют по формулам (1, 2). Результаты представлены в табл. 2.
Пример 4.
Определение количества бактерий в вакцине чумной живой сухой.
Вакцину чумную живую сухую регидратируют физиологическим раствором. Регидратированный препарат вакцины чумной живой сухой при необходимости разводят физиологическим раствором. Дальнейшую подготовку проб и измерение флуоресцентных показателей проводят, как описано в примере 1. Общее количество бактерий в суспензии и количество живых бактерий рассчитывают по формулам (1, 2).
Пример 5.
Определение количества бактерий P. mallei в культуральной жидкости.
Культуральную жидкость микробов P.mallei готовят к анализу, как описано в примере 1. Определение количества бактерий проводят по формулам (1, 2). Результаты представлены в табл. 2.
Пример 6.
Определение количества бактерий S.enteritidis (var. Danych) в культуральной жидкости.
Культуральную жидкость микробов S. enteritidis готовят к анализу, как описано в примере 1. Определение количества бактерий проводят по формулам (1, 2). Результаты представлены в табл. 2.
Таким образом, можно сделать вывод, что заявляемое изобретение позволяет осуществить способ определения количества бактерий в биопрепарате.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ УСТОЙЧИВОСТИ КЛЕТОК ЧУМНОГО МИКРОБА ШТАММА EV К ЛИОФИЛИЗАЦИИ | 2007 |
|
RU2380420C2 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ МИКРОБНОЙ ПОПУЛЯЦИИ | 2001 |
|
RU2195496C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ЖИВЫХ МИКРОБОВ В БИОПРЕПАРАТЕ | 1992 |
|
RU2037805C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДЫХАТЕЛЬНОГО КОНТРОЛЯ У ПОПУЛЯЦИИ БАКТЕРИЙ | 2003 |
|
RU2247780C2 |
| СПОСОБ МОНИТОРИНГА СТАДИИ КУЛЬТИВИРОВАНИЯ В ТЕХНОЛОГИИ ЧУМНОЙ ВАКЦИНЫ | 2017 |
|
RU2677954C1 |
| СПОСОБ ИНДИКАЦИИ БИОЦИДНОЙ АКТИВНОСТИ ПЕРЕКИСНЫХ ДЕЗИНФИЦИРУЮЩИХ РАСТВОРОВ К БОТУЛИНИЧЕСКОМУ НЕЙРОТОКСИНУ | 2003 |
|
RU2265057C2 |
| ЖИДКАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ГЛУБИННОГО КУЛЬТИВИРОВАНИЯ БАКТЕРИЙ PLESIMONAS SHIGELLOIDES ШТАММ № 16 | 2002 |
|
RU2239654C2 |
| Способ определения концентрации бактерий в суспензии | 1984 |
|
SU1231077A1 |
| АНТИГЕННЫЙ СОСТАВ ЧУМНОЙ ХИМИЧЕСКОЙ ВАКЦИНЫ | 2001 |
|
RU2190424C1 |
| ЦЕНТРОБЕЖНЫЙ СЕПАРАТОР ДЛЯ КУЛЬТУРАЛЬНЫХ ЖИДКОСТЕЙ | 1999 |
|
RU2150333C1 |
Способ включает разведение биопрепарата в буферном растворе, обработку микробной суспензии через клеточную оболочку бактерии, определение разницы в интенсивности флуоресценции этидиум бромида в буферном растворе и в микробной суспензии, подвергнутой обработке, определение по значению разницы общего количества бактерий. Способ позволяет определить количество живых клеток в биопрепарате. 1 з.п. ф-лы, 2 табл.
| SU, патент, 1231077, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1998-08-10—Публикация
1997-05-28—Подача