Данное изобретение относится к процессу получения ценных промежуточных продуктов для пестицидов. Более конкретно, оно относится к процессу получения галоидированных соединений, полезных в качестве промежуточных соединений для инсектицидов.
Из патента Великобритании N 1520443 известно, что галоидированные сложные эфиры, такие как алкил 3,3-диметил-4,6,6,6-тетрагалоидгексаноаты, могут превращаться в алкил 3-/2,2-дигалоидвинил/-2,2-диметилциклопропанкарбоксилаты с помощью обработки основанием, и что соответствующие циклопропанкарбоновые кислоты могут превращаться в сложные эфиры, например, с 3-феноксибензиловым спитом, давая ценные инсектицидные продукты.
До настоящего времени получение этих галоидированных сложных эфиров предусматривало взаимодействие летучих галоидалканов, таких как четыреххлористый углерод и 1,1,1-трихлортрифторэтан, с ненасыщенными сложными эфирами, и процесс необходимо было проводить на химическом заводе /установке/ и при условиях, в которых указанные компоненты могли бы содержаться так, чтобы предотвратить выброс летучих веществ в атмосферу.
Настоящее изобретение касается нового процесса, по которому летучие галоидалканы заменяются относительно нелетучими реагентами, посредством чего значительно уменьшается возможность попадания летучих галоидалкановых компонентов в атмосферу.
Согласно настоящему изобретению предлагается процесс получения соединения формулы I, приведенной в конце описания, в которой X, Y и Z каждый выбран из галоида, предпочтительно, хлора, фтора или брома; R представляет галоид, алкил или галоидалкил, или арил, который необязательно может быть замещен галоидом; и R1 выбран из гидрокси, галоида, предпочтительно, хлора или брома, алкокси с числом атома углерода до 6, алкила с числом атомов углерода до 4, который может быть необязательно замещен галоидом; или R1 представляет группу -OR2, происходящую из спирта R2OH, сложные эфиры которого с 3-(2,2-дихлорвинил)-2,2-диметилциклопропанкарбоновой кислотой являются инсект ицидными соединениями, включая те, у которых R2 представляет собой алкарил, предпочтительно бензил, который может быть необязательно замещен в метиленовом фрагменте циано группой, или алкинилом с числом атомов углерода до 4, и в фенильном фрагменте - заместителями в количестве до 5, выбранными из галоида, предпочтительно хлора или фтора, алкила с углеродными атомами в количестве до 4, предпочтительно метила, галоидалкила с числом атомов углерода до 4, предпочтительно, трифторметила, алкоксиалкила с числом атомов углерода до 4, предпочтительно метоксиметила, галоидалкокси, предпочтительно трифторметокси, фенокси и галоидфенокси; согласно которому соединение формулы II, приведенной в конце описания подвергается реакции с сульфонилгалогенидом формулы III, приведенной также в конце описания.
Особенно полезные соединения, которые могут быть получены с помощью процесса изобретения, включают:
метил X,3-диметил-4,6,6,6-тетрахлоргексаноат,
метил 3,3-диметил-4,6,6,6-тетрабромгексаноат,
этил 3,3-диметил-4,6,6,6-третрахлоргексаноат,
метил 3,3-диметил-4-бром-6,6,6-трифторгексаноат,
4,4-диметил-1,5,7,7,7-пентахлоргептан-2-он,
4,4-диметил-1,5,7,7-тетрахлор-7-/4-хлорфенил/-гептан-2-он,
3,3-диметил-4,6,6,6-тетрахлоргексановая кислота,
метил 3,3-диметил-4,6,6,6-трихлор-7,7,7-трифторгептаноат,
этил 3,3-диметил-4,6,6-трихлор-7,7,7-трифторгептаноат,
метил-3,3-диметил-4,6,6-трихлор-6-/4-хлорфенил/-гексаноат,
бензил 3,3-диметил-4,6,6-трихлор-7,7,7-трифторгептаноат,
2,6-дихлорбензил 3,3-диметил-4,6,6,-трихлор-7,7,7-трифторгептаноат,
4-метил-2,3,5,6-тетрафторбензил 3,3-диметил-4,6,6-трихлор-7,7,7-трифторгептаноат,
пентафторбензил 3,3-диметил-4,6,6,6-тетрахлоргексаноат,
2,3,5,6-тетрафторбензил 3,3-диметил-4,6,6,6-тетрахлоргексаноат,
2-метил-3-фенилбензил 3,3-диметил-4,6,6,-трихлор-7,7,7-трифторгептаноат,
3-феноксибензил 3,3-дтметил-4,6,6,6-тетрахлоргексаноат,
α - циано-3-феноксибензил 3,3-диметил-4,6,6,6-тетрахлоргексаноат,
α - циано-3-феноксибензил 3,3-диметил-4,6,6,6-тетраборомгексаноат,
α - циано-4-фтор-3-феноксибензил 3,3-диметил-4,6,6,6/тетрахлоргексаноат,
α -циано-3-феноксибензил 3,3-диметил-2,6,6-трихлор-7,7,7-трифторгептаноат, и
α -циано-4-фтор-3-феноксибензит 3,3-диметил-4,6,6-трихлор-7,7,7-трифторгептаноат.
Соединения формулы II, которые являются полезными в процессе изобретения, включают следующее:
метил 3,3-диметилпент-4-еноат,
этил 3,3-диметилпент-4-еноат,
4,4-диметил-1-хлоргекс-5-ен-2-он,
3,3-диметилпент-4-еновая кислота,
бензил 3,3-диметилпент-4-еноат,
2,6-дихлорбензил 3,3-диметлпент-4-еноат,
4-метил-2,3,5,6-тетрафторбензил 3,3-диметилпент-4-еноат,
пентафторбензил 3,3-диметил-4-еноат,
2,3,5,6-татрафторбензил 3,3-диметил-4-еноат,
2-метил-3-фенилбензил 3,3-диметилпент-4-еноат,
3-феноксибензил 3,3-диметилпент-4-еноат,
α -циано-3-феноксибензил-3,3-диметилпент-4-еноат, и
α -циано-4-фтор-3-феноксибензил 3,3-диметилпент-4-еноат,
Соединения формулы III которые полезны в процессе изобретения, включают:
трихлорметансульфонилхлорид,
триборомметансульфонибромид,
трифторметансульфонилбромид,
1,1-дихлор-2,2,2-трифторметансульфонилхлорид, и
1,1-дихлор-1-/4-хлорфенил/метансульфонилхлорид.
Процесс может проводиться в присутствии или в отсутствии растворителя или жидкого разбавителя для реагентов. Когда используется растворитель или разбавитель, удобно применять любой жидкий материал, который является химическим инертным в условиях процесса, который позволяет протекать процессу при желаемой температуре, и легко отделяться от получающегося в результате продукта, например, с помощью выпаривания или фрикционной перегонки. Подходящие растворители включают ароматические углеводородные растворители, такие как толуол или ксилол, или алифатические растворители, такие как сложные эфиры, кетоны алканы, или галоидированные растворители, такие как галоидалканы.
Процесс может проводиться при любой температуре, при которой реакция проходит с приемлемой скоростью. Скорость реакции увеличивается с температурой, и часто удобно проводить реакцию при повышенных температурах, например, в интервале 50 - 150oC, причем, верхний предел определяется температурой дефлегмации растворителя или разбавителя, когда он применяется. Продолжительность реакции зависит от скорости реакции при используемой температуре, но обычно она находится в интервале от 1 до 60 ч, и предпочтительно 3 - 40 ч.
Скорость реакции может часто увеличиваться, или температура реакции понижаться при использовании катализаторов, которые промотируют реакцию. По-видимому полезными для данного процесса является свободно-радикальные катализаторы, включая, например, органические перекиси, такие как перекись бензоила, азо соединения, такие как азобисизобутиронитрил, и аналогичные. Еще одним классом катализаторов, которые полезны, являются комплексы некоторых металлов с фосфинами, такие как трис-/трифенилфосфинил/-рутений/П/дихлорид.
Сульфонилгалогениды формулы III удобным образом получаются с помощью окисления соответствующих сульфонилгалогенидов формулы IV; приведенной в конце описания.
Окисление сульфенилгалогенидов формулы IV в сульфонилгалогениды формулы III похоже не было описано ранее. Данное окисление может удобно осуществляться с помощью использования перекиси водорода, или надкислот, таких как надуксусная или надбензойная кислота, например, с помощью обработки сульфенилгалогенида смесью перекиси водорода и ледяной уксусной кислоты. Процесс может проводиться при повышенных температурах, если необходимо.
Поэтому согласно следующему аспекту настоящее изобретение предоставляет процесс получения соединения формулы I, описанной выше, согласно которому на предварительной стадии сульфонилгалогенид формулы III получается с помощью окисления соответствующего сульфенилгалогенида формулы IV.
Сульфенилгалогениды формулы IV могут получаться с помощью гидрогенолиза подходящих предшественников, таких как дисульфид формулы V, приведенной в конце описания или простой тиоэфир формулы VI (также приведенной в конце описания), при котором галоидирование метиленовой группы, несущей R группу, сопровождается галогенолизом серо-бензильной связи, давая сульфенилгалогенид формулы III и бензилгалогенид.
Дополнительные подробности процесса изобретения даются в примерах, которые следуют ниже.
Пример 1.
Данный пример иллюстрирует получение бис-/2,2,2-трифторметил/дисульфида.
Смесь 2,2,2-трифторэтилбромида /9,8 г/, нонагидрата сульфида натрия /14,4 г/, серы /1,9 г/, гексадецилтрибутилфосфонийбромида /1,0 г/ и воды /18,0 г/ загружалась в трубку Кариуса в атмосфере азота и трубка /пробирка/ запаивалась или герметизировалась. Трубка нагревалась до 70oC в течение 8 часов, охлаждалась, и содержимое подвергалось перегонке с паром, давая бис-/2,2,2-трифторэтил/дисульфид в виде масла с выходом 67%. Продукт идентифицировался с помощью IX-массспектроскопии.
Пример 2.
Данный пример иллюстрирует получение 1,1-дихлор-2,2,2-трифторэтансульфенилхлорида.
Сульфенилхлорид /4,46 г/ добавлялся по каплям к раствору бис-/2,2,2-трифторэтил/дисульфида /1,0 г/ в дихлорметане /5,0 куб.см/ при температуре окружающей среды в атмосфере сухого азота. Спустя 3 часа выход желаемого продукта оценивался в 60% по данным газожидкостной хроматографии. Продукт был идентичен продукту, полученному в примере 4, приведенном ниже.
Пример 3
Данный пример иллюстрирует получение 2,2,2-трифторэтилтиометилбензола.
Смесь 1-хлор-2,2,2-трифторэтана /20 г/, бензилмеркаптана /12,4 г, 99% крепости/, гидроокиси натрия /22,0 г 22% водного раствора/ и гексадецилтрибутилфосфонийбромида /0,51 г/ загружалась в повторно герметизируемую трубку Кариуса в атмосфере азота и нагревалась при 70oC в течение 10 часов. Трубка затем охлаждалась до 0oC, разгерметизировалась, и содержимое разделялось на два слоя. Нижний органический слой собирался, промывался водой и очищался с помощью перегонки, давая 2,2,2-трифторэтилтиометилбензол, т.кип. 60 - 70oC /10 мм рт.ст. 17,4 г/ выход 84%, крепость 99%/. Идентичность продукта подтверждалась данными гх-масс спектроскопии и ядерно-магнитного резонанса, и сравнением с данными, приведенными в C.Bunyagidi и др., J. Org. Chem., 1981, 46, 3335.
Пример 4
Данный пример иллюстрирует получение 1,1-дихлор-2,2,2-трифторэтансульфенилхлорида.
Раствор 2,2,2-трифторэталтиометилбензола /20,0 г, крепость 99%, полученный по способу примера 3, приведенного выше/, в 1,1,2,2-тетрахлорэтане /26,4 куб. см/ охлаждался до 0oC, и в раствор пропускался газ хлор в течение приблизительно 3 часов при данной температуре. Полученный таким образом оранжевый раствор продувался азотом и подвергался фракционной перегонке, давая 1,1-дихлор-2,2,2-трифторэтансульфенилхорид в виде масла глубокого желтого цвета, т.кип. 63-65oC/ 200 мбар /17,4 г, 73% крепость, молярный выход 60%/, загрязненный остаточным тетрахлорэтаном и менее 1% бензилхлорида/. Продукт идентифицировался с помощью гх-масс спектроскопии, и сравнивался с данными, приведенными авторами H. Fritz и др., Chem., Ber., 1989, 122, 1757.
Пример 5
Данный пример иллюстрирует получение 1,1-дихлор-2,2,2-трихлорэтансульфонилхлорида.
1,1-Дихлор-2,2,2-трихлорэтансульфенилхлорид /6,3 г/, полученный по способу примера /4/ растворялся в ледяной уксусной кислоте /16,0 г/ при 10oC, и раствор охлаждался до 5oC. К раствору сульфенилхлорида на протяжении 30 минут по каплям добавлялась перекись водорода /16,8 г 30% раствора в воде/, после чего раствор нагревался до 60" до тех пор, пока полностью не исчезала желтая окраска /приблизительно 2 часа/. Смесь охлаждалась до температуры окружающей среды, и избыток перекиси водорода разлагался с помощью обработки водным раствором /10% вес/вес/метанбисульфита натрия. Смесь разделялась на две фазы, нижний органический слой собирался и анализировался с помощью гх-масс спектроскопии. Он содержал 75% вес/вес требуемого 1,1-дихлор-2,2,2-трифторэтансульфонилхлорида, показывая молярный выход 57%. Идентичность продукта подтверждалась сравнением с материалом, полученным по способу авторов H.Wei-Yvan и др., Acta Chim. Sinica, 1986, 44 45 /Chemical Abstracts 105, 171793 о/.
Пример 6
Данный пример иллюстрирует получение метил 3,3-дтметил-4,6,6,6-тетрахлоргексаноата.
Трихлорметансульфонилхлорид /22,5 г/ добавлялся к раствору метил 3,3-диметилпетнт-4-еноата /8,26 г/ в толуоле /8,67 г/ в присутствии дихлорида трис-/трифенилфосфинил/рутения/П/ /0,2 г/, и смесь нагревается в атмосфере азота при температуре кипения с обратным холодильником /приблизительно 111oC/ в течение 40 часов. Состав реакционной смеси затем определяется с помощью газожидкостной хроматографии /гжх/. Целевой продукт присутствовал с количестве, указывающем на выход 76% по весу в расчете на загруженный метил 3,3-диметилпент-4-еноат, и 90% в расчете на потребленный метил 3,3-диметилпент-4-еноат. Идентичность данного продукта подтверждалась с помощью гжх-масс спектроскопии и по 3,3-диметил-4,6,6,6-тетрахлоргексаноату, полученному по способу, описанному в патенте Великобритании N 1520443.
Пример 7
Данный пример иллюстрирует получение метил 3,3-диметил-4,6,6,6-тетрахлоргексаноата.
Трихлорметансульфонилхлорида /44,5 г/ добавлялся к смеси метил 3,3-диметилпент-4-еноата /16,52 г/, толуола /17,34 г/ и перекиси бензоила /0,563 г/, и смесь нагревалась при 90" в течениеи3,5 часов. Определение состава реакционной смеси с помощью газо-жидкостной хроматографии показало, что желаемый продукт получался с выходом 92% в расчете на загруженный метил 3,3-диметилпент-4-еноат.
Пример 8
Данный пример иллюстрирует получение метил 3,3-диметил-4,6,6-трихлор-7,7,7-трифторгептаноата.
Смесь 1,1-дихлор-2,2,2-трихлорэтансульфонилхлорида /1,5 г/ и метил 3,3-диметилпент-4-еноата /2,0 г/ нагревалась при 110oC в течение 40 минут, и состав определялся по данным анализа гжх. Данный анализ показал что выход требуемого продукта составил 79%.
Пример 9
Данный пример иллюстрирует получение метил 3,3-диметил-4,6,6-трифтор-7,7,7-трифторгептаноата.
1,1-Дихлор-2,2,2-трифторэтансульфонилхлорид /0,2 г/ добавлялся к смеси метил 3,3-диметилпент-4-еноата /0,18 г/, толуола /0,13 г/ и перекиси дибензоила /0,015 г/, и смесь нагревалась при температуре кипения с обратным холодильником /дефлегмации, приблизительно 111oC/ в течение 2 часов. Определение состава получающейся в результате реакционной смеси показало, что требуемый продукт получался с выходом 82%, и что не оставалось никакого сульфонилхлорида.
Химические формулы
/в описании/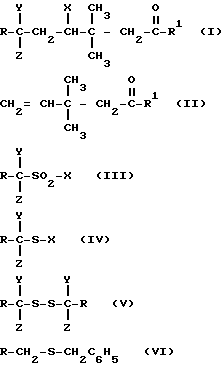 щ
щ
Описывается процесс получения галоидированных соединений формулы RCY(Z)CH2CH(X)С-(СH3)2CH2COR1 , в которой X, Y и Z представляют собой галоид, R представляет алкил , галоид, галоидалкил или арил, и R1 представляет гидрокси, галоид, алкокси, алкил или галоидалкил, или остаток пиретроидного спирта, согласно которому соединение формулы CH2=CHC(CH3)2-CH2-COR1 подвергается взаимодействию с сульфонилгалогенидом формулы RCY(Z)SO2X. Процесс устраняет необходимость использования летучих галоидуглеродов при получении ценных промежуточных соединений для инсектицидов. 8 з.п. ф-лы, 1 ил.
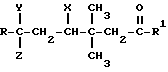
где X, Y, Z - каждый выбран из галоида;
R - галоид, алкил с числом углеродных атомов до 6, галоидалкил, содержащий алкил с числом углеродных атомов до 6, или арил, который может быть замещен галоидом;
R1 - алкоксигруппа с числом атомов углерода до 6 или группа OR2 - остаток спирта R2OH, сложные эфиры которого с 3-(2,2-дихлорвинил)-2,2-диметилциклопропанкарбоновой кислотой обладают инсектицидной активностью,
отличающийся тем, что соединения общей формулы II
подвергают взаимодействию с сульфонилгалогенидом формулы III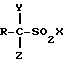
2. Способ по п.1, отличающийся тем, что соединение формулы II выбирают из метил 3,3-диметилпент-4-еноата или этил 3,3-диметилпент-4-еноата или 2,6-дихлорбензил 3,3-диметилпент-4-еноата.
8. Способ по п. 7, отличающийся тем, что сульфенилгалогенид получают путем галогенолиза дисульфида формулы V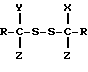
или простого тиоэфира формулы VI
9. Способ по п.1, отличающийся тем, что R2 в соединении формулы I имеет значение бензила, который может быть замещен в метиленовом фрагменте цианогруппой, а в фенильном фрагменте - заместителями в количестве до 4, выбранными из фенокси, галоида или алкила с числом атомов углерода до 4.
| GB, патент 1520443, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1998-08-20—Публикация
1992-01-08—Подача