1
Изобретение отн(.:сится к усовершенствованному способу получения сложных эфиров замещенных циклопропанкарбоновых кислот общей формулы (I)
lX
«,
СООБ5
где R, Rg, Rg и R могут быть одинаковыми или различными, причем каждЕлй представляет собой атом водорода, C -Cg-алкил, Сз-Сд-циклоапкил, Cg-Cg-арил или С-,-С о-аралкилр
R) и R или R и R могут вместе с атомом углерода, с которым они связаны, образовывать цикл;
Н5- С Сд-алкил, бензил, 3-феноксибензил, 3-фенокси-о1-цианобензил, З-фенокси-сб-этинилбензил, 5-бензил-3-фурилметил или 2-алкил-З-метил-2-циклопентен-1-он-4-ил;
Y и Z - атом водорода или гiaлoген.
Соединения формулы (I) находят применение в сельском хозяйстве в качестве инсектицидов или полупродуктов для их получения.
Известен способ получения сложных эфиров замещенных циклопропан.карбоновых кислот, заключаюитийся в том, что низшие алкиловые эфиры хризантемовой кислоты обрабатывают озоном и образовавшиеся при этом низшие алкиловые эфиры 3-Фоомил 2,2-диметилциклопропанкарбоновой кислоты подвергают действию реактива Виттига 1,
Недостатками такого способа являются использование труднодоступных сложных эфиров хризантемовой кислоты, реактивов на основе трехваоггентного фосфора, а также необходимость энергозатрат в связи с озонолизом.
Целью изобретения является упрощение процесса.
Цель достигается способом получения сложных эфиров замещенной дик-лопропанкарбоновой кислоты формулы (I), отличительная особенность которого состоит в том, что 1- галоген-З-алкен-2-ол общей формулы (И) RI ОН
.xSCXYZ
RS
где R, ivg
R.
3
Z имеют указанные выше значения; X - галоген, подвергают взаимодействию со сложным эфиром ортокарбоновой-кислоты общей Формулы (III) R,-CH-C(OR, где . и имеют указанные выше зн чения, а три группы К5 могут быть одинаковыми или различными, при 100-200°С, полученный при этом слож ный эфир З-галоген-сГ-ненасыщенной карбоновой кислоты общей формулы IV С ОН X в4 COOR5 где R, Rg, Rg, R, Rg-, У, Z, X имеют указанные выше значения обр абатывают основанием, взятым в кол честве 0,3-0,7 моль на 1 моль сложн го эфира формулы (IY), при (-80) С+100)С, целевой продукт выделяют как таковой или в случае необхо,цимости гидролизуют или переэтерифицируют соответствующим спиртом в пр делах значений радикала , Процесс взаимодействия спирта фо мулы (II) со сложным эфиром формулы (III) целесообразно вести в присутствии кислотного катализатора в органического растворителя при 120- 160 С с непрерьшной отгонкой вода, образующейся в процессе реакции, и при мольном соотношении между 1-галрген-З-алкен-2-олом и сложным эфиром формулы (III), равном l,3:3fO, Предпочтительными 1-галоген-З-алкен-2-олами для указанной реакци являются 1,1,1-трихлор-4-метил-3-пен-ген-2-ол; 1,1,1-трибРОМ-4-метил -З-пентен-2-ол; 1-хлор-1,1-дибром-4 -метил-З-пентен-2-ол 1-бром-1, -дихлор-4-метил-3-пентен-2-ол;1,1-дихлор-4-метил-3-пентен-2-ол; 1,1-дибром-4-метил-3-пентен-2-ол 1,1,1-трихлор-4-метил-3-гептен-2-ол 1,1,1-трибром-4-метил-3-гептен-2.--ол; 1,1-дихлор-4-метил-3-гептен 2 -ол; 1,1-дибром-4-метил-3-гептен-2 -ол, 1,1,1-трихлор-4,б,б-триметил-З-гептен-2-ол, 1,1,1-трибром-4,б,б -триметил-З-гептен-2-ол, 1,1,1-трихлор-4-этил-3-гексен-2-ол, 1,1,1-трибром-4-этил-3-гексен-2-ол,, 1,1,1-трихлор-4-метил-3-гексен-2-ол, 1,1, 1-трибром-4-метил-3-гексен-2-ол, 1,1,1-трихлор-З-гептен-2-ол и 1,1,1-трибром-З-гептан-2-ол 1-Галоген-3-апкен-2-олы формулы (11) получают по реакции Принса взаимодействием непредельного углеводорода общей формулы (Y) R2 Н где R, R, Rj имеют значения, укаванные выше, с галогенацетальдегидом общей формулы CXYZCHO где X,Y,Z имеют значения, указанные выше, и при необходимости изомеризацией двойной связи продукта, получающегося по этой реакции. В качестве ненасыщенного углеводорода формулы (V) могут быть взяты, например, пропилен, изобутилен, 2-метил 1-бутен, диизобутилен, 1-пентен, 2 этил-1-бутен и 2-метил-1-пентен, а в качестве галогенацетальдегида формулы (YI), например, трихлорацетальдегид (хлораль), трибромацетальдегид (бромаль) дихлорацетальдегид, дибромацетальдегид, монохлорацетальдегид, г-юнобромацет альдегид, дихлорбромацетальдегид и дибромхлорацетальдегид. Кислотным катализатором, который используется в реакции (реакции Принса) между ненасьлценным углеводородом формулы (Y) и галогенацетальдегидом формулы (YI), могут служить, например, кислоты Льюиса, такие, как хлористый алюминий, бромистый алюминий, эфират трехфтористого бора, хлористый цинк, хлорное железо,хлорное олово,бромное олово, четыреххлористый титан, треххлористый таллий, треххлористый висмут, четыреххлористый теллур, двуххлористый теллур, пятихлористый мышьяк и пятиокись фосфора, неорганические кислоты, такие, как соляная, серная и фосфорная, сульфоновые кислоты, в частности бензолсульфоновая, ортотолуолсульфоновая, метатолуолсульфоновая и паратолуолсульфоновая, и ионообменные смолы, содержащие сульфонильные или карбонильные группы. Из кислотных катализаторов предпочтительны хлористый алюминий, бромистый алюминий, хлористый цинк, хлорное олово, четыреххлористый титан,эфират трехфтористого бора, серная и фосфорная кислоты. Используемое количество кислотного катализатора изменяется в зависимости от его типа, однако обычно его берут в количестве 0,5-30, предпочтительно 3-15 мол,% (врасчете на галогенадетальдегид формулы .YI). Ненасыщенный углеводород формулы (Y) берут в относительно широких пределах: от 0,5 до 6,0 моль на 1 моль галогенацетальдегида формулы (YI), однако для полного превращения последнего в реакции следует ненасыщенный углеводород формулы (Y) использовать в количестве 1,0- 4,0 моль на 1 моль галогенацетальдегида формулы (YI). Реакцию обычнопроводят при температуре от (-20)с до комнатной температуры при атмосферном давлении, ноа если необходимо, реакцию можно
осуществлять под давлением при темnepaTSTse, превышающей комнатную.
Растворитель в этой реакции использовать не обязательно, можно, однако, применять растворитель, не принимающий участия в реакции, например петролейный эфир, н-пентан, н-гексан и нитрометан.
Когда по реакции Принса получают 1-галоген-4-алкен-2-ол как основной продукт реакции, этот ненасыщенный спирт превращают в 1-галоген-З-алкен-2-ол изомеризацией двойной связи путем нагревания в присутствии или в отсутствии катализатора.
Предпочтительные катализаторы изомеризации: ацетилацетонат хрома (+3), дисульфид молибдена, трехокись вольфрама, ацетилацетонат марганца (+3), треххлористый рутений, ацетилацетонат кобальта ( + 2) , гексааммиакат хлористого кобальта, ацетилацетонат родия (+3), треххлористый родий, треххлористый иридий, никел Ренея, ацетилацетонат никеля (+2), хлористый палладий, палладиевая чернь, 5%-ный палладий на угле и т.п.
Изомеризацию можно осуществлять при 60-250°С в зависимости от типа исходного 1-галоген-4-алкен-2-ола.
Катализатор используют в коли.честве 0,001-30 вес.%.
Предпочтительными сложными эфирам ортокарбоновой кислоты формулы (III) являются те, где R - водород, С -С -алкил, циклогексил, фенил, бензил, а именно 1,1,1-триметоксиэтан (метиловый эфир ортоуксусной кислоты), 1,1,1-триэтоксиэтаг; (этиловый эфир ортоуксусной кислоты), 1,1,1-трициклогексилоксиэтан, 1,1,1-три-н-бутилоксиэтан, 1,1,1-триэтоксипропан (этиловый эфир ортопропионовой кислоты), 1,1,1-триэтоксибутан, 1,1,1-триэтоксипентан, З-метил-1,1,1-триэтоксибутан, 3,7-диметил-1,1,1-триэтоксиоктан, 2-фенил-1,1,1-триэтоксиэтан, 2-(ортометилфенил)-1,1,1-триэтоксиэтан, 2-(метаметилфенил)-1,1,1-триэтоксиэтан, 2-циклогексил-1,1,1-триметоксиэтан, 1,1-диметокси-1-циклогексилоксиэтан, 1,1-диметокси-1-амилоксиэтан, З-метил-1,1,1-триэтоксибутен, 1,1,1-триэтокси-б-гептин, 1-бензилокси-1,1-диэтоксиэтан, 1,1-диэтокси-1-геранилоксиэтан 1,1,1-трибензилоксиэтан, 1,1,1-триоктилоксиэтан, 1,1-диэтокси-1-октилксиэтан, 1,1-диэтокси-1-фенилоксиэтан, 1,1-диэтокси-1-аллетронилоксиэтан, 1,1-диэтокси-1-пиретронилоксиэтан, 1,1-диэтокси-1-(3-феноксибензилокси)-этан, 1,1-диэтокси-1 -(5-бензил-З-фурилметилокси)-этан, 1,1-диэтокси-1-(тетрагидрофталимидометилокси)-этан и 1,1-диэтокси-1-(3-бензилпропаргилокси)-этан.
В качестве кислотных катализаторов, используемых в реакции взаимодействия спирта формулы (II) с эфиром формулы (III) , могут быть взяты низшие жирные кислоты., такие, как
o уксусная, прогшоновая, масляная, изомасляная, валериановая, циклогексилкарбоновая, малоновая, янтарная и адипиновая; ароматические карбоновые кислоты, такие, как бензойная
5 и метахлорбензойная кислоты, фенолы, в частности фенол, о-нитрофенол, м-нитрофенол; п-нитрофенол, о-крезол, м-крезол, п-крезол, о-ксиленол, п-ксиленол, 2,6-диметилфенол, 2,6-ди0-трет-бутилфенол, 2,4,б-три-втор.-бутилфенол,- 2,4, 6-три-трет . -бутилфенол, 4-метил-З, 5-ди-трет. -бутилфенол, гидрохинон; 4-метил-2j б-ди-трет.-бутилфенол ,2,5-ди-трет.-бутилгидрохинон, фенолы,о(.-нафтол, Ргнафтол; сульфоновые
5 кислоты, такие, как бензолсульфоновая и паратолуолсульфоновая кислота; неорганические кислоты, в частности соляная,серная,фосфорная и борная и кислоты Льюиса,такие,как хлористый
0 алюминий,хлористый цинк,хлорное железо и треххлористый бор,Предпочтительно использование жирной кислоты, имеющей от 2 до 6 атомов углерода. Кислотный катализатор берут в количестве
5 0,001-20, предпочтительно 0,01- 15 вес.% от исходного 1-галоген-З-алкен-2-ола формулы (II).
В качестве растворителя при предпочтительном варианте процесса ис0пользуют растворители, не принимающие участия в реакции, такие, как н-октан, толуол, о ксилол, м-ксилол, п-ксилол, ди-и-бутиловый эфир и тет- . ралин.
Если сложный эфир ортокарбоновой
5 кислоты берут в избытке по отношению к 1-галоген-алкен-2-олу формулы (II), то такой эфир может выполнять и функцию растворителя. Сложный эфир ортокарбоновой кислоты желательно
0 использовать в количестве 1,3-3 моль на 1 моль 1-галоген-3-алкен-2-ола.
Промежуточные продукты процесса по способу согласно изобретению - сложные эфиры -галоген-с -нена5сыщенной карбоновой кислоты формулы (IY) являются новыми соединениями; физико-химические характеристики этих эфиров представлены в табл.1.
Таблица 1












| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сложных эфиров дигалоидвинилциклопропан карбоновых кислот | 1975 |
|
SU664558A3 |
| Способ получения 1,1,1-тригалоген4-метил-3-пентен-2-олов | 1975 |
|
SU634660A3 |
| Способ получения низших С @ -С @ -алкиловых эфиров 2,2-диметил-3-(2,2-дихлорэтенил) циклопропанкарбоновой кислоты | 1991 |
|
SU1817771A3 |
| Способ получения дигалоидвиниловых соединений | 1980 |
|
SU961555A3 |
| Способ получения производных циклопропана | 1967 |
|
SU691076A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДИРОВАННЫХ СОЕДИНЕНИЙ | 1992 |
|
RU2117657C1 |
| Способ получения -метиловых сложныхэфиРОВ гидАНТОиНА | 1978 |
|
SU850003A3 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
| Способ получения сложных эфиров циклопропанкарбоновой кислоты | 1977 |
|
SU688122A3 |
| Способ получения эфиров 2,2-диметилциклопропанкарбоновых кислот | 1980 |
|
SU1053744A3 |

Этил-3,З-диметил-4,6,6-трихлор-5 гексеноат
Метил-3,З-диметил-4,6,6-трихлор-5-гексеноат
Этил-3, 3-димегил--4 ,6,6-трибром-5-гексеноат
Трет.-бутил-3,3-диметил-4,6,6-трибром-5-гексеноат
Этил-2,3,З-триметил-4,6,6-трихлор-5-гексеноат
н.-Пропил-2,3,3-триметил-4,6,6-трихлор-5-гексеноат
,3,З-триметил-4,6,6-трибром-5-гексеноат
Н.-ОКТИЛ-2, 3, 3-триметил-4,6,6-трибром-5-гексеноат
Этил-З-метил-4,6,6-трихлор-5-гексеноат
Бензил-З-метил-4,6,6-трихлор-5-гексеноат
Этил-З-метил-4,6,6-трибром-5-гексеноат
.Этил-3-метил-З-этил-4,6, 6-трибром-5-гёксеноат
Циклогексил-3-метил-3-этил-4,6,6-трибром-5-гексеноат
Этил-3-метил-3-фенил-4,6,6-трихлор-5-гексеноат
Метил-3-метил-3-фенил-4,6,6-трихлор-5-гексеноат
Этил-3-метил-З-бенэил-4,6,6-трихлор-5-гексеноат
Этил-2-циклогексил-3,3-диметил 4,6,6-трихлор-5-гексеноат
Этил-3,З-димэтил-4,6-дихлор-5-гексеноат
Метил-3,З-диметил-4-хлор-5-гексеноат
Бензил-3,З-диметил-4,6 , 6-трихлор-5 гексеноат
43,77(43,90) 5,47(5,53)
41,42(41,65) 5,36(5,05)
30,31 (29,52) 3,90(3,72)
32,08(33,13) 3,98(4,40)
46,20(45,94) 6,02(5,96
48,90(47,78) 6,85(6,35)
30,Ь2(31,39) 4,90(4,07)
40,76(40,42) 5,05(5,79)
42,38(41,65) .4,08(5,05)
52,99(52,28) 5,38(4,70),
28,04(27,51) 3,72(3,34)
31,45(31,39) 4,49(4,07)
38,38(37,92) 4,72(4,88)
53,92(53,68) 5,56(5,11)
53,12(52,28) 4,20(4,70)
55,08(54,96) 5,92(5,48)
55,08(54,02) 7,75(7,081
50,58(50,23) 6,55(6,741
56,99(56,69) 7,85(7,93)
53,65(53,68) 5,32(5,11)
н-Октил-3,3-диметил-4,6,6-трибром-5-гексеноат
м-Феноксибенэил-3,3-диметил-4,6,6-трихлор-5
-гексеноат
м-Феноксибензил-3,3-диметил-4,6,б-трибром-5-гексеноат
Пиретронил-3,3-диметил-4,6,6гтрихлор-5-гексеноат
Аллетронил-3,3 диметил-4,6,6-трихлор-5-гексеноат
5-Бенэил-З-фурилметил-3,З-диметил-4,6,6-трихлор-5-гексеноат
5-Бензил-З-фурилметил-З,3-диметил-4,6,6-трибром-5-гексеноат
3,4,5,6-Тетрагидрофталимидометил-3,З-диметил-4,6,6-трихлор-5-гексеноат
5-Феноксифурфурил-З,3-диметил-4,6,6-трихлор-5-гексеноат
5-Пропаргилф рифурил-3,3-диметил-4,6,6-трихлор-5-гексеноатРеакция получения целевого продук та протекает по следующей схеме I X В качестве основания в этой реакции, используют, например, гидроокиси щелочных металлов, такие, как гидроокиси натрия и калия, гидроокиси щелочноземельных металлов, в частности гидроокиси кальция и бария, алкоголя ты щелочных металлов, такие, как метил ат натрия, этилат натрия, метилат калия, этилат калия, н-пропилат натрия, н-бутилат натрия, изоамилат натрия, трет.-бутилат калия и изоамилат калия, азотсодержащие органические основания, например 1,5-диаза бицикло 13,4,0 нонен-5-(ДБН) , 1,5-диПродолжение табл. 1
40,В5(39,13) 5,05(5,54)
58,85(58,97) 4,51(4,95)
43,82(44,95) 4,05(3,77)
57,00(56,24) Ь,21 (5,71)
53,56(53,77) 5,85(5,57)
58,82(57,78) Ь,79(5,09
42,63(43,75) 3,56(3,86)
48,83(49,96) 5,57(4,93)
53,72(54,63) 4,98(4,58)
53,75(52,84) 5,36(4,71) азабицикло 5,4,0 ундецен-5(ДНУ), 1,4-диазабицикло 2,2,2 октан(ДАБЦО), 2-диметиламино-1-пирролин и 5-метил-1-азабицикло 3,3,0 октан, литийорганические соединения, такие, как н-бутиллитий, втор.-бутиллитий, диизопропиламинолитий и дициклогексиламинолитий, гидриды щелочных металлов, в частности гидриды натрия и калия, С1МИДЫ щелочных металлов, такие как амиды натрия и калия, и щелочные металлы, например металлический натрий и металлический калий. Обработку продукта, образующегося по реакции, таким основанием проводят при (-80)-(+100) С. Рекомендуется при использовании алкоголята щелочного металла, гидроокиси щелочного металла и азотсодержащего органического основания обработку проводят при 10-100°С, а в случае применения гидрида натрия, амида натрия и других, оснований - при (-70)( + 25)С. Если полученный таким образом сложный зфир замещенной циклопропанкарбоновой кислоты без его выделения из реакционной массы обработать водой в среде спирта,, смешивающегося с ней, то его можно перевести в соответствующую замещенную циклопропанкарбоновую кислоту.
Обработку сложного эфира формулы (IY) основанием, в процессе которой идет циклизация, лурие вести в среде растворителей, таких, как этиловый эфир, тетрагидрофуран, бензол, толуол, метанол, н-пропанол, изопропанол, н-бутанол, трет-бутанол, н-гексан, н-октан, хлорбензол, хлористый метилен, этилацетат, четыреххлористый углерод. Функцию растворителя может выполнять и азотсодержащее органическое основание, взятое в значительном избытке.
Уели в качестве растворителя используют спирт, то полученный сложный эфир замещенной циклопропанкарбоновой кислоты под действием этого спирта может быть переэтерифицирован.
Переэтерификацию можно осуществить и в случае применения реакционного производного сложного эфира циклопропанкарбоновой кислоты,а именно ангидрида карбоновой кислоты, галогенангидрида карбоновой кислоты, соли карбоновой кислоты со спиртом формулы (УН) , где к,К5Если в качестве растворителя берут спирт, как это показано в нижеследующих примерах, то часто образуюищйся сложный эфир замещенной циклопропанкарбоновой кислоты полностью или частично превращается в сложный эфир замещенной циклопропанкарбоновой кислоты соответствующего спирта, используемого в качестве растворителя, т.е. получающийся сложный эфир замещенной циклопропанкарбоновой кислоты подвергается сложноэфирному обмену в присутствии спирта, используемого в качестве растворителя.
В качестве спирта формулы (YII) применяют аллетролон, пиретролон, О-, м- или п-феноксибензиловый спирт, с -циано-м-феноксибензиловый спирт, 3-бензилбензиловый спирт, 5-феноксиФурфуриловый спирт, 5-Пропаргилф;урфуриловый спирт, 5-бензил-З-фурилметиловый спирт.
Реакцию сложноэфирного обмена между сложн|ам эфиром циклопропанкарбоновой кислоты и спиртом формулы (YII) можно осуществить в присутствии в качестве катализатора алкоголята Щ1Элочного металла с удалением из реакционной системы низщего спирта, полученного в процессе реакции. Если в этой реакции используют инертный расворитель, такой, как бензол, толуол, н-октан, н-гексан, то реакция протекает более благоприятно.
В реакцию переэтерификации вступает сложный эфир циклопропанкарбоново кислоты общей формулы (I), в которой группа R является метильной, этильно н-пропильной, изопропильной, н-бутильной или трет.-бутильной группой.
Если в этой переэтерификации используют циклопропанкарбоновую кислоту указанных выше эфиров, то взаимодействие со спиртом формулы (YII) проводят в безводных условиях.
Для установления в системе безводных условий реакцию осуществляют при нагревании в присутствии кислотного катализатора/ такого, как соляная или серная кислота, и рс1створителя, способного образовывать азеотропную смесь с водой, такого, как бензол, или толуол, для удаления из реакционной системы воды, образующейся в ходе реакции. Кроме того, можно использовать дегидратируюсшй агент, такой, как дициклогексилкарбодиимид.
Если в качестве реакционноспособного производного сложного эфира циклопропанкарбоновой кислоты формулы (I), подлежащего переэтерификации, применяют галогенангидрид циклопропанкарбоновой кислоты, а в качестве дегидрогалогенирующего агента третичный амин, такой, как пиридин или триэтиламин, то необходимый сложный эфир можно получить при более мягких условиях реакции.
Если для переэтерификации в качестве реакционноспособного производного сложного эфира циклопропанкарбоновой кислоты формулы (I) берут серебряную или свинцовую соль или соль щелочного металла циклопропанкарбоновой кислоты, которую подвергают взаимодействию с арилсульфонатом спирта формулы (YII) в качестве реакционноспособного производного спирта ,(YII), то peaцию можно эффективно осуществить в присутствии инертного растворителя, например бензола, ацетона, хлороформа, лигроина или диэтилового эфира, нагреванием при температуре кипения растворителя или при низкой температуре.
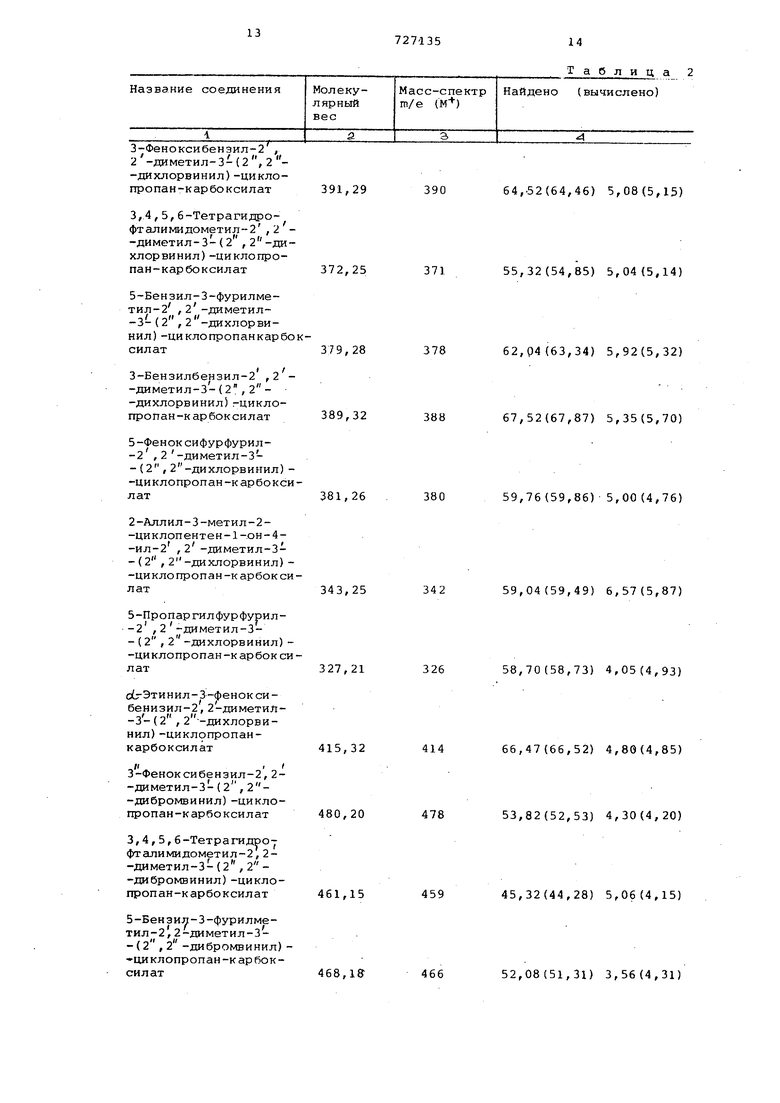
Физико-химические свойства сложных эфиров полученных в результате переэтерификации представлены в табл.2.
З-Феноксибензил-2 , 2-диметил-3-(2,2 -дихлорвинил)-циклопропан-карбоксилах
3,4,5,б-Тетрагидрофталимидометил-2 , 2 -диметил-3-(2,2 -дихлорвинил)-циклопропан- карбоксил ат
5-Бензил-З-фурилметил-2 ,2-диметил-3-(2,2 -дихлорвинил)-циклопропанкарбосилат
З-Бензилбензил-2 ,2 -диметил-3-{2,2 -дихлорвинил)гциклопропан-карбоксилат
5-Феноксифурфурил-2 ,2-диметил-3-(2,2 -дихлорвинил)-циклопропан-карбоксилат
2-Аллил-3-метил-2-циклопентен-1-он-4-ил-2 ,2 -диметил-3-(2,2 -дихлорвинил)-циклопропан-к арбок силат
5-Пропаргилфурфурил-2,2-диметил-3-(2,2 -дихлорвинил)-циклопропан-карбок силат
о(гЭтинил-3-феноксибенизил-2, 2-диметил-3- ( 2 , 2 --дихлорвинил) -циклопропанкарбоксилат
II, I
З-Феноксибензил-2,2-диметил-3-(2,2 -дибромвинил)-циклопропан-карбоксилат
3,4,5,6-Тетрагидроу фтсШимидометил-2, 2-диметил-3-(2,2 -дибромвинил)-циклопропан -карбоксил ат
5-Бензил-З-фурилметил-2 2-диметил-З- (2 , 2 -дибромвинил)-циклопропан-карбоксилат
Т а б л и Ц а 2
64,52(64,46) 5,08(5,15)
390
55,32(54,85) 5,04(5,14)
371
62,р4(63,34) 5,92(5,32)
378
67,52(67,87) 5,35(5,70)
388
59,76(59,86) 5,00 (4,76)
380
59,04(59,49) 6,57(5,87)
342
58,70(58,73) 4,05(4,93)
326
66,47(66,52) 4,80(4,85)
414
53,82(52,53) 4,30(4,20)
478
45,32(44,28) 5,06(4,15)
459
52,08(51,31) 3,56(4,31)
466
З-Феноксибензил-2,2-диметил-3-(2 -монохлорвинил) -циклопропан-карбоксилат
3 -Феноксибензил-1 , 2 , 2 -триметил-3-(2 ,2-дихлорвинил)-циклопропан-карбоксилат
г
3-Фенокси6енэил-2-метил-2-фенил-З-(2,2 -дихлорвинил)-циклопропан-карбоксилах
5-Бензил-З-фурилметил-2, 2-диметил-З винилциклопропан-к арбок силат
сС-Ииано-3-феноксибензиловый эфир 2, 2-диметил-3-(2,2 -дихлорвинил)-циклопропанкарбоновой кислоты В приводимых ниже примерах под частями имеют ввиду весовые части. Пример 1.0,1ч изомасяяно кислоты добавляют к смеси 10,2ч 1,1,1-трихлор-4-метил-3-пентен-2-ол и 16,2 ч. этилового эфира ортоуксус ной кислоты и смесь перемешивают в течение 2 ч при 130-145°С и 2 ч при 145-155с в атмосфере азота. Спирт, образовавшийся в качестве побочного продукта в течение реакци непрерывно отгоняют из реакционной системы. По з.авершении реакции жидкую реакционную смесь немедленно перегоняют при пониженном давлении и получают 11,1 ч. маслянистой фрак ции с т.кип. 83-84 0/0,28 мм рт.ст Выход 81% в расчете на исходный 1,1,1-трихлор-4-метил-3-пентен-2-ол Свойства полученного продукта Оледующие, ИК-спектр (жидкая пленка) : 1610 см-МС С) , 1730 см-МС 0) . ЯМР-спектр (100 МГц) сРссе ТМС: 1,08 (синглет, 6Н), 1,20 (триплет, J 7 Г, ЗН) , 2,14 (дублет, J 14 Гц, 1Н), 2,42 (дублет, J , 14 Гц, 1Н) , 4,01 (квартет, J 2Н) , 4,83 (дублет, J 11 Гц, 1Н) 5,95 (дублет J 11 Гц, 1Н) . Найдено, %: С 43,77; Н 5,47. Вычислено, %: С 43,90; Н 5,53. По вышеприведенным свойствам пол ченное соединение идентифицировано как этиловый эфир 3,З-диметил-4,6,6 -трихлор-5-гексеновой кислоты. 2,7 ч. полученного соединения растворяют в 25 ч. безводно1Х1 беняо
Продолжение таблицы 2
70,32(70,68) 6,82(5,93)
66,08(65,19) 5,32(5,47)
68,32(68,88) 4,05(4,89)
77,30(77,39) 7,29(7,14)
310
63,44(63,47) 4,90(4,60) и к раствору добавляют 1,9 ч. трет,-бутилата натрия, смесь перемешивают при комнатной температуре в течение 1 ч. Жидкую реакционную смесь вылиBcUOT в ледяную воду и экстрагируют эфиром. Эфир и бензол удаляют из органического слоя перегонкой и остаток перегоняют при пониженном давлении для получения 2,1 ч. целевого . этилового эфира 2,2-диметил-З-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты (выход 89%). Температура кипения образовавшегося соединения 102-103 С/2,0 ммрт.ст. ИК-спектр (жидкая пленка): 1620 см () , 1730 см-(). ЯМР-спектр (100 МГц) в ССе. (ГТМС: 1,15 (синглет), 1,20 (триплет, J 7 Гц), 1,22 (синглет), 9Н; 1,47 (дублет, J 5 Гц, 1Н); 2,10 (двойной дублет, J 5,8 Гц, 1Н), 4,03 (квартет, J 7 Гц, 2Н), 5,52 (дублет,- J 8 Гц, 1Н) . Найдено, %: С 50,51; Н 6,24. Вычислено, %: С 50,65; Н 5,95. Масс-спектр, м/е () : 236, 238, 240. Пример 2. По примеру 1, используя 0,4 ч. фенола вместо иэомасляной кислоты, получают 9,7 ч. маслянистой фракции с т.кип. 83-84 С/ /О,28 мм рт.ст. 0,5 ч. полученного маслянистого вещества - этилового эфира 3,3-диметил-4,6,6-трихлор-5-гексеновой кислоты растворяют в 10 ч. безводного тетрагидрофурана, к раствору добавляют 0,4 ч. порошкообразной гидроокиси калия и смесь перемешивают при 45-so С в течение 1,5 ч. Жидку реакционную смесь немедленно отфильт ровывают с использованием целита для удаления твердых продуктов. Из фильтрата перегонкой удаляют тетрагидрофуран. При анализе маслянистого вещества с помощью газовой хроматографией установлено, что получен целе вой этиловый эфир 2,2-диметил-З-(2 , 2-дихлорвинил)-циклопропанкарбоновой кислоты с выходом . Пример 3. 1,4 ч. металличес кого натрия растворяют в 50 ч. безводного метанола и к раствору прибав ляют 5,5 ч. этилового эфира 3,3-диметил-4,6,б-трихлор-5-гексеновой кис лоты, полученного, как в примере 1„ Смесь перемешивают в течение 2 ч при температуре кипения метанола. Жидкую реакционную смесь постепенно охлажда ют, затем к ней добавляют 20 ч. воды и массу перемешивают при 45-50с в течение 2 ч. Далее при пониженном давлении перегоняют метанол, остаток нейтрализуют соляной кислотой и экст рагируют диэтиловым эфиром. Эфирный экстракт сушат и отгоняют Эфир для получения 3,7 ч, кристаллов 2,2-диме тил-3-(2,2 -дихлорвинил)-циклопропанкарбоновой кислоты. Выход 88% в расчете на этиловый эфир 3,3-диметил -4,6,б-трихлоргексеновой кислоты. Соотношение цис- и трансизомеров в продукте, определенное по ЯМР-спектру составляет 28: 72. При фракционированной перекристаллизации этих крисТсшлов из н-гексана их можно разделит на цисизомер с т .nii,88-89°С и трансизомер с т.пл. 94-96°С. По результатам ЯМР-спектрального анализа (60 МГц чистый трансизомер имеет следующие химсдвиги в CCe dTMC: 1,18 (синглет ЗН), 1,30 (синглет, ЗН), 1,53 (дублет J 15,5 Гц, 1Н), 2,20 (двойной дублет, J 8 Гц и 5,5 Гц, 1Н), 5,58 (дублет, J 8 Гц, 1Н). Пример 4.1,1ч. гидроокиси Ксшия растворяют в 30 ч. безводного метанола и к раствору прибавляют 2,7 ч. этилового эфира 3,3-диметил-4,6,б-трихлор-5-гексеновой кислоты, полученного, как в примере 2. Смесь перемешивают в течение 2 ч при температуре кипения метанола. Жидкую реакционную массу разбавляют примерно со 100 ч. диэтилового эфира и промывают примерно 25 ч. воды. Водный слой экстрагирую-: трижды диэтиловым эфиром.. Извлеченный эфирный экстракт перегоняют для удаления из него низкокипящих веществ и извлекают 1,0 ч. (выход 45%) метиловог эфира 2,2-диметил-3-(2,2-дихлорвинил) -циклопропанкарбоновой кислоты с нижеуказанными свойствами. Соотношение цис:транс-изомеров в продукте, определенное с помощью газовой хрома тографии, составляет 35:65. Температура кипения эфира 67-68С/ /0,2 мм рт.ст, ЯМР-спектр (60 МГц) в СС(4 (/ ТМС: 1,12-1,25 (мультиплет, бН), 1,422,25 (мультиплет, 2Н) , 3,60 (синглет. ЗН), 5,57 (дублет 3 8,5 Гц) Ь,23 (дублет, 3 8,5 Гц) 1Н. При нейтрсшизации вышеуказанного водного слоя соляной кислотой и экстракции диэтиловым эфиром получают 0,8 ч. 2,2-диметил-З-(2,2-дихлорвинил) -циклопропанкарбоновой кислоты. Выход 38%. При анализе продукта по примеру 4, установлено, что соотношение цис и транс изомеров составляет 21-:79. . Пример 5. О,4 ч, металлического натрия растиоряют в 30 ч. безводного метанола и к раствору прибав1Тяют 2,7 ч. этилового эфира 3,3-диметил-4,6,б-трихлор-5-гексеновой кислоты, полученного, как в примере 3. Смесь перемешивают в течение 2 ч при температуре кипения метанола. Жидкую реакционную смесь охлаждают, ледяной водой и нейтрализуют насыпанным раствором соляной кислоты в метаноле.Выпадающие в осадок твердые продукты удаляют фильтрованием, а фильтрат концентрируют до тех пор, пока объем не уменьшится до 1/10. Концентрат разбавляют диэтиловым эфиром, промывают водой и высушивают. Затем перегонкой удаляют растворитель и остаток перегоняют при пониженном давлении для получен ия 2,0 ч. метилового эфира 2,2-диметил-З-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты с т.кип. 68-70 С/ /0,2 мм рт.ст. Выход 90%. Соотношение цис- и транс-изомеров в продукте, определенное с помощью газовой хро saтoгpaфии, составляет 22:78, Пример б. О,4 ч, металлического натрия растворяют в 20 ч. безводного этанола и к раствору прибавляют 2,7 ч. этилового эфира 3,3-диметил-4,6,б-трихлор-5-гексеновой кислоты. Смесь перемешивают в течение 2 ч. при температуре кипения этанола. Жидкую реакционную смесь разбавляют примерно 50 ч. диэтилового эфира и нейтрализуют безводным газообразным хлористым водородом. Выпадающие в осадок кристаллы хлористого натрия удаляют фильтрованием и из фильтрата перегонкой удаляют низкокипящие вещества. Остаток перегоняют при пониженном давлении-для получения 2,1 ч. этилового эфира 2, 2-диметил-З-(2 , 2 -дихлорвинил)-циклопропанкарбоновой кислоты с т.кип, 72-73 С/0,3 мм рт.ст. Выход 87%. Свойства продукта совпадают со свойствами этилового эфира 2,2-диметил-З- (2,2-дихлорвинил)-циклопропанкарбоновой кислоты, описанного в примере 1.
Пример 7. 0,03 ч, изомасляной кислоты прибавляют к смеси 4,,1 ч 1,1,1-трихлор-4-метил-3-пентен-2-ола и 7,0 ч. этилового эфира ортопропионовой кислоты, смесь перемешивают при 130-145 С в течение 4 ч в атмосфере азота. Этиловый спирт, образующийся в качестве побочного продукта, непрерывно перегоняют из реакционной смеси в ходе реакции. По завершении реакции жидкую реакционную смесь перегоняют при пониженном давлении для получения 4,9 ч, фракции маслянистого вещества с т.кип. 92-99 С/ /0,25 мм рт.ст. При газовой хроматографии продукта установлено, что он состоит из двух веществ.
Продукт подвергают колоночной 5фоматографии на силикагеле, используя бензол в качестве элюирующей жидкости, и получают 1,6 ч. соединения, т.кип. 104-106 С/О,4 мм рт.ст.
ИК-спектр (жидкая пленка): 1610 см- () , 1730 см (С-0) .
ЯМР-спектр (100 МГц) в ССедсГтМС: 1,20 (триплет, J 7 Гц) и 0,9-1,3 (12Н) , 2,4-2,7 (мультиплет, 1Н) , 4,01 (квартет, J 7 Гц) и 4,03 (квартет, J 7 Гц) 2Н, 4,63 (дублет J 11Гц) и 4,78 (дублет, J 11 Гц) 1Н, 5,96 (дублет, J 11 Гц) и Ь,97 (дублет, J 11Гц) 1Н.
Найдено, %: С 46,20; Н 6,02.
Вычислено,%: С 45,94; Н 5,96:
По вышеприведенным свойствам полученный продукт идентифицирован как эфир 2,3,З-триметил-4,6,6-трихлор-5-гексеновой кислоты.
1,0 ч. этого соединения растворяют в 5 ч. безводного бензола и к раствору прибавляют 0,67 ч. трет-бутилата натрия, смесь перемешивают при температуре кипения бензола в течение 30 мин. Жидкую реакционную смесь выливают в ледяную воду и экстрагируют диэтиловым эфиром, а затем из органического слоя отгоняют эфир и бензол для получения 0,72 ч. этилового эфира 1,2,2-трИметил-3-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты в виде маслянистого продукта. Выход 82%.
ЯМР-спектр (60 МГц) в ССЕдсУтМС 1,04 (синглет) , 1,13 (синглет) , 1,, 18 (синглет) , 1,23 (триплет, J 7 Гц), 12 Н, 2,25 (дублет, J Гц, 1Н), 4,08 (квартет, J 7 Гц, 2Н), 5,57 (дублет,. J 8 Гц, 1Н) .
0,72 ч. вышеуказанного сложного эфира перемешивают при 40-50 С в течение 3 ч в присутствии 3,26 ч, 10%-ного водного раствора гидроокиси натрия и метилового спирта для осуществления гидролиза сложного эфира
и получения 0,60 ч. 1,2,2-триметил-3- (2 ,2 -дихлорвинил) -циклопропанкарбоновой кислоты.
Температура плавления полученного соединения 137-138 С.
ЯМР-спектр (60 МГц) в СС€4С ТМС 1,08 (синглет), 1,22 (синглет) и 1,25 (синглет), 9Н, 2,33 (дублет, J 8 Гц, 1Н), 5,56 (дублет, J 8 Гц, 1Н) .
ИК-спектр (таблетка КВг): 1685 см () ..
0,60 ч. вышеуказанной карбоновой кислоты перемешивают с 0,38 ч. хлористого тионила при ВО С в течение 30 мин в бензоле в качестве растворителя для получения хлорангидрида 1,2,2-триметил-З-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты. Хлорангидрид кислоты перемешивают с 0,53 ч. 3-феноксибензилового спирта в присутствии пиридина при комнатной температуре в бензоле в качестве растворителя и получают 1,02 ч. 3-феноксибензилового эфира l ,2,2 -триметил-3-(2,2 -дихлорвинил)-циклопропанкарбоновой кислоты.
ЯМР-спектр (60 МГц) полученного соединения в ССб ТМС: 0,94 (син- . глет, ЗН), 1,05 (синглет, ЗН), 1,12 и 1,13 (синглеты, ЗН), 2,29 (дублет, J 8 Гц, 1Н), 4,99 (синглет, 2Н), 5,54 (дублет, J 8 Гц, 1Н), 6,7-7,4 (мультиплет, 9Н) .
П р и м ер 8. Реакцией сложноэфирного обмена промежуточного продукта, полученного в примере 1 (этиловый эфир 3,З-диметил-4,6,б-трихлор-5-гексеновой кислоты) получают 5-бензил-З-фурилметиловый (IX), м-феноксибензиловый (X) и аллетрониловый (XI) эфиры 3,З-диметил-4,6,6-трихлор-5-гексеновой кислоты.
Полученный таким образом сложный эфир в количестве, указанном в табл.3, растворяют в 30 ч. безводног бензола и к раствору прибавляют соответствующее количество трех-бутилата натрия или тре1;-бутилата калия и . смесь перемешивают в течение 20 мин при температуре кипения бензола, дкую реакционную смесь выливают в ледяную воду и быстро экстрагируют диэтиловым эфиром. Из органического слоя отгоняют эфир и бензол, а остаток подвергают хроматографии на колонке для получения соответствующего сложного эфира 2,2-диметил-З-(2 ,2 -дихлорвинил)-циклопропанкарбоновой кислоты, а именно 5-бензил-З-фурилме тилового (XII), м-феноксибензилового (XIII) или сшлетронилового эфира (XIV). Пример 9. 0,3 ч. изомасляной кислоты прибавляют к смеси 33,7 ч, 1,1,1 -ТЕ 1ором-4 -метил-З-пентен-2-ола и 48,7 ч. этилового эфира ортоуксусной кислоты и смесь перемешивают в атмосфере азота в течение 2 ч при ISO-I S C и еще 2ч при 145-155С. Этиловый спирт, образующийся в качестве побочного продукта в процессе реакции, непрерывно отгоняют из реак ционной системы в ходе реакции. Жидкую реакционную смесь немедленно перегоняют в вакууме для получения фракции маслянистого вещества с т.кип. 125-127с/0,25 ммрт„ст. Таким образом получают 28,3 ч. этилового эфира 3,З-диметил-4,6,б-трибром -5-гексеновой кислоты. Выход 70% в расчете на 1,1,1-трибром-4-метил-З-пентен-2-ол. Физические свойства продукта следующие: ИК-спектр (метод жидкой пленки): 1600 см () , 1730 см- () . ЯМР-спектр (60 1-;Гц) в ССвдСГ ТКС; 1,12 (синглет, бН), 1,22 (триплет, J 7 Гц, ЗН), 2,17 (дублет, J 15 Гц, 1Н), 2,49 (дублет, J 15 1Н), 4,08 (квартет, J 7 Гц, 2Н), 4,93 (дублет, J 11,Гц, 1Н), б,бб (дублет, J 11 Гц, 1Н). 4,1 ч. полученного этилового эфи ра 3,З-диметил-4,б,б-трибром-5-гексеновой кислоты растворяют в 35 ч. безводного бензола и к раствору при бавляют 1,9 ч. трет-бутилата натрия смесь перемешивают в течение 1 ч при температуре кипения бензола. Жидкую реакционную смесь- выливают в ледяную воду и экстрагируют диэтиловым эфиром, затем из органическог слоя отгоняют эфир и бензол. Остато перегоняют в вакууме и получает 3,2 этилового эфира 2,2-диметил 3-(2 ,2 -дибромвинил)-циклопропанкарбоновой кислоты с т.кип. 92-94 0/0,5 мм рт. Выход 98%. ИК-спектр (метод жидкой пленки): 1600 см- () , 1730 см- () . ЯМР-спектр (100 МГц) в ССбд f ТМС 1,19 (синглет); 1,23 (триплет, J 7 Гц), 1,26 (синглет, 9Н) , 1,53 (дублет, J 5 Гц, 1Н), 2,08 (двойной дублет, J 5 Гц и 8 Гц, 1Н);
Таб.лицаЗ 4,03 (квартет, J 7 Гц, 2Н), 6,04 (дублет, J 8 Гц, 1Н). П р и м е р 10. Аналогично примеру 1, но используя 1,1-дихлор-4 -метил-З-пентен-2-ол вместо 1,1,1-трихлор-4-;у1етил-3-пентен-2-ола, по(пучают этиловый эфир 3,3-диметил-4,6-дихлор-5-гексеновоЙ кислоты. Образовавшийся сложный эфир обрабатывают трет.-бутилатом натрия при температуре кипения бензола и получают этиловый эфир 2,2-диметил-З-(2-хлорвинил)-циклопропанкарбоновой кислоты с выходом 57% в расчете на исходный спирт. Структура сложного эфира подтверждается анализом ИК- и ЯМР-спектров. ИК-спектр (метод жидкой пленки); 1730 см- (СО) . Пример 11, Аналогично примеру 9, используя 1,1,1-трибром-4 метил-3-гептен-2-ол вместо 1,1,1-Tpti5pOM-4-метил-З-пентен-2-ола, получают этиловый эфир 3-метил-З-пропил 4,6,6-трибром-5-гексеновой кислоты. Сложный эфир обрабатывают трет,-бутилатом натрия при температуре кипения бензола и получают этиловый эфир 2-метил-2-пропил-3-(2,2-дибромвинил)-циклопропанкарбоновой кислоты с выходом 38% в расчете на исходный спирт. Структура сложного эфира подтверждается анализом ЯМР-спектра. Пример 12. 0,1 г изобутиловой кислоты добавляют К смеси г 1,1,1-трихлор-4-метил-3-пентен-2-ола и 12,0 г метил-о-ацетата и смесь перемешивают в течение 2 ч в атмосфере азота при 90-120 0 и еще в течение 2 ч при 120-160°С. Метанол, получающийся в качестве полупродукта в течение реакции непрерывно отгоняют из системы. По окончании реакции образовавшуюся жидкую реакционную смесь перегоняют в вакууме и получают 11,7 г маслоподобной фракции с т. кип. 80-82с/ /0,3 мм рт.ст. Выход 90%,, считая на исходный 1,1,1-трихлор-4-метил-3-пентен-2-ол. ИК-спектр (метод жидкой пленки): 1615 см-(, 1735 см- () .
ямр-спектр (60 МГц) в
1,15 (S) бН, 2,22 (d,y 15 HZ), IH 2,55 {d,y 15 HZ), IH, 3,68 (S) 3H, 4,93 (d,y 11 HZ), IH, 6,10 (d,y 11 HZ) IH,
Найдено, %: С 41,45; И 5,33.
Вычислено, %; С 41,65 И 5,05.
Полученное соединение идентифицировано по вышеприведенным свойствам как метил-3,З-диметил-4,б,6-трихлор-5-гексеноат.
Повторяют методику примера 6, применяя вместо 2,7 г этил-3,3-;алметил-4,6,6-трихлор-5-гексеноата 2,6 г метил-3,З-диметил-4,6,6-трихлор-5-гексеноата. Получают 2,1 г метил-2, 2-диметил-З- (2 , 2 -дихл(эрвинил)-циклопропанкарбоксилата. Выход 94%. Свойства продукта совпадают со свойствами метил-2,2-ди метил-3-(2,2-дихлорвинил)-циклопропанкарбоксилата, описанного в при1мер е 9..
Пример13. 0,04 г и.зобутиловой кислоты прибавляют к см«эс:и 5,1 г 1,1,1-трихлор-4-метил-3-пентен-2-ола и 20,7 г н-октил-о-ацетата и смесь перемешивают при 140-170с в течение 24 ч в атмосфере азота. Затем жидкую реакционную смесь подвергают колоночной хроматографии на силикагеле с использованием бензола как элюента. Получают 1,9 г соедданеВИЯ с нижеследующими свойствами,,. Выход 21%, считая на исходный 1,, 1,1-трихлор-4-метил-3-пентен-2-ол.
ЯМР-спектр {60 МГц) в ССе4СТМС: 0,85 (t,j 6HZ) ЗН; (S) 6Н 1,29 (b,S), 12 Н 2,16 (d,j 15 HZ) IH, 2,49 {d,j 15 HZ) IH, 4,02 (t,j 6 HZ) 2H, 4,90 (d,j 11 HZ) IH, 6,07 (d,j 11 HZ) IH.
Найдено, %: С 53,45; Н 7,65.
Вычислено,%: С 53,72; Н 7,61.
Полученный продукт представляет собой н-октил-3,З-диметил-4,6,6 трихлор-5-гексеноат.
1 г н-октил-3,З-диметил-4,6,6-тризслор-5-гексеноата растворяют в 15 г сухого бензола и прибавляют к этому раствору 0,63 г трет.-бутилата калия, после чего смесь кипятят при перемешивании с обратным холодильником в течение 60 мин. Жидкую реакционную смесь выливают в ледяную воду и немедленно экстрагируют Д1аэтиловым эфиром. Эфир и бензол отгоняют из органического слоя и остаток подвергают колоночной хроматографии. Получают при этом 0,50 г к-октлл-2, 2-диметил-З-(2 , 2 -дихлорвин:ил) -циклопропанкарбоксилата. Выход 56%, считая на н-октил-3,З-диметил-4,6,6-трихлор-5-гексеноат.
Найдено, %: С 59,27; Н 8,36.
Вычислено, %: С 59,81; Н 8,16.
Пример 14. Применяя 17,4 г бензил-о-ацетата по примеру 13, получают 1,2-бекзил-З,3-диметил-4,6,6-трихлор-5-гексеноат. Выход 14%, считая на исходный 1,1,1-1рихлор-4-метил-3-пентен-2-(5л.
ЯМР-спектр (60 МГц)(3ссе4- ТМС: 1,05 (S) бН, 2,17 (d,j 15 HZ), IH, g 2,53 (d,j 15 HZ) IH, 4,86 (d,j 11 HZ) IH, 5,05 (S) 2H, 6,03 (d,S 11 HZ), 7,33 (S) 5H.
Найдено, %: С 53,25; Н 5,92. Вычислено, %: С 53,57; Н 5,10. Q 0,50 г полученного таким образом 1, 2-бензил-3, З-диметил-4 ,6,6-трих.пор-5-гексеноата растворяют в 10 г сухого бензола и к раствору добавляют 0,33 г трет.-бутилата калия. Аналогично примеру 13 получают 0,27 г бен5 зил-2,2-диметил-3-(2,2-дихлорвинил)-циклопропанкарбоксилата. Выход 60%, считая на 1,2-бензил-З,3-диметил-4,6,6-трихлор-5-гексеноат.
Найдено, %: С 60,25; Н 5,49. 0Вычислено, %: С 60,22; Н 5,39.
Пример 15. Аналогично примеру 13, но используя 15,8 г 1,1-диэтокси-1-(З-феноксибензилокси)-этана вместо 20,7 г н-октил-о-адета5 та, получают 0,8 г 3-феноксибензил-З,3 -диметил-4 , б ,б -трихлор-5-гексеноата. Выход 8%, считая на исходный 1,1,1-трихлор-4-метил-3-пентен-2-ол.
ЯМР-спектр (60 МГц) 6 CCt ТМС
1,03 (S) бН, 2,18 (d,j 15 HZ) IH, 2,52 (d,j 15 HZ) IH, 4,87 (d,j 11 HZ) IH, 5,02 (S) 2H, 6,02 (d,j 11 HZ) IH, 6,,50 (m) 9H.
5Найдено, %: С 58,85; Н 4,51.
Вычислено,% С 58,97; Н 4,95. 0,43 г полученного таким образом 3-феноксибен;зил-3, 3-диметил-4 ,б , 6 -трихлор-5-гексеноата растворяют
0 в 10 г сухого бензола и к раствору прибавляют 0,22 г трет.-бутилата калия. Тем же способом, что и в примере 13, получают 0,25 г 3-феноксибензил-2,2-диметил-З -(2,2 е -дихлорвинил)-циклопропанкарбоксилата. Выход 64%, считая на 3-феноксибензил-з,З-диметил-4 ,б ,6 -трихлор-5-гексеноат. Свойства продукта совпадают со свойствами 3-феноксибенчитт-5 - 5 -ттим тип-: - С 2 . 2 -ттихлоозил-2 ,2 -диметил-З-(2,2 -дихлорвинил)-циклопропанкарбоксилата, описанного в примере 8.
Пример 16. Аналогично, примеру 1, но используя 13,0 г 1,1,1-трихлор-4,6,6-триметил-З-гептен5 2-ола вместо 10,2 г 1,1,1-трихлор-4-метил-3-пентен-2-ола из примера 1 получают этил-3-метил-З-неопентил-4,6,6-трихлор-5-гексеноат. Полученный таким способом сложный эфир обрабаQ гывают трет.-бутилатом натрия в бензоле при кипячении с обратным холодильником, в результате чего получают 10,0 г этил-2-метил-2-неопентил-3-(2 , 2-дихлорвинил)-циклопропан5 карбоксилата. Выход 68%, считая -на
исходный 1,1,1-трихлор-4,6,6-триметил-З-гептен-2-ол.
ЯМР-спектр (100 МГц) dccE TMC: 0,88, 0,42 (each S) 9Н, 1,03-2,28 (m ЮН, 3,97 (d,j 7 HZ), 3,99 (d,j 7 HZ) 2H, 5,46 (d,j 8 HZ), 6,16 (d,j 8 HZ) IH.
Найдено, %: С 57,30; Н 7,72.
Вычислено, %: С 57,34; Н 7,56,
5,86 г этил-2-метил-2-неопентил-3-(2,2 -дихлорвинил)-циклопропанкарбоксилата гидролизуют и обрабатывают тионилхлооидом, чтобы получить соответствующий хлорид 2-метил-2-неопентил-3-(2,2-дихлорвинил) -циклопропанкарбоновой кислоты. Полученное соединение перемешивают с 4,80 г 3-феноксибензилового спирта в бензоле-растворителе в присутствии пиридина и получают 5,40 г 3-феноксибензил-2-метил-2-неопентил-з- (2, 2 -дихлорвинил)-циклопропанкарбоксилата. Выход 60%, считая на этил-2-метил-2-неопентил-3-(2 ,2 -дихлорвинил) -циклопропанкарбоксилат.
ЯМР-спектр (100 МГц) (J ССб. TMS: 0,84, 0,89 (each S) 9Н, 1,10-2,30 (т) 7Н, 4,85-4,97 (т) 2Н, 5,40 (d,j 8 HZ) 6,14 (d,j 8 HZ) IH, 6,63 7,26 (m) 9H.
Найдено, %: С 67,29; Н 6,56.
Вычислено,%: С 67,12; Н 6,31.
Пример 17. К смеси 20,3 г 1,1.1-трихлор-4-метил-3-пентен-2-ола 16,2 г этилового эфира ортоуксусной кислоты и ЗОг толуола добавляют ОД г изомасляной кислоты.Смесь в атмосфер азота сначала перемешивают при 100°С затем температуру смеси в течение 2 ч поввзшают до 130°С и в течение последующих 2 ч- до 160 С. Смесь дополнительно перемешивают в течение 1,5 ч при вышеуказанной температуре. Образующийся в качестве побочного продукта этиловый эфир непрерывно отгоняют вместе с толуолом из реакционной системы. После завершения реакции реакционную смесь непосредственно перегоняют в вакууме в результате чего получают 16,6 г этилового эфлра 3,З-диметил-4,6,6-трихлор-5-гексеновой кислоты с т.кип. 83-84с/0,28 мм рт . ст . Выход продукта 57%.
Пример 18. К смеск 10,2 г 1,1,1-тоихлор-4-метил-3-пентен-2-ола и 16,2 г этилового эфира ортоуксусно кислоты добавляют 0,1 г изомасляной кислоты. Смесь в атмосфере азота перемешивают в течение 2 ч при 130- и затем температуру ее постепенно повышают до 200°С в течение последующих 2 ч. Образующийся в качестве побочного продукта этиловый спирт непрерывно отгоняют из реакционной системы. После завершения реакции, реакционную смесь подвергаю прямой перегонке в вакууме. В результате получают 8,3 г маслянистой
фракции с т.кип. 83-84°С/0,28 мм рт.ст. Полученное соединение идентифицировано как этиловый эфир 3,3-диметил-4,6,6-трихлор-5-гексеновой кислоты. Выход 61%.
5Пример 19. 2,7г этилового
эфира 3,З-диметил-4,6,6-трихлор-5-гексеновой кислоты растворяют в 25 г безводного тетрагидрофурана и таким образом приготовленный раствор охлажQ дают до -78° С в холодильной ацетоновой бане с сухим льдом. На этой стадии к указанному раствору прикапывают 5,1 г 15%-ного раствора н-бутиллития в н-гексане и затем температуру полученной реакционной массы посте5 пенно повышают до комнатной. Далее к реакционной смеси добавляют 20 г Iacыщeннoгo водного раствора хлористого аммония, после чего приливают 100 мл воды. Реакционную массу экстра0 гируют диэтиловым эфиром и эфирный слой сушат над безводным сульфатб 1 магния. Затем перегонкой отгоняют низкокипящие вещества. Остаток перегоняют в вакууме, получая 1,2 г этило-
5 вого эфира 2,2-диметил-3-(2 ,2-дихлорвинил)-циклопропанкарбоновой кислоты. Выход продукта 51%,т.кип. 102103°С/2 мм рт.ст.
Пример 20. В 25 г толуола
Q растворяют 2,7 г этилового эфира 3,3т -диметил-4,6,6-трихлор-5-гексеновой . кислоты, к раствору добавляют 1,2 г трет.-бутияата натрия и смесь перемешивают при 100 С в течение 30 мин. Реакционный раствор естественно охлаждают, затем вьшивают в Ледяную воду и экстрагируют серным эфиром. Эфирный слой сушат над безводным сульфатом магния и затем из него перегонкой в вакууме отделяют низкокипящие соединения. В результате получают 2,0 г этилового эфира 2,2-диметил-3-(2 ,2 -дихлорвинил)-циклопропанкарбоновой кислоты. Выход продукта 84%, т.кип, 102-ЮЗ С/
/ 2 мм рт . ст .
Пример 21. 2,1 г 2,2-диметил-3-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты, сйнтезированной в соответствии с методикой примера 3, перемешивают при кипячении с обратным холодильником в течение 8 ч с 4,8 г тионилхлорида и 5 г бензола. Приготовленную таким способом реакционную смесь перегоняют в вакууме с целью удаления низкокипящих веществ и извлекают хлорангидрид 2,2-диметил-З-(2 ,2 -дихлорвинил)-циклопропанкарбоновой кислоты. К смеси полученного хлорангидрида,
2,3 г о6-циано-3-феноксибензилового спирта и 25 г бензола добавляют 1,6 г пиридина и смесь перемешивают в течение 12 ч при комнатной температуре. Приготовленную реакционную
массу разбавляют серным эфиром, про
Авторы
Даты
1980-04-05—Публикация
1975-10-02—Подача