Изобретение относится к сельскому хозяйству, в частности к способам размножения растений.
Известен способ получения безвирусных клонов винограда при помощи термотерапии (Т. Д.Вердеревская, В.Г.Маринеску, "Вирусные и микоплазменные заболевания плодовых культур винограда", Кишинев, "Штиинца", 1985 г., с. 276).
Недостатком способa является то, что применение термотерапии в ряде случаев приводит к отставанию в росте и деформации органов меристемных растений. Этот прием может также увеличить латентные и термостойкие вирусные инфекции.
Известен способ культивирования меристематических верхушек в асептических условиях на искусственных питательных средах (Г.С.Муромцев, Р.Г.Бутенко и др., "Основы сельскохозяйственной биотехнологии", М., 1990 г., стр. 225) - прототип. Наибольшее число здоровых растений получается в этом случае при использовании меристематических эксплантов предельно малого размера (0,075-0,1 мм).
Недостатком способа является то, что меристематические экспланты таких размеров характеризуются наименьшей способностью к регенерации. Процесс морфогенеза, заканчивающийся получением целого, нормального пробирочного растения идет в этом случае наиболее трудно.
Для устранения указанных недостатков с целью повышения регенерационной способности меристем в способе, включающем вычленение меристематических эксплантов в асептических условиях, высадку их на стерильную питательную среду в пробирки, вычлененные меристематические экспланты обрабатывают электромагнитным СВЧ-полем с частотой 37,5 ГГц и напряженностью 20 мВт в течение 65-75 мин в комплексе с узкополосным лазерным лучом.
Такое выполнение способа позволяет путем воздействия на высаженные на питательную среду меристемы волнами электромагнитного излучения низкой интенсивности в комплексе с узкополосным лазерным лучом ускорить прохождение ими фаз развития, увеличить размерные характеристики, снизить гибель из-за некроза тканей и в конечном итоге обеспечить повышение регенерационной способности. Лучи СВЧ-поля, проникая в клетку, модифицируют мембраны, производят их перестройку и подвергают разрыву двойные связи в непредельных жирных кислотах липидов. Этот разрыв сопровождается образованием в липидах свободных радикалов. В зависимости от уровня радикалов в объектах наблюдается стимулирующее, угнетающее воздействие или стационарная фаза. Стимуляция происходит в тот момент, когда достигается определенный уровень свободных радикалов (в основном их начальных форм). При этом происходит изменение проницаемости клеточных мембран, усиливает приток питательных веществ, воды и кислорода и активизируются ферментные системы обмена веществ. Использование лазера в комплексной обработке усиливает стимулирующий эффект и ускоряет прохождение фаз развития.
Способ осуществляется следующим образом. Для получения эксплантов срезают растущие побеги диаметром 2-4 мм с глазками, удаляют листья, разрезают поперек на отрезки 1,0-1,5 см и вдоль, чтобы отрезок стебля с глазком (сегмент) имел плоское основание. Затем осуществляют поверхностную стерилизацию.
Техника стерилизации заключается в следующем. Сегменты тщательно моют теплой водой с мылом и промывают дистиллированной водой, опускают на несколько секунд в спирт, а затем в 10%-ный раствор гипохлорида кальция. Через 30 мин сегменты переносят в стакан со стерильной дистиллированной водой, выдерживают 10 мин, а затем меняют воду еще 2 раза, выдерживая в каждой порции 15-20 мин.
Экспланты вычленяют в асептических условиях в бокс-комнате в ламинарном боксе "Роботрон" под бинокулярным микроскопом МБС-9 при 25-кратном увеличении с помощью препаровальных и дисцизионных игл. Экспланты представляют собой меристематический купол с одним-двумя примордиальными листьями размером 0,17-0,25 мм или без листовых примордиев размером 0,075 - 0,1 мм.
Сразу после вычленения экспланты высаживают на твердую стерильную питательную среду в короткие пробирки (70х80 мм) и закрывают стерильными пробками. Основной средой является питательная среда Мурасиге и Скуга, модифицированная следующим образом: 3/4 макроэлементов, микроэлементы и хелат железа по Мурасиге или Скугу; 170 мг/л NaH2PO4, мезоинозит - 100 мг/л, сахароза - 30 г/л, БА -1 мг/л рH-5,1. Приготовление среды осуществляют по общепринятой методике.
Затем приступают к облучению пробирок с меристематическими эксплантами электромагнитным СВЧ-полем в комплексе с узкополосным лазерным лучом. Для облучения используют генератор высокочастотных сигналов с диапазоном частот 37,5 - 53,57 ГГц. Мощность СВЧ-сигнала 20 мВт. Точность определения длины волны не менее 0,01 мм. Лазер применяют узкополосный с тонким лучом. 5 пробирок размещают на расстоянии 65 мм от генератора высокочастотных сигналов и 95 мм от лазера и облучают в течение 65-75 мин.
После облучения культивирование осуществляют в культуральной комнате при освещенности 2,0-3,0 тыс. лк, фотопериоде 16 ч, температуре 25-27oC, влажности воздуха - 70-75%.
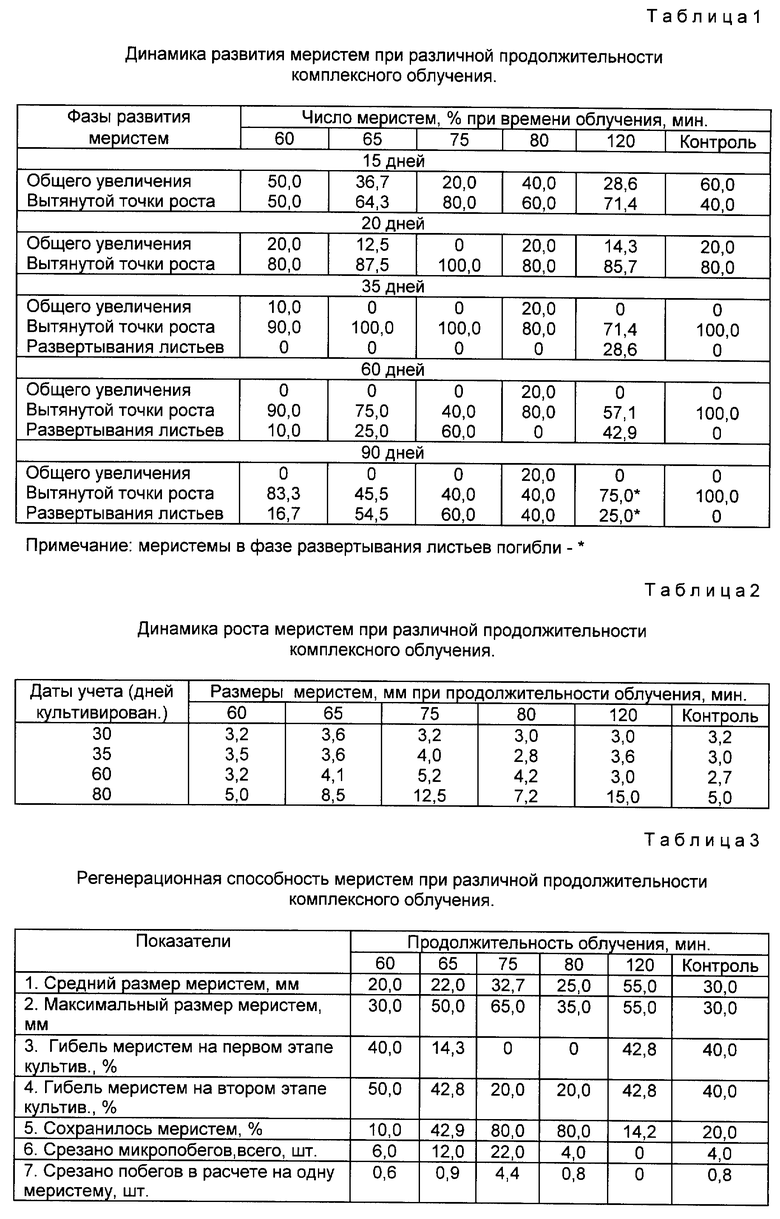
Наблюдение за выделенными и облученными эксплантами показали, что комплексное воздействие СВЧ-лучей и лазера повышает интенсивность их развития. Ускоряется прохождение фазы общего увеличения, переход к фазе вытянутой точки роста, к фазе развертывания листьев. Разница в скорости развития облученных меристем по сравнению с необлученными видна уже через 15-20 дней и сохраняется до 90 дней культивирования. В течение всего периода культивирования более интенсивное развитие наблюдается при продолжительности облучения 120, 75 и 65 минут. При 60 и 80 мин интенсивность прохождения фаз развития несколько замедлялась (табл. 1).
Облучение меристем оказало влияние и на их ростовые характеристики. Более интенсивное развитие сопровождалось изменением размерных характеристик меристем (табл. 2). Размерные характеристики облученных меристем во всех вариантах были выше контрольных. Выделились варианты с продолжительность облучения 75, 65 и 120 мин. Последовательное увеличение меристем в течение всего периода культивирования отмечено при продолжительности облучения 75 и 65 мин, через 80 дней культивирования резко вырос размер меристем в варианте с облучением в течение 120 мин.
Увеличившиеся в размере меристемы в фазе развертывания листьев и вытянутой точки роста асептически переносят на жидкую питательную среду Мурасиге и Скуга в колбы объемом 150 мл на мостики из фильтровальной бумаги. Для пролиферации (новообразования) узлов и побегов в питательной среде увеличивают содержание цитокинина БА до 2 мг/л.
Колбы снова помещают в культуральную комнату на аппарат для встряхивания. Объем среды в колбе 8-10 мл, через каждые две недели меристем и образующиеся из них конгломераты узлов и побегов пересаживают на свежую питательную среду.
В процессе культивирования из меристем образовались конгломераты узлов и побегов. Их размеры как средние по варианту, так и максимальные также зависели от продолжительности облучения. Наиболее крупные конгломераты были при продолжительности облучения 120 и 75 мин (табл. 3).
Комплексное облучение также оказало положительное влияние на сохранность меристем. Как на первом, так и на втором этапе культивирования резко снизилась гибель меристем из-за отсутствия развития и некроза тканей при продолжительности облучения 75-80 мин. А в варианте с продолжительностью облучения 120 мин, где наблюдался интенсивный рост меристем и конгломератов, отмечена почти полная их гибель.
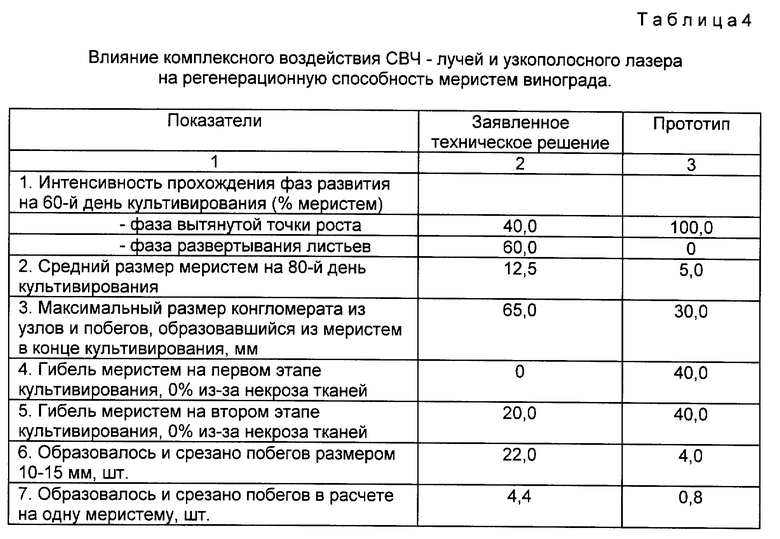
Регенерационная способность меристем характеризуется в основном количеством образовавшихся побегов размером 10-25 мм, которые можно срезать для ускорения. Наибольшее число побегов образовалось и срезано для ускорения при облучении в течение 75 и 65 мин (табл. 4).
В пересчете на одну выделенную меристему это составило 0,9 и 4,4 побега. В сравнении с контролем регенерационная способность меристем при воздействии СВЧ-лучами и лазером возросла в 5,5 раза.
Таким образом, воздействие электромагнитного излучения низкой интенсивности в комплексе с узкополосным лазером на высаженные на питательную среду меристемы способствует ускоренному прохождению ими фаз развития, увеличению размерных характеристик, снижает гибель из-за некроза тканей, обеспечивает повышение регенерационной способности, а в конечном итоге создание безвирусного посадочного материала винограда.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕГЕНЕРАЦИИ МЕРИСТЕМ | 2003 |
|
RU2265319C2 |
| СПОСОБ МИКРОКЛОНАЛЬНОГО РАЗМНОЖЕНИЯ ВИНОГРАДА "ИН ВИТРО" | 1993 |
|
RU2041609C1 |
| СПОСОБ ФОРМИРОВАНИЯ КОЛЛЕКЦИИ И ДЛИТЕЛЬНОГО ДЕПОНИРОВАНИЯ ВИНОГРАДА IN VITRO | 2021 |
|
RU2764104C1 |
| СПОСОБ ДЛИТЕЛЬНОГО СОХРАНЕНИЯ IN VITRO РАСТЕНИЙ ВИНОГРАДА | 1995 |
|
RU2110172C1 |
| СПОСОБ КЛОНАЛЬНОГО МИКРОРАЗМНОЖЕНИЯ СМОРОДИНЫ И АНТИОКСИДАНТ ДЛЯ КЛОНАЛЬНОГО МИКРОРАЗМНОЖЕНИЯ СМОРОДИНЫ | 1994 |
|
RU2080060C1 |
| СПОСОБ РАЗМНОЖЕНИЯ ВИНОГРАДА IN VITRO | 1995 |
|
RU2077192C1 |
| Способ размножения винограда IN VIтRо | 1987 |
|
SU1601117A1 |
| СПОСОБ ПОЛУЧЕНИЯ АСЕПТИЧЕСКОЙ КУЛЬТУРЫ IN VITRO ДРЕВЕСНЫХ РАСТЕНИЙ ЛИСТВЕННЫХ ПОРОД СРЕДНЕГО И СТАРШЕГО КЛАССОВ ВОЗРАСТА | 2024 |
|
RU2834363C1 |
| СПОСОБ КЛОНАЛЬНОГО МИКРОРАЗМНОЖЕНИЯ В КУЛЬТУРЕ IN VITRO СОРТА МИСКАНТУСА "СОРАНОВСКИЙ" | 2024 |
|
RU2829652C1 |
| СПОСОБ УСКОРЕННОГО СОЗДАНИЯ БЕЗВИРУСНОЙ РОСТКОВОЙ КУЛЬТУРЫ IN VITRO НОВЫХ СОРТОВ КАРТОФЕЛЯ | 2002 |
|
RU2242118C2 |
Изобретение может быть использовано в сельском хозяйстве и касается способа размножения растений. Вычлененный в асептических условиях эксплант высаживают на стерильную питательную среду в пробирку. Осуществляют культивирование 65 - 75 мин под воздействием электромагнитного СВЧ-поля с частотой 37,5 ГГц и напряженностью 20 мВт. Одновременно воздействуют узкополостным лазерным лучом. В результате такой обработки регенерационная способность меристем возросла в 5,5 раза. 4 табл.
Способ регенерации меристем, включающий вычленение меристематических эксплантов в асептических условиях, высадку их на стерильную питательную среду в пробирки и культивирование, отличающийся тем, что пробирка с меристематическими эксплантами при культивировании в течение 65 - 75 мин обрабатывают электромагнитным СВЧ-полем с частотой 37,5 ГГц и напряженностью 20 мВт в комплексе с узкополосным лазерным лучом.
| Вердеревская Т.Д., Маринеску В.Г | |||
| Вирусные и микоплазменные заболевания плодовых культур винограда.- Кишинев, Штиинца, 1985, с | |||
| СПОСОБ СОСТАВЛЕНИЯ ЗВУКОВОЙ ЗАПИСИ | 1921 |
|
SU276A1 |
| Муромцев Г.С., Бутенко Р.Г | |||
| и др | |||
| Основы сельскохозяйственной биотехнологии.- М., 1990, с | |||
| Синхронизирующее устройство для аппарата, служащего для передачи изображений на расстояние | 1920 |
|
SU225A1 |
Авторы
Даты
1998-10-27—Публикация
1995-03-29—Подача