Изобретение относится к медицине, а именно к способам получения биологически активных веществ, обладающих иммунорегулирующими свойствами, и может найти применение в медицине, ветеринарии, а также в экспериментальной биохимии.
В практической медицине широко известны в качестве регуляторов иммунных процессов тимусные экстракты, в частности тимозин фракции 5 (Goldstein A.L., Guna A., Latz M.M., Hardy H.A., White A.), тималин и его растворы (М.Д. Машковский "Лекарственные средства" М. Медицина, ч. 2, с. 171, 1986; CH, N 659586). Эти экстракты состоят из комплекса веществ полипептидной природы и получение их из природных источников ограничено сложностью производства, малым выходом активных веществ и значительной вариабельностью их физико-химических характеристик и биологических свойств. Кроме того, из-за присутствия в природных препаратах тимуса балластных компонентов при их использовании у больных иногда возникают побочные явления. Последнее обстоятельство явилось стимулом для создания синтетических пептидов. В настоящее время осуществлен синтез ряда пептидов, обладающих иммунорегуляторными свойствами: SU N 1582393, EP N 230052, US N 5008246, US N 5013723. Каждый из полученных синтетических пептидов с ограниченным комплексом необходимых свойств обладает высокой активностью, низкой токсичностью, отсутствием побочных эффектов, которые определяют их возможное применение в медицине.
В настоящем изобретении предлагается для использования в экспериментальных и лечебных целях новый пептид формулы
H - Ile - Glu - Trp - OH
Пептид и композиция на его основе могут применяться в качестве средства, обладающего способностью влиять на регенерацию кроветворной и иммунной систем.
Согласно изобретению заявляемый пептид используется в качестве биологически активного компонента для приготовления фармацевтической композиции. Фармацевтическая композиция включает эффективное количество пептида, а также носитель, пригодный для использования в сочетании с этим биологически активным компонентом. Композиция может быть составлена в любой форме, пригодной для орального, назального и наружного применения, а также в виде инъекций.
Как правило, в составе композиции содержится от 0,001 до 0,1 мас.% (предпочтительно от 0,01 до 0,05 мас.%) пептида. Это количество зависит также от способа введения композиции в организм. Фармацевтическую композицию получают путем смешивания носителя и пептида при температуре 40 - 70oC, состав сохраняет стабильность в растворе в течение 24 ч (3 лет) при температуре 70oC (20oC) соответственно.
В композиции для инъекций в качестве растворителя может быть использован любой фармацевтически приемлемый растворитель, включая дистиллированную воду, физиологический, солевой, буферный растворы. Содержание пептида может составлять от 0,001 до 0,1 мас.%.
Приготовление раствора для инъекций осуществляют традиционно объемно-весовым методом. При этом к определенному весовому количеству порошка пептида добавляют растворитель до получения необходимого объема раствора. Далее раствор фильтруют через стерилизующие фильтры, разливают во флаконы или ампулы. Полученный раствор представляет собой бесцветную прозрачную жидкость, не содержит химических или иных примесей, стабилен.
Твердая форма для орального применения может быть в виде таблеток, порошков, капсул, мазей, кремов, может содержать среду для активного компонента и другие добавки, включая красители, ароматизаторы и т.д. Содержание пептида может составлять от 0,01 до 1 мас.% и обычно подбирается в зависимости от вида композиции для орального применения.
Способ иллюстрируется следующим примером.
Пример 1. H-Ile-Glu-Trp-OH.
1. Получение Boc-Ile-OPFP.
Смесь 46,0 г (0,2 моль) Boc-Ile-OH и 40,5 г (0,22 моль) пентафторфенола в 100 мл этилацетата, охлаждают до -5oC и добавляют 45,3 г (0,22 моль) N, N-дициклогексилкарбодиимида. Реакционную смесь перемешивают 3 ч при комнатной температуре, дициклогексилмочевину отфильтровывают, растворители упаривают в вакууме, остаток кристаллизуют в смеси этилацетат-гексан. Выпавший осадок отфильтровывают. Выход 71,3 г (90%).
2. Получение Boc-Ile-Glu-Trp-OH.
19,8 г (0,05 моль) Boc-Ile-OРFP растворяют в 100 мл диметилформамида и при перемешивании добавляют раствор 20 г (0,06 моль) Glu-Trp и 5,0 г (0,06 моль) NaHCO в воде. Раствор перемешивают в течение 20 ч при комнатной температуре, затем упаривают растворители в вакууме. К остатку добавляют 200 мл этилацетата и 200 мл 2%-ного раствора серной кислоты, перемешивают. Органический слой промывают раствором серной кислоты (2•100 мл), насыщенным раствором NaCl до pH 7, сушат над безводным сульфатом натрия, растворитель отгоняют в вакууме. Остаток кристаллизуют в системе этилацетат-гексан, осадок отфильтровывают и сушат в вакууме. Выход 20,5 г (75%),
3. Получение H-Ile-Glu-Trp-OH.
20,5 г BOC-H-Ile-Glu-Trp-OH растворяют в 150 мл муравьиной кислоты, перемешивают 3,5 ч при 45oC и растворитель упаривают в вакууме. К остатку добавляют 200 мл воды и упаривают в вакууме еще раз. Остаток заливают смесью 300 мл изопропанола, 200 мл эфира и выдерживают 10 часов. Осадок фильтруют и сушат в вакууме. Выход 15,3 г (75%).
Очистку пептида проводят с помощью обращенно-фазовой хроматографии в системе ацетонитрил-0,1%-ный раствор трифторуксусной кислоты. Выход 13 г (85%).
В результате изучения физико-химических свойств пептида были получены следующие его характеристики.
Первичная структура - H-Ile-Glu-Trp-OH.
Брутто-формула - C24H30N4O4.
Молекулярный вес - 446,5 Da.
Внешний вид - белый с желтоватым оттенком или серый порошок.
Растворитель - легко растворим в воде, умеренно в спирте, практически нерастворим в хлороформе.
У. Ф. - спектр в области 250-300 мм имеет максимум (280±2) мм, плечо (287±2) мм.
Биологическая активность нового пептида H-Ile-Glu-Trp-OH
а) Исследование радиотерапевтических свойств пептида и влияния на популяцию кроветворных клеток-предшественников.
Пример 2.
В этом примере описана возможность замены акцессорных T-клеток пептидом в процессах регуляции гемопоэза.
В опытах использовано 2500 мышей (CBA•C57BL)F1, самок в возрасте 2 месяцев и весом около 20 г.
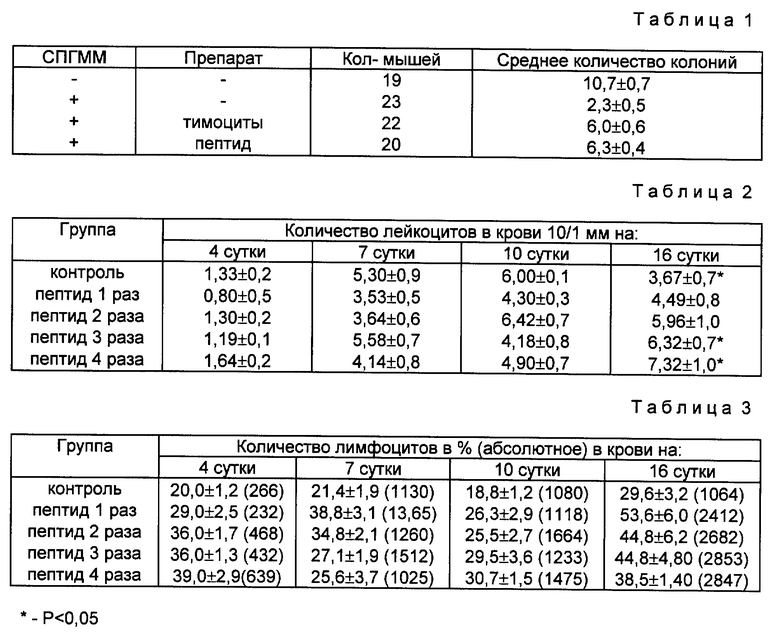
Известна тесная связь T-клеток с кроветворными предшественникам (Poverenny A. , Semina o., Semenets T. et al. Exp. Hematal, 1980, 8. 1221; Monette F., Wassa W. Exp. Hematel. 1981, 9, 1011). Показано, что в процессах формирования колоний на селезенках облученных мышей наряду с колониеобразующими единицами селезенки (KOE-C) принимают участие и тимоциты, осуществляющие контроль пролиферации кроветворных клеток-предшественников. Это установлено в тест-системе, суть которой состоит в избирательном удалении акцессорных T-клеток из костного мозга с помощью кроличьей сыворотки против головного мозга мышей (СПГММ) и замена их другими факторами. Суспензию костного мозга инкубируют с СПГММ в следующих соотношениях: 0,1 мл клеток (2•107) 0,1 мл сыворотки, 0,1 мл физиологического раствора. После инкубации в течение 1 ч при 37oC, отмывки центрифугированием и ресуспендирования клетки костного мозга вводят летально облученным мышам. При учете колоний на селезенке регистрируется существенное уменьшение их количества по сравнению с контролем. Восстановление колониеобразования достигается путем дополнительного введения мышам тимоцитов наряду с обработанным СПГММ клетками костного мозга, что служит доказательством участия T-клеток в колониеобразовании.
Вместо тимоцитов по представленной выше схеме мыши получают инъекцию 10 мкг/кг пептида за 30 мин до введения обработанной СПГММ костно-мозговой суспензии. Для инъекции используют физиологический раствор, содержащий 0,001 мас.% пептида. В табл. 1 представлены результаты.
Показано, что пептид в значительной степени способствует повышению выхода колоний и практически действует на уровне T-клеток
Пример 3.
В этом примере описана способность пептида снимать цитостатический эффект облучения (4 Гр) на стволовые и зрелые клетки гемопоэтической системы по тесту восстановления количества кариоцитов и размеров популяции KOE-C костном мозге бедренной кости и лейкоцитов крови (1 мм3).
Применяют 2 схемы лечения мышей, облученных дозой в 4 Гр, пептидом, вводимым в дозе 10 мкг/кг внутримышечно. Для инъекции используют физиологический раствор, содержащий 0,005 мас.% пептида.
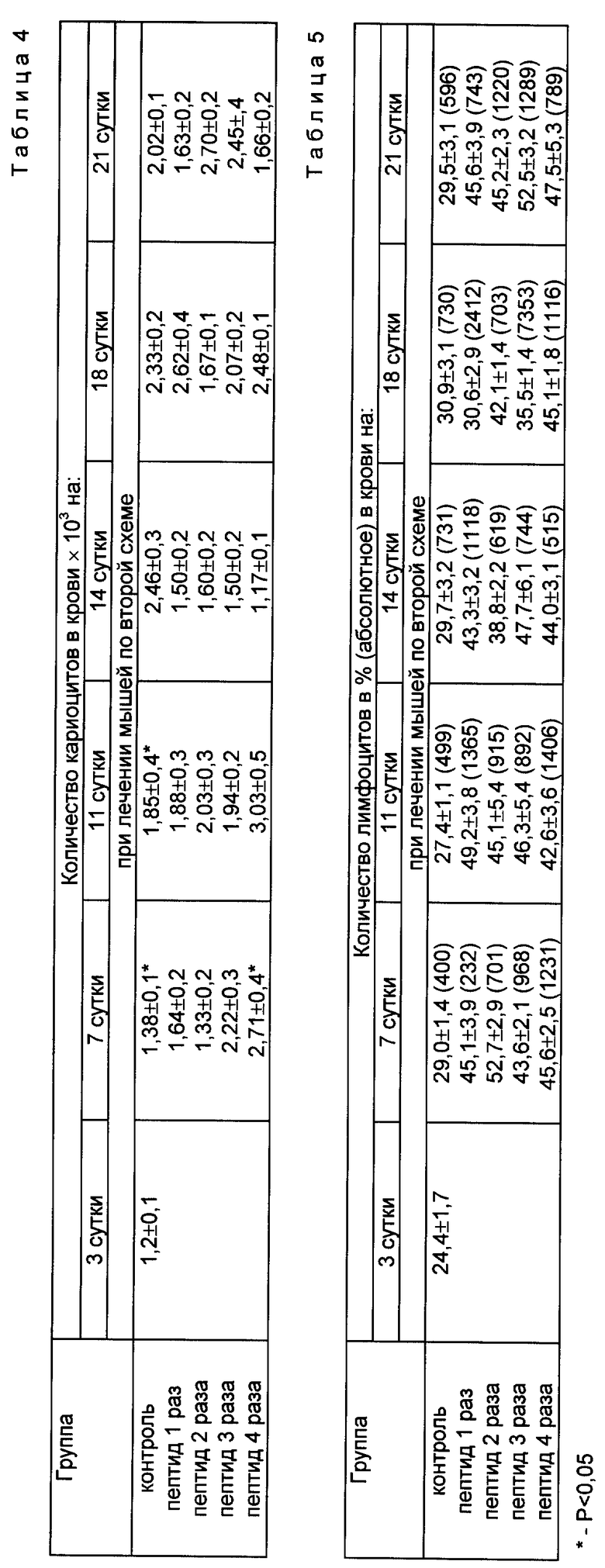
а) По первой схеме лечения мышей пептид начинают вводить сразу после облучения ежесуточно. Были сформированы группы мышей: контрольная - облученные дозой в 4 Гр, и опытные - облученные дозой 4 Гр и получавшие пептид 1, 2, 3 и 4 раза ежесуточно. Через 4 ч после последней инъекции пептида, а также 7, 10, 16 сутки после облучения осуществляют забор крови. Определяют общее количество лейкоцитов крови, процентное содержание лимфоцитов среди них и количество лейкоцитов и размеры популяции KOE-C в костном мозге бедренной кости (на 4,8 и 14 сутки). Результаты представлены в табл. 2 и 3, фиг. 1.
Как видно из табл. 2 вплоть до 16 суток после облучения ни одной группе опытных мышей количество лейкоцитов в крови не превышает контрольный уровень. На 16 сутки их число во всех группах пролеченных мышей достоверно выше, чем в контроле.
Из табл. 3 видно, что процентное содержание лимфоцитов в течение всего срока наблюдения у пролеченных мышей больше, чем в контроле, а нарастание их абсолютного количества происходит стремительнее. У мышей, получивших пептид более чем 1 раз, количество лимфоцитов в крови в период наибольшего опустошения пула зрелых клеток (4 сутки после облучения) значительно превосходит их содержание в контроле.
Пример 4.
В этом примере описана возможность стимуляции процесса регенерации популяции KOE-C косного мозга мышей, подвергнутым облучению дозой в 4 Гр, путем внутримышечного введения пептида.
Для инъекции используют физиологический раствор, содержащий 0,001 мас.% пептида.
С этой целью отбирают из каждой группы не менее 5 мышей, забивают, извлекают костный мозг, готовят суспензию клеток и вводят ее летально облученным мышам. Через 9 суток по количеству выросших колоний на селезенках рассчитывают содержание KOE-C у доноров, облученных дозой в 4 Гр и получивших пептид.
Результаты представлены на фиг. 1. Отмечено, что при внутримышечном введении пептида количество KOE-C в костном мозге облученных мышей, начиная с 4 суток, неуклонно растет, значительно опережая этот показатель у контрольных мышей. Особенно эффективно действует пептид, введенный дважды.
Этот пуп, пройдя весь путь деления и созревания от стволовой клетки до зрелой функционирующей, длящийся примерно 8 дней, выходит зрелыми клетками в кровь, что отмечается как увеличение числа лейкоцитов на 16 сутки. Следовательно, лечение облученных мышей пептидом, начатое сразу после воздействия радиации, то есть до наступления опустошения костного мозга, способствует увеличению выживаемости уцелевших кроветворных клеток-предшественников или скорости их пролиферации.
б) По второй схеме лечения пептид начинают вводить на 3 сутки после воздействия ионизирующей радиации, в момент максимального опустошения пула зрелых лейкоцитов и костного мозга. Группы мышей сформированы таким же образом, как и в первой схеме лечения. При этом отбор крови осуществляют через 4 ч после последней инъекции, т.е. на 6 сутки, а также на 11, 14, 18, 21 сутки.
В табл. 4 и 5 приведены данные по содержанию лейкоцитов и лимфоцитов в крови (на 1 мм3) мышей, пролеченных по второй схеме.
Показано, что количество лейкоцитов во все сроки наблюдения одного порядка в опытной и контрольной группах, исключение составляют мыши, получившие пептид 4 раза: на 6 и 11 сутки (фаза абортивного подъема) число лейкоцитов у них выше, чем у контрольных мышей. Обращает на себя внимание факт значительного снижения уровня этих клеток на 14 сутки и особенно в группе, получившей 4 инъекции пептида. По-видимому, это объясняется тем, что под влиянием пептида выжившие после облучения KOE-C быстрее проходят путь созревания до функционирующих клеток, быстрее истощается их пул и к 14 суткам поступление в кровь зрелых клеток из этого пула прекращается, тогда как у контрольных мышей еще наблюдается абортивный подъем количества лейкоцитов. В течение всего срока наблюдения доля лимфоцитов среди лейкоцитов крови значительно выше у мышей, пролеченных пептидом, чем у контрольных. Абсолютное же количество лимфоцитов в крови мышей опытных групп выше, чем у контрольных во время абортивного подъема (6-11 сутки после облучения) и на 21 сутки в период восстановления, в момент второго опустошения (14-18 сутки) количество лимфоцитов в опытных и контрольной группах равны.
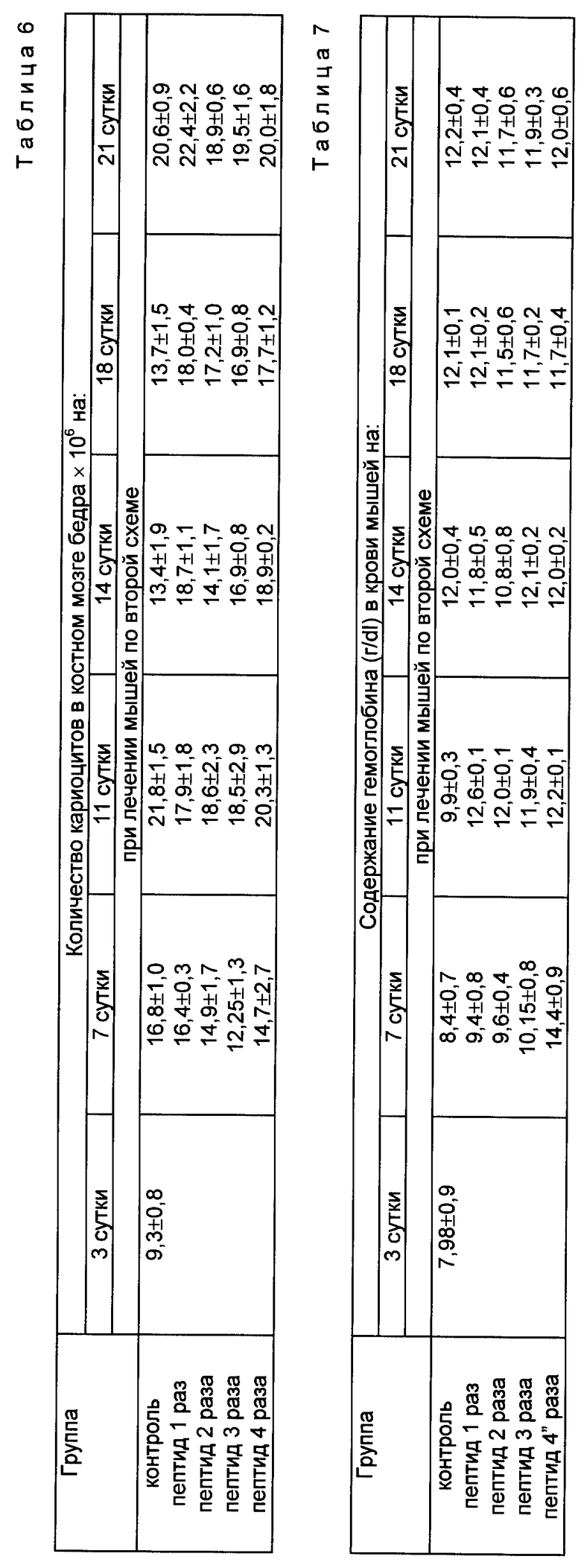
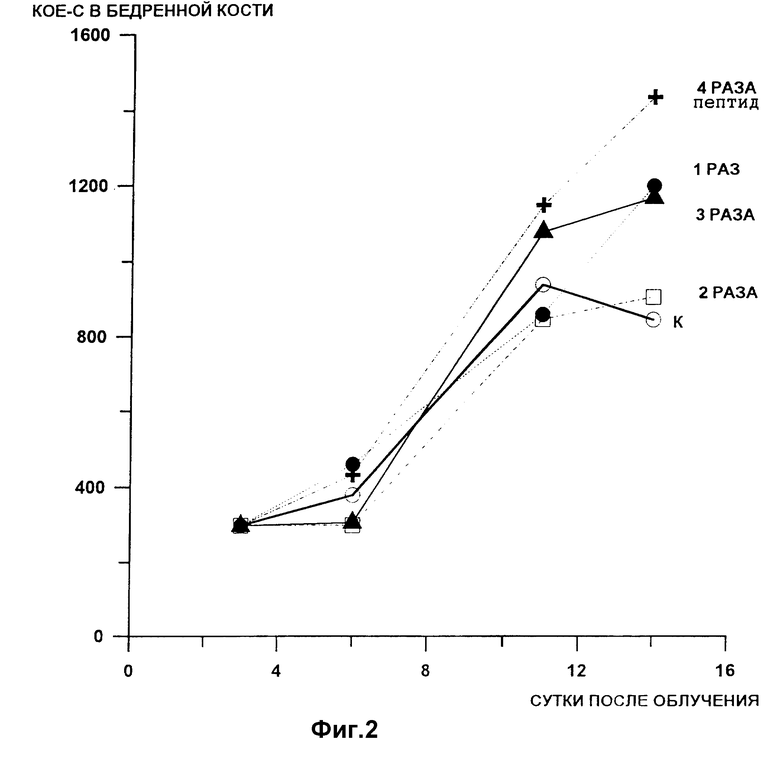
Результаты, представленные в табл. 6, отражают процесс регенерации костного мозга у контрольных и пролеченных пептидом по второй схеме облученных мышей (4 Гр). До 11 суток этот процесс идет с одинаковой интенсивностью во всех группах животных, с 14 по 18 сутки регистрируется значительное повышение количества лейкоцитов в костном мозге опытных мышей.
Влияние пептида на размеры популяции KOE-C костного мозга положительно сказывается на 11 сутки в группах мышей, получавших пептид в течение 3 и 4 дней, а к 14 суткам во всех группах количество KOE-C больше, чем в контроле. Результаты приведены на фиг. 2.
Изучено было также влияние пептида на эритропоэз. Количество эритроцитов в опытной и контрольной группах не отличается, уровень гемоглобина у пролеченных мышей восстанавливается интенсивнее и к 11 суткам он достигает нормы, тогда как у контрольных к 14 суткам.
В табл. 7 представлены результаты.
Особенно эффективным в данном случае является четырехразовый курс лечения.
Таким образом, результаты экспериментов позволяют заключить, что наиболее эффективным лечением облученных мышей пептидом, начатым на 3 день после воздействия ионизирующей радиации, то есть в момент максимального опустошения костного мозга и пула зрелых клеток крови, является четырехдневный курс лечения.
Пример 5.
В этом примере описаны иммуностимулирующие свойства пептида.
В этой серии опытов была определена иммуностимулирующая активность пептида при вторичных иммунодефицитных состояниях, в частности, индуцированных облучением, а также у интактных мышей.
Опыты проводят на мышах (CBA • C57BL)F1 самцах и самках в возрасте примерно 2,5 месяца и весом около 20 г. Облучение проводят на аппарате "Луч-1" гамма-лучами. Иммунологическую активность определяют по методу Jerne (количество антителообразующих клеток - AOK). Количество T-клеток в селезенке определяют по методу спонтанного розеткообразования с бараньими эритроцитами (E-POK). Пептид вводят внутримышечно.
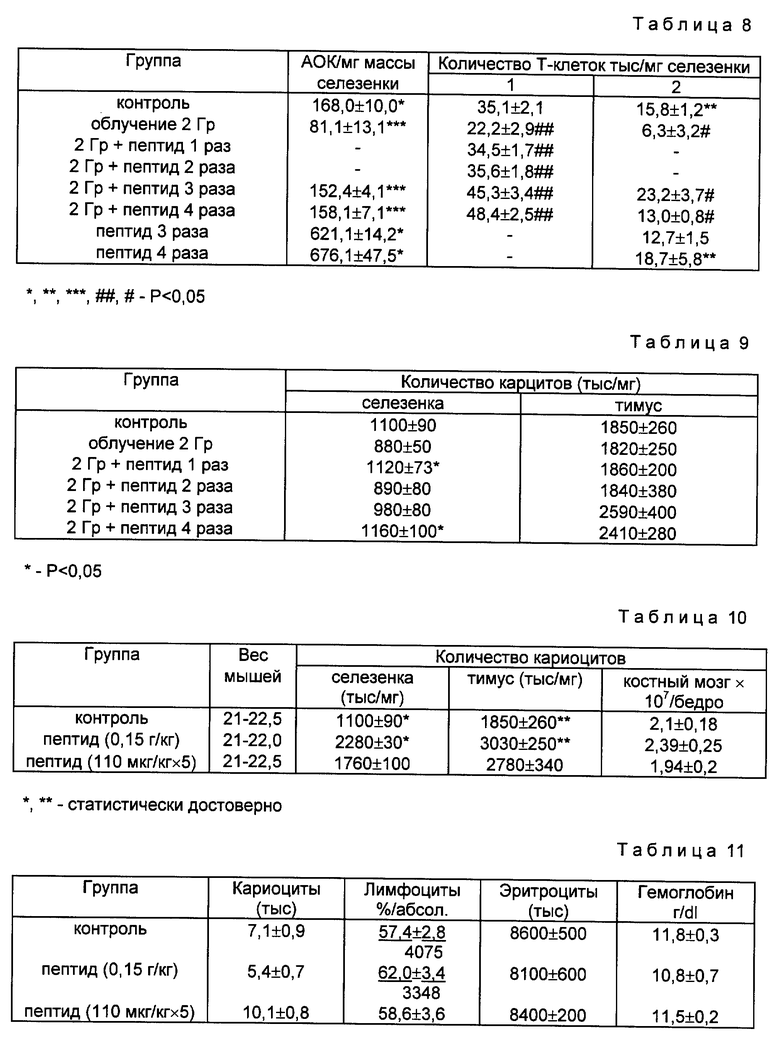
Мышей облучали дозой в 2 Гр, пептид вводят в количестве 10 мкг/кг по схеме (для определения количества T-клеток по методу спонтанного розеткообразования) : 1 раз - через 1 ч после облучения, 2 раза - через 1 ч и 1 сутки после облучения, 3 раза - через 1 ч, 1 сутки и 2 суток после облучения, 4 раза - через 1 ч, 1, 2, 3 суток после облучения (для определения количества T-клеток по методу спонтанного розеткообразования). Для инъекции используют физиологический раствор, содержащий 0,003 мас,% пептида. Интактные мыши получают пептид 3 и 4 раза. Контрольная группа (облучение 2 Гр) в аналогичные сроки получают инъекции физраствора. После окончания курса лечения пептидом по 10 мышей из каждой группы иммунизируют эритроцитами барана (ЭБ) и через 4-5 дней после этого у них определяют количество АОК в селезенке. У остальных мышей определяют число T-клеток методом спонтанного розеткообразования, количество лейкоцитов в тимусе и селезенке на мг массы органа. Результаты представлены в табл. 8 и 9.
Из табл. 8 и 9 следует, что лечение облученных мышей пептидом (одна и четыре инъекции) приводит к достоверному увеличению количества кариоцитов в селезенках на мг массы органа, к некоторому подъему числа кариоцитов в тимусе (3 и 4 инъкции) увеличению количества антителообразующих клеток почти в 2 раза, у пролеченных пептидом облученных мышей во всех группах зарегистрировано повышение численности T-клеток в селезенках, оно значительно в группах, получивших три и четыре инъекции
Иммуностимулирующая активность пептида наблюдается при лечении не только облученных мышей, но и при индукции гуморального иммунного ответа у интактных мышей к ЭБ (количество АОК увеличивается в 5 раз), хотя число T-клеток при этом не меняется. Следовательно, пептид обладает выраженной иммуномодулирующей активностью, что наблюдается при введении его как облученным, так и нормальным мышам.
Пример 6.
В этом примере описано определение токсичности пептида.
Для определения токсичности мышам-самцам вводят пептид, растворенный в физиологическом растворе, в количестве 0,15 г/кг массы тела однократно, что превышает терапевтическую дозу, оказывающую положительный эффект в пострадиационном восстановлении кроветворных клеток-предшественников в 15 тысяч раз. Второй группе мышей вводят пептид по 10 мкг/кг (терапевтическая доза) ежедневно в течение 5 дней. За выживаемостью животных наблюдают в течение 30 дней. И в первой и во второй группах гибель мышей не зарегистрирована. На 14 сутки после инъекции пептида по 10 мышей из каждой группы умерщвляют для анализа состояния их клеточных систем. Определяют количество ядросодержащих клеток в селезенке и тимусе (на мг массы органа), костном мозге, крови (в мл), количество эритроцитов и уровень гемоглобина. В табл. 10 и 11 представлены результаты.
Как видно из данных, приведенных в таблицах, через 14 суток после введения однократной большой дозы пептида отмечается увеличение количества кариоцитов в селезенке и тимусе, после введения пятикратной терапевтической дозы - лишь достоверное повышение ядросодержащих клеток в тимусе на мг массы тела. Величины остальных определяемых показателей в обеих опытных группах не отличается от контроля. Таким образом, даже превосходящая терапевтическую в 15 тысяч доза пептида не вызывает ни гибели мышей, ни токсических эффектов в отношении клеток крови, селезенки, тимуса, костного мозга. То же относится и к длительному (в течение 5 суток) применению пептида. Следует отметить, что в течение всего опыта не отмечались потери веса мышами, более того он увеличился к концу опыта в среднем на 2 г, также как в контрольной группе.
Таким образом, LD50 пептида обнаружить не удалось, т. к. даже при 15000-кратном превышении терапевтической дозы летальных исходов зарегистрировано не было, не вызывает пептид и побочных эффектов.
Пример 7.
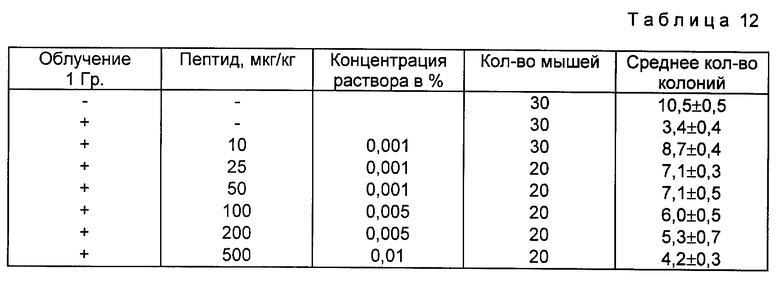
В этом примере описана способность пептида к стимуляции кроветворных клеток-предшественников (селезеночных экзоколоний) после воздействия ионизирующей радиации дозой в 1 Гр. Проанализирована зависимость между количеством пептида и выходом колоний, образуемых облучением костным мозгом. Для этого суспензию костного мозга от интактных доноров облучают in vitro дозой в 1 Гр. и сразу вводят летально облученным реципиентам, через 30 мин эти мыши дополнительно получают инъекцию пептида внутривенно в различных концентрациях (в физиологическом растворе). На 9 сутки животных умерщвляют и подсчитывают количество колоний на селезенке. Результаты опытов приведены в табл. 12.
Анализ полученной зависимости позволяет сделать следующий вывод: пептид в количестве 10 мкг/кг увеличивает выход колоний из облученного костного мозга почти до уровня интактного контроля, а в количестве от 25 до 100 мкг/кг - в 2 раза по сравнению с количеством колоний из только облученного костного мозга. Следовательно, пептид, инъецированный после введения облученных KOE-C, обладает способностью снижать повреждающее воздействие облучения дозой в 1 Гр. на клетки-предшественники кроветворения.
Согласно настоящему изобретению новый пептид формулы
H-Ile-Glu-Trp-OH
и фармацевтическая композиция на его основе, обладающие биологической активностью, могут найти применение в медицине.
Заявлен пептид формулы H-Ile-Glu-Trp-OH, обладающий влиянием на регенерацию кроветворной и иммунной систем. Фармацевтическая композиция содержит эффективное количество этого пептида. Композиция может быть в любой форме, пригодной для орального, назального, наружного применения и инъекционной. Предпочтительно она содержит 0,001-0,01 мас.% пептида. Изобретение расширяет ассортимент препаратов указанного действия, обладающих высокой активностью, низкой токсичностью при отсутствии побочного действия. 2 с. и 3 з.п. ф-лы, 2 ил.,12 табл.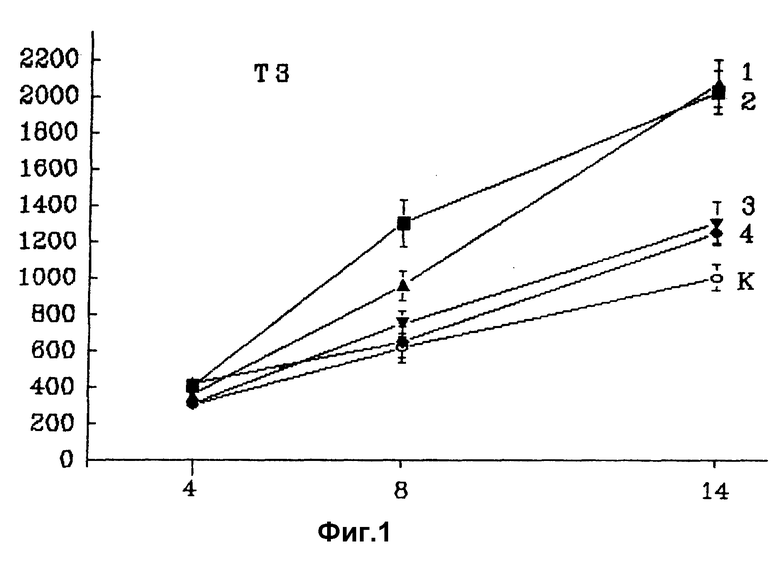
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1986, ч.II, с.171 | |||
| Композиция | 1975 |
|
SU659586A1 |
| Электрический соединитель | 1977 |
|
SU647789A2 |
| Устройство для взвешивания | 1976 |
|
SU678328A2 |
| US 4874844 A, 17.10.89 | |||
| Способ получения пептидов | 1987 |
|
SU1560058A3 |
Авторы
Даты
1998-11-10—Публикация
1996-02-28—Подача