Изобретение относится к биохимии и медицине, а именно к биологически активным пептидам, обладающим гемо- и иммунорегулирующими свойствами, и может найти применение в медицине, ветеринарии, а также в экспериментальной биологии.
В практической медицине широко известны в качестве регуляторов иммунных процессов тимусные экстракты, в частности тимозин фракция 5 /Goldstein A.L., Guna A., Latz M.M., Hardy H.A., White А./, тималин /CH,N 659586/. Эти экстракты состоят из комплекса веществ полипептидной природы и получение их из природных источников ограничено сложностью производства, малым выходом активных веществ и значительной вариабельностью их физико-химических характеристик и биологических свойств. Кроме того, из-за присутствия в природных препаратах тимуса балластных компонентов при их использовании у больных иногда возникают побочные явления.
Последнее обстоятельство явилось стимулом для создания синтетических пептидов. В настоящее время осуществлен синтез ряда пептидов, обладающих иммунорегуляторными свойствами /SU № 1582393, ЕР № 230052, US № 5008246, US № 5013723/.
Наиболее близким к заявляемым пептидам по структуре и гемо- и иммунорегулирующим свойствам является пептид формулы H-Ile-Glu-Trp-Y, где Y - ОН или замещенный амид (C1-С3) /US 6,051,683; US 6,159,940; WO 9640740/.
Каждый из полученных синтетических пептидов обладает высокой активностью, низкой токсичностью, отсутствием побочных эффектов, которые определяют их возможное применение в медицине. Одним из ограничений к широкому применению синтетических пептидов в качестве лекарственных средств является их нестабильность при пероральном применении. Известны различные способы стабилизации молекулы пептидов с целью повышения ферментативной устойчивости /Kolobov et al. US 5,916,878 and US 5,744,452/.
Задачей предлагаемого изобретения является расширение ассортимента пептидов, обладающих влиянием на регенерацию кроветворной системы.
Поставленная задача решается за счет новых пептидов общей формулы
R-A-B-C-D-Y,
где R - H,
A - Leu, Ile,
В - Asp, β-Asp,
С - Asp, β-Asp,
D - Tyr, Phe, Trp,
Y - OH
обладающих влиянием на регенерацию кроветворной системы, и создания фармацевтической композиции, которая содержит в качестве биологически активного компонента один из заявленных пептидов и носитель. Остаток аминокислоты, присоединенный к β-карбоксильной группе, в тексте обозначается в круглых скобках ().
Фармацевтическая композиция включает эффективное количество пептида как в свободном виде, так и в виде, содержащем фармацевтически приемлемый основной или кислотный противоион, а также носитель, пригодный для использования в сочетании с биологически активным компонентом. Композиция может быть составлена в любой форме, пригодной для орального и наружного применения, а также в виде инъекций.
Техническим результатом предлагаемого изобретения является получение новых индивидуальных соединений пептидной природы, обладающих высокой гемостимулирующей активностью, и устранение недостатков, свойственных описанным аналогам, в том числе и устранение значительной вариабельности физико-химических характеристик, и стабильность при пероральном введении.
В настоящем изобретении предлагаются для использования в экспериментальных и лечебных целях пептиды общей формулы
R-A-B-C-D-Y,
где R - H,
A - Leu, Ile,
В - Asp, β-Asp,
С - Asp, β-Asp,
D - Tyr, Phe, Trp
Y - OH
Согласно изобретению заявляемый пептид используется в качестве биологически активного компонента для приготовления фармацевтической композиции. Фармацевтическая композиция включает эффективное количество пептида как в свободном виде, так и в виде, содержащем фармацевтически приемлемый основный или кислотный противоион, а также носитель, пригодный для использования в сочетании с биологически активным компонентом. Композиция может быть составлена в любой форме, пригодной для орального и наружного применения, а также в виде инъекций.
Как правило, в составе композиции содержится от 0,01 до 1% (предпочтительно от 0,01 до 0,5%) пептида. Это количество зависит также от способа введения композиции в организм. Фармацевтическую композицию получают путем смешивания носителя и пептида при температуре 40 - 70°С, состав сохраняет стабильность в растворе в течение 3 лет при температуре до 25°С.
В композиции для инъекций в качестве растворителя может быть использован любой фармацевтически приемлемый растворитель, включая дистиллированную воду, физиологический, солевой, буферный растворы. Содержание пептида может составлять от 0,01 до 0,1%.
Приготовление раствора для инъекций осуществляют традиционно объемно-весовым методом. При этом к определенному весовому количеству порошка пептида добавляют растворитель до получения необходимого объема раствора. Далее раствор фильтруют через стерилизующие фильтры, разливают во флаконы или ампулы. Полученный раствор представляет собой бесцветную прозрачную жидкость, не содержит химических или иных примесей, стабилен.
Твердая форма для орального применения может быть в виде таблеток, порошков, капсул, может содержать среду для активного компонента и другие добавки, включая красители, ароматизаторы и т.д. Содержание пептида может составлять от 0,01 до 1% и обычно подбирается в зависимости от вида приготовления композиции для орального применения.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Rf1 - подвижность пептида на ТСХ (тонкослойной хроматограмме) в системе 1 (хлороформ-метанол-32% уксусная кислота=60:45:20).
Rf2 - подвижность пептида на ТСХ (тонкослойной хроматограмме) в системе 2 (бутанол-пиридин-вода-уксусная кислота=5:5:4:1).
Rt - время удерживания на хроматограмме ВЭЖХ.
Хроматографическая система Waters Alliance. Колонка 4,6×25 см, 5µ, Symmetry C18.
Градиент от 0 до 80% буфера Б в буфере А. Скорость потока 1 мл/мин. Буфер А - 0,05% трифторуксусная кислота (TFA), буфер Б - 0,025% TFA в 80% ацетонитриле. УФ-детектирование на длине волны 220 нм.
Все пептиды получают в растворе классическими методами с использованием максимальной защиты трифункциональных групп. Типовая схема синтеза приведена на схеме 1:
1. BOC-Asp(OBzl)-OH+TBTU+HCl·H-Trp-OMe+NMM→BOC-Asp(OBzl)-Trp-OMe
2. BOC-Asp(OBzl)-Trp-OMe+80%TFA→TFA·H-Asp(OBzl)-Trp-OMe
3. BOC-Asp(OBzl)-OH+TBTU+NMM+TFA·H-Asp(OBzl)-Trp-OMe→BOC-Asp(OBzl)-Asp(OBzl)-Trp-OMe
4. BOC-Asp(OBzl)-Asp(OBzl)-Trp-OMe+80%TFA→TFA·H-Asp(OBzl)-Asp(OBzl)-Trp-OMe
5. BOC-Ile-OH+TBTU+TFA·H-Asp(OBzl)-Asp(OBzl)-Trp-OMe+NMM→BOC-Ile-Asp(OBzl)-Asp(OBzl)-Trp-OMe
6. BOC-Ile-Asp(OBzl)-Asp(OBzl)-Trp-OMe+NaOH→BOC-Ile-Asp-Asp-Trp-OH
7. BOC-Ile-Asp-Asp-Trp-OH+80%TFA→TFA·H-Ile-Asp-Asp-Trp-OH
8. TFA·H-Ile-Asp-Asp-Trp-OH+NaOH→H-Ile-Asp-Asp-Trp-ONa
Boc - трет.-бутил-оксикарбонил;
OBzl - бензиловый эфир;
TBTU - N,N,N',N'-тетраметил-O-(бензотриазол-1-ил)урония тетрафторборат.
OMe - метиловый эфир;
NMM - 4-N-метилморфолин.
Очистку пептидов проводят с помощью препаративной обращенно-фазовой хроматографии на силикагеле C18 в системе изо-пропанол (фаза В) - 0,1% раствор уксусной кислоты (фаза А) в градиентном режиме от 5 до 50% фазы В. Колонка 5×30 см, силикагель Waters - C18, 35-70 мкм.
Индивидуальность получаемых соединений подтверждают методами ВЭЖХ, масс- и УФ-спектроскопии. Типичная аналитическая хроматограмма ВЭЖХ приведена в приложении 1.
Пример 2
Биологическая активность новых пептидов в сравнении с пептидом H-Ile-Glu-Trp-ОН
1. Облучение
Опыты проводят на мышах-самках линии (CBA/C57B1)F1, полученных из питомника "Столбовая". Мышей-реципиентов костного мозга облучают на радиотерапевтической установке "Луч-1" γ-лучами 60Со в дозе 8-8,5 Гр, мощность дозы 1,1 Гр/мин. Суспензию костного мозга интактных животных облучают в дозе 1 Гр за 5-10 мин до введения летально облученным животным,
2. Исследование гемостимулирующих свойств пептида и влияния на популяцию кроветворных клеток-предшественников
В этом примере описана стимуляция процесса кроветворения путем регенерации популяции КОЕ-С костного мозга мышей, подвергнутых облучению в дозе 1 Гр при различных способах введения пептидов.
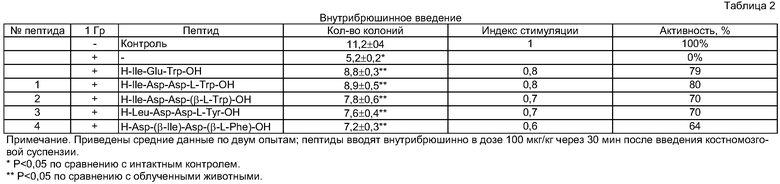
С этой целью отбирают из каждой группы не менее 5 мышей, забивают, извлекают костный мозг, готовят суспензию клеток и вводят ее летально облученным мышам. Через 9 суток по количеству выросших колоний на селезенках рассчитывают содержание КОЕ-С у доноров, облученных в дозе 1 Гр и получивших пептид. Результаты представлены в табл. 2 и 3.
Результаты исследований показывают, что ряд пептидов обладает высокой биологической активностью в модели восстановления гемопоэза после радиоактивного облучения животных. Последующие эксперименты позволяют установить, что в зависимости от первичной структуры полученных соединений биологическая активность проявляется при разных способах введения препарата. Пептиды (1 и 3, табл.2) обладают активностью только при системном введении (внутримышечно или интраперитонеально), а пептиды (2 и 4, табл. 2 и 3) проявляют активность как при системном, так и при пероральном введении.

Таким образом, полученные новые пептиды обладают гемостимулирующей активностью при различных способах введения препарата в организм.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| КОМБИНАЦИЯ ПЕПТИДОВ | 2009 |
|
RU2482127C2 |
| ПРОИЗВОДНЫЕ ГЕМИНА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2002 |
|
RU2238950C2 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ СРОДСТВОМ К РЕЦЕПТОРУ ПАРАТГОРМОНА (РТН) И СТИМУЛИРУЮЩИЕ АКТИВНОСТЬ АДЕНИЛАТЦИКЛАЗЫ | 1996 |
|
RU2157699C2 |
| Способ получения пептидов | 1988 |
|
SU1598881A3 |
| НОВЫЕ СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ ТРОЙНОЙ АКТИВНОСТЬЮ, ТРОМБОЛИЗИСНОЙ, АНТИТРОМБОТИЧЕСКОЙ И ЗАХВАТА РАДИКАЛОВ, И ИХ СИНТЕЗ, НАНОСТРУКТУРЫ И ПРИМЕНЕНИЕ | 2014 |
|
RU2660901C2 |
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2157379C2 |
| ПРОЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ С ВЫСОКОЙ СТЕПЕНЬЮ ПРОНИКНОВЕНИЯ НА ОСНОВЕ ПЕПТИДОВ И РОДСТВЕННЫХ ПЕПТИДАМ СОЕДИНЕНИЙ | 2010 |
|
RU2627065C2 |
| Способ получения пептидов | 1984 |
|
SU1477248A3 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ ЦИТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2482128C1 |

Изобретение относится к области биотехнологии, а именно к биологически активным пептидам, которые обладают влиянием на регенерацию кроветворной системы, и фармацевтической композиции на их основе. Данные пептиды могут найти применение в медицине, ветеринарии и экспериментальной биологии. Пептиды, влияющие на регенерацию кроветворной системы, определяются общей формулой: R-A-B-C-D-Y, где R - Н; А - Leu, Ile, B - Asp, β - Asp; С - Asp, β - Asp; D - Tyr, Phe, Trp; Y - OH. Предложенное изобретение позволяет получить новые индивидуальные соединения пептидной природы, обладающие высокой гемостимулирующей активностью и стабильностью при пероральном введении. 2 н. и 4 з.п. ф-лы, 3 табл.
1. Пептиды, имеющие аминокислотную последовательность, определяемую общей формулой:
R-A-B-C-D-Y,
где R-H,
A-Leu, Ile,
B-Asp, β-Asp,
C-Asp, β-Asp,
D-Tyr, Phe, Trp,
Y-OH, влияющие на регенерацию кроветворной системы.
2. Фармацевтическая композиция, влияющая на регенерацию кроветворной системы, включающая активный компонент и фармацевтически приемлемый носитель в виде растворителя или наполнителя, отличающаяся тем, что в качестве активного компонента содержит пептид по п.1 в эффективном количестве в виде свободного пептида или в сочетании с фармацевтически приемлемым противоионом.
3. Фармацевтическая композиция по п.2, отличающаяся тем, что представляет собой раствор.
4. Фармацевтическая композиция по п.3, отличающаяся тем, что представляет собой раствор для инъекций.
5. Фармацевтическая композиция по п.2, отличающаяся тем, что представляет собой твердые формы.
6. Фармацевтическая композиция по п.3, отличающаяся тем, что предпочтительное содержание указанного пептида составляет от 0,01 до 1%.
| WO 9640740 A1, 19.12.1996 | |||
| US 6051683, 18.04.2000 | |||
| US 6159940, 12.12.2000. |
Авторы
Даты
2011-01-27—Публикация
2009-06-03—Подача