Изобретение относится к новым производным 1,3-оксазин-4-она; к гербицидным композициям, содержащим эти производные; и к новым промежуточным соединениям, используемым для получения указанных производных.
Некоторые типы производных 1,3-оксазин-4-она, такие как 6-метил-3-(1-метил-1-фенилэтил)-5-фенил-2,3-дигидро-4H- 1,3-оксазин-4-она, и их гербицидная активность раскрываются, например, в WO 093/15064.
Однако соединения, описанные в вышеупомянутой международной публикации, отличаются от соединения настоящего изобретения тем, что ни одно из этих соединений не имеет амидокислотного заместителя в 3-положении 1,3-оксазинового кольца. Кроме того, вышеуказанные известные соединения не обладают достаточной гербицидной активностью и избирательной токсичностью.
Авторы настоящего изобретения досконально исследовали ряд производных 1,3-оксазин-4-она путем их синтеза и оценки физиологической активности. В результате этих исследований были обнаружены новые производные 1,3-оксазин-4-она, которые обладают значительной селективной гербицидной активностью и обнаруживают прекрасную гербицидную активность по отношению к различным сорнякам при очень небольших дозах, не оказывая при этом токсического действия на культурные растения. Таким образом, на основании полученных результатов было разработано настоящее изобретение.
Настоящее изобретение относится к производным 1,3-оксазин-4-она, имеющим общую формулу (I):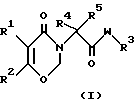
где R1 представляет собой фенильную группу, которая может быть замещенной;
R2 представляет собой атом водорода или низшую алкильную группу;
R3 представляет собой атом водорода, низшую алкильную группу, аралкильную группу или фенильную группу, которая может быть замещенной;
R4 и R5 независимо представляют собой низшую алкильную группу;
W представляет собой атом кислорода или группу формулы -N(R6)-, в которой R6 представляет собой атом водорода, низшую алкильную группу, низшую алкенильную группу или низшую алкинильную группу.
Настоящее изобретение также относится к гербицидным композициям, содержащим вышеописанные производные, а также к N-метиленаминокислотноэфирным производным как промежуточным соединениям, используемым для получения вышеописанных производных и имеющим формулу (II):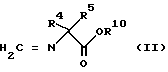
где R4 R5 независимо представляют собой низшую алкильную группу;
R10 представляет собой низшую алкильную группу или аралкильную группу.
Описание предпочтительных вариантов осуществления изобретения.
Ниже подробно описаны производные 1,3-оксазин-4-она общей формулы (I) и промежуточные соединения, используемые для получения этих производных и имеющие общую формулу (II).
Ниже приводятся примеры атомов и групп, представленных R1, R2, R3, R4, R5, R6 и R10 в вышеописанных соединениях, имеющих общие формулы (I) и (II).
Фенильная группа, которая может быть замещенной.
Фенильная группа или фенильная группа, замещенная атомом галогена, гидроксигруппой, низшей алкильной группой, низшей алкоксигруппой, феноксигруппой, низшей алкилтиогруппой, низшей алкилсульфонильной группой, низшей галогеналкильной группой, низшей галогеноалкоксигруппой, алкоксикарбонильной группой, алкоксикарбонилалкоксигруппой, ацильной группой, цианогруппой, или нитрогруппой. Примерами таких групп являются фенильная группа, 2-фторофенильная группа, 3-хлорофенильная группа, 3,5-дихлоро-4-гидроксифенильная группа, 3-толуильная группа, 2,5-ксилильная группа, 3-анизильная группа, 3-феноксифенильная группа, 3-метилтиофенильная группа, 2-хлоро-5-(метилсульфонил)фенильная группа, 3-(трифторометил)фенильная группа, 3,5-бис(дифторометокси)фенильная группа, 3-метоксикарбонилфенильная группа, 3-(1-метоксикарбонил)этоксифенильная группа, 3-нитрофенильная группа, 3-цианофенильная группа, 3-ацетилфенильная группа, 2-хлоро-5-нитрофенильная группа, 3,5-дихлорофенильная группа, 2-фторо-4-хлорофенильная группа, 2,5-дихлорофенильная группа, 3,5-дихлоро-4-метилфенильная группа и т.п.
Атом галогена
Атом фтора, атом хлора атом бром или атом йода.
Низшая алкильная группа
Низшая алкильная группа, имеющая от одного до шести атомов углерода, может быть прямой или разветвленной группой, такой как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, втор-бутильная трет-бутильная группа, н-пентильная группа, неопентильная группа, трет-пентильная группа или гексильная группа и т.п.
Низшая алкенильная группа
Низшая алкенильная группа, имеющая от двух до пяти атомов углерода, такая как аллильная группа, 2-метил-2-пропенильная группа, 2-бутенильная группа, 3-бутенильная группа, 3-метил-2-бутенильная группа и т.п.
Низшая алкинильная группа
Низшая алкинильная группа, имеющая от двух до пяти атомов углерода, такая как 2-пропинильная группа, 1-метил-2-пропинильная группа, 2-бутинильная группа, 3-бутинильная группа и т.п.
Низшая алкоксигруппа
Низшая алкоксигруппа, алкильная часть которой имеет значения, указанные выше, например, такая как этоксигруппа, метоксигруппа, пропоксигруппа, изопропоксигруппа, бутоксигруппа, пентоксигруппа и т.п.
Низшая алкилтиогруппа
Низшая алкилтиогруппа, алкильная часть которой имеет значения, указаные выше, например, такая как метилтиогруппа, этилтиогруппа, пропилтиогруппа, изопропилтиогруппа, бутилтиогруппа, пентилтиогруппа и т.п.
Низшая алкилсульфонильная группа
Низшая алкилсульфонильная группа, алкильная часть которой имеет значения, указанные выше, например, такая как метилсульфонильная группа, этилсульфонильная группа, пропилсульфонильная группа, изопропилсульфонильная группа, бутилсульфонильная группа, пентилсульфонильная группа и т.п.
Низшая галогеналкильная группа
Низшая галогеналкильная группа, имеющая от одного до четырех атомов углерода, например, такая как бромметильная группа, дифторметильная группа, дихлорометильная группа, трифторометильная группа, 1-хлорэтильная группа, 2-иодэтильная группа, 3-хлорпропильная группа, 2-метил-2-хлорпропильная группа, 2,2,2-трифторэтильная группа и т.п.
Низшая галогеналкоксигруппа
Низшая галогеналкоксигруппа, галогеналкильная часть которой имеет значения, определенные выше, например, такая как трифторметоксигруппа, дифторметоксигруппа, хлордифторметоксигруппа, 2-хлорэтоксигруппа, 1,1,2,2-тетрафторэтоксигруппа, 3-хлорпропоксигруппа и т.п.
Алкоксикарбонильная группа
Алкоксикарбонильная группа, имеющая около 2 - 8 атомов углерода, например, такая как метоксикарбонильная группа, этоксикарбонильная группа, изопропоксикарбонильная группа и т.п.
Алкоксикарбонилалкоксигруппа
Алкоксикарбонилалкоксигруппа, имеющая около 3 - 10 атомов углерода, например, такая как метоксикарбонилметоксигруппа, 1-(метоксикарбонил)этоксигруппа, 1-(этоксикарбонил)-этоксигруппа, 1-метил-3-(изопропоксикарбонил)пропильная группа и т.п.
Ацильная группа
Ацильная группа, такая как ацетильная группа, пропионильная группа, бутирильная группа, изобутирильная группа и т.п.
Аралкильная группа
Аралкильная группа, такая как бензильная группа, 1-фенилэтильная группа, 2-фенилэтильная группа, 1-метил-1-фенилэтильная группа, 1-этил-2-фенилэтильная группа, 3-фенилпропильная группа и т.п.
Исходя из вышеуказанных атомов и групп или в соответствии с общепринятыми значениями, обычно используемыми в данной области, могут быть выбраны, но необязательно, соответствующие комбинации групп, которые не были конкретно упомянуты в качестве примеров в вышеуказанных определениях.
Из вышеописанных соединений общей формулы (I), предпочтительными являются соединения общей формулы (I), в которых:
R1 представляет собой фенильную группу, 2-фторофенильную группу, 2-хлорофенильную группу или 2-метилфенильную группу;
R2 представляет собой атом водорода, метильную группу или этильную группу;
R3 представляет собой фенильную группу, фенильную группу, замещенную в 3-положении одним заместителем, выбранным из группы, включающей в себя атом галогена, низшую алкильную группу, низшую алкоксигруппу, феноксигруппу, низшую галогеноалкильную группу и низшую галогеноалкоксигруппу; либо фенильную группу, замещенную во 2- и 5-положениях или 3- и 5-положениях двумя заместителями, выбранными из группы, включающей в себя атом галогена, низшую алкильную группу, низшую алкоксигруппу, феноксигруппу, низшую галогеноалкильную группу или низшую галогеноалкоксигруппу;
каждый из R4 и R5 независимо представляют собой метильную группу или этильную группу;
W представляет собой группу формулы -N-(R6), где R6 является предпочтительно атомом водорода или метильной группой.
Более предпочтительным соединением общей формулы (I) является соединение общей формулы (I-I):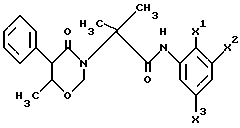
где каждый из X1, X2 и X3 независимо представляет собой атом водорода, атом галогена, низшую алкильную группу, низшую алкоксигруппу, феноксигруппу, низшую галогеноалкильную группу или низшую галогеноалкоксигруппу.
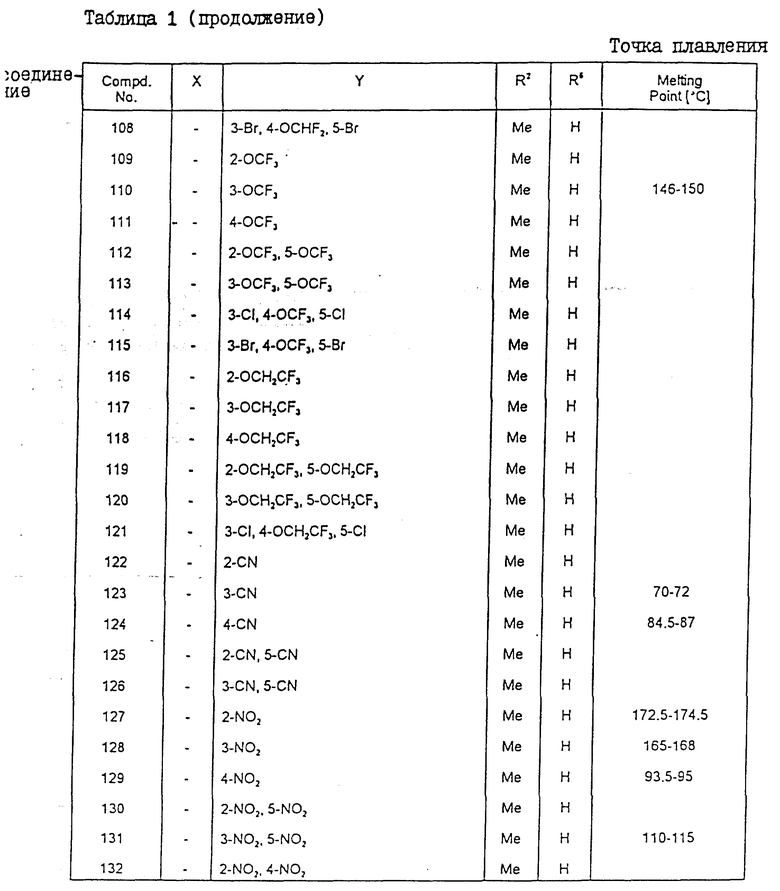
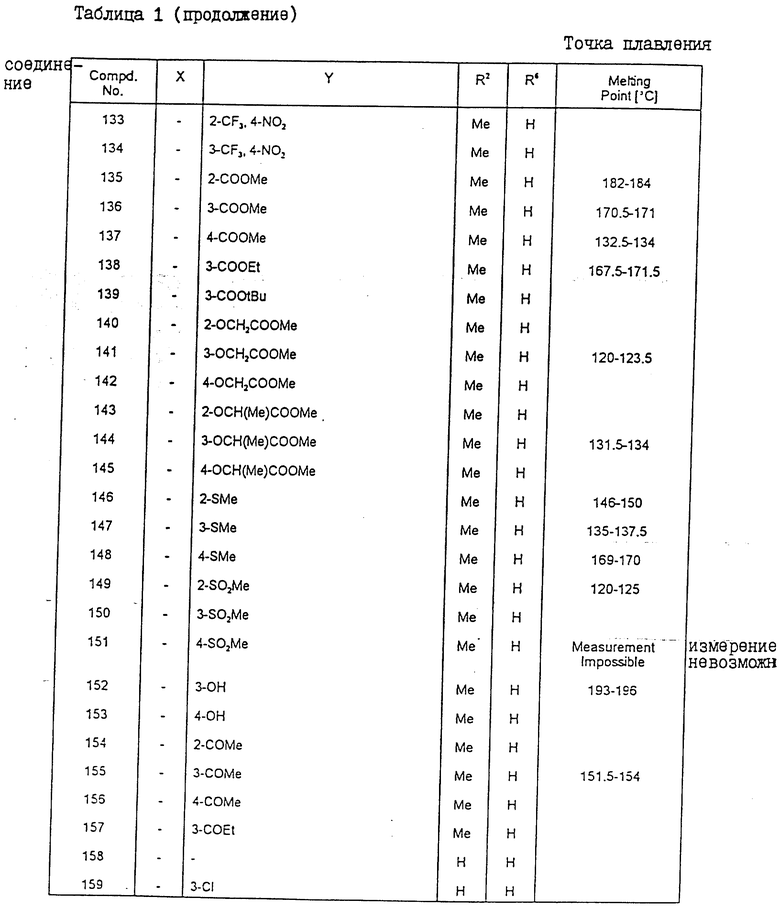
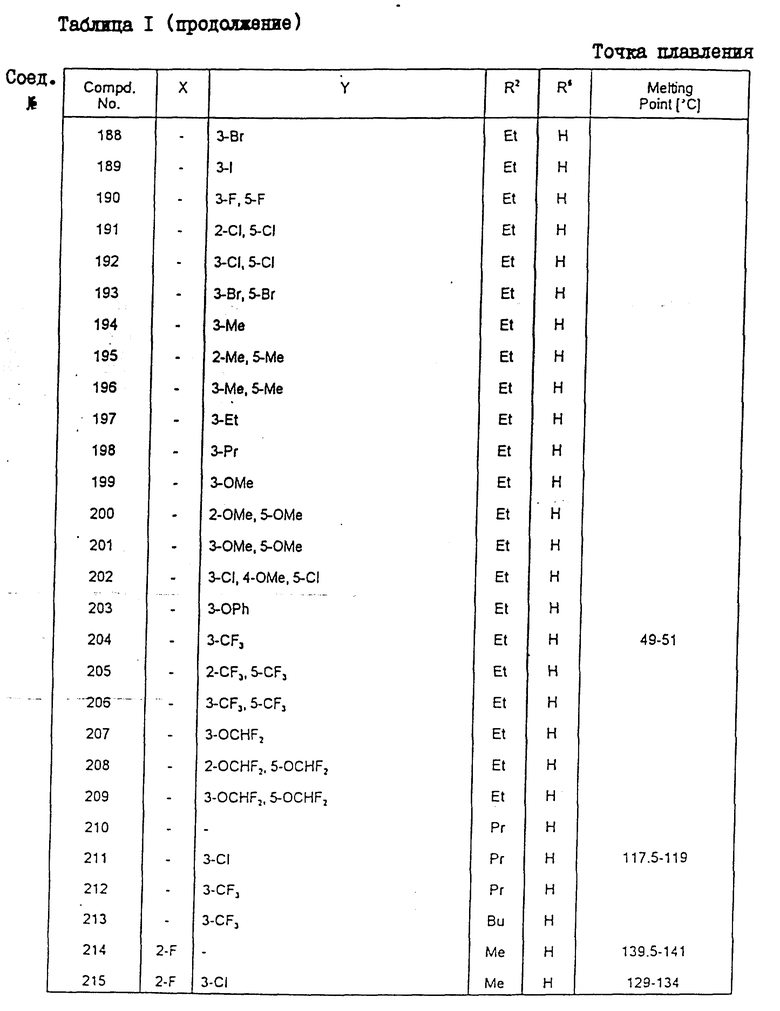
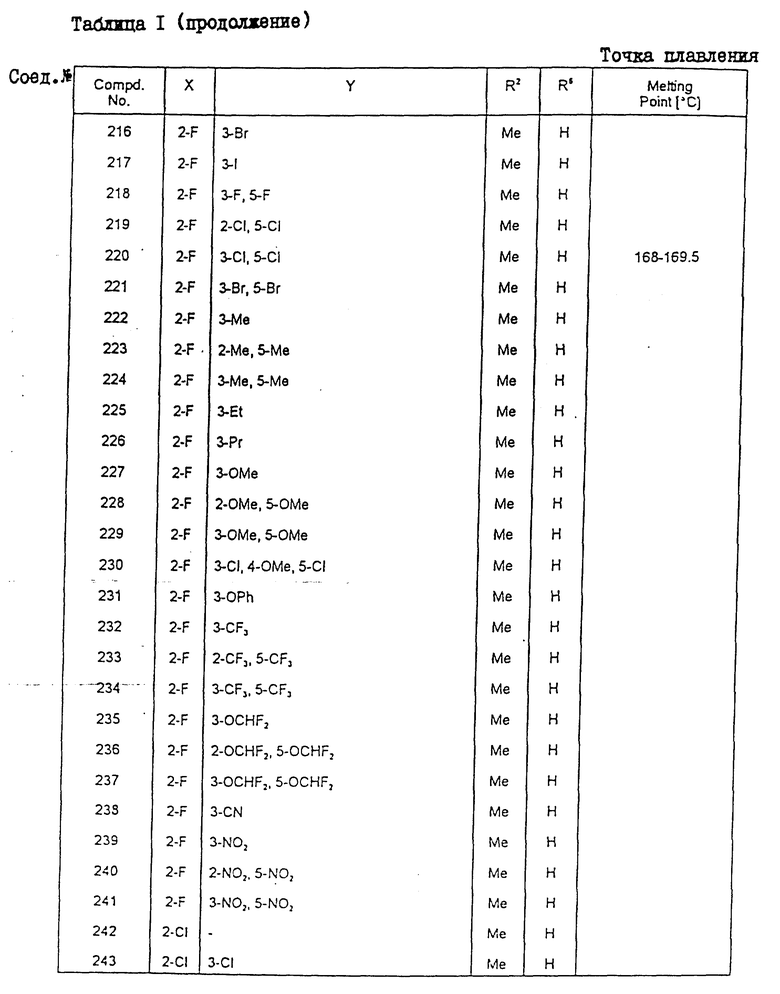
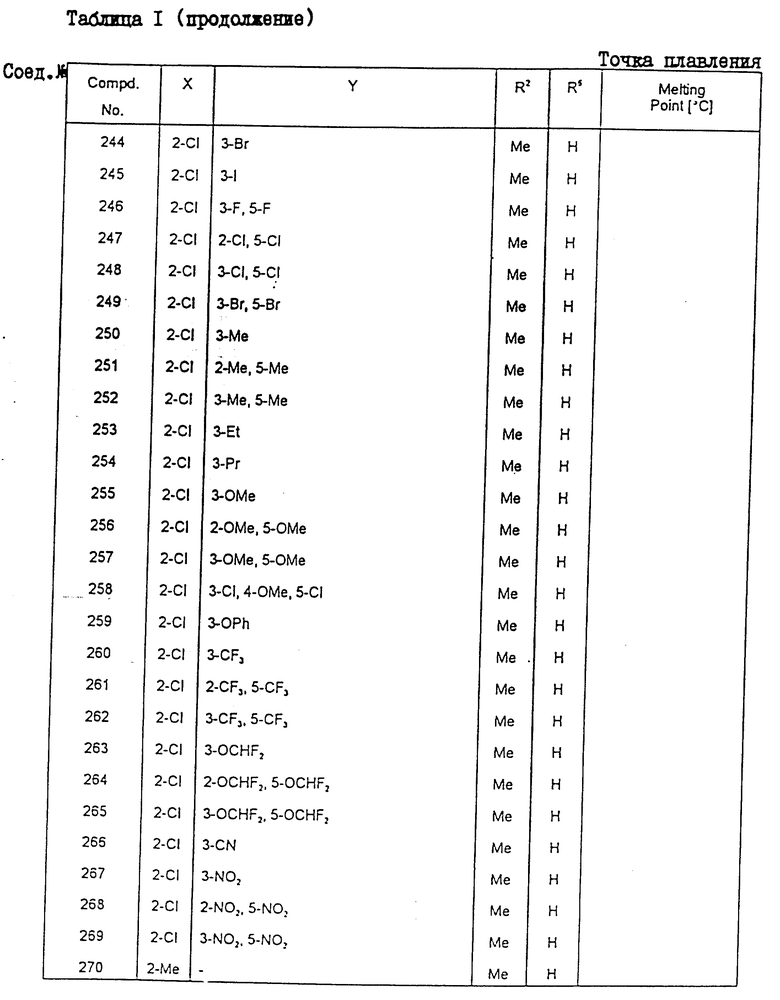
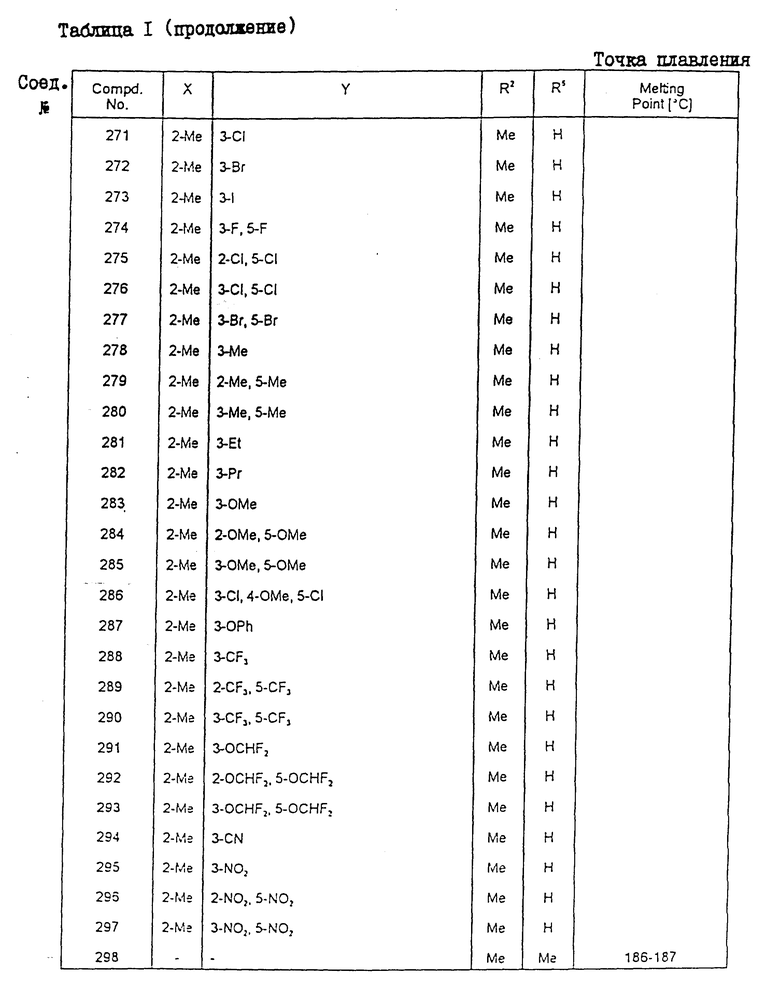
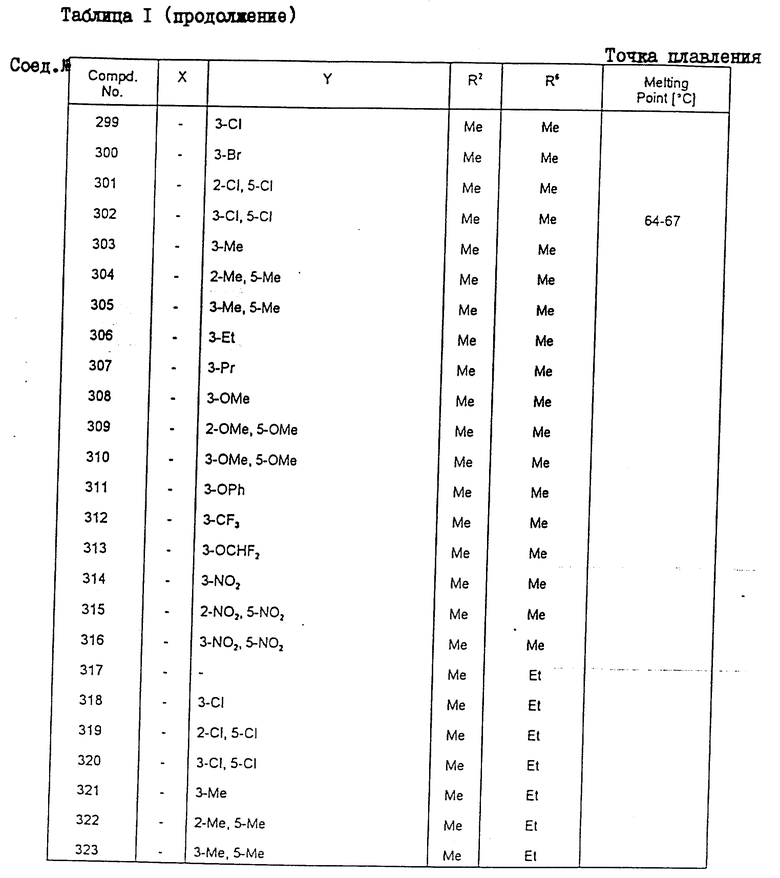
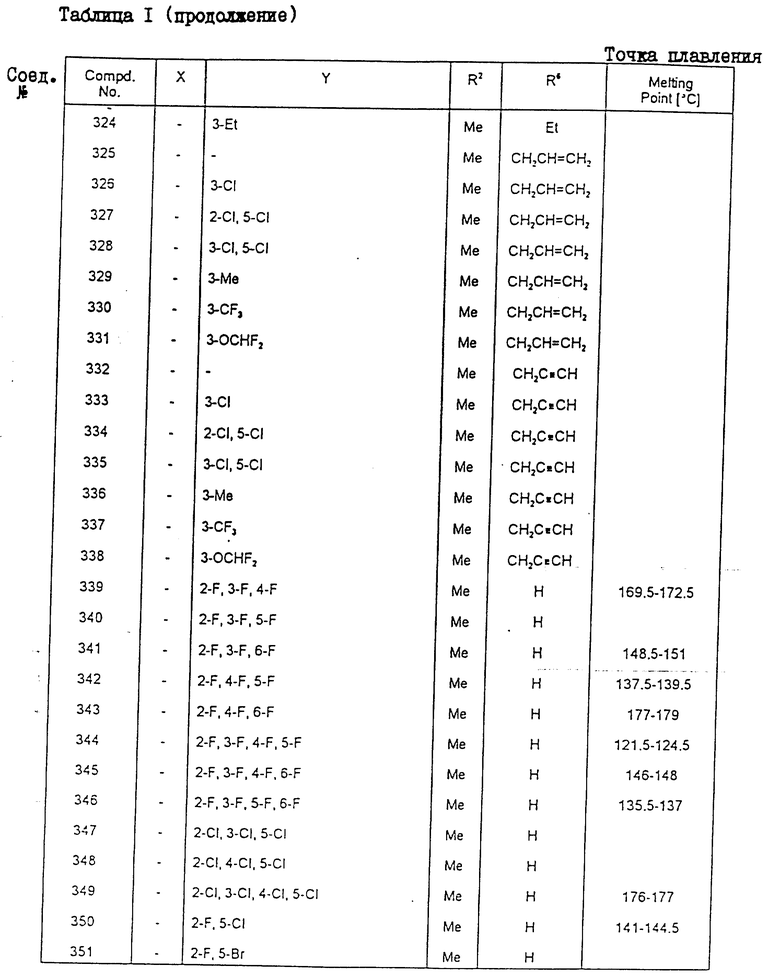
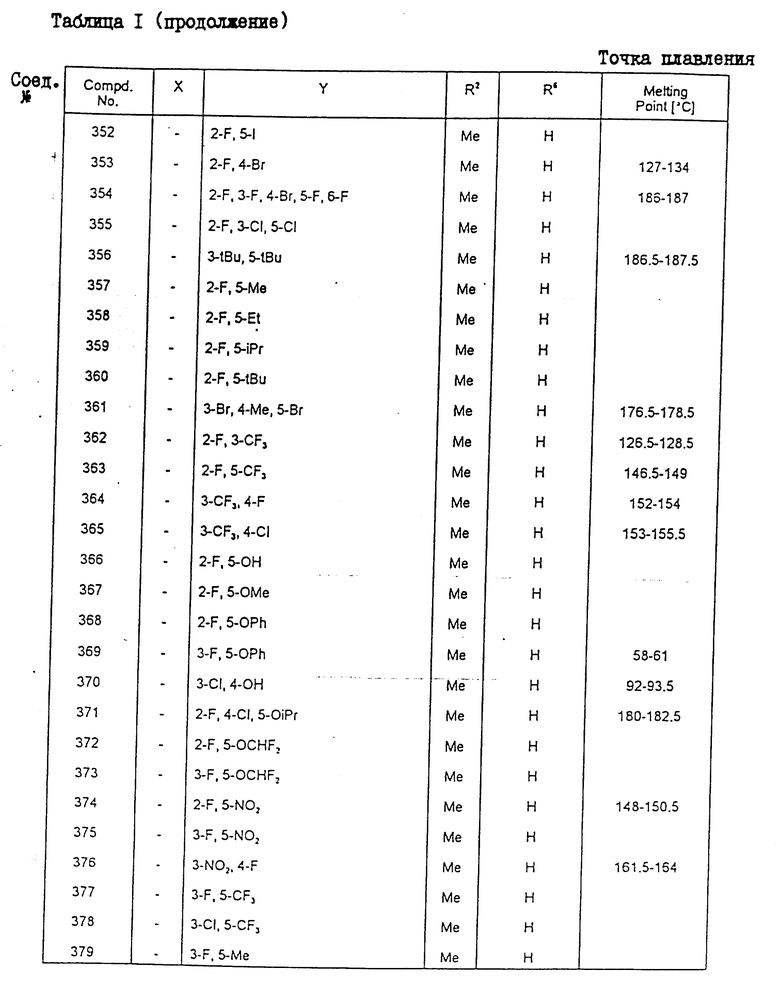
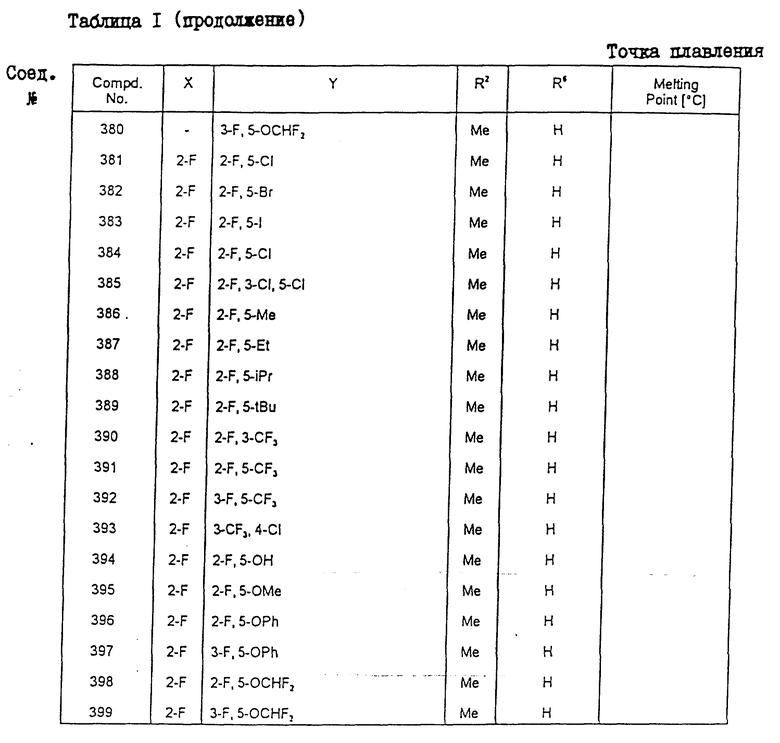
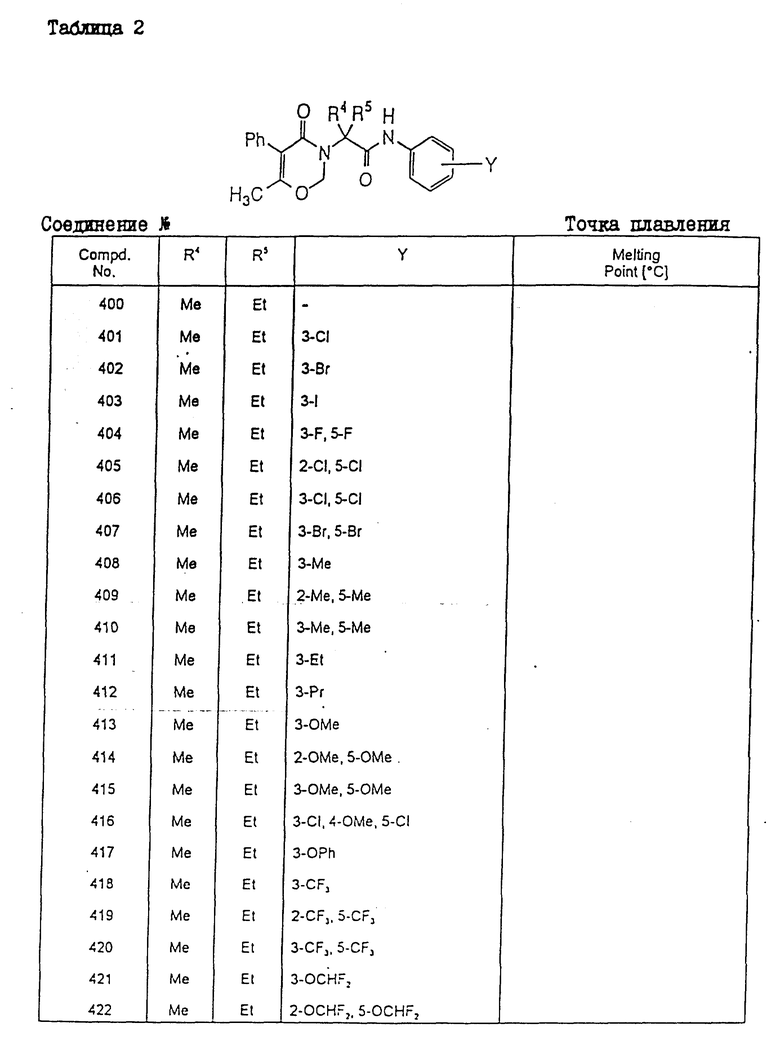
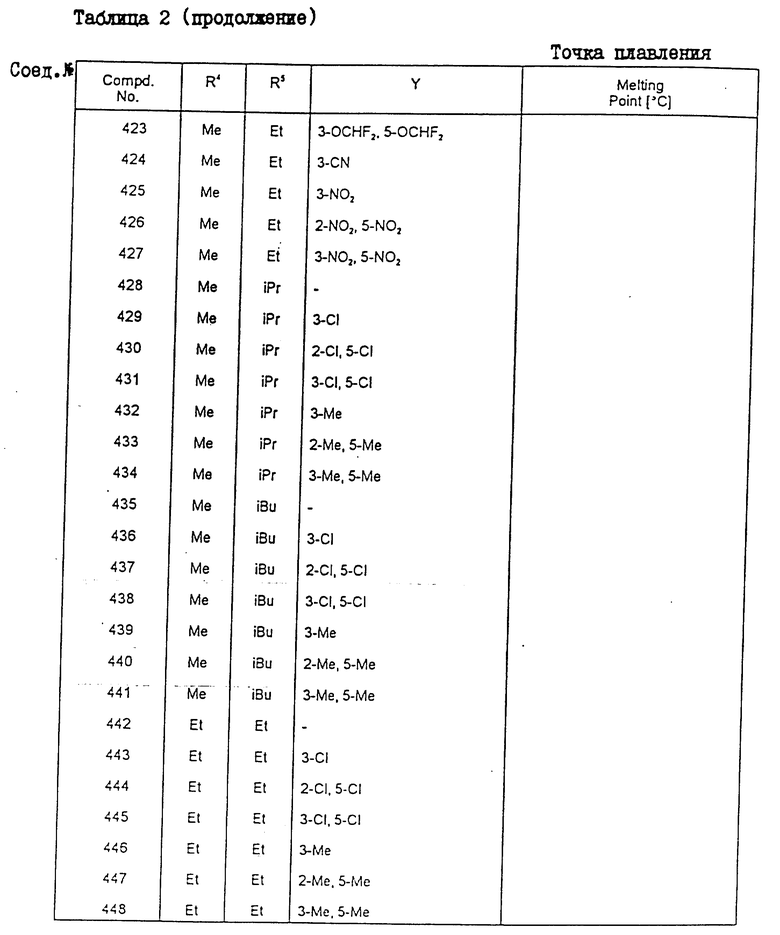
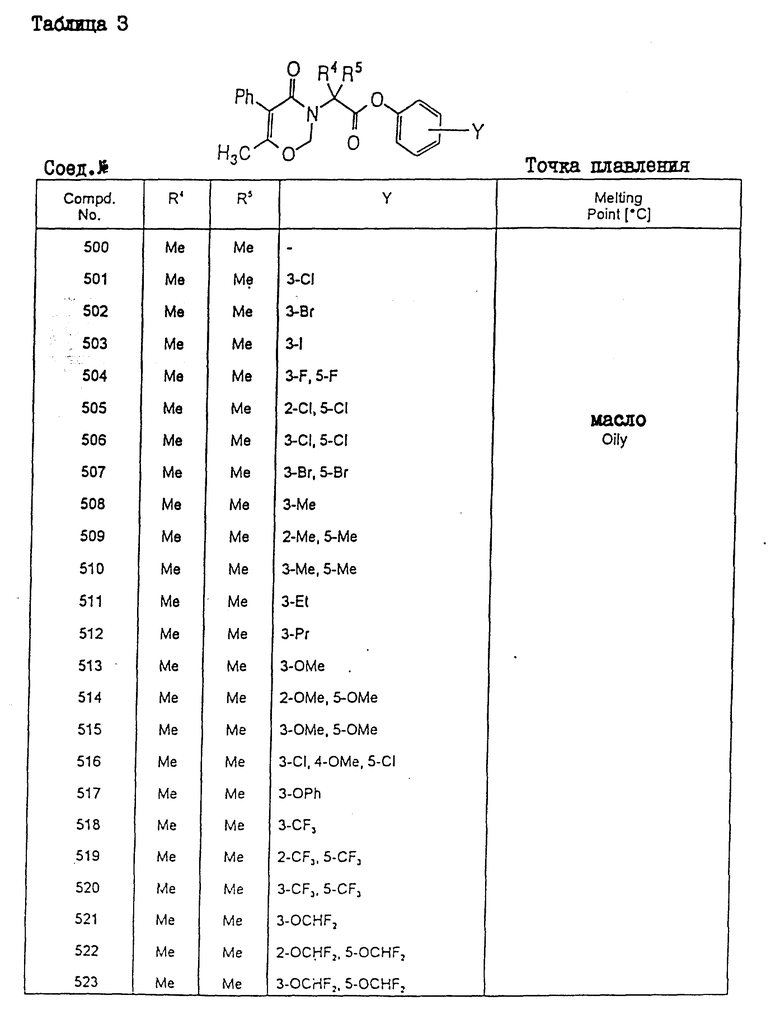
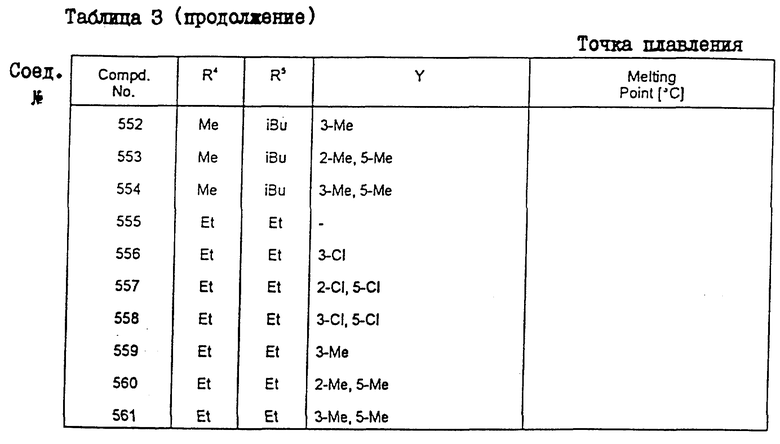
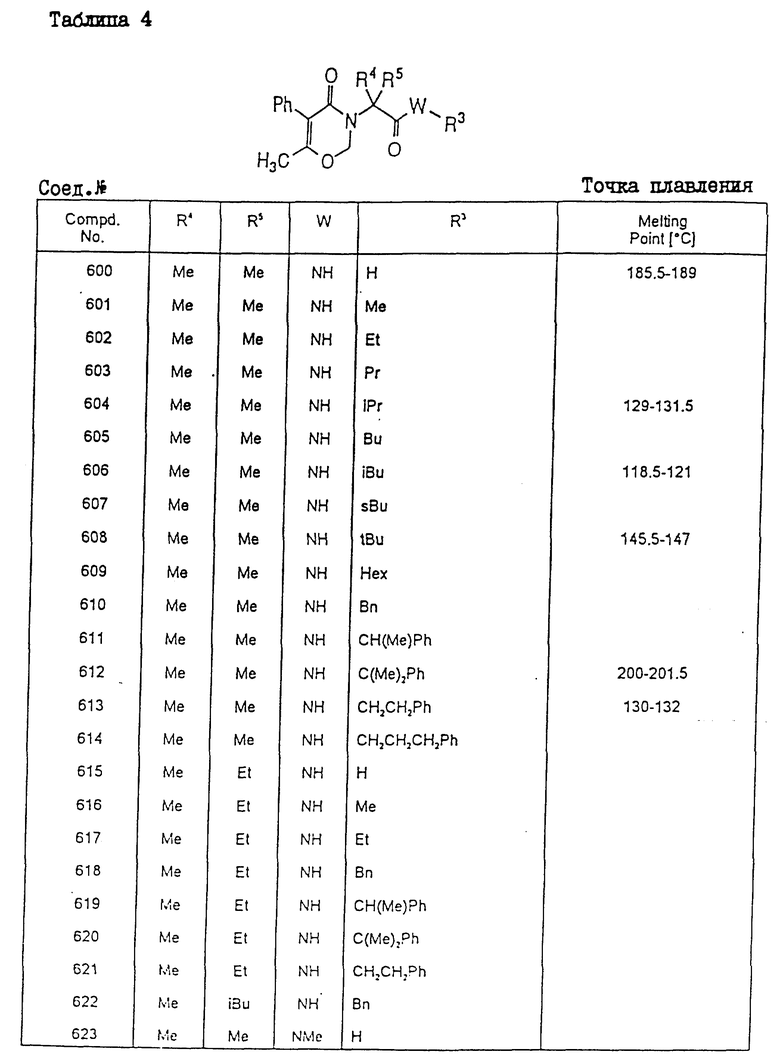
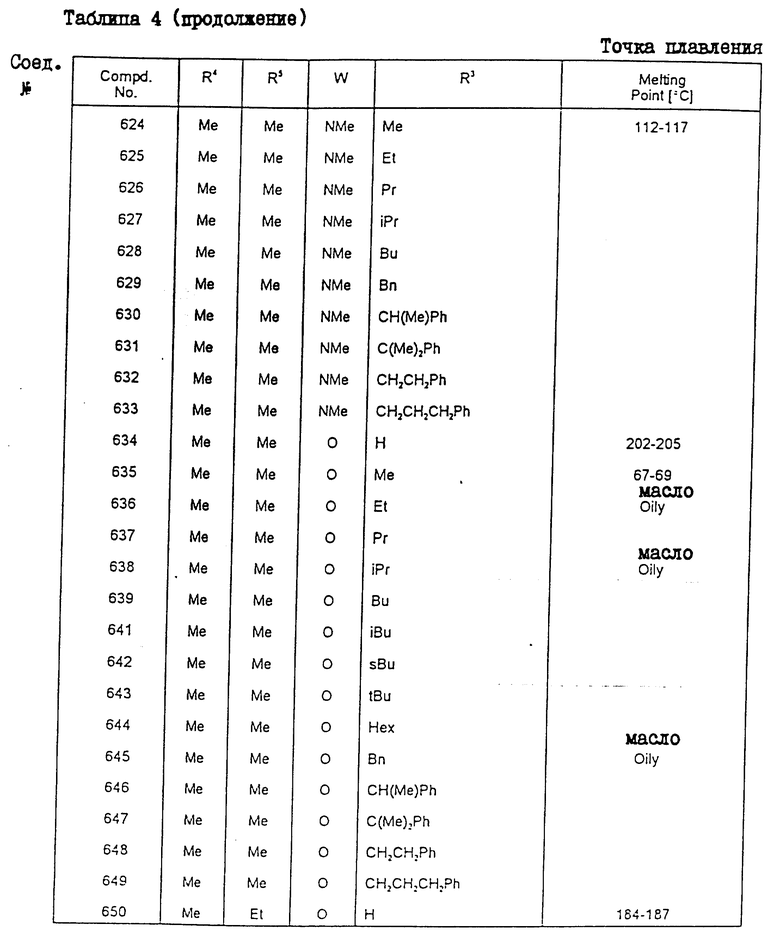
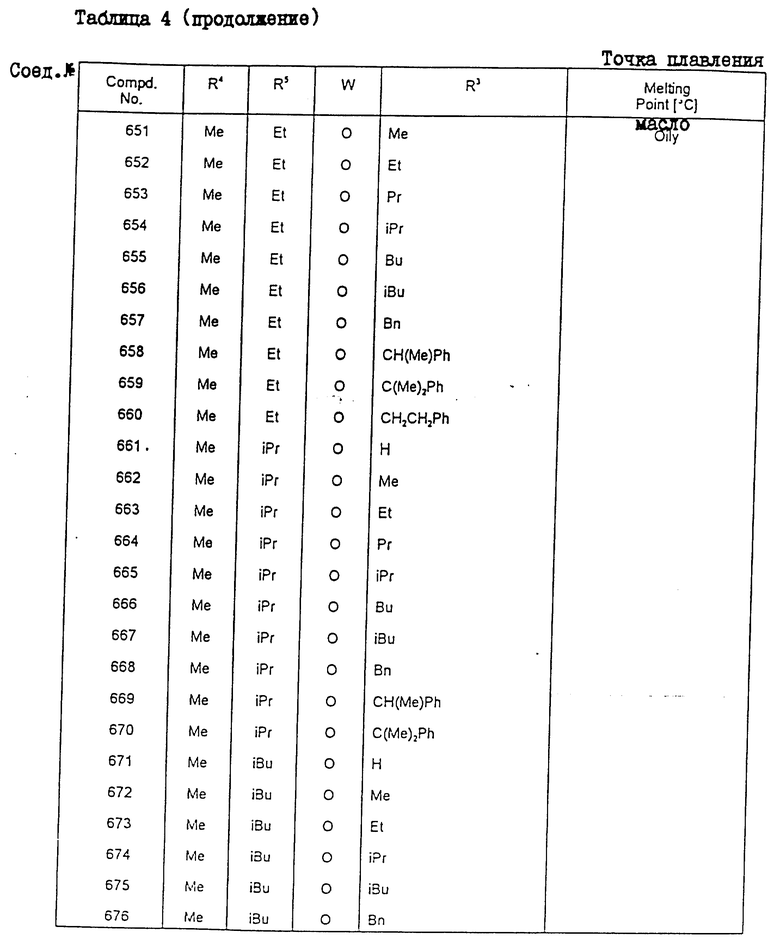
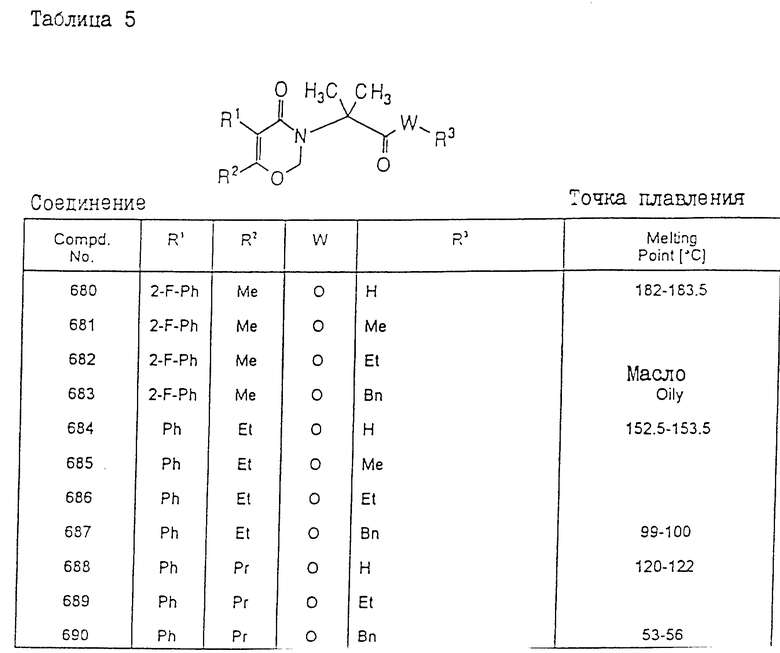
Конкретные примеры соединения настоящего изобретения общей формулы (I) представлены в табл. 1 - 5. В этих таблицах использованы следующие сокращения:
Me - метильная группа; Et - этинильная группа;
Pr - н-пропильная группа; iPr - изопропильная группа;
Bu - бутильная группа; iBu - изобутильная группа;
SB - втор-бутильная группа; tBu - трет-бутильная группа;
Hex - гексильная группа; Ph - фенильная группа;
Bn - бензильная группа; 2-F-PH- - 2-фторфенил; и
"-" заместитель отсутствует.
Соединения настоящего изобретения могут быть получены любыми известными методами. Например, соединение общей формулы (I) может быть получено следующими методами.
Метод A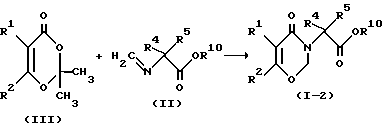
где R1, R2, R4 и R5 являются такими, как они были определены в общей формуле (I), а R10 является таким, как он был определен в общей формуле (II).
Соединение формулы (1-2) может быть получено посредством реакции соединения формулы (II) с соединением формулы (III) в отсутствии или в присутствии подходящего растворителя.
Реакционная температура может быть определена эмпирически и составлять в пределах от около 90 до 160oC или до точки кипения растворителя.
Растворитель, если он присутствует, может быть любым без каких-либо конкретных ограничений при условии, что он является инертным в отношении исходных соединений, используемых в методе A; однако, если учитывать реакционную температуру, то предпочтительно использовать растворитель с более высокой точкой кипения, например, такой как толуол, ксилол или мезитол.
Хотя время реакции зависит от используемых условий, однако в основном реакция может быть завершена за 1 - 240 мин.
Количественное соотношение соединений формулы (II) и формулы (III) не имеет конкретных ограничений, но в основном соединение формулы (III) используется в количестве 0,5 - 2 М, а предпочтительно 0,9 - 1,1 М на один моль соединения формулы (II).
Продукты формулы (1-2) могут быть выделены и очищены из реакционной смеси известными способами, такими как экстракция, перекристаллизация или хроматография.
N-метиленаминокислотноэфирное производное общей формулы (II) (см. ниже), используемое в вышеописанной реакции в качестве исходного материала, является новым соединением, а поэтому оно также входит в объем настоящего изобретения.
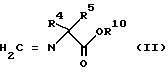
где R4 и R5 независимо представляют собой низшую алкильную группу, а R10 представляет собой низшую алкильную группу или аралкильную группу.
Из соединений общей формулы (II), описанных выше, предпочтительной группой соединений являются такие соединения общей формулы (II), в которых каждый из R4 и R5 независимо представляют собой метильную группу или этильную группу; а R10 представляет собой метильную группу, этильную группу или бензильную группу.
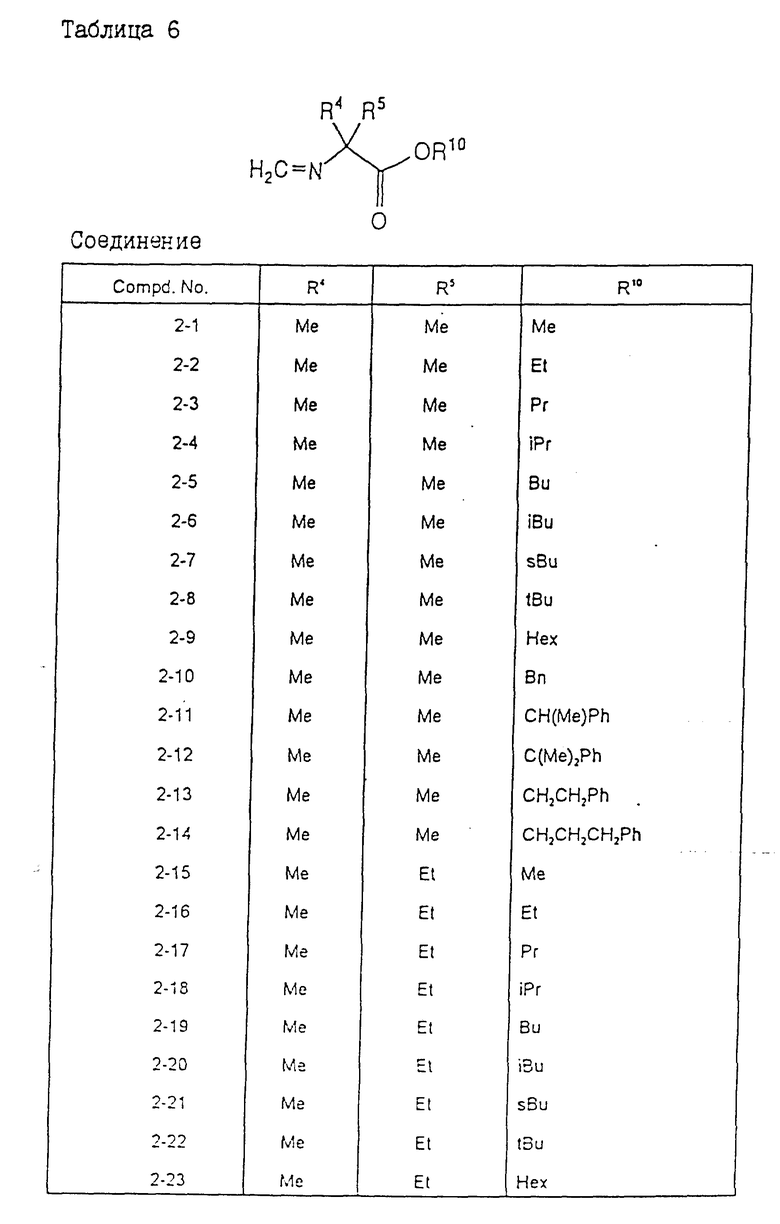
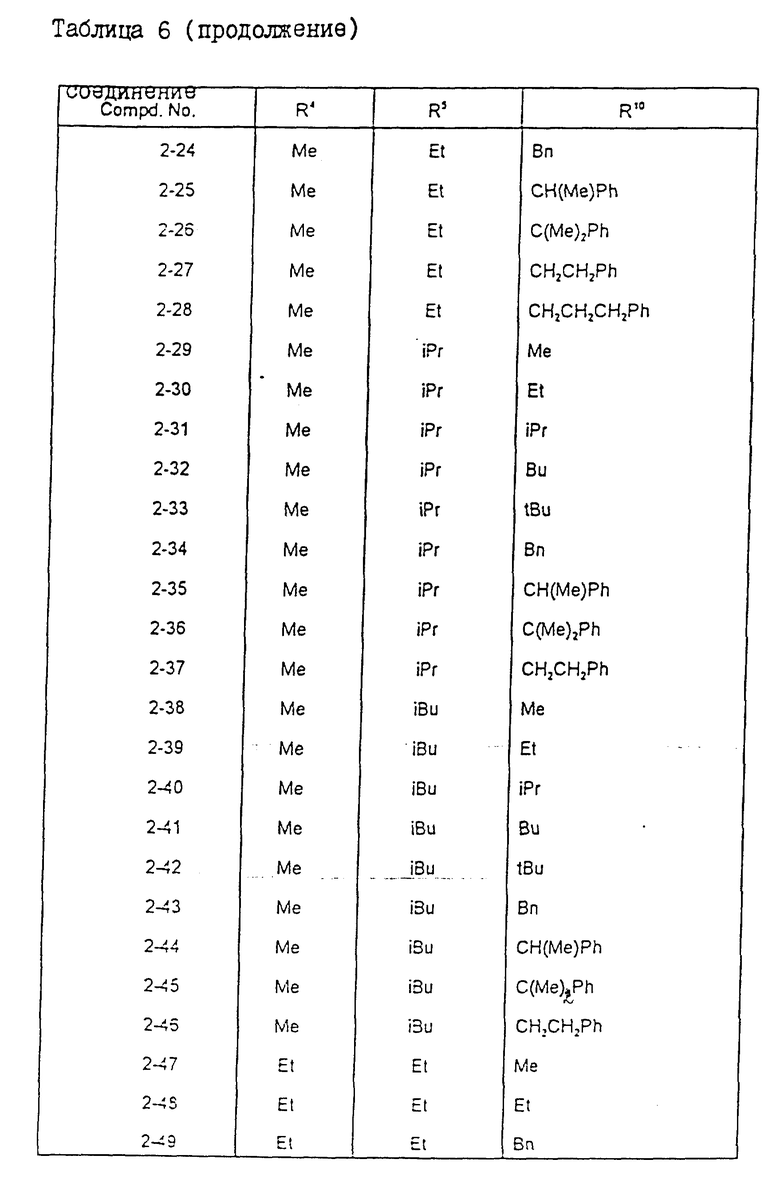
Конкретные примеры соединений настоящего изобретения, имеющих общую формулу (II), представлены в табл. 6. В табл. 6 использованы те же самые сокращения, что и в предыдущих таблицах.
Соединение формулы (II) может быть получено любым известным методом. Так, например, указанное соединение может быть получено следующим способом: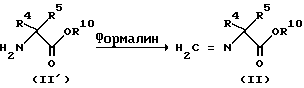
где R4 и R5 являются такими, как они были определены в общей формуле (I), а R10 является таким, как он был определен в общей формуле (II).
Соединения формулы (II) могут быть получены с помощью реакции одного из сложных эфиров аминокислоты формулы (II') с формалином в присутствии или в отсутствии подходящего растворителя.
Реакционная температура может быть определена эмпирически, и составляет обычно в пределах от около 0 до 140oC.
Растворитель, если он присутствует, может быть любым без каких-либо конкретных ограничений при условии, что он является инертным по отношению к соединениям, используемым в данном методе; при этом предпочтительными растворителями являются углеводороды, такие как толуол или ксилол; и простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир и тетрагидрофуран.
Время реакции может варьировать в зависимости от реакционных условий, однако в основном реакция может быть завершена за период времени от 1 ч до 1 дня.
Количественное отношение соединений формулы (II') и формалина не имеет конкретных ограничений, но в основном количество формалина составляет 1 - 5 М, а предпочтительно 1,1 - 2 М на один моль соединения формулы (II').
Продукты формулы (II) могут быть выделены и очищены из реакционной смеси известными способами, такими как экстракция, дистилляция, перекристаллизация или хроматография.
Сложные эфиры аминокислоты формулы (II'), используемые в вышеописанной реакции в качестве исходных соединений, могут быть получены известными методами или аналогичными методами.
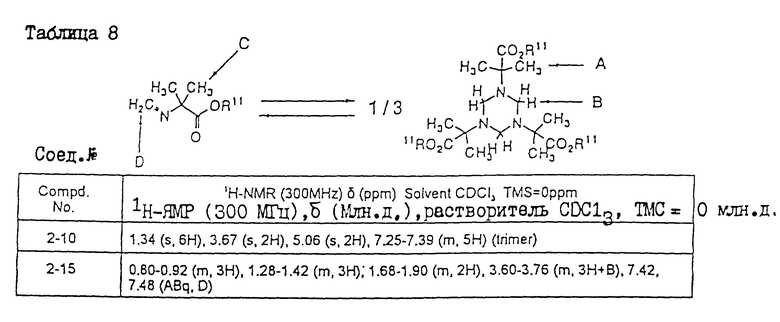
Соединение формулы (II) часто создает состояние равновесия со своими тримерами в условиях комнатной температуры, а поэтому это соединение может присутствовать в виде смеси самого соединения (т.е. мономеров) и его тримеров. Кроме того, в зависимости от конкретных условий все соединение в целом может присутствовать в виде тримера. Однако далее во избежание ненужных усложнений указанное соединение будет называться мономером независимо от формы, которую оно принимает.
Другим исходным соединением, используемым для синтеза соединения формулы (1-2), является соединение формулы (III), которое может быть получено несколькими методами, например методом, описанным в Chem. Pharm. Bull., 31(6), 1896-1901 (1983) или аналогичными методами.
Метод B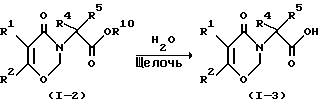
где R1, R2, R4 и R5 являются такими, как они были определены в общей формуле (I), а R10 является таким, как он был определен в общей формуле (II).
Соединение формулы (1-3) может быть получено путем гидролиза соединения формулы (1-2) щелочью.
Примерами щелочи, которая может быть использована для такого гидролиза, является раствор гидроксида натрия или гидроксида калия.
Растворитель, который используется помимо воды, может быть любым растворителем без каких-либо конкретных ограничений при условии, что он является инертным по отношению к реагентам, используемым в методе B; при этом предпочтительными растворителями являются спирты, такие как метанол или этанол; простые эфиры, такие как тетрагидрофуран или диоксан.
Температура реакции предпочтительно составляет от около комнатной температуры до 80oC.
Продукты формулы (1-3) могут быть выделены и очищены из реакционной смеси известными методами, такими как экстракция, перекристаллизация или хроматография.
Метод C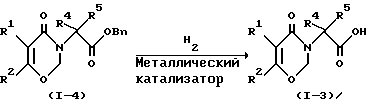
где R1, R2, R4 и R5 являются такими, как они были определены в общей формуле (I), а сокращение Bn означает бензильную группу.
Соединение формулы (1-3) может быть получено путем гидрирования соединения формулы (1-4) в присутствии металлического катализатора.
В данном методе, в качестве металлического катализатора может быть использовано большинство металлических катализаторов, которые обычно используются для промотирования реакции гидрирования, например, такие, как "палладий на угле", "родий на угле" или платиновая чернь.
В качестве растворителя может быть использован практически любой растворитель без каких-либо конкретных ограничений при условии, что он является инертным по отношению к реагентам, используемым в методе C; при этом предпочтительными растворителями являются спирты, такие как метанол или этанол, сложные эфиры уксусной кислоты, такие как этилацетат; и уксусная кислота.
Данная реакция может быть проведена в атмосфере водорода при нормальном давлении, при комнатной температуре и в течение периода времени от 1 ч до 1 дня; причем эта реакция может быть также промотирована использованием повышенной температуры и/или повышенного давления.
Количество добавляемого катализатора может быть установлено эмпирически в соответствии со скоростью реакции.
Продукты формулы (1-3) могут быть выделены и очищены из реакционной смеси с использованием стандартной техники, такой как экстракция, перекристаллизация или хроматография.
Метод D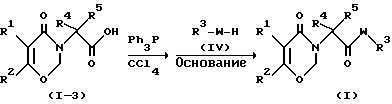
где R1, R2, R3, R4, R5 и W являются такими, как они были определены в общей формуле (I).
Соединение формулы (I) может быть получено с помощью реакции соединения формулы (1-3) с тетрахлорметаном и трифенилфосфином с последующей обработкой соединением формулы (IV) в присутствии основания.
Первую реакцию осуществляют при температуре предпочтительно от комнатной до около 140oC или до точки кипения растворителя; а вторую реакцию осуществляют предпочтительно от 0 до около 60oC.
В качестве растворителя может быть использован любой растворитель без каких-либо конкретных ограничений при условии, что он является инертным по отношению к реагентам, используемым в методе D; при этом предпочтительными растворителями являются галогенированные углеводородные растворители, такие как тетрагидрофуран, хлороформ или метиленхлорид; углеводородные растворители, такие как толуол, ксилол или мезитилен; и эфирные растворители, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан.
Примерами основания могут служить третичные амины, такие как триэтиламин, диизопропилэтиламин или пиридин; и неорганические основания, такие как гидроксид натрия или карбонат натрия. Если необходимо, основание может быть также использовано в виде водного раствора или в виде соли, образованной соединением формулы (IV). Кроме того, если соединение формулы (IV) является амином, то избыток этого соединения (IV) может быть также использован в качестве основания.
Продукты формулы (I) могут быть выделены и очищены из реакционной смеси известными способами, такими как экстракция, перекристаллизация или хроматография.
Метод E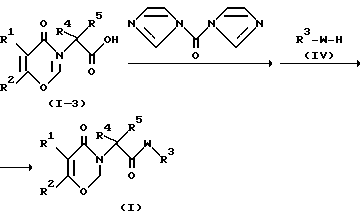
где R1, R2, R4, R5 и W являются такими, как они были определены в общей формуле (I).
Соединение формулы (I) может быть получено с помощью реакции соединения формулы (1-3) с карбонилдиимидазолом, с последующей обработкой соединением формулы (IV) или его соли.
Первую реакцию осуществляют предпочтительно при температуре от 0 до около 60oC, а вторую реакцию осуществляют предпочтительно при температуре в пределах от комнатной температуры до около 100oC или до точки кипения растворителя.
Время реакции обычно составляет от 0,5 до 24 ч.
В качестве растворителя может быть использован любой растворитель без каких-либо конкретных ограничений при условии, что он является инертным по отношению к реагентам, используемым в методе E; при этом предпочтительными примерами растворителя являются галогенированные углеводородные растворители, такие как тетрахлорметан, хлороформ или метиленхлорид; углеводородные растворители, такие как толуол, ксилол или мезитилен; эфирные растворители, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан; кетоновые растворители, такие как ацетон или метилэтилкетон; и полярные апротонные растворители, такие как ацетонитрил, N,N-диметилформамид или N,N-диметилацетоамид.
Продукты формулы (I) могут быть выделены и очищены из реакционной смеси известными методами, такими как экстракция, перекристаллизация или хроматография.
Метод F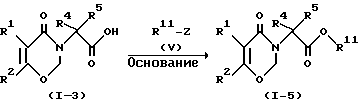
где R1, R2, R4, R5 являются такими, как они были определены в формуле (I); R11 является первичной или вторичной низшей алкильной группой или аралкильной группой; Z представляет собой атом галогена, п-толуолсульфонилоксигруппу, метилсульфонилоксигруппу, трифторметилсульфонилоксигруппу или группу, которая может быть хорошей уходящей группой при нуклеофильной реакции, например группу формулы OSO2OR11.
Соединение формулы (1-5) может быть получено с помощью реакции соединения формулы (1-3) с соединением формулы (V) в присутствии основания.
Реакцию осуществляют предпочтительно при температуре в пределах от комнатной температуры до около 140oC или до точки кипения растворителя.
Выбор растворителя для использования в реакции не имеет конкретных ограничений, за исключением того, что он должен быть инертным в условиях метода F; при этом предпочтительными примерами растворителя могут служить полярные апротонные растворители, такие как N,N-диметилформамид, диметилсульфоксид, ацетонитрил или ацетон; эфирные растворители, такие как тетрагидрофуран или диоксан; спирты, такие как метанол или этанол; и смеси указанных растворителей с водой.
Примерами основания являются неорганические карбонаты, такие как карбонат калия, бикарбонат калия, карбонат натрия или бикарбонат натрия; неорганические основания, такие как гидроксид натрия или гидроксид калия; метоксид натрия; и гидрид натрия. Если необходимо, то основание может быть также использовано в виде соли, образованной соединением формулы (1-3).
Продукт, имеющий общую формулу (1-5), может быть выделен или очищен из реакционной смеси стандартными методами, такими как экстракция, перекристаллизация или хроматография.
Метод G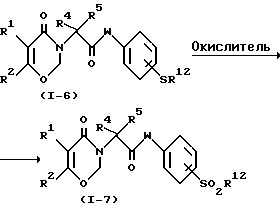
где R1, R2, R3, R4, R5 и W являются такими, как они были определены в общей формуле (I), а R12 является низшей алкильной группой.
Соединение, представленноe общей формулой (1-7), может быть получено путем окисления соединения формулы (1-6) с использованием соответствующего окисляющего агента.
Примерами окисляющего агента могут служить перекись водорода, м-хлоропербензойная кислота, метапериодат натрия, перуксусная кислота и перманганат калия.
Реакционная температура предпочтительно составляет от 0 до около 140oC или до точки кипения растворителя.
Выбор растворителя для использования в реакции не имеет конкретных ограничений, за исключением того, что он должен быть инертным в условиях метода G, при этом предпочтительными растворителями являются галогенированные углеводородные растворители, такие как 1,2-дихлорэтан, тетрахлорометан, хлороформ или метиленхлорид; метанол; уксусная кислота и их смеси.
Метод H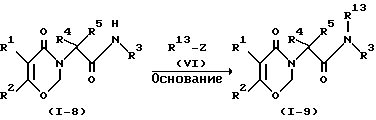
где R1, R2, R3, R4 и R5 являются такими, как они были определены в формуле (I); R13 представляет собой первичную или вторичную алкильную группу, низшую аралкенильную группу или низшую алкильную группу; а Z является таким, как он был определен в общей формуле (V).
Соединение формулы (1-9) может быть получено с помощью реакции соединения формулы (1-8) с соединением формулы (VI) в присутствии основания.
Реакцию осуществляют предпочтительно при температуре в пределах от комнатной температуры до около 140oC или до точки кипения растворителя.
В данной реакции может быть использован любой растворитель без каких-либо конкретных ограничений за исключением того, что должен быть инертным в условиях метода H; при этом предпочтительными растворителями являются полярные апротонные растворители, такие как N,N-диметилформамид, диметилсульфоксид, ацетонитрил или ацетон: эфирные растворители, такие как тетрагидрофуран или диоксан; спирты, такие как метанол или этанол; и смеси указанных растворителей с водой.
Примерами основания являются неорганические карбонаты, такие как карбонат калия, бикарбонат калия, карбонат натрия или бикарбонат; неорганические основания, такие как гидроксид натрия или гидроксид калия; метоксид натрия и гидрид натрия.
Продукты формулы (1-9) могут быть выделены и очищены из реакционной смеси с использованием известных методов, таких как экстракция, перекристаллизация или хроматография.
Соединение настоящего изобретения, имеющее общую формулу (I), обладает сильной гербицидной активностью против многих видов сорняков, и очень слабой фитотоксичностью в отношении культурных растений.
Если в качестве гербицида используется соединение общей формулы (I), то для получения композиций, которые обычно используются в качестве агрохимикатов, например смачивающихся порошков, гранул, вододиспергируемых гранул, концентратов эмульсий или концентратов суспензий, указанное соединение смешивают с агрохимически и садоводчески приемлемым носителем, разбавителем, добавками или адъювантом известными методами. Это соединение может быть смешано или использовано вместе с другими агрохимикатами, например с фунгицидами, инсектицидами, метицидами, гербицидами, регуляторами роста растений, удобрениями и кондиционерами почвы.
В частности, совместное использование соединения настоящего изобретения с другими гербицидами может привести не только к снижению дозы и трудовых затрат, но также и к расширению гербицидного спектра, обуславливаемому совокупной активностью, и к еще большему увеличению эффективности, обуславливаемому синергическим действием обоих агентов.
Ниже приводятся конкретные примеры других гербицидов, используемых в таком состоянии, при котором они могут смешиваться c соединениями настоящего изобретения, представленными общей формулой (I) (в скобках указано общепринятое название соединения, если это не оговорено особо).
Карбаматные гербициды:
метил-3,4-дихлорофенилкарбамат (Свеп);
изопропил-3-хлорофенилкарбамат (Хлоропрофам);
S-(4-хлоробензил)-диэтилтиокарбамат (Бентиокарб);
S-этил-N,N-гексаметиленэтиокарбамат (Молинат);
S-(1-метил-1-фенилэтил)-пиперидин-1-карботиоат (Димепиперат);
S-бензил-N-этил-N-(1,2-диметилпропил)тиолкарбамат (Эспрокарб);
3-(метоксикарбонил)аминофенил N-(3-метилфенил)карбамат (Фенмедифам);
этил-3-фенилкарбамоилоксифенилкарбамат (Десмедифам) и т.п.
Мочевинные гербициды:
1-(α,α-диметилбензил)-3-(4-метилфенил)мочевина (Димрон);
3-(3,4-дихлорофенил)-1,1-диметилмочевина (Диурон);
1,1-диметил-3- (α,α,α-трифторо-м-толил)мочевина (Флуометурон);
3-[4-(4-хлорофенокси)фенил]-1,1-диметилмочевина (Хлороксурон);
3-(3,4-дихлорофенил)-1-метокси-1-метилмочевина (Линурон);
3-(4-хлорофенил)-1-метокси-1-метилмочевина (Монолинурон);
3-(4-бром-3-хлорофенил)-1-метокси-метилмочевина (Хлорбромурон);
1-(α,α-диметилбензил)-3-(2-хлоробензил)мочевина (номер кода JC-940) и т. д.
Галогеноацетамидные гербициды:
2-xлоро-2',6'-диэтил-N-метоксиметилацетанилид (Алахлор);
N-бутоксиметил-2-хлор-2',6'-диэтилацетанилид (Бутахлор);
2-хлоро-N-изопропилацетанилид (Проахлор) и т.п.
Амидные гербициды:
3',4'-дихлоропропионанилид (Пропанил);
2-бромо-N-(1,1-диметилбензил)-3,3-диметилбутанамид (Бромобутид);
2-бензотиазол-2-илокси-N-метилацетанилид (Мефенацет);
N,N-диметилдифенилацетамид (Дифенамид) и т.п.
Динитрофениловые гербициды:
4,6-динитро-о-крезол (DNOC);
2-трет-бутил-4,6-динитрофенол (Динотерб);
2-втор-бутил-4,6-динитрофенол (Диносеб);
N,N-диэтилдинитро-4-трифторометил-м-фенилендиамин (Динитрамин);
α,α,α-трифторо-2,6-динитро-N,N-дипропил-п-толуидин (Трифлуралин);
4-метил-сульфонил-2,6-динитро-N,N-дипропиланилин (Нитралин);
N-(1-этилпропил)-2,6-динитро-3,4-ксилидин (Пендиметалин) и т.п.
Фенокси-гербициды:
2,4-дихлорофеноксиуксусная кислота (2,4-D);
2,4,5-трихлорофеноксиуксусная кислота (2,4,5-Т);
4-хлоро-о-толилоксиуксусная кислота (MCPA);
S-этил-(4-хлоро-2-метилфенокси)-этанэтиоат (тиоэтил-MCPA);
4-(4-хлоро-о-толилокси)масляная кислота (MCPB);
4-(2,4-дихлорофенокси)масляная кислота (2,4-DB);
2-(4-хлоро-о-толилокси)пропионовая кислота (Мекопроп);
2-(2,4-дихлорофенокси)пропионовая кислота (Дихлорпроп);
(RS)-2-[4-(2,4-дихлорофенокси)фенокси пропионовая кислота (Диклофоп)
и ее сложные эфиры;
(RS)-2-[4-(5-трифторометил-2-пиридилокси)]-пропионовая кислота (Флуазифоп) и ее сложные эфиры;
2-(2,4-дихлоро-3-метилфенокси)пропионанилид (Кломепроп);
S-этил-4-хлоро-2-метилфенокси-тиоацетат (Фенотиол);
2-(2-нафтокси)пропионанилид (Напроанилид) и т.п.
Гербициды на основе карбоновых кислот:
2,2-дихлорпропионовая кислота (Далапон);
трихлороуксусная кислота (TCA);
2,3,6-трихлоробензойная кислота (2,3,6-TBA);
3,6-дихлоро-о-анисовая кислота (Дикамба);
3-амино-2,5-дихлоробензойная кислота (Хлорамбен) и т.п.
Фосфорорганические гербициды:
О-этил О-(2-нитро-5-метилфенил)-N-втор-бутил-фосфорамидэтионат (Бутамифос);
О-О-диизопропил S-(2-бензолсульфониламиноэтил)фосфородитионат (SAP);
S-(2-метилпиперидин-1-ил)-карбонилметил-О, О-дипропил-фосфородитиоат (Пиперофос) и т.д.
Бензонитрильные гербициды:
2,6-дихлоробензонитрил (Дихлоробенил);
3,5-дибромо-4-гидроксибензонитрил (Бромоксинил);
4-гидрокси-3,5-дииодобензонитрил (Локсинил) и т.п.
Дифенилэфирные гербициды:
2,4-дихлорофенил 4-нитрофениловый эфир (Нитрофен);
2,4,6-трихлорофенил 4'-нитрофениловый эфир (Хлорнитрофен);
2,4-дихлорофенил 3-метокси-4-нитрофениловый эфир (Хлорометоксифен);
метил 5-(2,4-дихлорофенокси)-2-нитробензоат (Бифенокс);
4-нитрофенил α,α,α-трифторо-2-нитро-п-толиловый эфир (Фтордифен);
2-хлоро-4-трифторометилфенил-3-этокси-4-нитрофениловый эфир (Оксифторфен);
5-(2-хлоро-α,α,α-трифтор-п-толилокси)-2-нитробензойная кислота (Ацифторфен);
5-(2-хлоро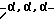 трифторо-п-толилокси)-2-нитробензойная кислота т.п.
трифторо-п-толилокси)-2-нитробензойная кислота т.п.
Триазиновые гербициды:
4-aмино-3-метил-6-фенил-1,2,4-триазин-5(4H)-он (Метамитрон);
4-амино-6-трет-бутил-3-метилтио-1,2,4-триазин-5(4H)-он (Метрибузин);
2-хлоро-4,6-бис-(этиламино)-1,3,5-триазин (Симетрин);
2,4-бис(изопропиламино)-6-метилтио-1,3,5-триазин (Прометрин);
2-(1,2-диметилпропиламино)-4-этиламино-6-метилтио-1,3,5-триазин (Диметаметрин) и т.п.
Гербициды на основе сульфомочевины:
2-xлоро-N-[4-метокси-6-метил-1,3,5-триазин-2-ил)амино-карбонил бензолсульфонамид (Хлоросульфон);
метил 2{ [((4,6-диметоксипиримидин-2-ил)аминокарбонил)аминосульфонил] метил}-бензоат (Метилбензульфурон);
этил 2-{[(4-хлоро-6-метоксипиримидин-2-ил)аминокарбонил]аминосульфонил} бензоат (Этилхлоримурон) и т.п.
Диазиновые гербициды:
4-(2,4-дихлоробензоил)-1,3-диметилпиразол-5-ил-п-толуолсульфонат (Пиразолат);
1,3-диметил-4-(2,4-дихлоробензоил)-5-фенацилоксипиразол (Пиразоксифен);
1,3-диметил-4-(2,4-дихлоро-3-метил-бензоил)-5-(4-метилфенацилокси) пиразол (Бензофенап) и т.п.
Другие гербициды:
3,6-дихлоропиридин-2-карбоновая кислота (Клопиралид);
4-амино-3,5,6-трихлоропиридин-2-карбоновая кислота (Пиклорам);
5-амино-4-хлоро-2-фенил-пирадизин-3(2H)-он (Хлоридазон);
3-циклогексил-1,5,6,7-тетрагидроцикло-ментенопиримидин-2,4 (3H)-дион (Ленацил);
5-бромо-3-втор-бутил-6-метилурацил (Бромацил);
3-трет-бутил-5-хлоро-6-метилурацил (Тербацил);
3-изопропил-(1H)-2,1,3-бензотиадизин-4(3H)-он-2,2-диоксид (Бентазон);
N-1-нафтилфталамовая кислота (Нафталам) и т.п.
В композиции, содержащей соединения настоящего изобретения как отдельно, так и в смеси с другими гербицидами, в качестве агрономически и садоводчески приемлемых носителей и разбавителей могут быть использованы твердые или жидкие носители, которые обычно применяются в сельскохозяйственной практике.
Примерами твердых носителей или разбавителей являются глины, такие как каолиниты, монтмориллониты, иллиты, палигорскиты и т.п.; а в частности, пироффиллит, аттапульгит, сепиолит, каолинит, бентонит, вермикулит, слюда, тальк и т.п.; и другие неорганические вещества, такие как гипс, карбонат кальция, доломит, диатомовая земля, магнезиевый известняк, фосфоритовый известняк, цеолит, ангидрид кремниевой кислоты, синтетический силикат кальция и т. п. ; органические вещества растительного происхождения, такие как соевая мука, мука из листьев табака, мука из ядер орехов, пшеничная мука, древесные опилки, крахмал, кристаллическая целлюлоза и т.п.; синтетические или натуральные полимеры, такие как кумаровая смола, кумароноинденовая смола, алкидная смола, поливинилхлорид, полиалкиленгликоль, кетонная смола, этерифицированная канифоль, копаловая смола, демаровая смола и т.п.; воски, такие как воск карнаубы, пчелиный воск и т.п.; или мочевина и т.п.
Примерами подходящих жидких носителей или разбавителей являются углеводороды парафинового ряда или нафтенового ряда, такие как керосин, минеральное масло, веретенное масло, вазелиновое масло и т.п.; ароматические углеводороды, такие как ксилол, этилбензол, кумол, метилнафталин и т.п.; хлорированные углеводороды, такие как рихлороэтилен, монохлоробензол, о-хлортолуол и т. п. ; сложные эфиры, такие как диоксан, тетрагидрофуран и т.п.; кетоны такие как ацетон, метилэтилкетон, диизобутилкетон, циклогексанон, ацетофенон, изофорон; сложные эфиры, такие как этилацетат, амилацетат, этиленгликольацетат, диэтиленгликольацетат, дибутилмалеат, диэтилсукцинат, и т.п.; спирты, такие как метанол, н-гексанол, этиленгликоль, диэтиленгликоль, циклогенсанол, бензиловый спирт и т.п.; неполные эфиры многоатомные спирты, такие как этиловый эфир элиленгликоля, бутиловый эфир диэтиленгликоля и т.п. ; полярные растворители, такие как диметилформамид, диметилсульфоксид и т.п. ; или вода.
Кроме того, для различных целей, например, таких как эмульгирование, диспергирование, увлажнение, распыление по поверхности, объемное расширение, комплексное регулирование деструкции, стабилизация активных ингредиентов, улучшение текучести, предупреждение коррозии, предупреждение затвердевания и т. п. соединений настоящего изобретения, могут быть использованы поверхностно-активные вещества (ПАВ) и другие добавки.
В качестве ПАВ могут быть использованы неионогенные, анионогенные, катионогенные, и амфотерные ПАВ, хотя обычно используются неионогенные и/или анионогенные поверхностно-активные вещества. Примерами походящих неионогенных ПАВ являются продукты присоединения этиленоксида к высшим спиртам, таким как лауриловый спирт, стеариловый спирт, олеиловый спирт и т.п.; продукты присоединения этиленоксида к алкилнафтолам, таким как бутилнафтол, октилнафтол и т. п. ; продукты присоединения этиленоксида к высшим жирным кислотам, таким как пальмитиновая кислота, стеариновая кислота, олеиновая кислота и т.п.; сложные эфиры высших жирных кислот и многоатомных спиртов, таких как сорбитан; а также продукты присоединения этиленоксида с указанными эфирами и т.п.
Примерами подходящих анионогенных поверхностно-активных веществ являются соли алкилсульфатов, такие как лаурилсульфат натрия; аминовые соли сложных эфиров серной кислоты и олеилового спирта и т.п.; соли алкилсульфонатов, такие как диоктилсульфосукцинат натрия, 2-этилгексилсульфонат натрия и т.п.; соли арилсульфонатов, такие как изопропилнафталинсульфонат натрия, метиленбиснафталинсульфонат натрия, лигносульфонат натрия, додецилбензолсульфонат натрия и т.п.
Кроме того, в целях улучшения свойств композиций, увеличения их эффективности и т. п., гербициды настоящего изобретения могут быть использованы в комбинации с полимерами и другими добавками, такими как казеин, желатин, альбумин, клей, альгинат натрия, карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиэтилцеллюлоза, поливиниловый спирт и т.п.
В зависимости от целей, принимаемых во внимание при изготовлении данной композиции, условий ее применения и т.п., вышеуказанные носители или разбавители, а также различные добавки могут быть использованы как отдельно, так и в комбинации с другими носителями или добавками.
Содержание активных ингредиентов в различных полученных таким образом композициях настоящего изобретения может широко варьировать в зависимости от формы композиции, но в основном оно составляет в пределах 0,1-99 мас.%, а предпочтительно 1 - 80 мас.%.
Содержание активных ингредиентов в смачивающемся порошке составляет в основном 25 - 90%, а остальное количество составляют твердые носители или разбавители и смачивающие диспергирующие агенты. Если необходимо, то в композицию могут быть добавлены коллоидные защитные агенты, противовспенивающие агенты и т.п.
В гранулах, например, содержание активных соединений составляет в основном 1-35%, а остальное количество составляют твердые носители или разбавители и поверхностно-активные вещества. Соединения, используемые в качестве активных ингредиентов, могут быть смешаны с твердыми носителями или разбавителями до получения однородной смеси либо они могут быть равномерно фиксированы или адсорбированы на поверхности твердых носителей или разбавителей. Диаметр гранул составляет предпочтительно в пределах от около 0,2 до 1,5 мм.
В концентрате эмульсии, например, содержание активных соединений составляет в основном 5 - 30%, а эмульгаторов от около 5 до 20 мас.%, остальное же количество составляют жидкие носители или разбавители. Если необходимо, то в композицию могут быть добавлены агенты для улучшения разбрызгивания и противокоррозионные агенты.
В концентрате суспензии, например, содержание активных соединений составляет в основном 5 - 50%, а диспергирующих смачивающих агентов 3 - 10 мас.%, остальное же количество составляет вода. Если необходимо, то в композицию могут быть добавлены защитные коллоидные агенты, консерванты, противовспенивающие агенты и т.п.
Соединения настоящего изобретения могут быть использованы в качестве гербицидов как в чистом виде, так и в виде композиций, описанных выше.
Гербициды настоящего изобретения могут быть внесены в эффективных количествах на различные участки, требующие защиты, например, на сельскохозяйственные угодья, такие как орошаемые рисовые поля и неорошаемые поля или земли, не занятые под культурой, до прорастания сорняков или на сами сорняки, находящиеся на различных стадиях своего развития, начиная от момента прорастания вплоть до последующих периодов их роста. Доза активных ингредиентов составляет в основном в пределах от 0,1 до 10000 г/га, а предпочтительно от 1 до 5000 г/га. Эта доза может варьировать в зависимости от вида сорняков-мишеней, стадии их роста, места нанесения, погодных условий и т.п.
Соединение формулы (I) и гербицид настоящего изобретения обладают сильным гербицидным действием на многие виды сорняков, но при этом они обладают очень слабой фитотоксичностью по отношению к полезным культурам, как это будет показано в нижеследующих примерах.
Так, например, соединение настоящего изобретения, взятое в очень небольших дозах, обнаруживает высокую гербицидную активность по отношению к однолетним сорнякам, находящимся на самых разных стадиях развития, начиная от периода прорастания и кончая периодом роста, например, таким сорнякам как Echinochloa crus-galli (просо куриное), Cyperus difformis (сыть разнородная), Monochoria vaginalis (монохория влагалищная), Rotala indica (Ротала), Zindernia procumbens (Линдерния), Dopatrium junceum (ситник), Eleocharis acicularis (болотница) и Alisma canaliculatum (частуха обыкновенная); а также по отношению к многолетним сорнякам, находящихся на различных стадиях своего развития, например, таких как Scirpus juncoides (камыш) и Cyperus serotinus (сыть скрученная); при этом указанное соединение настоящего изобретения является в высокой степени безопасным по отношению к культуре риса-падди. Другим отличительным признаком соединения настоящего изобретения является то, что при почвенной или стеблевой и листовой обработке это соединение оказывает сильное гербицидное действие на различные сорняки, наносящие ущерб неорошаемому земледелию, например на многолетние и однолетние сорняки семейства Осоковых, таких как Cyperus rotundus (сыть круглая), Cyperus esculontus (сыть съедобная), Cyperus brevifolius, Cyperus microitia и Cyperus iria; и Echinochloa crus-galli (просо куриное), Digitaria sanguinalis (росичка кроваво-красная), Setaria viridis (щетинник зеленый), Poa annua (мятлик однолетний), Sorghum halepense (сорго алленское), Avena sativa (овес посевной) и Alopecurus myosuroides (лисохвост), а также широколистные сорняки, такие как Polygonum lapathifolium (горец), Amaranthus viridis (щирица зеленая), и Chenopodium album (марь белая); при этом указанное соединение является в высокой степени безопасным по отношению к таким культурным растениям, как соя, хлопчатник, сахарная свекла, кукуруза, неорошаемый рис, пшеница и т.п.
Кроме того, соединение настоящего изобретения может быть использовано не только для защиты орошаемых и неорошаемых полей, но также и для защиты плодовых садов, плантаций тутового дерева, газонов и земель, не занятых под культурой.
Соединение настоящего изобретения может быть также использовано в комбинации с другими известными агрохимикатами, и в результате такого совместного использования может быть получен полный гербицидный эффект в отношении таких сорняков, которые трудно поддаются уничтожению под действием какого-либо одного гербицидного соединения, но которые могут быть с высокой степенью эффективности уничтожены благодаря синергическому гербицидному действию соединений, взятых в дозах, при которых одно соединение, взятое отдельно, является неэффективным. Эти соединения также являются в высокой степени безопасными по отношению к культурам риса-падди, сои, хлопчатника, сахарной свеклы, кукурузы, неорошаемого риса, пшеницы и т.п., в результате чего могут быть получены гербициды, обладающие очень высокой эффективностью при их использовании в сельском хозяйстве.
Получение соединения формулы (I) и промежуточного соединения формулы (II) более подробно описано в следующих примерах.
Пример 1.
Получение метил-2-(N-метиленамино)-2-метилбутирата (cоединение N 2-15).
К метил 2-амино-2-метилбутирату (2,62 г) при комнатной температуре по капле добавляли 37%-ный формалин (2,27 г), и полученную смесь растворяли в эфире и промывали водой. Органическую фазу осушали сульфатом магния, фильтровали и выпаривали, в результате чего получали целевое соединение (2,80 г).
Пример 2.
Получение метил-2-метил-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-бутирата (cоединение N 651).
К смеси, состоящей из 2,2,6-триметил-5-фенил-4H-1,3-диоксин-4-она (2,18 г) и метил 2-(N-метиленамино)-2-метилбутирата (1,5 г), добавляли 20 мл ксилола и эту смесь нагревали с обратным холодильником в течение 1 ч. После выпаривания растворителя остаток очищали с помощью колоночной хроматографии на силикагеле и получали целевое соединение (2,4 г).
Пример 3.
Получение 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H- 1,3-оксазин-3-ил)масляной кислоты (cоединение N 650).
К раствору метил 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо- 4H-1,3-оксазин-3-ил)бутирата (1,91 г) в 20 мл этанола при комнатной температуре добавляли 30 мл водного раствора 0.3 н NaOH. После перемешивания в течение 24 ч этанол выпаривали, а смесь подкисляли соляной кислотой. Осадок отфильтровывали и осушали с получением целевого соединения (1,36 г).
Пример 4.
Получение бензил 2-(N-метиленамино)-2-метилпропионата (cоединение N 2-10).
К бензилу 2-амино-2-метилбутирату (12,96 г) при комнатной температуре по капле добавляли 37%-ный формалин (7,62 г) и эту смесь перемешивали в течение 4 ч. Полученную реакционную смесь растворяли в эфире и промывали водой. Органическую фазу осушали сульфатом магния, фильтровали и выпаривали, в результате чего получали целевое соединение (13,7 г).
Пример 5.
Получение бензил 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо- 4H-1,3-оксазин-3-ил)пропионата (cоединение N 645).
К смеси 2,2,6-триметил-5-фенил-4H-1,3-диоксин-4-она (13,97 г) и бензил 2-(N-метиленамино)-2-метилпропионата (13,8 г) добавляли 130 мл ксилола и полученную смесь нагревали с обратным холодильником в течение 2 ч. После выпаривания растворителя остаток очищали с помощью хроматографии на колонках с силикагелем, в результате чего получали целевое соединение (21,1 г).
Пример 6.
Получение 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)пропионовой кислоты (cоединение N 634).
К раствору бензил 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо- 4H-1,3-оксазин-3-ил)пропионата (21,1 г) в 100 мл этанола добавляли 1 г 5%-ного палладия на угле и эту смесь гидрировали при нормальном давлении и комнатной температуре. После выпаривания этанола к смеси добавляли насыщенный водный раствор бикарбоната натрия, а катализатор отфильтровывали. Фильтр подкисляли путем добавления соляной кислоты. Образовавшийся осадок отфильтровывали и осушали, в результате чего получали целевое соединение (10,8 г).
Пример 7.
Получение этил 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)пропионата (cоединение N 636).
К смеси 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо- 4H-1,3-оксазин-3-ил)пропионовой кислоты (0,83 г) и карбоната калия (0,45 г) в 4 мл диметилформамида (ДМФ) добавляли этилиодид (0,56 г) и эту смесь перемешивали в течение 5 ч при температуре 60oC. Реакционную смесь выливали в воду и экстрагировали этилацетатом. Органический слой промывали солевым раствором, осушали сульфатом магния и выпаривали. Остаток очищали с помощью хроматографии на колонках с силикагелем и получали целевое соединение (0,87 г).
Пример 8.
Получение 3,5-дихлорофенил 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил) пропионата (cоединение N 506).
К суспензии 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H- 1,3-оксазин-3-ил)пропионовой кислоты (1,1 г) в 14 мл CCl4/CH2Cl2 (1:1) добавляли трифенилфосфин (1,38 г) и эту смесь нагревали с обратным холодильником в течение 40 мин. Полученную реакционную смесь охлаждали льдом, а затем медленно добавляли 3,5-дихлорофенол (0,65 г) и триэтиламин (0,4 г), после чего, смесь перемешивали при комнатной температуре в течение 1 ч. После выпаривания растворителя остаток растворяли в этилацетате. Затем нерастворившиеся вещества отфильтровывали, а фильтрат выпаривали. Остаток очищали с помощью хроматографии на колонках с силикагелем, в результате чего получали целевое соединение (0,7 г).
Пример 9,
Получение N-фенил-2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо- 4H-1,3-оксазин-3-ил)пропанамида (cоединение N 1).
К суспензии 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H- 1,3-оксазин-3-ил)пропионовой кислоты (0,83 г) в 10,4 мл CCl4/CH2Cl2 (1:1) добавляли трифенилфосфин (1,04 г) и эту смесь нагревали с обратным холодильником в течение 40 мин. Затем реакционную смесь охлаждали льдом, медленно добавляли анилин (0,28 г) и триэтиламин (0,3 г) и полученную смесь перемешивали в течение 1 ч при комнатной температуре. После выпаривания растворителя остаток растворяли в этилацетате. Затем нерастворившиеся вещества отфильтровывали, а фильтрат выпаривали. Остаток очищали с помощью хроматографии на колонках с силикагелем и получали целевое соединение (0,58 г).
Пример 10.
Получение N-(3,5-дихлорофенил)-2-метил-2-(6-метил-5-фенил-2,3- дигидро-4-оксо-4H-1,3-оксазин-4-ил)-пропанамида (cоединение N 27).
Целевое соединение (1,05 г) получали способом, аналогичным описанному в примере 9, за исключением того, что в качестве исходного продукта использовали 3,5-дихлороанилин.
Пример 11.
Получение N-[3-(трифторометил)фенил]-2-метил-2-(6-метил-5-фенил- 2,3-дигидро-4-оксо-4H-1,3-оксазин-4-ил)-пропанамида (cоединение N 93).
Целевое соединение (0,72 г) получали способом, аналогичным описанному в примере 9, за исключением того, что в качестве исходного продукта использовали 3-(трифторометил)анилин.
Пример 12.
Получение N-изопропил-2-метил-2-(6-метил-5-фенил- 2,3-дигидро-4-оксо-4H-1,3-оксазин-4-ил)-пропанамида (cоединение N 604).
К раствору 2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-пропионовой кислоты (0,83 г) в 6 мл тетрагидрофурана (ТГФ) добавляли карбонилдиимидазол (0,59 г). После перемешивания в течение 30 мин при комнатной температуре к смеси добавляли изопропиламин (0,23 г) и полученную реакционную смесь перемешивали в течение 5 ч при температуре 60oC. Затем эту смесь выливали в воду и экстрагировали этилацетатом. Органический слой промывали солевым раствором, осушали сульфатом магния и выпаривали. Остаток очищали с помощью хроматографии на колонках с силикагелем и получали целевое соединение (0,38 г).
Пример 13.
Получение N-(3,5-дихлорофенил)-N-метил-2-метил-2-(6-метил-5- фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-пропанамида (cоединение N 302).
Раствор N-(3,5-дихлорофенил)-N-метил-2-метил-2-(6-метил-5- фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-пропанамида (0,6 г) в 2 мл диметилформамида охлаждали в ледяной бане, а затем добавляли 60%-ный гидрид натрия в масле (0,06 г). После перемешивания в течение 30 мин при комнатной температуре к смеси добавляли метилиодид (0,31 г) и полученную смесь перемешивали при комнатной температуре в течение 5 ч. Затем реакционную смесь выливали в воду и экстрагировали этилацетатом. Органический слой промывали солевым раствором, осушали сульфатом магния и выпаривали. Остаток очищали с помощью хроматографии на колонках с силикагелем и получали целевое соединение (0,51 г).
Пример 14.
Получение N-[4-(метилсульфонил)фенил]-2-метил-2-(6-метил-5- фенил-2,3-дигидро-4H-4-оксо-4H-1,3-оксазин-3-ил)-пропанамида (cоединение N 151).
Раствор N-(4-метилтиофенил)-2-метил-2-(6-метил-5- фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-пропанамида (0,6 г) в 12 мл 1,2-дихлороэтана охлаждали в ледяной бане, а затем добавляли 70%-ную метахлоропербензойную кислоту (0,8 г). После перемешивания в течение 24 ч при комнатной температуре, реакционную смесь промывали насыщенным водным раствором бикарбоната натрия, осушали сульфатом магния и выпаривали. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали целевое соединение (0,5 г).
Пример 15.
Получение N-[2-фторо-5-(трифторометил)фенил] -2-метил-2-(6-метил-5-фенил-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)-пропанамида (cоединение N 363).
Целевое соединение (0,93 г) получали способом, аналогичным описанному в примере 9, за исключением того, что в качестве исходного соединения использовали 2-фторо-5-(трифторометил)анилин.
Пример 16.
Получение N-(3-хлорфенил)-2-метил-2-[6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропанамид (соединение N 271)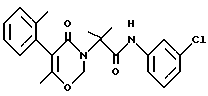
Целевое соединение получают в 4 стадии.
Стадия 1.
Получение бензил-2-(N-метиленамино)-2-метилпропионата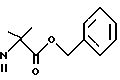
К бензил-2-амино-2-метилпропионату (13,0 г, 67 ммоль) прикапывают 37%-ный формалин (7,62 г, 94 ммоль) при комнатной температуре и смесь перемешивают в течение 4 ч.
Затем реакционную смесь растворяют в эфире и промывают водой. Органическую фазу сушат над сульфатом магния, фильтруют и выпаривают с получением указанного в заголовке соединения (13,7 г).
Стадия 2.
Получение бензил-2-метил-2-[6-метил-5-(2-толил)-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропионата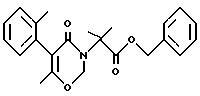
Смесь 2,2,6-триметил-5-(2-толил)-2H, 4H-1,3-диоксин-4-она (14,9 г, 64 ммоль), бензил-2-(N-метиленамино)-2-метилпропионата (13,7 г, 67 ммоль) и ксилола (130 мл) нагревают при температуре около 140oC в течение 2 ч, удаляя образующийся ацетон.
Реакционную смесь упаривают в вакууме досуха. Остаток очищают хроматографией на силикагеле с получением названного выше соединения (20,7 г, 85%).
Стадия 3.
Получение 2-метил-2-(6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропионовой кислоты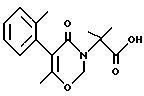
К раствору бензил 2-метил-2-(6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил)пропионата (20.7 г, 54,5 ммоль) в 100 мл этанола добавляют 1 г 5%-ного Pd на угле и проводят гидрирование при комнатной температуре и нормальном давлении.
После выпаривания этанола к смеси добавляют насыщенный водный раствор бикарбоната натрия и отфильтровывают катализатор.
Фильтрат подкисляют соляной кислотой.
Осадок отделяют фильтрованием и сушат с получением названного в заглавии соединения (11,4 г, 72%).
Стадия 4.
Получение N-(3-хлорфенил)-2-метил-2-[6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил)пропанамида (соединение N 271).
К суспензии 2-метил-2-(6-метил-5-(2-толил)-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил)пропионовой кислоты (0,87 г, 3 ммоль) в 10,4 мл смеси CCl4/CH2Cl2 (1: 1) добавляют трифенилфосфин (1,04 г, 3,9 ммоль) и нагревают при температуре кипения с обратным холодильником в течение 40 мин.
Реакционную смесь охлаждают льдом и медленно добавляют 3-хлоранилин (0,38 г, 3 ммоль) и триэтиламин (0,41 мл), затем перемешивают при комнатной температуре в течение 1 ч.
После выпаривания растворителя остаток растворяют в этилацетате.
Нерастворимый остаток отфильтровывают и фильтрат концентрируют в вакууме досуха. Остаток очищают хроматографически на колонке из силикагеля получением указанного в заглавии соединения (0,78 г, 65%).
Температура плавления 120-122oC.
1H-ЯМР (м. д.) (CDCl3, ТМС = 0 м.д.). 1,7 (с, 6H), 1,8 (с, 3H), 2,1 (с, 3H), 5,3 (с, 2H), 7,0 (м, 2H), 7,2 (м, 5H), 7,6 (т, 1H), 8,7 (с, 1H).
Соединения 276, 288 и 274 были получены в соответствии с вышеописанной методикой, но с использованием на 4-й стадии соответственно замещенных анилинов:
N-(3,5-дифторфенил)-2-метил-2-[6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропанамид (соединение N 274):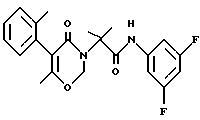
Температура плавления 112 - 114oC.
1H-ЯМР (м. д.) (CDCl3, ТМС = 0 м.д.). 1,7 (с, 6H), 1,8 (с, 3H), 2,1 (с, 3H), 5,3 (с, 2H), 6,5 (м, 1H), 7,1 - 7,3 (м, 6H), 8,8 (с, 1H).
N-(3,5-дихлорфенил)-2-метил-2-[6-метил-5-(2-толил)-2,3-дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропанамид (соединение N 276):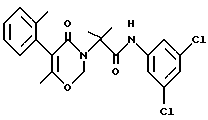
Температура плавления 154 - 160oC.
1H-ЯМР (м. д.) (CDCl3, ТМС = 0 м.д.). 1,7 (с, 6H), 1,8 (с, 3H), 2,1 (с, 3H), 5,3 (с, 2H), 7,0 - 7,3 (м, 5H), 7,5 (с, 2H), 8,8 (с, 1H).
N-[(3-трифторметил)-фенил)] -2-метил-2-[6-метил-5-(2-толил)-2,3- дигидро-4-оксо-4H-1,3-оксазин-3-ил]пропанамид (соединение N 288):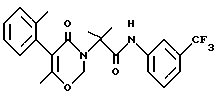
Температура плавления 116 - 118oC.
1H-ЯМР (м. д.) (CDCl3, ТМС = 0 м.д.). 1,7 (с, 6H), 1,8 (с, 3H), 2,1 (с, 3H), 5,3 (с, 2H), 7,1 (д, 1H), 7,2 - 7,4 (м, 5H), 7,7 (д, 1H), 7,8 (с, 1H), 8,8 (с, 1H).
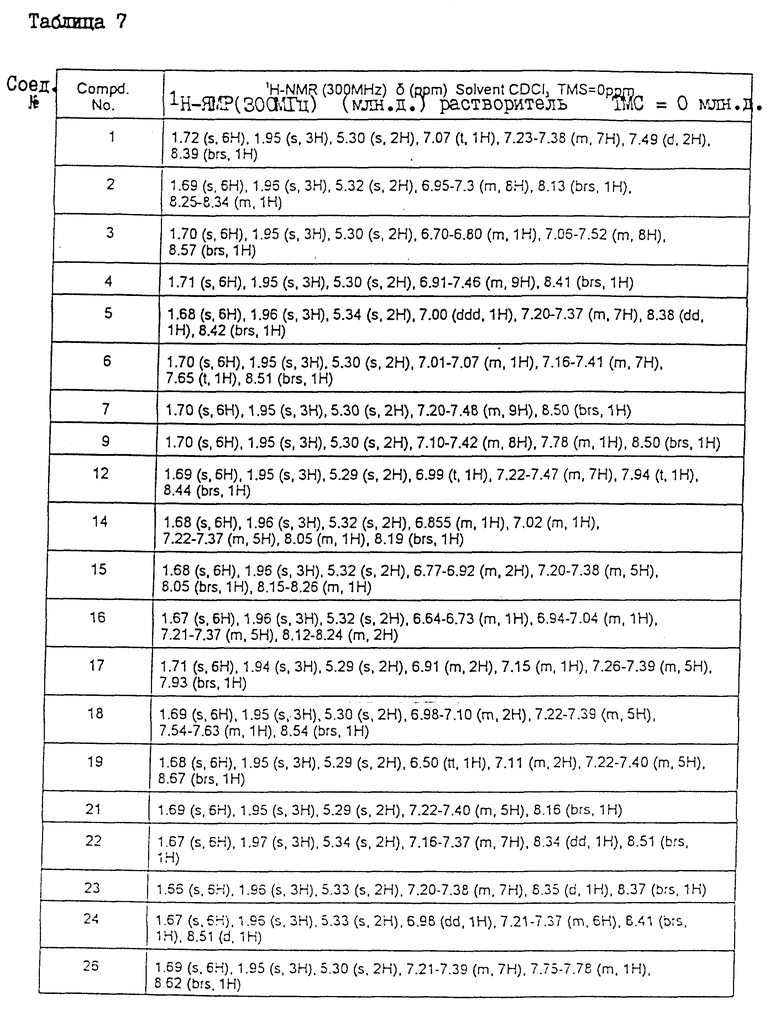
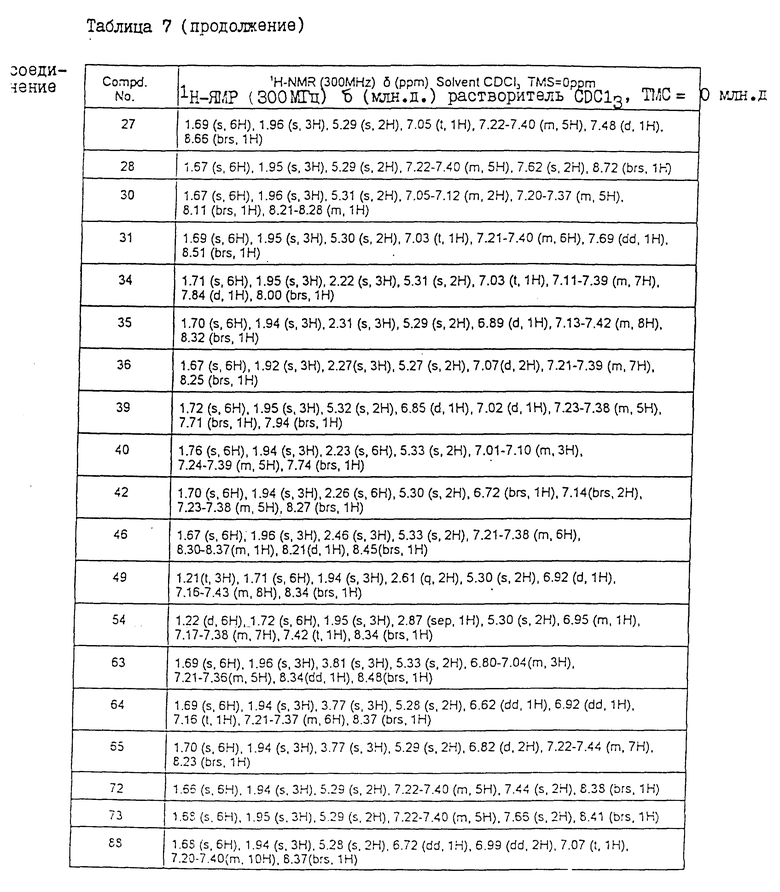
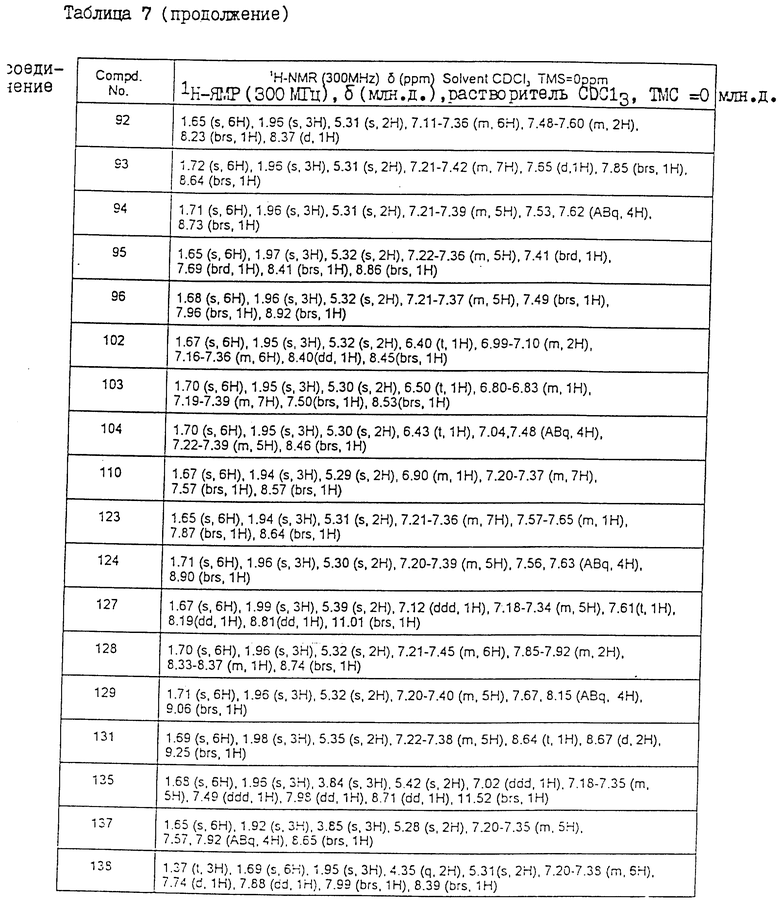
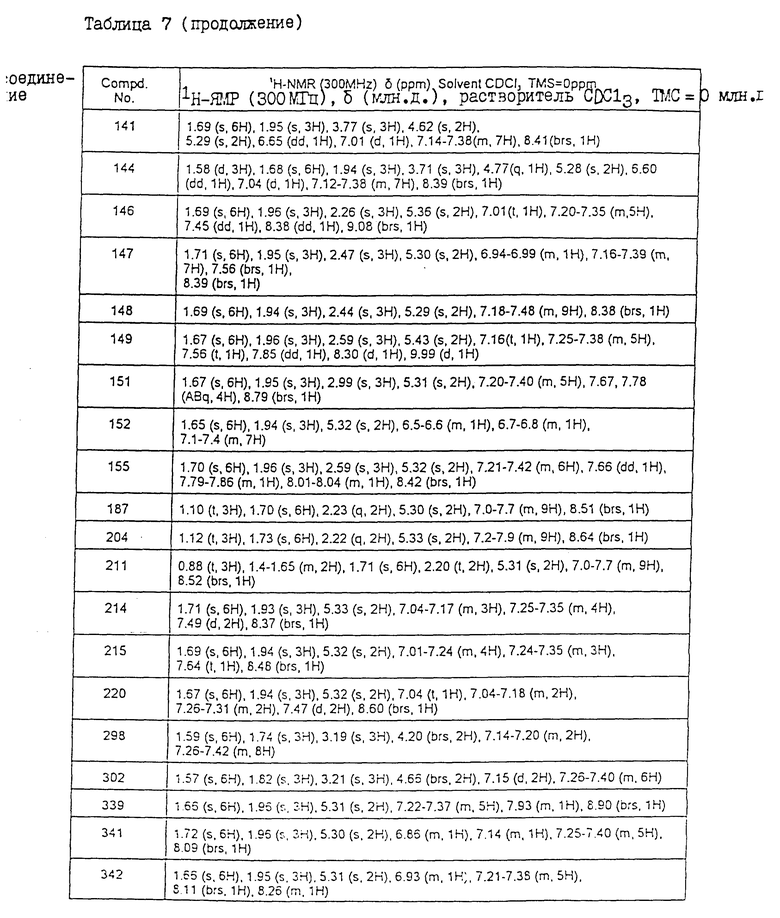
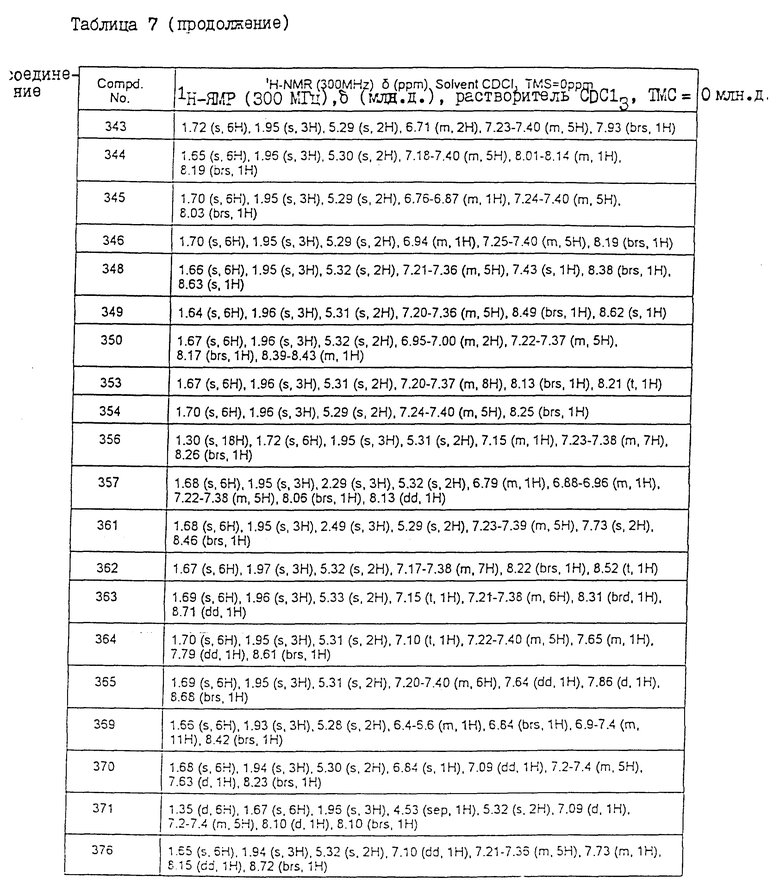
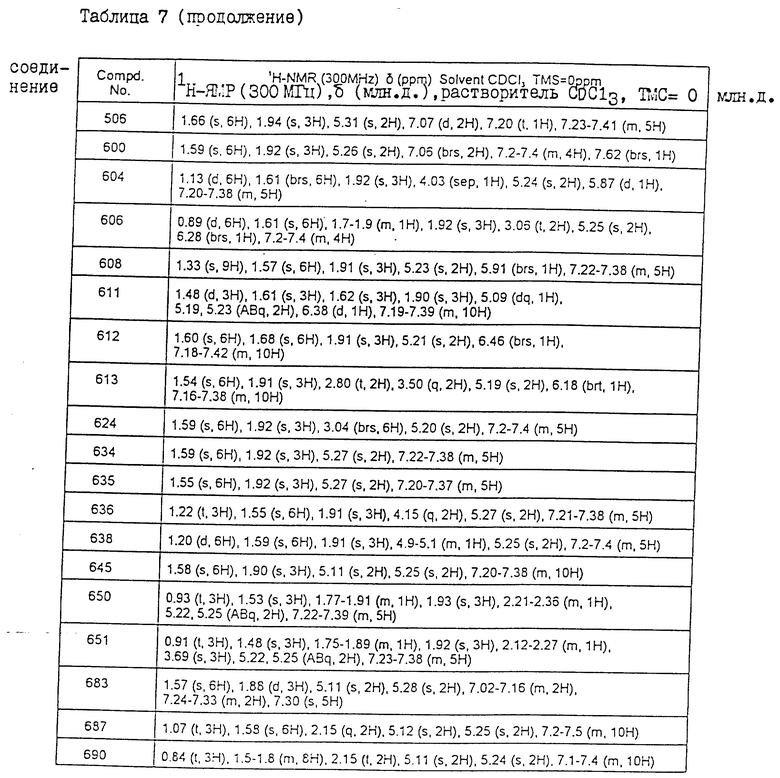
Физические свойства различных соединений, полученных аналогичными способами, описанными в примерах, показаны в табл. 1 - 6, а 1H-ЯМР-данные этих соединений представлены в табл. 7 и 8.
В табл. 7 и 8 используются следующие сокращения:
s - синглет (с)
t - триплет (т)
m - мультиплет (м)
d - дублет (д)
brs - широкий синглет (шир.с.)
q - квартет (кв.)
dd - двойной дублет (дд.)
ddd - двойной дублет дублетов (ддд.)
Далее представлено несколько вариантов получения композиций с использованием соединения настоящего изобретения. В представленных составах все "части" даны по массе.
Пример получения композиции 1 (концентрат эмульсии):
Соединение N 1 - 20 частей
Ксилол - 63 части
Додецилбензолсульфонат кальция - 7 частей
Полиоксиэтиленстирилфенилэфир - 5 частей
Диметилформамид - 5 частей
Вышеуказанные вещества смешивали до однородности и растворяли, в результате чего получали 100 частей концентрата эмульсии
Пример получения композиции 2 (cмачивающийся порошок):
Соединение N 1 - 20 частей
Каолинит - 70 частей
Лигносульфонат кальция - 7 частей
Конденсат алкилнафталенсульфоновой кислоты - 3 части
Вышеуказанные вещества смешивали и измельчали с использованием струйной мельницы, в результате чего получали 100 частей смачивающегося порошка.
Пример получения композиции 2 (концентрат суспензии):
Соединение N 1 - 20 частей
Ди(2-этилгексил)сульфосукцинат натрия - 2 части
Полиоксиэтиленнонифенилэфир - 2 части
Противопенное средство - 0,5 частей
Пропиленгликоль - 5 частей
Ксантановая камедь - 0,01 частей
Вода - 70,49 частей
Вышеуказанные вещества измельчали и смешивали до однородности с использованием шаровой мельницы мокрого помола, в результате чего получали 100 частей концентрата суспензии.
Пример получения композиция 4 (гранулы):
Соединение N 1 - 1 часть
Ди(2-этилгексил)сульфосукцинат натрия - 2 части
Бентонит - 30 частей
Тальк - 67 частей
Вышеуказанные вещества тщательно перемешивали, а затем замешивали с добавлением соответствующего количества воды и гранулировали с помощью гранулятора, в результате чего получали 100 частей гранул.
Гербицидное действие соединений настоящего изобретения будет подробно проиллюстрировано в нижеследующих примерах испытаний.
Испытательный пример 1 (внесение в почву орошаемых рисовых полей).
Вегетационные сосуды Вагнера (500 см2) заполняли почвой с орошаемыx рисовых полей, добавляли соответствующее количество воды и химических удобрений и замешивали для придания почве состояния, соответствующего орошаемым рисовым полям. Посадочный материал растений риса-падди (сорт Koshihikari), состоящий из пары двух проростков, которые были предварительно выращены в теплице до стадии двух листьев, высаживали в каждый из вегетационных сосудов в количестве одного посадочного материала на сосуд. Затем в каждый сосуд высевали заранее определенное количество семян Echinochloa crus-galli, Monochoria vaginalis, Zindernia procumbens и Sciprus juncoides соответственно, после чего сосуды заполняли водой до глубины 3 см.
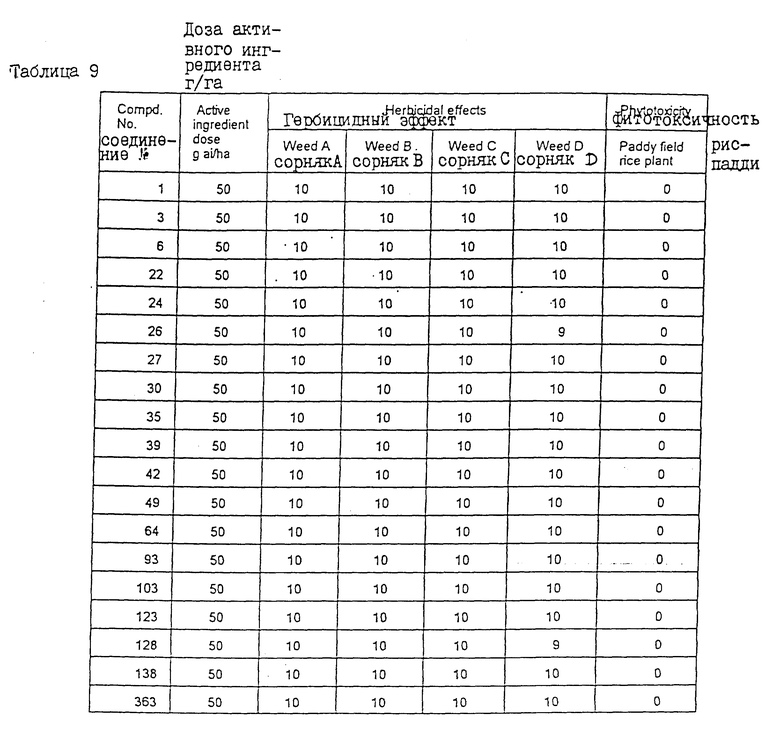
На следующий день с использованием соединений, представленных в табл. 9, и в соответствии с описанием, приведенным в примере получения композиции 2, получали смачивающиеся порошки, которые затем разводили соответствующим количеством воды так, чтобы эти порошки содержали активные ингредиенты в количестве 50 г/га. После этого полученную композицию вносили с помощью пипетки.
Через 21 день после внесения химикатов гербицидное действие этих химикатов на каждый из сорняков и их фитотоксичность в отношении культуры риса-падди оценивали в соответствии с нижеследующими критериями. Полученные результаты представлены в табл. 9.
В табл. 9 - 12 были использованы следующие сокращения в названиях сорняков:
Сорняк A: Echinocloa crus-galli
Сорняк B: Monochoria vaginalis
Cорняк C: Zindemia procumbens
Сорняк D: Scripus juncoides
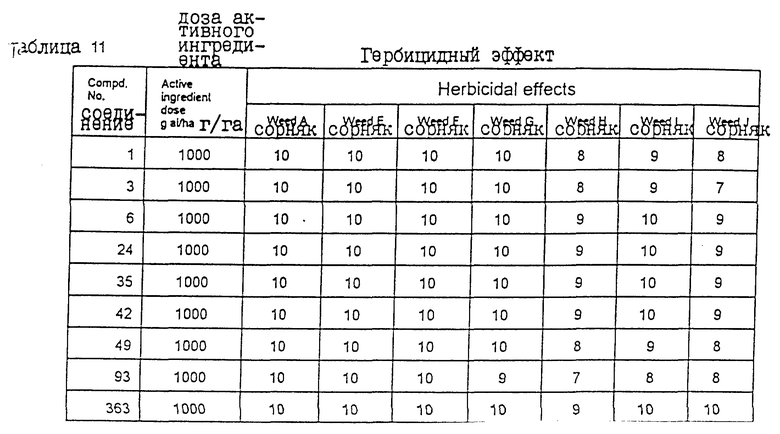
Сорняк E: Digitania sanguinalis
Сорняк F: Setaria viridis
Сорняк G: Abutilon theophrasti
Сорняк H: Xanthium strumarium
Сорняк I: Polygonum laparhifolium
Сорняк J: Datura stramonium
Пример испытаний 2 (листовая обработка на орошаемых рисовых полях).
Вегетационные сосуды Вагнера (500 см2) заполняли почвой с орошаемых рисовых полей, затем добавляли соответствующее количество воды и химических удобрений и замешивали для придания почве состояния, соответствующего орошаемым рисовым полям. Посадочный материал растений риса-падди (сорт Koshihikari), состоящий из пары двух проростков, которые были предварительно выращены в теплице до стадии двух листьев, высаживали в каждый из вегетационных сосудов в количестве одного посадочного материала на сосуд. Затем в каждый сосуд высевали заранее определенное количество семян Echinochloa crus-galli, Monochoria vaginalis, Zindernia procumbens и Scirpus juncoides соответственно, после чего сосуды заполняли водой до глубины 3 см.
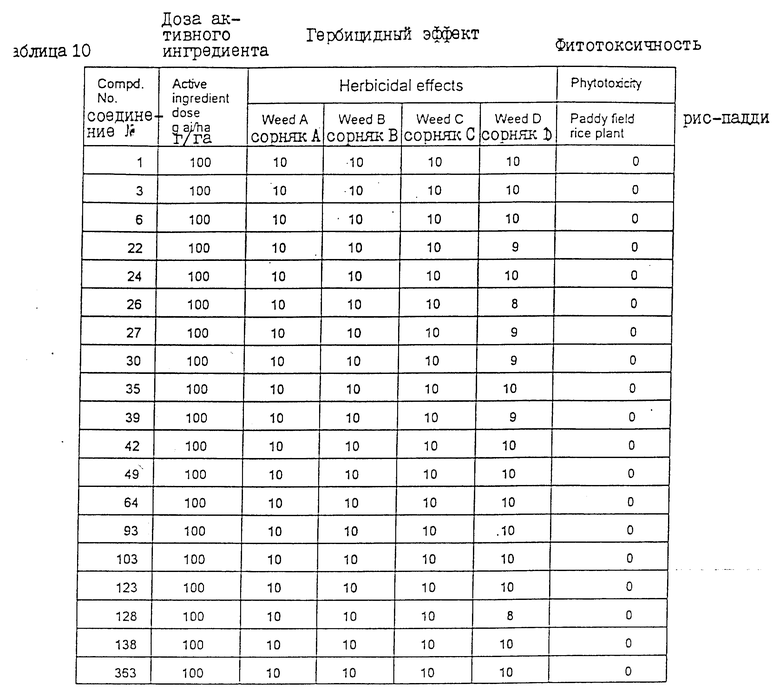
После выращивания растений в теплице до тех пор, пока Echinochloa crus-galli не достигали стадии в полтора листа, приготавливали (с использованием соединений, представленных в табл. 10, и в соответствии с описанием, приведенным в примере получения композиции 2) смачивающиеся порошки, которые затем разводили соответствующим количеством воды так, чтобы содержание в них активных ингредиентов составляло 100 г/га. После этого полученные композиции вносили с помощью пипетки.
Через 21 день после внесения химикатов гербицидное действие этих химикатов на каждый из сорняков и их фитотоксичность в отношении растений риса-падди оценивали в соответствии с критериями, указанными выше в примере испытаний 1. Полученные результаты представлены в табл. 10.
Пример испытаний 3 (внесение в неорошаемую почву).
В пластиковые сосуды (900 см2), наполненные почвой с неорошаемых полей, засевали заранее определенное количество семян Echinochloa crus-galli, Digitaria sanguinalis, Setaria viridis, Abutilon theophrasti, Xanthium strumarium, Polygonum laparhifolium и Datura stramonium соответственно, после чего их засыпали почвой толщиной 1 см.
На следующий день после посева приготавливали (с использованием соединений, представленных в табл. 11, и в соответствии с описанием, приведенным в примере получения композиции 2) смачивающиеся порошки, которые затем разводили соответствующим количеством воды так, чтобы содержание в них активных ингредиентов составляло 1 кг/га. Полученные композиции равномерно наносили на поверхность почвы путем опрыскивания.
Через 21 день после внесения химикатов гербицидное действие этих химикатов на каждый сорняк оценивали в соответствии с критериями, указанными выше в примере испытаний 1. Полученные результаты представленны в табл. 11.
Пример испытаний 4 (листовая обработка в условиях неорошаемого земледелия).
В пластиковые сосуды (900 см2), наполненные почвой с неорошаемых полей, засевали заранее определенное количество семян Echinochloa crus-galli, Digitaria sanguinalis, Setaria viridis, Abutilon theophrasti, Xanthium strumarium, Polygonum lapathifolium и Datura stramonium соответственно, после чего их присыпали почвой толщиной 2 см.
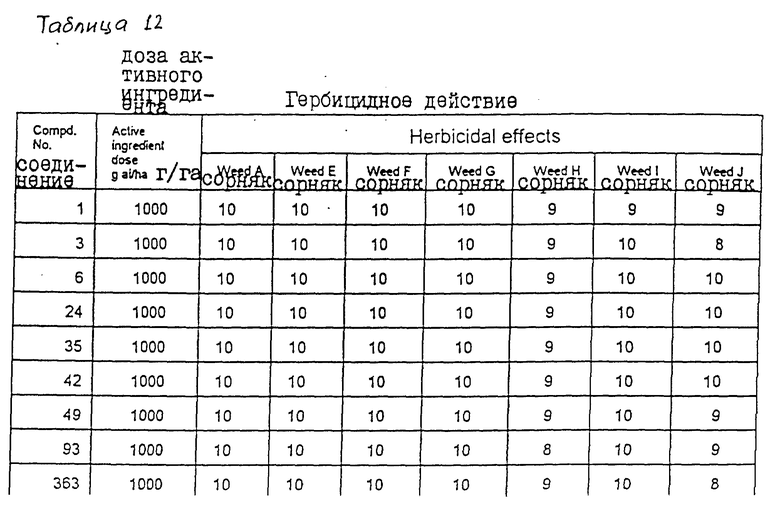
После выращивания растений в теплице до тех пор, пока каждое растение не достигало стадии 2 - 4 листьев, приготавливали смачивающиеся порошки (с использованием соединений, представленных в табл. 12, и в соответствии с описанием, приведенным в примере получения композиций 2), которые разводили соответствующим количеством воды так, чтобы содержание в них активных ингредиентов составляло 1 кг/га. После этого полученные композиции равномерно наносили на поверхность листьев путем опрыскивания.
Через 21 день после нанесения химикатов гербицидное действие этих химикатов на каждый сорняк оценивали в соответствии с критериями, указанными выше в экспериментальном примере 1. Полученные результаты представлены в табл. 12.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА | 1992 |
|
RU2049781C1 |
| ПРОИЗВОДНЫЕ ТРИАЗИНОНА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ ПОДАВЛЕНИЯ СОРНЯКОВ | 1989 |
|
RU2047296C1 |
| ПРОИЗВОДНЫЕ ПИКОЛИНОВОЙ КИСЛОТЫ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, НЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1991 |
|
RU2091380C1 |
| ПРОИЗВОДНЫЕ АЗОЛА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И АНТИГРИБКОВОЕ СРЕДСТВО | 1994 |
|
RU2131417C1 |
| ПРОИЗВОДНЫЕ СУЛЬФАМИДОСУЛЬФОНИЛМОЧЕВИНЫ И СЕЛЕКТИВНАЯ ГЕРБЕЦИДНАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2088583C1 |
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2028294C1 |
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ (ВАРИАНТЫ) | 1993 |
|
RU2133569C1 |
| ПРОИЗВОДНЫЕ ИМИНОСУЛЬФОНИЛМОЧЕВИНЫ, СПОСОБ УНИЧТОЖЕНИЯ ИЛИ ПОДАВЛЕНИЯ СОРНЯКОВ | 1992 |
|
RU2109011C1 |
| ПРОИЗВОДНЫЕ АМИДОВ ПИРАЗОЛГЛИКОЛЕВОЙ КИСЛОТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1992 |
|
RU2090560C1 |
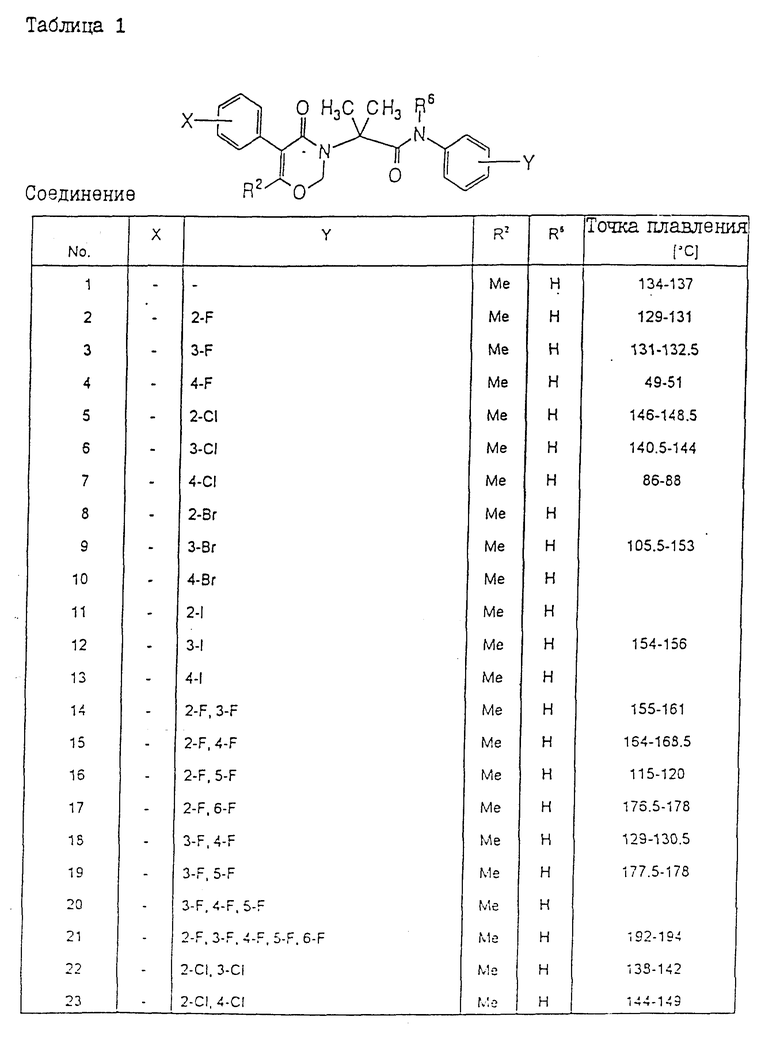

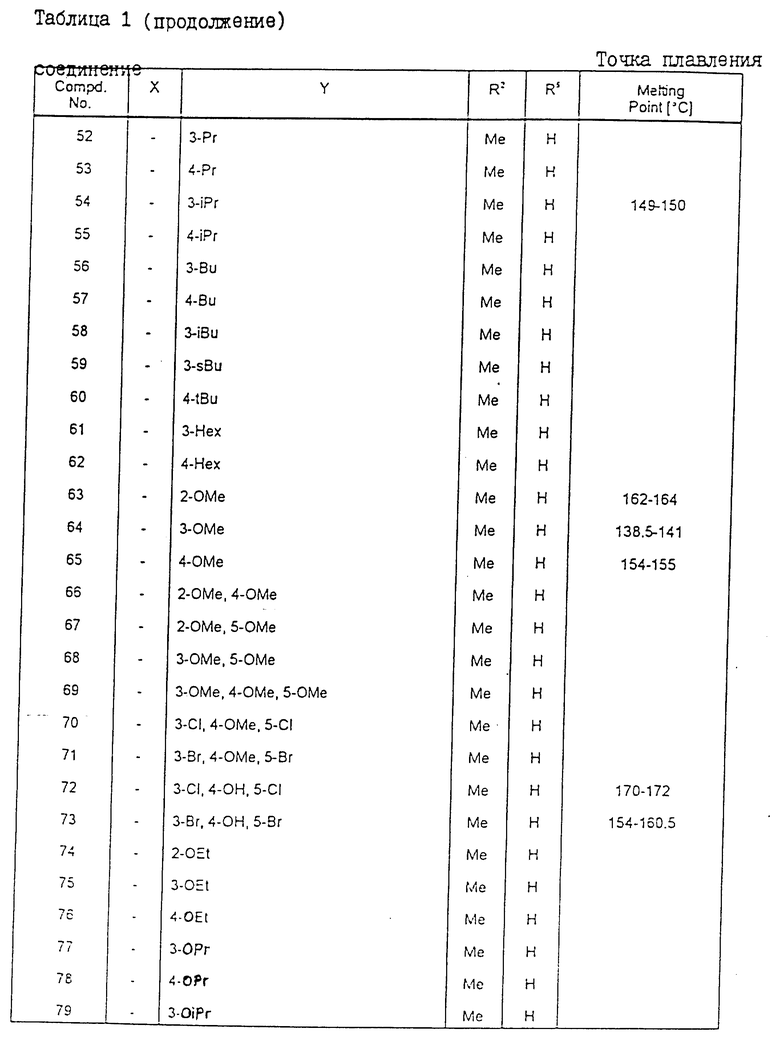
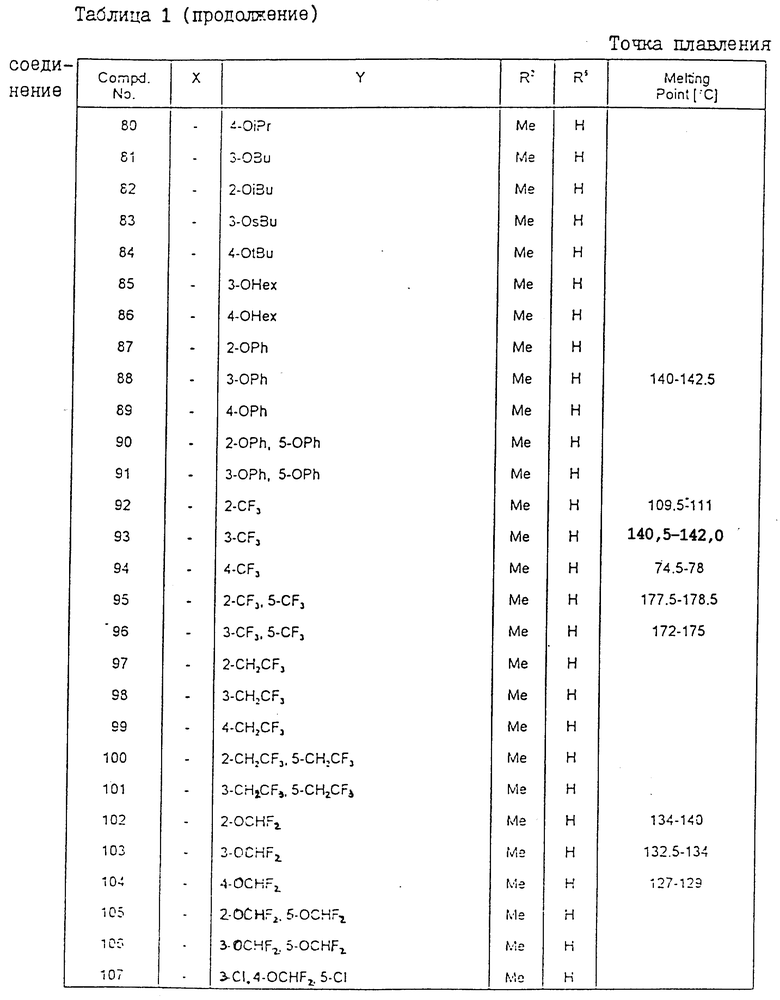



Производные 1,3-оксазин-4-она, формулы I, где R1-фенил, возможно замещенный галогеном или низшим алкилом; R2, R6 - H, низший алкил; R3 - H, низший алкил, 1-фенилэтил, 2-фенилэтил, 1-метил-1-фенилэтил или фенил, возможно замещенный галогеном, гидрокси, низшим алкилом, низшим алкоксилом, фенокси, алкилтио-, алкилсульфонилгруппой, низшим галогеналкилом, галогеналкоксилом, алкоксикарбонилом, алкоксикарбонилалкоксилом, ацетилом, CN или NO2; R4 и R5 - низший алкил; W - атом кислорода или - N(R6). Соединения I могут использоваться в качестве гербицидов как в чистом виде, так и в виде композиций, обладают сильным гербицидным действием на многие виды сорняков, но при этом они обладают очень слабой фитотоксичностью по отношению к полезным культурам. 4 с. и 12 з.п. ф-лы, 12 табл.
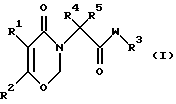
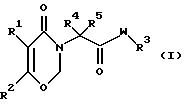
где R1 представляет собой фенильную группу, которая может быть замещена галогеном или низшим алкилом;
R2 представляет собой атом водорода или низшую алкильную группу;
R3 представляет собой атом водорода, низшую алкильную группу, 1-фенилэтильную группу, 2-фенилэтильную группу, 1-метил-1-фенилэтильную группу или фенильную группу, которая может быть замещена атомом галогена, гидроксигруппой, низшей алкильной группой, низшей алкоксигруппой, феноксигруппой, низшей алкилтиогруппой, низшей алкилсульфонилгруппой, низшей галогеналкильной группой, низшей галогеналкоксигруппой, алкоксикарбонильной группой, имеющей 2 - 8 атомов углерода, алкоксикарбонилалкоксигруппой, имеющей 3 - 10 атомов углерода, ацетильной группой, цианогруппой или нитрогруппой;
R4 и R5 независимо представляет собой низшую алкильную группу;
W представляет собой атом кислорода или группу, имеющую формулу - N (R6)-, в которой R6 представляет собой атом водорода или низшую алкильную группу.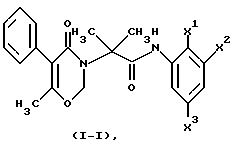
где X1, X2 и X3 независимо представляют собой атом водорода, атом галогена, низшую алкильную группу, низшую алкоксигруппу, феноксигруппу, низшую галогеналкильную группу или низшую галогеналкоксигруппу.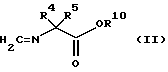
где R4 и R5 независимо представляют собой низшую алкильную группу, а R10 представляет собой низшую алкильную группу или бензильную группу.
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Устройство для регулирования температурного режима в колонне синтеза метанола | 1981 |
|
SU977450A1 |
| Способ получения 3-гетероциклических производных 4-нитро-2-хлор(или 2,6-дихлор)-4-трифторметилдифениловых эфиров | 1981 |
|
SU999969A3 |
| ВСЕСОЮЗНАЯ I | 0 |
|
SU372586A1 |
| DE 3836742 A1, 1990 | |||
| НАПРАВЛЯЮЩАЯ НАСАДКА НА ГРЕБНОЙ ВИНТ | 0 |
|
SU384736A1 |
| EP 0557691 A1, 01.09.93. | |||
Авторы
Даты
1999-01-27—Публикация
1994-12-20—Подача