Настоящее изобретение относится к новым композициям вещества, содержащего оптически чистый R(-)-кетопрофен. Эти композиции обладают сильной активностью при лечении боли, включая зубную боль, головную боль, боль, связанную с растяжениями, суставной болью и хирургической болью, например, стоматологической болью и офтальмической болью, но не ограничиваясь ими, при существенном снижении неблагоприятных результатов, связанных с применением рацемической смеси кетопрофена, включая желудочно-кишечные, поперечные и печеночные токсичности, а также лейкоцитопению, но не ограничиваясь ими. Кроме того, эти новые композиции вещества, содержащего оптически чистый R(-)-кетопрофен полезны при лечении или профилактике гипертермии при существенном уменьшении неблагоприятных результатов, связанных с применением рацемического кетопрофена. Также описываются способы лечения вышеописанных состояний у человека путем назначения указанному человеку R(-)-изомера кетопрофена при существенном уменьшении неблагоприятных результатов, связанных с рацемической смесью кетопрофена.
Активное соединение этих композиций и способов представляет собой оптический изомер кетопрофена. Кетопрофен описан в Патенте США N 3641127. С химической точки зрения активное соединение представляет собой R(-)-изомер 2-(3-бензоилфенил)-пропионовой кислоты, впоследствии называемый R(-)-кетопрофеном. Термин "R(-)-изомер кетопрофена" и, в частности, термин "R(-)-кетопрофен" охватывает оптически чистый и, по существу, оптически чистый R(-)-кетопрофен.
Кетопрофер, который представляет собой объект настоящего изобретения, имеется в промышленности только в виде рацемической смеси 1:1. То есть, кетопрофен доступен только в виде смеси оптических изомеров, называемых энантиомерами.
Много органических соединений существуют в оптически активных формах, т. е. они обладают способностью вращать плоскость плоскополяризованного света. При описании оптически активного соединения префиксы D и L или R и S используют для обозначения абсолютной конфигурации молекулы относительно хирального центра (центров). Префиксы d и 1 или (+) и (-) используют для указания на знак вращения плоскополяризованного света соединением, причем (-) или 1 означает, что соединение является левовращающим. А соединение с префиксом (+) или d является правовращающим. Для данного химического строения эти соединения, называемые стереоизомерами, являются идентичными за исключением того, что они представляют собой зеркальные отображения друг друга. Отдельный стереоизомер может также называться энантиомером, а смесь таких изомеров часто называют энантиомерной или рацемической смесью.
Стереохимическая чистота важна в области фармацевтических препаратов, где 12 из 20 наиболее используемых лекарств проявляют хиральность. Рассматриваемый случай подтверждается L-формой пропранолола - блокирующего средства для бетаадреноргика, которая, как известно, является в 100 раз более сильнодействующей, чем D-энантиомер.
Кроме того, оптическая чистота важна, поскольку определенные изомеры могут, в действительности, быть вредными, а не просто инертными. Например, считалось, что D-энантиомер талидомида при применении для контроля за утренней тошнотой во время беременности представляет собой безопасное и эффективное седативное средство, в то время как соответствующий L-энантиомер, как полагали, является сильнодействующим тератогенным средством.
Кетопрофен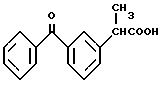
представляет собой нестероидное противовоспалительное лекарство (NSAID), которое, как известно, ингибирует биосинтез простагландинов посредством ингибирования фермента циклооксигеназы, который является убиквитарным в тканях молочной железы.
Энантиомеры кетопрофена описываются в Yamaguсhi et al, Nippon Yakurigaku Zasshi, 90: 295-302 (1987). Этот источник утверждает, что S-энантиомеры 2-арилпропионовых кислот обладают в 15-300 раз более высокими активностями по ингибированию синтеза простагландина у крыс, чем R-энантиомеры. Кроме того, S-энантиомер кетопрофена описан в Патентах США N 4868214, 4962124 и 4927854. Каждый из этих патентов утверждает, что болеутоляющая активность кетопрофена принадлежит исключительно (+)-энантиомерам, утверждение, которое резко противоречит настоящему изобретению.
Энантиомеры кетопрофена также описывают в Abas et al., J. Pharmacol. Exp. Ther. , 240: 637-641 (1987). Этот источник утверждает, что у кролика R-кетопрофен метаболически превращается в S-кетопрофен. Предполагалось, что у человека подобная инверсия существует лишь до малой степени. Смотри Jamali et al. , J. Pharm. Sci., 79: 460-461 (1990). Jamali et al., указывают, что, предполагается, что фармакологическая активность кетопрофена принадлежит S-энантиомеру и что превращение R-энантиомера в S-энантиомер возможно клинически незначительно.
Кроме того, Caldwell et al., Biochem. Pharmacol 37: 105-114 (1988) утверждают, что превращение R-2-арилпропионовых кислот в S-2-арилпропионовые кислоты представляет собой явление, которое, как предполагалось, существует у ряда 2-арилпропионовых кислот, Caldwell et al. также указывают, что сочетание хиральной инверсии и стереоселективного метаболизма обеспечивает более быструю очистку от R-энантиомеров 2-арилпропионовых кислот. Кроме того, Caldwell et al. утверждают, что "в оптимальном случае R-изомеры действуют как пролекарства для терапевтически активных S-форм", когда назначается рацемическое лекарство, и поэтому увеличивают как терапевтическое, так и токсическое воздействия активных S-энантиомеров. Этот источник также утверждает, что "в наилучшем случае R-энантиомеры являются нежелательными примесями в активном лекарстве", вызывая сложности, обусловленные нестереоселективной токсичностью. Поэтому этот источник утверждает, что использование только S-изомеров обеспечило бы более безопасное и более эффективное применение этого класса лекарств.
Аналогично считалось, что фармакокинетика энантиомеров 2-арилпропионовых кислот различна вследствие, по крайней мере отчасти, единонаправленной метаболической инверсии R-энантиомера в S. Однако, было обнаружено, что это превращение зависит от конкретного соединения и конкретных субъектов, которым его назначают, Jamali, Eur. J. Drug. Metabolism. Pharmaco. 13(1): 1-9 (1988).
Рацемическую смесь кетопрофена в настоящее время используют в основном в качестве болеутоляющего средства при лечении боли, включая боль, связанную с зубными болями, головными болями, растяжениями, болью в суставах и хирургической болью, например, стоматологической болью (например, после периодонтальной операции) и офтальмической болью (например, после операции на катаракте), но не ограничиваясь ею.
Боль представляет собой обычный симптом, отражающий или физический (т.е. результат повреждения или воспаления ткани) или эмоциональный дискомфорт. Боль представляет собой сложное субъективное явление, состоящие из ощущения, отражающего явное или скрытое поражение ткани, и эмоциональной реакции, которую оно порождает. Боль можно классифицировать как острую или хроническую, и она бывает ряда конкретных типов. Острая боль представляет собой неотъемлемый биологический сигнал возможности или степени повреждения ткани. В противоположность этому хроническая боль является физически и психологически ослабляющей и больше не выполняет свою адаптирующую биологическую роль. У многих пациентов болезнь органов может быть недостаточной для объяснения степени боли. Хроническую боль, включая остеоартрит, ревматоидный артрит, синдромы болей мягких тканей и головные боли, но не ограничиваясь ими, можно связать с состоянием человека.
Многие из NSAID вызывают побочные неблагоприятные действия. Эти неблагоприятные действия включают желудочно-кишечные, почечные и печеночные токсичности, но не ограничиваются ими. Было обнаружено, что применение рацемической смеси кетопрофена вызывает эти, а также другие неблагоприятные действия. Эти другие неблагоприятные действия включают увеличения во времени кровотечения вследствие нарушения функции тромбоцитов (например, тромбоцитопении) и увеличение продолжительности беременности вследствие маточных явлений, но не ограничиваются ими.
Кроме того, лейкоцитопения (понижение количество белых клеток в крови) представляет собой известное побочное действие NSAID. Агранулоцитоз представляет собой острое заболевание, вызываемое резким падением количества белых кровяных клеток. Синдром лейкопении/агранулоцитоза был описан для нескольких таких как индометацин, кетопрофен и ибупрофен. Действительно, такие NSAID противопоказаны пациентам, иммунные системы которых ослаблены HIV инфекцией, химиотерапией, ионизирующим излучением, кортикостероидами, иммунодепрессантами и т.д. или такими состояниями, как эмфизема, бронхоэктаз, сахарный диабет, лейкемия, ожоги и т.п. Несмотря на то, что суммарная заболеваемость низка, агранулоцитоз представляет собой угрожающий жизни синдром, который очень быстро развивается. Поэтому периодические подсчеты белых кровяных клеток мало помогают в представлении раннего предупреждающего симптома этого синдрома.
Таким образом, было бы особенно желательно найти соединение с преимуществами смеси кетопрофена, которое не имело бы вышеупомянутых недостатков.
Было обнаружено, что оптически чистый R(-)-изомер кетопрофена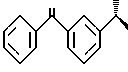
представляет собой сильнодействующее болеутоляющее средство, которое существенно снижает отрицательные действия, связанные с применением рацемических смесей кетопрофена, включая желудочно-кишечные, почечные и печеночные токсичности, увеличение времени кровотечения, лейкоцитопению и увеличение продолжительности беременности, но не ограничиваясь ими. Было также обнаружено, что эти новые композиции вещества, содержащего оптически чистый R(-)-кетопрофен пригодны при лечении или профилактике гипертермии при существенном уменьшении вышеописанных отрицательных действий, связанных с применением рацемического кетопрофена. Настоящее изобретение также включает способы лечения вышеописанных состояний у человека путем назначения оптически чистого R(-)-изомера кетопрофена указанному человеку при существенном уменьшении отрицательных действий, которые связаны с рацемической смесью кетопрофена.
Настоящее изобретение охватывает способ получения болеутоляющего результата у человека при существенном уменьшении сопутствующей помехи, состоящей в отрицательных действиях, связанных с применением рацемического кетопрофена, который включает назначение человеку, нуждающемуся в болеутоляющей терапии, количества R(-)-кетопрофена или его фармацевтически приемлемой соли, по существу не содержащего его S(+)-стереоизомер, причем указанное количество является достаточным для облегчения боли, но не достаточным для того, чтобы вызвать отрицательные действия, связанные с рацемической смесью кетопрофена.
Настоящее изобретение также охватывает болеутоляющую композицию для лечения людей, нуждающихся в болеутоляющей терапии, которая включает количество R(-)-кетопрофена или его фармацевтически приемлемой соли, по существу, не содержащее его S(+)-стереоизомер, причем указанное количество является достаточным для облегчения боли, но недостаточным для того, чтобы вызвать отрицательные действия, связанные с рацемическим кетопрофеном.
Доступная рацемическая смесь кетопрофена (т.е. смесь этих двух энантиомеров 1:1) обладает болеутоляющей и жаропонижающей активностью, однако, эта рацемическая смесь, давая вероятность воздействия, вызывает отрицательное действие. Использование, по существу, оптического чистого или оптически чистого R(-)-изомера кетопрофена приводит к определенности действия, связанной с более явной дозой, уменьшенным отрицательным действием и, соответственно, к улучшенному терапевтическому индексу. Поэтому более желательно использовать R(-)-изомер кетопрофена, чем рацемический кетопрофен.
Термин "отрицательные действия" включает желудочно-кишечные, почечные и печеночные токсичности, лейкоцитопению, увеличение продолжительности кровотечения вследствие, например, тромбоцитопении и увеличение продолжительности беременности, но не ограничивается ими. Термин "желудочно-кишечные токсичности" включает желудочные и кишечные язвы и эрозии, но не ограничивается ими. Термин "почечные токсичности" включает такие состояния, как некротический папиллит и хронический интерстициальный нефрит, но не ограничивается ими.
В одном варианте осуществления термин "по существу, не содержащий его S(+)-изомер", в соответствии с используемым здесь означает, что композиция содержит по крайней мере 90 мас.% R(-)-кетопрофена и 10 мас.% или менее соответствующего S(+)-кетопрофена. В предпочтительном варианте осуществления термин "по существу, не содержащий S(+)-стереоизомера" означает, что композиции содержит по крайней мере 99 мас.% R(-)-кетопрофена и 1% или менее соответствующего S(+)-кетопрофена. В наиболее предпочтительном варианте осуществления термин "по существу, не содержащий его S(+)-стереоизомера", в соответствии с используемым здесь означает, что композиция содержит более 99 мас. % R(-)-кетопрофена и менее 1% соответствующего S(+)-кетопрофена. Эти процентные соотношения основаны на суммарном количестве кетопрофена, присутствующем в композиции. Термины "по существу, оптически чистый R(-)-изомер кетопрофена" или "по существу, оптически чистый R(-)-кетопрофен" и "оптически чистый R(-)-кетопрофен" или "оптически чистый R(-)-изомер кетопрофена" также охватываются вышеописанными количествами.
Термин "получение болеутоляющего результата" в соответствии с используемым здесь означает лечение, ослабление, уменьшение интенсивности или профилактику для уменьшения боли. Например, такая боль включает боль, связанную с зубными болями, головными болями, растяжениями, болью в суставах, хирургическую боль, стоматологическую боль и офтальмическую боль, но не ограничивается ими.
Химический синтез рацемической смеси кетопрофена можно осуществить посредством способа, описанного в Патенте США N 3641127, включенного в настоящее описание ссылкой.
R(-)-изомер кетопрофена можно получить из его рацемической смеси путем разделения энантиомеров с использованием традиционных средств, например оптически активного разделяющего основания. Смотри, например, Патенты США N 4983765 и 4973745, которые включены в настоящее описание ссылкой. Кроме того, оптически чистый R(-)-изомер кетопрофена можно получить из соответствующей акриловой кислоты посредством каталитического гидрирования с использованием хирального катализатора. Смотри, например, Европейские Заявки на Патент N EP/402433 и O 90/015790, которые включены в настоящее описание в качестве ссылок. Кроме того, оптически частый R-изомер кетопрофена можно получить из рацемической смеси посредством ферментативного биокаталитического разделения. Смотри, например, Патенты США N 5057427 и 5077217, которые включены в настоящее описание в качестве ссылок.
Величина профилактической или терапевтической дозы R(-)-кетопрофена при резком или хроническом лечении болезни будет изменяться в зависимости от серьезности состояния, которое нужно лечить, и способа применения. Доза и, возможно, частота доз также будут изменяться в соответствии с возрастом, весом тела и восприимчивостью отдельного пациента. Как правило, для описанных выше состояний пределы суммарной дневной дозы для R(-)-кетопрофена составляют от около 25 мг до около 2000 мг в одноразовой или раздельных дозах. Предпочтительно, пределы дневной дозы должны находиться между около 200 мг и около 1000 мг в одноразовой или раздельных дозах. При лечении пациента терапию следует начинать при более низкой дозе, возможно около 25 мг до около 200 мг, и повышенной вплоть до около 1000 мг или выше в зависимости от общей восприимчивости пациента. Дополнительно рекомендуется, чтобы младенцы, дети, пациенты старше 65 лет и пациенты с нарушенной почечной или печеночной функцией исходно получали малые дозы и чтобы к ним подходили индивидуально в зависимости от индивидуальной восприимчивости (восприимчивостей) и состояния (состояний) крови. В некоторых случаях может быть необходимо использовать дозы вне этих пределов, как это будет ясно специалистам. Далее отмечается, что клиницист или лечащий врач хочет знать, как и когда прервать, отрегулировать или закончить лечение в связи с реакцией отдельного пациента. Термины "количество, достаточное для облегчения боли, но недостаточное для того, чтобы вызывать указанные неблагоприятные результаты", и "количество, достаточное для облегчения или профилактики гипертермии, но недостаточное для того, чтобы вызвать указанные неблагоприятные результаты", охватываются вышеописанными дозовыми количествами и графиком частоты доз.
Для введения пациенту эффективной дозы R(-)-кетопрофена можно использовать любой подходящий способ применения. Например, могут быть использованы пероральный, ректальный, чрескожный, парентеральный (подкожный, внутримышечный, внутривенный) и аналогичные формы применения.
Фармацевтическая композиция настоящего изобретения включает в качестве активного компонента R(-)-кетопрофен или его фармацевтически приемлемую соль и может также содержать фармацевтически приемлемый носитель и, необязательно, другие терапевтические ингредиенты.
Термины "фармацевтически приемлемые соли" или "его фармацевтически приемлемая соль" относятся к солям, полученным из фармацевтически приемлемых нетоксичных кислот или оснований, включая неорганические кислоты и основания и органические кислоты и основания. Поскольку соединение настоящего изобретения является кислотным, соли могут быть получены из фармацевтически приемлемых нетоксичных оснований, включая неорганические и органические основания. Подходящие фармацевтически приемлемые соли, полученные добавлением оснований, для соединения настоящего изобретения включают соли металлов, полученные на основании алюминия, кальция, лития, магния, калия, натрия и цинка, или органические соли, полученные на основании лизина, N,N-дибензилэтилендиамина, хлорпрокаина, холина, диэтаноламина, этилендиамина, меглумина (N-метилглюкамина) и прокаина.
Композиции настоящего изобретения включают композиции, такие как суспензии, растворы эликсиры и аэрозоли. В случае пероральных твердых препаратов могут быть использованы носители, например крахмалы, сахара, микрокристаллическая целлюлоза, разбавители, гранулирующие средства и т.п. Пероральные твердые препараты (такие как порошки, капсулы и таблетки) являются предпочтительными по отношению к жидким пероральным препаратам. Наиболее предпочтительный пероральный твердый препарат представляет собой таблетки. При желании таблетки могут быть покрыты с использованием стандартных водных или неводных методов.
Помимо обычных лекарственных форм, представленных выше, соединения настоящего изобретения могут также применяться при помощи средств контролируемого выделения и и/или устройств доставки таких, как описаные в Патентах США N 3845770, 3916899, 3536809, 3598123 и 4008719, которые полностью включены в настоящее описание в качестве ссылок.
Фармацевтические композиции настоящего изобретения, пригодные для перорального применения, могут быть представлены в виде дискретных единиц, например капсул, крахмальных капсул или таблеток, или аэрозолей, каждая из которых содержит заранее определенное количество активного компонента в виде порошка или гранул, или в виде раствора или суспензии в водной жидкости, неводной жидкости, эмульсии масло-в-воде или в жидкой эмульсии вода-в-масле. Такие композиции могут быть получены посредством любого из способов фармации, но все способы включают стадию связывания активного компонента с носителем, который составляет один или более необходимых компонентов. Обычно композиции получают, одновременно и тщательно смешивая активный компонент с жидкими носителями или мелко измельченными твердыми носителями или обоими и затем, при необходимости, придавая продукту желаемую форму.
Например, таблетку можно получить посредством прессования или формования необязательно с одним или более вспомогательным компонентом. Прессованные таблетки могут быть получены посредством прессования в соответствующем устройстве активного компонента в свободно-текущей форме, такой как порошки или гранулы, необязательно смешанного со свяывающим веществом, смазывающим веществом, инертным разбавителем, поверхностно-активным или диспергирующим средством. Формованные таблетки могут быть получены формованием в соответствующем устройстве смеси порошкообразного соединения, увлажненного инертным жидким разбавителем. Желательно, чтобы каждая таблетка содержала от около 12,5 мг до около 1000 мг активного компонента, а каждая крахмальная капсула или капсула содержала от около 12,5 мг до около 600 мг активного компонента. Более предпочтительно, таблетка, крахмальная капсула или капсула содержит любую одну из трех доз: около 50 мг, около 100 мг и около 200 мг активного компонента.
Изобретение дополнительно определяется посредством ссылки на следующие примеры, описывающие получение композиций настоящего изобретения, а также их полезность.
Пример 1.
Получение R(-)-катопрофена.
Нижеследующее представляет собой описание разделения рацемического кетопрофена посредством ферментативного способа. Включено описание синтеза используемого водорастворимого сложного эфира (трехстадийная методика), а также реальное ферментативное разделение, следующий за ним основной гидролиз и выделение R(-)-кетопрофеновой кислоты.
A. Синтез кетопрофена.
Диметилэтаноламинный эфир.
Рацемический кетопрофен (0,5 моль) добавляли к тионил хлориду (1,0 моль) в колбе, снабженной осушительной трубкой. Диметилформамид (0,25 мл) добавляли к реакционной смеси и смесь перемешивали и подогревали до тех пор, пока кетопрофен не растворялся и не прекращалось выделение газа. Тепло отводили и смесь перемешивали при комнатной температуре в течение 18 часов. Тионил хлорид удаляли при пониженном давлении и маслянистый остаток хлорида кислоты медленно отверждали.
Хлорид кислоты растворяли в тетрагидрофуране (125 мл) и добавляли к раствору N,N-диметилэтаноламина (1,0 моль) в тетрагидрофуране (500 мл), охлажденном до 0oC, в колбе, снабженной осушительной трубкой. После добавления реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Насыщенный водный раствор карбоната калия (500 мл) добавляли к реакционной смеси и получающийся органический слой удаляли. Водный слой экстрагировали диэтиловым эфиром (2 х 250 мл) и органические соли смешивали, промывали насыщенным водным раствором хлорида натрия, сушили над карбонатом калия, и растворитель удаляли при пониженном давлении. Продукт выделяли в виде бесцветного вязкого масла.
B. Кватернизация N,N-диметилэтаноламинного эфира.
Получающийся N,N-диметилэтаноламинный эфир растворяли в диэтиловом эфире (500 мл) и охлаждали до 0oC. Раствор диметилсульфата (0,36 моль) в диэтиловом эфире (500 мл) добавляли к охлажденному раствору, и получающийся раствор перемешивали при комнатной температуре в течение 18 часов. Получающееся твердое вещество удаляли фильтрованием, промывали диэтиловым эфиром и сушили в вакууме, получая N,N,N-триметилэтаноламмониевый эфир кетопрофена (кетопрофен холиновый эфир) в виде белого твердого вещества.
C. Ферментативная переэтерификация рацемического кетопрофен холинового эфира.
Холиновый эфир (0,36 моль) растворяли в 0,2М буферном растворе фосфата натрия (900 мл, pH 7,0). К этому раствору добавляли метанол (100 мл) и протеазу типа XXVII (3 г), получаемую от Sigma Chemical Co. Реакции давали осторожно перемешиваться при комнатной температуре в течение 24 часов. Реакционную смесь экстрагировали диэтиловым эфиром (2 х 250 мл) и органический слой сохраняли. Водный слой доводили до pH 2 посредством добавления концентрированной серной кислоты и получающуюся смесь промывали эфиром (2 х 150 мл). Водный слой концентрировали при пониженном давлении и объем доводили до 900 мл посредством добавления 0,2М буферного раствора фосфата натрия (pH 7,0). К этому раствору добавляли метанол (100 мл) и протеазу типа XVII (2 г). Реакции давали осторожно перемешиваться при комнатной температуре в течение 24 часов. Реакционную смесь экстрагировали диэтиловым эфиром (2 х 250 мл) и этот органический слой смешивали со слоем, сохраненным от первой ферментативной реакции. Смешанные эфирные слои сушили над сульфатом магния и растворитель удаляли при пониженном давлении, оставляя сырой R(-)-кетопрофен метиловый эфир, который сушили в вакууме.
Получение R(-)-кетопрофена.
Сырой эфир смешивали с этанольным раствором гидроксида калия (pH 13) и получающуюся смесь перемешивали в течение 1 часа при комнатной температуре.
Получающийся раствор доводили до pH 2 посредством добавления соляной кислоты. Получающийся раствор экстрагировали диэтиловым эфиром, и смешанные эфирные растворы сушили над сульфатом магния, а растворитель удаляли при пониженном давлении, оставляя сырой R(-)-кетопрофен. Сырую кислоту перекристаллизовывали из диэтилового эфира, получая R(-)-кетопрофен.
Пример 2.
Испытание на корчи, вызванные фенилхиноном, представляет собой стандартный метод определения и сравнения болеутоляющей активности у лабораторных животных и обычно коррелируется с эффективностью у человека. В качестве реакции на впрыснутый, вызывающий местное раздражение раствор животные испытывают судороги ("корчи"), которые ингибируются болеутоляющими средствами.
Мышам сначала давали определенными дозами, составляющими по крайней мере два дозовых уровня, каждый из R(-)-кетопрофена, S(+)-кетопрофена и рацемического кетопрофена. Затем мышам внутрибрюшинно вводили раствор фенил-п-бензохинона и наблюдали за характерным синдромом вытягивания-корчей. Отсутствие корчей указывает на болеутоляющее действие. Степень болеутоляющего действия рассчитывали на основе подавления корчей в сравнении с контрольными животными, проведенными в тот же самый день. Данные по времени реакции получали, вводя мышам раствор фенилхинона через различные промежутки времени после введения им в определенных дозах испытываемых лекарственных препаратов.
В этом испытании 100% животных демонстрировали по крайней мере 50% уменьшение числа корчей после перорального введения в дозе 30 мг/кг или R(-)-кетопрофена или S(+)-кетопрофена. Всех животных испытывали через один час после применения лекарства. Было обнаружено, что в этом испытании болеутоляющее действие зависит от дозы.
Осложняющим фактором при изучении фармакологических действий R(-)- и S(+)-кетопрофена у некоторых животных является то, что R(-)-кетопрофен обращается в S(+)-кетопрофен по печеночному ферментативному пути. Через один час после перорального применения R(-)-кетопрофена у мышей приблизительно 39% циркулирующего лекарства обращается в S(+)-форму. (Подобная инверсия не имеет места у человека).
Поскольку через один час (когда произошла относительно небольшая инверсия) болеутоляющие действия R(-)-кетопрофена и S(+)-кетопрофера в испытании на корче были приблизительно эквиваленты, можно сделать вывод, что R(-)-кетопрофен является приблизительно таким же сильнодействующим, как и S(+)-кетопрофен в качестве болеутоляющего средства.
Пример 3. Токсичность.
Нижеследующее представляет собой описание исследования действия изомеров кетопрофена на морскую свинку. Группам из 6-10 морских свинок вводят в определенных дозах перорально с любым наполнителем рацемический кетопрофен (20, 10, 5, 1 и 0,1 мг/кг), S(+)-кетопрофен (20, 10, 5, 1 и 0,1 мг/кг и R(-)-кетопрофен (20, 10, 5, 1 и 0,1 мг/кг). В пределах 24 часов после введения дозы животных умерщвляют и в желудочно-кишечных трактах регистрируют очевидные нарушения, особое внимание обращая на слизистую оболочку желудка. Отмечаются микроэррозии и покраснение (раздражение), и результаты сравнивают у обработанных групп в соответствии с описанным Aberg & Larrson (Acta Pharmacol. Toxicol. 28: 249-257, 1970). На основе этих наблюдений видно, что R(-)-изомер фактически не вызывает желудочно-кишечного раздражения.
Пример 4. Лейкоцитопения.
Для испытания выживания белых клеток используют способ испытания in vitro, в котором клеточную культуру костного мозга позвоночника подвергают действию возрастающих концентраций испытываемых соединений, таких как R(-)-кетопрофен и S(+)-кетопрофен. В качестве положительного контрольного средства используют известное средство, вызывающее лейкоцитопению, например тиоурацил. Выживаемость гранулоцитов измеряют, используя стандартную дифференциальную методику подсчета клеток.
Риск лейкоцитопенных результатов от возрастающих концентраций лекарств in vivo излучается у групп животных, у которых слабая гранулоцитопения исходно вызвана или при помощи лекарств, например, тиоурацила или хлорамфеникола, или посредством облучения. Для регистрации развития лейкоцитопении у животных осуществляют повторные подсчеты белых клеток.
Пример 5. Действие по ингибированию активности циклооксигеназы.
Хорошо известным фактом является то, что ингибиторы циклооксигеназы (например, аспирин и индометацин) вызывают поражение и раздражение желудочной слизистой оболочки.
Испытания с целью определения ингибирующего действия R(-)-, S(+)- и рацемического кетопрофена, эталонных средств и наполнителей на активность циклооксигеназы осуществляют, используя RBL-1 клетки (безофильные лейкемические клеточные линии крысы). Действие испытываемых соединений, эталонных средств или наполнителей оценивают на получении PGF2-alpha, в котором циклооксигеназа является промежуточным соединением.
RBL-1 клетки выращивают в культуре в минимальной необходимой среде Иглса, дополненной 12% зародышевой бычьей сывороткой и смесью антибиотика/противогрибкового средства 1:100, при 37oC. Клетки собирают посредством центрифугирования, промывают холодным фосфатным буферным рассолом (PBS) и суспендируют в PBS, дополненном 0,88 мк М CaCl2. Клетки инкубируют в присутствии экранирующей концентрации испытываемого соединения или эталонного средства. Или же, клетки инкубируют в присутствии наполнителя.
После инкубационного периода активность циклооксигеназы стимулируют посредством добавления 5 мк М ионофора кальция к инкубационной среде. Реакцию обрывают посредством резкого охлаждения трубок на льду.
Клетки затем отделяют центрифугированием и удаляют надосадочную жидкость. Аликвоты надосадочной жидкости используют для измерения стимулированного ионофором кальция получения PGF2-alpha посредством радиоимунного анализа.
Для каждого эксперимента оценивают контроль с наполнителем. Эталонный стандарт также оценивается с каждым анализом при единственной концентрации.
Пример 6. Технология приготовления перорального средства.
Активный компонент R(-)-кетопрофен просеивают и смешивают с наполнителями. Используя соответствующие устройства, смесью заполняют состоящие из двух частей твердые желатиновые капсулы соответствующих размеров. Другие дозы можно получить, изменяя вес заполнения и, при необходимости, изменяя для соответствия размер капсулы.
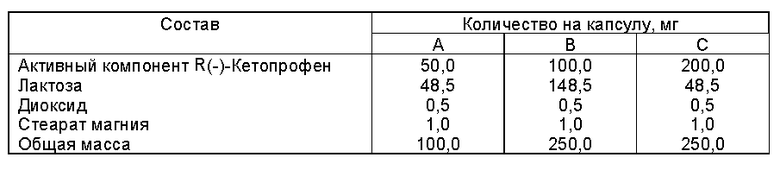
Изобретение может быть использовано при лечении боли, включая зубную боль, головную боль, боль, связанную с растяжениями, суставной болью и др. Композиция содержит в качестве активного компонента R(-)-кетопрофен в смеси с S(+)-кетопрофеном или его фармацевтически приемлемую соль. Смесь энантиомеров R(-) и S(+) содержит не более 10 мас.% S(+)-кетопрофена. Способ достижения болеутоляющего эффекта у человека осуществляют введением эффективного количества композиции. Количество вводимого R(-)-кетопрофена или его фармацевтически приемлемой соли предпочтительно 25-2000 мг в день. Изобретение позволяет избежать неблагоприятных побочных эффектов от применения известных противовоспалительных препаратов: желудочно-кишечные, почечные и печеночные токсичности, кровотечения и др. 2 с. и 6 з.п. ф-лы, 1 табл.
| US 4868214 A, 19.09.89 | |||
| Способ получения производных фенилуксусной кислоты или их солей | 1981 |
|
SU1053743A3 |
Авторы
Даты
1999-02-10—Публикация
1993-03-08—Подача