По этой заявке испрашивается приоритет предварительной заявки на патент США № 60/097665, поданной 24 августа 1998 г, и предварительной заявки на патент США № 60/099306, поданной 2 сентября 1998г., которые полностью включены в описание изобретения в качестве ссылки.
Область техники
Это изобретение относится к композициям, содержащим ингибиторы обратного захвата допамина, в частности, рацемические и оптически чистые метаболиты сибутрамина, и к способам их применения.
Предпосылки изобретения
Сибутрамин, имеющий химическое название [N-1-[1-(4-хлорфенил)циклобутил]-3-метилбутил]-N,N-диметиламин, является ингибитором обратного захвата моноамина нейронами, который описан в патентах США №№ 4746680 и 4806570. Сибутрамин ингибирует обратный захват норэпинефрина и в меньшей степени серотонина и допамина. См., например, Buckett et al., Prog. Neuropsychopharm. & Biol. Psychiat., 12:575-584, 1988; King et al., J. Clin. Pharm., 26:607-611 (1989).
Рацемический сибутрамин продается в виде моногидрата гидрохлорида под торговым названием MERIDIA® и предназначен для лечения ожирения. Physician's Desk Reference® 1494-1498 (53rd ed., 1999). Лечение ожирения с использованием рацемического сибутрамина описано, например, в патенте США № 5436272.
Всесторонние исследования сибутрамина позволили установить, что его можно использовать для лечения разных болезней. Например, в патентах США №№ 4552828, 4746680, 4806570 и 4929629 описаны методы лечения депрессии с использованием рацемического сибутрамина и в патентах США №№ 4871774 и 4939175 описаны соответственно методы лечения болезни Паркинсона и старческого слабоумия с использованием рацемического сибутрамина. Другие применения сибутрамина описаны в публикациях РСТ WO 95/20949, WO 95/21615, WO 98/11884 и WO 98/13033. Кроме того, рассмотрены возможности использования оптически чистых энантиомеров сибутрамина. Например, в публикациях WO 94/00047 и 94/00114 описаны методы лечения депрессии и родственных заболеваний с использованием соответственно (+)- и (-)-энантиомеров сибутрамина.
Сибутрамин быстро поглощается из желудочно-кишечного тракта после перорального введения и активно участвует в первичном обмене веществ, в результате чего образуются первичные метаболиты, десметилсибутрамин и дидесметилсибутрамин, показанные ниже.
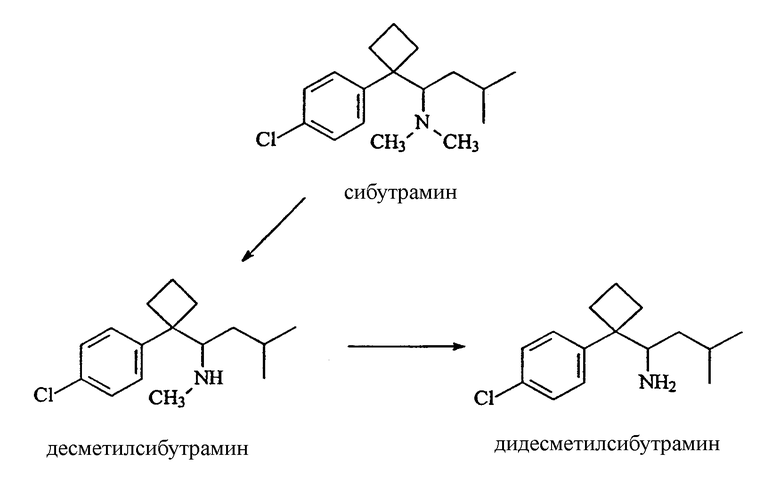
Установлено, что десметилсибутрамин и дидесметилсибутрамин являются более эффективными ингибиторами обратного захвата in vitro норадреналина и 5-гидрокситриптамина (5НТ, серотонина), чем сибутрамин. Stock, M.J., Int'l J. Obesity, 21 (Supp. 1):S25-S29 (1997). Однако далее установлено, что сибутрамин и его метаболиты обладают чрезвычайно низкой степенью сродства к целому ряду нейротрансмиттерных рецепторов, включая серотонергические (5-НТ1, 5-НТ1А, 5-НТID, 5-НТ2А, 5-НТ2С), адренергические, допаминергические, мускариновые, гистаминергические, глутаматные и бензодиазепиновые рецепторы. Там же.
Сибутрамин вызывает много побочных эффектов. См., например, Physician's Desk Reference® 1494-1498 (53rd ed., 1999). С учетом выявленных преимуществ и терапевтических недостатков сибутрамина была поставлена задача создать соединения и композиции, которые можно использовать для лечения или профилактики разных заболеваний, включающих, но не ограничивающихся ими, нарушения эрекции, аффективные расстройства, увеличение веса или ожирение, нарушения функции головного мозга, болевой синдром, обсессивно-компульсивное расстройство, злоупотребление веществами, хронические болезни, состояние тревоги, нарушения питания, мигрени и недержание. В частности, необходимы соединения и композиции, которые при лечении и профилактике таких заболеваний и нарушений, вызывают гораздо меньше побочных эффектов, чем сибутрамин.
Краткое изложение существа изобретения
Это изобретение относится к фармацевтическим композициям и лекарственным формам, а также к способам их применения для лечения и профилактики болезней, ослабление симптомов которых достигается ингибированием поглощения моноамина нейронами у млекопитающих, включая человека. Примерами таких заболеваний являются, но не ограничиваются ими, нарушения эрекции, аффективные расстройства, увеличение веса или ожирение, нарушения функции головного мозга, болевой синдром, обсессивно-компульсивное расстройство, злоупотребление веществами, хронические болезни, состояние тревоги, нарушение питания, мигрени и недержание. Способы по этому изобретению заключается в том, что субъекту, нуждающемуся в таком лечении или профилактике, вводят терапевтически или профилактически эффективное количество рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Это изобретение относится также к способу лечения или профилактики нарушения эрекции, который включает одновременное введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективных количеств ингибитора обратного захвата допамина и антагониста 5-НТ3.
Фармацевтические композиции по этому изобретению содержат терапевтически или профилактически эффективное количество ингибитора обратного захвата моноамина нейронами. Предпочтительными ингибиторами обратного захвата моноамина нейронами являются, но не ограничиваются ими, апоморфин, рацемические и оптически чистые метаболиты сибутрамина, их фармацевтически приемлемые соли, сольваты и клатраты. Фармацевтически композиции по этому изобретению могут дополнительно содержать другие лекарственные средства, которые включают, но не ограничиваются ими, антагонисты 5-НТ3.
Это изобретение относится к применению рацемических и оптически чистых метаболитов сибутрамина в качестве эффективных ингибиторов обратного захвата допамина, серотонина и норэпинефрина. Рацемические и оптически чистые метаболиты сибутрамина включают, но не ограничиваются ими, (+)-десметилсибутрамин, (-)-десметилсибутрамин, (±)-десметилсибутрамин, (+)-дидесметилсибутрамин, (-)-дидесметилсибутрамин и (±)-дидесметилсибутрамин.
Подробное описание изобретения
Это изобретение относится к способам и композициям подавления обратного захвата нейронами моноаминов (например, допамина, серотонина и норэпинефрина). Это изобретение далее относится к способу лечения или профилактики заболевания, ослабление симптомов которого достигается ингибированием обратного захвата моноамина нейронами, который заключается в том, что субъекту (т.е. человеку), нуждающемуся в таком лечении или профилактике, вводят терапевтически или профилактически эффективное количество ингибитора обратного захвата моноамина нейронами. Предпочтительными ингибиторами обратного захвата моноамина нейронами являются рацемические и оптически чистые метаболиты сибутрамина, их фармацевтически приемлемые соли, сольваты и клатраты.
В используемом в описании значении термин “лечение или профилактика заболевания, ослабление симптомов которого достигается ингибированием обратного захвата моноамина нейронами” означает ослабление симптомов заболеваний, обусловленных аномальными уровнями моноамина в нейронах. Заболевания, ослабление симптомов которых достигается ингибированием обратного захвата моноамина нейронами, включают, но не ограничиваются ими, нарушение эрекции, аффективные расстройства, увеличение веса или ожирение, нарушения функции головного мозга, болевой синдром, обсессивно-компульсивное расстройство, злоупотребление веществами, хронические болезни, состояние тревоги, нарушения питания, мигрени и недержание.
Первый вариант осуществления изобретения относится к способу лечения или профилактики нарушения эрекции, который заключается в том, что субъекту, нуждающемуся в таком лечении или профилактике, одновременно вводят терапевтически или профилактически эффективные количества ингибитора обратного захвата допамина и антагониста 5-НТ3. Предпочтительными ингибиторами обратного захвата допамина являются, но не ограничиваются ими, апоморфин, сибутрамин, рацемические и оптически чистые метаболиты сибутрамина, их фармацевтически приемлемые соли, сольваты и клатраты. Особенно предпочтительными ингибиторами обратного захвата допамина являются рацемические и оптически чисты метаболиты сибутрамина. Предпочтительными антагонистами 5-НТ3 являются противорвотные средства. Примерами приемлемых антагонистов 5-НТ3 являются, но не ограничиваются ими, гранисетрон (KYTRIL®), метоклопрамид (REGLAN®), ондансетрон (ZOFRAN®), рензаприд, закоприд, тропизетрон, их оптически чистые стереоизомеры, активные метаболиты, фармацевтически приемлемые соли, клатраты и сольваты.
В предпочтительном способе по этому изобретению ингибитор обратного захвата допамина вводят чрескожно или через слизистую оболочку (например, назально, подъязычно или трансбуккально). В более предпочтительном способе по этому варианту осуществления изобретения ингибитор обратного захвата допамина и антагонист 5-НТ3 вводят чрескожно или через слизистую оболочку.
Второй вариант осуществления изобретения относится к способу лечения или профилактики нарушения эрекции, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, вводят терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. В предпочтительном способе по этому варианту осуществления изобретения рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат вводят чрескожно или через слизистую оболочку.
Третий вариант осуществления изобретения относится к способу лечения или профилактики аффективного расстройства, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. Аффективными расстройствами являются, но не ограничиваются ими, депрессия (например, меланхолия), нарушение внимания (включая отсутствие внимания в сочетании с повышенной активностью и заболевание, обусловленное отсутствием внимания/повышенной активностью), биполярный и маниакальный синдром, дистимия и циклотимия. В используемом здесь значении термины “нарушение внимания” (ADD), “нарушение внимания в сочетании с повышенной активностью” (ADDH) и “заболевание, обусловленное дефицитом внимания/повышенной активностью” (AD/HD) использованы в соответствии со значениями, употребляемыми в этой области. См., например, Diagnostic and Statistical Manual of Mental Disorders, Fourth Ed., American Psychiatric Association, 1997 (DSM-IV™) и Diagnostic and Statistical Manual of Mental Disorders, 3rd Ed., American Psychiatric Association (1981) (DSM-III™).
Предпочтительным способом по этому варианту осуществления изобретению является способ лечения или профилактики дефицита внимания, который заключается в том, что субъекту, нуждающемуся в таком лечении или профилактике, вводят терапевтически или профилактически эффективное количество рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. Для лечения или профилактики дефицита внимания в качестве рацемического или оптически чистого метаболита сибутрамина используют оптически чистый метаболит сибутрамина и более предпочтительно (-)-десметилсибутрамин или (-)-дидесметилсибутрамин.
Другим предпочтительным способом по этому варианту осуществления изобретения является способ лечения или профилактики депрессии, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболитасибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. В используемом значении термин “лечение или профилактика депрессии” означает ослабление интенсивности или предупреждение возникновения симптомов депрессии, которыми являются, но не ограничиваются ими, изменения настроения, чувство глубокого уныния, отчаяние, замедление мышления, потеря концентрации, пессимизм, волнение и заниженная самооценка. При помощи этого способа можно устранить или предупредить физические изменения, которые включают, но не ограничиваются ими, бессонницу, анорексию, пониженную активность и либидо, а также неправильный гормональный циркадный ритм.
Четвертый вариант осуществления изобретения относится к способу лечения или профилактики увеличения веса или ожирения, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. В используемом значении термин “лечение или профилактика увеличения веса или ожирения” означает уменьшение веса, избавление от избыточного веса, прекращение увеличение веса или избавление от ожирения и профилактику ожирения, причем все эти понятия обычно связаны с чрезмерным потреблением пищи.
Пятый вариант осуществления изобретения относится к способу лечения или профилактики нарушения функции головного мозга, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. Нарушения функции головного мозга включают, но не ограничиваются ими, старческое слабоумие, болезнь Альцгеймера, потерю памяти, амнезию/синдром потери памяти, расстройство сознания, коматозное состояние, понижение внимание, нарушения речи, болезнь Паркинсона, синдром Леннокса, аутизм, эпилепсию, гиперкинетический синдром и шизофрению. Нарушения функции головного мозга могут быть вызваны разными факторами, которые включают, но не ограничиваются ими, цереброваскулярные заболевания, такие как инфаркт головного мозга, кровоизлияние в головной мозг, артериосклероз головного мозга, тромбофлебит головного мозга и травмы головы, а также заболевания, характеризующиеся наличием симптомов, выбираемых из группы, включающей расстройство сознания, старческое слабоумие, коматозное состояние, понижение внимания и нарушения речи. В используемом значении термин “лечение или профилактика нарушения функции головного мозга” означает ослабление или предупреждение появления одного или нескольких симптомов, связанных с нарушениями функции головного мозга.
Шестой вариант осуществления изобретения относится к способу лечения или профилактики боли, включающей хроническую боль, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Седьмой вариант осуществления изобретения относится к способу лечения или профилактики обсессивно-компульсивного расстройства, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Восьмой вариант осуществления изобретения относится к способу лечения или профилактики злоупотребления веществами, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. В используемом значении термин “злоупотребление веществами” означает злоупотребление и физическое и/или психологическое привыкание к наркотическим средствам или алкогольным напиткам. Термин “злоупотребление веществами” далее имеет значение, принятое в этой области. См., например, DSM-IV™ и DSM-III™.
Предпочтительным способом по этому варианту осуществления изобретения является способ лечения или профилактики привыкания к кокаину и/или героину.
Девятый вариант осуществления изобретения относится к способу лечения или профилактики привыкания к никотину, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. Привыкание к никотину включает все известные формы зависимости от никотина, такие как курение сигарет, сигар и/или трубки, а также нюхание табака.
Десятый вариант осуществления изобретения относится к способу избавления от привычки курить, который включает введение субъекту, привыкшему курить табак, терапевтически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
В предпочтительном способе по этому варианту осуществления изобретения рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат вводят перорально, через слизистую оболочку или чрескожно. В более предпочтительном способе рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат вводятся чрескожно.
Другим предпочтительным способом по этому варианту осуществления изобретения является способ избавления от привычки курить, который включает введение субъекту, привыкшему курить табак, терапевтически эффективные количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата и никотина. Никотин и/или рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат предпочтительно вводят перорально, через слизистую оболочку или чрескожно. Никотин и/или рацетически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат более предпочтительно вводят чрескожно.
Другим способом по этому варианту осуществления изобретения является способ лечения или профилактики увеличения веса вследствие избавления от привычки курить, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Одиннадцатый вариант осуществления изобретения относится к способу лечения или профилактики хронической болезни, выбранной из группы, включающей нарколепсию, синдром хронической усталости, сезонное аффективное расстройство, фибромиалгию и предменструальный синдром (или предменструальную дисфорию). Этот способ включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Предпочтительными способами по этому варианту осуществления изобретения являются способы лечения или профилактики предменструального синдрома, нарколепсии и синдрома хронической усталости.
Двенадцатый вариант осуществления изобретения относится к способу лечения или профилактики состояния тревоги, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Тринадцатый вариант осуществления изобретения относится к способу лечения или профилактики нарушения питания, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
Четырнадцатый вариант осуществления изобретения относится к способу лечения или профилактики мигрени или головной боли, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата.
В используемом здесь значении термины “обсессивно-компульсивное расстройство”, “предменструальный синдром”, “состояние тревоги”, “нарушение питания” и “мигрень” употребляются в значениях, принятых в этой области. См., например, DSM-IV™ и DSM-III™. Термин “способы лечения или профилактики”, употребляемый в сочетании с этими заболеваниями, означает достижение положительной динамики заболевания, предупреждение возникновения или ослабление симптомов и/или проявлений, характерных для этих заболеваний.
Пятнадцатый вариант осуществления изобретения относится к способу лечения или профилактики недержания, который включает введение субъекту, нуждающемуся в таком лечении или профилактике, терапевтически или профилактически эффективного количества рацемического или оптически чистого метаболита сибутрамина, его фармацевтически приемлемой соли, сольвата или клатрата. В частности, рацемический или оптически чистый метаболит сибутрамина можно использовать для лечения недержания кала, недержания мочи при напряжении (“SUI”), недержания мочи при усилии, недержания мочи при позыве на мочеиспускание, рефлекторного недержания, пассивного недержания и недержания мочи вследствие переполнения мочевого пузыря.
В используемом в описании значении термин “лечение или профилактика недержания” означает лечение, предупреждение возникновения или ослабление симптомов недержания, включая непроизвольное выделение кала или мочи и просачивание кала или мочи, что может быть вызвано одной или несколькими причинами, которые включают, но не ограничиваются ими, патологию управления сфинктером, потерю чувствительности, перерастяжение мочевого пузыря, гиперрефлексию и/или непроизвольное расслабление мочеиспускательного канала, ослабление мускулатуры мочевого пузыря или нейрологические нарушения.
Предпочтительным способом по этому варианту осуществления изобретения является способ лечения или профилактики недержания мочи при напряжении. В соответствии с другим предпочтительным способом по этому варианту осуществления изобретения нуждающимся субъектом является пожилой человек в возрасте старше 50 лет или ребенок в возрасте моложе 13 лет.
Шестнадцатый вариант осуществления изобретения относится к фармацевтическим композициям и лекарственным формам, содержащим рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат. Эти фармацевтические композиции и лекарственные формы являются особенно полезными при осуществлении вышеописанных способов. Лекарственные формы по этому изобретению пригодны для перорального введения, введения через слизистую оболочку (например, назального, подъязычного, трансбуккального, ректального и вагинального), парентерального (например, внутривенного и внутримышечного), чрескожного или подкожного введения. Предпочтительные лекарственные формы по этому изобретению предназначены для перорального, чрескожного введения или введения через слизистую оболочку.
Предпочтительные рацемические и оптические чистые метаболиты сибутрамина включают, но не ограничиваются ими, (+)-десметилсибутрамин, (-)-десметилсибутрамин, (±)-десметил-сибутрамин, (+)-дидесметилсибутрамин, (-)-дидесметилсибутрамин и (±)-дидесметилсибутрамин.
Оптически чистые метаболиты сибутрамина являются наиболее предпочтительными. В используемом значении термин “оптически чистый” означает, что композиция содержит более 90 вес.% требуемого стереоизомера, предпочтительно более 95 вес.% стереоизомера и наиболее предпочтительно более 99 вес.% требуемого стереоизомеры в расчете не общую массу активного ингредиента. Например, оптически чистый (+)-десметилсибутрамин по существу не содержит (-)-десметилсибутрамина. В используемом значении термин “по существу не содержит” означает, что композиции содержит менее 10 вес.%, предпочтительноменее 5 вес.% и наиболее предпочтительно менее 1 вес.% другого соединения.
Предполагается, что фармацевтически приемлемые соли, сольваты и клатраты рацемических и оптически чистых метаболитов сибутрамина должны использоваться в фармацевтических композициях, лекарственных формах и способах по этому изобретению. В используемом значении термин “фармацевтически приемлемая соль” означает соль, полученную из фармацевтически приемлемой нетоксичной неорганической или органической кислоты. Неорганическими кислотами являются, но не ограничиваются ими, хлористоводородная, бромистоводородная, иодистоводородная, азотная, серная и фосфорная кислоты. Органическими кислотами являются, но не ограничиваются ими, алифатические, ароматические, карбоновые и сульфоновые органические кислоты, к которым относятся, но не ограничиваются ими, муравьиная, уксусная, пропионовая, янтарная, бензойная, камфорсульфоновая, лимонная, фумаровая, глюконовая, изэтионовая, молочная, яблочная, слизевая, винная, паратолуолсульфоновая, гликолевая, глюкуроновая, малеиновая, фуроновая, глутаминовая, бензойная, антраниловая, салициловая, фенилуксусная, миндальная, памовая, метансульфоновая, этансульфоновая, пантотеновая, бензолсульфоновая, стеариновая, сульфаниловая, альгиновая и галактуроновая кислоты. Особенно предпочтительными кислотами являются бромистоводородная, хлористоводородная, фосфорная и серная кислоты, и наиболее предпочтительной кислотой является хлористоводородная кислота.
Во всех способах по этому изобретению метаболит сибутрамина, или его фармацевтически приемлемую соль, сольват или клатрат можно вводить вместе с одним или несколькими дополнительными фармакологически активными соединениями, т.е. метаболит сибутрамина и по крайней мере одно дополнительное фармакологически активное соединения вводят в виде комбинации, одновременно, но раздельно, или последовательно любым приемлемым способом (например, перорально, чрескожно или через слизистую оболочку). Кроме того, предпочтительные фармацевтические композиции и лекарственные формы по этому изобретению могут содержать фармацевтически приемлемый наполнитель и/или по крайней мере одно дополнительное фармакологически активное соединение.
Дополнительными фармакологически активными соединениями, которые можно использовать в способах и композициях по этому изобретению, являются, но не ограничиваются ими, лекарственные средства, воздействующие на центральную нервную систему (“CNS”), к которым относятся, но не ограничиваются ими, агонисты и антагонисты 5-НТ (например, 5-НТ3 и 5-НТ1А); избирательно действующие ингибиторы обратного захвата серотонина (“SSRI”); снотворные и седативные средства; лекарственные средства для лечения психиатрических заболеваний, включая антипсихотические и нейролептические средства, средства против страха, антидепрессанты и транквилизаторы; стимуляторы центральной нервной системы, такие как амфетамины; агонисты рецепторов допамина; сурьмянокислые средства; средства против панического состояния; сердечно-сосудистые средства (например, блокаторы бета-рецепторов и ингибиторы ангиотензин-превращающих ферментов); противовирусные средства; антибиотики; противогрибковые средства и противоопухолевые средства.
Более специфическими лекарственными средствами, воздействующими на центральную нервную систему, являются, но не ограничиваются ими, SSRI, соединения бензодиазепина, трициклические антидепрессанты, антипсихотические средства, транквилизаторы, антагонисты β-адренергических рецепторов, антагонисты рецепторов 5-НТ1А и агонисты рецепторов 5-НТ3. Еще более специфическими лекарственными средствами, воздействующими на центральную нервную систему, являются, но не ограничиваются ими, лоразепам, томоксетин, оланзапин, респирадон, буспирон, гидроксизин и валиум.
Избирательно действующими ингибиторами обратного захвата серотонина являются соединения, которые подавляют поглощение серотонина центральной нервной системой, характеризуясь при этом слабым или ограниченным сродством к другим нейрологически активным рецепторам. Примеры SSRI включают, но не ограничиваются ими, циталопрам (CELEXA®), флуоксетин (PROZAC®), флувоксамин (LUVOX®), пароксетин (PAXIL®), сертралин (ZOLOFT®), венлафаксин (EFFEXOR®) и их оптически чистые стереоизомеры, активные метаболиты, фармацевтически приемлемые соли, сольваты и клатраты.
Соединения бензодиазепина, которые можно использовать в способах и композициях по этому изобретению, включают, но не ограничиваются ими, соединения, описанные в статье Goodman & Gilman, The Pharmacological Basis of Therapeu-tics, 362-373 (9th ed. McGraw-Hill, 1996). Примерами специфических бензодиазепинов являются, но не ограничиваются ими, альпразолам, бротизолам, хлордиазепоксид, клобазам, клоназепам, клоразепат, демоксепам, диазепам, эстазолам, флумазенил, флуразепам, галазепам, лоразепам, мидазолам, нитразепам, нордазепам, оксазепам, празепам, квазепам, темазепам, триазолам, их фармакологически активные метаболиты и стереоизомеры, фармацевтически приемлемые соли, сольваты и клатраты. Ниже приведены торговые названия некоторых из этих соединений.
Альпразолам, имеющий химическое название 8-хлор-1-метил-6-фенил-4Н-s-триазоло[4,3-α][1,4]бензодиазепин, продается под торговым названием XANAX®. XANAX® предназначен для лечения состояния тревоги (состояния, которое ближе всего соответствует диагнозу генерализованного состояния страха DSM-III™) или кратковременного ослабления симптомов тревоги. Physician's Desk Reference® 2516-2521 (53rd ed., 1999).
Хлористоводородная соль хлордиазепоксида, имеющая химическое название гидрохлорид 7-хлор-2-(метиламино)-5-фенил-3Н-1,4-бензодиазепин-4-оксида, продается под торговым названием LIBRIUM®. LIBRIUM® предназначен для лечения состояния тревоги или кратковременного ослабления симптомов состояния тревоги, снятия симптомов алкогольного опьянения, ощущения тревоги и страха перед операцией. Physician's Desk Reference® 1369-1370 (53rd ed., 1999).
Клоназепам, имеющий химическое название 5-(2-хлорфенил)-1,3-дигидро-7-нитро-2Н-1,4-бензодиазепин-2-он, продается под торговым названием KLONOPIN®. KLONOPIN® предназначен для использования в качестве основного или вспомогательного лекарственного средства при лечении синдрома Леннокса-Гастота (разновидность плохого аппетита), акинетических и миоклонических припадков. KLONOPIN® предназначен также для лечения панического состояния, сопровождающегося или не сопровождающегося агорафобией, диагностируемого в DSM-IV™. Physician's Desk Reference® 2688-2691 (53rd ed., 1999).
Двукалиевая соль клоразепата, имеющая химическое название 7-хлор-2,3-дигидро-2,2-дигидрокси-5-фенил-1Н-1,4-бензодиазепин-3-карбоксильное двукалиевое соединение, продается под торговым названием TRANXENE®. TRANXENE® предназначен для лечения состояния тревоги или для кратковременного ослабления симптомов тревоги, в качестве вспомогательного лекарственного средства для лечения частичных припадков и для снятия симптомов синдрома отмены алькоголя. Physician's Desk Reference® 475-476 (53rd ed., 1999).
Диазепам, имеющий химическое название 7-хлор-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бензодиазепин-2-он, продается под торговым названием VALIUM®. VALIUM® предназначен для лечения состояния тревоги или для кратковременного ослабления симптомов тревоги. Physician's Desk Reference® 2735-2736 (53rd ed., 1999).
Эстазолам, имеющий химическое название 8-хлор-6-фенил-4Н-s-триазоло[4,3-α][1,4]бензодиазепин, продается под торговым названием PROSOM®. PROSOM® предназначен для кратковременного лечения бессонницы, характерными симптомами которой являются плохое засыпание, частое просыпание ночью и/или ранее пробуждение утром. Physician's Desk Reference® 473-475 (53rd ed., 1999).
Флумазенил, имеющий химическое название этил-8-фтор-5,6-дигидро-5-метил-6-оксо-4Н-имидазо[1,5-a][1,4]бензодиазепин-3-карбоксилат, продается под торговым названием ROMAZICON®. ROMAZICON® предназначен для полного или частичного устранения седативного действия бензодиазепинов в случае их использования для проведения наркоза, для выполнения диагностических и терапевтических процедур и для лечения последствий передозировки бензодиазепина. Physician's Desk Reference® 2701-2704 (53rd ed., 1999).
Хлористоводородная соль флуразепама, имеющая химическое название дигидрохлорид 7-хлор-1-[2-(диэтиламино)этил]-5-(о-фторфенил)-1,3-дигидро-2Н-1,4-бензодиазепин-2-она, продается под торговым названием DALMANE®. DALMANE® является снотворным средством, предназначенным лечения бессонницы, характерными симптомами которой являются плохое засыпание, частое просыпание ночью и/или ранее пробуждение утром. Physician's Desk Reference® 2520 (52rd ed., 1998).
Лоразепам, имеющий химическое название 7-хлор-5-(о-хлорфенил)-1,3-дигидро-3-гидрокси-2Н-1,4-бензодиазепин-2-он, продается под торговым названием ATIVAN®. ATIVAN® предназначен для лечения состояния тревоги или для кратковременного ослабления симптомов состояния тревоги или беспокойства, связанного с депрессивными симптомами. Physician's Desk Reference® 3267-3272 (53rd ed., 1999).
Хлористоводородная соль мидазолама, имеющая химическое название гидрохлорид 8-хлор-6-(2-фторфенил)-1-метил-4Н-имидазо[1,5-a][1,4]-бензодиазепина, продается под торговым названием VERSED®. VERSED® предназначен для предоперационного воздействия седативным средством/подавления состояния тревоги/амнезии и общего наркоза. Physician's Desk Reference® 2720-2726 (53rd ed., 1999).
Оксазепам, имеющий химическое название 7-хлор-1,3-дигидро-3-гидрокси-5-фенил-2Н-1,4-бензодиазепин-2-он, продается под торговым названием SERAX®. SERAX® предназначен для лечения состояния тревоги или для кратковременного ослабления симптомов состояния тревоги. Physician's Desk Reference® 3383-3384 (53rd ed., 1999).
Квазепам, имеющий химическое название 7-хлор-5-(о-фторфенил)-1,3-дигидро-1-(2,2,2-трифторэтил)-2Н-1,4-бензодиазепин-2-тион, продается под торговым названием DORAL®. DORAL® предназначен для лечения бессонницы, характерными симптомами которой являются плохое засыпание, частое просыпание ночью и/или ранее пробуждение утром. Physician's Desk Reference® 2958 (52rd ed., 1998).
Темазепам, имеющий химическое название 7-хлор-1,3-дигидро-3-гидрокси-1-метил-5-фенил-2Н-1,4-бензодиазепин-2-он, продается под торговым названием RESTORIL®. RESTORIL® предназначен для кратковременного лечения бессонницы. Physician's Desk Reference® 2075-2078 (53rd ed., 1999).
Триазолам, имеющий химическое название 8-хлор-6-(о-хлорфенил)-1-метил-4Н-s-триазоло[4,3-α][1,4]бензодиазепин, продается под торговым названием HALCION®. HALCION® предназначен для кратковременного лечения бессонницы. Physician's Desk Reference® 2490-2493 (53rd ed., 1999).
Клиницистам, врачам или психиатрам должно быть известно, какое из вышеуказанных соединений можно использовать в комбинации с рацемическим или оптически чистым метаболитом сибутрамина, его фармацевтически приемлемой солью, сольватом или клатратом для лечения или профилактики данного заболевания, хотя в этом описании изобретения рассмотрены только предпочтительные комбинации.
Заболевания, которые можно лечить или предупредить, используя рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с бензодиазепином, аналогичным вышеуказанным соединениям, включают, но не ограничивается ими, аффективные расстройства (например, депрессию), состояние тревоги, нарушения питания и нарушения функции головного мозга.
Это изобретение далее относится к фармацевтическим композициям, содержащим рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с антипсихотическим средством, и к способам их применения. Антипсихотические средства используют, прежде всего, для лечения пациентов, страдающих психотическими или другими серьезными психиатрическими заболеваниями, характерными симптомами которых являются беспокойство и нарушение логического мышления. Эти лекарственные средства обладают и другими свойствами, которые полезны в клинических условиях, включая противорвотное и антигистаминное действие и способность усиливать действие анальгетиков, седативных средств и анестезирующих средств общего действия. Специфическими антипсихотическими средствами являются трициклические антипсихотические средства, которые можно подразделить на три типа: фенотиазины, тиоксантены и другие гетероциклические соединения, которые можно использовать в способах и композициях по этому изобретению. См., например, Goodman & Gilman, The Pharmacological Basis of Therapeutics, 404 (9th ed. McGraw-Hill, 1996).
Специфическими трициклическими антипсихотическими соединениями являются, но не ограничиваются ими, хлорпромазин, мезоридазин, тиоридазин, ацетофеназин, флуфеназин, перфеназин, трифлуоперазин, хлорпротиксен, тиотиксен, клозапин, галоперидол, локсапин, молиндон, пимозид, рисперидон, дезипрамин, их фармакологически активные метаболиты и стереоизомеры, фармацевтически приемлемые соли, сольваты и клатраты. Ниже приведены торговые названия некоторых из этих соединений.
Хлорпромазин, имеющий химическое название 10-(3-диметиламинопропил)-2-хлорфенотиазин, продается под торговым названием THORAZINE®. THORAZINE® предназначен наряду с прочим для лечения психотических нарушений. Physician's Desk Reference® 3101-3104 (53rd ed., 1999).
Безилат мезоридазина, имеющий химическое название 10-[2-(1-метил-2-пиперидил)этил]-2-метилсильфинил)фенотиазин, продается под торговым названием SERENTIL®. SERENTIL® предназначен для лечения шизофрении, нарушений поведения при умственной неполноценности и хроническом мозговом синдроме, алкоголизма и психоневротических нарушений. Physician's Desk Reference® 764-766 (53rd ed., 1999).
Перфеназин, имеющий химическое название 4-[3-(2-хлорфенотиазин-10-ил)пропил-1-пиперазинэтанол, продается под торговым названием TRILAFON®. TRILAFON® предназначен для лечения психотических нарушений, сильной тошноты и рвоты у взрослых. Physician's Desk Reference® 2886-2888 (53rd ed., 1999).
Трифлуоперазин, имеющий химическое название 10-[3-(4-метил-1-пиперазинил)пропил]-2-(трифторметил)-10Н-фенотиазин, продается под торговым названием STELAZINE®. STELAZINE® предназначен для лечения психотических нарушений и для кратковременного лечения генерализованного непсихотического состояния страха. Physician's Desk Reference® 3092-3094 (53rd ed., 1999).
Тиотиксен, имеющий химическое название N,N-диметил-9-[3-(4-метил-1-пиперазинил)пропилиден]тиоксантен-2-сульфонамид, продается под торговым названием NAVANE®. NAVANE® предназначен для лечения психотических нарушений. Physician's Desk Reference® 2396-2399 (53rd ed., 1999).
Клозапин, имеющий химическое название 8-хлор-11-(4-метил-1-пиперазинил)-5Н-дибензо[b,e][1,4]диазепин, продается под торговым названием CLOZARIL®. CLOZARIL® предназначен для лечения пациентов с тяжелой формой шизофрении, которые неадекватно реагируют на лечение стандартными антипсихотическими средствами. Physician's Desk Reference® 2004-2009 (53rd ed., 1999).
Галоперидол, имеющий химическое название 4-[4-(п-хлорфенил)-4-гидроксипиперидонол-4'-фторбутирофенон, продается под торговым названием HALDOL®. HALDOL® предназначен для лечения пациентов, нуждающихся в длительном парентеральном введении антипсихотических средств (например, пациентов, страдающих хронической шизофренией). Physician's Desk Reference® 2190-2192 (53rd ed., 1999).
Локсапин, имеющий химическое название 2-хлор-11-(4-метил-1-пиперазинил)дибенз[b,f][1,4]оксаксепин, продается под торговым названием LOXITANE®. LOXITANE® предназначен для лечения психотических нарушений. Physician's Desk Reference® 3224-3225 (53rd ed., 1999).
Молиндон, имеющий химическое название гидрохлорид 3-этил-6,7-дигидро-2-метил-5-(морфолинометил)индол-4(5Н)-она, продается под торговым названием MOBAN®. MOBAN® предназначен для лечения психотических нарушений. Physician's Desk Reference® 978-979 (53rd ed., 1999).
Пимозид, имеющий химическое название 1-[1-[4,4-бис(4-фторфенил)-бутил]-4-пиперидинил]-1,3-дигидро-2Н-бензимида-зол-2-он, продается под торговым названием ORAP®. ORAP® предназначен для подавления двигательных и голосовых тиков у пациентов, страдающих болезнью Туретта, лечение которых стандартными методами не дает удовлетворительных результатов. Physician's Desk Reference® 1054-1056 (53rd ed., 1999).
Рисперидон, имеющий химическое название 3-[2-[4-(6-фтор-1,2-бензизоксазол-3-ил)-1-пиперидинил]этил]-6,7,8,9-тетрагидро-2-метил-4Н-пиридо[1,2-a]пиримидин-4-он, продается под торговым названием RISPERDAL®. RISPERDAL® предназначен для лечения психотических нарушений. Physician's Desk Reference® 1432-1436 (53rd ed., 1999).
Хлористоводородная соль дезипрамина, имеющая химическое название 5Н-дибенз[b,f]азепин-5-пропанамин-10,11-дигидро-N-метилмоногидрохлорид, продается под торговым названием NORPRAMIN®. NORPRAMIN® предназначен для лечения депрессии. Physician's Desk Reference® 1332-1334 (53rd ed., 1999).
Заболевания, которые можно лечить или предупредить, используя рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с антипсихотическим соединения и, в частности, с трициклическим антипсихотическим соединением, включают, но не ограничиваются ими, аффективные расстройства (например, депрессию), состояние тревоги, нарушения питания и нарушения функции головного мозга (например, шизофрению), которые аналогичны рассмотренным в этом описании изобретения.
Это изобретение далее относится к фармацевтическим композициям, содержащим рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с антагонистом рецепторов
5-НТ1А и/или антагонистом β-адренергических рецепторов, и к способам их применения. Примерами антагонистов рецепторов 5-НТ1А и антагонистов β-адренергических рецепторов, которые можно использовать в способах и композициях по этому изобретению, являются, но не ограничиваются ими, альпренолол, WAY 100135, спиперон, пиндолол, (S)-UH-301, пенбутолол, пропранолол, тертатолол, соединение формулы I, описанное в патенте США № 5552429, который включен в это описание изобретения в качестве ссылки; их фармакологически активные метаболиты и стереоизомеры, фармацевтически приемлемые соли, сольваты и клатраты.
Альпренолол, имеющий химическое название 1-(1-метилэтил)амино-3-[2-(2-пропенил)фенокси]-2-пропанол, описан в патенте США № 3466325, который включен в это описание изобретения в качестве ссылки.
WAY 100135, имеющий химическое название N-(трет-бутил)-3-[4-(2-метоксифенил)пиперазин-1-ил]-2-фенилпропанамид, описан в патенте США № 4988814, который включен в это описание изобретения в качестве ссылки. См. также Cliffe et al., J. Med. Chem., 36:1509-1510 (1993).
Спиперон, имеющий химическое название 8-[4-(4-фторфенил)-4-оксобутил]-1-фенил-1,3,8-триазаспиро[4,5]де-кан-4-он, описан в патентах США №№ 3155669 и 3155670, которые включены в это описание изобретения в качестве ссылки. См. также Middlmiss et al., Neurosci. and Biobehav. Rev., 16:75-82 (1992).
Пиндолол, имеющий химическое название 4-(2-гидрокси-3-изопропиламинопропокси)индол, описан в патенте США № 3471515, который включен в это описание изобретения в качестве ссылки. См. также Dreshfield et al., Neurochem. Res., 21(5):557-562 (1996).
(S)-UH-301, имеющий химическое название (S)-5-фтор-8-гидрокси-2-дипропиламинотетралин, хорошо известен фармакологам и фармацевтам. См., например, Hillyer et al., J. Med. Chem., 33:1541-44 (1990) and Moreau et al., Brain Res. Bull., 29:901-04 (1992).
Пенбутолол, имеющий химическое название (1-(трет-бутиламино)-2-гидрокси-3-(2-циклопентилфенокси)пропан), продается под торговым названием LEVATOL®. LEVATOL® предназначен для лечения легкой и средней формы артериальной гипертензии. Physician's Desk Reference® 2908-2910 (53rd ed., 1999).
Хлористоводородная соль пропранолола, имеющая химическое название гидрохлорид 1-изопропиламино-3-(1-нафталинилокси)-2-пропанола, продается под торговым названием INDERAL®. INDERAL® предназначен для лечения гипертензии. Physician's Desk Reference® 3307-3309 (53rd ed., 1999).
Тертатолол, имеющий химическое название 8-(3-трет-бутиламино-2-гидроксипропилокси)тиохроман, описан в патенте США № 3960891, который включен в это описание изобретения в качестве ссылки.
Заболевания, которые можно лечить или предупредить, используя рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с антагонистом рецепторов 5-НТ1А, включают, но не ограничиваются ими, депрессию, обсессивно-компульсивные расстройства, нарушения питания, гипертензию, мигрень, эссенциальное дрожание, гипертрофический субаортальный мышечный стеноз и феохромоцитому. При помощи этих соединений можно лечить или предупредить такое специфическое заболевание, как посттравматическую депрессию.
Заболевания, которые можно лечить или предупредить, используя рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с антагонистом β-адренергических рецепторов, включают, но не ограничиваются ими, депрессию после инфаркта миокарда. Специфическими антагонистами β-адренергических рецепторов являются, но не ограничиваются ими, S(-)-пиндолол, пенбутолол и пропранолол.
Это изобретение далее относится к фармацевтическим композициям, содержащим рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с веществами, не являющимися бензодиазепином или трициклическими средствами, и к способам их применения. Примерами таких дополнительных фармакологически активных соединений являются, но не ограничиваются ими, оланзапин, буспирон, гидроксизин, томоксетин, их фармакологически активные метаболиты и стереоизомеры, фармацевтически приемлемые соли, сольваты и клатраты.
Оланзапин, имеющий химическое название 2-метил-4-(4-метил-1-пиперазинил)-10Н-тиено[2,3-b][1,5]бензодиазепин, продается под торговым названием ZYPREXA®. ZYPREXA® предназначен для лечения психотических нарушений. Physician's Desk Reference® 1641-1645 (53rd ed., 1999).
Хлористоводородная соль буспирона, имеющая химическое название моногидрохлорид 8-[4-[4-(2-пиримидинил)-1-пиперазинил]бутил]-8-азаспиро[4,5]декан-7,9-диона, продается под торговым названием BUSPAR®. BUSPAR® предназначен для лечения состояния страха или для кратковременного ослабления симптомов страха. Physician's Desk Reference® 823-825 (53rd ed., 1999).
Хлористоводородная соль гидроксизина, имеющая химическое название дигидрохлорид 1-(п-хлорбензгидрил)-4[2-(2-гидроксиэтокси)этил]пиперазина, продается под торговым названием ATARAX®. ATARAX® предназначен для ослабления симптомов страха и напряжения, связанных с психоневрозом, и в качестве вспомогательного средства при лечении заболеваний разных органов, сопровождающихся состоянием страха. Physician's Desk Reference® 2367-2368 (53rd ed., 1999).
Заболевания, которые можно лечить или предупредить, используя рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемую соль, сольват или клатрат в комбинации с соединением, выбираемым из группы, включающей лоразепам, томоксетин, оланзапин, респирадон, буспирон, гидроксизин, валиум, их фармакологически активные метаболиты и стереоизомеры, фармацевтически приемлемые соли, сольваты, клатраты, включают, но не ограничиваются ими, состояние тревоги, депрессию, гипертензию и нарушение внимания.
Несмотря на то, что все комбинации рацемических и оптически чистых метаболитов сибутрамина, их фармацевтически приемлемых солей, сольватов и клатратов и одного или нескольких вышеописанных фармакологически активных соединений являются полезными и ценными, некоторые комбинации являются особенно предпочтительными. Примерами предпочтительных комбинаций являются такие комбинации, в которых рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемая соль, сольват или клатрат использован вместе с одним из нижеследующих соединений:
Синтез метаболитов сибутрамина
Рацемический сибутрамин, десметилсибутрамин и дидесметилсибутрамин можно получить при помощи методов, хорошо известных специалистам в этой области. См., например, патент США № 4806570, который включен в это описание изобретения в качестве ссылки; J. Med. Chem., 2540 (1993) (тозилирование и замещение азида); Butler, D., J. Org. Chem., 36:1308 (1971) (циклоалкилирование в ДМСО); Tetrahedron Lett., 155-58 (1980) (реакция присоединения реактива Гриньяра к нитрилу в бензоле); Tetrahedron Lett., 857 (1997) (ОН к азиду) и Jeffery, J.E., et al., J.Chem.Soc.Perkin.Trans 1, 2583 (1996).
Предпочтительный способ получения рацемического сибутрамина описан в нижеследующем примере 1.
Рацемический сибутрамин, десметилсибутрамин и дидесметилсибутрамин можно получить друг из друга так же, как и оптически чистые формы этих соединений. Предпочтительные способы получения одного соединения из другого описаны в нижеследующих примерах 2, 3 и 8. Оптически чистые энантиомеры сибутрамина и его метаболиты можно получить при помощи методов, известных в этой области. Предпочтительным методом является разделение фракционной кристаллизацией диастереомерных солей, полученных при помощи оптически активных разделяющих агентов. См., например, “Enantiomers, Racemates and Resolutions”, by J. Jacques, A. Collet, ans S.H. Wilen, (Wiley-Interscience, New York, 1981); S.H. Wilen, A. Collet, and J. Jacques, Tetrahedron, 2725 (1977); E.L. Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill. NY, 1962); and S.H. Wilen, Tables of Resolving Agents and Optical Resolutions 268 (E.L. Eliel ed., Univ. of Notre Dame Press, Notre Dame, IN, 1972).
Поскольку сибутрамин, десметилсибутрамин и дидесметилсибутрамин являются основными аминами, диастереомерные соли этих соединений, пригодные для разделения фракционной кристаллизацией, можно легко получить путем присоединения разделяющих агентов на основе оптически чистых хиральных кислот. Приемлемыми разделяющими агентами являются, но не ограничиваются ими, оптически чистые винная, камфорсульфоновая, миндальная кислоты и их производные. Оптически чистые изомеры сибутрамина, десметилсибутрамина и дидесметилсибутрамина можно выделить из кристаллизованного диастереомера или маточного раствора в зависимости от растворимости используемого разделяющего агента на основе кислоты и используемого энантиомера кислоты. Идентичность и оптическую чистоту полученного таким образом сибутрамина или изомера метаболита сибутрамина можно определить при помощи поляриметрии или других аналитических методов.
Рацемические и оптически чистые метаболиты сибутрамина предпочтительно синтезируют способами, описанными Jeffery, J.E., et al., J. Chem. Soc. Perkin. Trans 1, 2583 (1996). Предпочтительный способ прямого синтеза рацемического десметилсибутрамина включает восстановление циклобутанкарбонитрила (CCBC) для получения промежуточного альдегида, который затем подвергают взаимодействию с амином, таким как метиламин. Это способ использован в нижеследующем примере 4.
Другой предпочтительный способ прямого синтеза рацемического десметилсибутрамина включает взаимодействие ССВС с соединением формулы i-BuMX, в которой Х обозначает Br или I и М выбирают из группы, включающей Li, Mg, Zn, Cr и Mn. Это соединение предпочтительно имеет формулу i-BuMgBr. В результате выполнения этой реакции получают продукт, который затем восстанавливают, превращают в промежуточное соединение, представляющее собой альдегид, связанный с атомом азота, которое в конечном счете превращают в десметилсибутрамин на стадии добавление кислоты Льюиса. Предпочтительные кислоты Льюиса выбирают из группы, включающей BH3 .ТГФ, BF3 .ТГФ, La(O-i-Pr)3, Zr(O-i-Pr)4, Ti(O-i-Pr)2Cl2, SnCl4 и MgBr2 .OEt2. Наиболее предпочтительной кислотой Льюиса является BH3 .ТГФ. Этот способ использован в нижеследующем примере 5.
Энантиомеры десметилсибутрамина можно получить в результате образования хиральных солей, как это описано выше. Предпочтительными хиральными кислотами, используемыми для получения хиральных солей, являются, но не ограничиваются ими, винная и миндальная кислоты. При использовании винной кислоты предпочтительными системами растворителей являются, но не ограничиваются ими, этанол/вода и изопропиловый спирт/вода. При использовании миндальной кислоты предпочтительной системой растворителей является этилацетат/гексан. Выделение десметилсибутрамина описано в нижеследующих примерах 6 и 7.
Предпочтительный способ прямого синтеза рацемического дидесметилсибутрамина включает взаимодействие ССВС с соединением формулы i-BuMX, в которой Х обозначает Br или I и М выбирают из группы, включающей Li, Mg, Zn, Cr и Mn. Это соединение предпочтительно имеет формулу i-BuMgBr. Продукт этой реакции затем восстанавливают в приемлемых условиях реакции. Применение этого способа показано в нижеследующем примере 9.
Энантиомеры дидесметилсибутрамина можно получить в результате образования хиральных солей, как это описано выше. Предпочтительной хиральной кислотой, используемой для получения хиральных солей, является, но не ограничивается ею, винная кислота. Предпочтительными системами растворителей являются, но не ограничиваются ими ацетонитрил/вода/метанол и ацетонитрил/метанол. Выделение дидесметилсибутрамина описано в нижеследующих примерах 11 и 12.
Фармацевтические композиции и способы их применения
Величина профилактической или лечебной дозы активного ингредиента при лечении острой или хронической формы заболевания или нарушения изменяется в зависимости от тяжести заболевания и способа введения. Величина дозы и частота введения лекарственного средства зависят также от возраста, массы тела, реакции и анамнеза пациента. Специалист в этой области может легко выбрать приемлемые схемы введения лекарственных средств с учетом этих факторов.
Можно легко определить приемлемые дневные дозы лекарственных средств, предназначенных для лечения или профилактики описанных здесь заболеваний. Рекомендуемая доза рацемического или оптически чистого метаболита сибутрамина составляет от около 0,1 мг до около 60 мг/день при введении в виде однократной дозы один раз в день утром или в виде нескольких доз в течение всего дня. Дневная доза предпочтительно составляет от около 2 мг до около 30 мг/день, более предпочтительно от около 5 мг до около 15 мг/день.
Приемлемые дневные дозы дополнительных фармакологически активных соединений, которые можно вводить вместе с рацемическим или оптически чистым метаболитом сибутрамина можно легко определить с учетом доз, указанных в научной литературе и рекомендуемых в справочнике Physician's Desk Reference® (53rd ed., 1999).
Например, приемлемые легко определяемые дневные дозы антагонистов 5-НТ3 изменяются в зависимости от вышеуказанных факторов и конкретных используемых антагонистов 5-НТ3. Как правило, общая дневная доза антагониста 5-НТ3, предназначенного для лечения или профилактики описанного здесь заболевания, составляет от около 0,5 мг до около 500 мг, предпочтительно от около 1 мг до около 350 мг и более предпочтительно от около 2 мг до около 250 мг/день.
Введение активного ингредиента по этому изобретению в лечебных или профилактических целях начинают с более низкой дозы, например от около 2 мг до около 8 мг метаболита сибутрамина и необязательно от около 15 мг до около 60 мг антагониста 5-НТ3, после чего при необходимости дозу увеличивают до рекомендуемой дневной дозы, вводимой в виде однократной дозы или нескольких раздельных доз, в зависимости от общей реакции пациента. Пациентам в возрасте старше 65 лет рекомендуется вводить дозы метаболита сибутрамина от около 5 мг до около 30 мг/день в зависимости от общей реакции пациента. Иногда могут потребоваться дозы, выходящие за пределы указанных диапазонов, которые могут быть легко определены специалистами в фармацевтической области.
Количество и частота введения доз лекарственного препарата определяется используемыми терминами “терапевтически эффективный”, “профилактически эффективный” и “терапевтически или профилактически эффективный”. При использовании для определения количества рацемического или оптически чистого метаболита сибутрамина эти термины далее означают количество рацемического или оптически чистого метаболита сибутрамина, которое вызывает меньшее число или менее серьезные вредные эффекты, связанные с введением рацемического сибутрамина. Побочные эффекты, вызываемые рацемическим сибутрамином, включают, но не ограничиваются ими, значительное увеличение частоты сердечных сокращений в положении лежа на спине и в положении стоя, включая тахикардию, повышение кровяного давления (гипертензию), усиление психомоторной активности, сухость во рту, кариес зубов, запоры, гипогидроз, неясность зрения, напряжение, мидриаз, припадки, образование желчного конкремента, нарушение функции почек/печени, лихорадку, артрит, тревожное возбуждение, судороги икроножных мышц, гипертонию, неправильное мышление, бронхит, одышку, зуд, ослабление зрения, нарушение менструального цикла, экхимоз/кровотечение, интерстициальный нефрит и повышенную возбудимость. См., например, Physician's Desk Reference® 1494-1498 (53rd ed., 1999).
Совместное введение двух или более активных ингредиентов в соответствии со способами по этому изобретению может быть одновременным, последовательным или тем и другим вместе. Например, ингибитор обратного захвата допамина и антагонист 5-НТ3 можно вводить в виде комбинации, одновременно, но раздельно или последовательно.
Можно использовать любой приемлемый способ введения пациенту терапевтически или профилактически эффективной дозы активного ингредиента. Например, можно использовать такие способы, как пероральное введение, введение через слизистую оболочку (например, назальное, подъязычное, трансбуккальное, ректальное, вагинальное), парентеральное (например, внутривенное, внутримышечное), чрескожное и подкожное введение. Предпочтительными способами введения являются пероральный, чрескожный и через слизистую оболочку. Как указывалось выше, для лечения или профилактики нарушения эрекции активный ингредиент предпочтительно вводят через слизистую оболочку или чрескожно. Приемлемыми лекарственными формами для таких способов введения являются, но не ограничиваются ими, чрескожные пластыри, растворы для закапывания в глаза, распыляемые растворы и аэрозоли. Композиции для чрескожного введения могут быть также получены в виде кремов, лосьонов и/или эмульсий, которые могут быть смешаны с соответствсующим связующим веществом для фиксации на коже или введены в чрескожный пластырь матричного или емкостного типа, обычно применяемого для этой цели.
Предпочтительной лекарственной формой для чрескожного введения является пластырь “емкостного типа” или “матричного типа”, который фиксируют на коже в течение определенного периода времени для проникновения через кожу требуемого количества активного ингредиента. Например, если активным ингредиентом является метаболит сибутрамина, предпочтительный пластырь фиксируют на коже в течение 24 часов, в результате чего общая дневная доза составляет от около 0,1 мг до около 60 мг/день. Дневная доза предпочтительно составляет от около 2 мг до около 30 мг/день, более предпочтительно от около 5 мг до около 15 мг/день. Этот пластырь можно заменить свежим пластырем, если необходимо обеспечить постоянное введение активного ингредиента пациенту.
Другими лекарственными формами по этому изобретению являются, но не ограничиваются ими, таблетки, пилюли, лепешки, пастилки, дисперсии, суспензии, суппозитории, мази, припарки, пасты, порошки, повязки, кремы, пластыри, растворы, капсулы, мягкие эластичные желатиновые капсулы и наклейки.
В одном варианте осуществления изобретения фармацевтические композиции и лекарственные формы по этому изобретению содержат ингибитор обратного захвата допамина, такой как рацемический или оптически чистый метаболит сибутрамина, его фармацевтически приемлемая соль, сольват или клатрат, и необязательно дополнительное фармакологически активное вещество, такое как антагонист 5-НТ3. Предпочтительными рацемическими или оптически чистыми метаболитами сибутрамина являются (+)-десметил-сибутрамин, (-)-десметилсибутрамин, (±)-десметилсибутрамин, (+)-дидесметилсибутрамин, (-)-дидесметилсибутрамин и (±)-дидесметилсибутрамин. Фармацевтические композиции и лекарственные формы могут содержать фармацевтически приемлемый носитель и необязательно другие лечебные ингредиенты, известные специалистам в этой области.
В практическом применении активный ингредиент можно использовать для получения однородной смеси с фармацевтическим носителем в соответствии с известными фармацевтическими методами смешения. Носитель можно использовать в разных формах в зависимости от требуемой формы лекарственного препарата. При изготовлении композиций для пероральной лекарственной формы в качестве носителей можно использовать обычные фармацевтические среды, такие как, например, вода, гликоли, масла, спирты, ароматизаторы, консерванты, красители и тому подобные, предназначенные для жидких пероральных препаратов (таких как суспензии, растворы и эликсиры) или аэрозолей; и при изготовлении твердых пероральных препаратов предпочтительно без лактозы можно использовать такие носители, как крахмалы, сахара, микрокристаллическая целлюлоза, разбавители, гранулирующие средства, смазывающие вещества, связывающие вещества и дезинтегрирующие средства. Например, приемлемыми носителями являются порошки, капсулы и таблетки, причем твердые пероральные препараты более предпочтительны, чем жидкие препараты.
Благодаря простоте введения таблетки и капсулы являются наиболее предпочтительными пероральными лекарственными формами, в которых использованы твердые фармацевтические носители. При желании на таблетки можно нанести покрытие стандартными водными или неводными методами.
Помимо вышеуказанных обычных лекарственных форм активный ингредиент можно также вводить при помощи приспособлений с регулируемым высвобождением или устройств для доставки лекарственного средства, которые хорошо известны специалистам в этой области и аналогичны описанным в патентах США №№ 3845770, 3916899, 3536809, 3598123, 4008719, 5674533, 5059595, 5591767, 5120548, 5073543, 5639476, 5354556 и 5733566, которые включены в это описание изобретения в качестве ссылки. Эти лекарственные формы можно использовать для медленного или регулируемого высвобождения одного или нескольких активных ингредиентов при помощи, например, гидропропилметилцеллюлозных и других полимерных матриц, гелей, проницаемых мембран, осмотических систем, многослойных покрытий, микрочастиц, липосом, микросфер или их комбинаций для достижения требуемого профиля высвобождения в изменяющихся пропорциях. Для использования с фармацевтическими композициями по этому изобретению можно легко выбрать приемлемые препараты с регулируемым высвобождением, известные специалистам в этой области, в том числе и рассмотренные в этом описании изобретения. Таким образом, в объем этого изобретения входят однократные лекарственные формы, пригодные для перорального введения, такие как таблетки, капсулы, пилюли и лепешки, которые изготовлены с возможностью регулируемого высвобождения.
Все фармацевтические продукты с регулируемым высвобождением используют для достижения более высоких результатов лечения лекарственными средствами по сравнению с применением лекарственных средств с нерегулируемым высвобождением. В идеальном случае применение препарата с регулируемым высвобождением в медицинской практике отличается тем, что выздоровление или улучшение состояния пациента достигается при использовании минимального количества лекарственного средства в течение минимального периода времени. Препараты с регулируемым высвобождением имеют следующие преимущества: 1) более продолжительное действие лекарственного средства; 2) большие промежутки времени между введением лекарственного средства и 3) лучшее соблюдение больным режима и схемы лечения. Кроме того, препараты с регулируемым высвобождением можно использовать для изменения времени воздействия или других характеристик, таких как содержание лекарственного средства в крови, благодаря чему можно контролировать возникновение побочных эффектов.
Большинство препаратов с регулируемым высвобождением изготавливают с возможностью первоначального высвобождения такого количества лекарственного средства, которое сразу же обеспечивает достижение требуемого лечебного эффекта, и последующего постепенного высобождения других количеств лекарственного средства для сохранения полученного лечебного эффекта в течение продолжительного периода времени. Для сохранения постоянного уровня лекарственного средства в организме это лекарственное средство должно высвобождаться из лекарственной формы со скоростью, позволяющей возобновлять количество лекарственного средства, участвующего в обмене веществ и выводимого из организма. Регулируемое высвобождение активного ингредиента можно стимулировать разными индукторами, которые включают, но не ограничиваются ими, рН, температуру, ферменты, воду или другие физиологические условия или соединения.
Фармацевтические композиции по этому изобретению, пригодные для перорального введения, могут быть получены в виде отдельных лекарственных форм, таких как капсулы, крахмальные облатки, таблетки или аэрозоли, которые содержат заранее определенное количество активного ингредиента в виде порошка, гранул, раствора или суспензии в водном или неводном растворе, эмульсии масла в воде или жидкой эмульсии воды в масле. Такие лекарственные формы можно получить любыми методами, применяемыми в фармации, но все эти методы включают стадию смешения активного ингредиента с носителем, который состоит из одного или нескольких необходимых ингредиентов. Как правило, такие композиции получают, однородно смешивая активный ингредиент с жидкими носителями, тонко измельченными твердыми носителями или теми и другими вместе, при необходимости с последующим приданием продукту требуемой формы.
Например, таблетку можно получить прессованием или формованием необязательно с одним или несколькими вспомогательными ингредиентами. Прессованные таблетки можно получить прессованием в соответствующей таблетирующей машине свободно текущего активного ингредиента, такого как порошок или гранулы, необязательно смешанного с наполнителем, который включает, но не ограничивается ими, связывающее вещество, смазывающее вещество, инертный разбавитель и/или поверхностно-активное вещество или диспергирующее средство. Формованные таблетки можно получить формованием в соответствующей таблетирующей машине смеси порошкообразного соединения, смоченного инертным жидким разбавителем.
Это изобретение далее относится к фармацевтическим композициям и лекарственным формам без лактозы. Лактозу используют в качестве наполнителя в препаратах на основе сибутрамина. См., например, Physician's Desk Reference® 1494 (53rd ed., 1999). Однако в отличие от исходного лекарственного средства десметилсибутрамин и дидесметилсибутрамин являются соответственно вторичными и первичными аминами и поэтому могут разлагаться с течением времени под действием лактозы. Таким образом, композиции по этому изобретению, в состав которых входят метаболиты сибутрамина, предпочтительно содержат небольшое количество или вообще не содержат лактозу и другие моно- или дисахариды. В используемом здесь значении термин “без лактозы” означает, что имеющееся количество лактозы, если она вообще использована, является недостаточным для существенного увеличения скорости разложения активного ингредиента.
Композиции без лактозы по этому изобретению могут содержать наполнители, которые хорошо известны в этой области и приведены в USP (XXI)/NF (XVI), включенном в это описание изобретения в качестве ссылки. Как правило, композиции без лактозы содержат активный ингредиент, связывающее вещество/наполнитель и смазывающее вещество в фармацевтически совместимых и фармацевтически приемлемых количествах. Предпочтительные лекарственные формы без лактозы содержат активный ингредиент, микрокристаллическую целлюлозу, предварительно желатинированный крахмал и стеарат магния.
Это изобретение далее относится к безводным фармацевтическим композициям и лекарственным формам, содержащим активный ингредиент, так как вода облегчает разложение некоторых соединений. Например, общепринятой практикой в фармацевтической области является добавление воды (например, 5%) в качестве способа имитации долговременного хранения с целью определения таких характеристик, как срок годности или стабильность препаратов с течением времени. См., например, Jens T. Carstensen, Drug Stability: Principles & Practice, 2d. Ed., Marcel Dekker, NY, NY, 1995, pp. 379-80. Вода и тепло действительно ускоряют разложение. Таким образом, вода может иметь важное значение, так как во время изготовления, расфасовки, упаковки, хранения, транспортировки и использования препаратов трудно избежать воздействия влаги и/или влажности.
Безводные фармацевтические композиции и лекарственные формы по этому изобретению можно получать, используя безводные ингредиенты или ингредиенты с низким содержанием влаги, в условиях низкой влажности. Фармацевтические композиции и лекарственные формы, содержащие рацемический или оптически чистый метаболит сибутрамина в сочетании с лактозой, предпочтительно являются безводными, если предполагается, что во время изготовления, упаковки и/или хранения они будут подвергаться воздействию влаги и/или находиться во влажных условиях.
Безводную фармацевтическую композицию необходимо получить и хранить так, чтобы она оставалась безводной. Поэтому для упаковки безводных композиций предпочтительно используют материалы, которые, как известно, препятствуют проникновению воды, комплектуя в одной упаковке несколько лекарственных форм. Примерами приемлемых упаковок являются, но не ограничиваются ими, герметические упаковки из фольги, пластиковые или тому подобные, емкости для стандартных доз, блистерные и упаковки в виде полос.
В этой связи следует отметить, что это изобретение относится к способу получения твердого фармацевтического препарата, содержащего активный ингредиент, который заключается в том, что активный ингредиент и наполнитель (например, лактозу), практически не содержащие воды, смешивают в безводных условиях или в условиях низкой влажности. Этот способ далее включает упаковку безводного или негигроскопического твердого препарата в условиях низкой влажности. Благодаря созданию таких условий уменьшается риск соприкосновения с водой, что позволяет предотвратить или значительно уменьшить разложение активного ингредиента.
Связывающими веществами, используемыми в фармацевтических композициях и лекарственных формах, являются, но не ограничиваются ими, кукурузный крахмал, картофельный крахмал или другие крахмалы, желатин, природные и синтетические камеди, такие как аравийская камедь, альгинат натрия, альгиновая кислота, другие альгинаты, порошкообразный трагант, гуаровая камедь, целлюлоза и ее производные (например, этилцеллюлоза, ацетат целлюлозы, кальций карбоксиметилцеллюлоза, натрий карбоксиметилцеллюлоза), поливинилпирролидон, метилцеллюлоза, предварительно желатинированный крахмал, гидроксипропилметилцеллюлоза (например, №№ 2208, 2906, 2910), микрокристаллическая целлюлоза и их смеси.
Приемлемыми формами микрокристаллической целлюлозы являются, например, материалы, продаваемые под товарными знаками AVICEL-PH-101, AVICEL-PH-103, AVICEL-RC-581 и AVICEL-PH-105 (корпорации FMC Corporation, American Viscose Division, Avicel Sales, Marcus Hook, PA, USA). Типичным приемлемым связывающим вещество является смесь микрокристаллической целлюлозы и натриевой карбоксиметилцеллюлозы, продаваемой под товарным знаком AVICEL-RC-581. Приемлемыми безводными или содержащими небольшое количество влаги наполнителями или добавками являются AVICEL-PH-103™ и крахмал 1500 LM.
Примерами приемлемых наполнителей, используемых в фармацевтических композициях и лекарственных формах по этому изобретению, являются, но не ограничиваются ими, тальк, карбонат кальция (например, гранулы или порошок), микрокристаллическая целлюлоза, порошкообразная целлюлоза, декстраты, каолин, маннит, кремниевая кислота, сорбит, крахмал, предварительно желатинированный крахмал и их смеси. Связывающее вещество/наполнитель в фармацевтических композициях по настоящему изобретению обычно составляет от около 50 до около 99 вес.% от массы фармацевтической композиции.
В композициях по этому изобретению использованы дезинтеграторы для получения таблеток, распадающихся в водных условиях. При использовании слишком большого количества дезинтегратора таблетки могут распадаться уже во флаконе. Слишком маленькое количество дезинтегратора может быть недостаточным для дезинтеграции таблеток, в результате чего может измениться скорость и степень высвобождения активного ингредиента из лекарственной формы. Таким образом, для получения лекарственных форм, содержащих описанные здесь соединения, необходимо использовать достаточное количество дезинтегратора, которое не должно быть слишком маленьким или слишком большим. Количество используемого дезинтегратора изменяется в зависимости от типа препарата и способа введения и может быть легко определено специалистами в этой области. Фармацевтическая композиция обычно содержит от около 0,5 до около 15 вес.%, предпочтительно от около 1 до около 5 вес.% дезинтегратора.
Дезинтеграторы, которые можно использовать для получения фармацевтических композиций и лекарственных форм по этому изобретению, включают, но не ограничиваются ими, агар-агар, альгиновую кислоту, карбонат кальция, микрокристаллическую целлюлозу, натриевую кроскармеллозу, кросповидон, калиевый полакрилин, гликолят натриевого крахмала, картофельный крахмал или крахмал из кассавы, другие крахмалы, предварительно желатинированный крахмал, другие крахмалы, глины, другие альгины, другие целлюлозы, камеди или их смеси.
Смазывающие вещества, которые можно использовать для получения фармацевтических композиций и лекарственных форм по этому изобретению, включают, но не ограничиваются ими, стеарат кальция, стеарат магния, минеральное масло, легкое минеральное масло, глицерин, сорбитол, маннитол, полиэтиленгликоль, другие гликоли, стеариновую кислоту, лаурилсульфат натрия, тальк, гидрированное растительное масло (например, арахисовое масло, хлопковое масло, подсолнечное масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло), стеарат цинка, этилолеат, этиллауреат, агар или их смеси. Дополнительными смазывающими вещества являются, например, силоидный силикагель (AEROSIL 200 фирмы W.R. Grace Co. of Baltimore, MD), коагулированный аэрозоль синтетического кремнезема (фирмы Degussa Co. of Plano, Texas), CAB-O-SIL (пирогенный продукт диоксида кремния фирмы Cabot Co. of Boston, Mass) или их смеси. Смазывающее вещество необязательно добавляют в количестве менее примерно 1 вес.% от массы фармацевтической композиции.
Лекарственные формы по этому изобретению, в состав которых входит метаболит сибутрамина, предпочтительно содержат от около 0,1 до около 60 мг метаболита, его фармацевтически приемлемой соли, сольвата или клатрата. Например, таблетка, облатка или капсула содержит от около 0,1 мг до около 60 мг активного ингредиента. Таблетка, облатка или капсула наиболее предпочтительно содержит одну из трех доз, например, около 10 мг, около 20 мг или около 30 мг рацемических или оптически чистых метаболитов сибутрамина (в виде таблеток без лактозы, которые являются предпочтительной лекарственной формой).
Это изобретение далее описано со ссылкой на нижеследующие примеры. Специалистам в этой области должно быть ясно, что в объем этого изобретения входят многочисленные модификации, которые относятся как к веществам, так и к способам.
Примеры
В примерах 1-2 описано получение рацемического и оптически чистого сибутрамина.
В примерах 3-8 описано получение рацемических и оптически чистый форм десметилсибутрамина (DMS). Во всех этих примерах энантиомерную чистоту DMS определяют, используя аналитическую колонку Chirobiotic V (10 мкм, 4,6 мм х 25 мм) с 20 мМ ацетата аммония/IPA (65:35) в качестве подвижной фазы. Ультрафиолетовый детектор установлен на длину волны, равную 222 нм.
В примерах 9-12 описано получение рацемических и оптически чистых форм дидесметилсибутрамина (DDMS). Во всех этих примерах энантиомерную чистоту DDMS определяют, используя аналитическую колонку ULTRON ES-OVM (150 мм х 4,6 мм) с 0,01 М KH2PO4/MeOH (70:30) в качестве подвижной фазы. Ультрафиолетовый детектор установлен на длину волны, равную 200 нм.
В примерах 13-14 описаны способы определения сродства связывания соединений по этому изобретения и приведены значения сродства связывания, измеренные этими способами.
И, наконец, в примере 15 описаны препараты для перорального введения, содержащие соединения по этому изобретению.
Пример 1. Синтез сибутрамина
Синтез 1-(4-хлорфенил)циклобутанкарбонитрила
К суспензии NaH (17,6 г 60%, промытого гексаном) в диметилсульфоксиде (150 мл), перемешиваемой механической мешалкой, при комнатной температуре в течение одного часа добавляют смесь хлорбензилнитрила (30,3 г) и 1,3-дибромпропана (22,3 мл, 44,5 г). Реакционную смесь перемешивают в течение еще одного часа и медленно добавляют изопропиловый спирт (10 мл), чтобы погасить избыток NaH. Добавляют воду (150 мл). Реакционную смесь экстрагируют трет-бутилметиловым эфиром (МТВЕ) (2 х 200 мл), объединенные экстракты промывают водой (3 х 200 мл), насыщенным раствором соли и сушат над MgSO4. Растворитель удаляют в роторном испарителе и конечный продукт очищают перегонкой, что дает целевое соединение (22 г, 56%) в виде бледно-желтого масла, т.к. 110-120°С/1,0 мм Hg. Продукт исследуют при помощи 1Н ЯМР.
Синтез 1-[1-(4-хлорфенил)циклобутил]-3-метилбутиламина
Раствор бромида изобутилмагния (2 М раствор, 108 мл) в диэтиловом эфире (Aldrich) концентрируют, чтобы удалить большую часть эфира. Остаток растворяют в толуоле (150 мл) и добавляют полученный выше нитрил (22 г). Реакционную смесь нагревают до 105°С в течение 17 часов. Реакционную смесь охлаждают до комнатной температуры и добавляют суспензию NaBH4 в изопропиловом спирте (450 мл). Реакционную смесь нагревают с обратным холодильником в течение 6 часов, охлаждают до комнатной температуры и концентрируют. Остаток разбавляют водой (350 мл) и экстрагируют этилацетатом (3 х 200 мл). Объединенные экстракты промывают водой (100 мл), сушат (MgSO4) и концентрируют, что дает 24,2 г сырого продукта (83%).
Синтез свободного основания сибутрамина
1-[1-(4-Хлорфенил)циклобутил]-3-метилбутиламин (21,6 г) добавляют к муравьиной кислоте (27 мл) и водному формальдегиду (46 мл). Реакционную смесь нагревают до 85-95°С в течение 18 часов и охлаждают до комнатной температуры. Добавляют 30% NaOH, пока смесь не станет основной (рН > 11). Раствор экстрагируют хлороформом (3 х 200 мл), экстракты объединяют, промывают водой и насыщенным раствором соли и концентрируют, что дает 15 г продукта.
Хлористоводородная соль сибутрамина
Свободное основание сибутрамина (2,25 г) растворяют в МТВЕ (20 мл) и полученный раствор добавляют к 20 мл 1 М раствора HCl в диэтиловом эфире. Реакционную смесь перемешивают в течение 30 минут, твердое вещество собирают фильтрованием и сушат с получением 1,73 г продукта. Полученный продукт исследуют при помощи 1Н ЯМР.
Разделение сибутрамина
12,3 г рацемического сибутрамина растворяют в этилацетате (85 мл) и добавляют раствор 21,7 г L-дибензилвинной кислоты (“L-DBTA”) в этилацетате (85 мл). Реакционную смесь нагревают до температуры кипения с обратным холодильником и охлаждают до комнатной температуры. Белый осадок собирают (эффективность получения соли примерно 85%). Затем твердое вещество суспендируют в 220 мл этилацетата и нагревают при температуре кипения с обратным холодильником в течение 30 минут. Твердое вещество собирают с эффективностью получения >95%. Соль кристаллизуют в изопропиловом спирте (450 мл), что дает 11,3 г соли с эффективностью получения >99,3% L-DBTA (-)-сибутрамина (выход 76%). Свободное основание получают, обрабатывая соль насыщенным водным раствором NaHCO3 и экстрагируя хлороформом. Хлористоводородную соль (-)-сибутрамина получают, обрабатывая свободное основание при помощи HCl/Et2O, как описано выше. Оптическое вращение хлористоводородной соли составляет [α] = 3,15 (с = 0,9, Н2О), 1Н ЯМР 13С (CD3OD) и М+ = 279. Разделяемый маточный раствор сначала обрабатывают NaOH, что дает частично обогащенный (+)-сибутрамин, и затем обрабатывают D-DBTA, как описано выше, что дает соль D-DBTA (+)-сибутрамина с эффективностью получения >99,3%. Энантиомеры сибутрамина исследуют при помощи 1Н и 13С ЯМР: М+ = 179. Это вещество также исследуют ВЭЖХ и хиральной ВЭЖХ.
Пример 2. Получение сибутрамина из его метаболитов
Рацемический и оптически чистый сибутрамин можно также получить метилированием десметилсибутрамина или диметилированием дидесметилсибутрамина в приемлемых условиях реакции. Пример этого способа показан на схеме 1.
Схема 1
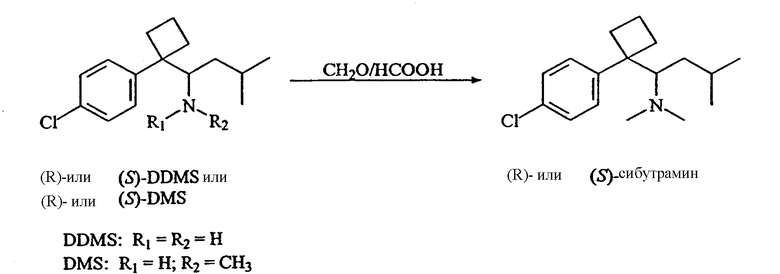
Пример 3. Получение десметилсибутрамина из сибутрамина
(-)-Сибутрамин (1,25 г) растворяют в толуоле (90 мл) и добавляют диэтилазодикарбоксилат (“DEAD”) (0,8 г, 1,1 экв.). Реакционную смесь нагревают при 50°С в течение 6 часов и добавляют 0,8 г DEAD. Реакционную смесь нагревают при 50°С еще 6 часов, охлаждают до комнатной температуры и удаляют толуол в вакууме. Остаток суспендируют в 45 мл этанола и 45 мл насыщенного водного раствора NH4Cl. Реакционную смесь нагревают с обратным холодильником в течение 3 часов. Реакционную смесь охлаждают до комнатной температуры и концентрируют, чтобы удалить этанол. Добавляют водный раствор NaHCO3, пока концентрат не станет основным. Основный концентрат экстрагируют дихлорметаном (3 х 50 мл). Экстракты объединяют, сушат сульфатом натрия, фильтруют и концентрируют с получением сырого продукта. Флеш-хроматография на колонках (SiO2) (этилацетат/ТЕА, 99:1) дает 0,43 г продукта. Полученный продукт исследуют при помощи 1Н и 13С ЯМР, М+ = 266 и оптическое вращение [α] = -10,6, с = 3,3 (CHCl3). Другой энантиомер и рацемат получают аналогичным образом, и данный изомер исследуют как (-)-изомер.
Синтез изомеров гидрохлорида десметилсибутрамина
К раствору (-)-десметилсибутрамина (0,78 г) в этилацетате (5 мл) при 0°С добавляют HCl/диэтиловый эфир (1 М раствор, 5 мл). Реакционную смесь перемешивают в течение 1 часа и твердое вещество собирают фильтрованием. Затем твердое вещество сушат с получением 0,68 г белого твердого вещества. Продукт исследуют при помощи 1Н и 13С ЯМР (ДМСО-d6) и химическую чистоту, равную >99%, определяют ВЭЖХ. [α] = -5° (с = 0,5, Н2О). Рацемат и другой энантиомер получают и исследуют аналогичным образом.
Пример 4. (R/S)-Десметилсибутрамин
Другой способ получения рацемического десметилсибутрамина ((R/S)-DMS) показан на схеме 2 и подробно описан ниже:
Схема 2
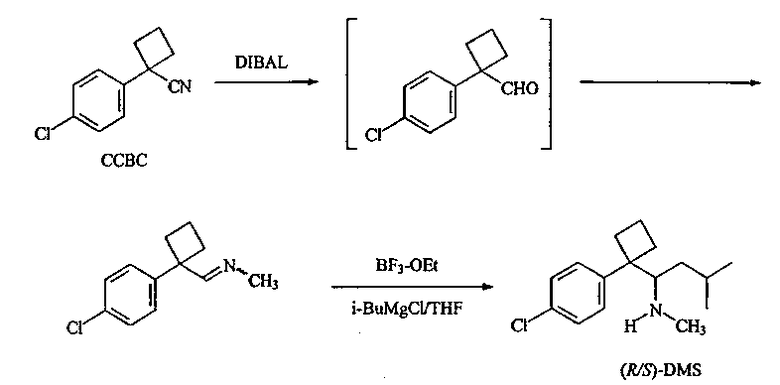
Получение 1-(4-хлорфенил)-1-циклобутилкарбоксальдегида
В соответствии со схемой 2 гидрид диизобутилалюминия (DIBAL-H) (87 мл, 1 М раствор в ТГФ, 87,0 ммоль) добавляют к раствору 1-(4-хлорфенил)циклобутанкарбонитрила (ССВС; 10 г, 52,1 ммоль), находящемуся при -20°С. Полученную смесь перемешивают в течение 4-5 часов при 0°С, выливают в 10% водный раствор лимонной кислоты и разбавляют 200 мл MTBE. Смесь перемешивают при комнатной температуре в течение 3-4 часов. Водный слой промывают МТВЕ (1 х 50 мл), объединенные органические слои сушат над MgSO4 и концентрируют, что дает 9 г (89%) вышеуказанного альдегида в виде масла. Спектр 1Н ЯМР (CDCl3) δ 9,52 (с, 1Н), 7,35-7,06 (м, 4Н), 2,77-2,68 (м, 2Н), 2,43-2,32 (м, 2Н), 2,06-1,89 (м, 2Н). Спектр 13С ЯМР δ 198,9, 139,4, 132,9, 128,9, 127,8, 57,1, 28,3, 15,8.
Получение 1-(4-хлорфенил)-1-циклобутил-N-метилкарбаимина
Смесь 1-(4-хлорфенил)-1-циклобутилкарбоксальдегида (3 г, 15,4 ммоль) и метиламина (12 мл, 40% водный раствор в весовом отношении, 154 ммоль) перемешивают при комнатной температуре в течение 18-40 часов. Реакционную смесь экстрагируют МТВЕ (2 х 50 мл). Объединенные органические слои сушат над К2СО3 и концентрируют, что дает 2,5 г (78%) вышеуказанного имина в виде масла. Спектр 1Н ЯМР (CDCl3) δ 7,65 (м, 1Н), 7,33-7,11 (м, 4Н), 3,34 (с, 3Н), 2,69-2,44 (м, 2Н), 2,44-2,34 (м, 2Н), 2,09-1,84 (м, 2Н). Спектр 13С ЯМР δ 168,0, 144,0, 131,8, 128,4, 127,4, 50,6, 47,6, 30,6, 15,8.
Получение 1-(4-хлорфенил)-N-метил-2-(2-метилпропил)-
циклобутанметамина
К раствору 1-(4-хлорфенил)-1-циклобутил-N-метилкарбаи-мина (0,5 г, 2,4 ммоль), охлажденному до 0°С, добавляют BF3 .OEt2 (0,34 г, 2,4 ммоль). Смесь перемешивают в течение 1 часа и охлаждают до -78°С. При этой температуре добавляют бромид изобутилмагния (2,5 мл, 2 М раствор в простом эфире, 5 ммоль), полученную смесь перемешивают при -78°С в течение 2 часов, нагревают до комнатной температуры и перемешивают в течение ночи. Реакционную смесь гасят насыщенным раствором NaHCO3 (10 мл) и разбавляют МТВЕ (15 мл). Органический слой сушат над MgSO4, концентрируют и очищают хроматографией на силикагеле (производя элюирование 1% NEt3 в этилацетате), что дает 380 мг вышеуказанного амина в виде масла. Спектр 1Н ЯМР (CDCl3) δ 7,35-7,19 (м, 4Н), 2,65-2,74 (м, 1Н), 2,57 (с, 3Н), 2,20-2,56 (м, 5Н), 1,60-2,00 (м, 3Н), 1,20-1,00 (м, 2Н), 0,95-0,90 (м, 6Н), 0,67-0,60 (м, 1Н). Спектр 13С ЯМР δ 144,7, 131,3, 129,1, 127,4, 65,5, 51,7, 41,4, 37,4, 33,7, 32,3, 25,4, 24,0, 22,0, 16,3.
Пример 5. Хлористоводородная соль (R/S)-десметилсибутрамина
Способ получения хлористоводородной соли рацемического десметилсибутрамина ((R/S)-DMS.HCl) показан на схеме 3.
Схема 3

В соответствии со схемой 3 толуол (150 мл) и раствор ССВС (50,0 г, 261 ммоль) в толуоле (45 мл) добавляют к раствору бромида изобутилмагния в ТГФ (392 мл, 1 М раствор в ТГФ, 392 ммоль). Полученную смесь перегоняют, пока температура внутри нее не достигнет 105-110°С, и нагревают с обратным холодильником при этой температуре в течение 2-4 часов. Затем реакционную смесь охлаждают до 0°С и гасят метанолом (295 мл). NaBH4 (11 г, 339 ммоль) добавляют порциями к реакционной смеси при 0°С в течение 15 минут. Реакционную смесь перемешивают в течение 15 минут и переносят в 2 н водный раствор HCl (365 мл). Органическую фазу перегоняют, пока температура внутри нее не достигнет 105°С, и оставляют охлаждаться до комнатной температуры. Затем к реакционной смеси добавляют муравьиную кислоту (24 г, 522 ммоль) и нагревают до температуры кипения с обратным холодильником (92-96°С) в течение 6-8 часов, после чего реакционную смесь перегоняют, пока температура внутри нее не достигнет 108°С. Смесь охлаждают до 10°С и добавляют BH3 .ТГФ (653 мл, 1,0 М раствор, 653 ммоль). Полученную смесь нагревают до температуры кипения с обратным холодильником (69°С) в течение 15 часов. Смесь охлаждают до 5°С, смешивают с метанолом (105 мл) и снова нагревают с обратным холодильником в течение 45 минут. Реакционную смесь перегоняют, пока температура внутри нее не достигнет 116°С, и оставляют охлаждаться до 25°С. Затем к смеси добавляют хлористоводородную кислоту в МТВЕ (373 г, 18 вес.% HCl, 1840 ммоль) с получением белой суспензии, которую нагревают с обратным холодильником в течение 1 часа и фильтруют, что дает 62,3 г (79,0%) (R/S)-DMS.HCl. Спектр 1Н ЯМР (CDCl3) δ 0,85-1,1 (м, 6Н), 1,24-1,5 (ш, 2Н), 1,65-2,14 (ш, 4Н), 2,2-2,5 (ш, 4Н), 2,5-2,7 (м, 2Н), 3,4-3,6 (ш, 1Н), 7,3-7,5 (м, 4Н), 9,0-9,5 (ш, 2Н). Спектр 13С ЯМР δ 15,5, 21,4, 23,5, 24,7, 31,4, 32,4, 33,2, 35,9, 49,1, 64,2, 128,5, 129,4, 133,0, 141,6.
Пример 6. Хлористоводородная соль (R)-десметилсибутрамина
Способ получения хлористоводородной соли (R)-десметилсибутрамина ((R)-DMS.HCl) показан на схеме 4 и подробно описан ниже.
Схема 4
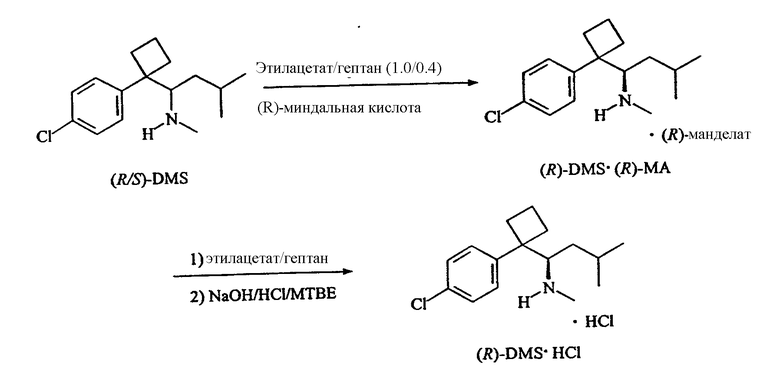
Получение (R)-манделата (R)-DMS
Хлористоводородную соль (R/S)-десметилсибутрамина ((R/S)-DMS.HCl) (60 г) добавляют к этилацетату (300 мл) и полученную смесь охлаждают до 0°С. Затем к реакционной смеси добавляют водный раствор NaOH (1,5 н раствор, 300 мл) и перемешивают в течение 30 минут. Органическую фазу отделяют, промывают водой (150 мл) и концентрируют. (R)-Миндальную кислоту (30,3 г), этилацетат (всего 510 мл) и гептан (204 мл) добавляют к концентрированной органической фазе. Полученную смесь нагревают до температуры кипения с обратным холодильником в течение 1 часа и охлаждают до 20-23°С. Полученную суспензию фильтруют, что дает 36,4 г (43,8%) (R)-манделата (R)-десметилсибутрамина ((R)-DMS.(R)-MA; эффективность 95,5%).
Обогащение (R)-DMS . (R)-MA
Смесь (R)-DMS.(R)-MA (30 г, 0,072 моль), этилацетата (230 мл) и гептана (230 мл) нагревают до температуры кипения с обратным холодильником в течение 1 часа. Продукт охлаждают до 20-23°С, фильтруют и сушат, что дает 29,6 г (98%) (R)-DMS.(R)-MA (эффективность 99,9%).
Получение хлористоводородной соли (R)-DMS
Смесь (R)-DMS.(R)-MA (50 г, 0,12 моль), NaOH (100 мл, 3,0 н раствор) и толуола (500 мл) перемешивают в течение 30 минут. Органическую фазу промывают водой (200 мл), концентрируют примерно до 300 мл и охлаждают до комнатной температуры. К смеси медленно добавляют HCl/MTBE (100 мл, 14%, 0,34 моль) с получением (R)-DMS.HCl. Суспензию перемешивают в течение 30 минут и фильтруют, полученную мокрую фильтровальную лепешку дважды промывают МТВЕ и сушат, что дает 34,5 г (95,5%) (R)-DMS.HCl (эффективность 99,9%; химическая чистота 99,9% по результатам ЯМР). Спектр 1Н ЯМР (CDCl3) δ 0,85-1,1 (м, 6Н), 1,24-1,5 (ш, 2Н), 1,65-2,14 (ш, 4Н), 2,2-2,5 (ш, 4Н), 2,5-2,7 (м, 2Н), 3,4-3,6 (ш, 1Н), 7,3-7,5 (м, 4Н), 9,0-9,5 (ш, 2Н). Спектр 13С ЯМР δ 15,5, 21,4, 23,5, 24,7, 31,4, 32,4, 33,2, 35,9, 49,1, 64,2, 128,5, 129,4, 133,0, 141,6.
Пример 7. Хлористоводородная соль (S)-десметилсибутрамина
Способ получения хлористоводородной соли (S)-десметилсибутрамина ((S)-DMS.HCl) показан на схеме 5 и подробно описан ниже.
Схема 5
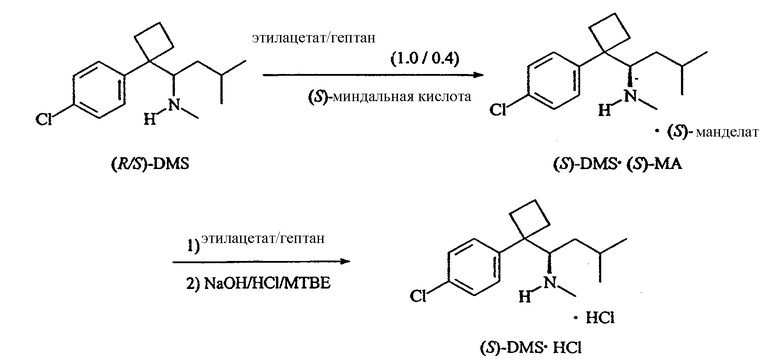
Получение (S)-Манделата (S)-DMS
В соответствии со схемой 5 смесь (R/S)-DMS.HCl (5,0 г, NaOH (1,5 н раствор, 20 мл) и этилацетат (50 мл) перемешивают в течение 30 минут. Органическую фазу промывают водой (20 мл) и концентрируют с получением свободного основания десметилсибутрамина (4,2 г, 96%).
Свободное основание десметилсибутрамина (1,1 г, 4,1 ммоль) смешивают с (S)-миндальной кислотой (0,62 г, 4,1 ммоль), этилацетатом (11 мл) и гептаном (4,4 мл). Полученную смесь нагревают до температуры кипения с обратным холодильником в течение 30 минут и охлаждают до 20-23°С. Полученную суспензию фильтруют, что дает 0,76 г (S)-манделата (S)-десметилсибутрамина ((S)-DMS.(S)-MA) (эффективность 96%).
Обогащение (S)-DMS . (S)-MA
Смесь (S)-манделата (S)-десметилсибутрамина (0,76 г), этилацетата (5 мл) и гептана (5 мл) нагревают до температуры кипения с обратным холодильником в течение 1 часа. Продукт охлаждают до 20-23°С, фильтруют и сушат, что дает 0,72 г (95%) (S)-DMS.(S)-MA (эффективность 99,9%).
Выделение (S)-манделата (S)-DMS из маточного раствора
(S)-DMS . (R)-MA
К раствору (S)-DMS.(R)-MA в этилацетате/гептане (маточный раствор с эффективностью получения 67%) добавляют NaOH (3 н раствор, 400 мл) и реакционную смесь перемешивают в течение 30 минут. Органическую фазу промывают водой и концентрируют. К полученному остатку (130 г, 0,49 моль и эффективность получения 67%) добавляют (S)-миндальную кислоту (28,5 г, 0,49 моль), этилацетат (1400 мл) и гептан (580 мл). Смесь нагревают до температуры кипения с обратным холодильником в течение 1 часа и медленно охлаждают до комнатной температуры. Полученную суспензию фильтруют и сушат, что дает 147 г (86% в расчете на (S)-изомер) (S)-DMS. (S)-MA (эффективность 99,9%).
Получение хлористоводородной соли (S)-DMS
(S)-Манделат (S)-десметилсибутрамина (20 г, 0,048 моль) добавляют к смеси NaOH (60 мл, 3,0 н раствор) и толуола (200 мл). Смесь перемешивают в течение 30 минут, органическую фазу промывают водой (100 мл), концентрируют примерно до 100 мл и охлаждают до комнатной температуры. К смеси медленно добавляют хлористоводородную кислоту в МТВЕ (40 мл, 14%, 0,13 моль) с получением (S)-DMS.HCl. Суспензию перемешивают в течение 30 минут и фильтруют, полученную мокрую фильтровальную лепешку дважды промывают МТВЕ и сушат, что дает 14 г (96,7%) (S)-DMS. (L)-MA (эффективность 99,9%; химическая чистота 99,9%).Спектр 1Н ЯМР (CDCl3) δ 0,84-1,1 (м, 6Н), 1,25-1,5 (ш, 2Н), 1,65-2,15 (ш, 4Н), 2,2-2,5 (ш, 4Н), 2,5-2,7 (м, 2Н), 3,4-3,6 (ш, 1Н), 7,3-7,5 (м, 4Н), 9,0-9,5 (ш, 2Н). Спектр 13С ЯМР δ 15,5, 21,4, 23,5, 24,7, 31,4, 32,4, 33,2, 35,9, 49,1, 64,2, 128,5, 129,4, 133,0, 141,6.
Пример 8. Получение десметилсибутрамина из дидесметил-сибутрамина
Рацемический и оптически чистый дидесметилсибутрамин можно также получить метилированием дидесметилсибутрамина в приемлемых условиях реакции. Пример этого способа показан на схеме 6.
Схема 6
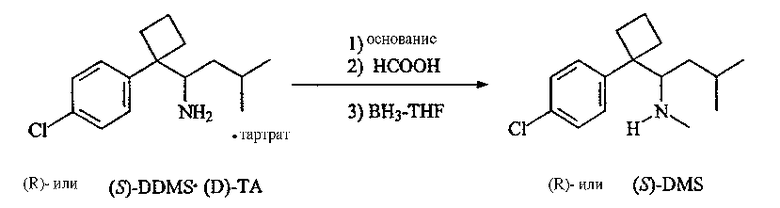
Пример 9. (R/S)-Дидесметилсибутрамин
Предпочтительный способ получения свободного основания рацемического дидесметилсибутрамина ((R/S)-DDMS) показан на схеме 7 и подробно описан ниже.
Схема 7
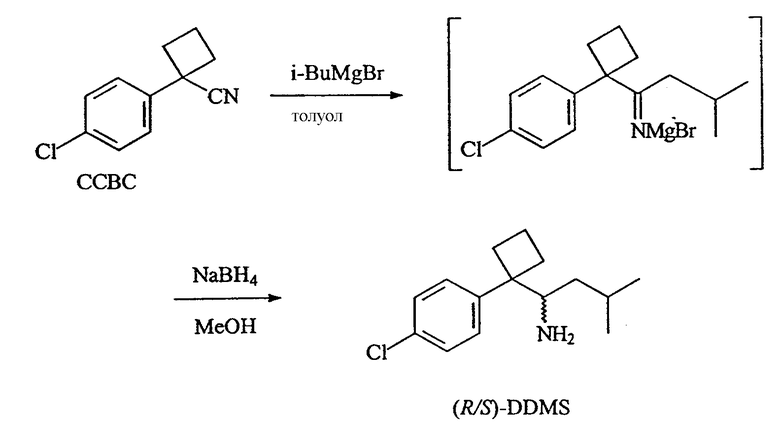
В соответствии со схемой 7 в трехгорлую круглодонную колбу емкостью 1 л вводят бромид изобутилмагния (200 мл, 2,0 М раствор в диэтиловом эфире) и толуол (159 мл) и полученную смесь перегоняют для удаления большей части эфира. Смесь охлаждают до 20°С, добавляют ССВС (50,0 г) в толуоле (45 мл) и полученную смесь нагревают с обратным холодильником в течение 2-4 часов. Реакционную смесь охлаждают до 0°С, добавляют метанол (300 мл), после чего медленно добавляют NaBH4 (11 г). Полученную смесь перемешивают при 0-10°С в течение 15 минут. Реакционную смесь медленно добавляют к водному раствору HCl (365 мл, 2 н раствор), находящемуся при 0°С, и полученную смесь нагревают до комнатной температуры при непрерывном перемешивании. Органическую фазу отделяют и водную фазу промывают толуолом (200 мл). Объединенные органические фазы промывают водой (200 мл) и концентрируют, что дает (R/S)-DDMS (55 г, 85%). Спектр 1Н ЯМР (CDCl3) δ 0,6-0,8 (м, 1Н), 0,8-1,0 (м, 6Н), 1,1-1,3 (м, 1Н), 1,6-2,6 (м, 7Н), 3,0-3,3 (м, 1Н), 7,0-7,6 (м, 4Н). Спектр 13С ЯМР δ 15,4, 21,5, 24,3, 24,7, 31,5, 31,9, 41,1, 50,73, 56,3, 127,7, 129, 131,6, 144,2,
Пример 10. (D)-Тартрат (R/S)-дидесметилсибутрамина
Предпочтительный способ получения (D)-тартрата рацемического дидесметилсибутрамина ((R/S)-DDMS.(D)-TA) показан на схеме 8. Необходимо отметить, что (L)-тартрат рацемического дидесметилсибутрамина ((R/S)-DDMS.(L)-TA) можно получить аналогичным образом.
Схема 8
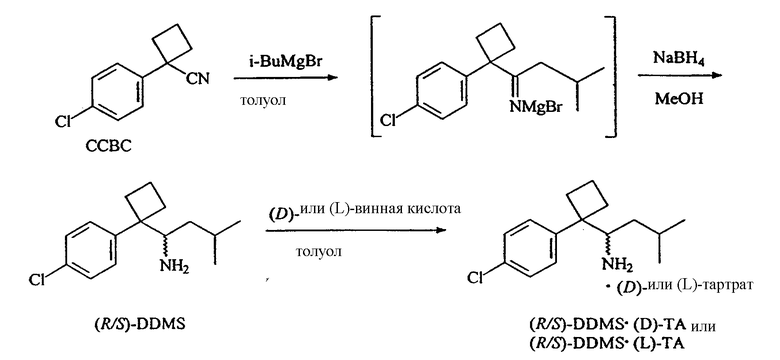
В соответствии со схемой 8 смесь рацемического дидесметилсибутрамина (15,3 г) и толуола (160 мл) нагревают до 70-80°С и медленно добавляют (D)-винную кислоту (9,1 г) в воде (20 мл) и ацетон (10 мл). Полученную смесь нагревают с обратным холодильником в течение 30 минут, после чего отгоняют воду и ацетон. Реакционную смесь охлаждают до комнатной температуры и полученную суспензию фильтруют. Мокрую фильтровальную лепешку дважды промывают МТВЕ (20 мл х 2) и сушат, что дает (R/S)-DDMS.(D)-TA (22,5 г,98%). Спектр 1Н ЯМР (ДМСО) δ 0,6-0,92 (м, 6Н), 0,92-1,1 (м, 1Н), 1,1-1,3 (м, 1Н), 1,5-2,8 (м, 2Н), 1,8-2,1 (м, 1Н), 2,1-2,4 (м, 3Н), 2,4-2,6 (м, 1Н), 3,4-3,6 (м, 1Н), 3,9-4,2 (с, 2Н), 6,4-7,2 (ш, 6Н, ОН, СООН и NH2), 7,3-7,6 (м, 4Н). Спектр 13С ЯМР δ 15,5, 2,1, 23,3, 23,7, 31,5, 31,8, 37,7, 39,7, 54,5, 72,1, 128, 129,7, 131,3, 142,2, 174,6.
Пример 11. (D)-Тартрат (R)-дидесметилсибутрамина
Выделение из свободного основания дидесметилсибутрамина
Способ выделения (D)-тартрата (R)-дидесметилсибутрамина ((R)-DDMS. (D)-TA из свободного основания рацемического дидесметилсибутрамина показан на схеме 9А и подробно описан ниже.
Схема 9А
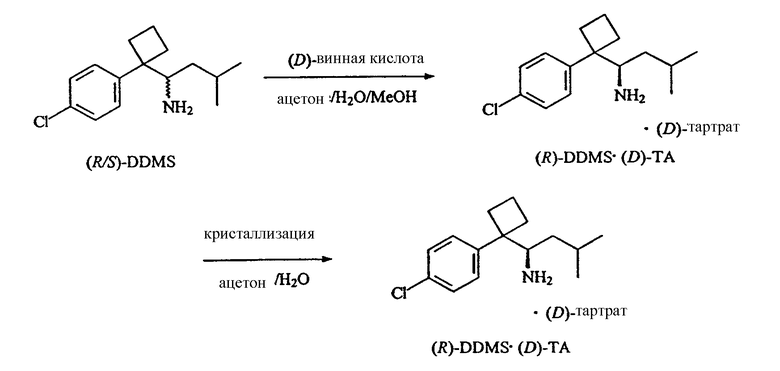
В соответствии со схемой 9А смесь (R/S)-дидесметилсибутрамина (20,3 г), ацетона/воды/метанола (350 мл, 1:0,13:0,7, в объемном отношении) и (D)-винной кислоты (12,1 г) вводят в трехгорлую круглодонную колбу емкостью 500 мл. Реакционную смесь нагревают до температуры кипения с обратным холодильником в течение 30 минут и охлаждают до 45°С. Затем к реакционной смеси добавляют (R)-DDMS.(D)-TA (10 мг, эффективность 99,6%) и перемешивают при 40-45°С в течение 30 минут. Смесь охлаждают до комнатной температуры и перемешивают в течение 1 часа. Полученную суспензию фильтруют, мокрую фильтровальную лепешку промывают холодной смесью ацетона/воды и сушат, что дает 10,3 г (33%) (R)-DDMS. (D)-TA (эффективность 90%).
Выделение из (D)-тартрата (R/S)-дидесметилсибутрамина
Способ выделения (D)-тартрата (R)-дидесметилсибутрамина ((R)-DDMS.(D)-TA) из (D)-тартрата рацемического дидесметилсибутрамина показан на схеме 9В и подробно описан ниже.
Схема 9В
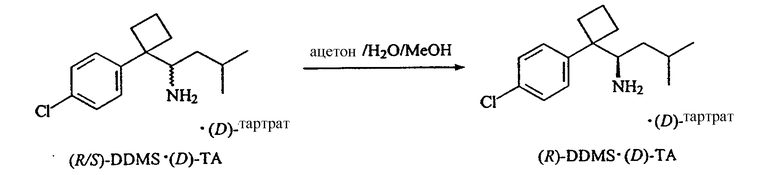
В соответствии со схемой 9В смесь (D)-тартрата (R/S)-дидесметилсибутрамина (5,0 г) в ацетоне (50 мл), воде (6,7 мл) и метаноле (3,3 мл) нагревают с обратным холодильником в течение 30 минут. Затем смесь охлаждают до комнатной температуры, полученную суспензию фильтруют и мокрую фильтровальную лепешку промывают холодным ацетоном и сушат, что дает (R)-DDMS.(D)-TA (1,4 г, 28%; эффективность 92%).
Обогащение (D)-тартрата (R)-DDMS
Смесь (R)-DDMS.(D)-TA (25 г, эффективность 92%) и ацетонитрила/воды/этанола (300 мл:65 мл:30 мл) нагревают с обратным холодильником в течение 1 часа. Затем смесь охлаждают до комнатной температуры, полученную суспензию фильтруют и сушат, что дает (R)-DDMS.(D)-TA (18 г, 71,3%, эффективность 99,7% и химическая чистота 99,91%). Спектр 1Н ЯМР (ДМСО-d6) δ 0,7-0,9 (м, 6Н), 0,9-1,05 (т, 1Н), 1,1-1,24 (ш, 1Н), 1,5-1,8 (ш, 2Н), 1,8-2,02 (ш, 1Н), 2,1-2,4 (3, 3Н), 2,4-2,6 (ш, 1Н), 3,5 (м, 1Н), 4,0 (с, 2Н), 7,1-7,6 (м, 4Н, с 6Н из NH2, OH и СООН). Спектр 13С ЯМР δ 15,4, 21,5, 22,0, 22,2, 32,0, 32,2, 38,4, 49,0, 54,0, 72,8, 128,8, 130,0, 132,0, 143,0, 175,5.
Пример 12. (L)-Тартрат (S)-дидесметилсибутрамина
Способ выделения (L)-тартрата (S)-дидесметилсибутрамина (S)-DDMS. (L)-TA из свободного основания рацемического дидесметилсибутрамина показан на схеме 10 и подробно описан ниже.
Схема 10
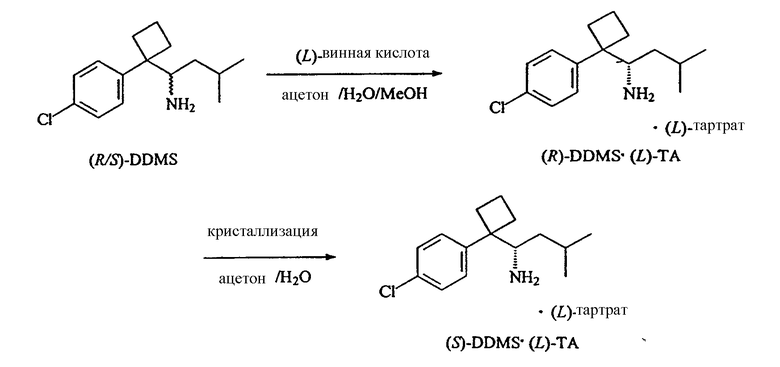
Получение (L)-тартрата (S)-DDMS
(R/S)-Дидесметилсибутрамин (20,5 г), ацетон/воду/метанол (350 мл, 1:0,13:0,7, в объемном отношении) и (L)-винную кислоту (12,2 г) вводят в трехгорлую круглодонную колбу емкостью 500 мл. Смесь нагревают до температуры кипения с обратным холодильником в течение 30 минут и охлаждают до 45°С. Затем к реакционной смеси добавляют (S)-DDMS.(L)-TA (10 мг и эффективность 99,7%) и перемешивают при 40-45°С в течение 30 минут. Смесь охлаждают до комнатной температуры и перемешивают в течение 1 часа. Полученную суспензию фильтруют, мокрую фильтровальную лепешку промывают холодной смесью ацетона/воды и сушат, что дает 10,8 г (33,4%) (S)-DDMS.(L)-TA (эффективность 89,7%).
Получение (L)-тартрата (S)-DDMS из маточного раствора
(R)-DDMS . (D)-TA
Раствор тартрата DDMS в ацетоне/воде/метаноле (маточный раствор (R)-DDMS.(D)-TA) концентрируют для удаления ацетона и метанола. Остаток обрабатывают водным раствором NaOH (3 н раствор, 150 мл) и экстрагируют этилацетатом. Органическую фазу промывают водой (100 мл) и концентрируют, что дает свободное основание дидесметилсибутрамина (45 г, 0,18 моль и эффективность получения (S)-изомера 36%). К свободному амину добавляют (L)-винную кислоту (53,6 г, 0,35 моль), ацетон (600 мл), воду (80 мл) и метанол (40 мл). Смесь нагревают до температуры кипения с обратным холодильником в течение 1 часа и охлаждают до комнатной температуры. Полученную суспензию фильтруют и мокрую фильтровальную лепешку дважды промывают холодной смесью ацетона/воды, что дает 26,7 г (56% в расчете на (S)-дидесметилсибутрамин) (S)-DDMS.(L)-TA (эффективность 96%).
Обогащение (S)-DDMS . (L)-TA
Смесь (S)-DDMS.(L)-TA (26,7 г) в ацетонитриле/воде (475 мл, 1:0,2, в объемном отношении) нагревают с обратным холодильником в течение 1 часа и охлаждают до комнатной температуры. Полученную суспензию фильтруют и сушат, что дает 17,4 г (65%) (S)-DDMS.(L)-TA (эффективность 99,9%; химическая чистота 99,94%). Спектр 1Н ЯМР (ДМСО-d6) δ 0,7-0,9 (м, 6Н), 0,9-1,05 (м, 1Н), 1,1-1,3 (ш, 1Н), 1,52-1,8 (ш, 2Н), 1,84-2,05 (ш, 1Н), 2,15-2,4 (ш, 3Н), 2,4-2,6 (ш, 1Н), 3,65-3,58 (м, 1Н), 4,0 (с, 2Н), 6,7-7,3 (ш, 6Н из NH2, ОН и СООН), 7,1-7,6 (м, 4Н). Спектр 13С ЯМР δ 15,4, 21,5, 22,0, 22,2, 32,0, 32,2, 38,4, 49,0, 54,0, 72,8, 128,8, 130,0, 132,0, 143,0, 175,5.
Пример 13. Определение активности и специфичности
Фармакологическое исследование выполняют с целью определения относительной активности, сравнительной эффективности, сродства связывания и токсичности рацемической смеси сибутрамина, его энантиомеров, метаболитов сибутрамина и их энантиомеров. Профиль относительной специфичности ингибирования обратного захвата моноамина определяют на основании ингибирования испытуемыми соединениями обратного захвата норэпинефрина (NE) в ткани головного мозга по сравнению с ингибированием обратного захвата допамина (DA) и серотонина (5-НТ).
Высокоаффинное поглощение 3Н-радиоактивных моноаминов исследуют с использованием синаптосомных препаратов, полученных из полосатого тела крыс (для ингибирования обратного захвата DA) и коры головного мозга (для 5-НТ и NE), при помощи методов, описанных Kula et al., Life Science 34(26):2567-2575, 1984, and Baldessarini et al., Life Science 39: 1765-1777, 1986. Свежие ткани иссекают на льду и взвешивают. Полученные ткани гомогенизируют вручную (14 ударов в 10-35 объемах охлаждаемого льдом 0,32 М изотонического раствора сахарозы, содержащего ниаламид, 34 мкМ) в стеклянном гомогенизаторе с тефлоновым покрытием, после чего ткань центрифугируют в течение десяти минут со скоростью 900 х градиент; полученный “раствор” супернатанта содержит синаптосомы, которые используют без дальнейшей обработки. В каждую пробирку вводят 50 мкл гомогената головного мозга, меченого радиоактивными изотопами 3Н-моноамина, и испытуемое соединение (например, чистые энантиомеры сибутрамина, рацемат и соответствующие эталоны) в только что полученном физиологическом растворе с буфером с конечным объемом 0,5 мл. До анализа ткани предварительно инкубируют в течение 15 минут при 37°С. Пробирки помещают на лед до начала инкубации, которую начинают, добавляя 3Н-амин до достижения конечной концентрации 0,1 мкМ. Пробирки инкубируют при 37°С в течение 10 минут с 3Н-DA (26 Ci/ммоль) и в течение 20 минут с 3Н-5НТ (около 20 Ci/ммоль) и 3Н-NE (около 20 Ci/ммоль). Удельная активность радиоактивного моноамина изменяется в зависимости от используемого вещества в несущественных пределах. Реакцию прекращают, погружая пробирки в лед и разбавляя их содержимое 3 мл охлаждаемого льдом изотонического физиологического раствора, содержащего 20 мМ TRIS буфера (рН 7,0). Эти растворы фильтруют через микрофильтры из сложного эфира целлюлозы и промывают двумя 3 мл объемами аналогичного буфера. Затем подсчитывают 3Н-радиоактивность фильтра в 3,5 мл Polyfluor примерно при 50% эффективности в отношении трития. Результаты, полученные для контрольных проб (инкубируемых или при 0°С, или с известными специфическими ингибиторами поглощения DA [GRB-12909, 10 мкМ], 5НТ [зимелидин, 10 мкМ] или NE [дезипрамин, 10 мкМ], обычно не отличаются от результатов анализов, выполняемых без использования ткани, и в среднем составляют 2-3% от общего числа импульсов в минуту (СРМ).
Сравнение величин 3Н-радиоактивности на фильтрах позволяет определить относительную способность чистых энантиомеров и рацемической смеси сибутрамина (и известных ингибиторов обратного захвата DA, 5-HT и NE) блокировать обратный захват этих моноаминов указанными тканями. Эти данные являются полезными для определения относительной активности и эффективности соединений по этому изобретению (например, ингибиторов обратного захвата допамина, таких как рацемический или оптически чистый метаболит сибутрамина, и антагонистов 5-НТ3).
Острую токсичность соединений по этому изобретению определяют, выполняя исследования, во время которых крысам вводят возрастающие дозы (мг/кг) чистых изомеров или рацемата. Летальная доза, которая при пероральном введении вызывает гибель 50% подопытных животных, определяется как LD50. Сравнение значений LD50 для энантиомеров и рацемата позволяет определить относительную токсичность композиций.
Пример 14. Сродство связывания
Сродство связывания рацемического и оптически чистого сибутрамина ((±)-, (+)- и
(-)-сибутрамина), десметилсибутрамина ((±)-, (+)- и (-)-десМе) и дидесметилсибутрамина ((±)-, (+)- и (-)-дидесМе) определяют с использованием неизбирательного рецептора мускарина и участка обратного захвата серотонина (5-НТ) из коры головного мозга крыс, участка обратного захвата рекомбинантного норэпинефрина (NE) человека и β3-рецептора из жировой ткани крыс. Сначала соединения подвергают двойному испытанию в количестве 10 мкм, и при обнаружении ≥50% ингибирования специфического связывания эти соединения далее подвергают двойному испытанию в 10 разных концентрациях, чтобы получить полные кривые успешности конкурирования. Значения IC50 (концентрации, необходимой для ингибирования 50% специфического связывания) определяют при помощи нелинейного регрессионного анализа кривых, и полученные данные приведены в нижеследующей таблице.
Ни одно из соединений не характеризуется более чем 15% ингибированием связывания с β3-рецептором, и сродство с участком поглощения мускарина является слабым по сравнению с атропином. Кроме того, связывание с участками поглощения NE и 5-НТ является на несколько порядков величины меньше, чем аналогичные показатели у эталонов.
Приведенные выше данные, полученные в соответствии с описанием, приведенным в примере 13, показывают, что (+)-десметилсибутрамин и (+)-дидесметилсибутрамин являются сильнодействующими ингибиторами поглощения NE и 5-НТ, но обладают ничточжно низкой активностью на участках рецепторов мускарина.
Пример 15. Препарат для перорального введения
Лекарственные формы без лактозы, содержащие метаболиты сибутрамина, в твердых желатиновых капсулах можно получить, используя нижеследующие ингредиенты.
капсула
капсула
капсула
Рацемический или оптически чистый метаболит сибутрамина просеивают и смешивают с указанными выше наполнителями. Твердые желатиновые капсулы требуемого размера, состоящие из двух частей, наполняют полученной смесью, используя для этой цели соответствующие механизмы и методы, известные в этой области. См., например, Remington's Pharmaceutical Sciences, 16th or 18th Editions, которые полностью включены в это описание изобретения в качестве ссылки. Можно изготовить лекарственные формы с другими дозами, для чего нужно изменить массу наполнителя и при необходимости изменить должным образом размеры капсулы. Можно получить любые вышеуказанные стабильные препараты без лактозы в твердых желатиновых капсулах.
Лекарственные формы в виде прессованных таблеток, содержащих метаболиты сибутрамина, можно получить, используя нижеследующие ингредиенты.
Рацемический или оптически чистый метаболит сибутрамина просеивают через соответствующее сито и смесишают с не содержащими лактозы наполнителями до образования однородной смеси. Сухую смесь просеивают и смешивают со стеаратом магния. Полученную порошкообразую смесь прессуют в таблетки требуемой формы и размера. Таблетки с другими степенями прочности можно получить, изменяя соотношение активного ингредиента с наполнителем (наполнителями) или изменяя массу компонентов.
Вышеописанные варианты осуществления этого изобретения приведены только в качестве примеров, и специалистам в этой области должно быть понятно, или они могут убедиться путем простого экспериментирования, что существуют многочисленные эквивалентны описанных способов. Все такие эквиваленты входят в объем этого изобретения и сформулированы в нижеследующей формуле изобретения.
Предложено применение (-)-дидесметилсибутрамина или его фармацевтически приемлемой соли, сольвата или клатрата для изготовления лекарственного средства для лечения болезни Паркинсона. Показано улучшение двигательной активности и облегчение симптомов паркинсонизма. 4 з.п. ф-лы, 3 табл.
1. Применение (-)-дидесметилсибутрамина или его фармацевтически приемлемой соли, сольвата или клатрата для изготовления лекарственного средства для лечения болезни Паркинсона.
2. Применение по п.1, где метаболит сибутрамина вводят перорально, через слизистую оболочку или чрескожно.
3. Применение по п.1, где лекарственное средство адаптировано для введения (-)-дидесметилсибутрамина в количестве от около 0,1 мг до около 60 мг в день.
4. Применение по п.3, где лекарственное средство адаптировано для введения (-)-дидесметилсибутрамина в количестве от около 2 мг до около 30 мг в день.
5. Применение по п.1, где лекарственное средство адаптировано для введения (-)-дидесметилсибутрамина в количестве от около 5 мг до около 15 мг в день.
| Экономайзер | 0 |
|
SU94A1 |
| D.J | |||
| Heal et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Br | |||
| J | |||
| Pharmacol | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Способ получения замещенных 1-(1-фенилциклобутил)-алкиламинов или их фармакологически приемлемых солей | 1982 |
|
SU1482522A3 |
| Способ получения (1-арилциклобутил)-алкиламинов или их фармакологически приемлемых солей | 1985 |
|
SU1461372A3 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Руководство по медицине "THE MERCK MANUAL" | |||
| - M.: Мир, 1997, т.1, | |||
Авторы
Даты
2009-06-20—Публикация
2004-05-27—Подача