Настоящее изобретение относится к биотехнологии. Конкретнее, настоящее изобретение относится к способу получения рекомбинантной стрептокиназы.
В настоящее время сильнодействующие тромболитические агенты включают рекомбинантный активатор тканевого плазминогена человека (rt-PA), стрептокиназу (SK) и комплекс анизоилированного плазминогена и стрептокиназы (APSAC), и др. В сентябре 1993 профессор Ridker с сотр. из Brigharm and women's hospital, США, обобщили лечебное действие тромболитической терапии 100 000 больных острым инфарктом миокарда (AM1). В результате выяснилось, что нет существенных различий в эффективности и побочных эффектах между этими тремя тромболитическими средствами. rt-PA является весьма дорогим, а цена SK в три раза ниже, чем rt-PA. Кроме того, степень рестеноза при использовании SK ниже, и SK традиционна для использования.
Зарубежные фирмы используют в качестве материала для продуцирования природной стрептокиназы патогенный гемолитический streptococcus aureus. При этом необходимо заботиться об охране окружающей среды и безопасности персонала, об удалении токсинов, которые могут вызвать гипотензию и лихорадку, поэтому процедуры и оборудование для получения природной SK были сложными, а стоимость высокой, из-за низкого уровня экспрессии SK в гемолитическом streptococcus aureus и трудностей очистки. В начале 80-х Ferritti JJ. et al выделили гены SK из фагов гемолитического streptococcus aureus и осуществили экспрессию гена. Уровень экспрессии r-SK был очень низким - только несколько сотен единиц на 1 мл среды. Продукт генной инженерии не создали. В патенте США DD 24898 и в патенте Японии JP 5317044 ген SK выделяли таким же способом, как способ Ferritti, но векторы экспрессии и условия культивирования отличались и уровни экспрессии составляли 60-274 мкг из 1 мл среды, 6420-29300 единиц/мл среды, соответственно. Не приводится данных о выходе очищенных продуктов, а также об образовании генно-инженерной SK. В 1992 HerrenaL Куба, получена рекомбинантная стрептокиназа сложными путями генетического конструирования и способами очистки. Кроме того, используются материалы, такие как аффинные абсорбенты плазминогена, которые являются очень дорогими, а чистота и выход продукта были низкими, следовательно, стоимость такой r-SK является очень высокой.
Цель настоящего изобретения состоит в представлении нового способа получения рекомбинантной стрептокиназы (r-SK) методами современной биотехнологии. Способ получения является безопасным, выход и чистота продукта высокие, а стоимость низкая.
Способ получения рекомбинантной стрептокиназы отличается тем, что
(1) в соответствии с нуклеотидными последовательностями конструируют праймеры и используют для амплификации гена SK с помощью полимеразной цепной реакции (OCR), в то время как в качестве матрицы используют макромолекулярную ДНК Streptococcus aureus;
(2) конструируют прокариотический вектор экспрессии гена SK;
(3) трансформируют бактерии-хозяева вектором экспрессии и отбирают;
(4) трансформированные бактерии-хозяева культивируют при подходящих условиях и индуцируют экспрессию продукта r-SK;
(5) выделяют и очищают.
Термин "праймер" в настоящем изобретении означает олигонуклеотидный фрагмент одноцепочечной ДНК, который полностью или частично комплементарен амплифицируемой ДНК-последовательности, и используется в качестве источника продуктов удлинения. Длина и последовательность праймера должны быть способны к индуцированию удлиненных PCR продуктов.
Лучше, когда праймер включает 5-50 нуклеотидов. Конкретные длина и последовательность определяются сложностью ДНК- или РНК-мишени, а также условиями, такими как температура и ионная сила.
Термин "вектор" включает плазмиду, космиды, фаги или вирусы. В оптимальном варианте вектором является плазмида для экспрессии в прокариотах. Продукты, амплифицированные с помощью PCR, могут быть клонированы в определенные сайты вектора экспрессии для образования рекомбинантного экспрессирующего вектора.
После получения вектора экспрессии он может быть введен в подходящую клетку-хозяина любым подходящим способом, таким как трансформация, трансфекция, электропорация, осаждением фосфатом кальция и прямой микроинъекцией и т.п.
Подходящие для настоящего изобретения клетки-хозяева могут представлять собой прокариотические или эукариотические клетки. Идеальные прокариоты-хозяева включают E.coli и Bacillus subtitles и пр. Наилучшим прокариотом-хозяином является E.col, в то время как идеальным эукариотическим хозяином являются дрожжи.
Клетки-хозяева, в которые введен вектор, выращивают на селективной питательной среде, и отбирают клетки, содержащие вектор экспрессии. Отобранные клетки, которые содержат вектор экспрессии, затем выращивают при подходящих условиях, и при определенных условиях индуцируют эксперссию гена SK. Оптимально использовать для индукции экспрессии гена SK нагревание.
Продукты экспрессии гена SK могут быть очищены рядом процедур выделения и очистки, которые, вообще, хорошо известны специалистам в этой области техники, с помощью которых можно получить очищенные продукты. Лучше, чтобы продукты экспрессии присутствовали в клетке-хозяине в форме телец включений, в результате чего упрощается процедура очистки, и возрастает чистота продукта.
(1) Из ротовой полости человека выделяют гемолитический streptococcus aureus. Очищают стрептокиназу из питательной среды. Определяют 5 аминокислот из N- и C-конца SK, соответственно. Конструируют праймеры в соответствии с этими N- и C-концевыми последовательностями, и используют их для амплификации гена SK непосредственно с помощью PCR, в которой в качестве матрицы используют бактериальную макромолекулярную ДНК.
(2) Амплифицированный ген, проверенный методом анализа нуклеотидной последовательности, лигируют с прокариотическим экспрессирующим вектором, который содержит промоторы PL, PR, ген Clt 857, сигнал терминации 5S-РНК и другие регуляторные элементы для образования плазмиды высокоэффективной экспрессии psTE-SK-1.
E. coli трансформируют psTE-SK-1. Экспрессию гена SK индуцируют температурой. Продукты экспрессии r-SK, представленной в сконструированных бактериях, формируются в тельца включений. Молекулярную массу r-SK проверяют SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия), и определяют ее в 43000, и r-SK составляет более 40% от общего количества бактериального белка. Сконструированную бактерию называют STE-SK-1.
(3) Сконструированные бактерии STE-SK-1 ферментируют в менее питательной среде, которую пополняют средой LB, глюкозой и микроэлементами до и после температурной индукции. Ферментацию осуществляют при 30-40oC. DO (растворенный кислород) 50-80%, pH 6-8, причем скорость перемешивания уменьшают при возрастании DO. Бактерии разрушают гомогенизатором высокого давления. Тельца включения собирают центрифугированием, промывают буферным раствором и растворяют гуанидингидрохлоридом. После повторной обработки r-SK и двух стадий очистки получают очищенную r-SK. По способу настоящего изобретения из 1 литра питательного бульона получают 20-30 г сырых бактерий, и затем получают 600 мг очищенного продукта r-SK с чистотой 97-99% и с удельной активностью 100 000 ME/мг. К очищенной r-SK добавляют сывороточный человеческий альбумин, глутамат натрия и фосфаты, затем фильтруют через фильтр Millipore и лиофилизуют. Продукт имеет вид белого порошка. Продукт, растворенный в воде для инъекций, и используют, главным образом, при лечении острого инфаркта миокарда и других тромбозных заболеваний.
При лечении острого инфаркта миокарда у собак и тромба бедренной артерии у кроликов (0,3 мг/кг) растворение тромба происходит за 30-60 мин, и просветы сосудов восстанавливаются. При лечении гифемы у кроликов гифема исчезает в течение 24 часов, и при лечении внутриглазной экссудации экссудат исчезает в течение нескольких часов.
В настоящем изобретении технологию рекомбинантных ДНК применяют для экспрессии r-SK с эффективностью непатогенных E.coli. Способ безопасен и безвреден для окружающей среды и персонала. Благодаря высокой эффективности экспрессии и простой процедуре очистки чистоты и выход продукта являются достаточно высокими, и эти преимущества могут в большой степени снизить стоимость получения r-SK
Рис. 1. Физическая карта вектора экспрессии PLY-4.
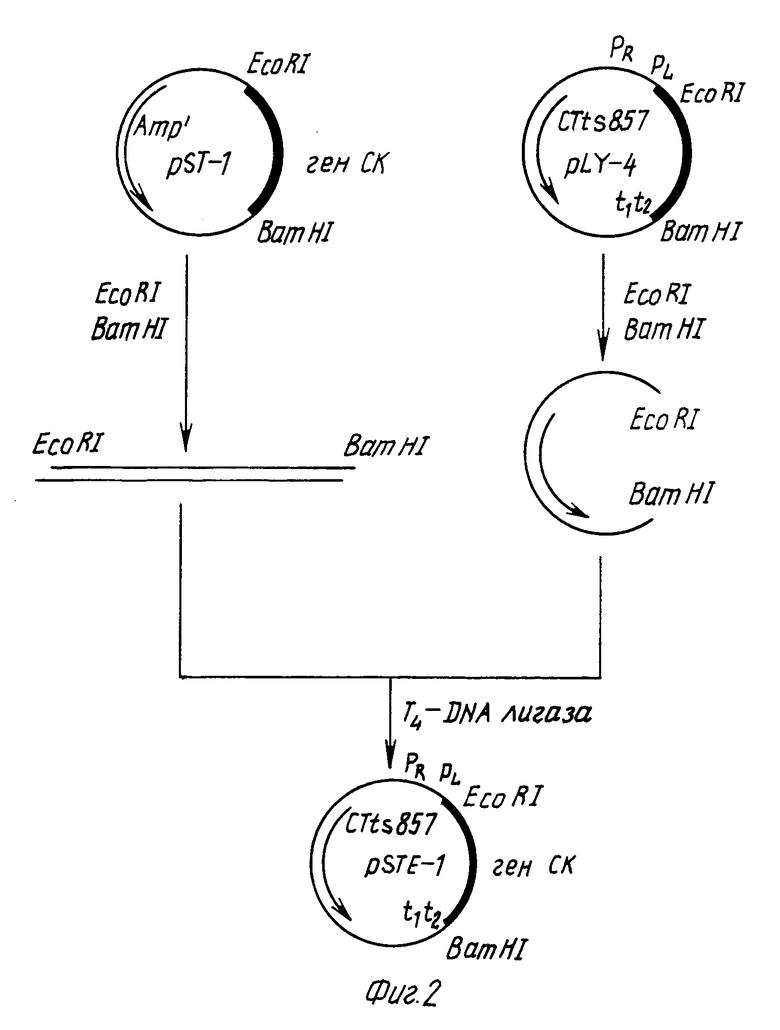
Рис. 2. Физическая карта вектора экспрессии psTE-SK.
1. Амплификация гена SK с помощью PCR.
Получают 60 штаммов streptococcus aureus из больничной лаборатории, и выращивают их в течение ночи. Отбирают штамм, который секретирует SK с наибольшей активностью (N 8), и выращивают его в большом количестве. Выделяют SK из питательной среды, и анализируют последовательности 5 аминокислот у N- и C-концов SK с помощью секвенатора белков или вручную. В соответствии с результатами анализа аминокислот у N- и C-концов конструируются праймеры PCR. В соответствии с показанными ниже праймерами получают специфическую полосу PCR.
Пример I:
5' CGC GAA TTC GGG ATG TTT GCA CTG CTG TTT GCA 3' - EcoR 1
Пример II:
5' GGC GGA TCC TTA TTT GTA TTT AGG GTT CTC AGG 3' - Bam H I
Эти два праймера синтезируют твердофазным фосфотриэфирным методом с помощью ДНК-синтезатора. После очистки праймеры используют для амплификации гена SK. 5'-конец каждого из этого пары праймеров PCR содержит сайты рестрикции, соответственно.
Макромолекулярную ДНК Streptococcus aureus N 8 получают по способу Frerick M. Ausubel, и отношение A260/A280 > 2,0.
Система и условия PCP.
Матрица ДНК - 3 мкл (1 мкг)
Праймер I - 1 мкл (50,0 пмоль)
Праймер II - 1 мкл (50,0 пмоль)
dNTP - 10 мкл (2,0 ммоль/л)
Буфер, 5 x PCR - 20 мкл
dd H2O - 64 мкл
Tao ДНК-полимераза - 1 мкл (25 E).
PCR включает денатурацию при 90oC в течение 60 с, удлинение при 72oC в течение 120 с и отжиг при 52oC в течение 60 с. После 15 циклов в реакционную систему добавляют еще 25 E Tag ДНК-полимеразы, и осуществляют еще 15 циклов. По окончании реакции анализируют электрофорезом на агарозном геле 2,5 мкл образца, и наблюдают полосу в 1,3 т.п.о., которая совпадает с длиной полного гена SK.
2. Конструирование и секвенирование ДНК-гена из клона.
Продукты PCR и плазмиду pUC гидролизуют одной и той же рестриктазой, смешивают с ДНК-лигазой фага T4 при комнатной температуре в течение 1 часа, и используют для трансформации E.coli JM 83, которая рассеяна на планшетах LB с ампициллином, и инкубируют при 37oC для селективного культивирования.
Отбирают единичную колонию, и используют ее для получения плазмиды. После анализа с несколькими рестриктазами плазмиду со специфичным фрагментом называют psT-1.
Анализ последовательности нуклеотидов плазмиды
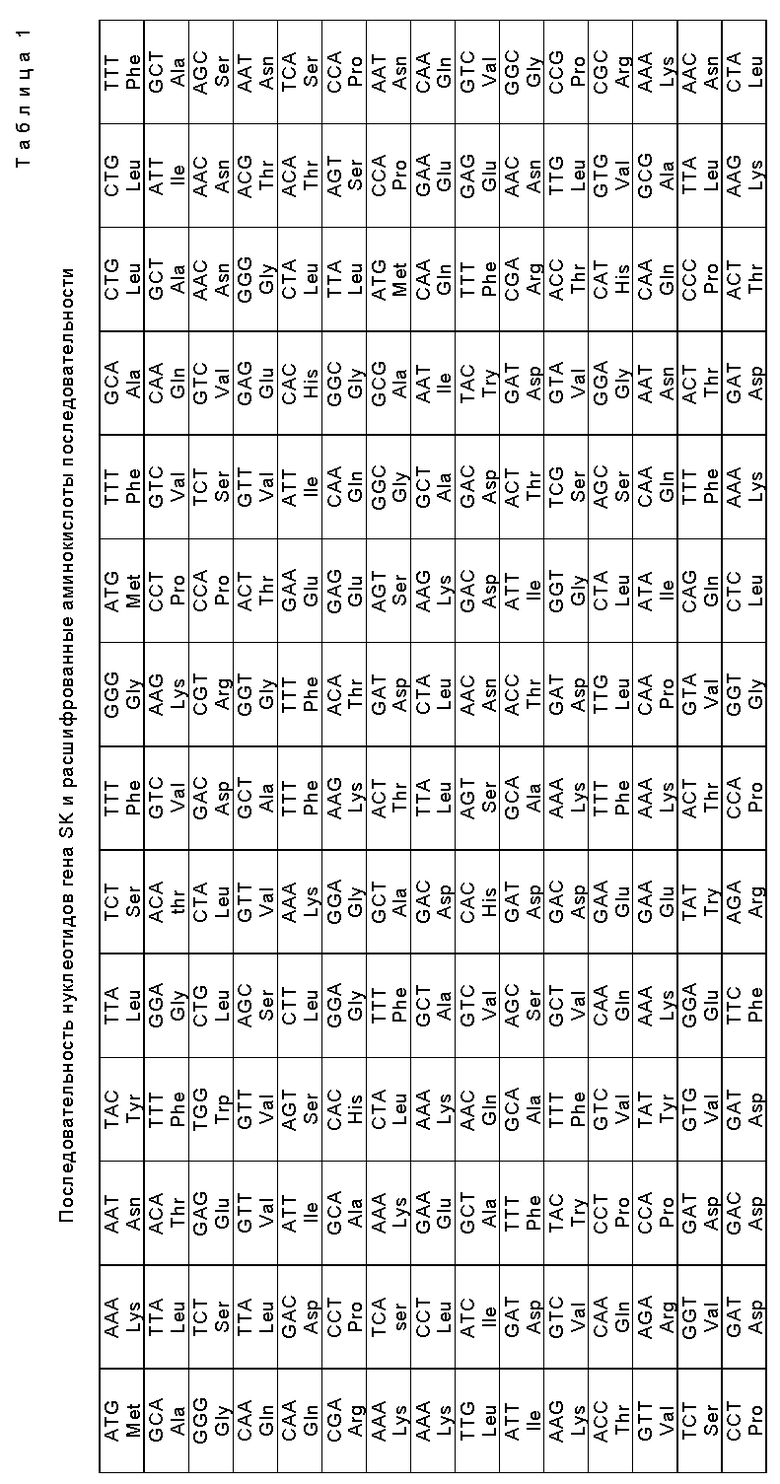
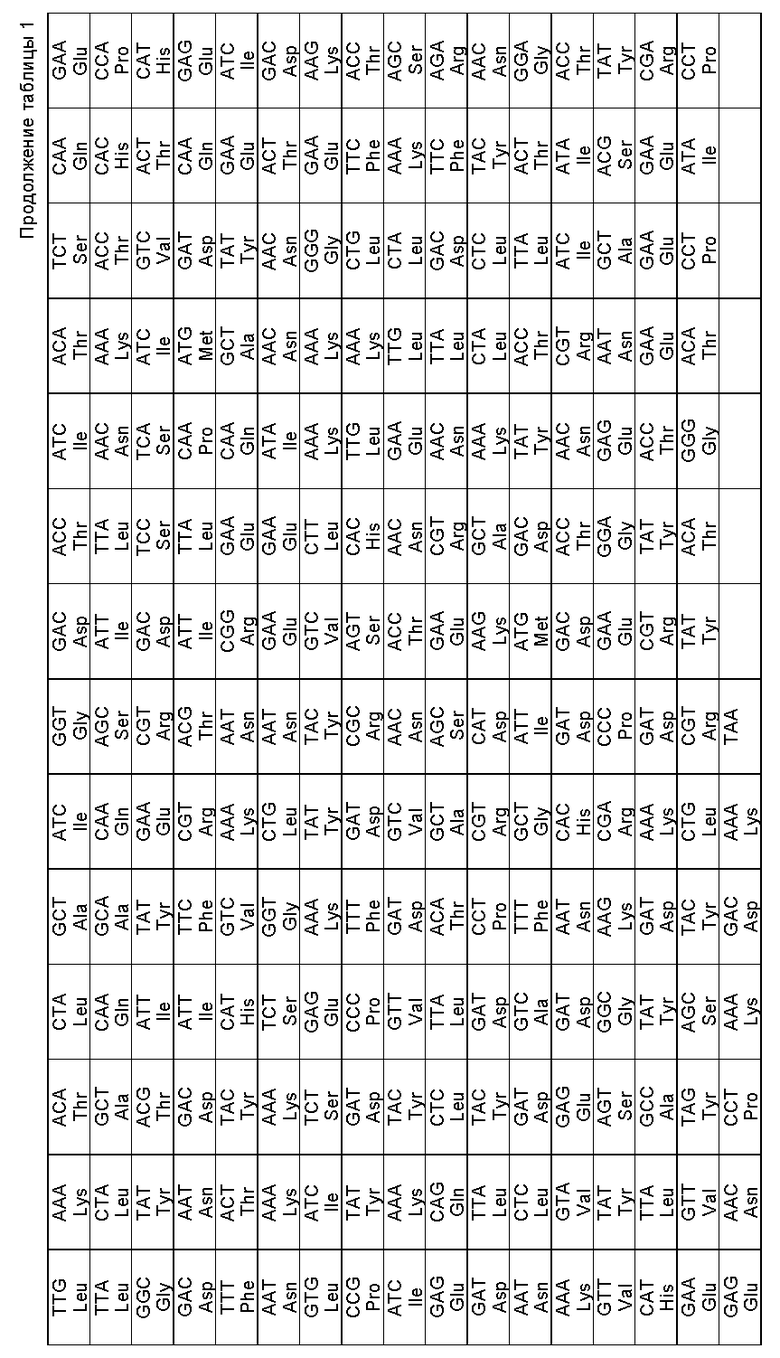
Так как существует сайт Hind III в гене SK, конструируют два субклона с фрагментами из 770 п. о. и 570 п.о. После определения последовательности нуклеотидов утверждается рамка гена SK. Результаты определения приводятся в табл. 1.
3. Экспрессия гена SK клона в E.coli
Конструирование вектора экспрессии. Удаляют ген в сайте Lacz вектора pGEM (3z), и в pGEM (3z) лигируют ген Clt 857, промоторы PR и PL, фрагмент со многими сайтами рестрикции, сигнал терминации PHK 5s и терминальные кодоны t1, t2, как показано на рис.1.
Конструирование экспрессирующей плазмиды. Плазмиду pST-1 переваривают двумя рестриктазами и разделяют электрофорезом на агарозном геле. Извлекают и очищают ген SK 1,3 т.п.о., затем лигируют с экспрессирующим вектором.
Трансформируют E.coli К802 лигирующей смесью по способу с фосфатом кальция и выращивают в питательной среде на планшете LB с ампициллином. Получают плазмиды из отобранной единичной колонии, и идентифицируют с помощью рестриктаз. Плазмиду, содержащую специфичные фрагменты гена SK, называют экспрессирующей плазмидой pSTE-SK-1, и сконструированные бактерии называют STE-SK-1.
4. Экспрессия гена в E.col
Отбирают единичную колонию STE-SK-1 и выращивают в жидкой питательной среде LB при 30oC в течение ночи при встряхивании при 2000 об/мин. Смесь разбавляют средой в соотношении 1:100, и встряхивают при 30oC до достижения A600 порядка 0,6 (примерно 4-5 ч). Поднимают температуру до 42oC в течение 3-4 мин, и снова встряхивают в течение 3-4 ч. Бактерии собирают центрифугированием при 5000 об./мин, дважды промывают ЗФР (pH 7,4), и хранят при -20oC, или сразу выделяют продукты экспрессии.
5. Идентификации продуктов экспрессии
Применяют электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) для определения молекулярной массы и уровня экспрессии r-SK, и для идентификации фибринолитической активности r-SK используют реверсивный фибрин-планшет.
Образец солюбилизирующего раствора содержит 0,0625 М трис-HCl (pH 6,7), 2% SDS, 10% глицерина, 5% 2-меркаптоэтанола и 0,001% бромфенолового синего.
Получение и загрузка образца
Центрифугируют 1 мл индуцированной бактериальной суспензии. Осадок суспендируют в 100 мкл образца солюбилизирующего раствора, нагревают в кипящей воде в течение 5 мин, и осадок должен раствориться. Образец, соответствующий хроматографическому пику, смешивают с 2 объемами солюбилизирующего раствора и нагревают. Количество загрузки 10 мкл. Так же обрабатывают контрольные бактерии и бактерии до индукции.
Окрашивают гели кумассии бриллиантовым голубым или солями серебра.
Сканирование белковых полос. Гель сканируют с помощью сканирующего денситометра с двойной длиной волны shimadzu CS-9100 данные обрабатывают на компьютере, и получают результаты в виде процента каждой белковой полосы относительно общего количества бактериальных белков.
Результаты. В лизатах индуцированных бактерий существует очень темная полоса 15 кД, что соответствует MW 43000, в то время как такой полосы не наблюдают в контрольных и неиндуцированных бактериях. Результаты показывают, что r-SK составляет более 65% общих белков бактерий.
Идентификация фибринолитической активности продуктов экспрессии. Упомянутый гель промывают 2,5% тритоном X-100 и обычным солевым раствором для удаления додецилсульфата натрия (SDS), затем помещают на агарозный гель, содержащий фибриноген, плазминоген человека и тромбин, и затем инкубируют при 37oC в течение 2 ч. В агарозном геле имеется литическая зона, соответствующая локализации полосы 43 кД, так как фибрин в этой области растворяется. Это означает, что продукт экспрессии обладает фибринолитической активностью.
Структура продуктов экспрессии, присутствующих в бактерии. Бактерии разрушают гомогенизатором высокого давления или ультразвуком и центрифугируют. Осадки и супернатант идентифицируют SDS-PAGE. Результаты показывают, что полоса 43 кД появляется в осадках, а не в супернатанте. Это означает, что продукты экспрессии r-SK образуют тельца включения.
Определение удельной активности r-SK. Для определения активности r-SK используют фибрин-планшет, пробу с хромогеном или растворение фибриновых сгустков, в то время как для определения концентрации белков используют способ lowrry. Удельная активность = ед-цы активности r-SK в ед-це объема (E)/содержание белков в ед-це объема (мг).
6. Ферментация бактерий, полученных генной инженерией.
Ферментация при встряхивании колбы.
Единичную колонию STE-SK-1 инокулируют в среде LB-Amp (ампициллин), инкубируют при 30oC в течение ночи, разбавляют на следующий день улучшенной средой M9 в отношении 1:50 до достижения культурой A600 0,6 - 0,8, и индуцируют в течение 3-4 часов. Суспензию бактерий центрифугируют при 5000 об/мин в течение 10 мин при 4oC. Бактерии промывают ЗФР (pH 7,4), взвешивают и хранят при 20oC.
Ферментация в ферментере 5LNBS BiO F III.
Единичную колонию STE-SK-1 инокулируют в 100 мл питательной среды LB, инкубируют при 30oC в течение ночи, определяют A600 и используют в качестве инокулятивного раствора для ферментации.
Ферментер автоклавируют при 120oC, 15 pd (pd = psu=103 кПа), в течение 15 мин. После охлаждения устанавливают следующие параметры: температура -30oC, pH 6-8, растворенный кислород (DO) 50-80%, скорость перемешивания 225-800 об/мин (изменяется с изменением величины DO). Когда все параметры становятся стабильными, взвесь STE-SK-1 инокулируют в ферментер при соотношении 1:50 (инокулятивный раствор : среда). Когда A600 достигает примерно 0,6, ферментацию продолжают при условиях индукции без каких-либо изменений упомянутых параметров в течение 3-4 ч. Бактерии собирают и хранят при -20oC.
7. Очистка r-SK изоэлектрофокусированием Rotofor и гель-фильтрацией.
(1) Полученные генной инженерией бактерии (4 г) суспендируют в 25 мл гипотонического буферного раствора (0,05 M трис-JCl, pH 7,8, 0,2 М ЭДТК, лизоцим - 0,5 мг/мл/, перемешивают при комнатной температуре в течение 60 мин, и добавляют до 2% тритон X-100 и до 0,5 M NaCl. Бактерии диспергируют гомогенизатором, центрифугируют при 8000 об/мин в течение 60 мин при 10oC, и промывают буферным раствором (0,05 M трис-HCl, pH 7,8, 0,02 M ЭДТК) три раза. Собирают осадки, и суспендируют их в 20 мл воды, диализуют против воды, и к удержанному веществу добавляют мочевину до 4 M для растворения телец включения.
(2) Выделение r-SK изоэлектрофокусированием Rotofor и извлечение r-SK.
К 49 мл вышеупомянутого раствора телец включений добавляют 1 мл амфолина (pH 3-10). После фокусирования в течение 4 часов на аппаратуре для изоэлектрофокусирования Rotofor при 12 в при 4oC образцы каждого сегмента идентифицируют SDS-PAGE. Растворы, содержащие SK, сливают, диализуют в 0,05 M ЗФР, pH 7,4, и 0,02 M ЭДТК для удаления мочевины, разбавляют буфером, солюбилизирующим аминокислоты, и повторяют процесс (refolding) при 4oC в течение 72 ч. После центрифугирования при 8000 об./мин собирают супернатант и концентрируют ультрафильтрацией.
(3) Гель-фильтрация и стерилизующая фильтрация.
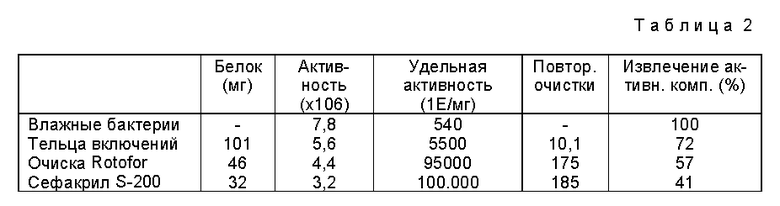
Образец, сконцентрированный ультрафильтрацией, загружают в сефакрил S-200 (уравновешанный буфером, солюбилизирующим аминокислоты), и элюируют при скорости потока 1 мл/мин. Фракции, проверенные на аппаратуре для жидкостной хроматографии низкого давления Econo, собирают, и анализируют чистоту и удельную активность SDS-PAGE. Полученный раствор фильтруют через фильтр Millipore 0,2 мкм, и стерилизуют фильтрацией через Millipore 2,2 мкм и лиофилизуют. Концентрация белков, активность и удельная активность r-SK число очисток и степень извлечения приводится в табл. 2.
Пример 2.
1. Хранение полученных генной инженерией бактерий.
Инокулят помещают на хранение и хранят при -70oC в холодильнике.
Регулярно идентифицируют карту плазмиды, и проверяют, сохраняется ли уровень экспрессии 65%.
2. Выращивание сконструированных бактерий.
Среда.
Планшет LB-Amp.
Дрожжевой экстракт, г - 5
NaCl, г - 5
Триптон, г - 10
Агар, г - 10
Вода, мл - до 1000
Все автоклавируют при давлении 1 кг/см2 в течение 20 мин, и после охлаждения добавляют ампициллин.
Жидкая среда LB.
То же, что и для планшета LB, за исключением агара и ампициллина.
Берут посевной бактериальный материал, хранящийся в холодильнике при -70oC, инокулируют на планшет (содержащий 100 мкг/мл ампициллина) и инкубируют при 30oC в течение ночи. Отбирают с планшета единичную колонию, инокулируют ее в жидкую питательную среду LB и инкубируют при 30oC в течение ночи. Получают инокулят первого порядка, который инокулируют в жидкую питательную среду LB в соотношении 1:10, и инкубируют при 30oC в течение ночи, чтобы получить инокулят второго порядка.
3. Ферментация
После автоклавирования в ферментер добавляют питательную среду, чтобы заменить ею воду. Устанавливают параметры, и инокулят второго порядка инокулируют в ферментер в соотношении 1:10. Ферментацию осуществляют при повышении давления воздуха в ферментере.
Во время ферментации поддерживают следующие условия: температура - 30oC, pH - 6-8, DO - 50-80%, скорость перемешивания изеняется с изменением величины DO. Каждый час следует отбирать 5 мл бактерий для определения плотности бактерий (OD600) и концентрации глюкозы.
Регулируют pH среды водным раствором аммиака, чтобы сохранять величину pH 6-8, и при необходимости следует добавлять пеногаситель.
Количество триптона, глюкозы и микроэлементов следует пополнять до и после индукции.
После индукционного культивирования в течение 3-4 ч, когда OD600 превысит 15, ферментацию останавливают, и бактерии собирают, центрифугируют, взвешивают и сразу же разбивают на изолированные тельца включения. В противном случае, бактерии хранят при -70oC.
4. Разрушение бактерий.
Влажные бактерии суспендируют в буферном растворе, загружают в гомогенизатор и разрушают при определенном давлении.
Показатель качества. Степень разрушения бактерий проверяют методом микроскопии следующим образом. Бактериальную суспензию разбавляют, намазывают на стеклянную пластину, окрашивают по способу Грамма и подсчитывают число бактерий (A) в 4 полях зрения микроскопа - до гомогенизации. Такие же процедуры проделывают с суспензией после гомогенизации, и получают число бактерий (B).
Степень разрушения бактерий = (A-B) A • 100%.
Когда упомянутая степень превысит 95%, осуществляют центрифугирование, и собирают осадок, который представляет собой сырые тельца включения. В них чистота r-sk составляет более 75-85% относительно общих белков бактерий.
5. Очистка телец включения.
Сырые тельца включения промывают несколько раз, и чистота r-SK составляет более 90% от общих белков бактерий.
6. Растворение и извлечение.
Очищенные тельца включения растворяют гуанидингидрохлоридом и центрифугируют при 10000 об/мин в течение 30 мин. Супернатант диализуют в ФБ (PB) несколько раз и центрифугируют при 20000 об/мин в течение 30 мин. Чистота r-SK будет более 95% при удельной активности 65000 ME/мг, и извлечение r-SK будет порядка 65%.
7. Очистка.
Ионообменная хроматография. Используют системы хроматографии Waters 650 или Econo. Извлеченную r-SK загружают в анионообменную колонку, уравновешенную PB, при скорости потока 1,0 мл/мин. Элюируют PB линейным градиентом pH при скорости потока 4,00 мл/мин. Собирают первый пик элюирования (r-SK).
Анализ SDS-PAGE показывает, что чистота r-SK достигает 94% при удельной активности 80000 ME/мг, извлечение r-SK> 55%, и концентрация белка 7 мг/мл.
Гель-фильтрация. Гелю дают набухать в свободной от эндотоксинов и бактерий деионизованной воде, автоклавируют, заполняют им колонку и уравновешивают PB. В колонку загружают образец, профильтрованный через фильтр Millipore 0,22 мкм, и элюируют PB при скорости потока 5,0 мл/мин. Активность r-SK проверяют методом фибринового гелевого растворения и сливают вместе с содержимое пробирок с активным пиком. В этом случае удельная активность продукта составляет около 100000 ME/мг. Из 1 литра бульона получают около 600 мг очищенного продукта, и извлечение r-SK составляет 40-50%.
8. Фильтрация для освобождения от бактерий, расфасовка и лиофилизация.
В соответствии с концентрацией белка и активностью r-SK добавляют вспомогательные материалы и стабилизаторы в следующих пропорциях:
r-SK, ME - 500000
Фосфаты, мг:
Na3HPO4 - 1,33
NaH2PO4 - 0,31
Глутамат натрия (для инъекций), мг/ампула - 30
Человеческий альбумин, мг/ампула - 30
Вышеупомянутые материалы должны соответствовать требованиям к лекарственным средствам для инъекций.
Стерилизация для освобождения от бактерий. Для достижения нужной степени очистки осуществляют 100 фильтрацией через 0,22 мкм.
Продукт разливают в ампулы по 500000 или 1500000 ME/ампула.
Аликвоты лиофилизуют, затем ампулы запаивают, наклеивают этикетки, и упаковывают ампулы в коробки.
Продукты хранят в холодильнике при 8-12oC.
Методом ангиографии доказывается, что r-SK является сильнодействующим средством при лечении тромба бедренной артерии и тромба коронарной артерии у собак.
Изобретение относится к способу получения рекомбинантной стрептокиназы. Ген стрептокиназы амплифицируют с помощью РСR и рекомбинируют с прокариотическим экспрессирующим вектором-плазмидой RLY-4. Трансформируют E. coli pSTE-SK-I и индуцируют для экспрессии гена SK с помощью температуры. Полученные бактерии ферментируют и разрушают высоким давлением. Собирают тельца включения, затем извлеченную r-SK очищают в два этапа, включающих ионный обмен и гель-фильтрацию. Чистота и выход r-SK, полученной по настоящему изобретению, являются весьма высокими, а стоимость низкой. 7 з.п. ф-лы, 2 ил., 2 табл.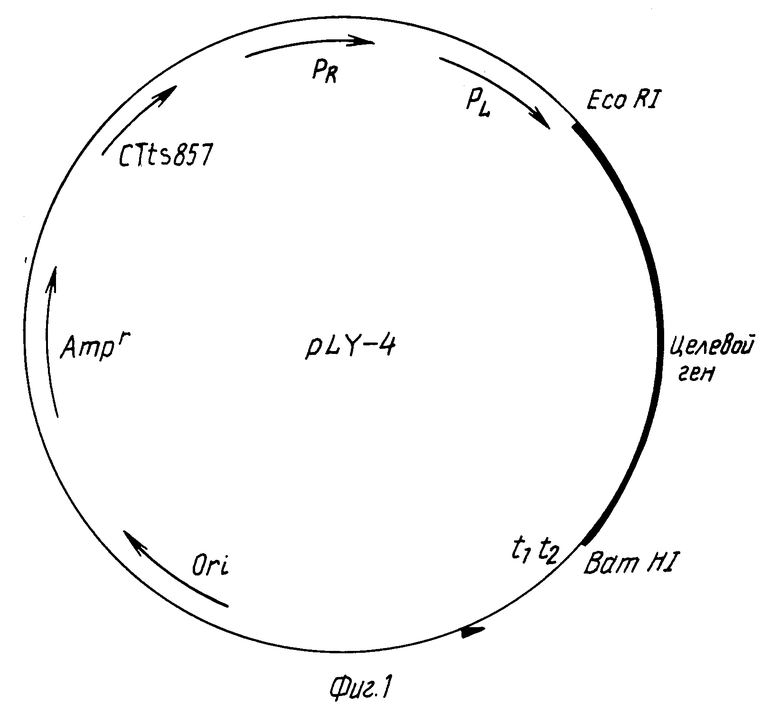
5'CGC CAA TTC GGG ATG GCA CTG CTG TTT GCA3' - EcoRI
5'CGC GGA TTC TTA TTT GTA TTT AGG CTT GTC AGG3' - Bam HI
соответствующие нуклеотидным последовательностям SK в гемолитическом Streptococcus aureus, амплифицируют ген с помощью полимеразной цепной реакции (PCR), при этом макромоллекулярную ДНК стрептококка, содержащую ген SK, используют в качестве матрицы; ген SK лигируют с прокариотическими экспрессирующими векторами с образованием рекомбинантного экспрессирующего вектора; клетки E.coli трансформируют рекомбинантным экспрессирующим вектором, отбирают трансформированные клетки, трансформированные клетки культивируют в подходящих условиях и индуцируют экспрессию гена SK; выделяют и очищают экспрессированную r-SK.
| 0 |
|
SU151337A1 | |
| Устройство дискретного сжатия динамического диапазона сигнала | 1973 |
|
SU489201A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМАЗКИ ДЛЯ ХОЛОДИОЙ ОБРАБГГПОГ МЕТАЛЛОВ ДАВЛЕНИЕМ | 0 |
|
SU407942A1 |
| Способ получения стрептокиназы | 1983 |
|
SU1147749A1 |
Авторы
Даты
1999-03-20—Публикация
1995-04-03—Подача