Изобретение относится к медицине, конкретно к трансфузионной медицине, и предназначается для использования в учреждениях службы крови.
Известен способ получения концентрата тромбоцитов из плазмы, обогащенной тромбоцитами, регламентируемый в [1] . Полимерные контейнеры "Гемакон" 500/300 с заготовленной и идентифицированной донорской кровью укладываются в центрифужные стаканы. Стаканы с полимерными контейнерами уравновешиваются попарно на весах, устанавливаются в диаметрально противоположные чашки ротора центрифуги модели ЦЛ-4000 (допускаются центрифуги моделей ЦР-3 или К-70Д) и центрифугируются на определенном режиме (центробежное ускорение - 680g, время центрифугирования - 13 мин), в результате чего кровь разделяется на плазму, обогащенную тромбоцитами, и эритроцитную массу. Полимерный контейнер с осевшими форменными элементами крови осторожно помещается в плазмоэкстрактор этикеткой к задней его пластине и прижимается передней подвижной пластиной, затем снимается зажим с трубки, ведущей к добавочному пустому контейнеру, и в него переводится плазма. Когда граница раздела плазмы и эритроцитов окажется у выходного отверстия основного контейнера, на трубку накладывается зажим на расстоянии 2-5 см от контейнера с плазмой. Контейнер с эритроцитной массой извлекается из плазмоэкстрактора. Из контейнера с плазмой, обогащенной тромбоцитами, путем сжатия его стенок полностью удаляется воздух в соединительную трубку или в контейнер с эритроцитной массой, далее контейнеры герметизируются и разделяются с помощью аппарата для запайки. Контейнер с эритроцитной массой этикетируется и помещается в холодильник на хранение при температуре +4oC. Полимерные контейнеры с плазмой, обогащенной тромбоцитами, укладываются в центрифужные стаканы, которые попарно уравновешиваются на весах, устанавливаются в диаметрально противоположные чашки ротора центрифуги модели ЦЛ-4000 (допускаются центрифуги моделей ЦР-3 или К-70Д) и центрифугируются на определенном режиме (центробежное ускорение - 2400 g, время центрифугирования - 20 мин), в результате чего тромбоциты из плазмы оседают на дно контейнера, а над ними располагается плазма, бедная тромбоцитами. К контейнерам, извлеченным из центрифуги и помещенным в плазмоэкстрактор, присоединяется пустой полимерный контейнер "Компопласт 300". Затем давлением подвижной пластины плазмоэкстрактора на контейнер большая часть плазмы, бедной тромбоцитами, переводится в пустой полимерный контейнер. Когда над тромбоцитами остается 45-65 мл плазмы, необходимой для дальнейшего их ресуспендирования, соединительная трубка перекрывается на расстоянии 2-5 см от контейнера с концентратом тромбоцитов.
Контейнер с концентратом тромбоцитов удаляется из плазмоэкстрактора, ослабляется зажим на трубке и переводится воздух из контейнера с концентратом тромбоцитов в соединительную трубку или контейнер с плазмой, бедной тромбоцитами. Далее контейнеры герметизируются и разделяются с помощью аппарата для запайки. Контейнер с плазмой этикетируется и отправляется на хранение. Контейнер с концентратом тромбоцитов выдерживается без перемешивания в спокойном состоянии в течение 1 часа при температуре 22±2oC. Через час тромбоциты ресуспендируют в оставшейся плазме осторожным размешиванием до тех пор, пока концентрат клеток не приобретает вид гомогенной взвеси без видимых агрегатов. Контейнер с концентратом тромбоцитов этикетируется, взвешивается и отправляется на хранение. Хранится концентрат тромбоцитов, выделенный из свежезаготовленной крови, в полимерном контейнере при температуре 22±2oC в течение 24 ч или при постоянном помешивании в автоматических мешалках в течение 72 ч при этой же температуре.
Для производства концентрата тромбоцитов по известному способу, донорская кровь заготавливается и фракционируется на компоненты в комплектах полимерных контейнеров, приготовленных посредством последовательного присоединения контейнера "Компопласт" 300 к контейнеру "Гемакон" 500/300, причем соединение контейнеров должно осуществляться непосредственно перед отделением плазмы, бедной тромбоцитами, от концентрата тромбоцитов и поэтому невозможно гарантировать стерильного соединения. Кроме того, вышеуказанные контейнеры изготовлены из поливинилхлорида марки ПМ-1/42 [2], который не обладает свойством газопроницаемости и не гарантирует доступ кислорода к тромбоцитам для сохранения их жизнеспособности и стабильного качества. Поэтому концентрат тромбоцитов, заготовленный в указанные полимерные контейнеры, хранится в этих контейнерах при температуре 22±2oC не более 24 ч, а при постоянном помешивании в автоматических мешалках не более 72 ч.
Для разделения консервированной крови на компоненты известный способ регламентирует производить центрифугирование крови в два этапа на центрифуге модели ЦЛ-4000 (допускается на центрифуге ЦР-3 или К-70Д). Для центрифугирования полимерных контейнеров с консервированной кровью вышеуказанные центрифуги снабжены роторами, имеющими только по четыре стакана для укладки контейнеров, то есть максимальное количество контейнеров, загружаемых единовременно в центрифугу - 4 шт. Концентрат тромбоцитов, заготовленный с применением вышеуказанных центрифуг, содержит не менее 50•109 тромбоцитов в 45-65 мл плазмы (при подсчете после максимального срока хранения в течение 72 ч).
В качестве хладагента в системах охлаждения центрифуг используется экологически небезопасный фреон, отрицательно воздействующий на природу (разрушает озоновый слой). Уровень шума, создаваемый указанными центрифугами во время работы при измерительном расстоянии 1 м, составляет 85 дБ.
Таким образом, известный способ не обеспечивает стабильного качества концентрата тромбоцитов, не гарантирует исключения вероятности нарушения стерильности соединения пластикатных контейнеров, имеет низкую производительность центрифугирования, а использование фреона отрицательно воздействует на природу и создаваемый центрифугами шум вреден для персонала.
Задачей изобретения является обеспечение стабильного качества концентрата тромбоцитов, увеличение концентрации тромбоцитов, исключение вероятности нарушения стерильности соединения пластикатных контейнеров, повышение производительности центрифугирования, исключение вредного воздействия фреона на природу и улучшение условий труда персонала.
Выполнение указанной задачи достигается тем, что донорская кровь, предназначенная для получения концентрата тромбоцитов, заготавливается в газопроницаемые строенные пластикатные контейнеры, гарантирующие доступ кислорода к тромбоцитам для сохранения их жизнеспособности и обеспечения стабильного качества концентрата тромбоцитов в течение 5 сут., и представляющие собой единую закрытую систему с предварительно залитым антикоагулянтом и позволяющие не производить операцию присоединения контейнеров для исключения вероятности нарушения стерильности, а центрифугирование консервированной крови производится на низкоскоростных рефрижераторных центрифугах (например, модель RC-3CPlus), имеющих ротор с шестью чашками для укладки и центрифугирования контейнеров и обеспечивающих за счет плавного старта и мягкой остановки качественную сепарацию и увеличение концентрации тромбоцитов не менее, чем до 60•109 клеток в 50-60 мл плазмы. Кроме этого, в системах охлаждения центрифуг используется хладагент, не содержащий экологически опасный фреон, а уровень шума, создаваемый работающей центрифугой, составляет не более 58 дБ.
На фиг. 1 схематично изображен общий вид строенного пластикатного контейнера.
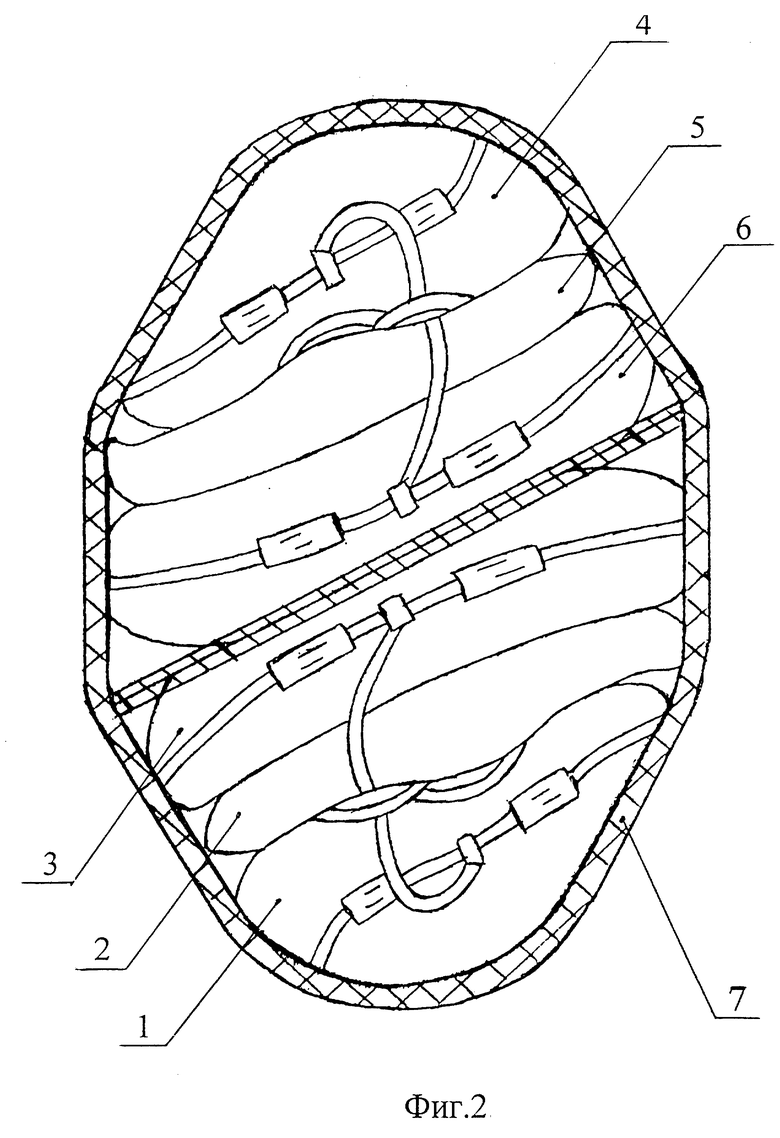
На фиг. 2 указана схема укладки двух комплектов строенных пластикатных контейнеров в адаптер центрифуги.
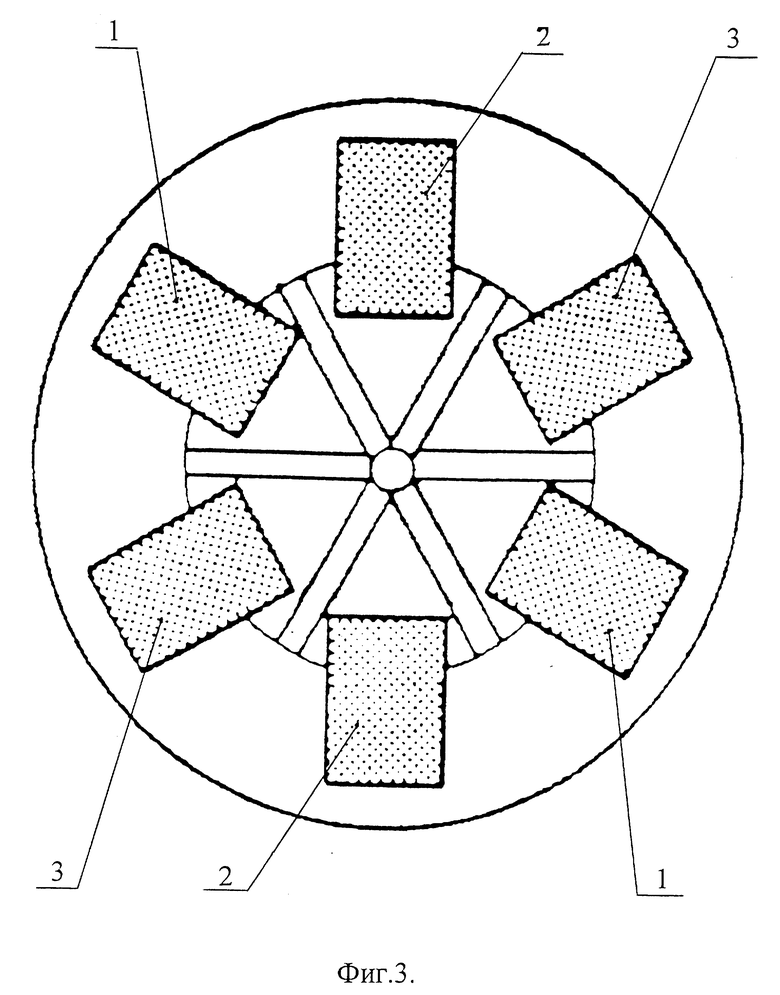
На фиг. 3 указана схема загрузки ротора центрифуги.
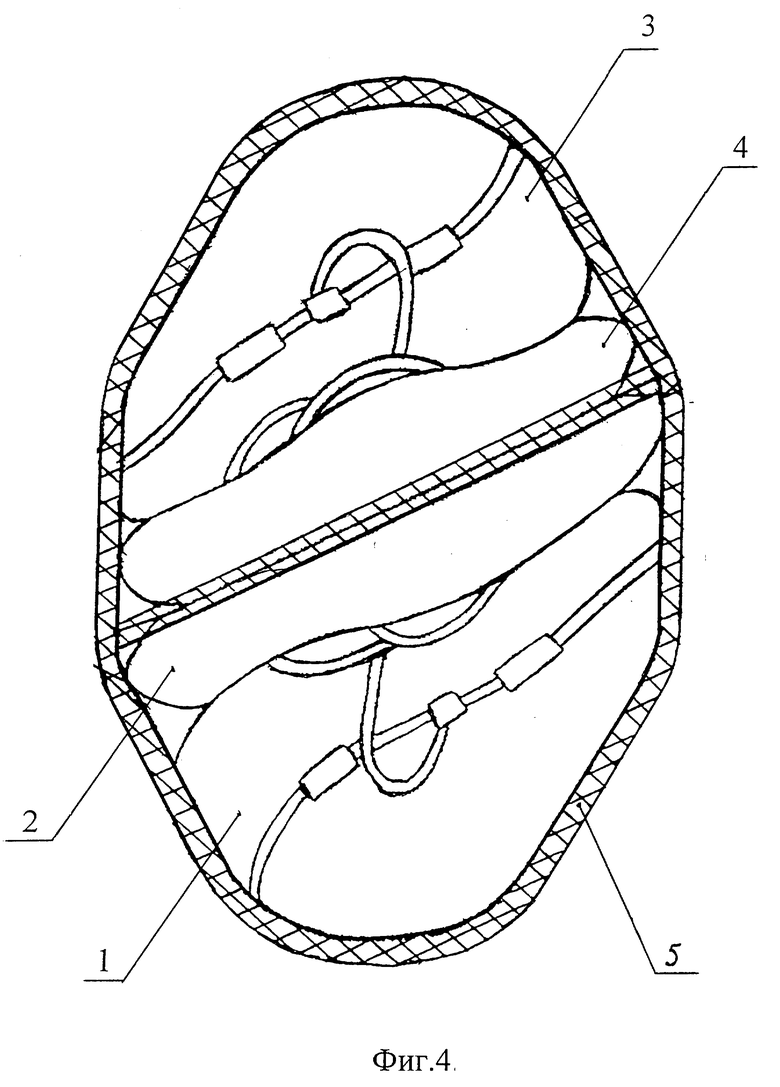
На фиг. 4 указана схема укладки двух комплектов сдвоенных пластикатных контейнеров в адаптер центрифуги.
Получение концентрата тромбоцитов по технологии "Дельрус" осуществляется следующим образом:
во время донации кровь, предназначенная для получения концентрата тромбоцитов, заготавливается в газопроницаемые строенные пластикатные контейнеры 450/400/400, CPD/SAGM (например, производства фирмы "Terumo" - Япония).
Строенный пластикатный контейнер (см. фиг. 1) состоит из контейнера 1 объемом 450 мл с антикоагулянтом CPD для донорской крови, пустого контейнера 2 объемом 400 мл и контейнера 3 объемом 400 мл с ресуспендирующим раствором SAGM.
Допускается заготавливать донорскую кровь в газопроницаемые строенные пластикатные контейнеры 450/450/300 CPD/SAGM, 500/500/300 CPD/SAGM, 450/300/300 CPD/SAGM, 450/400/400 CPD/SAGM и др.
Донорская кровь во время донации заготавливается в контейнер с антикоагулянтом CPD. Пластикатные контейнеры с заготовленной донорской кровью должны поступать в переработку для получения концентрата тромбоцитов в день взятия крови.
Идентифицированные пластикатные контейнеры с донорской кровью укладываются в адаптеры низкоскоростной рефрижераторной центрифуги (например, модель RC-3CPlus производства фирмы "SORVALL" - США) согласно фиг. 2, где 1 - пластикатный контейнер первого комплекта с кровью; 2 - пустой пластикатный контейнер первого комплекта; 3 - пластикатный контейнер первого комплекта с ресуспендирующим раствором SAGM; 4 - пластикатный контейнер второго комплекта с кровью; 5 - пустой пластикатный контейнер второго комплекта; 6 - пластикатный контейнер второго комплекта с ресуспендирующим контейнером SAGM; 7 - адаптер с перегородкой.
Адаптеры с пластикатными контейнерами уравновешиваются попарно с допустимой разностью веса не более 10 г и устанавливаются в диаметрально противоположные чашки ротора центрифуги согласно фиг. 3, где 1-1, 2-2, 3-3 - диаметрально противоположные чашки ротора центрифуги, загруженные попарно уравновешенными адаптерами с пластикатными контейнерами.
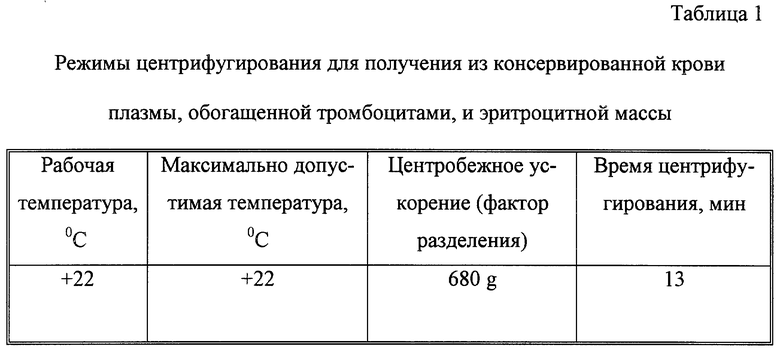
На панели центрифуги устанавливаются переключателями режимы центрифугирования согласно табл. 1.
Величина фактора разделения (центробежного ускорения) для каждой модели центрифуги вычисляется по формуле: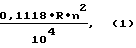
где R - радиус ротора центрифуги в см;
n - количество оборотов в минуту.
В результате центрифугирования консервированная кровь разделяется на плазму, обогащенную тромбоцитами, и эритроцитную массу.
Пластикатный контейнер с осевшими форменными элементами крови осторожно извлекается из центрифуги, помещается в плазмоэкстрактор этикеткой к задней его пластине, открывается клапан контейнера с фракционированной кровью перегибанием соединительной трубки в месте расположения клапана, затем с помощью подвижной пластина плазмоэкстрактора плазма, обогащенная тромбоцитами, переводится в пустой пластикатный контейнер.
На соединительную трубку накладывается зажим на расстоянии 2-5 см от контейнера с плазмой, обогащенной тромбоцитами.
Открывается клапан контейнера с раствором SAGM перегибанием соединительной трубки в месте расположения клапана и раствор SAGM переводится в контейнер с эритроцитной массой, образуя эритроцитную взвесь.
Контейнер с эритроцитной взвесью извлекается из плазмоэкстрактора. Из контейнера с плазмой, обогащенной тромбоцитами, путем сжатия его стенок полностью удаляется воздух, далее контейнер с эритроцитной взвесью герметизируется и отделяется с помощью аппарата для запайки.
Контейнер с эритроцитной взвесью взвешивается, проверяется правильность его маркировки, произведенной во время донации, и помещается в холодильник на хранение при температуре +4oC.
Сдвоенные пластикатные контейнеры с плазмой, обогащенной тромбоцитами, укладываются в адаптеры низкоскоростной рефрижераторной центрифуги (например, модель RC-3CPlus производства фирмы "SORVALL" - США) согласно фиг. 4, где 1 - пластикатный контейнер первого комплекта с плазмой, обогащенной тромбоцитами; 2 - пустой пластикатный контейнер первого комплекта; 3 - пластикатный контейнер второго комплекта с плазмой, обогащенной тромбоцитами; 4 - пустой пластикатный контейнер второго комплекта; 5 - адаптер с перегородкой.
Адаптеры со сдвоенными пластикатными контейнерами уравновешиваются попарно на весах с допустимой разностью веса не более 10 г и устанавливаются в диаметрально противоположные чашки ротора центрифуги согласно фиг. 3.
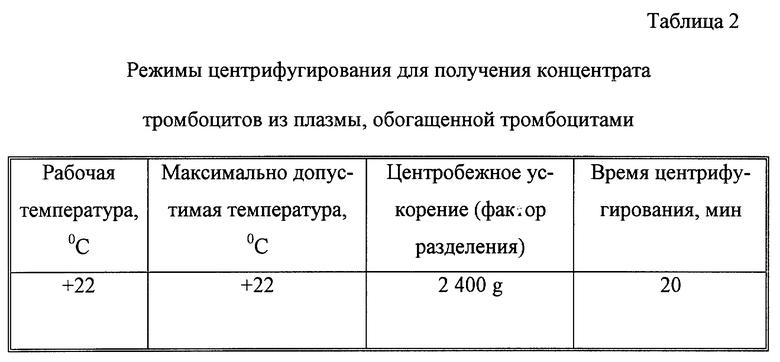
На панели центрифуги устанавливаются переключателями режимы центрифугирования согласно табл. 2.
Величина фактора разделения (центробежного ускорения) для каждой модели центрифуги вычисляется по формуле (1).
В результате центрифугирования тромбоциты из плазмы, обогащенной тромбоцитами, оседают на дно контейнера, а над ними располагается плазма, бедная тромбоцитами.
Из помещенного в плазмоэкстрактор пластикатного контейнера с осевшими тромбоцитами плазма, бедная тромбоцитами, переводится в пустой пластикатный контейнер.
Контейнер с концентратом тромбоцитов извлекается из плазмоэкстрактора, герметизируется и отделяется с помощью аппарата для запайки, взвешивается и помещается в тромбомиксер на хранение.
Хранение концентрата тромбоцитов в пластикатном контейнере производится в течение 5 сут. при температуре 22±2oC и при постоянном помешивании.
Пластикатный контейнер с плазмой, бедной тромбоцитами, отправляется на хранение или на дальнейшую переработку для получения препаратов плазмы по действующим регламентам.
Таким образом, предлагаемый способ позволяет
1. За счет применения газопроницаемых строенных пластикатных контейнеров для заготовки крови и за счет применения центрифуг, обеспечивающих плавный старт и мягкую остановку повысить концентрацию тромбоцитов не менее, чем до 60•109 клеток в 50-60 мл плазмы, обеспечить их стабильное качество (содержание тромбоцитов в дозе не менее 60•109, pH 6,0-7,4) и сохранить жизнеспособность тромбоцитов в течение 5 сут.
Полученный по известному способу концентрат тромбоцитов содержит 50•109 (не менее) клеток в 45-65 мл плазмы и имеет нестабильное качество (не исключается содержание микро- и макроскопических агрегатов; pH ниже 6,0; фактическое количество не достигает требуемого уровня - 50•109) при контроле после максимального срока хранения в течение 72 ч.
2. За счет применения строенных пластикатных контейнеров, представляющих собой единую закрытую систему с предварительно залитым антикоагулянтом, исключается вероятность нарушения стерильности.
При работе по известному способу существует вероятность нарушения стерильности, так как полимерный контейнер "Компопласт" 300 присоединяется к контейнеру "Гемакон" 500/300 непосредственно перед отделением плазмы, бедной тромбоцитами, от концентрата тромбоцитов.
3. За счет применения центрифуг, имеющих ротор с шестью чашками для укладки и центрифугирования пластикатных контейнеров с кровью, увеличивается максимальное количество единовременно загруженных в центрифугу строенных и сдвоенных пластикатных контейнеров до 12 шт. и, как следствие, увеличивается производительность центрифугирования.
В известном способе применяются центрифуги, имеющие роторы с четырьмя чашками для укладки и центрифугирования пластикатных контейнеров, то есть максимальное количество контейнеров, загружаемых единовременно в центрифугу - 4 шт.
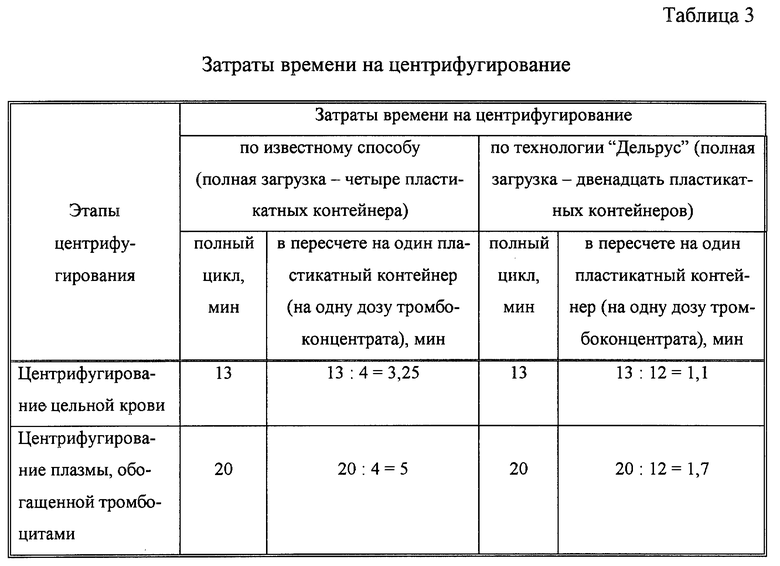
В табл. 3 приведены затраты времени на центрифугирование консервированной крови и плазмы, обогащенной тромбоцитами.
Из табл. 3 видно, что затраты времени на центрифугирование для получения одной дозы тромбоконцентрата по технологии "Дельрус" в 3 раза меньше, чем затраты времени на центрифугирование по известному способу.
4. За счет применения центрифуг, в системах охлаждения которых используется хладагент, не содержащий экологически опасный фреон, исключается вредное воздействие фреона на природу.
В известном способе применяются центрифуги, в системах охлаждения которых используется хладагент, содержащий экологически небезопасный фреон.
5. За счет применения центрифуг, создающих во время работы уровень шума не более 58 дБ, улучшаются условия труда персонала.
При получении концентрата тромбоцитов по известному способу применяются центрифуги, имеющие уровень шума во время работы 85 дБ при измерительном расстоянии 1 м.
Описанные выше этапы производства концентрата тромбоцитов оформлены в виде технологического процесса, в котором изложена определенная последовательность технологических операций с подробным описанием действий медперсонала и указанием всей необходимой информации по специальным требованиям, режимам переработки и хранения, оборудованию, инструменту, расходным материалам и их количеству, нормам времени и т.д.
При разработке технологического процесса за основу взяты принципы оформления, компоновки и изложения, применяемые в машиностроительной технологии.
Источники информации
1. Инструкция по фракционированию консервированной крови на клеточные компоненты и плазму (утверждена Минздравом СССР 06-14/24 от 11.06.87).
2. Инструкция по применению полимерных контейнеров "Гемакон" и "Компопласт" (утверждена Минздравом СССР от 11.08.83).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА ПЛАЗМЫ И ЭРИТРОЦИТНОЙ МАССЫ | 1999 |
|
RU2151617C1 |
| СПОСОБ ЗАГОТОВКИ ЭРИТРОЦИТОВ | 2003 |
|
RU2274459C2 |
| УСТРОЙСТВО ДЛЯ УДАЛЕНИЯ ГЕЛЕЙ, МИКРОАГРЕГАТНЫХ ЧАСТИЦ И ЛЕЙКОЦИТОВ ИЗ ПРОДУКТОВ КРОВИ | 2005 |
|
RU2285543C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ НАСЛЕДСТВЕННЫМ ГЕМОХРОМАТОЗОМ | 1993 |
|
RU2082440C1 |
| Мобильное устройство для гравитационной сепарации крови и способ его применения | 2019 |
|
RU2710356C1 |
| Устройство для криоконсервирования и подготовки тромбоцитов к трансфузии | 2019 |
|
RU2715746C1 |
| Добавочный раствор для хранения концентрата тромбоцитов | 2019 |
|
RU2720487C1 |
| ПОДВИЖНЫЙ КОМПЛЕКС ЗАГОТОВКИ И СЕПАРАЦИИ КРОВИ | 2009 |
|
RU2403001C1 |
| Устройство для криоконсервирования эритроцитов и способ его применения | 2023 |
|
RU2817924C1 |
| ЦЕНТРИФУГА ДЛЯ ФРАКЦИОНИРОВАНИЯ КРОВИ | 1999 |
|
RU2140332C1 |
Изобретение относится к медицине, конкретно к трансфузионной медицине, предназначено для использования в учреждениях службы крови. Технический результат: получен концентрат тромбоцитов высокого качества и обеспечено повышение производительности и улучшение условий труда персонала, исключено вредное воздействие на природу. Донорскую кровь, предназначенную для получения концентрата тромбоцитов, заготавливают в газопроницаемые строенные пластикатные контейнеры, гарантирующие доступ кислорода к тромбоцитам, представляющие собой единую закрытую систему с предварительно залитым антикоагулянтом. Центрифугирование проводится на низкочастотной рефрижераторной центрифуге, обеспечивающей за счет плавного старта и мягкой остановки качественную сепарацию и увеличение концентрации тромбоцитов до 60 • 109 клеток в 50 - 60 мл плазмы. 4 ил., 3 табл.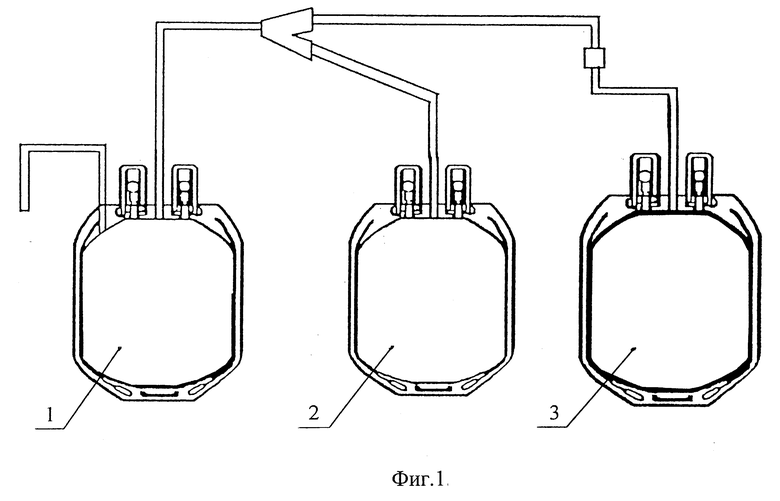
Способ получения концентрата тромбоцитов из плазмы, обогащенной тромбоцитами, заключающийся в том, что консервированную кровь центрифугируют, в результате чего она разделяется на плазму, обогащенную тромбоцитами, и эритроцитную массу, затем с помощью плазмоэкстрактора плазму, обогащенную тромбоцитами, переводят в пустой контейнер, контейнер с эритроцитной массой герметизируют, используя аппарат для запайки, и отделяют, контейнер с плазмой, обогащенной тромбоцитами, центрифугируют, в результате чего тромбоциты из плазмы оседают на дно контейнера, а над ними располагается плазма, бедная тромбоцитами, которую с помощью плазмоэкстрактора переводят в пустой контейнер, после чего контейнеры с плазмой, бедной тромбоцитами, и с концентратом тромбоцитов герметизируют, используя аппарат для запайки, разделяют и хранят контейнер с концентратом тромбоцитов при температуре 22 ± 2 oC, отличающийся тем, что донорскую кровь, предназначенную для получения концентрата тромбоцитов, заготавливают в газопроницаемые строенные пластикатные контейнеры, гарантирующие доступ кислорода к тромбоцитам, представляющие собой единую закрытую систему с предварительно залитым антикоагулянтом, а центрифугирование консервированной крови и плазмы, обогащенной тромбоцитами, производят на низкоскоростных рефрижераторных центрифугах, имеющих ротор с шестью чашками для одновременной укладки и центрифугирования двенадцати сдвоенных или строенных пластикатных контейнеров.
Авторы
Даты
1999-05-10—Публикация
1998-07-08—Подача