Изобретение относится к биотехнологии, а именно к производству биопрепаратов-пробиотиков.
В настоящее время существует целый ряд биопрепаратов, подавляющих рост патогенных и условно-патогенных бактерий: лактобактерин, бифидумбактерин, колибактерин, бактисубтил и споробактерин. Однако эти препараты нельзя применять совместно с антибиотиками.
Наиболее близким к изобретению является препарат-пробиотик "Споробактерин", содержащий биомассу Bacillus subtilis и наполнитель, который предназначен для профилактики и лечения заболеваний желудочно-кишечного тракта, дисбактериозов (1). Однако известный препарат чувствителен к антибиотикам, за исключением поломиксина, что ограничивает сферу его применения при тяжелых формах гнойно-воспалительных заболеваний, лечение которых требует совместного введения бактериального препарата и антибиотика.
Задача, решаемая изобретением, - создание нового препарата-пробиотика, применение которого возможно совместно с антибиотиками.
Результат, получаемый от использования нового препарата, выражается в повышении эффективности лечения за счет возможности сочетанного применения бактериального препарата с антибиотиками.
Это достигается тем, что в качестве основы биопрепарата используют штамм Bacillus subtilis 3H, депонированный в коллекции ГИСК им. Л.А.Тарасевича под N 248, патент N 2067616 (2). Штамм Bacillus subtilis 3H характеризуется высокой антагонистической активностью в отношении широкого спектра патогенных и условно-патогенных микроорганизмов и устойчивостью к целому ряду антибиотиков.
Препарат содержит в качестве основы живые клетки Bacillus subtilis 3H (ГИСК N 248) и наполнитель, при следующем соотношении компонентов, мас.%:
Биомасса Bacillus subtilis 3H - 1•109-5•109 живых микробных клеток в 1 мл растворителя - 92 - 95
Наполнитель - 5 - 8
В качестве растворителя можно использовать физиологический раствор, дистиллированную или кипяченую воду. В качестве наполнителя препарат может содержать 5% лактозы или 8% сахарозо-желатиновой смеси (7% сахарозы и 1% желатина). Необходимость наполнителя обусловлена его защитным действием для бактериальных клеток при дальнейшем лиофильном высушивании препарата.
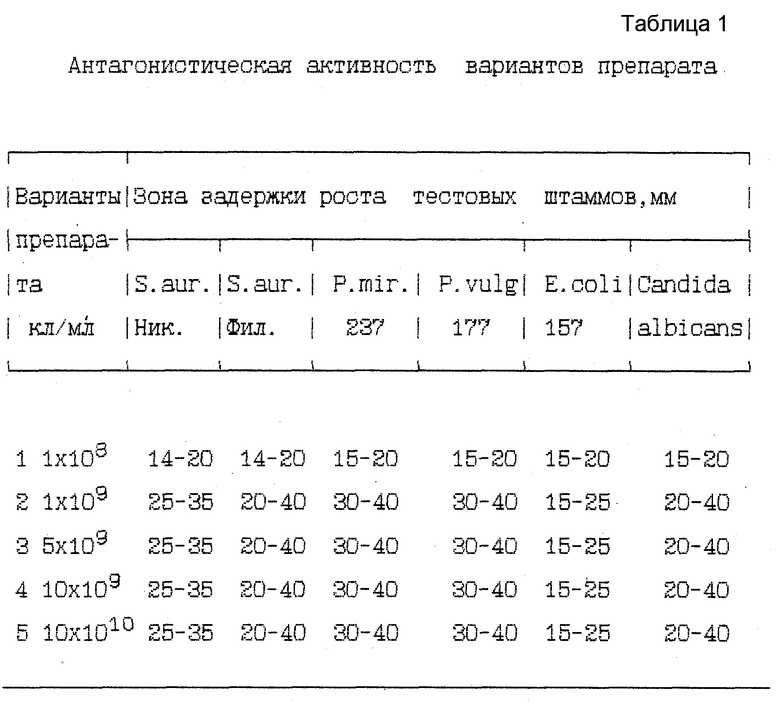
Препарат характеризуется высокой антагонистической активностью в отношении патогенных и условно-патогенных микроорганизмов. Антагонистическую активность проверяли методом отсроченного антагонизма (табл. 1).
Препарат характеризуется безвредностью (таб. 2) и устойчивостью к ряду антибиотиков (табл. 3).
Пример. На основе штамма B.subtilis 3H с типичными морфологическими, культуральными, биохимическими свойствами приготовлены 5 вариантов препарата с различным содержанием микробных клеток в составе препарата.
Вариант 1. Препарат, содержащий, мас.%:
Биомасса B. subtilis 3H 1•108 живых микробных клеток в 1 мл физиологического раствора - 92
Наполнитель - сахарозо-желатиновая смесь - 8
Вариант 2. Препарат, содержащий, мас.%:
Биомасса B. subtilis 3H 1•109 живых микробных клеток в 1 мл физиологического раствора - 93
Наполнитель - сахарозо-желатиновая смесь - 7
Вариант 3. Препарат, содержащий, мас.%:
Биомасса B. subtilis 3H 5•109 живых микробных клеток в 1 мл физиологического раствора - 94
Наполнитель - сахарозо-желатиновая смесь - 6
Вариант 4. Препарат, содержащий, мас.%:
Биомасса B. subtilis 3H 5•1010 живых микробных клеток в 1 мл физиологического раствора - 95
Наполнитель - сахарозо-желатиновая смесь - 5
Вариант 5. Препарат, содержащий, мас.%:
Биомасса B. subtilis 3H 5•1010 живых микробных клеток в 1 мл физиологического раствора - 95
Наполнитель - лактоза - 5
Изготовленные варианты препарата разливали в стерильные ампулы, высушивали лиофильно, ампулы запаивали. Проверяли безвредность полученных вариантов препарата на лабораторных животных, специфическую антагонистическую активность в отношении тест-культур - представителей различных групп патогенных и условно-патогенных микроорганизмов.
Для определения безвредности содержимое ампулы разводили в 0,5 мл физиологического раствора и вводили эту дозу перорально мышам. Для каждого варианта опыта использовали не менее 10 мышей массой 15 - 16 г. Препарат считали безвредным, если все мыши оставались живыми в течение пяти суток наблюдения и ни у одной из них не выявлено заболевания.
Для определения специфической активности исследовали антагонистическую активность вариантов препарата в отношении тест-культур. Исследование осуществляли методом отсроченного антагонизма. Для этого содержимое ампулы растворяли в 1 мл физиологического раствора. Полученную взвесь высевали штрихом по диаметру чашки Петри с агаризованной средой Гаузе N 2. Посевы инкубировали в термостате при 37oC в течение 72 ч. Затем к выросшей культуре подсевали штрихом тест-микроорганизмы (500-миллионные суспензии суточных культур в физиологическом растворе). Учет результатов проводили через 18 часов инкубирования при 37oC по величине зон отсутствия роста тест-культур. Контролем роста тест-культур служило параллельное выращивание их на чашках с агаризованной средой Гаузе N 2 без исследуемой культуры.
Чувствительность препарата к антибиотикам определяли с помощью стандартных дисков, пропитанных антибиотиками. В чашку Петри с МПА наливали 1 мл суспензии суточной культуры штамма в 0,9%-ном растворе натрия хлорида, содержащей 1•109 микробных клеток, и равномерно распределяли по поверхности агара. Избыток удаляли пастеровской пипеткой. На поверхности засеянного агара пинцетом раскладывали диски с антибиотиками, по 5 дисков на каждую чашку. Чашки выдерживали в термостате при температуре (37±1)oC в течение (18±2) ч, после чего измеряли зоны задержки роста вокруг дисков, включая диаметр самого диска.
Полученные результаты испытания вариантов препарата представлены в таблицах 1 - 3.
Из данных таблицы 1 следует, что оптимальным количеством живых микробных клеток в одной дозе препарата является 1•109 - 5•109. Дальнейшее увеличение количества микробных клеток не изменяет существенным образом антагонистическую активность препарата в отношении тест-культур микроорганизмов.
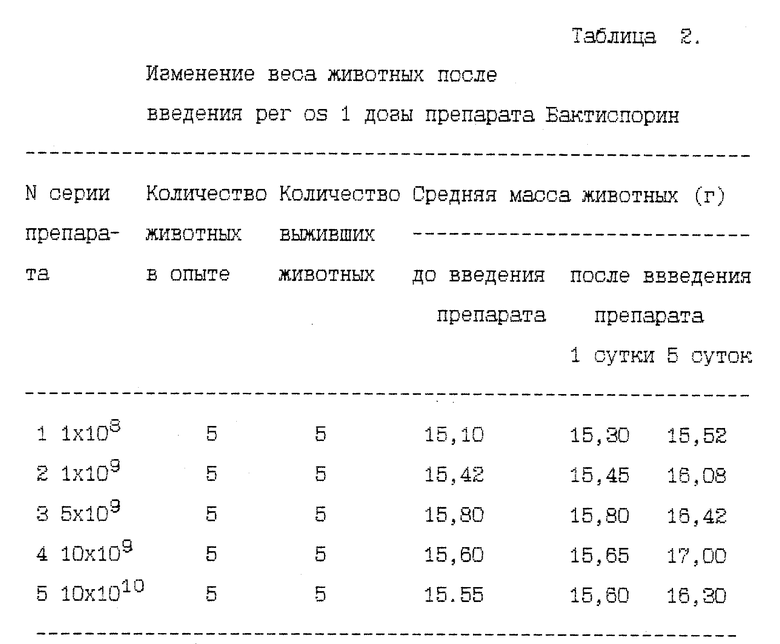
Проведено изучение безвредности различных вариантов препарата на белых аутбредных мышах при введении per os 1 дозы. Наблюдение за изменением веса животных осуществляли в течение 5 суток. Полученные данные представлены в таблице 2.
Испытание показало, что все животные остались живыми, их первоначальная масса увеличивалась, отсутствовали какие-либо признаки заболевания.
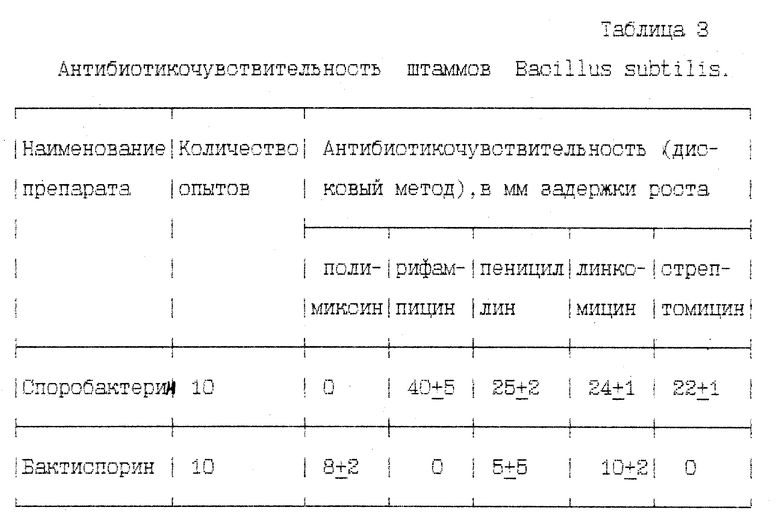
Проведено сравнительное изучение антибиотикоустойчивости препаратов Бактиспорин и Споробактерин. Полученные данные представлены в таблице 3.
Полученные данные свидетельствуют, что новый препарат обладает выраженной антибиотикоустойчивостью.
Проведены клинические испытания препарата в детском отделении городской клинической больницы N 6 г. Уфы. Показана его абсолютная безвредность, хорошая переносимость и высокая эффективность.
Пример 1. Пациент Давлетбаев К., 1995 года рождения. Находился на стационарном лечении по поводу ОРВИ, осложненной острой гнойной ангиной. Сопутствующая патология: ассоциированный дисбактериоз кишечника, субкомпенсированная форма. При поступлении жалобы (матери) на повышение температуры тела, вялость. Практически с рождения у мальчика наблюдались выраженные изменения характеристик стула в виде разжижения кала и наличие в нем патологических примесей (слизи, комочков непереваренной пищи). Последнее обострение клинических проявлений дисбактериоза было обусловлено присоединением ОРВИ и в последующем острой гнойной ангины. Учитывая выше описанную симптоматику, в комплексную терапию, наряду с назначением курса антибиотика, был включен бактиоспорин по 1 дозе 2 раза в день в течение 10 дней.
Со второго для приема препарата было отмечено уменьшение проявлений болезненности по ходу толстого кишечника (при пальпации). С третьего дня стул стал практически полностью переваренным.
Пример 2. Больной Сакаев М., 1995 года рождения.
Находился на стационарном лечении с диагнозом: ОРВИ. Сопутствующие заболевания: дисбактериоз кишечника ассоциированный, субкомпенсированная форма, атопический дерматит. Проявление диспептического синдрома в виде разжижения стула, появления в кале слизи, непереваренных комочков пищи отмечаются с 4-х месяцев после перевода ребенка на искусственное вскармливание. При осмотре живот умеренно вздут, отмечается болезненность и урчание по ходу толстого кишечника, стул желто-зеленого цвета с большим количеством слизи. Жалобы на вялость, снижение аппетита. В связи с обострением дисбактериоза назначен бактиспорин по 1 дозе 2 раза в день в течение 10 дней.
С 4-го дня приема аппетит и самочувствие нормализовались. С 6-го дня полностью исчезли явления метеоризма, стул стал гомогенным.
Пример 3. Больной Климов Д., 1994 года рождения.
Находился на стационарном лечении с диагнозом: ОРВИ, обструктивный бронхит. Сопутствующие заболевания: атопический дерматит, пищевая сенсибилизация. Дисбактериоз кишечника, субкомпенсированная форма. В связи с обструктивным бронхитом мальчик получил курс ампицилина, на фоне которого у ребенка появился диспептический синдром: периоды тошноты, спонтанные боли в животе, разжижение стула, в кале появились комочки слизи. Таким образом, в период реконвалесценции обструктивного бронхита назначен бактиспорин по 1 дозе 2 раза в день в течение 10 дней.
К третьему дню приема восстановился аппетит, кожные проявления дерматита не нарастали, а интенсивность зуда даже несколько уменьшилась. К четвертому дню стул стал полностью переваренным, а к шестому дню исчезли явления метеоризма.
Таким образом, проведенные исследования препарата Бактиспорин показали, что он безвреден, характеризуется высокой антагонистической активностью в отношении тестовых штаммов патогенных и условно-патогенных микроорганизмов, обладает выраженной антибиотикоустойчивостью и обладает лечебным действием.
Применение: лечебно-профилактический препарат Бактиспорин используют при расстройствах желудочно-кишечного тракта, дисбактериозах, ферментной недостаточности органов пищеварения, гнойных инфекция, пищевой аллергии, для лечения хирургической инфекции мягких тканей, для профилактики хирургической инфекции при травмах и оперативных вмешательствах.
Источники информации:
1. Споробактерин сухой, ВФС 42-371ВС-92 утв. 18.12.92.
2. Патент РФ N 2067616, кл. C 12 N 1/20, 10.10.96.
Изобретение предназначено для коррекции микрофлоры желудочно-кишечного тракта при дисбактериозах, ферментной недостаточности органов пищеварения, гнойных инфекциях, пищевой аллергии, для лечения хирургической инфекции мягких тканей, для профилактики хирургической инфекции при травмах и оперативных вмешательствах. Биопрепарат содержит в качестве основы антибиотикоустойчивый антагонистически активный штамм Bacillus subtilis 3H (ГИСК 248) и наполнитель. Наполнитель содержит 5% лактозы или 8% сахарозожелатиновой смеси. Препарат характеризуется высокой антагонистической активностью в отношении широкого спектра патогенных и условно-патогенных микроорганизмов и устойчивостью к целому ряду антибиотиков. 3 табл.
Лечебно-профилактический биопрепарат, включающий биомассу штамма Bacillus subtilis 3H (ГИСК N 248), отличающийся тем, что он дополнительно содержит наполнитель при следующем соотношении компонентов, мас.%:
Биомасса штамма Bacillus subtilis 3H (ГИСК N 248) - живых микробных клеток - (1 - 5) • 109 в 1 мл растворителя - 92 - 95
Наполнитель - 5 - 8
| ШТАММ БАКТЕРИЙ BACILLUS SUBTILIS, НЕСУЩИЙ СВОЙСТВО АНТИБИОТИКОРЕЗИСТЕНТНОСТИ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРЕПАРАТА "БАКТИСПОРИН" | 1995 |
|
RU2067616C1 |
Авторы
Даты
1999-05-20—Публикация
1997-01-23—Подача