Изобретение относится к области прикладной биотехнологии, а именно к способам получения липосомальных препаратов для лечения и профилактики заболеваний человека и животных.
Известны способы получения липосомальных препаратов путем диспергирования компонентов в растворителе и последующего получения липосом, имеющие различные модификации (Liposomes: a practical approach. Ed. News R.R.C., IRL Press, Oxford, 1989, pp. 1-142).
При физическом диспергировании фосфолипиды высушивают на твердой подложке и затем диспергируют в водной среде, содержащей лекарственные вещества. В этих условиях липиды отслаиваются от подложки и образуют замкнутые многослойные липосомы с включенным во внутренний объем лекарственным веществом. После получения мультиламеллярных везикул получает липосомальные лекарственные препараты с улучшенными свойствами путем их обработки ультразвуком, микроэмульгаторами, замораживанием-оттаиванием, Ca++-индуцированным слиянием или иными методами (пат. США N 4927637, кл. A 61 K 37/22, 1990; пат. США N 4883665, кл. A 61 K 37/22, 1990; заявка РСТ N 89/03679, кл. A 61 K 37/22, 1989; пат. Японии N 201117, кл. A 61 K 9/10, 1988; Михайлова С. Фармация, 1988, т. 38, N 6, с. 24-30).
При использовании способа диспергирования с помощью растворителя фосфолипиды растворяют в органическом растворителе, который затем приводят в контакт с водной фазой, содержащей лекарственные препараты, которые должны быть включены в липосомы (Lasic D.D. Les liposomes. La Recherche. 1989. v. 20, N 212, p. 904-913).
При использовании способа детергентной солюбилизации фосфолипиды приводят в контакт с водной фазой через посредник - детергент, который ассоциирован с фосфолипидными молекулами и служит для экранирования гидрофобных частей молекул от воды. При удалении детергента путем диализа или хроматографии происходит образование моноламеллярных липосом (пат. США N 5019394, кл. A 61 K 9/127, 1991).
Недостатком данных способов является: получение водных нестабильных дисперсий липосомальных препаратов, которые должны быть стабилизированы лишь с помощью дополнительных процессов лиофилизации или распылительной сушки, сложность в изготовлении, низкий процент включения биологически активных веществ и лекарств в липосомы, что исключает возможность получения препаратов в промышленных объемах.
Наиболее близким по технической сущности и достигаемому результату к заявляемому способу является способ получения липосомальных лекарственных препаратов путем приготовления раствора лекарственного средства (ЛС) в смеси воды, этилового спирта, поверхностно-активного вещества (ПАВ), липидов и введении в него многоступенчато при интенсивном перемешивании буферного раствора. В ходе процесса образуется дисперсия липосом, содержащих ЛС, в водно-спиртовом растворе липосом, содержащих ЛС (Евр. пат. N 0158441, кл. A 61 K 9/50, 1985).
Недостатками прототипа являются возможность получения препаратов только с растворимыми в воде ЛС и растворимыми в этиловом спирте липидами, относительно невысокая (около 40%) степень включения ЛС в липосомы, многостадийность процесса, получение в виде конечного продукта неудобной при транспортировке, хранении и применении жидкой лекарственной формы.
Задачей настоящего изобретения является разработка более универсального и технологически простого способа получения липосомальных препаратов, содержащих биологически активные вещества, лекарства и/или антигены, повышение технологичности способа и обеспечение возможности получения различных форм липосомальных лекарственных препаратов (ЛЛП) в промышленных масштабах.
Поставленная задача решается путем смешивания биологически активного вещества (БАВ), фосфолипидов, органического растворителя, способного растворять фосфолипиды, и порошкообразного наполнителя в одной емкости с последующим удалением растворителя в условиях пониженного давления (вакуума) при сохраняющемся постоянном перемешивании. В результате получают сухой порошкообразный препарат биологически активного вещества, при растворении которого в воде или в биологических жидкостях организма образуется липосомальный препарат.
В качестве фосфолипидов могут быть использованы как индивидуальные фосфолипиды, так и их смеси, полученные из растительного, животного или биотехнологического сырья.
В качестве органических растворителей могут быть использованы хлороформ, метанол, этанол, гексан, эфир, бензол и другие растворители, в которых могут растворяться используемые фосфолипиды.
Фосфолипиды и растворитель могут вводиться в смесь в виде раствора фоосфолипидов в данном растворителе.
В качестве сухих порошкообразных наполнителей могут быть использованы сахара и/или полисахариды (глюкоза, лактоза, декстраны и т.п.), полиолы (сорбит, ксилит и другие), соли (поваренная соль и другие) и другие порошкообразные вещества.
Состав конкретных смесей определяется экспериментальным путем исходя из особенностей смешиваемых компонентов и заданных характеристик конечного продукта.
Липосомальные препараты, полученные по предлагаемому способу, как показала экспериментальная проверка, пригодны для лечения и профилактики различных заболеваний.
Сущность и промышленная применимость изобретения иллюстрируется следующими примерами.
Пример 1 (по прототипу).
В емкость поместили 500 мг яичного лецитина, 400 мг этанола, 100 мг водного раствора (500 мг/мл) БАВ - глюкозы и 100 мг ПАВ - спана-80 и перемешали. К полученной композиции добавляли дробно 4 мл 50 mM фосфатного буфера с pH 7.4 при интенсивном встряхивании в ходе процесса добавления, а также через 1, 15 и 30 минут после добавления буферного раствора.
Затем к полученной суспензии добавили еще 6 мл вышеуказанного буфера и энергично встряхнули сразу после добавления, а также через 1, 15 и 30 минут после указанной операции. Полученная взвесь липосом показана на фото фиг. 1. Содержание глюкозы в липосомах составило 35±5% от исходного.
Пример 2 (по предлагаемому способу).
В емкость при перемешивании поместили 800 мг БАВ - глюкозы, 200 мг яичного лецитина и 700 мг этанола и при перемешивании со скоростью 50 об/мин при 37oC подвергли смесь в течение часа воздействию вакуума (пониженного до 0,2 ати давления).
Было получено 1.0 г сухого порошка с влажностью 0.8%. Порошок диспергировали в 10 мл дистиллированной воды. Полученная взвесь липосом (фото фиг. 2) содержала в липосомах 75±7% глюкозы от исходного количества, что вдвое больше чем при использовании способа-прототипа по степени включения и в 15 раз больше по количеству включенного лекарственного вещества.
Пример 3 (использование гидрофобного БАВ).
В емкость помещали 50 мг бета-каротина, 750 мг сорбита и раствор 200 мг яичного лецитина в 2000 мл хлороформа, тщательно перемешивали и отгоняли растворитель под вакуумом в условиях, описанных в примере 2.
Было получено 1.0 г сухих липосом. Порошок диспергировали в 10 мл воды и с помощью спекрофотометрии определяли содержание бета-каротина в липосомах. Анализ показал совпадение пиков при длиннах волн 270 нм (липосомальный пик) и 436 нм (пик бета-каротина), что свидетельствует о полном включении БАВ в липосомы.
При проведении процесса по методике прототипа в полученных липосомах БАВ присутствовало в следовых (менее 1% от исходного) количествах.
Пример 4 (масштабирование процесса получения липосомальных препаратов).
а). Получение липосомального препарата в малом объеме.
Смешали 0.2 г кристаллического бета-каротина, 1.0 г суммарных фосфолипидов из семян подсолнечника, 8.8 г сорбита и 5.0 г хлороформа в герметически закрывающейся емкости объемом 15 см3 при температуре 37oC. Емкость закрыли и начали откачивать воздух до достижения вакуума 0.1 атм. Сушку проводили при вакуумировании в течение 1 часа при температуре 37oC и постоянном перемешивании со скоростью 50 об/мин. В результате получили 10.0 г сухого мелкодисперсного порошка с влажностью 0.7%.
б). Получение липосомального препарата в промышленном объеме.
Смешали 0.2 кг кристаллического бета-каротина, 1.0 кг суммарных фосфолипидов из семян подсолнечника, 8.8 кг сорбита и 5.0 кг хлороформа в герметически закрывающейся емкости объемом 0.5 м3, снабженной водяной рубашкой. Емкость закрыли герметично и начали откачивать воздух до достижения вакуума 0.1 атм. Сушку проводили при вакуумировании в течение 5 часов при температуре 37oC и постоянном перемешивании со скоростью 50 об/мин. В результате получили 10.0 кг сухого мелкодисперсного порошка с влажностью 0.7%.
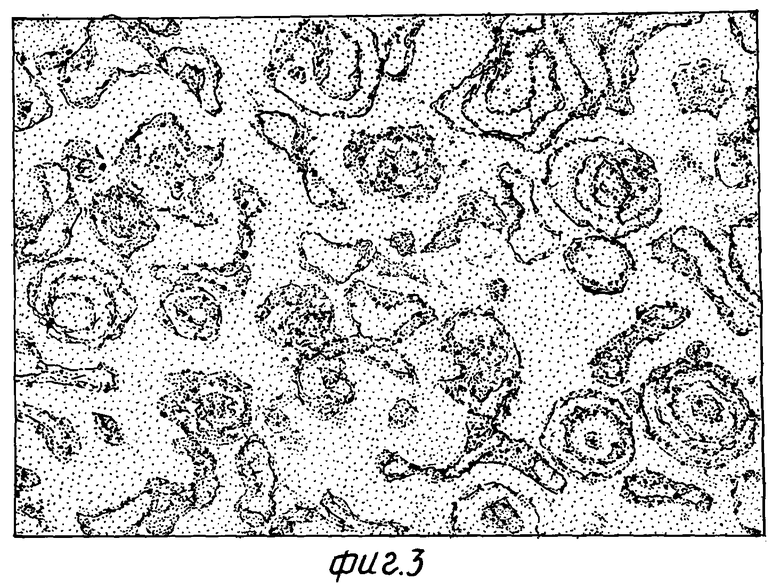
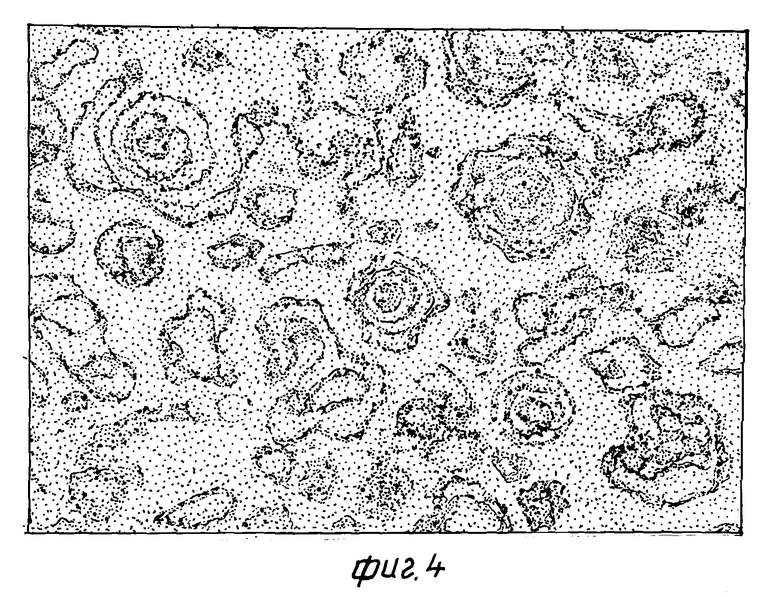
По 1.0 г порошка, полученного в малом и промышленных объемах, растворяли в 10 мл дистиллированной воды, оба липосомальных препарата представляли собой взвесь моно- и мультиламеллярных липосом (фиг. 3 и 4).
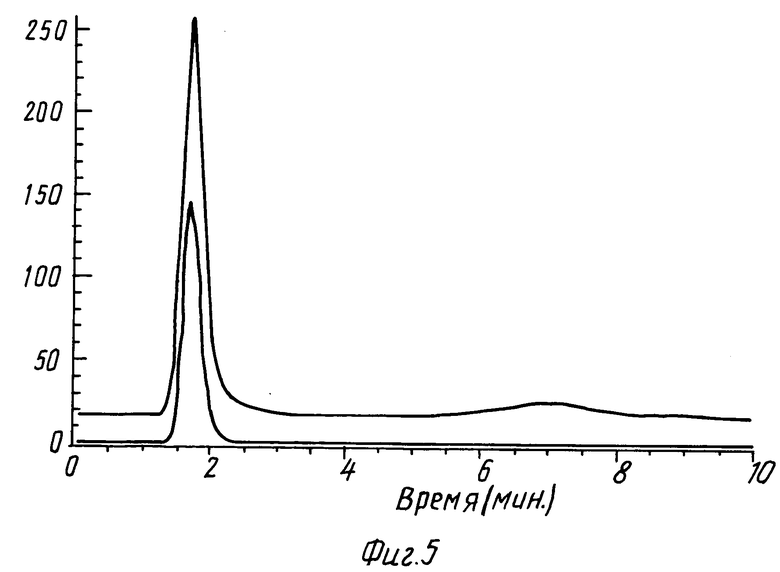
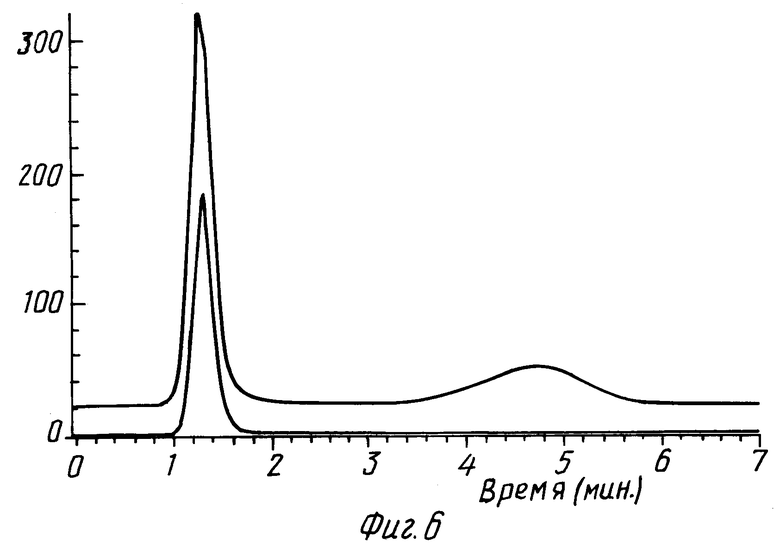
Разделили оба препарата на липосомальную и нелипосомальную фракции с помощью гельпроникающей хроматографии. Детекцию проводили при длинах волн 270 нм (липосомальный пик) и 436 нм (пик бета-каротина). В каждом препарате весь бетакаротин был связан с липосомами, о чем свидетельствует полное совпадение на хроматограммах пика бета-каротина (1) и пика липосом (2) (фиг. 5 и 6).
Определили содержание бета-каротина в сухих препаратах, полученных по методикам а) и б) спектрофотометрическим способом (Бета-каротин кристаллический. ТУ 9353-041-00481134-96). Содержание бета-каротина было одинаковым и составляло 20±1 мг на 1 г липосом в каждом препарате.
Таким образом, при масштабировании процесса получения липосомального препарата бета-каротина в 1000 раз получен препарат бета-каротина, аналогичный препарату бета-каротина, полученному в малых объемах, по влажности, содержанию бета-каротина в сухом препарате и по степени включения бета-каротина в липосомы.
Пример 5 (исследование влияния составов фосфолипидов на качество липосомальных препаратов бета-каротина).
С использованием различных образцов фосфолипидов в условиях примера 3а были получены 4 образца липосомального препарата бета-каротина.
В качестве фосфолипидов препараты содержали:
1. Яичный лецитин (препарата N 1).
2. Лецитин, холестерин и додецилфосфат в молярном соотношении 10:2:1 (препарат N 2).
3. Суммарные фосфолипиды из мозга крупного рогатого скота (препарат N 3).
4. Суммарные фосфолипиды из микроорганизмов E.coli штамм М-17 (препарат N 4).
Характеристика полученных препаратов приведена в табл. 1.
Данные табл. 1 показывают, что состав фосфолипидов не оказывает влияния на качество липосомальных препаратов бета-каротина, т.е. способ является универсальным и для получения препаратов могут быть использованы отдельные фосфолипиды, искусственные смеси фосфолипидов, суммарные фосфолипиды из сырья различного происхождения.
Пример 5 (влияние концентрации фосфолипидов на качество липосомальных препаратов).
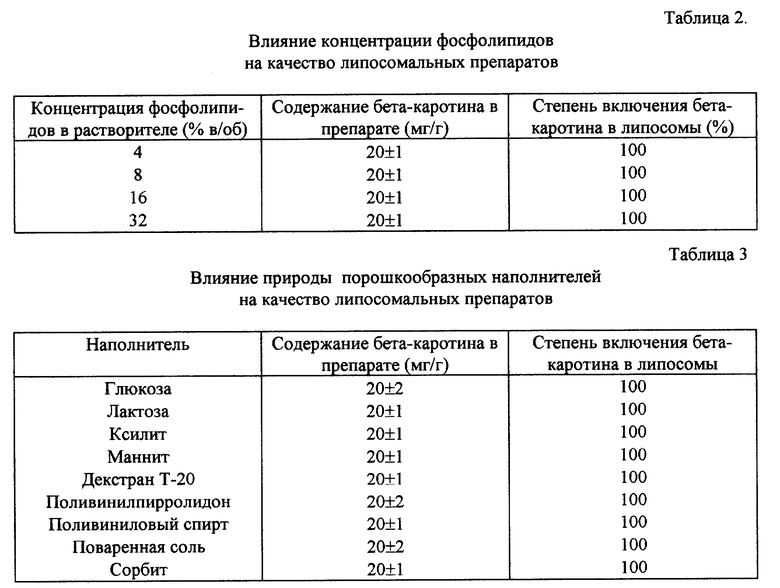
В условиях примера 3а были получены 4 образца липосомального препарата бета-каротина с использованием следующих концентраций фосфолипидов по оотношению к органическому растворителю: 4%, 8%, 16%, 32% (вес/объем). (32% является пределом растворимости суммарных фосфолипидов из семян подсолнечника в хлороформе при температуре 20±2oC). Определяли содержание бета-каротина в полученных сухих препаратах сразу после изготовления и степень включения бета-каротина в липосомы.
Результаты анализов представлены в табл. 2.
Данные табл. 2 показывают, что при использовании практически любых растворов фосфолипидов в пределах их растворимости в органическом растворителе могут быть получены кондиционные липосомальные препараты.
Пример 6 (влияние природы порошкообразных наполнителей на качество липосомальных препаратов).
По методике примера 3а были получены образцы липосомального препарата бета-каротина с использованием различных порошкообразных наполнителей.
Характеристика полученных препаратов приведена в табл. 3.
Данные табл. 3 показывают возможность получения кондиционных липосомальных препаратов при использовании носителей разной природы.
Пример 7 (исследование эффективности липосомальных препаратов биологически активных веществ, лекарств и антигенов при лечении и профилактике различных заболеваний).
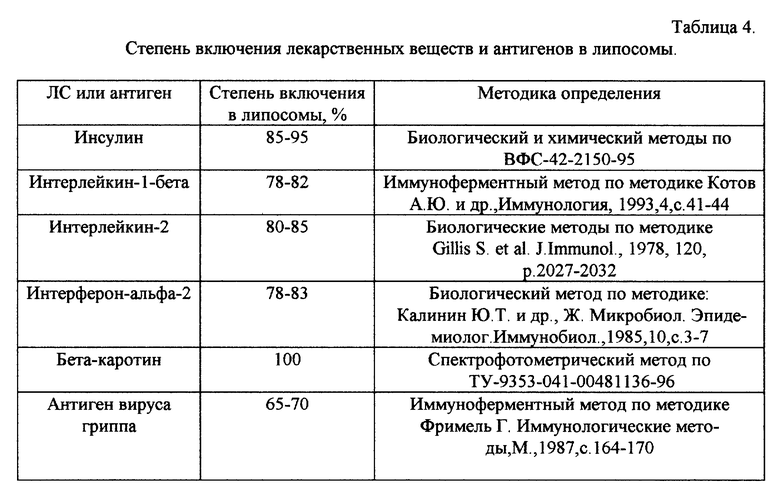
По методике примера 3а были приготовлены липосомальные препараты инсулина (100 ED/г), бета-каротина (20 мг/г), интерферона альфа-2 (3.0•106 ED/г), интерлейкина 1-бета (1 мг/г), интерлейкина-2 (36 млн ED/г) и инактивированной гриппозной вакцины из штамма вируса гриппа A/Nib-31/93/814 (H3N2) (30 мг/г гемаглютинина).
Исследовали степень включения указанных лекарственных веществ и вирусов в липосомы. Результаты исследования представлены в табл. 4.
Данные табл. 4 показывают, что предлагаемый способ обеспечивает высокий процент включения ЛС и антигенов в липосомы.
Лечебную и профилактическую эффективность полученных препаратов изучали на моделях диабета (инсулин), гриппозной инфекции (бета-каротин, интерлейкин 1-бета, гриппозная вакцина), индуцированных опухолей (бета-каротин), инфекционного процесса, вызванного вирусом везикулярного стоматита в культуре клеток человека L-41 (интерферон) и в клинических условиях при лечении токсикозов, вызванных цитостатиками при лечении онкологических больных (бета-каротин).
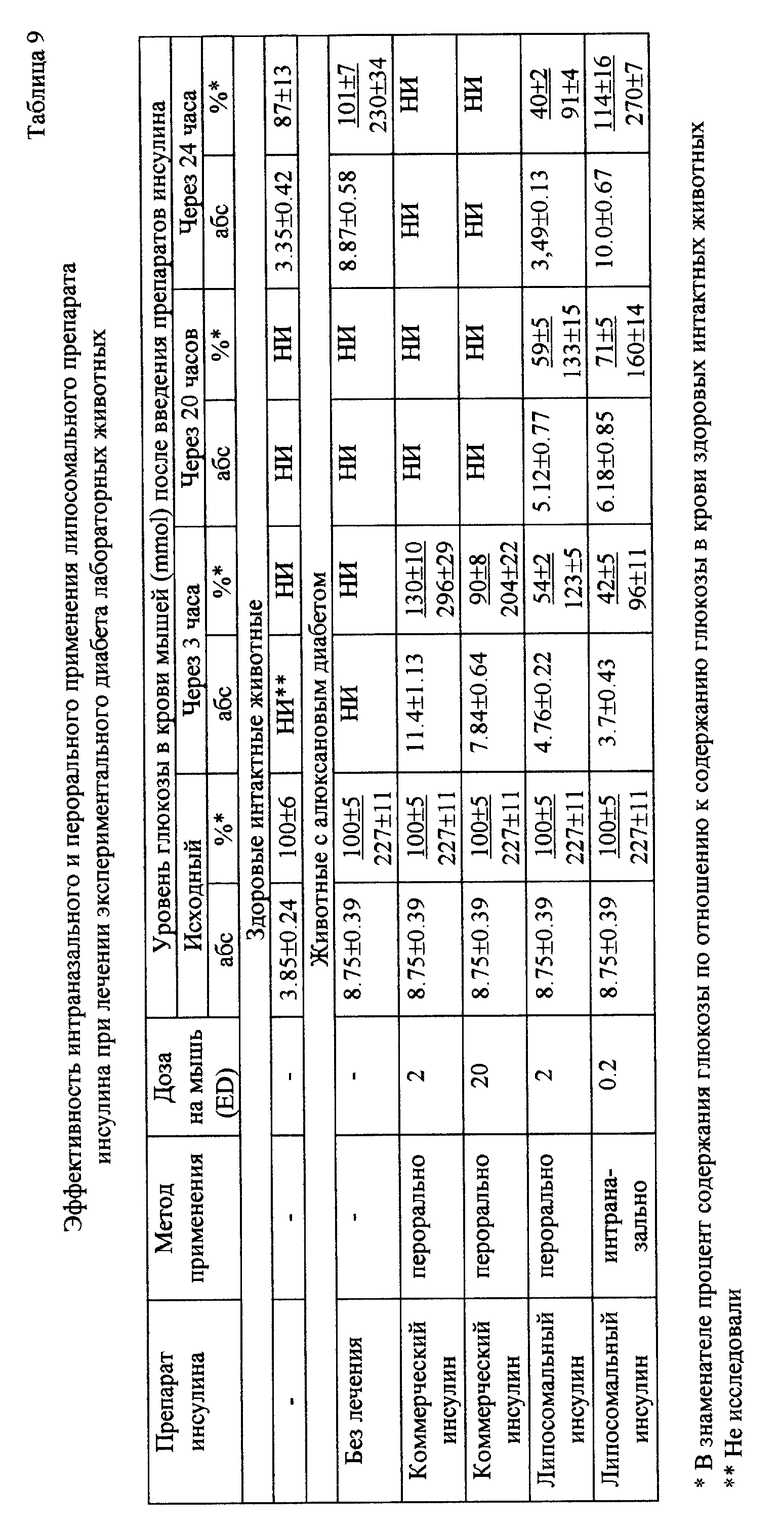
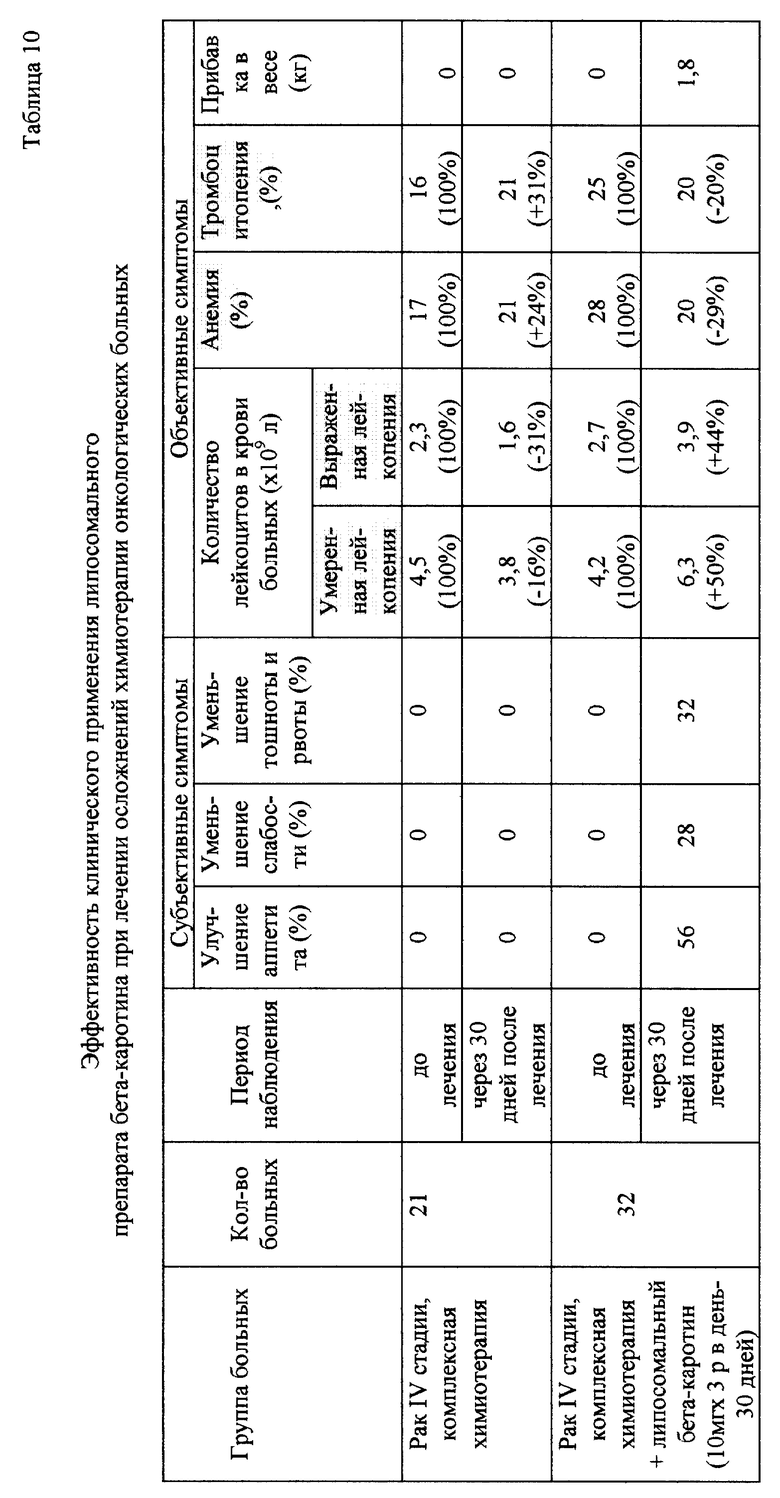
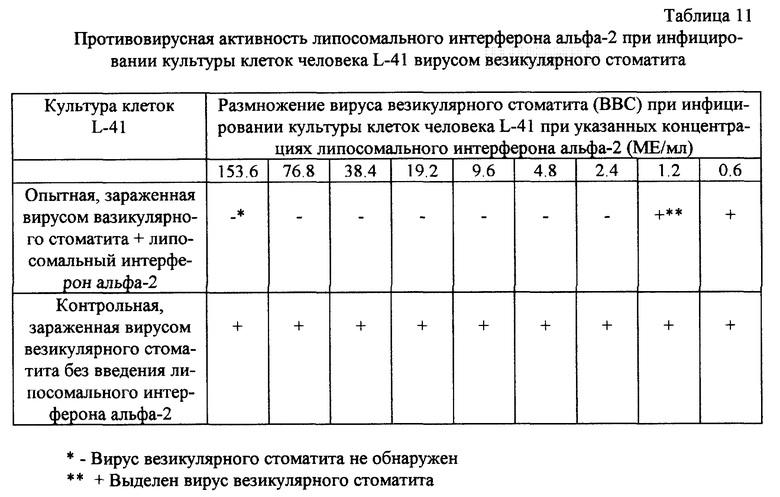
Результаты исследований представлены в табл. 5-11.
Результаты исследования эффективности липосомального препарата инсулина, полученного по предлагаемому способу показали, что полученный препарат обладает хорошей лечебной эффективностью и обеспечивает нормализацию уровня глюкозы в крови животных, больных диабетом, в течение 24 часов после однократного перорального применения в дозе 2ED на животное. Однократное интраназальное введение липосомального инсулина в дозе 0,2 ED/мышь нормализует уровень глюкозы у животных с диабетом в течение 20 часов после введения. Коммерческий препарат инсулина при пероральном применении в дозах 2ED и 20ED на животное не оказывал действия на снижение уровня глюкозы у экспериментальных животных, больных диабетом.
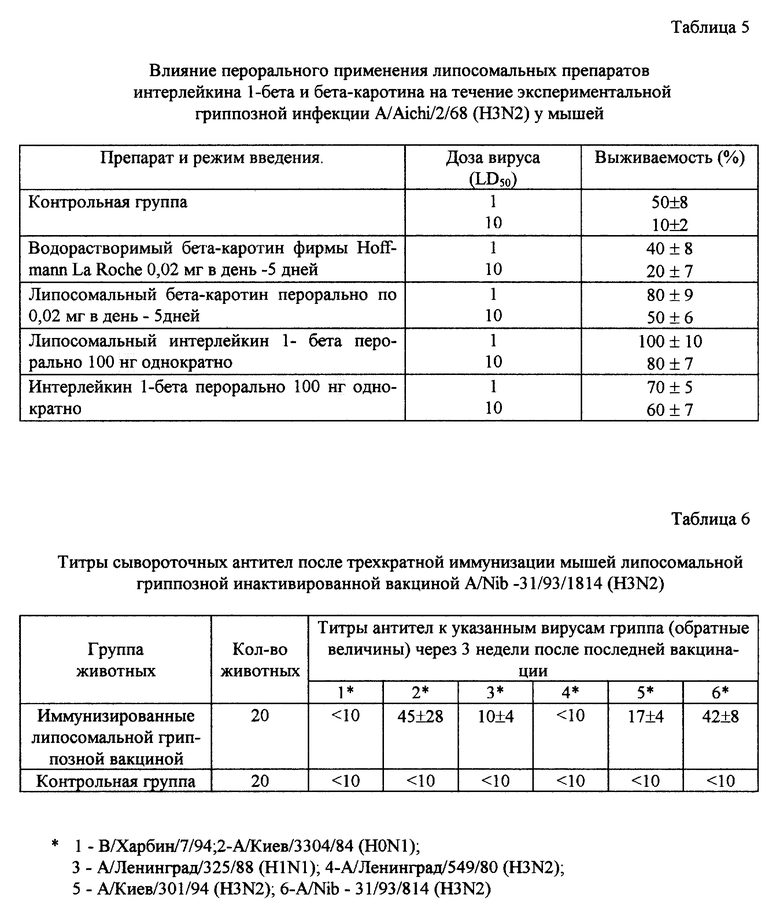
Липосомальный интерлейкин 1-бета обладает выраженной профилактической эффективностью и при однократном пероральном применении в дозе 100 нг защищает 80-100% животных от летательной гриппозной инфекции. Липосомальный бета-каротин обладает хорошей профилактической эффективностью и при пероральном применении в дозе 0,02 мг в день в течение 5 дней защищает 50-80% животных от смертельного вируса гриппа. Коммерческие нелипосомальные препараты интерлейкина 1-бета и бета-каротина обладают более слабой защитной эффективностью, чем их липосомальные аналоги.
Анализ эффективности иммунизации лабораторных животных липосомальной гриппозной инактивированной вакциной показал, что после пероральной иммунизации мышей вакциной на основе вируса гриппа A/Nib-31/93/814 (H3N2) максимальные титры антител к гомологичному вирусу составляли 1:42. Кроме этого, иммунизация липосомальной вакциной на основе вируса группы A2 (H3N2) приводила к формированию иммунитета и к гетерологичным вирусам группы A (Киев) 3304/84 (H1N1) и A/Ленинград/325/88 (H0N1), что свидетельствует о высокой иммуногенности липосомальной вакцины.
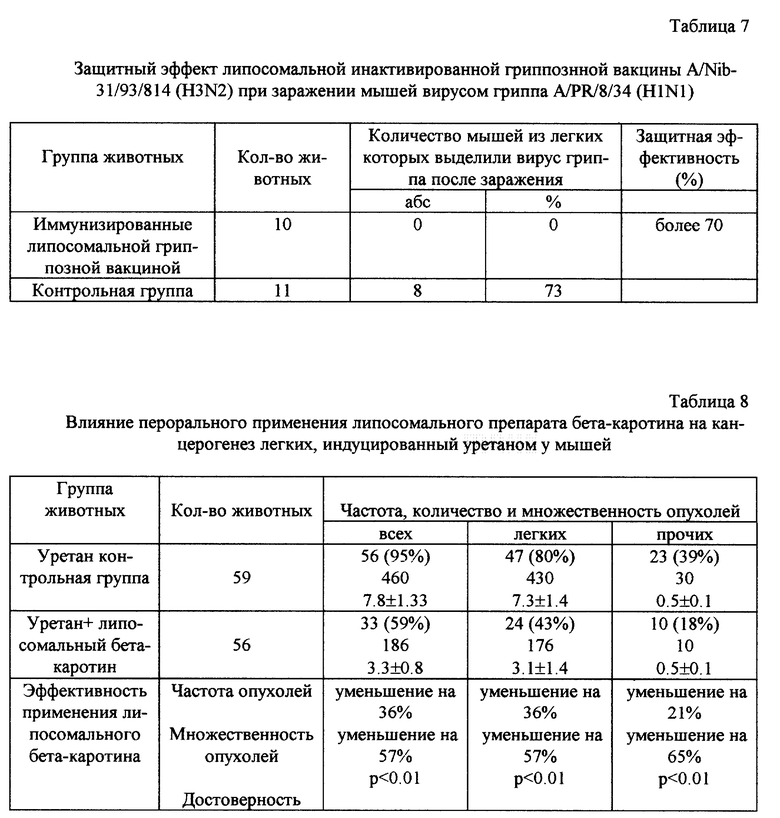
Липосомальная гриппозная инактивированная вакцина на основе штамма вируса гриппа A/Nib-31/93/814 (H3N2) обладала выраженной защитой эффективностью и обеспечивала защиту от заражения гетерологичным вирусом гриппа A/PR/8/34/ (H0N1).
Результаты профилактического применения липосомального препарата бета-каротина, изготовленного по предлагаемому способу, при индуцированном раке легких у мышей показывают, что профилактическое пероральное применение липосомального бета-каротина обеспечивает уменьшение частоты возникновения злокачественных опухолей, индуцированных канцерогеном уретаном, на 36% и множественности опухолей на 57%, в том числе частоты возникновения и множественности опухолей легких на 37% и 57% и частоты возникновения и множественности прочих опухолей на 21% и 65% соответственно.
Данные по противовирусной активности липосомального препарата интерферона альфа-2 при инфицировании культуры клеток человека L-41 вирусом везикулярного стоматита показывает, что липосомальный интерферон обладает выраженной активностью и инактивирует вирус везикулярного стоматита в культуре клеток в минимальной концентрации 2,4 ME интерферона в 1 мл.
Данные клинического изучения эффективности применения липосомального препарата бета-каротина, изготовленного по предлагаемому способу, при лечении осложнений химиотерапии онкологических больных показывают, что применение липосомального бета-каротина в дозе 10 мг три раза в день в течение 30 дней существенно улучшает субъективные и объективные симптомы осложнений комплексной химиотерапии больных раком IV стадии. При применении липосомального бета-каротина наблюдается улучшение аппетита у 56% больных, уменьшение слабости у 28% больных, изменение частоты тошноты и рвоты у 32% больных. Количество лейкоцитов в крови больных, на фоне лечения липосомальным бета-каротином, увеличивается на 50% при умеренной лейкопении и на 44% при выраженной лейкопении. У больных уменьшаются случаи анемии (на 29%) и тромбоцитопении (на 20%). Через 30 дней после применения липосомального бета-каротина больные поправились в среднем на 1.8 кг.
Данные представленные в примерах, показывают, что предлагаемый способ значительно упрощает и удешевляет приготовление липосомальных препаратов, содержащих различные типы БАВ и других ЛС, обеспечивает высокий процент включения их в липосомы и создает возможность масштабирования процесса в промышленном производстве.
Лекарственные и вакцинные препараты, изготовленные по предлагаемому способу, обладают высокой лечебной и профилактической активностью при различных заболеваниях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА БЕТА-КАРОТИНА, ДИСПЕРГИРУЕМОГО В ВОДЕ | 1996 |
|
RU2102073C1 |
| КОСМЕТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2116778C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМАЛЬНЫХ ПРЕПАРАТОВ | 2002 |
|
RU2217129C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУХИХ ЛИПОСОМАЛЬНЫХ ПРЕПАРАТОВ (ВАРИАНТЫ) | 2009 |
|
RU2437649C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТОЧУВСТВИТЕЛЬНЫХ ЛИПОСОМ | 2007 |
|
RU2357724C1 |
| ЛЕКАРСТВЕННАЯ ФОРМА СПЕЦИФИЧЕСКОГО ИММУНОБИОЛОГИЧЕСКОГО ЛЕКАРСТВЕННОГО СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИЧ ИНФЕКЦИИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2600031C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОРАЛЬНОЙ ФОРМЫ СУБСТАНЦИИ, СОДЕРЖАЩЕЙ ИНСУЛИН | 2022 |
|
RU2818017C2 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ОЛИГОПЕПТИДНОГО ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2561582C2 |
| Способ получения липосомальной косметической сыворотки в сухой лиофилизированной форме для ухода за кожей лица, шеи и зоны декольте | 2023 |
|
RU2825130C1 |
| ЛИПОСОМЫ, СОДЕРЖАЩИЕ ОЛИГОПЕПТИДЫ - ФРАГМЕНТЫ ОСНОВНОГО БЕЛКА МИЕЛИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2009 |
|
RU2448685C2 |

Изобретение относится к области прикладной биотехнологии. Липосомальные препараты получают путем смешивания в емкости биологически активного вещества, фосфолипидов, растворителя и порошкообразного наполнителя и после достижения однородности массы растворитель при перемешивании отгоняют в условиях пониженного давления. Предлагаемый способ значительно упрощает и удешевляет приготовление липосомальных препаратов, обеспечивает высокий процент включения в липосомы биологически активных веществ. 1 з.п. ф-лы, 11 табл., 6 ил.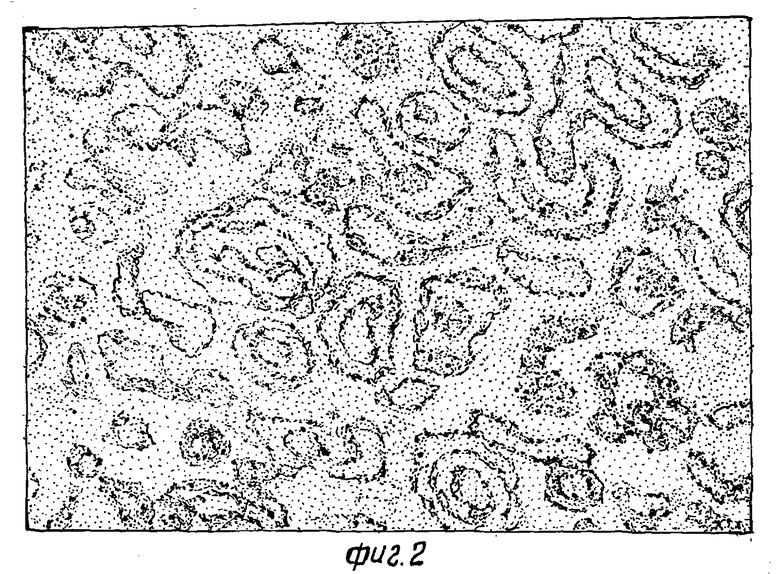
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМАЛЬНОЙ ФОРМЫ АЛЬФА-ТОКОФЕРОЛА И ГОМОГЕНИЗИРУЮЩИЙ КЛАПАН ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2085192C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| RU, 2104691 C1, 20.02.98 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| GB 1575343 A, 17.09.80 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| DE 19639811 A1, 02.04.98. | |||
Авторы
Даты
1999-05-27—Публикация
1998-06-01—Подача