Настоящее изобретение относится к новому способу получения 3-арил-бензофуранонов, предназначенных для стабилизации органических материалов от окислительного, термического и индуцированного светом распада.
Некоторые бензофуран-2-оны известны по ряду публикаций и упоминаются, например, в Beilstein, 18, 17 и Beilstein E III/IV, 18, 154-166, или описаны у Th.Kappe et al., Monatshefte fur Chemie 99, 990 (1968); J. Morvan et al., Bull. Soc. Chim. Fr. 1979, 583; L.F.Clarke et al., Journ. Org. Chem. 57, 362 (1992); M. Julia et al., Bull. Soc. Chim. Fr. 1965, 2175 или у H.Sterk et al. , Monatshefte fuer Chemie 99, 2223 (1968). Ни в одной из перечисленных публикаций нет указаний на применение этих соединений в качестве стабилизаторов для органических материалов.
Применение некоторых 3-фенил-3H-бензофуран-2-онов в качестве стабилизаторов для органических полимеров известно, например, из патентов США 4325863, 4338244 и 5175312.
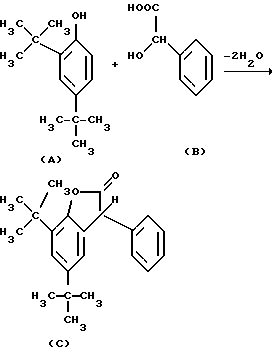
Применяемый до настоящего времени предпочтительный способ получения 3-фенил-3H-бензофуран-2-онов, как, например, 5,7-ди-трет.-бутил-3-фенил-3H-бензофуран-2-он формулы С, отличается тем, что 2,4-ди-трет.-бутил-фенол формулы А подвергают реакции с минеральной кислотой формулы В при отщеплении воды (см. патент США 4325863, пример 1, колонка 8, строки 34-45).
Способ, применяемый для синтеза 3-фенил-3H-бензофуран-2-онов, замещенных в фенильном кольце 3, или для получения 3H-бензофуран-2- онов, замещенных в положении 3 гетероциклом, имеет тот недостаток, что для его осуществления требуется использовать замещенные в фенильном кольце миндальные кислоты или гетероциклические миндальные кислоты. Однако из существующих публикаций известны лишь немногие из названных кислот, а методы синтеза, используемые для получения этих миндальных кислот, относительно сложны и неэкономичны.
Настоящее изобретение относится поэтому к способу получения соединений формулы I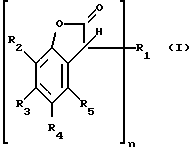
где при значении n, равном 1,
R1 обозначает незамещенную либо замещенную карбоциклическую либо гетероциклическую ароматическую систему,
а при n, равном 2,
R1 представляет собой незамещенный либо замещенный C1-C4-алкилом или гидроксильной группой фенилен или нафтилен; или же - R6-X-R7-,
R2, R3, R4 и R5 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, C1-C25-алкил, C7-С9-фенилалкил, незамещенный либо замещенный C1-C4-алкилом фенил, незамещенный либо замещенный C1-С4-алкилом C5-C8-циклоалкил; C1-C18-алкокси, C1-C18-алкилтио, C1-C4-алкиламино, ди-(С1-C4-алкил)амино, C1-C25-алканоилокси, C1-C25-алканоиламино, С3-C25-алкеноилокси, разорванный кислородом, серой или 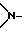 R8 C3-C25-алканоилокси; C6-C9-циклоалкилкарбонилокси, бензоилокси либо замещенный C1-C12-алкилом бензоилокси, или, далее, радикалы R2 и R3 или радикалы R3 и R4 или радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо, R4 представляет собой дополнительно -(CH2)p-COR9 или -(CH2)qОН, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II
R8 C3-C25-алканоилокси; C6-C9-циклоалкилкарбонилокси, бензоилокси либо замещенный C1-C12-алкилом бензоилокси, или, далее, радикалы R2 и R3 или радикалы R3 и R4 или радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо, R4 представляет собой дополнительно -(CH2)p-COR9 или -(CH2)qОН, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II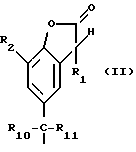
где R1 имеет то же значение, что и при n, равном 1,
R6 и R7 независимо друг от друга представляют собой незамещенный либо замещенный C1-C4-алкилом фенилен или нафтилен,
R8 представляет собой водород или C1-C8-алкил,
R9 обозначает гидроксильную группу, 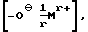 C1-C18-алкокси или
C1-C18-алкокси или 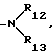
R10 и R511 независимо друг от друга представляют собой водород, CF3, C1-C12-алкил или фенил, или R10 и R11 вместе с C-атомом, по которому они связаны, образуют незамещенное либо замещенное 1-3 C1-C4-алкилом C5-C8-циклоалкилиденовое кольцо;
R12 и R13 независимо друг от друга представляют собой водород или C1-C18-алкил,
R14 обозначает водород или C1-C18-алкил,
М представляет собой r-валентный катион металла,
X обозначает прямую связь, кислород, серу или -NR14-,
n обозначает 1 или 2,
p обозначает 0, 1 или 2,
q обозначает 1, 2, 3, 4, 5 или 6 и
r обозначает 1, 2 или 3,
отличающемуся тем, что соединение формулы III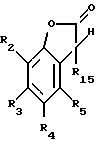
где R15 представляет собой галоген или -OR'15
R'15 обозначает водород, C1-C25-алканоил, С3-C25-алкеноил, разорванный кислородом, серой или 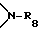 С3-C25-алканоил; C6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C12-алкилом бензоил; нафтоил или замещенный C1-C12-алкилом нафтоил; C1-C25-алкансульфонил, замещенный фтором C1-C25-алкансульфонил; фенилсульфонил или замещенный C1-C12-алкилом фенилсульфонил;
С3-C25-алканоил; C6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C12-алкилом бензоил; нафтоил или замещенный C1-C12-алкилом нафтоил; C1-C25-алкансульфонил, замещенный фтором C1-C25-алкансульфонил; фенилсульфонил или замещенный C1-C12-алкилом фенилсульфонил;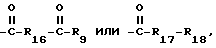
R16 представляет собой прямую связь, С1-C18-алкилен, разорванный кислородом, серой 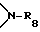 C2-C18-алкилен; C2-C18-алкенилен, C2-C20-алкилиден, C7-C20-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен,
C2-C18-алкилен; C2-C18-алкенилен, C2-C20-алкилиден, C7-C20-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен,
R17 обозначает кислород, -NH- или 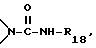 и
и
R18 представляет собой C1-C18-алкил или фенил, подвергают обменной реакции с соединением формулы IV
[H]n-R1
Галоген обозначает, например, хлор, бром или йод. Предпочтителен из них хлор.
Алканоил с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, формил, ацетил, пропионил, бутаноил, пентаноил, гексаноил, гептаноил, октаноил, нонаноил, деканоил, ундеканоил, додеканоил, тридеканоил, тетрадеканоил, пентадеканоил, гексадеканоил, октадеканоил, эйкозаноил либо докозаноил. R'15 в качестве алканоила имеет предпочтительно 2-18, прежде всего 2-12, например, 2-6 атомов углерода. Особенно предпочтителен ацетил.
Замещенный ди(С1-C6-алкил)фосфонатной группой C2-C25-алканоил обозначает, например, (CH3CH2O)2)POCH2CO-, (CH3O)2POCH2CO-, (CH3CH2CH2CH2О)2POCH2СО-, (CH3CH2O)2POCH2CH2CO-, (CH3O)2POCH2CH2CO-, (CH3CH2CH2CH2O)2POCH2CH2CO-,
(CH3CH2O)2PO(CH2)4СО-, (CH3CH2O)2PO(CH2)8СО- либо (CH3CH2O)2PO(CH2)17CO-. Алканоилокси с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, формилокси, ацетокси, пропионилокси, бутаноилокси, пентаноилокси, гексаноилокси, гептаноилокси, октаноилокси, нонаноилокси, деканоилокси, ундеканоилокси, додеканоилокси, тридеканоилокси, тетрадеканоилокси, пентадеканоилокси, гексадеканоилокси, гептадеканоилокси, октадеканоилокси, эйкозаноилокси либо докозаноилокси. Предпочтителен алканоилокси с числом атомов углерода 2-18, прежде всего 2-12, например, 2-6. Среди перечисленных особенно предпочтителен ацетокси.
Алкеноил с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропеноил, 2-бутеноил, 3-бутеноил, изобутеноил, n-2,4-пентадиеноил, 3-метил-2-бутеноил, n-2-октеноил, n-2-додеценоил, изо-додеценоил, олеоил, n-2-октадеценоил или n-4-октадеценоил. Предпочтителен алкеноил с 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4 атомами углерода.
Разорванный кислородом, серой или 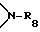 C3-C25-алкеноил обозначает, например, CH3OCH2CH2CH=CHCO- или CH3OCH2CH2OCH=CHCO-.
C3-C25-алкеноил обозначает, например, CH3OCH2CH2CH=CHCO- или CH3OCH2CH2OCH=CHCO-.
Алкеноилокси с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропеноилокси, 2-бутеноилокси, 3-бутеноилокси, изобутеноилокси, n-2,4-пентадиеноилокси, 3-метил-2-бутеноилокси, n-2-октеноилокси, n-2-додеценоилокси, изо-додеценоилокси, олеоилокси, n-2-октадеценоилокси либо n-4-октадеценоилокси. Предпочтителен алкеноилокси с 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4 атомами углерода.
Разорванный кислородом, серой или 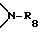 C3-C25-алкеноилокси обозначает, например, CH3OCH2CH2CH=CHCOO- или, CH3OCH2CH2OCH=CHCOO-.
C3-C25-алкеноилокси обозначает, например, CH3OCH2CH2CH=CHCOO- или, CH3OCH2CH2OCH=CHCOO-.
Разорванный кислородом, серой или 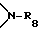 C3-C25-алканоил обозначает, например, CH3-O-CH2CO-, CH3-S-CH2CO-, CH3-NH-CH2CO-, CH3-N(CH3)-CH2CO-,
C3-C25-алканоил обозначает, например, CH3-O-CH2CO-, CH3-S-CH2CO-, CH3-NH-CH2CO-, CH3-N(CH3)-CH2CO-,
CH3-O-CH2CH2-O-CH2CO-, CH3-(O-CH2CH2-)2O-CH2CO-, CH3-(O-CH2CH2-)3O-CH2CO- либо CH3-(O-CH2CH2-)4O-CH2CO-.
Разорванный кислородом, серой или 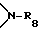 C3-C25-алканоилокси обозначает, например, CH3-O-CH2COO-, CH3-S-CH2COO-, CH3-NH-CH2COO-, CH3-N(CH3)-CH2COO-,
C3-C25-алканоилокси обозначает, например, CH3-O-CH2COO-, CH3-S-CH2COO-, CH3-NH-CH2COO-, CH3-N(CH3)-CH2COO-,
CH3-O-CH2CH2-O-CH2COO-, CH3-(O-CH2CH2-)2O-CH2COO-, CH3-(O-CH2CH2-)3O-CH2COO- или CH3-(O-CH2CH2-)4O-CH2COO-.
C6-C9-циклоалкилкарбонил обозначает, например, циклопентилкарбонил, циклогексилкарбонил, циклогептилкарбонил или циклооктилкарбонил. Циклогексилкарбонил предпочтителен.
C6-C9-циклоалкилкарбонилокси обозначает, например, циклопентилкарбонилокси, циклогексилкарбонилокси, циклогептилкарбонилокси или циклооктилкарбонилокси. Циклогексилкарбонилокси предпочтителен.
Замещенный C1-C12-алкилом бензоил, несущий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, o-, m- либо p-метилбензоил, 2,3-диметилбензоил, 2,4-диметилбензоил, 2,5-диметилбензоил, 2,6-диметилбензоил, 3,4-диметилбензоил, 3,5-диметилбензоил, 2-метил-б-этилбензоил, 4-трет. -бутилбензоил, 2-этилбензоил, 2,4,6-триметилбензоил, 2,6-диметил-4-трет.-бутилбензоил либо 3,5-ди-трет.-бутилбензоил. Предпочтительными заместителями являются C1-C8-алкил, прежде всего C1-C4-алкил.
Замещенный C1-C12-алкилом бензоилокси, несущий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, o-, m- либо p-метилбензоилокси, 2,3-диметилбензоилокси, 2,4-диметилбензоилокси, 2,5-диметилбензоилокси, 2,6-диметилбензоилокси, 3,4-диметилбензоилокси, 3,5-диметилбензоилокси, 2-метил-6-этилбензоилокси, 4-трет.-бутилбензоилокси, 2-этилбензоилокси, 2,4,6-триметилбензоилокси, 2,6-диметил-4-трет.-бутилбензоилокси либо 3,5-ди-трет. -бутилбензоилокси. Предпочтительными заместителями являются C1-C8-алкил, прежде всего C1-C4-алкил.
Замещенный C1-C12-алкилом нафтоил, обозначающий 1-нафтоил либо 2-нафтоил и содержащий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, 1-, 2-, 3-, 4-, 5-, 6-, 7- либо 8-метил-нафтоил, 1-, 2-, 3-, 4-, 5-, 6-, 7- либо 8-этил- нафтоил, 4-трет.-бутил-нафтоил либо 6-трет. -бутил-нафтоил. Особенно предпочтительными заместителями являются C1-C8-алкил, прежде всего C1-C4-алкил.
C1-C25-алкансульфонил обозначает разветвленный либо неразветвленный радикал, как, например, метансульфонил, этансульфонил, пропансульфонил, бутансульфонил, пентансульфонил, гексансульфонил, гептансульфонил, октансульфонил, нонансульфонил или докозансульфонил. Предпочтителен алкансульфонил с числом атомов углерода 1-18, прежде всего 1-12, например, 2-6. Особенно предпочтителен метансульфонил.
Замещенный фтором C1-C25-алкансульфонил обозначает, например, трифторметансульфонил.
Замещенный C1-C12-алкилом фенилсульфонил, несущий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, o-, m- или p-метилфенилсульфонил, p-этилфенилсульфонил, p-пропилфенилсульфонил либо p-бутилфенилсульфонил. Предпочтительными заместителями являются C1-C8-алкил, прежде всего C1-C4-алкил. Особенно предпочтителен p-метилфенилсульфонил.
Алкил с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, метил, этил, пропил, изопропил, n-бутил, втор. -бутил, изобутил, трет.-бутил, 2-этилбутил, n-пентил, изопентил, 1-метилпентил, 1,3-диметилбутил, n-гексил, 1-метилгексил, n-гептил, изогептил, 1,1,3,3-тетраметилбутил, 1-метилгептил, 3-метилгептил, n-октил, 2-этилгексил, 1,1,3-триметилгексил, 1,1,3,3-тетраметилпентил, нонил, децил, ундецил, 1-метилундецил, додецил, 1,1,3,3,5,5-гексаметилгексил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, эйкозил или докозил. Одним из предпочтительных значений R2 и R4 является, например, C1-C18-алкил. Особым предпочтительным значением R4 является C1-C4-алкил.
Алкенил с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропенил, 2-бутенил, 3-бутенил, изобутенил, n-2,4-пентадиенил, 3-метил-2-бутенил, n-2-октенил, n-2-додеценил, изо-додеценил, олеил, n-2-октадеценил либо n-4-октадеценил. Предпочтителен алкенил с числом атомов углерода 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4.
Алкенилокси с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропенилокси, 2-бутенилокси, 3-бутенилокси, изобутенилокси, n-2,4-пентадиенилокси, 3-метил-2-бутенилокси, n-2-октенилокси, n-2-додеценилокси, изо-додеценилокси, олеилокси, n-2-октадеценилокси либо n-4-октадеценилокси. Предпочтителен алкенилокси с числом атомов углерода 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4.
Алкинил с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропинил (-CH2-C≡CH), 2-бутинил, 3-бутинил, n-2-октинил либо n-2-додецинил. Предпочтителен алкинил с числом атомов углерода 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4.
Алкинилокси с числом атомов углерода 3-25 обозначает разветвленный либо неразветвленный радикал, как, например, пропинилокси (-OCH2-C≡CH), 2-бутинилокси, 3-бутинилокси, n-2-октинилокси либо n-2-додецинилокси. Предпочтителен алкинилокси с числом атомов углерода 3-18, прежде всего 3-12, например, 3-6, в первую очередь 3-4.
Разорванный кислородом, серой или 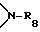 C2-C25-алкил обозначает, например, CH3-O-CH2-, CH3-S-CH2-, CH3-NH-CH2-, CH3-N(CH3)-CH2-, CH3-O-CH2CH2-O-CH2-, CH3-(O-CH2CH2-)2O-CH-, CH3-(O-CH2CH2-)3O-CH2- либо CH3-(O-CH2CH2-)4O-CH2-.
C2-C25-алкил обозначает, например, CH3-O-CH2-, CH3-S-CH2-, CH3-NH-CH2-, CH3-N(CH3)-CH2-, CH3-O-CH2CH2-O-CH2-, CH3-(O-CH2CH2-)2O-CH-, CH3-(O-CH2CH2-)3O-CH2- либо CH3-(O-CH2CH2-)4O-CH2-.
C7-C9-фенилалкил обозначает, например, бензил, α- метилбензил, α,α- диметилбензил или 2-фенилэтил. Предпочтительны среди них бензил и α,α- диметилбензил.
Незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-С9-фенилалкил обозначает, например, бензил, α- метилбензил, α,α- диметилбензил, 2-фенилэтил, 2-метилбензил, 3-метилбензил, 4-метилбензил, 2,4-диметилбензил, 2,6-диметилбензил либо 4-трет.-бутилбензил. Предпочтителен бензил.
Разорванный кислородом, серой или 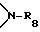 незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C25-фенилалкил обозначает разветвленный либо неразветвленный радикал, как, например, феноксиметил, 2-метил-феноксиметил, 3-метил-феноксиметил, 4-метил- феноксиметил, 2,4-диметил-феноксиметил, 2,3-диметил-феноксиметил, фенилтиометил, N-метил-N-фенил-метил, N-этил-N-фeнил-мeтил, 4-трет. -бутил-феноксиметил, 4-трет.-бутил-феноксиэтоксиметил, 2,4-ди-трет. -бутил-феноксиметил, 2,4-ди-трет.-бутил-феноксиэтоксиметил, феноксиэтоксиэтоксиэтоксиметил, бензилоксиметил, бензилоксиэтоксиметил, N-бензил-N-этил-метил или N-бензил-N- изопропил-метил.
незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C25-фенилалкил обозначает разветвленный либо неразветвленный радикал, как, например, феноксиметил, 2-метил-феноксиметил, 3-метил-феноксиметил, 4-метил- феноксиметил, 2,4-диметил-феноксиметил, 2,3-диметил-феноксиметил, фенилтиометил, N-метил-N-фенил-метил, N-этил-N-фeнил-мeтил, 4-трет. -бутил-феноксиметил, 4-трет.-бутил-феноксиэтоксиметил, 2,4-ди-трет. -бутил-феноксиметил, 2,4-ди-трет.-бутил-феноксиэтоксиметил, феноксиэтоксиэтоксиэтоксиметил, бензилоксиметил, бензилоксиэтоксиметил, N-бензил-N-этил-метил или N-бензил-N- изопропил-метил.
C7-C9-фенилалкокси обозначает, например, бензилокси, α- метилбензилокси, α,α- диметилбензилокси либо 2-фенилэтокси. Предпочтителен бензилокси.
Замещенный C1-C4-алкилом фенил, содержащий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, o-, m- или p-метилфенил, 2,3-диметилфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 3,4-диметилфенил, 3,5-диметилфенил, 2-метил-6-этилфенил, 4-трет.-бутилфенил, 2-этилфенил или 2,6-диэтилфенил.
Замещенный C1-C4-алкилом фенокси, содержащий предпочтительно 1-3, прежде всего 1-2 алкильные группы, обозначает, например, o-, m- либо p-метилфенокси, 2,3-диметилфенокси, 2,4-диметилфенокси, 2,5-диметилфенокси, 2,6-диметилфенокси, 3,4-диметилфенокси, 3,5-диметилфенокси, 2-метил-6-этилфенокси, 4-трет.-бутилфенокси, 2-этилфенокси или 2,6-диэтилфенокси.
Незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкил обозначает, например, циклопентил, метилциклопентил, диметилциклопентил, циклогексил, метилциклогексил, диметилциклогексил, триметилциклогексил, трет.-бутилциклогексил, циклогептил или циклооктил. Предпочтительны циклогексил и трет.-бутилциклогексил.
Незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкокси обозначает, например, циклопентокси, метилциклопентокси, диметилциклопентокси, циклогексокси, метилциклогексокси, диметилпиклогексокси, триметилциклогексокси, трет. -бутилциклогексокси, циклогептокси либо циклооктокси. Предпочтительны из них циклогексокси и трет.-бутилциклогексокси.
Алкокси с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, метокси, этокси, пропокси, изопропокси, n-бутокси, изобутокси, пентокси, изопентокси, гексокси, гептокси, октокси, децилокси, тетрадецилокси, гексадецилокси либо октадецилокси. Предпочтителен алкокси с числом атомов углерода 1-12, прежде всего 1-8, например, 1-6.
Разорванный кислородом, серой или 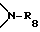 C2-C25-алкокси обозначает, например, CH3-O-CH2CH2O-, CH3-S-CH2CH2O-, CH3-NH-CH2CH2O-, CH3-N(CH3)-CH2CH2O-,
C2-C25-алкокси обозначает, например, CH3-O-CH2CH2O-, CH3-S-CH2CH2O-, CH3-NH-CH2CH2O-, CH3-N(CH3)-CH2CH2O-,
CH3-O-CH2CH2-O-CH2CH2O-, CH3-(O-CH2CH2-)2O-CH2CH2O-, CH3-(O-CH2CH2-)3O-CH2CH2O- или CH3-(O-CH2CH2-)4O-CH2CH2O-.
Алкилтио с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, метилтио, этилтио, пропилтио, изопропилтио, n-бутилтио, изобутилтио, пентилтио, изопентилтио, гексилтио, гептилтио, октилтио, децилтио, тетрадецилтио, гексадецилтио либо октадецилтио. Предпочтителен алкилтио с числом атомов углерода 1-12, прежде всего 1-8, например, 1-6.
Алкиламино с числом атомов углерода до 4 обозначает разветвленный либо неразветвленный радикал, как, например, метиламино, этиламино, пропиламино, изопропиламино, n-бутиламино, изобутиламино либо трет.-бутиламино.
Ди-(C1-C4-алкил)амино обозначает также, что оба радикала независимо друг от друга являются разветвленными либо неразветвленными, как, например, диметиламино, метилэтиламино, диэтиламино, метил-n-пропиламино, метил-изопропиламино, метил-n-бутиламино, метилизобутиламино, этилизопропиламино, этил-n-бутиламино, этилизобутиламино, этил-трет.-бутиламино, диэтиламино, диизопропиламино, изопропил-n-бутиламино, изопропилизобутиламино, ди-n-бутиламино или диизобутиламино.
Алканоиламино с числом атомов углерода до 25 обозначает разветвленный либо неразветвленный радикал, как, например, формиламино, ацетиламино, пропиониламино, бутаноиламино, пентаноиламино, гексаноиламино, гептаноиламино, октаноиламино, нонаноиламино, деканоиламино, ундеканоиламино, додеканоиламино, тридеканоиламино, тетрадеканоиламино, пентадеканоиламино, гексадеканоиламино, гептадеканоиламино, октадеканоиламино, эйкозаноиламино или докозаноиламино. Предпочтителен алканоиламино с числом атомов углерода 2-18, прежде всего 2-12, например, 2-6.
C1-C18-алкилен обозначает разветвленный либо неразветвленный радикал, как, например, метилен, этилен, пропилен, триметилен, тетраметилен, пентаметилен, гексаметилен, гептаметилен, октаметилен, декаметилен, додекаметилен либо октадекаметилен. Предпочтителен C1-C12-алкилен, прежде всего C1-C8-алкилен.
Замещенное C1-C4-алкилом C5-C12-циклоалкиленовое кольцо, содержащее преимущественно 1-3, предпочтительно 1-2 разветвленных либо неразветвленных радикала из алкильных групп, обозначает, например, циклопентилен, метилциклопентилен, диметилциклопентилин, циклогексилен, метилциклогексилен, диметилциклогексилен, триметилциклогексилен, трет.-бутилциклогексилен, циклогептилен, циклооктилен либо циклодецилен. Предпочтительны из них циклогексилен и трет.-бутилциклогексилен.
Разорванный кислородом, серой или 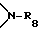 C2-C18-алкилен обозначает, например, -CH2-O-CH2-, -CH2-S-CH2, -CH2-NH-CH2-, -CH2-N(CH3)-CH2-, -CH2-O-CH2CH2-O-CH2-, -CH2-(O-CH2CH2-)2O-CH2-, -CH2-(O-CH2CH2-)3O-CH2-, -CH2-(O-CH2CH2-)4O-CH2- или -CH2CH2-S-CH2CH2-.
C2-C18-алкилен обозначает, например, -CH2-O-CH2-, -CH2-S-CH2, -CH2-NH-CH2-, -CH2-N(CH3)-CH2-, -CH2-O-CH2CH2-O-CH2-, -CH2-(O-CH2CH2-)2O-CH2-, -CH2-(O-CH2CH2-)3O-CH2-, -CH2-(O-CH2CH2-)4O-CH2- или -CH2CH2-S-CH2CH2-.
C2-C18-алкенилен обозначает, например, винилен, метилвинилен, октенилэтилен либо додеценилэтилен. Предпочтителен C2-C8-алкенилен.
Алкилиден с числом атомов углерода 2-20 обозначает, например, этилиден, пропилиден, бутилиден, пентилиден, 4-метилпентилиден, гептилиден, нонилиден, тридецилиден, нонадецилиден, 1-метилэтилиден, 1-этилпропилиден или 1-этилпентилиден. Предпочтителен C2-C8-алкилиден.
Фенилалкилиден с числом атомов углерода 7-20 обозначает, например, бензилиден, 2-фенилэтилиден либо 1-фенил-2-гексилиден. Предпочтителен C7-C9-фенилалкилиден.
C5-C8-циклоалкилен обозначает насыщенную углеводородную группу с двумя свободными валентностями и по крайней мере с одним кольцевым фрагментом и представляет собой, например, циклопентилен, циклогексилен, циклогептилен или циклооктилен. Предпочтителен среди них циклогексилен.
C7-C8-бициклоалкилен обозначает, например, бициклогептилен или бициклооктилен.
Незамещенный либо замещенный C1-C4-алкилом фенилен или нафтилен обозначает, например, 1,2-, 1,3-, 1,4-фенилен, 1,2-, 1,3-, 1,4-, 1,6-, 1,7-, 2,6- или 2,7-нафтилен. Предпочтителен из них 1,4-фенилен.
Замещенное C1-C4-алкилом C5-C8-циклоалкилиденовое кольцо, содержащее предпочтительно 1-3, прежде всего 1-2 разветвленные либо неразветвленные радикальные алкильные группы, обозначает, например, циклопентилиден, метилциклопентилиден, диметилциклопентилиден, циклогексилиден, метилциклогексилиден, диметилциклогексилиден, триметилциклогексилиден, трет.-бутилциклогексилиден, циклогептилиден или циклооктилиден. Предпочтительны среди них циклогексилиден и трет.-бутилциклогексилиден.
Одно-, двух- или трехвалентный катион металла представляет собой предпочтительно катион щелочного, щелочноземельного металла либо катион алюминия, например, Na+, К+, Mg++, Ca++ либо Al+++.
R1 при n, равном 1, может представлять собой любую ароматическую карбоциклическую или гетероциклическую систему, незамещенную либо замещенную.
Соответствующие карбоциклические системы базируются на бензольном кольце или на системе аннелированных бензольных колец, состоящей, например, из 2-5, прежде всего 2 или 3 колец, причем одно или несколько из них могут быть полностью или частично гидрированы. Существенным является то, что связывание до бензофуранона осуществляют через ароматическое кольцо. Бензольное кольцо, соответственно аннелированные бензольные кольца могут содержать также присоединенные путем конденсации гетероциклические кольца, которые сами могут быть ароматическими либо не ароматическими, в частности такие из них, которые имеют 5 или 6 кольцевых звеньев, например, 1-3 гетероатома из группы азот, кислород и сера.
Соответствующие гетероциклические ароматические системы представляют собой предпочтительно 5- или 6-звенные гетероциклические кольца ароматического характера, содержащие 1-3, предпочтительно 1 или 2 гетероатома из группы азот, кислород и сера. Эти кольца могут содержать еще и другие карбоциклические или гетероциклические ароматические либо не ароматические кольца, присоединяемые путем конденсации, причем предпочтительны карбоциклические 6-звенные, прежде всего ароматические кольца.
В качестве заместителей для ароматического радикала R1 (при n=1) могут рассматриваться, например, такие, которые имеют значения, расшифрованные ниже для радикалов R19-R23. Такими заместителями являются прежде всего хлор, амино, гидрокси, C1-C18-алкил, C1-C18-алкокси, C1-C18-алкилтио, C3-C4-алкенилокси, C3-C4-алкинилокси, C1-C4-алкиламино, ди-(C1-C4-алкил) амино, фенил, бензил, бензоил или бензоилокси, прежде всего хлор, амино, гидрокси, C1-C4-алкил, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкиламино или ди(C1-C4-алкил)амино.
Интерес представляет способ получения соединений формулы I, где при значении n, равном 1, R1 обозначает незамещенное либо замещенное 5- или 6-звенное ароматическое кольцо, к которому при определенных условиях путем конденсации присоединены другие кольца.
Интерес представляет также способ получения соединений формулы I, где при значении n, равном 1, R1 обозначает незамещенный либо замещенный фенил, нафтил, фенантрил, антрил, 5,6,7,8-тетрагидро-2- нафтил, тиенил, бензо[b] тиенил, нафто [2,3-b] тиенил, тиатренил, фурил, бензофурил, изобензофурил, дибензофурил, хроменил, ксантенил, феноксатиинил, пирролил, имидазолил, пиразолил, пиразинил, пиримидинил, пиридазинил, индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, карбазолил, β- карболинил, фенантридинил, акридинил, перимидинил, феназинил, изотиазолил, фенотиазинил, изоксазолил, фуразанил, бифенил, тетралинил, флуоренил или феноксазинил. К предпочтительным заместителям указанных выше гетероциклических систем относятся хлор, аминогруппы, гидроксильные группы, C1-C4-алкил, C1-C4-алкокси, С1-C4-алкилтио, C1-C4-алкиламино или ди(C1-C4-алкил)амино.
Особый интерес представляет способ получения соединений формулы I, где при значении n, равном 1, R1 представляет собой фенантрил, тиенил, дибензофурил, незамещенный либо замещенный C1-C4-алкилом карбазолил; или флуоренил, или R1 обозначает остаток формулы V или VI,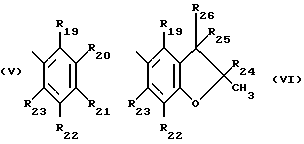
где R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, галоген, гидроксильную группу, C1-C25-алкил, разорванный кислородом, серой или 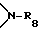 C2-C25-алкил; C1-C25-алкокси, разорванный кислородом, серой или
C2-C25-алкил; C1-C25-алкокси, разорванный кислородом, серой или 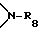 C2-C25-алкокси; C1-C25-алкилтио, C3-C25-алкенил, C3-C25-алкенилокси, C3-C25-алкинил, C3-C25-алкинилокси, C7-C9-фенилалкил,
C2-C25-алкокси; C1-C25-алкилтио, C3-C25-алкенил, C3-C25-алкенилокси, C3-C25-алкинил, C3-C25-алкинилокси, C7-C9-фенилалкил,
C7-C9-фенилалкокси, незамещенный либо замещенный C1-C4-алкилом фенил; незамещенный либо замещенный C1-C4-алкилом фенокси; незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкил; незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкокси; C1-C4-алкиламино, ди-(C1-C4-алкил)амино, C1-C25-алканоил, разорванный кислородом, серой или 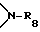 (C3-C25-алканоил; C1-C25-алканоилокси, разорванный кислородом, серой или
(C3-C25-алканоил; C1-C25-алканоилокси, разорванный кислородом, серой или 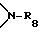 С3-C25-алканоилокси; C1-C25-алканоиламино, С3-C25-алкеноил, разорванный кислородом, серой или
С3-C25-алканоилокси; C1-C25-алканоиламино, С3-C25-алкеноил, разорванный кислородом, серой или 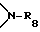 C3-C25-алкеноил; C3-C25-алкеноилокси, разорванный кислородом, серой или
C3-C25-алкеноил; C3-C25-алкеноилокси, разорванный кислородом, серой или 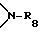 C3-C25-алкеноилокси; C6-C9-циклоалкилкарбонил, C6-C9-циклоалкилкарбонилокси, бензоил или замещенный C1-C12-алкилом бензоил; бензоилокси или замещенный C1-C12-алкилом бензоилокси;
C3-C25-алкеноилокси; C6-C9-циклоалкилкарбонил, C6-C9-циклоалкилкарбонилокси, бензоил или замещенный C1-C12-алкилом бензоил; бензоилокси или замещенный C1-C12-алкилом бензоилокси; 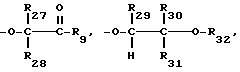 или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо,
или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо,
R24 обозначает водород, C1-C4-алкил, незамещенный либо замещенный C1-C4-алкилом фенил,
R25 и R26 обозначают водород, C1-C4-алкил или фенил, при условии, что по крайней мере один из радикалов R25 и R26 является водородом,
R27 и R28 представляют собой независимо друг от друга водород, C1-C4-алкил или фенил,
R29 представляет собой водород или C1-C4-алкил,
R30 обозначает водород, незамещенный либо замещенный C1-C4-алкилом фенил; C1-C25-алкил, разорванный кислородом, серой или 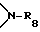 C2-C25-алкил; незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или
C2-C25-алкил; незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или 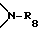 незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C25-фенилалкил, или, далее, радикалы
незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C25-фенилалкил, или, далее, радикалы
R29 и R30 вместе с атомами углерода, по которым они связаны, образуют незамещенное либо замещенное 1-3 C1-C4-алкилом C5-C12-циклоалкиленовое кольцо;
R31 представляет собой водород или C1-C4-алкил,
R32 обозначает водород, C1-C25-алканоил, C3-C25-алкеноил, разорванный кислородом, серой или 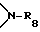 C3-C25-алканоил; замещенный ди(C1-C6- алкил)фосфонатной группой C2-C25-алканоил; C6-C9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C12-алкилом бензоил;
C3-C25-алканоил; замещенный ди(C1-C6- алкил)фосфонатной группой C2-C25-алканоил; C6-C9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C12-алкилом бензоил;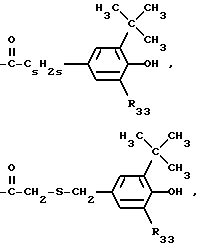
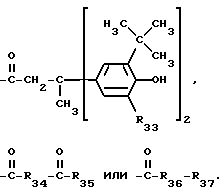
R33 представляет собой водород или C1-C8-алкил,
R34 представляет собой прямую связь, C1-C18-алкилен, разорванный кислородом, серой или 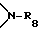 C2-C18-алкилен; C2-C18-алкенилен, C2-C20-алкилиден, C7-C20-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен,
C2-C18-алкилен; C2-C18-алкенилен, C2-C20-алкилиден, C7-C20-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен, 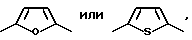
R35 обозначает гидроксильную группу, 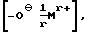 C1-C18-алкокси или
C1-C18-алкокси или 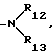
R36 представляет собой кислород, -NH- или 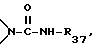
R37 представляет собой C1-C18-алкил или фенил и s обозначает 0, 1 или 2.
Также особый интерес представляет способ получения соединений формулы I, где при значении n, равном 2,
R1 представляет собой -R6-X-R7-,
R6 и R7 обозначают фенилен,
X является кислородом или -NR14- и
R14 обозначает C1-C4-алкил.
Значительный интерес представляет способ получения соединений формулы I, где при значении n, равном 1,
R1 обозначает фенантрил, тиенил, дибензофурил, незамещенный либо замещенный C1-C4-алкилом карбазолил; или флуоренил, или R1 представляет собой остаток формулы V или VI,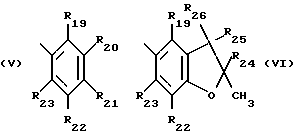
где R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, галоген, гидроксильную группу, C1-C18-алкил, разорванный кислородом, серой или 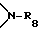 C2-C18-алкил; C1-C18-алкокси, разорванный кислородом, серой или
C2-C18-алкил; C1-C18-алкокси, разорванный кислородом, серой или 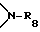 C2-C18-алкокси; C1-C18-алкилтио, C3-C18-алкенил, C3-C18-алкенилокси, C3-C18-алкинил, C3-C18-алкинилокси, С7-C9-фенилалкил,
C2-C18-алкокси; C1-C18-алкилтио, C3-C18-алкенил, C3-C18-алкенилокси, C3-C18-алкинил, C3-C18-алкинилокси, С7-C9-фенилалкил,
C7-C9-фенилалкокси, незамещенный либо замещенный C1-C4-алкилом фенил; незамещенный либо замещенный C1-C4-алкилом фенокси; незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкил; незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкокси; C1-C4-алкиламино, ди-(C1-C4-алкил)амино, C1-C18-алканоил, разорванный кислородом, серой или 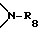 C3-C18-алканоил; C1-C18-алканоилокси, разорванный кислородом, серой или
C3-C18-алканоил; C1-C18-алканоилокси, разорванный кислородом, серой или 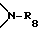 C3-C18-алканоилокси; C1-C18-алканоиламино, C3-C18-алкеноил, разорванный кислородом, серой или
C3-C18-алканоилокси; C1-C18-алканоиламино, C3-C18-алкеноил, разорванный кислородом, серой или 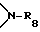 C3-C18-алкеноил; C3-C18-алкеноилокси, разорванный кислородом, серой или
C3-C18-алкеноил; C3-C18-алкеноилокси, разорванный кислородом, серой или 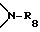 C3-C18-алкеноилокси; C6-C9-циклоалкилкарбонил, C6-C9-циклоалкилкарбонилокси, бензоил или замещенный C1-C12-алкилом бензоил; бензоилокси или замещенный C1-C8-алкилом бензоилокси;
C3-C18-алкеноилокси; C6-C9-циклоалкилкарбонил, C6-C9-циклоалкилкарбонилокси, бензоил или замещенный C1-C12-алкилом бензоил; бензоилокси или замещенный C1-C8-алкилом бензоилокси; 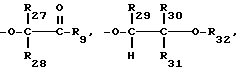 или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 вместе с атомами углерода, по которым они) связаны, образуют бензойное кольцо,
или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 вместе с атомами углерода, по которым они) связаны, образуют бензойное кольцо,
R24 обозначает водород, C1-C4-алкил, незамещенный либо замещенный C1-C4-алкилом фенил;
R25 и R26 обозначают водород, C1-C4-алкил или фенил, при условии, что по крайней мере один из радикалов R25 и R26 является водородом,
R27 и R28 независимо друг от друга представляют собой водород, C1-C4-алкил или фенил,
R29 представляет собой водород или C1-C4-алкил,
R30 обозначает водород, незамещенный либо замещенный C1-C4-алкилом фенил; C1-C18-алкил, разорванный кислородом, серой или 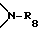 C2-C18-алкил; незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или
C2-C18-алкил; незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или 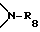 незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C18-фенилалкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, по которым они связаны, образуют незамещенное либо замещенное 1-3 C1-C4-алкилом C5-C9-циклоалкиленовое кольцо;
незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C18-фенилалкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, по которым они связаны, образуют незамещенное либо замещенное 1-3 C1-C4-алкилом C5-C9-циклоалкиленовое кольцо;
R31 представляет собой водород или C1-C4-алкил,
R32 обозначает водород, C1-C18-алканоил, C3-C18-алкеноил, разорванный кислородом, серой или 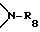 C3-C18-алканоил; замещенный ди(C1-C6- алкил)фосфонатной группой C2-C18-алканоил; C6-C9-циклоалкилкарбонил, теноил, фуроил, бензоил либо замещенный C1-C8-алкилом бензоил;
C3-C18-алканоил; замещенный ди(C1-C6- алкил)фосфонатной группой C2-C18-алканоил; C6-C9-циклоалкилкарбонил, теноил, фуроил, бензоил либо замещенный C1-C8-алкилом бензоил;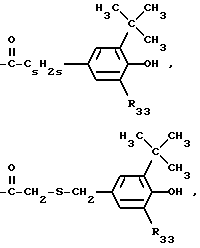
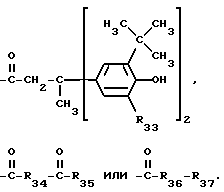
R33 представляет собой водород или C1-C4-алкил,
R34 представляет собой прямую связь, C1C18-алкилен, разорванный кислородом, серой или 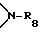 C2-C12-алкилен; C2-C12-алкенилен, C2-C12-алкилиден, C7-C12-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен,
C2-C12-алкилен; C2-C12-алкенилен, C2-C12-алкилиден, C7-C12-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен, незамещенный либо замещенный C1-C4-алкилом фенилен, 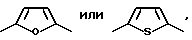
R35 обозначает гидроксильную группу, 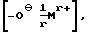 C1-C18-алкокси или
C1-C18-алкокси или 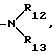
R36 представляет собой кислород, -NH- или 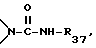
R37 представляет собой C1-C12-алкил или фенил и s обозначает 0, 1 или 2.
Предпочтительным является способ получения соединений формулы I, где R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, хлор, бром, гидроксильную группу, C1-C18-алкил, разорванный кислородом или серой C2-C18-алкил; C1-C18-алкокси, разорванный кислородом или серой C2-C18-алкокси; C1-C18-алкилтио, C3-C12-алкенилокси, C3-C12-алкинилокси, C7-C9-фенилалкил, C7-C9-фенилалкокси, незамещенный либо замещенный C1-C4-алкилом фенил; фенокси, циклогексил, C5-C8-циклоалкокси, C1-C4-алкиламино, ди-(C1-C4-алкил)амино, C1-C12-алканоил, разорванный кислородом или серой C3-C12-алканоил; C1-C12-алканоилокси, разорванный кислородом или серой C3-C12-алканоилокси; C1-C12-алканоиламино, C3-C12-алкеноил, C3-C12-алкеноилокси, циклогексилкарбонил, циклогексилкарбонилокси, бензоил или замещенный C1-C4-алкилом бензоил; бензоилокси или замещенный C1-C4-алкилом бензоилокси; 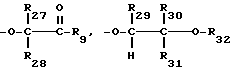 или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 образуют вместе с атомами углерода, по которым они связаны, бензойное кольцо,
или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 образуют вместе с атомами углерода, по которым они связаны, бензойное кольцо,
R24 обозначает водород или C1-C4-алкил,
R25 и R26 обозначает водород или C1-C4-алкил, при условии, что по крайней мере один из радикалов R25 и R26 является водородом,
R27 и R28 независимо друг от друга представляют собой водород или C1-C4-алкил,
R29 является водородом,
R30 обозначает водород, фенил, C1-C18-алкил, разорванный кислородом или серой C2-C18-алкил; C7-C9-фенилалкил, разорванный кислородом или серой незамещенный либо замещенный в фенильном остатке 1-3 C1-C4-алкилом C7-C18-фенилалкил, или, далее, радикалы R29 и R30 образуют вместе с атомами углерода, по которым они связаны, незамещенное либо замещенное 1-3 C1-C4-алкилом циклогексиленовое кольцо,
R31 обозначает водород или C1-C4-алкил,
R32 представляет собой водород, C1-C18-алканоил, C3-C12-алкеноил, разорванный кислородом или серой C3-C12-алканоил, замещенный ди(C1-C6-алкил)фосфонатной группой C2-C12-алканоил; C6-C9-циклоалкилкарбонил, бензоил,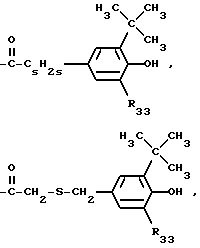
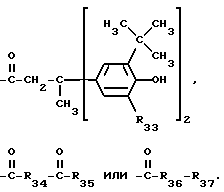
R33 обозначает водород или C1-C4-алкил,
R34 представляет собой C1-C12-алкилен, C2-C8-алкенилен, C2-C8-алкилиден, C7-C12-фенилалкилиден, C5-C8-циклоалкилен или фенилен,
R35 обозначает гидроксильную группу, 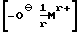 или C1-C18-алкокси,
или C1-C18-алкокси,
R36 представляет собой кислород или -NH-,
R37 представляет собой C1-C8-алкил или фенил и s обозначает 1 или 2.
Также предпочтителен способ получения соединений формулы I, где R1 представляет собой фенантрил, тиенил, дибензофурил, незамещенный либо замещенный C1-C4-алкилом карбазолил; или флуоренил; или R1 обозначает остаток формулы V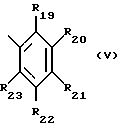
где R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, C1-C18-алкил, C1-C18-алкокси, C1-C18-алкилтио, C3-C4-алкенилокси, C3-C4-алкинилокси, фенил, бензоил, бензоилокси или 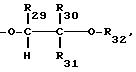
R29 является водородом,
R30 представляет собой водород, фенил или C1-C18-алкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, по которым они связаны, образуют незамещенное либо замещенное 1-3 C1-C4- алкилом циклогексиленовое кольцо,
R31 обозначает водород или C1-C4-алкил и
R23 представляет собой водород, C1-C12-алканоил или бензоил.
Особенно предпочтителен способ получения соединений формулы I, где
R19 представляет собой водород или C1-C4-алкил,
R20 обозначает водород или C1-C4-алкил,
R21 представляет собой водород, хлор, гидроксильную группу, C1-C12-алкил, C1-C4-алкокси, C1-C4-алкилтио, фенил или -O-CH2-CH2-O-R32, R22 представляет собой водород или C1-C4-алкил,
R23 представляет собой водород или C1-C4-алкил и
R32 обозначает C1-C4-алканоил.
Совершенно особо предпочтительным является способ получения соединений формулы I, где
R2, R3, R4 и R5 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, C1-C25-алкил, C7-C9-фенилалкил, незамещенный либо замещенный C1-C4-алкилом фенил, незамещенный либо замещенный C1-C4-алкилом C5-C8-циклоалкил; C1-C12-алкокси, C1-C12-алкилтио, C1-C4-алкиламино, ди-(C1-C4-алкил)амино, C1-C18-алканоилокси, C1-C18-алканоиламино, C3-C18-алкеноилокси, разорванный кислородом, серой или 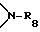 C3-C18-алканоилокси; C6-C9-циклоалкилкарбонилокси, бензоилокси или замещенный C1-C8-алкилом бензоилокси, или, далее, радикалы R2 и R4, либо радикалы R3 и R4, либо радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо, R4 представляет собой дополнительно -(CH2)p-COR9 или -(CH2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II
C3-C18-алканоилокси; C6-C9-циклоалкилкарбонилокси, бензоилокси или замещенный C1-C8-алкилом бензоилокси, или, далее, радикалы R2 и R4, либо радикалы R3 и R4, либо радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо, R4 представляет собой дополнительно -(CH2)p-COR9 или -(CH2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II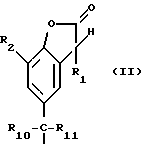
R8 представляет собой водород или C1-C6-алкил,
R9 обозначает гидроксильную группу, C1-C18-алкокси или 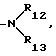
R10 и R11 являются метиловыми группами или вместе с C-атомом, по которому они связаны, образуют незамещенное либо замещенное 1-3 C1-C4-алкилом C5-C8-циклоалкилиденовое кольцо;
R12 и R13 независимо друг от друга представляют собой водород или C1-C8-алкил и
q обозначает 2, 3, 4, 5 или 6.
К особо предпочтительным относится способ получения соединений формулы I, где по крайней мере два из радикалов R2, R3, R4 и R5 являются водородом.
Также к особо предпочтительным относится способ получения соединений формулы I, где R3 и R5 являются водородом.
Особое место среди предпочтительных способов занимает способ получения соединений формулы I, где
R2, R3, R4 и R5 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, C1-C18-алкил, C7-C9-фенилалкил, фенил, C5-C8-циклоалкил, C1-C6-алкокси, циклогексилкарбонилокси или бензоилокси, или, далее, радикалы R2 и R3 либо радикалы R3 и R4 либо радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензойное кольцо, R4 представляет собой дополнительно -(CH2)p-COR9, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II,
R9 обозначает гидроксильную группу или C1-C18-алкокси и
R10 и R11 являются метиловыми группами или вместе с C-атомом, по которому они связаны, образуют C5-C8-циклоалкилиденовое кольцо.
Предпочтительный интерес представляет способ получения соединений формулы I, где
R2 обозначает C1-C18-алкил или циклогексил,
R3 является водородом,
R4 представляет собой C1-C4-алкил, циклогексил или остаток формулы II,
R5 является водородом и
R10 и R11 вместе с C-атомом, по которому они связаны, образуют циклогексилиденовое кольцо.
Также предпочтительный интерес вызывает способ получения соединений формулы I, где
R'15 представляет собой водород, C1-C18-алканоил, C3-C18-алкеноил, разорванный кислородом, серой или 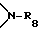 C3-C18-алканоил; C6-C9- циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C8-алкилом бензоил; нафтоил или замещенный C1-C8-алкилом нафтоил; C1-C18-алкансульфонил, замещенный фтором C1-C18-алкансульфонил; фенилсульфонил или замещенный C1-C8-алкилом фенилсульфонил;
C3-C18-алканоил; C6-C9- циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный C1-C8-алкилом бензоил; нафтоил или замещенный C1-C8-алкилом нафтоил; C1-C18-алкансульфонил, замещенный фтором C1-C18-алкансульфонил; фенилсульфонил или замещенный C1-C8-алкилом фенилсульфонил;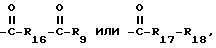
R16 представляет собой прямую связь, C1-C12-алкилен, разорванный кислородом, серой или 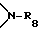 C2-C12-алкилен; C2-C12-алкенилен, C2-C12-алкилиден, C7-C12-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен или фенилен, R17 обозначает кислород или -NH- и
C2-C12-алкилен; C2-C12-алкенилен, C2-C12-алкилиден, C7-C12-фенилалкилиден, C5-C8-циклоалкилен, C7-C8-бициклоалкилен или фенилен, R17 обозначает кислород или -NH- и
R18 представляет собой C1-C12-алкил или фенил.
Совершенно особый предпочтительный интерес представляет способ получения соединений формулы I, где
R15 представляет собой хлор, бром или -OR15,
R'15 обозначает водород, C1-C12-алканоил, разорванный кислородом C3-C12-алканоил; циклогексилкарбонил, бензоил, нафтоил, C1-C12-алкансульфонил, замещенный фтором C1-C12-алкансульфонил; фенилсульфонил или замещенный C1-C4-алкилом фенилсульфонил; или 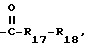
R17 представляет собой -NH- и
R18 представляет собой C1-C8-алкил или фенил.
Также совершенно особый предпочтительный интерес представляет способ получения соединений формулы I, где
R15 представляет собой - OR'15,
R'15 обозначает водород, C1-C4-алканоил или 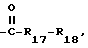
R17 представляет собой -NH- и
R18 является C1-C4-алкилом.
Для осуществления способа по изобретению предпочтительны следующие условия реакции.
Реакция может проводиться при повышенной температуре, прежде всего в диапазоне от 70 до 200oC, в расплаве или в растворителе, при определенных условиях в легком вакууме.
Особенно предпочтительно осуществлять реакцию в диапазоне температур кипения применяемого соединения формулы IV.
В качестве растворителя предпочтительно применять соединение формулы IV, которое одновременно является реагентом.
В то же время в качестве растворителей могут использоваться те из них, которые не участвуют в реакции, как, например, галогенированные углеводороды, углеводороды, простые эфиры или дезактивированные ароматические углеводороды.
Предпочтительными галогенированными углеводородами являются, например, дихлорметан, 1,2-дихлорэтан, хлороформ или тетрахлорметан.
К применяемым предпочтительно углеводородам относятся, например, октан и имеющиеся в продаже фракции изомеров, как, например, фракции гексана, кипящий бензин или лигроин.
Среди предпочтительных простых эфиров следует назвать, например, дибутиловый эфир, метил-трет.-бутиловый эфир или диэтиленгликолевый диметиловый эфир.
Примерами дезактивированных ароматических углеводородов являются нитробензол или пиридин.
Если в соединении формулы III R'15 обозначает водород (3- гидрокси-ЗH-бензофуран-2-оны), то воду, образующуюся во время реакции, целесообразно удалять непрерывно. Предпочтительно осуществлять это добавками средства, абсорбирующего воду. Таковым является, например, молекулярное сито. Но особенно предпочтительно непрерывно удалять воду путем азеотропной отгонки через водоотделитель.
Интересен также способ получения соединений формулы I, в котором обменную реакцию осуществляют в присутствии катализатора.
В качестве катализаторов пригодны протоновые кислоты, кислоты Льюиса, силикаты алюминия, ионитовые смолы, цеолиты, встречающиеся в природе слоистые силикаты или модифицированные слоистые силикаты.
Пригодными для использования в указанных целях протоновыми кислотами являются, например, кислоты неорганических и органических солей, как, например, соляная кислота, серная кислота, фосфорная кислота, метансульфокислота, p-толуолсульфокислота или карбоновые кислоты, как, например, уксусная кислота. Особенно предпочтительна среди них p-толуолсульфокислота.
Пригодными кислотами Льюиса являются, например, тетрахлорид олова, хлорид алюминия, хлорид цинка или этерат трифторида бора. Тетрахлорид олова и хлорид алюминия особенно предпочтительны.
Пригодными силикатами алюминия являются, например, такие, которые находят широкое применение в нефтехимии и которые называют также аморфными силикатами алюминия. Эти соединения содержат приблизительно 10-30% окиси кремния и 70-90% окиси алюминия. Особенно предпочтителен силикат алюминия HA-HPV® Ketjen (Akzo).
Пригодными ионитовыми смолами являются, например, стирол-дивинилбензольные смолы, несущие еще и сульфокислотные группы, как, например, Amberlite 200® и Amberlyst® фирмы Rohm и Haas или Dowex 50® фирмы Dow Chemicals; перфорированные ионитовые смолы, как, например, Nafion H® фирмы DuPont; или другие сверхкислые ионитовые смолы, как описанные T.Jamaguchi, Applied Catalysis, 61, 1-25 (1990) или M.Hino et al., Journ. Chem. Soc. Chem. Commun. 1980. 851-852.
Пригодными цеолитами являются, например, такие из них, которые широко распространены в нефтехимии, где их используют в качестве катализаторов крекинга, и известны как кристаллические окиси кремния-алюминия с различной кристаллической структурой. Особенно предпочтительны фауязиты фирмы Union Carbide, как, например, Zeolith X®,Zeolith Y® и сверхстабильный Zeolith Y®;Zeolith Beta® и Zeolith ZSM-12® фирмы Mobil Oil Co., и Zeolith Mordenit® фирмы Norton.
Пригодными, встречающимися в природе слоистыми силикатами, называемыми также "Кислыми землями", являются, например, бентониты или монмориллониты, которые промышленным способом расщепляют, измельчают, обрабатывают минеральными кислотами и кальцинируют. Особенно пригодными из вышеназванных слоистых силикатов являются силикаты типа Fulcat® фирмы Laporte Adsorbents Co., как, например, Fulcat 22A®,Fulcat 22B®,Fulcat 20®, Fulcat 30® или Fulkat 40®; или силикаты типа Fulmont® фирмы Laporte Adsorbents Co., как, например, Fulmont XMP-3® или Fulmont XMP-4®. Особо предпочтительным катализатором для использования в способе по изобретению является Fulcat 22B®. Но и другие силикаты типа Fulcat® и типа Fulmont® вписываются в этот предпочтительный ряд, поскольку между отдельными типами имеются лишь незначительные различия, как, например, в количестве кислотных центров.
Модифицированные слоистые силикаты, называемые также "Pillared Clays", представляют собой модификации описанных выше, встречающихся в природе слоистых силикатов, поскольку содержат между слоями еще и окислы, например, циркония, железа, цинка, никеля, хрома, кобальта или магния. Этот тип катализаторов описан в ряде публикаций, как, например, у J.Clark et al., Journ. Chem. Soc. Chem. Commun. 1989, 1353-1354, широко распространен, однако его изготовлением занимается очень мало фирм. Особенно предпочтительны среди модифицированных слоистых силикатов, например, Envirocat EPZ-10®, Envirocat EPZG® или Envirocat EPIC® фирмы Contract Chemicals.
Очень предпочтителен также способ получения соединений формулы I, где обменную реакцию осуществляют в присутствии катализатора, представляющего собой встречающийся в природе слоистый силикат или модифицированный слоистый силикат.
Особенно предпочтителен способ получения соединений формулы I, в котором обменную реакцию осуществляют в присутствии катализатора типа Fulcat®. Катализатор применяют предпочтительно в количестве от 1 до 60 мас.%, при использовании особенно предпочтительного катализатора типа Fulcat® количество этого последнего составляет 1-30 мас.% по отношению к применяемому соединению формулы III.
Особый интерес представляет также способ получения соединений формулы I, где при n=1 молярное соотношение между соединением формулы III и соединением формулы IV составляет 1: 1-1:20, а при n=2 это молярное соотношение между соединением формулы III и соединением формулы IV составляет 3:1-2:1.
В способе по изобретению при взаимодействии с соединениями формулы IV, с помощью которых и в других известных электрофильных реакциях замещения получают смеси изомеров, также могут образовываться смеси изомеров соединений формулы I. Относительное распределение изомеров происходит по общеизвестным основным принципам органической химии касательно электрофильных ароматических реакций замещения.
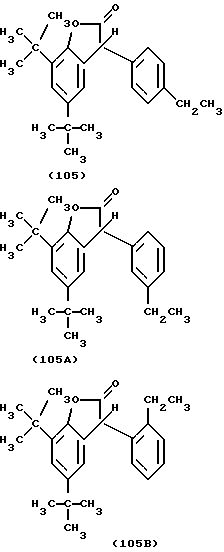
Как описано в примере 4, например, исходя из 5,7-ди-трет.- бутил-3-гидрокси-ЗH-бензофуран-2-она (соединение (201), таблица 2), с помощью этилбензола и Fulcat 22В в качестве катализатора получают 59,2% пара-изомера (соединение (105), таблица 1), 10,8% мета-изомера (соединение (105А)) и 21,1% орто-изомера (соединение (105В)).
Изомеры могут очищаться и разделяться путем кристаллизации фракций или посредством хроматографии, например, на силикагеле. В качестве стабилизаторов органических материалов применяют предпочтительно смеси изомеров.
Соединения формулы IV известны и частично имеются в продаже или же могут быть получены с помощью известных способов.
Соединения формулы III, где R'15 обозначает водород, могут быть представлены, как это описано у H.Sterk et al., Monatshefte fuer Chemie 99. 2223 (1968), частично в их таутомерных формах согласно формулам IIIa или IIIb.
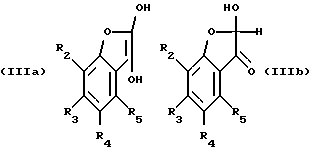
В рамках настоящей заявки формулу III во всех случаях следует понимать как включающую в себя обе вышеприведенные таутомерные формулы IIIa и IIIb.
Соединения формулы III могут быть получены аналогично тому, как это описано в упомянутых выше публикациях. Предпочтителен, однако, новый способ, являющийся предметом изобретения параллельной заявки, отличающийся тем, что
а) один эквивалент фенола формулы VII,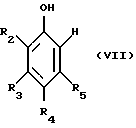
где общие символы имеют те же значения, что и в формуле I, с помощью 0,8-2,0 эквивалентов глиоксиловой кислоты, прежде всего 0,8-1,2 эквивалента глиоксиловой кислоты, преобразуют в соединение формулы VIII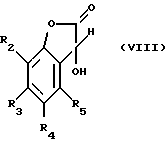
где общие символы имеют те же значения, что и в формуле I, и
б) для получения соединений формулы I, где R'15 обозначает не водород, полученное соединение формулы VIII подвергают обменной реакции с галогеноводородной кислотой, галогенидом кислоты, содержащей серу и кислород, галогенидом фосфорной кислоты, галогенидом фосфористой кислоты, кислотой формулы IX
R'15-OH
галогенидом кислоты формулы X
R'15-Y
сложным эфиром формулы XI
R'15-O-R38
симметричным либо несимметричным ангидридом формулы XII
R'15-O-R'15
или изоцианатом формулы XIII
R39-N=C=O
где R'15 имеет указанное выше значение, при условии, что R'15 в соединениях формул IX, X, XI и XII обозначает не водород;
R38 представляет собой C1-C8-алкил,
R39 обозначает C1-C18-алкил или фенил и
Y обозначает фтор, хлор, бром или йод.
Глиоксиловую кислоту можно применять либо в кристаллической форме либо предпочтительно в виде имеющегося в продаже водного раствора, как правило, 40-60%-ного водного раствора.
Особый интерес поэтому представляет также способ получения соединений формулы VIII, где глиоксиловую кислоту применяют в виде 40-60%-ного, прежде всего 50%-ного, водного раствора этой кислоты.
Содержащуюся в глиоксиловой кислоте воду, равно как и реакционную воду во время проведения обменной реакции отгоняют. При этом используют предпочтительно азеотропно кипящий с водой растворитель.
Такими азеотропно кипящими с водой растворителями являются, например, углеводороды, как, например, циклогексан или метилциклогексан; ароматические углеводороды, как, например, бензол или толуол; галогенированные углеводороды, как, например, 1,2-дихлорэтан; или же простые эфиры, как, например, метил-трет.-бутиловый эфир.
Если преобразование фенола формулы VII с помощью глиоксиловой кислоты в соединения формулы VIII проводить без растворителя в расплаве, то реакционную воду целесообразно отгонять при нормальном давлении, прежде всего предпочтительно в легком вакууме.
Реакцию осуществляют предпочтительно при повышенной температуре, прежде всего в диапазоне от 60 до 120oC. Особенно предпочтителен диапазон температур от 60 до 90oC.
За счет добавок небольшого количества протоновой кислоты, как, например, p-толуолсульфокислота, метансульфокислота, серная кислота или соляная кислота, одной из кислот Льюиса, как, например, этерат трифторида бора или хлорид алюминия, реакции можно придать каталитический характер. Количество катализатора составляет 0,01-5 мол.%, предпочтительно 0,1-1,0 мол.% по отношению к массе используемого фенола формулы VII.
Условия проведения ступени б) способа получения соединений формулы III, где R'15 обозначает не водород, исходя из соединений формулы VIII, общеизвестны и могут выбираться, например, аналогично рекомендациям по этерификации, описанным в Organikum 1986. стр.186-191, стр.388 и стр.402-408.
Пригодными галогеноводородными кислотами являются, например, соляная кислота, бромистоводородная кислота или йодистоводородная кислота. Предпочтительна соляная кислота.
Пригодными галогенидами кислоты, содержащей серу и кислород, являются, например, тионилхлорид, сульфурилхлорид или тионилбромид. Предпочтителен среди них тионилхлорид.
Пригодными галогенидами фосфорной кислоты и фосфористой кислоты являются, например, трихлорид фосфора, трибромид фосфора, трийодид фосфора, пентахлорид фосфора, хлорокись фосфора или пентафторид фосфора. Особенно предпочтительна хлорокись фосфора.
При проведении ступени б) способа предпочтительно применяют галогенид кислоты, содержащей серу и кислород, как, например, тионилхлорид; галогенид кислоты формулы X; сложный эфир формулы XI; или симметричный ангидрид формулы XII.
Если при проведении ступени б) способа применяют галогенид кислоты, содержащей серу и кислород, как, например, тионилхлорид, то обменную реакцию с соединением формулы VIII осуществляют предпочтительно без растворителя и при температуре в диапазоне от 0 до 40oC, прежде всего при комнатной температуре. При этом тионилхлорид целесообразно применять с 2-10-кратным, прежде всего с 2-6-кратным избытком по отношению к количеству используемого соединения формулы VIII. Реакцию можно проводить также в присутствии катализатора, как, например, диметилформамид.
Если на ступени б) способа применяют кислоту формулы IX (R'15-OH), то обменную реакцию с соединением формулы VIII проводят предпочтительно в присутствии инертного органического растворителя, как, например, дихлорметан, диоксан, простой диэтиловый эфир или тетрагидрофуран, и в присутствии реагента, связывающего воду физическим или химическим путем, как, например, молекулярное сито или дициклогексилкарбодиимид.
Если при проведении ступени б) способа применяют галогенид кислоты формулы X (R'1-Y), где Y обозначает предпочтительно хлор или бром, прежде всего хлор, то обменную реакцию с соединением формулы VIII осуществляют предпочтительно в присутствии растворителя и основания.
Основание можно применять в различных количествах, начиная от каталитического и стехиометрического и кончая многократным молярным избытком по отношению к соединению формулы VIII. Образующийся, например, при реакции хлористый водород при определенных условиях переводят с помощью основания в хлорид, который может быть удален посредством фильтрации и/или промывания соответствующей жидкой либо твердой фазой; при этом может использоваться также еще один, несмешиваемый с водой растворитель. Очистку продукта целесообразно осуществлять путем перекристаллизации остатка концентрированной или упаренной до сухого состояния органической фазы.
Пригодными для проведения реакции растворителями являются в частности углеводороды (например, толуол, ксилол, гексан, пентан или другие петролейноэфирные фракции), галогенированные углеводороды (например, ди- либо трихлорметан, 1,2-дихлорэтан, 1,1,1-трихлорэтан), простые эфиры (например, диэтиловый эфир, дибутиловый эфир или тетрагидрофуран), далее, ацетонитрил, диметилформамид, диметилсульфоксид или N-метилпирролидон.
Пригодными для проведения реакции основаниями являются в частности амины, например, триэтиламин, триметиламин, трибутиламин, N,N-димeтилaнилин, N, N-диэтиланилин; пиридины; гидриды (например, гидрид лития, гидрид натрия, гидрид калия) или алкоголяты (например, метилат натрия).
Если при проведении ступени б) способа применяют сложный эфир формулы XI (R'15-O-R38), где R38 обозначает предпочтительно C1-C4-алкил, прежде всего метил или этил, то обменную реакцию с соединением формулы VIII осуществляют предпочтительно в присутствии растворителя, образующего со спиртами азеотропные смеси. Образующийся во время реакции спирт (R38-OH) может отгоняться непрерывно.
Пригодные для проведения реакции азеотропно кипящие со спиртами растворители не участвуют в ней; таковыми являются, например, углеводороды, как, например, циклогексан; ароматические углеводороды, как, например, бензол или толуол; галогенированные углеводороды, как, например, 1,2-дихлорэтан; или же простые эфиры, как, например, метил-трет.-бутиловый эфир.
Скорость реакции можно регулировать за счет введения добавок катализаторов, а именно, небольшого количества какой-либо протоновой кислоты, как, например, p-толуолсульфокислота, метансульфокислота, серная кислота или соляная кислота; а также одной из кислот Льюиса, как, например, этерат трифторида бора или хлорид алюминия.
Если при проведении ступени б) способа применяют симметричный ангидрид формулы XII (R'15-O-R'15), где R'15 обозначает предпочтительно C2-C6-алканоил, прежде всего ацетил, то обменную реакцию с соединением формулы VIII осуществляют предпочтительно без добавок второго растворителя и при температуре в диапазоне от 20 до 200oC, например, при температуре кипения ангидрида формулы XII, прежде всего в диапазоне 60-180oC.
Если при проведении ступени б) способа применяют изоцианат формулы XIII (R39-N= C= O), то обменную реакцию с соединением формулы VIII осуществляют предпочтительно без добавок второго растворителя и при температуре в диапазоне от 20 до 200oC, например, при температуре кипения изоцианата формулы XIII, прежде всего в диапазоне 60-180oC.
Обменную реакцию с изоцианатом осуществляют также предпочтительно в присутствии катализатора. Предпочтительными являются те же самые катализаторы, которые упоминались выше при описании обменной реакции между соединением формулы III и соединением формулы IV.
Фенолы формулы VII известны или могут быть получены с помощью известных методов.
Бисфенольные соединения формулы XIV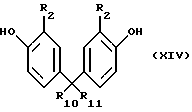
могут быть получены по методу согласно Houben-Weyl, Methoden der organischen Chemie, том 6/1c, 1030.
Соединения формулы I можно получать также по так называемому методу получения в одном аппарате, исходя из фенолов формулы VII.
Настоящее изобретение относится поэтому также к способу получения соединений формулы I,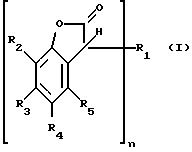
отличающемуся тем, что один эквивалент фенола формулы VII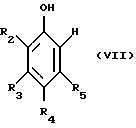
с помощью 0,8-2,0 эквивалентов глиоксиловой кислоты преобразуют в соединение формулы VIII,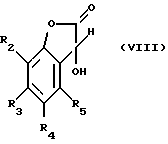
которое затем без выделения подвергают реакции с соединением формулы IV
[H]n-R1
Расшифровка общих символов в заявляемом по изобретению способе получения в одном аппарате аналогична расшифровке, приведенной выше для другого способа согласно изобретению.
Предпочтительные параметры реакции в способе получения в одном аппарате соответствуют предпочтительным параметрам, указанным подробно выше для двух ступеней способа.
Образующиеся сначала при осуществлении способа получения в одном аппарате 3-гидрокси-3H-бензофуран-2-оны формулы VIII до проведения последующей обменной реакции с соединением формулы IV могут подвергаться реакции на дополнительной стадии, заключающейся в том, что гидроксильную группу замещают галогеном или активируют уходящей группой.
Настоящее изобретение относится поэтому к способу получения соединений формулы I в одном аппарате, отличающемуся тем, что один эквивалент фенола формулы VII с помощью 0,8-2,0 эквивалентов глиоксиловой кислоты преобразуют в 3-гидрокси-3H-бензофуран-2-оны формулы VIII и без выделения до проведения последующей обменной реакции с соединением формулы IV на дополнительной стадии способа с помощью галогенводородной кислоты, галогенида кислоты, содержащей серу и кислород, галогенида фосфорной кислоты, галогенида фосфористой кислоты, кислоты формулы IX,
R'15-OH
галогенида кислоты формулы X,
R'15-Y
сложного эфира формулы XI,
R'15-O-R38
симметричного либо несимметричного ангидрида формулы XII
R'15-O-R'15
или изоцианата формулы XIII,
R39-N=C=O
где R'15 в формулах IX, X, XI и XII обозначает не водород;
R38 представляет собой C1-C8-алкил,
R39 представляет собой C1-C18-алкил или фенил и
Y обозначает фтор, хлор, бром или йод, преобразуют в соединения формулы III,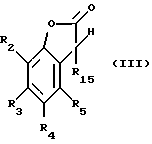
где R15 представляет собой -OR'15, a R'15 является не водородом.
Предпочтительные параметры реакции на этой дополнительной стадии осуществления способа аналогичны параметрам, описанным подробно выше при получении соединений формулы III, исходя из соединений формулы VIII.
Особо предпочтительный способ получения соединений формулы I в одном аппарате отличается тем, что применяемое соединение формулы VII не идентично применяемому соединению формулы IV.
Изобретение поясняется подробнее на нижеследующих примерах. Все данные, указанные в частях или процентах, относятся к массе.
Пример 1: Способ получения 5,7-ди-трет.-бутил-3-(2,5- диметилфенил)-3H-бензофуран-2-она (соединение (101), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью p-ксилола, а также Fulcat 22В в качестве катализатора.
а) Получение 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2).
Смесь из 212,5 г (1,00 моль) 2,4-ди-трет.-бутил-фенола (97%-ный), 163,0 г (1,10 моля) 50%-ной водной глиоксиловой кислоты и 0,5 г (2,6 ммоля) моногидрата p-толуолсульфокислоты в 300 мл 1,2-дихлорэтана кипятят в атмосфере азота в течение 3,5 ч с использованием водоотделителя и обратного холодильника. Затем реакционную смесь концентрируют в вакуумно-ротационном испарителе. Остаток растворяют в 800 мл гексана и трижды промывают водой. Водные фазы отделяют в разделительной воронке, после чего экстрагируют с помощью 300 мл гексана. Органические фазы соединяют, сушат над сульфатом магния и концентрируют в вакуумно-ротационном испарителе. В качестве остатка получают 262,3 г (~100%) аналитически чистого 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она в виде густой смолы желтоватого цвета (соединение (201), таблица 2).
Аналогично примеру 1а из соответствующих фенолов, как, например, 2-трет. -бутил-4-метил-фенол, 4-трет.-бутил-2-метил-фенол, 2,4-дициклогексил-фенол, 2-(гексадец-2-ил)-4-метил-фенол, 3-[3-трет.-бутил-4-гидрокси-фенил]-пропионовая кислота, 2,4-ди α,α- диметилбензил)-фенол и 4-метил-2-(1,1,3,3-тетраметил-бут-1-ил)-фенол, с помощью глиоксиловой кислоты получают соединения (202), (203), (204), (205), (209), (210) и (211). Для получения соединения (207) используют, исходя из 1,1-бис-(3-трет.-бутил-4-гидрокси-фенил)- циклогексана, два эквивалента глиоксиловой кислоты.
б) Получение 5,7-ди-трет.-бутил-3-(2,5-диметилфенил)-3H- бензофуран-2-она (соединение (101), таблица 1).
Раствор из 262,3 г (1,00 моль) 5,7-ди-трет.-бутил-3-гидрокси- 3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а) в 500 мл (4,05 моля) p-ксилола обрабатывают 40 г Fulcat 22В и кипятят с обратным холодильником в течение 1,5 ч в водоотделителе. Затем катализатор Fulcat 22В отфильтровывают, а избыточный p-ксилол отгоняют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из 400 мл метанола получают 280,6 г (80%) 5,7-ди-трет. -бутил-3-(2,5- диметилфенил)-3H-бензофуран-2-она, т. пл. 93-97oC (соединение (101), таблица 1).
Пример 2: Способ получения 5,7-ди-трет.-бутил-3-(2,5- диметилфенил)-3H-бензофуран-2-она (соединение (101), таблица 1), исходя из 3-ацетокси-5,7-ди-трет.-бутил-3H-бензофуран-2-она (соединение (206), таблица 2), с помощью p-ксилола, а также Fulcat 22В в качестве катализатора.
а) Получение 3-ацетокси-5,7-ди-трет.-бутил-3H-бензофуран-2-она (соединение (206), таблица 2).
Смесь из 21,2 г (0,10 моля) 2,4-ди-трет.-бутил-фенола (97%-ный), 16,3 г (0,11 моля) 50%-ной водной глиоксиловой кислоты и 0,05 г (0,26 ммоля) моногидрата p-толуолсульфокислоты в 30 мл 1,2-дихлорэтана кипятят с обратным холодильником в атмосфере азота в течение 3,5 ч в водоотделителе. Затем реакционную смесь концентрируют в вакуумно-ротационном испарителе. Остаток обрабатывают 9,9 мл (0,105 моля) ангидрида уксусной кислоты и кипятят в течение 90 мин с обратным холодильником. Затем реакционную смесь охлаждают до комнатной температуры, разбавляют 100 мл трет.-бутил-метилового эфира и промывают последовательно водой и разбавленным раствором бикарбоната натрия. Водные фазы отделяют и экстрагируют с помощью 50 мл трет.-бутил-метилового эфира. Органические фазы соединяют, сушат над сульфатом магния и концентрируют в вакуумно-ротационном испарителе. После хроматографии остатка на силикагеле с помощью системы растворителей дихлорметан/гексан=2:1 получают 28,0 г (92%) 3-ацетокси-5,7-ди- трет.-бутил-3H-бензофуран-2-она в виде густой, красноватой смолы (соединение (206), таблица 2).
б) Получение 5,7-ди-трет.-бутил-3-(2,5-диметилфенил)-3H- бензофуран-2-она (соединение (101), таблица 1).
Раствор из 15,3 г (50,0 ммолей) 3-ацетокси-5,7-ди-трет.-бутил- 3H-бензофуран-2-она (соединение (206), таблица 2, пример 2а) в 25 мл (0,20 моля) p-ксилола обрабатывают 1,0 г Fulcat 22В и кипятят с обратным холодильником в течение 17 ч в водоотделителе. Затем катализатор Fulcat 22В отфильтровывают, а избыточный p-ксилол отгоняют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из 20 мл метанола получают 10,5 г (60%) 5,7-ди-трет. -бутил-3-(2,5- диметилфенил)-3H-бензофуран-2-она, т. пл. 93-97oC (соединение (101), таблица 1).
Пример 3: Способ получения 3-(3,4-диметилфенил)-5,7-ди-трет.- бутил-3H-бензофуран-2-она (соединение (103), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью o-ксилола, а также Fulcat 22В в качестве катализатора.
Раствор из 262,3 г (1,00 моль) 5,7-ди-трет.-бутил-3-гидрокси- 3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а) в 500 мл (4,05 моля) о-ксилола обрабатывают 40 г Fulcat 22В и кипятят с обратным холодильником в течение 1,5 ч в водоотделителе. Затем катализатор Fulcat 22В отфильтровывают, а избыточный o-ксилол отгоняют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из 500 мл метанола получают 244 г (69%) 3-(3,4-диметилфенил)-5,7-ди-трет. -бутил-3H-бензофуран-2-она, т. пл. 130-132oC (соединение (103), таблица 1), содержащего еще приблизительно 1,3% структурного изомера [3-(2,3-диметилфенил)-5,7-ди-трет.-бутил- 3H-бензофуран-2-она, соединение (103А)] . Из маточного раствора получают еще 42,4 г продукта, состоящего согласно анализу ГХ-МС из 12,3% соединения (103) и 87,7% изомерного соединения (103А).
Пример 4: Способ получения 5,7-ди-трет.-бутил-3-(4-этилфенил)- 3H-бензофуран-2-она (соединение (105), таблица 1), исходя из 5,7- ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью этилбензола, а также Fulcat 22В в качестве катализатора.
Раствор из 262,3 г (1,00 моль) 5,7-ди-трет.-бутил-3-гидрокси- 3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а) в 500 мл (4,08 моля) этилбензола обрабатывают 40 г Fulcat 22В и кипятят с обратным холодильником в течение 1,5 ч в водоотделителе. Затем катализатор Fulcat 22В отфильтровывают, а избыточный этилбензол отгоняют в вакуумно-ротационном испарителе. Согласно анализу ГХ-МС в качестве остатка получают смесь из 59,2% пара-изомера (соединение (105), таблица 1), 10,8% мета-изомера (соединение (105А)) и 21,1% орто-изомера (соединение (105В)). После кристаллизации остатка из 400 мл метанола получают 163,8 г 5,7-ди-трет.-бутил-3-(4-этилфенил)-3H-бензофуран-2-она (соединение (105), таблица 1) (пара-изомер), содержащего еще 5,6% мета-изомера (5,7-ди-трет. -бутил-3-(3-этилфенил)-3H-бензофуран-2-он (соединение (105А)) и 1,3% орто-изомера (5,7-ди-трет.-бутил-3-(2-этилфенил)- 3H-бензофуран-2-он (соединение (105В)). Посредством повторной кристаллизации из метанола может быть получен практически чистый пара-изомер (соединение (105), таблица 1), т. пл. 127-132oC.
Аналогично примеру 4 из 5,7-ди-трет.-бутил-3-гидрокси-3H- бензофуран-2-она (соединение (201), таблица 2, пример 1а) и соответствующих ароматических углеводородов, как, например, m-ксилол, изопропилбензол (кумол), трет. -бутилбензол, 2,6- диметиланизол, анизол, ацетоксиэтоксибензол, хлорбензол, бифенил, тиофен, p-ксилол, дибензофуран, фенантрен и простой дифениловый эфир, получают соединения (102), (106), (107), (116), (117), (118), (120), (122), (123), (124), (125), (126) и (127). Для получения соединения (127), исходя из простого дифенилового эфира, используют два эквивалента 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она.
Пример 5: Способ получения 5,7-ди-трет.-бутил-3-(2,3,4,5,6- пентаметилфенил)-3H-бензофуран-2-она (соединение (III), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью пентаметилбензола, а также тетрахлорида цинка в качестве катализатора.
Раствор из 19,7 г (75,0 ммолей) 5,7-ди-трет.-бутил-3-гидрокси- 3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а) в 50 мл 1,2-дихлорэтана обрабатывают 11,5г (77,5 ммолей) пентаметилбензола и 10 мл (85,0 ммолей) тетрахлорида цинка и затем кипятят с обратным холодильником в течение одного часа. Реакционную смесь обрабатывают водой и трижды экстрагируют с помощью толуола. Органические фазы отделяют, промывают водой, соединяют, сушат над сульфатом натрия и концентрируют в вакуумно-ротационном испарителе. После кристаллизации остатка из этанола получают 26,3 г (89%) 5,7- ди-трет.-бутил-3-(2,3,4,5,6-пентаметилфенил)-3H-бензофуран-2-она, т. пл. 185-190oC (соединение (III), таблица 1).
Аналогично примеру 5 из 5,7-ди-трет.-бутил-3-гидрокси-3H- бензофуран-2-она (соединение (201), таблица 2, пример 1а) и соответствующих ароматических углеводородов, как, например, n-додецилбензол и 1,2,3-триметилбензол, получают соединения (109) и (110).
Пример 6: Способ получения 5,7-ди-трет.-бутил-3-фенил-3H- бензофуран-2-она (соединение (108), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью бензола, а также трихлорида алюминия в качестве катализатора.
Раствор из 131,2 г (0,50 моля) 5,7-ди-трет.-бутил-3-гидрокси- 3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а) в 250 мл (2,82 моля) бензола обрабатывают в течение 25 мин 73,3 г (0,55 моля) измельченного трихлорида алюминия и в течение 1,5 часа нагревают с обратным холодильником, после чего кипятят с обратным холодильником еще в течение 1,5 часа. Реакционную смесь охлаждают до комнатной температуры и при охлаждении осторожно обрабатывают сначала 200 мл воды и потом таким количеством концентрированной соляной кислоты, пока не образуется гомогенная двухфазовая смесь. Затем органическую фазу отделяют, промывают водой, сушат над сульфатом натрия и концентрируют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из этанола получают 97,8 г (64%) 5,7-ди-трет.-бутил-3-фенил-3H-бензофуран-2-она, т. пл. 116-119oC (соединение (109), таблица 1).
Аналогично примеру 6 из соответствующих 3-гидрокси-3H- бензофуран-2-онов, как, например, 7-[2-(гексадец-2-ил)]-3-гидрокси- 5-метил-3H-бензофуран-2-он (соединение (205), таблица 2), 5,7-дициклогексил-3-гидрокси-3H-бензофуран-2-она (соединение (204), таблица 2) и 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2) и соответствующих ароматических углеводородов, как, например, бензол и тиоанизол, получают соединения (113), (114) и (119).
Пример 7: Способ получения 5,7-ди-трет.-бутил-3-(4-метилфенил)-3H-бензофуран-2-она (соединение (104), таблица 1), исходя из 2,4-ди-трет.-бутилфенола, без выделения 5,7-ди-трет. - бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2) с помощью глиоксиловой кислоты и толуола, а также Fulcat 22В в качестве катализатора.
Смесь из 21,2 г (0,10 моля) 2,4-ди-трет.-бутилфенола (97%-ный), 16,3 г (0,11 моля) 50%-ной водной глиоксиловой кислоты, 2,0 г Fulcat 22В и 50 мл толуола кипятят с обратным холодильником в атмосфере азота в течение 8 ч в водоотделителе. Затем катализатор Fulcat 22В отфильтровывают, а избыточный толуол отгоняют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из 40 мл этанола получают 14,2 г (42%) 5,7-ди-трет.-бутил-3-(4- метилфенил)-3H-бензофуран-2-она, т. пл. 130-133oC (соединение (104), таблица 1).
Аналогично примеру 7, исходя из 2-трет. -бутил-4-метилфенола вместо 2,4-ди-трет.-бутилфенола, получают соединение (112).
Пример 8: Способ получения 4,4'-ди-(5,7-ди-трет.-бутил-3H- бензофуран-2-он-3-ил)-N-метил-дифениламина (соединение (121), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью N-метил-дифениламина, а также p-толуолсульфокислоты в качестве катализатора.
В кипящий раствор из 9,20 г (50,0 ммолей) N-метил-дифениламина и 0,20 г моногидрата p-толуолсульфокислоты в 50 мл лигроина (алкановая смесь с диапазоном кипения 140-160oC) в течение 2 ч добавляют 30,2 г (115,0 ммолей) 5,7-ди-трет.-бутил-3-гидрокси-3H- бензофуран-2-она (соединение (201), таблица 2, пример 1а). Затем реакционную смесь в течение 4 ч кипятят с обратным холодильником в водоотделителе, после чего реакционную смесь охлаждают и концентрируют в вакуумно-ротационном испарителе. После двухкратной кристаллизации остатка из изопропанола/воды= 9:1 получают 18,9 г (56%) 4,4'-ди-(5,7-ди-трет. -бутил-3H-бензофуран-2-он-3-ил)-N-метил- дифениламина, т. пл. 135-145oC (соединение (121), таблица 1).
Пример 9: Способ получения 5,7-ди-трет.-бутил-3-(3,5-диметил- 4-гидрокси-фенил)-3H-бензофуран-2-она (соединение (115), таблица 1), исходя из 5,7-ди-трет.-бутил-3-гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2), с помощью 2,6-диметилфенола, а также p-толуолсульфокислоты в качестве катализатора.
В кипящий раствор из 12,2 г (100,0 ммолей) 2,6-диметилфенола и 0,20 г моногидрата p-толуолсульфокислоты в 50 мл уксусной кислоты в течение 2 ч добавляют 30,2 г (115,0 ммолей) 5,7-ди-трет.-бутил-3- гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2, пример 1а). Затем реакционную смесь кипятят с обратным холодильником в течение 4 ч, после чего реакционную смесь охлаждают и концентрируют с помощью вакуумно-ротационного испарителя. После двухкратной кристаллизации остатка из изопропанола/воды=9:1 получают 28,5 г (78%) 5,7-ди-трет. -бутил-3-(3,5-диметил-4-гидрокси-фенил)-3H- бензофуран-2-она, т. пл. 225-228oC (соединение (115), таблица 1).
Пример 10: Способ получения 7-трет.-бутил-5-метил-3-(9-метил- 9Н-карбазол-3-ил)-3H-бензофуран-2-она (соединение (128), таблица 1), исходя из 7-трет.-бутил-3-гидрокси-5-метил-3H-бензофуран-2-она (соединение (202), таблица 2), с помощью N-метилкарбазола и n-октана, а также Fulcat 22В в качестве катализатора.
Смесь из 2,2 г (10,0 ммолей) 7-трет.-бутил-3-гидрокси-5-метил- 3H-бензофуран-2-она (соединение (202), пример 1а, таблица 2), 1,8 г (10,0 ммолей) N-метилкарбазола и 0,2 г Fulcat 22В и 20 мл n-октана кипятят с обратным холодильником в атмосфере азота в течение 5 ч. Затем катализатор Fulcat 22В отфильтровывают, а избыточный n-октан отгоняют с помощью вакуумно-ротационного испарителя. После хроматографии остатка на силикагеле с помощью системы растворителей дихлорметан/гексан = 1:2-1:1 и последующей кристаллизации чистых фракций из метанола получают 0,70 г (10%) 7-трет.-бутил-5-метил-3-(9-метил-9Н-карбазол-3-ил)-3H-бензофуран-2-она, т. пл. 84-90oC (соединение (128), таблица 1). Этот продукт может содержать в малом количестве еще и другие структурные изомеры касательно замещения в карбазольном кольце.
Пример 11: Способ получения 5,7-ди-трет.-бутил-3-(9Н-флуорен-3-ил)-3H-бензофуран-2-она (соединение (129), таблица 1), исходя из 2,4-ди-трет.-бутилфенола, без выделения 5,7-ди-трет.-бутил-3- гидрокси-3H-бензофуран-2-она (соединение (201), таблица 2) с помощью глиоксиловой кислоты и флуорена, а также p-толуолсульфокислоты и Fulcat 22В в качестве катализатора.
Смесь из 15,9 г (75 ммолей) 2,4-ди-трет.-бутилфенола (97%-ный), 12,2 г (82 ммоля) 50%-ной водной глиоксиловой кислоты, 40 мг (0,20 ммоля) моногидрата p-толуолсульфокислоты и 25 мл 1,2-дихлорэтана кипятят в атмосфере азота с обратным холодильником в течение 3,5 ч в водоотделителе. Затем реакционную смесь концентрируют с помощью вакуумно-ротационного испарителя. Остаток растворяют в 30 мл n-октана и обрабатывают 12,5 г (75 ммолей) флуорена и 3 г Fulcat 22В. Эту смесь кипятят с обратным холодильником в атмосфере азота в течение 3,5 ч в водоотделителе. Затем реакционную смесь охлаждают, фильтруют и фильтрат концентрируют с помощью вакуумно-ротационного испарителя. После хроматографии остатка на силикагеле с помощью системы растворителей дихлорметан/гексан=2:1 и последующей кристаллизации чистых фракций из метанола получают 5,28 г (17%) 5,7-ди-трет.-бутил-3-(9Н-флуорен-3-ил)-3H-бензофуран-2-она, т. пл. 140-153oC (соединение (129), таблица 1). Этот продукт может содержать в малом количестве еще и другие структурные изомеры касательно замещения во флуореновом кольце.
Пример 12: Способ получения приблизительно 5,7:1 изомерной смеси из 3-(3,4-диметилфенил)-5,7-ди-трет.-бутил-3H-бензофуран-2-она (соединение (103), таблица 1) и 3-(2,3-диметилфенил)-5,7-ди- трет.-бутил-3H-бензофуран-2-она (соединение (103А)), исходя из 2,4-ди-трет.-бутилфенола, с помощью глиоксиловой кислоты и o-ксилола, а также Fulcat или Fulmont в качестве катализатора.
В реактор с двойной рубашкой объемом 1,5 л, снабженный водоотделителем, загружают 206,3 г (1,0 моль) 2,4-ди-трет.- бутилфенола, 485 г (5,5 молей) o-ксилола, 0,5 г (2,6 ммоля) моногидрата p-толуолсульфокислоты и 163 г (1,1 моля) 50%-ной водной глиоксиловой кислоты. Смесь при перемешивании нагревают до 85-90oC и одновременно из аппаратуры откачивают воздух до остаточного давления примерно 450 мбар. Как только внутренняя температура достигнет 85-90oC, начинают отгонку смеси из o-ксилола/воды, причем o-ксилол идет обратным потоком, а вода выводится из цикла. Вакуум непрерывно повышают, с тем чтобы поддерживать температуру на уровне 85-90oC. В течение 3-4 ч отгоняют в общей сложности приблизительно 98-100 мл воды.
Вакуум декомпрессуют азотом и в прозрачный раствор желтоватого цвета добавляют 40 г катализатора (Fulcat 30 либо 40, Fulmont ХМР-З либо ХМР-4). Из аппаратуры откачивают воздух до остаточного давления 700 мбар и суспензию перемешивают при температуре нагревательной бани 165oC. Образующуюся воду по достижении внутренней температуры примерно 128oC начинают отгонять азеотропным путем. К концу внутренняя температура повышается до максимум 140oC. В общей сложности в течение 1-2 ч выделяется приблизительно 20 мл воды. Затем вакуум декомпрессуют с помощью азота. Реакционную смесь охлаждают до 90-100oC и фильтруют. Аппаратуру и фильтрат промывают 100 г o-ксилола. Фильтрат помещают в реактор с двойной рубашкой объемом 1500 мл и концентрируют в вакууме. При этом повторно получают 360 г o-ксилола. Красновато-желтый остаток охлаждают до 70oC и с помощью капельной воронки осторожно обрабатывают 636 г метанола. Внутреннюю температуру при этом поддерживают на уровне 60-65oC. В раствор вводят затравку и кристаллизуют при перемешивании в течение приблизительно 30 мин при 60-65oC. Затем кристаллическую суспензию в течение 2 ч охлаждают до внутренней температуры -5oC и при этой температуре продолжают перемешивание еще в течение одного часа. Кристаллы фильтруют на нутче и остаток промывают 400 г холодного (-5oC) метанола пятью порциями. Полученный продукт помещают в вакуумно-сушильный шкаф, где сушат его при 50-60oC. В результате получают 266 г белого твердого вещества. Согласно газохроматографическому анализу это вещество состоит из примерно 85% 3-(3,4-диметилфенил)-5,7-ди-трет. - бутил-3H-бензофуран-2-она (соединение (103), таблица 1) и примерно 15% изомерного 3-(2,3-диметилфенил)-5,7-ди-трет.-бутил-3H-бензофуран-2-она (соединение (103А)).
Пример 13: Способ получения 3-(N-метилкарбамоилокси)-5-метил-7-трет.-бутил-3H-бензофуран-3-она (соединение (212), таблица 2).
Смесь из 5,5 г (25,0 ммолей) 7-трет.-бутил-3-гидрокси-5-метил-3H-бензофуран-2-она (соединение (202), пример 1а), 3 мл (50,0 ммолей) метилизоцианата и 2 капель метансульфокислоты кипятят с обратным холодильником в течение 3 1/4 ч. Затем повторно добавляют 3 мл (50,0 ммолей) метилизоцианата и 2 капли метансульфокислоты. После нагрева с обратным холодильником еще в течение 16 ч реакционную смесь охлаждают, разбавляют дихлорметаном и промывают водой и 5%-ным водным раствором гидрокарбоната натрия. Органические фазы соединяют, сушат над сульфатом магния и концентрируют с помощью вакуумно-ротационного испарителя. После кристаллизации остатка из толуола получают 4,45 г (65%) 3-(N-метилкарбамоилокси)-5-метил-7- трет.-бутил-3H-бензофуран-2-она, т. пл. 138-143oC (соединение (212), таблица 2).
Пример 14: Способ получения 7-трет.-бутил-3-хлор-5-метил-3H- бензофуран-2-она (соединение (208), таблица 2).
Суспензию из 2,2 г (10,0 ммолей) 7-трет.-бутил-3-гидрокси-5- метил-3H-бензофуран-2-она (соединение (202), пример 1а, таблица 2) в 2,4 мл (55,0 ммолей) тионилхлорида обрабатывают одной каплей диметилформамида и перемешивают в течение 2 ч при комнатной температуре. Затем избыточный тионилхлорид отгоняют с помощью вакуумно-ротационного испарителя. После хроматографии остатка на силикагеле с помощью системы растворителей дихлорметан/гексан= 1: 1 и кристаллизации чистых фракций из метанола получают 0,30 г (13%) 7- трет. -бутил-3-хлор-5-метил-3H-бензофуран-2-она, т. пл. 81-86oC (соединение (208), таблица 2).
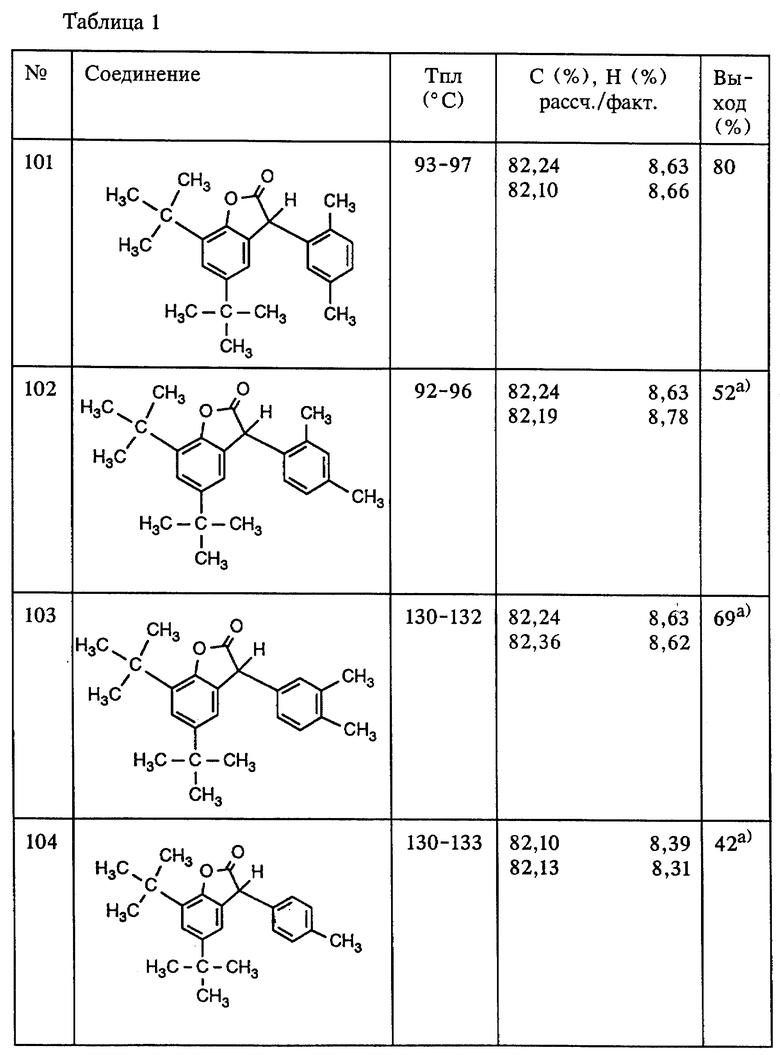
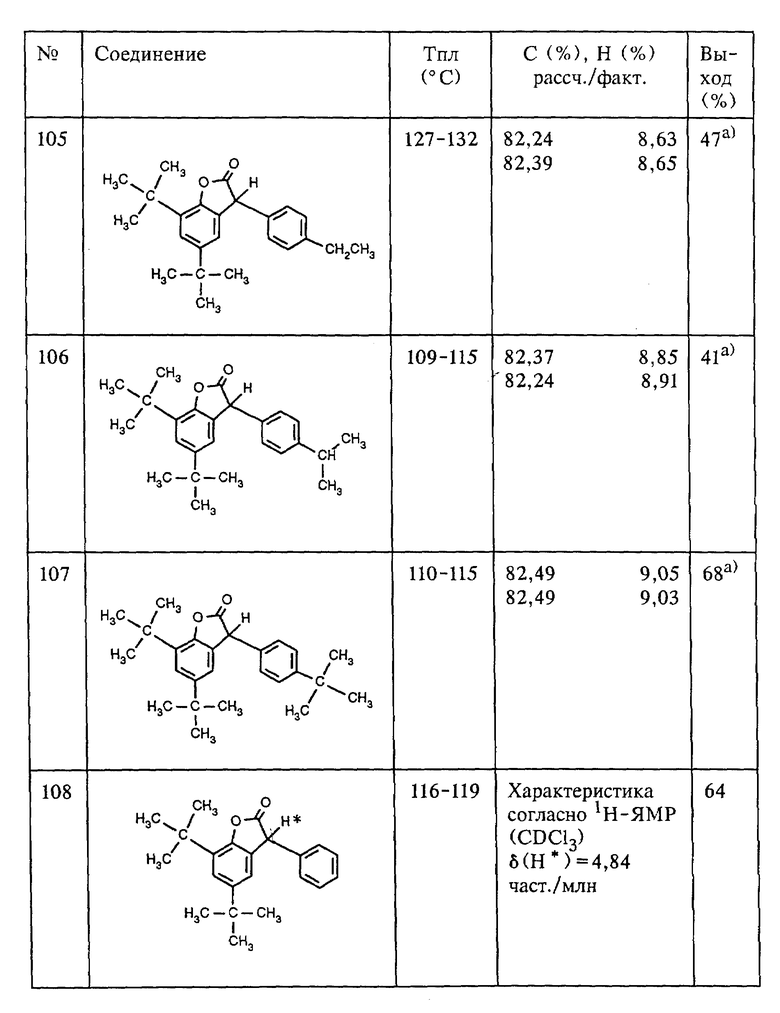
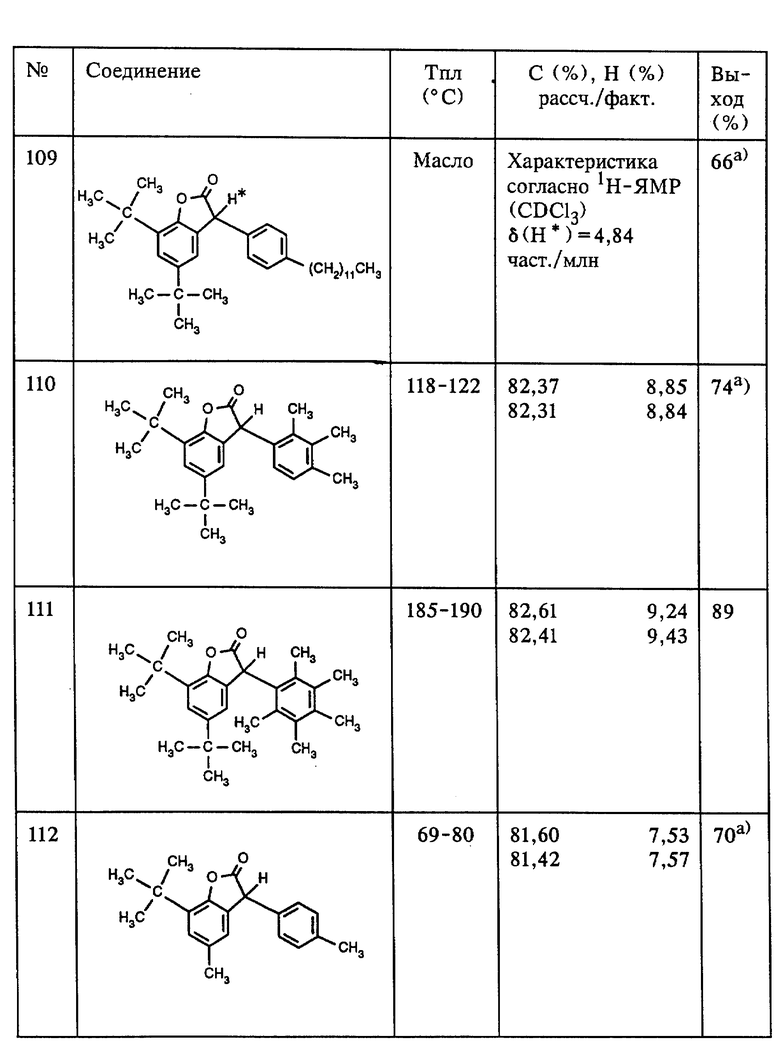
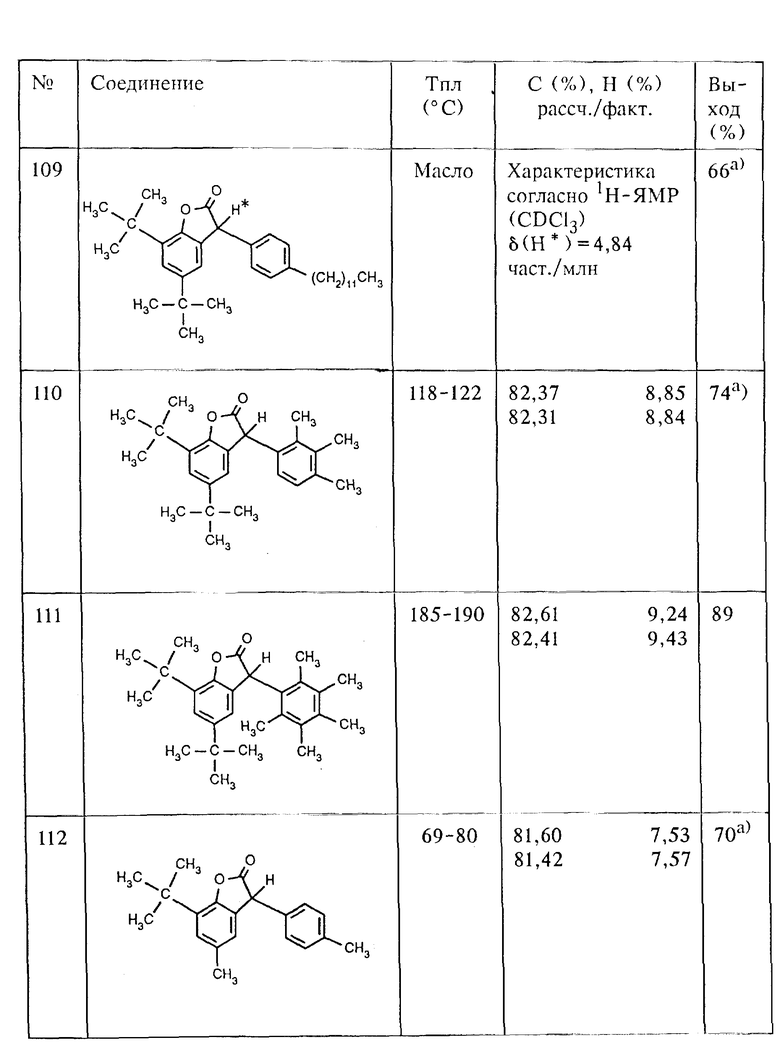
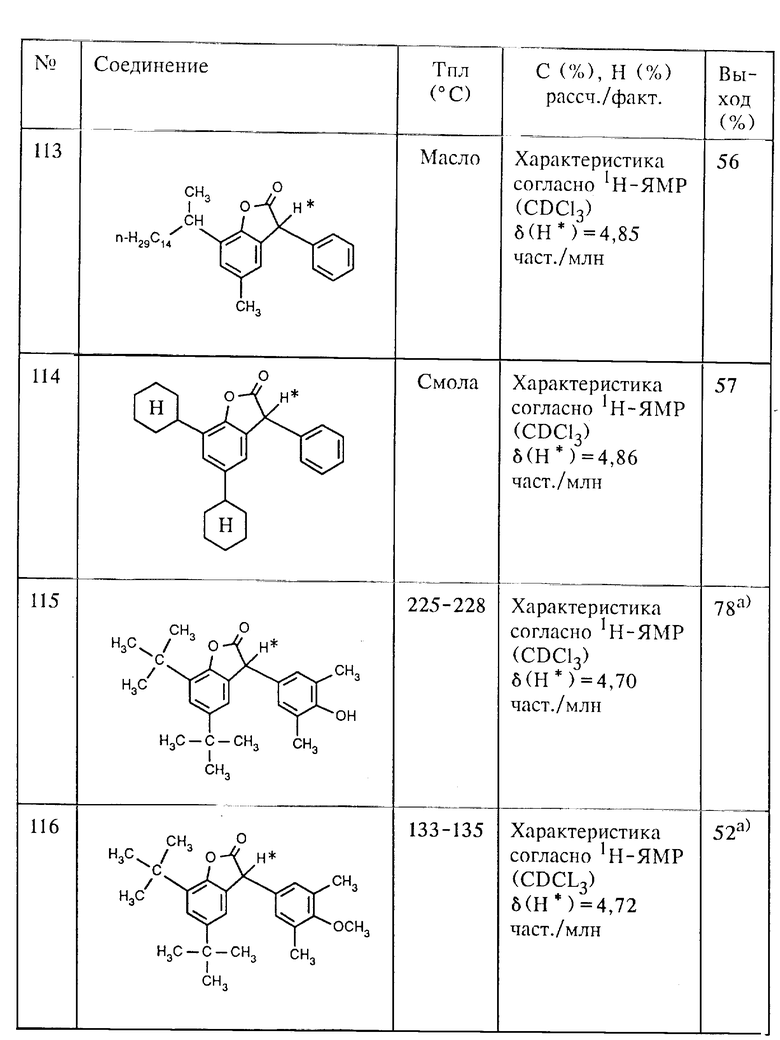
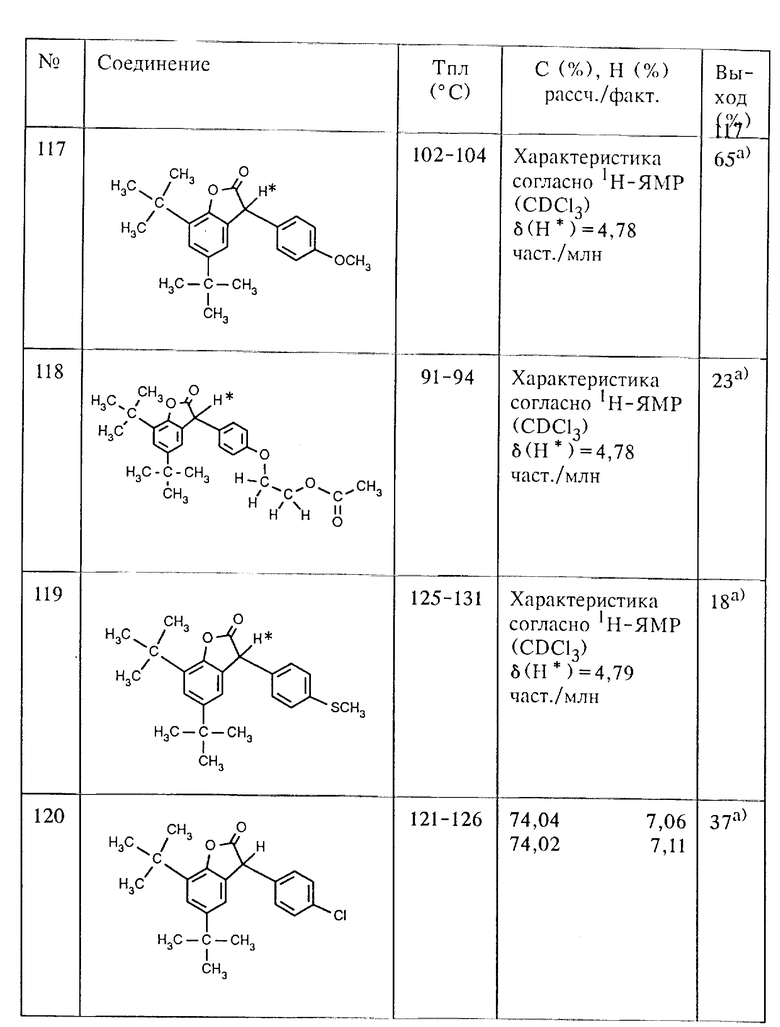
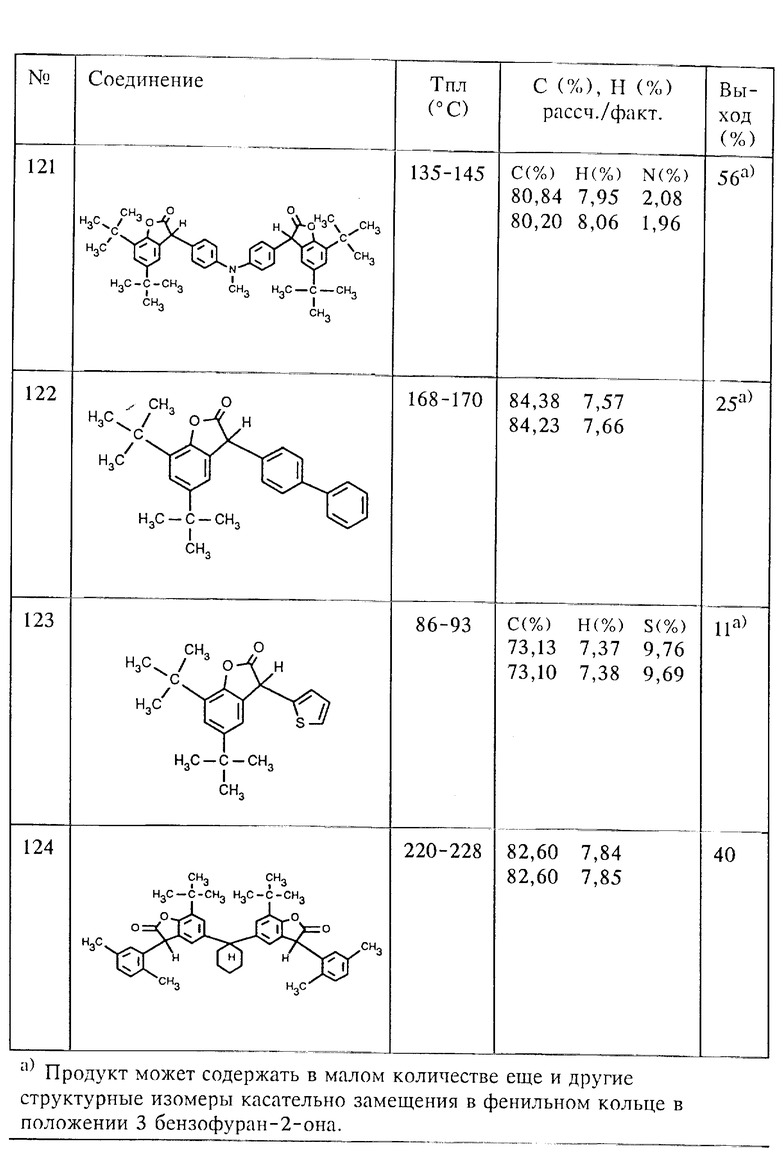
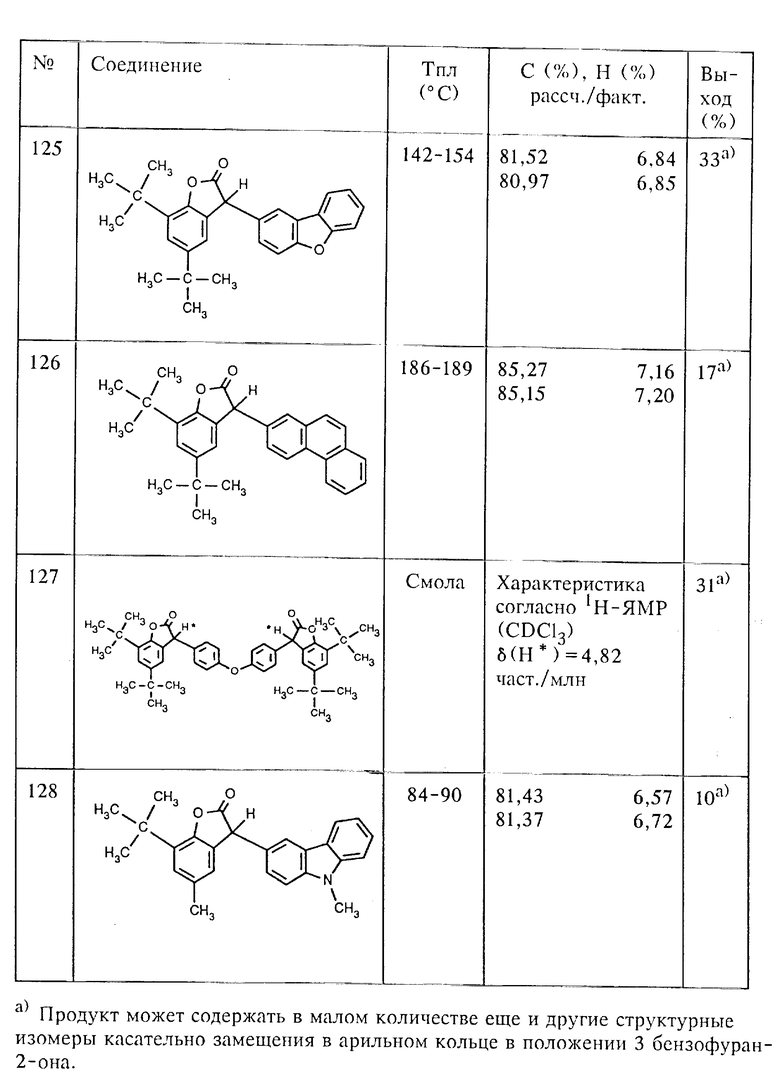
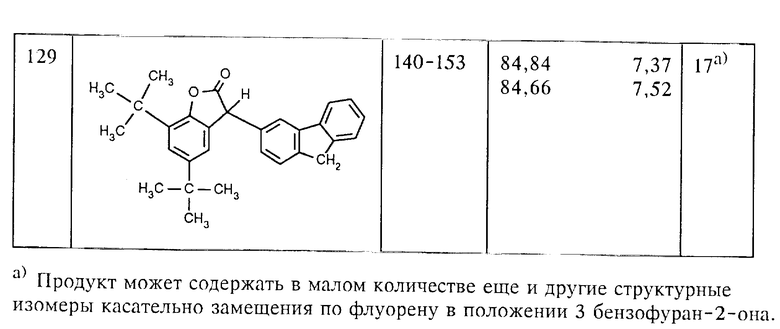
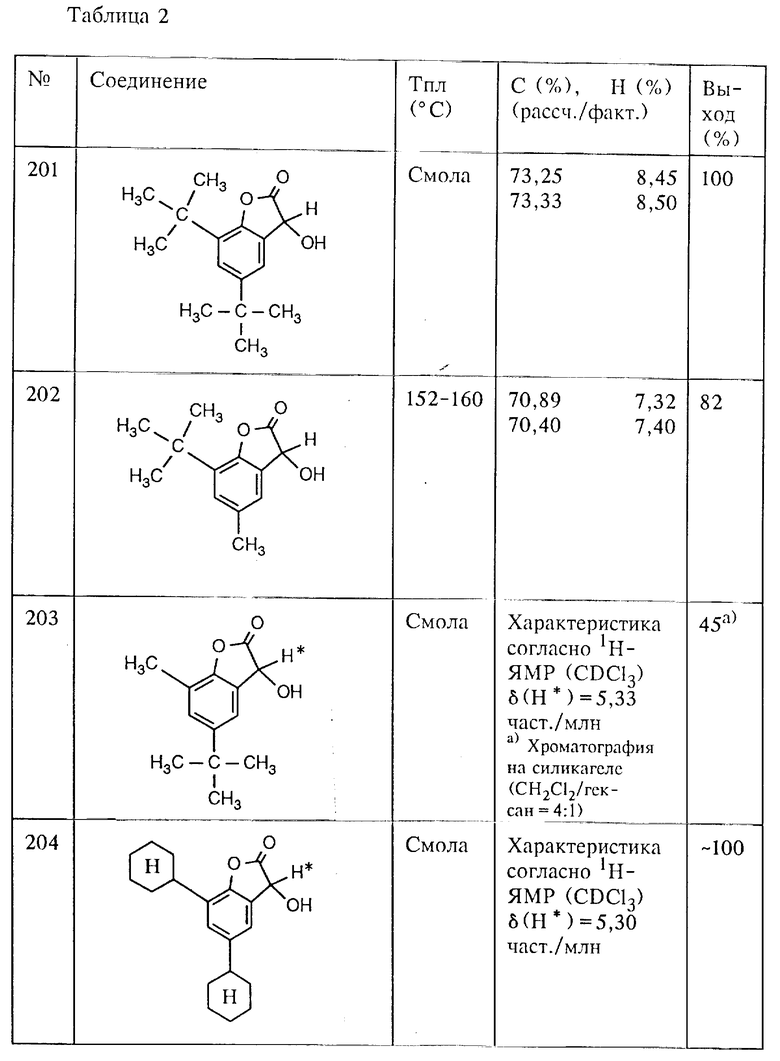
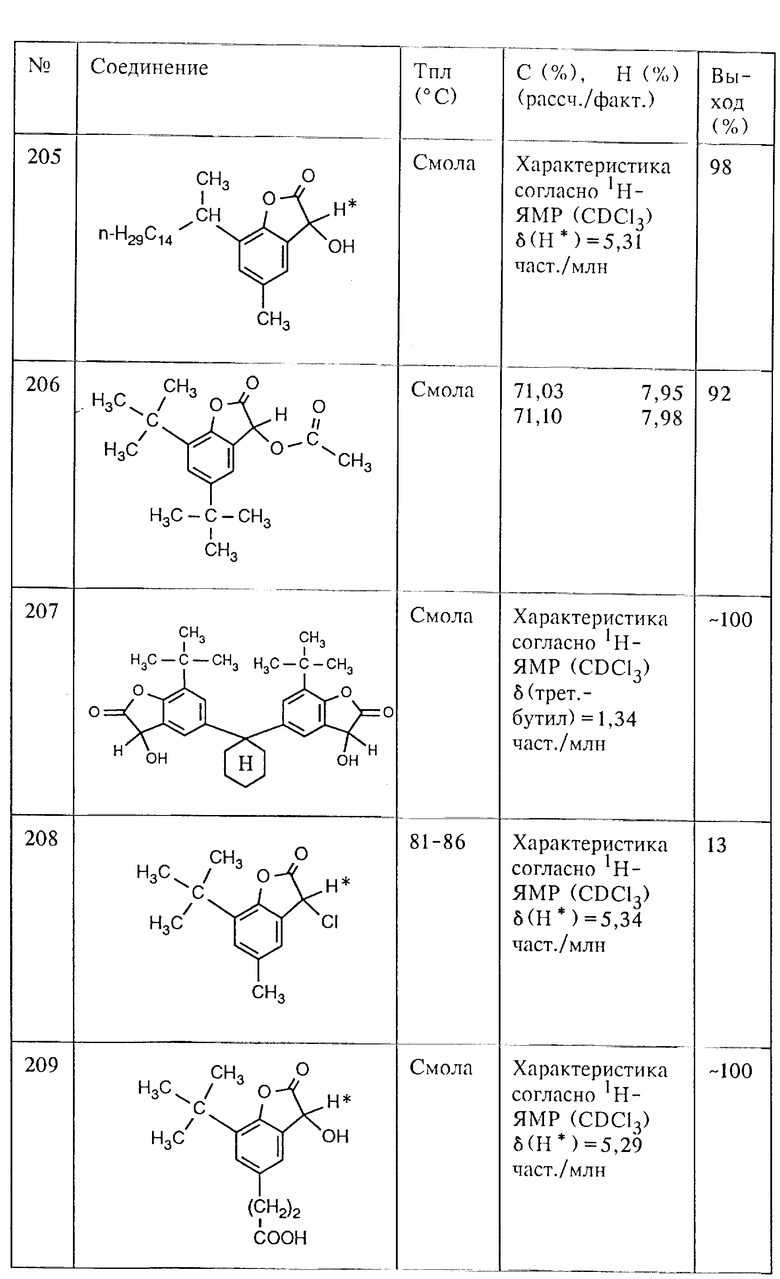
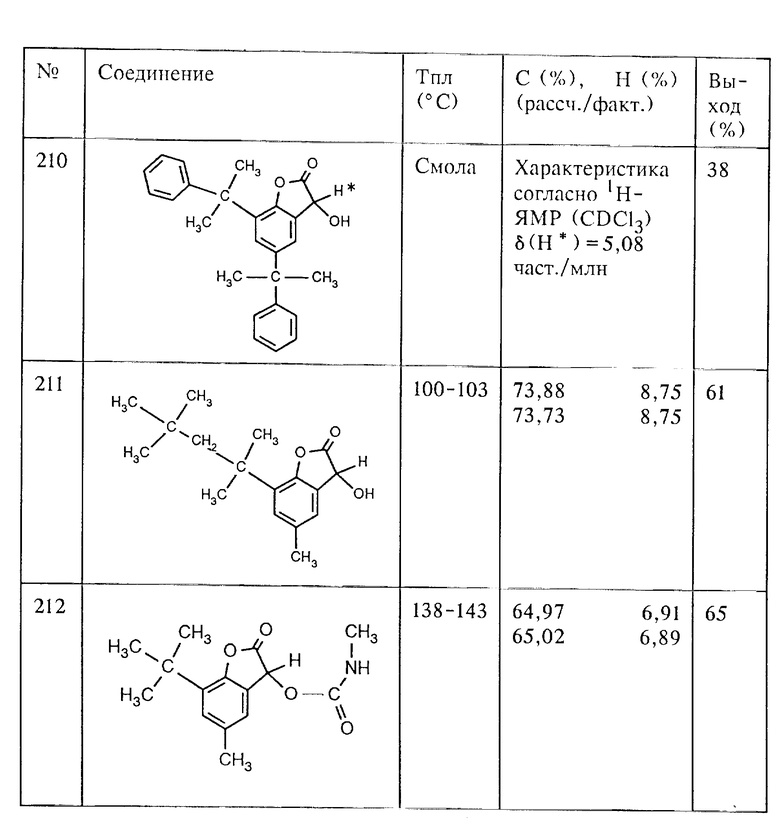
Описывается новый способ получения соединений формулы I, где значения R1 - R5 и n даны в п. 1 формулы, предназначенных для стабилизации органических материалов от окислительного, термического и индуцированного светом распада. Технический результат - упрощение процесса и повышение его экономичности. 2 с. и 18 з.п.ф-лы, 2 табл.
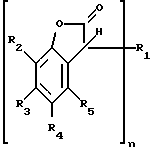
где при значении n, равном 1, R1 представляет собой незамещенный либо замещенный хлором, аминогруппой, гидроксильной группой, С1-С18-алкилом, С1-С18-алкоксигруппой, С1-С18-алкилтиогруппой, С3-С4-алкенилоксигруппой,
С3-С4-алкинилоксигруппой, С1-С4-алкиламиногруппой, ди-(С1-С4-алкил)аминогруппой, фенилом, бензилом, бензоилом или бензоилоксигруппой нафтил, фенантрил, антрил, 5,6,7,8-тетрагидро-2-нафтил, тиенил, бензо[b] тиенил, нафто[2,3-b] - тиенил, тиатренил, фурил, бензофурил, изобензофурил, дибензофурил, хроменил, ксантенил, феноксатиинил, пирролил, имидазолил, пиразолил, пиразинил, пиримидинил, пириданизил, индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, карбозолил, β-карболинил, фенантридинил, акридинил, перимидинил, фенантролинил, феназинил, изотиазолил, фенотиазинил, изоксазолил, фуразанил, бифенил, тетралинил, флуоренил или феноксазинил или R1 обозначает остаток формулы V или VI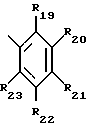
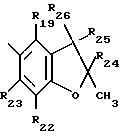
а при значении n, равном 2, R1 представляет собой незамещенный либо замещенный С1-С4-алкилом или гидроксильной группой фенилен или нафтилен; или - R6-Х- R7-;
R2, R3, R4 и R5 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, С1-С25-алкил, С7-С9-фенилалкил, незамещенный либо замещенный С1-С4-алкилом фенил, незамещенный либо замещенный С1-С4-алкилом, С5-С8-циклоалкил, С1-С18-алкокси, С1-С18-алкилтио, С1-С4-алкиламино, ди-(С1-С4-алкил)амино, С1-С25-алканоилокси, С1-С25-алканоиламино, С3-С25-алкеноилокси, разорванный кислородом, серой или 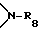 С3-С25-алканоилокси; С6-С9-циклоалкилкарбонилокси, бензоилокси либо замещенный С1-С12-алкилом бензоилокси, или, далее, радикалы R2 и R3, или радикалы R3 и R4, или радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензольное кольцо, R4 представляет собой дополнительно -(СН2)р -COR9 или -(СН2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II
С3-С25-алканоилокси; С6-С9-циклоалкилкарбонилокси, бензоилокси либо замещенный С1-С12-алкилом бензоилокси, или, далее, радикалы R2 и R3, или радикалы R3 и R4, или радикалы R4 и R5 вместе с атомами углерода, по которым они связаны, образуют бензольное кольцо, R4 представляет собой дополнительно -(СН2)р -COR9 или -(СН2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II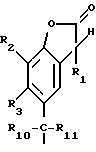
где R1 имеет то же значение, что и при n, равном 1,
R6 и R7 независимо друг от друга представляют собой незамещенный либо замещенный С1-С4-алкилом фенилен или нафтилен;
R8 представляет собой водород или С1-С8-алкил;
R9 обозначает гидроксильную группу, 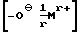 , С1-С18-алкокси
, С1-С18-алкокси
или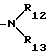
R10 и R11 независимо друг от друга представляют собой водород, CF3, С1-С12-алкил или фенил или R10 и R11 вместе с С-атомом, по которому они связаны, образуют незамещенное либо замещенное 1-3 С1-С4-алкилом С5-С8-циклоалкилиденовое кольцо;
R12 и R13 независимо друг от друга представляют собой водород или С 1-С18-алкил;
R14 обозначает водород или С1-С 18-алкил;
R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, галоген, гидроксильную группу, С1-С25-алкил, разорванный кислородом, серой или 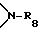 С2-С25-алкил; С1-С25-алкокси, разорванный кислородом, серой или
С2-С25-алкил; С1-С25-алкокси, разорванный кислородом, серой или 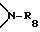 С2-С25-алкил; С1-С25-алкилтио, С3-С25-алкенил, С3-С25-алкенилокси, C3-C25-алкинил, С3-С25-алкинилокси, С7-С9-фенилалкил,
С2-С25-алкил; С1-С25-алкилтио, С3-С25-алкенил, С3-С25-алкенилокси, C3-C25-алкинил, С3-С25-алкинилокси, С7-С9-фенилалкил,
С7-С9-фенилалкокси, незамещенный либо замещенный С1-С4-алкилом фенил; незамещенный либо замещенный С1-С4-алкилом фенокси; незамещенный либо замещенный С1-С4-алкилом С5-С8-циклоалкил; незамещенный либо замещенный С1-С4-алкилом С5-С8-циклоалкокси; С1-С4-алкиламино, ди-(С1-С4-алкил)амино, С1-С25-алканоил, разорванный кислородом, серой или 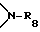 С3-С25-алканоил; С1-С25-алканоилокси, разорванный кислородом, серой или
С3-С25-алканоил; С1-С25-алканоилокси, разорванный кислородом, серой или 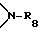 С3-С25-алканоилокси; С1-С25-алканоиламино, С3-С25-алкеноил, разорванный кислородом, серой или
С3-С25-алканоилокси; С1-С25-алканоиламино, С3-С25-алкеноил, разорванный кислородом, серой или 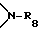 С3-С25-алкеноил; С3-С25-алкеноилокси, разорванный кислородом, серой или
С3-С25-алкеноил; С3-С25-алкеноилокси, разорванный кислородом, серой или 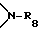 С3-С25-алкеноилокси; С6-С9-циклоалкилкарбонил, С6-С9-циклоалкилкарбонилокси, бензоил или замещенный С1-С12-алкилом бензоил; бензоилокси или замещенный С1-С12-алкилом бензоилокси;
С3-С25-алкеноилокси; С6-С9-циклоалкилкарбонил, С6-С9-циклоалкилкарбонилокси, бензоил или замещенный С1-С12-алкилом бензоил; бензоилокси или замещенный С1-С12-алкилом бензоилокси;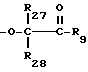
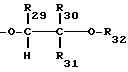
или, далее, в формуле V радикалы R19 и R20 или радикалы R20 и R21 вместе с атомами углерода, с которыми они связаны, образуют бензольное кольцо;
R24 обозначает водород, С1-С4-алкил, незамещенный либо замещенный С1-С4-алкилом фенил;
R25 и R26 обозначают водород, С1-С4-алкил или фенил, при условии, что по крайней мере один из радикалов R25 и R26 является водородом;
R27 и R28 представляют собой независимо друг от друга водород, С 1-С4-алкил или фенил;
R29 представляет собой водород или С1-С4-алкил;
R30 обозначает водород, незамещенный либо замещенный С1-С4-алкилом фенил; С1-С25-алкил, разорванный кислородом, серой или 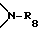 С2-С25-алкил; незамещенный либо замещенный в фенильном остатке 1-3 С1-С4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или
С2-С25-алкил; незамещенный либо замещенный в фенильном остатке 1-3 С1-С4-алкилом C7-C9-фенилалкил; разорванный кислородом, серой или 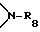 незамещенный либо замещенный в фенильном остатке 1-3 С1-С4-алкилом С7-С25-фенилалкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, с которыми они связаны, образуют незамещенное либо замещенное 1-3 С1-С4-алкилом С5-С12-циклоалкиленовое кольцо;
незамещенный либо замещенный в фенильном остатке 1-3 С1-С4-алкилом С7-С25-фенилалкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, с которыми они связаны, образуют незамещенное либо замещенное 1-3 С1-С4-алкилом С5-С12-циклоалкиленовое кольцо;
R31 представляет собой водород или С1-С4-алкил;
R32 обозначает водород, С1-С25-алканоил, С3-С25-алкеноил, разорванный кислородом, серой или 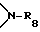 С3-С25-алканоил; замещенный ди(С1-С6-алкил) фосфатной группой С2-С25-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С12-алкилом бензоил;
С3-С25-алканоил; замещенный ди(С1-С6-алкил) фосфатной группой С2-С25-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С12-алкилом бензоил; 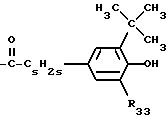
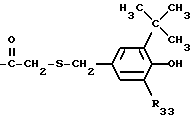
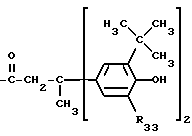

R33 представляет собой водород или С1-С8-алкил;
R34 представляет собой прямую связь, С1-С18-алкилен, разорванный кислородом, серой или 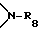 С2-С18-алкилен, С2-С18-алкенилен, С2-С20-алкилиден, С7-С20-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен, незамещенный либо замещенный С1-С4-алкилом фенилен,
С2-С18-алкилен, С2-С18-алкенилен, С2-С20-алкилиден, С7-С20-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен, незамещенный либо замещенный С1-С4-алкилом фенилен, 
R35 обозначает гидроксильную группу, 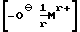 С1-С18-алкокси или
С1-С18-алкокси или 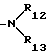
R36 представляет собой кислород, -NH- или 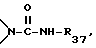
R37 представляет собой С1-С18-алкил или фенил;
М представляет собой r-валентный катион металла;
Х обозначает прямую связь, кислород, серу или -NR14-;
n обозначает 1 или 2;
р обозначает 0,1 или 2;
q обозначает 1, 2, 3, 4, 5 или 6;
r обозначает 1, 2 или 3;
s обозначает 0,1 или 2,
отличающийся тем, что соединение формулы III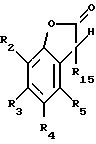
где R15 представляет собой галоген или -OR' 15;
R' 15 обозначает водород, С1-С25-алканоил, С3-С25-алкеноил, разорванный кислородом, серой или 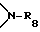 С3-С25-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С12-алкилом бензоил; нафтоил или замещенный С1-С12-алкилом нафтоил; С1-С25-алкансульфонил, замещенный фтором С1-С25-алкансульфонил; фенилсульфонил или замещенный С1-С12-алкилом фенилсульфонил;
С3-С25-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С12-алкилом бензоил; нафтоил или замещенный С1-С12-алкилом нафтоил; С1-С25-алкансульфонил, замещенный фтором С1-С25-алкансульфонил; фенилсульфонил или замещенный С1-С12-алкилом фенилсульфонил;
R16 представляет собой прямую связь, С1-С18-алкилен, разорванный кислородом, серой или 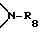 С2-С18-алкилен; С2-С18-алкенилен, С2-С20-алкилиден, С7-С20-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен, незамещенный либо замещенный С1-С4-алкилом фенилен,
С2-С18-алкилен; С2-С18-алкенилен, С2-С20-алкилиден, С7-С20-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен, незамещенный либо замещенный С1-С4-алкилом фенилен,
R17 обозначает кислород, -NH- или 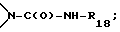
R18 представляет собой ; С1-С18-алкил или фенил,
подвергают взаимодействию с соединением формулы IV [Н]nR1.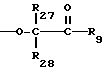
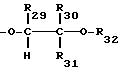
или, далее, в формуле V радикалы R19 и R20 либо радикалы R20 и R21 образуют вместе с атомами углерода, с которым они связаны, бензольное кольцо; R24 обозначает водород или С1-С4-алкил, R25 и R26 обозначают водород или С1-С 4-алкил, при условии, что по крайней мере один из радикалов R25 и R26 является водородом;
R27 и R28 независимо друг от друга представляют собой водород или С1-С4-алкил;
R29 является водородом;
R30 обозначает водород, фенил, С1-С18-алкил, разорванный кислородом или серой С2-С18-алкил; С7-С9-фенилалкил, разорванный кислородом или серой незамещенный либо замещенный в фенильном остатке 1-3 С1-С4-алкилом С7-С18-фенилалкил, или, далее, радикалы R29 и R30 образуют вместе с атомами углерода, с которыми они связаны, незамещенное либо замещенное 1-3 и С1-С4-алкилом циклогексиленовое кольцо;
R31 обозначает водород или С1-С 4-алкил;
R32 представляет собой водород, С1-С18-алканоил, С3-С18-алкеноил, разорванный кислородом или серой С3-С12-алканоил, замещенный ди(С1-С6-алкил) фосфонатной группой С2-С12-алканоил; С6-С9-циклоалкилкарбонил, бензоил,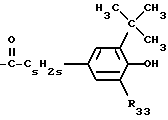
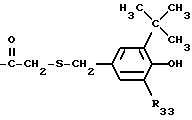
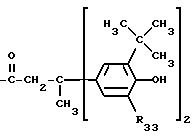

R33 обозначает водород или С1-С4-алкил;
R 34 представляет собой С1-С12-алкилен, С2-С8-алкенилен, С2-С8-алкилиден, С7-С12-фенилалкилиден, С5-С8-циклоалкилен или фенилен;
R35 обозначает гидроксильную группу 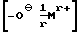 или С1-С18-алкокси;
или С1-С18-алкокси;
R36 представляет собой кислород или -NH-;
R37 представляет собой С1-С8-алкил или фенил;
s обозначает 1 или 2.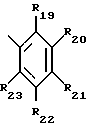
где R19, R20, R21, R22 и R23 независимо друг от друга представляют собой водород, хлор, гидроксильную группу, С1-С18-алкил, С1-С18-алкокси, С1-С18-алкилтио, C3-C4-алкенилокси, С3-С4-алкинилокси, фенил, бензоил, бензоилокси или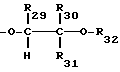
R29 является водородом;
R30 представляет собой водород, фенил или С1-С18-алкил, или, далее, радикалы R29 и R30 вместе с атомами углерода, с которыми они связаны, образуют незамещенное либо замещенное 1-3 С1-С4-алкилом циклогексиленовое кольцо; R31 обозначает водород или С1-С4-алкил;
R32 представляет собой водород С1-С12-алканоил или бензоил. С3-С18-алканоилокси; С6-С9-циклоалкилкарбонилокси, бензоилокси или замещенный С1-С8-алкилом бензоилокси, или, далее, радикалы R2 и R3, либо радикалы R3 и R4, либо радикалы R4 и R5 вместе с атомами углерода, с которыми они связаны, образуют бензольное кольцо, R4 представляет собой дополнительно -(СН2)р -COR9 или -(СН2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II
С3-С18-алканоилокси; С6-С9-циклоалкилкарбонилокси, бензоилокси или замещенный С1-С8-алкилом бензоилокси, или, далее, радикалы R2 и R3, либо радикалы R3 и R4, либо радикалы R4 и R5 вместе с атомами углерода, с которыми они связаны, образуют бензольное кольцо, R4 представляет собой дополнительно -(СН2)р -COR9 или -(СН2)qOH, или, если R3 и R5 являются водородом, R4 обозначает дополнительно остаток формулы II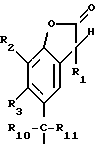
R8 представляет собой водород или С1-С6-алкил;
R9 обозначает гидроксильную группу, С1-С18-алкокси или 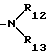
R10 и R11 являются метильными группами или вместе с С-атомом, с которым они связаны, образуют незамещенное либо замещенное 1-3 С1-С4-алкилом С5-С8-циклоалкилиденовое кольцо;
R12 и R13 независимо друг от друга представляют собой водород или С1-С8-алкил;
q обозначает 2, 3, 4, 5 или 6.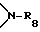 С3-С18-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С8-алкилом бензоил; нафтоил или замещенный С1-С8-алкилом нафтоил; С1-С18-алкансульфонил, замещенный фтором С1-С18-алкансульфонил; фенилсульфонил или замещенный С1-С8-алкилом фенилсульфонил;
С3-С18-алканоил; С6-С9-циклоалкилкарбонил, теноил, фуроил, бензоил или замещенный С1-С8-алкилом бензоил; нафтоил или замещенный С1-С8-алкилом нафтоил; С1-С18-алкансульфонил, замещенный фтором С1-С18-алкансульфонил; фенилсульфонил или замещенный С1-С8-алкилом фенилсульфонил;
R16 представляет собой прямую связь, С1-С12-алкилен, разорванный кислородом, серой или 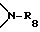 С2-С12-алкилен, С2-С12-алкенилен, С2-С12-алкилиден, С7-С12-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен или фенилен; R17 обозначает кислород или -NH-;
С2-С12-алкилен, С2-С12-алкенилен, С2-С12-алкилиден, С7-С12-фенилалкилиден, С5-С8-циклоалкилен, С7-С8-бициклоалкилен или фенилен; R17 обозначает кислород или -NH-;
R18 представляет собой С1-С12-алкил или фенил.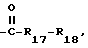 R17 представляет собой -NH- и R18 является С1-С4-алкилом.
R17 представляет собой -NH- и R18 является С1-С4-алкилом.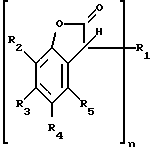
где общие символы имеют значения, указанные в п.1, отличающийся тем, что один эквивалент фенола формулы VII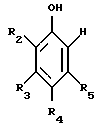
где общие символы имеют значения, указанные в п.1,
с помощью 0,8-2,0 эквивалентов глиоксиловой кислоты превращают в соединение формулы VIII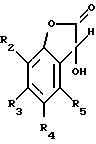
где общие символы имеют значения, указанные в п.1,
и затем это соединение без выделения подвергают взаимодействию с соединением формулы IV
[Н]n-R1,
где R1 и n имеют значения, указанные в п.1.
R' 15-ОН,
галогенангидридом кислоты формулы Х
R' 15-Y,
сложным эфиром формулы XI
R' 15-O-R38,
симметричным либо несимметричным ангидридом формулы XIII
R' 15-O-R15,
или изоцианатом формулы XIII
R39-N=C=O,
где R' 15 в соединениях формул IX, X, XI и XII имеет значения, указанные в п.1, при условии, что R' 15 не обозначают водород;
R38 представляет собой С1-С8-алкил;
R39 обозначает С1-С8-алкил или фенил;
Y представляет собой фтор, хлор, бром или иод,
с получением соединения формулы III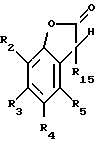
где радикалы R2, R3, R4, R5 и R15 имеют значения, указанные в п.1,
причем если R15 обозначает -ОR' 15, R' 15 не являются водородом.
| US 4325863, 1982 | |||
| US 4338244, 1982 | |||
| US 5175312 A, 1992 | |||
| 2-Бензофуранил- , -диметиламиноэтилкентон или его хлоргидрат в качестве стабилизатора резин | 1974 |
|
SU518950A1 |
Авторы
Даты
1999-07-10—Публикация
1994-09-16—Подача