Предлагаемый способ относится к органическому синтезу, в частности к способу получения (1+1)-аддуктов фуллерена C60 с норборнадиеном состава C67H8 и его производными (элементный состав включает C67H8 - фрагмент).
Известен способ получения (1+1)-аддукта фуллерена C60 состава C67H8, в основе которого лежит реакция циклоприсоединения к фуллерену не норборнадиена (НБД), а его валентного изомера - квадрициклана (Q) (квадрициклан получают из НБД фотохимическим способом) при 80oC в течение 5 ч в среде толуола (см. в конце описания).
Выход аддукта (1) составляет 43%, в реакционной массе содержится 46% непрореагировавшего фуллерена C60. ((1). М. Prato М. Magini, G. Scorano, V. Luchini. J.Org.Chem., 1993, 58, 3613-15).
Взаимодействие фуллерена C60 с U проходит неселективно, т.к. в реакционной массе был обнаружен еще третий изомер (~5%), структура которого осталась невыясненной [1] . Следует отметить, что судя по строению (1) является продуктом присоединения к (фуллерену норборнадиена по схеме [2+2].
Данный способ (прототип) имеет следующие недостатки:
1. Низкая селективность реакции (43%) и низкий выход целевого продукта. Из-за неполной конверсии фуллерена возникает необходимость разделения изомеров с помощью дорогостоящего и трудоемкого метода высокоэффективной жидкостной хроматографии.
2. Способ является препаративно неудобным и нетехнологичным, т.к. по существу процесс получения (1) - двухстадийный, ввиду того, что один из реагентов: квадрициклан - это нестабильное соединение и его приходится получать непосредственно перед реакцией по сложной методике УФ-облучением норборнадиена ((2) С. D. Smith, Org. Synth., 1971, V. 51, P. 133-136).

Реакция осуществляется в среде серного эфира при комнатной температуре в течение 48 ч при УФ-облучении ртутной лампой (λ - 254 нм) в присутствии триплетного стабилизатора ацетофенона. Образующийся при этом квадрициклан из-за значительного внутреннего напряжения является нестабильным соединением. Он достаточно легко изомеризуется в менее напряженный норборнадиен. Особенно легко этот процесс (Q ---> НБД) проходит под действием катализаторов (кислоты Льюиса, кислоты Бренстеда, комплексы переходных металлов), а также термически (так, например, время полупревращения Q в НБД при 100oC составляет 14 ч) ((3). В.А.Брень, А.Д.Дубоносов, В.Н.Минкин, В.А.Черноиванов. Усп. химии, 1991, 60 (10), 913-946). В частности, квадрициклан претерпевает изомеризацию в НБД при хранении в стеклянной посуде, что объясняется наличием на поверхности стекла силанольных групп 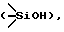 имеющих слабокислотные свойства [3]. Кроме того, для получения квадрициклана необходимо большое количество легковоспламеняющегося и взрывоопасного (из-за образования перекисей) серного эфира (для получения 1 кг Q необходимо 6,7 литров Et2O).
имеющих слабокислотные свойства [3]. Кроме того, для получения квадрициклана необходимо большое количество легковоспламеняющегося и взрывоопасного (из-за образования перекисей) серного эфира (для получения 1 кг Q необходимо 6,7 литров Et2O).
3. Значительная продолжительность реакции. С учетом стадии получения квадрициклана общая продолжительность процесса составляет (48+5) 53 часа.
Предлагается новый способ получения (1+1) аддукта C60 с норборнадиеном состава C67H8, а также (1+1-аддуктов фуллерена с замещенными норборнадиенами, в частности, 7-спироциклопропановым производным, не имеющий недостатков прототипа. Сущность метода заключается в циклоприсоединении к фуллерену C60 норборнадиена или 7-спироциклопропаннорборнадиена (2) в особых условиях, а именно, в среде специально подобранных растворителей, в частности, хлорбензола или 2-метилтиофена при повышенной температуре (160-160oC) в течение 5 ч в избытке НБД и (2) до 50-200 раз. В этих условиях выходы (1+1) аддуктов фуллерена с норборнадиеном (3) и 7-спироциклопропаннорборнадиеном (4) достигают 80% (см. в конце описания).
При проведении реакции в среде галоидуглеводородов (хлористый метилен, хлороформ, четыреххлористый углерод) и ароматических углеводородов (бензол, толуол, ксилолы) выход (3,4) не превышает 10-20%.
Следует отметить, что полученные в результате взаимодействия НБД и (2) с фуллереном соединения (3, 4) действительно являются (1+1) - аддуктами, причем соединения (1) и (3) имеют одинаковый элементный состав, но отличаются по структуре.
Преимущества предлагаемого изобретения перед прототипом.
1. Одностадийность и высокая селективность процесса.
2. Высокий выход целевого продукта - 80% (в прототипе 43%).
3. Отсутствие стадии хроматографического разделения и очистки целевого продукта. Экономия растворителей, уменьшение энерго- и трудозатрат.
4. Универсальность способа: в реакцию с фуллереном в выбранных условиях вступают норборнадиен и его 7-спироциклопропансодержащий аналог.
5. Сокращение продолжительности опыта с 53 до 5 часов.
6. Применение доступных и недорогих реагентов нефтехимического происхождения (норборнадиен, хлорбензол и 2-метилтиофен).
7. Простота технологического оформления процесса. Синтез целевых продуктов осуществляется с использованием типового оборудования и стандартных приемов: нагревание, упаривание растворителя.
8. Возможность многократного использования реагентов и растворителей. Непрореагировавший норборнадиен или (2), взятые в 50-200 кратном избытке, могут быть легко отделены перегонкой и возвращены в процесс.
Способ поясняется примерами (1-16).
Общая методика проведения реакции фуллерена с норборнадиеном и 7-спироциклопропаннорборнадиеном (2)
В микроавтоклав (V = 17 мл) помещали 10 мг (0,014 ммол) фуллерена C60, 0,7-2,8 ммолей норборнадиена или (2) и 6-12 мл растворителя (2-метилтиофен, хлорбензол). Герметично закрытый автоклав нагревали в масляной бане при перемешивании при 160-180oC в течение 20 ч (см.табл.1).
Литература
1. М. Proto, М. Magini, G. Scorano, V. Luchini, J. Org. Chem., 1993, 58, 3613-3615.
2. С. D. Smith, Org. Synth., 1971, V. 51, P. 133' 133-136.
3 В. А. Брень, А. Д. Дубоносов, В. Н. Минкин, В. Д. Черноиванов. Усп. химии. 1991, 60(10), 913-948.4
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-ПРОПИЛ)-2-ГИДРО[60]-ФУЛЛЕРЕНОВ | 1998 |
|
RU2135446C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ КВАДРИЦИКЛАНОВЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ | 2017 |
|
RU2703529C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-ПРОПИЛ)-2-МАГНИЙГАЛОГЕН [60]-ФУЛЛЕРЕНОВ | 1998 |
|
RU2135504C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2-МАГНИЙГАЛОИД [60] ФУЛЛЕРЕНОВ | 1998 |
|
RU2135505C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ (АЛКИЛ)-2-ГИДРО[60]ФУЛЛЕРЕНОВ | 1998 |
|
RU2135447C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ(АЛКИЛ)-2-МАГНИЙГАЛОГЕН [60] ФУЛЛЕРЕНОВ | 1998 |
|
RU2135506C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРПРОИЗВОДНЫХ ФУЛЛЕРЕНА C | 1998 |
|
RU2160226C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2,3-ФУЛЛЕРЕНАЛЮМАЦИКЛОПЕНТАНОВ | 1997 |
|
RU2132332C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИ(1-ЭТИЛ-1-(ДИАЛКИЛАМИН) АЛЮМИНИЙ)[60]ФУЛЛЕРЕНОВ | 1999 |
|
RU2160275C1 |
| СПОСОБ ПОЛУЧЕНИЯ Н-БУТИЛЗАМЕЩЕННЫХ ФУЛЛЕРЕНОВ C | 1998 |
|
RU2134255C1 |
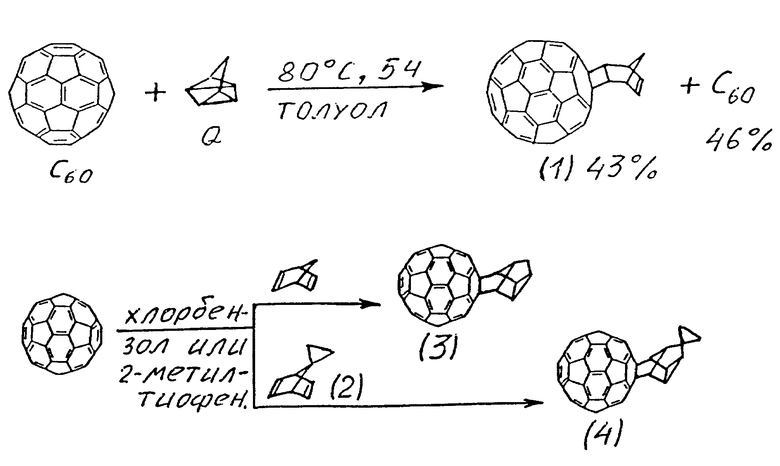
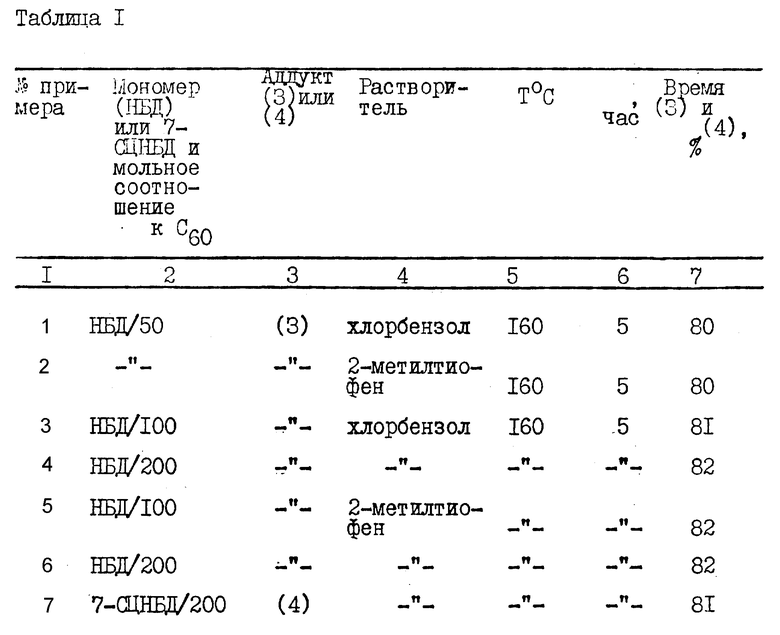

Сущность способа заключается в циклоприсоединении к фуллерену С60 норборнадиена или 7-спироциклопропаннорборнадиена в среде хлорбензола или 2-метилтиофена при 160-180°С в течение 5 ч в избытке норборнадиена и 7-спироциклопропаннорборнадиена до 50-200 раз. В этих условиях выход конечных продуктов достигает 80%. Предлагаемый процесс характеризуется высокой селективностью и простотой технического оформления. 1 табл.
Способ получения (1 + 1)-аддуктов фуллерена С60 с норборнадиеном и его 7-спироциклопропанзамещенным производным, отличающийся тем, что циклоприсоединение к фуллерену С60 норборнадиена или 7-спироциклопропаннорборнадиена, взятых в 50-200-кратном избытке, осуществляется в среде хлорбензола или 2-метилтиофена при температуре 160 - 180o в течение 5 ч.
| Maurizio Prato, et.al | |||
| Addition of Quadro cyclane to C: Easy Access to Fullere Derivatives Bearing a Reactive Double Bond in the Side Chain | |||
| J | |||
| ORG | |||
| CHEM., 1993, 58, N 14, s.3613-3615 | |||
| US 5177248 A, 05.01.93 | |||
| СПОСОБ ПРОМЫШЛЕННОГО ПРОИЗВОДСТВА ФУЛЛЕРЕНОВ | 1997 |
|
RU2086503C1 |
Авторы
Даты
1999-09-20—Публикация
1998-04-29—Подача