Изобретение относится к способам получения новых углеводородных соединений, конкретно к способу получения н-бутилзамещенных фуллеренов C60 общей формулы (1) H-BunC60Hn, где n = 1-6, C60 - новая аллотропная модификация углерода.
Полученные соединения могут найти применение в тонком органическом синтезе, а также в качестве исходных полупродуктов при получении биологически активных веществ для медицины и сельского хозяйства, современных присадок к маслам.
Известен способ ([I], Y. - Z. An, G. A. Ellis, A.L. Viado, Y. Rubin, J. Org, Chem., 1995, 60, 6353-6361) получения циклогексенфуллерена взаимодействием толуольного раствора фуллерена C60 с бутадиеном при 125oC по схеме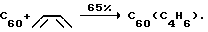
По известному способу не могут быть получены н-бутилзамещенные фуллерены C60 (I).
Известен способ ([2], J. Chen, R. - F. Cai, Z. - E. Huang, H. - M. Wu, S. - K. Jiang, Q. - F. Shao. J. Chem. Soc., Chem. Commun., 1995, 1553-1554) получения 1-бензил-2-гидро[60]-фуллерена взаимодействием калиевой соли фуллерена с бензилхлоридом в ТГФ при температуре 50oC в течение 4 часов с последующей обработкой реакционной массы уксусной кислотой по схеме
Известный способ не позволяет получать н-бутилзамещенные фуллерены C60 (I).
Предлагается новый способ синтеза н-бутилзамещенных фуллеренов C60. Сущность способа заключается во взаимодействии толуольногоо раствора фуллерена C60 с избытком эфирного раствора ди(н-бутил)магния (н-Bu2Mg), взятыми в мольном соотношении C60:(н-Bu2Mg)=1:(35-90), предпочтительно 1:60, в присутствии цирконацендихлорида (Cp2ZrCl2) в количестве 1-3 мол.% по отношению к н-Bu2Mg, предпочтительно 2 мол.%, в атмосфере аргона при комнатной температуре (22-23oC) и нормальном давлении в течение 8-12 часов, предпочтительно 10 часов, с последующей обработкой реакционной массы 5% водной HCl. Выход н-бутилзамещенных фуллеренов 70-94%. Реакция протекает по схеме
n = 1-6,
Дибутилмагния (н-Bu2Mg) берут в значительном избытке по отношению к исходному фуллерену C60 с целью введения в молекулу фуллерена большего числа бутильных групп. Снижение количества н-Bu2Mg по отношению к C60 приводит к уменьшению выхода целевых продуктов, а также к снижению вводимых в молекулу фуллерена бутильных групп. Изменение соотношения исходных реагентов в сторону увеличения содержания н-Bu2Mg по отношению к C60 не приводит к существенному повышению выхода целевых продуктов, а также увеличению количества вводимых в молекулу фуллерена н-бутильных групп.
Проведение указанной реакции в присутствии катализатора Cp2ZrCl2 больше 3 мол.% не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора Cp2ZrCl2 менее 1 мол.% снижает выход н-бутилзамещенных фуллеренов, что связано, возможно, со снижением каталитически активных центров в реакционной массе. Опыты проводили при комнатной температуре. При более высокой температуре, например 60oC, не наблюдается значительного увеличения выхода целевых продуктов, при меньшей температуре, например 0oC, снижается скорость реакции. Реакцию проводили в растворе толуола, т.к. он является лучшим растворителем для фуллерена. Исходный н-Bu2Mg синтезировали в эфире, т.к. он является одним из лучших растворителей для Mg-органических реагентов.
Существенные отличия предлагаемого способа следующие.
Предлагаемый способ базируется на использовании в качестве исходных реагентов н-Bu2Mg и фуллерена C60, реакция протекает в смеси ароматического (толуол) и эфирного растворителя в присутствии катализатора Cp2ZrCl2. В известном способе используются бензилхлорид и калиевая соль фуллерена.
Предлагаемый способ позволяет получать н-бутилсодержащие фуллерены общей формулы н-BunC60Hn с числом н-бутильных заместителей от 1 до 6, синтез которых в литературе не описан.
Пример 1. В стеклянный реактор объемом 100 мл, установленный на магнитной мешалке в атмосфере аргона при комнатной температуре, помещают 0.05 ммоль фуллерена C60, 40 мл сухого толуола, 3 ммоль н-Bu2Mg (0,8 М эфирный раствор) в 20 мл эфира и катализатор Cp2ZrCl2 в количестве 0.06 ммоль (2 мол.% по отношению к н-Bu2Mg), перемешивают 10 часов при комнатной температуре (22-23oC), реакционную массу обрабатывают 5%-ной водной HCl, экстрагируют толуолом, сушат MgSO4, растворитель упаривают. Получают н-бутилзамещенные фуллерены общей формулы н-BunC60Hn с числом н-бутильных групп от 1 до 6 с общим выходом 82%.
Спектральные характеристики н-бутилсодержащих фуллеренов (I): Спектр ПМР (δ, м. д. ): 0.89-1.26 м.д. (CH3, концевые н-бутильные), 1.32-1.89 м (CH2, н-бутильные), 4.32-5.20 м (CH, фуллереновые).
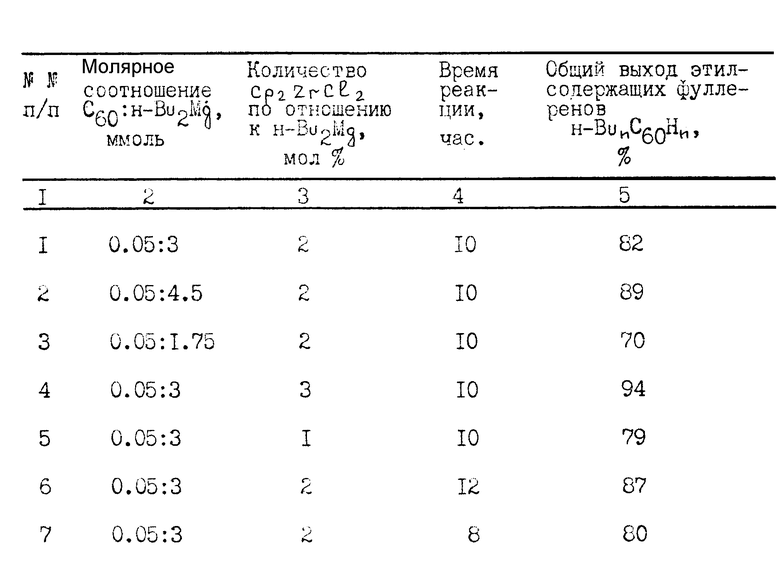
Масс-спектр отрицательных ионов н-бутилзамещенных фуллеренов С60 (I) состоит из следующих массовых линий: 778 (н-Bu1C60H1), 836 (н-Bu2C60H2), 894 (н-Bu3C60H3), 952 (н-Bu4C60H4), 1010 (н-Bu5C60H5), 1068 (н-Bu6C60H6). Другие примеры, подтверждающие способ, приведены в таблице.
Реакции проводили при комнатной температуре (22-23oC). Повышение температуры нецелесообразно, т.к. не наблюдается значительного увеличения выхода целевых продуктов. При более низкой температуре снижается скорость реакции. В качестве растворителя целесообразно использовать толуол и эфир, т. к. в них наибольшая растворимость соответственно фуллерена C60 и н-Bu2Mg.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-БУТИЛ)-2-МАГНИЙ(Н-БУТИЛ)[60]ФУЛЛЕРЕНОВ | 1998 |
|
RU2136687C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛСОДЕРЖАЩИХ ФУЛЛЕРЕНОВ C | 1998 |
|
RU2133727C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛИРОВАННЫХ ФУЛЛЕРЕНОВ | 1997 |
|
RU2119449C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ (АЛКИЛ)-2-ГИДРО[60]ФУЛЛЕРЕНОВ | 1998 |
|
RU2135447C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ МОНО [ЦИКЛОАЛКИЛ] ДИГИДРО [60] ФУЛЛЕРЕНОВ И БИС [ЦИКЛОАЛКИЛ] ТЕТРАГИДРО [60] ФУЛЛЕРЕНОВ | 1998 |
|
RU2136647C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-ПРОПИЛ)-2-МАГНИЙГАЛОГЕН [60]-ФУЛЛЕРЕНОВ | 1998 |
|
RU2135504C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-ПРОПИЛ)-2-ГИДРО[60]-ФУЛЛЕРЕНОВ | 1998 |
|
RU2135446C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2,3-ФУЛЛЕРЕНАЛЮМАЦИКЛОПЕНТАНОВ | 1997 |
|
RU2132332C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ(АЛКИЛ)-2-МАГНИЙГАЛОГЕН [60] ФУЛЛЕРЕНОВ | 1998 |
|
RU2135506C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2-МАГНИЙГАЛОИД [60] ФУЛЛЕРЕНОВ | 1998 |
|
RU2135505C1 |
Изобретение относится к области органической химии, а именно к новому способу получения новых углеводородных соединений, которые могут найти применение в тонком органическом синтезе, а также в качестве исходных полупродуктов при получении биологически активных веществ для медицины и сельского хозяйства, современных присадок к маслам. Для получения н-бутилзамещенных фуллеренов C60 толуольный раствор фуллерена взаимодействует с избытком эфирного раствора ди(н-бутил)магния в молярном соотношении C60 : (н-Bu2Mg) = 1 : (35 - 90) в присутствии цирконацендихлорида в качестве катализатора, взятого в количестве 1 - 3 мол.% по отношению к н-Bu2Mg. Реакция осуществляется в атмосфере аргона при нормальных условиях в течение 8 - 12 ч. После чего реакционная масса обрабатывается 5%-ной водной HCl. 1 табл.
Способ получения н-бутилзамещенных фуллеренов C60, отличающийся тем, что толуольный раствор фуллерена C60 взаимодействует с избытком эфирного раствора ди(н-бутил)магния (н-Bu2Mg) в молярном соотношении C60 : (н-Bu2Mg) = 1 : (35 - 90) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2), взятого в количестве 1 - 3 мол.% по отношению к н-Bu2Mg, в атмосфере аргона при нормальных условиях в течение 8 - 12 ч с последующей обработкой реакционной массы 5%-ной водной соляной кислотой.
| Jian Chen, Rui-Fang Cai, et al | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Подвижной аппарат для подъема жидкостей и густых масс помощью образования вакуума сжиганием горючей смеси | 1924 |
|
SU1553A1 |
| Yi-Zhong An, George A.Ellis, et al "A Methodology for the Reversible Solubilization of Fullerenes", J.Org.Chem., 1995, 60, s | |||
| КОНТРОЛЬНЫЙ АППАРАТ ДЛЯ РЕГИСТРАЦИИ ПРИХОДА И УХОДА СЛУЖАЩИХ | 1925 |
|
SU6353A1 |
| US 5177248 A, 1993 | |||
| СПОСОБ И УСТРОЙСТВО ДЛЯ ПРОИЗВОДСТВА ФУЛЛЕРЕНОВ | 1996 |
|
RU2085484C1 |
Авторы
Даты
1999-08-10—Публикация
1998-01-12—Подача