Изобретение относится к генной инженерии, а именно к технологии получения высокопродуктивных штаммов Escherichia coli - продуцентов рекомбинантных белков человека, используемых в современной медицине в качестве тромболитических агентов,
Известно, что урокиназа, выделяемая из мочи, представлена тремя формами: низкомолекулярной (33 кДа), высокомолекулярной двухцепочной (50-55 кДа) и высокомолекулярной одноцепочной (проурокиназа), со значительным преобладанием низкомолекулярной формы. Наибольшую ценность для медицины представляют тромболитические препараты в виде высокомолекулярных предшественников активаторов плазминогена, в особенности проурокиназа, вследствие ее низкой активности до момента ее активации на тромбе. Процесс получения проурокиназы из культуральной среды эукариотических клеток-продуцентов сравнительно несложен, но невыгоден из-за высокой стоимости культивирования клеток, что и послужило причиной развития генно-инженерного подхода к решению задачи производства активаторов плазминогена урокиназного типа на базе штаммов микроорганизмов.
Известна рекомбинантная плазмида pUK54trp207-I, кодирующая урокиназу человека и штамм Escherichia coli, полученный трансформацией клеток бактерий данной плазмидой (Holmes W.E., Pennica D. et al., Cloning and expression of human urokunaze type plasminogen activator in Esherichia coli, Bio Thechnology (1985) V. 3, p. 923-929).
Экспрессия рекомбинантной урокиназы в плазмиде pUK54trp207-I осуществляется с триптофанового промотора после индукции индолакриловой или индолуксусной кислотой. Выход составляет около 40 ед. активной урокиназы на 1 мл биомассы.
Известна рекомбинантная плазмидная ДНК pUABC, кодирующая модифицированный активатор плазминогена урокиназного типа (мАПУТ), и штамм Escherichia coli - продуцент мАПУТ (Патент РФ N 1692151, C 12 N 15/52, 1990).
Плазмида pUABC состоит из следующих структурных элементов:
XbaI - BglI - фрагмента (1.39 т.п.н.), содержащего район инициации репликации и промоторно-операторную область lac-оперона вектора pUC19;
BglI - PstI - фрагмента (1.28 т.п.н.), содержащего ген лактамазы вектора pUC18;
PstI - XbaI - фрагмента кДНК урокиназы человека (1.44 т.п.н.).
Модифицированный активатор плазминогена, кодируемый данной плазмидой, представляет собой рекомбинантную проурокиназу, которая отличается от природной проурокиназы заменой первых 24 аминокислот N-концевого домена, гомологичного эпидермальному ростовому фактору, на 15 чужеродных аминокислот.
Для конструирования плазмиды pUABC используют штамм Escherichia coli JM109, векторы pUC18 и pUC19 и фрагменты кДНК проурокиназы человека ScaI - EcoRI (0.42 т.п.н.), EcoRI - EcoRI (0.42 т.п.н.) и EcoRI - PstI (0.60 т.п.н. ), полученные в результате иммуно- и олигонуклеотидного скрининга библиотеки кДНК HL1011b из легочных фибробластов человека на основе вектора lambda gt11 (фирма CLONTECH, США). Характерной особенностью данной конструкции является модификация N-концевого домена проурокиназы, приводящая к утрате препаратом свойства придавать клеткам подвижность, промотируя тем самым рост и метастазирование опухолей.
Штамм-продуцент модифицированного АПУТ ВКПМ В-4534 получают трансформацией клеток Escherichia coli JM109 плазмидой pUABC. Штамм ВКПМ В-4534 устойчив к ампициллину и при выращивании в LB среде дает 2.2 г клеточной биомассы на 1 л культуральной среды и производит модифицированный АПУТ преимущественно в проферментной форме (мол. м. 43 кДа) в количестве 60000 ед. на 1 г биомассы (или 320 ед. на 1 мл биомассы) в лабораторном масштабе.
Однако данный продуцент недостаточно стабилен и продуктивен при широкомасштабном производстве.
Заявляемая группа изобретений позволяет значительно повысить продуктивность и стабильность штамма-продуцента мАПУТ.
Увеличение продуктивности и стабильности штамма-продуцента достигается прежде всего за счет изменения нетранслируемых последовательностей векторной части плазмиды pUABC, которые, не затрагивая последовательности гена, непосредственно кодирующего мАПУТ, повышают общую стабильности системы экспрессии мАПУТ в клетках Escherichia coli и усиливают ее транслирующую активность в отношении эукариотических генов. Таким образом, поскольку модификация не затрагивает кодирующих последовательностей, все свойства белкового продукта оказываются сохраненными, что подтверждается определением нуклеотидной последовательности гена мАПУТ и его N- и C-концевых аминокислот.
Новая рекомбинантная плазмидная ДНК pUABC22 (фиг. 1), кодирующая модифицированный активатор плазминогена урокиназного типа, имеет размер 4,5 т.п. н. и содержит:
- XmnI - BamHI - фрагмент ДНК плазмиды pUABC22 размером 2.99 т.п.н.;
- BamHI - KpnI - фрагмент ДНК размером 0.177 т.п.н., содержащий участок кодирующей области гена мАПУТ, соответствующий 12 C-концевым аминокислотам мАПУТ, и нетранслируемый элемент - искусственную межгенную последовательность МГП14;
- KpnI - SacI - фрагмент ДНК размером 0.57 т.п.н., содержащий ген тРНК Arg.;
- SacI - XmnI - фрагмент ДНК вектора pUC19 размером 0.79 т.п.н.;
- участок инициации репликации и промоторно-операторную область lac-оперона;
- генетические маркеры;
- ген устойчивости к ампициллину.
XmnI - BamHI - фрагмент ДНК плазмиды pUABC содержит 3'-концевую часть гена устойчивости к ампициллину, участок инициации репликации вектора pUC19 (ori), промоторную область и большую часть кодирующей области гена урокиназы, соответствующую последовательности мАПУТ с 1 по 389 аминокислоту.
Ген тРНК Arg кодирует соответствующую тРНК и не кодирует какой-либо белок.
SacI - XmnI - фрагмент ДНК вектора pUC19 содержит фрагмент гена бета-галактозидазы E.coli и 5'-концевую часть гена устойчивости к ампициллину.
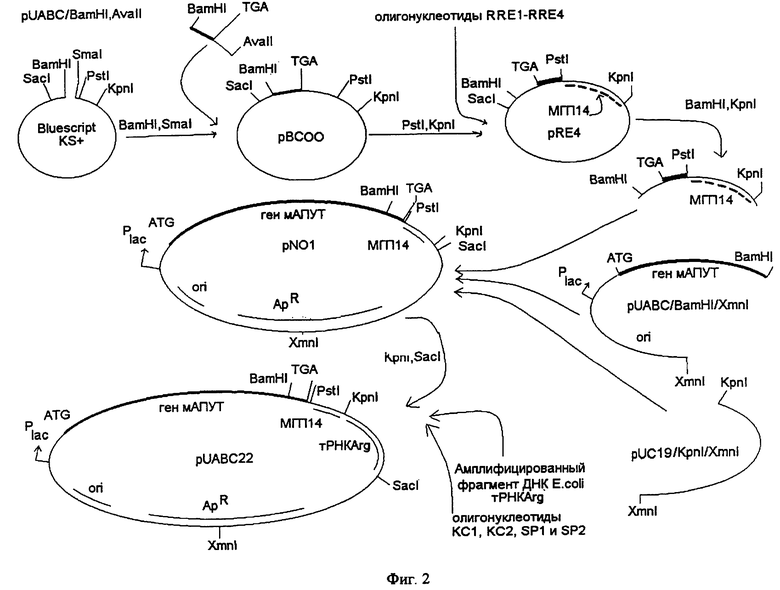
Плазмиду pUABC22 получают путем модификации плазмиды pUABC (фиг. 2), а именно введением в ее векторную часть двух нетранслируемых ДНК-элементов: искусственной межгенной последовательности МГП14 (0,13 т.п.н.), по структуре подобной межгенным повторам в геноме бактерий (МГП последовательности) (Cell (1984), V.37, р.1015-1026), и последовательности гена тРНК Arg (0,42 т.п.н. ), изолированной из хромосомы E.coli при помощи полимеразной цепной реакции.
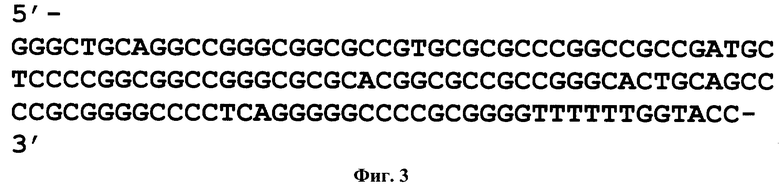
Новая искусственная межгенная последовательность МГП14 представлена на фиг.З. Данная последовательность не кодирует белковых продуктов.
Новый штамм-продуцент мАПУТ ВКПМ В-7666 получают трансформацией клеток Е. coli JM109 двумя плазмидами: pUABC22, кодирующей мАПУТ, и плазмидой pR4, продуцирующей дополнительное количество регуляторного белка LacI, также обладающего стабилизационным эффектом. Синтез рекомбинантного белка мАПУТ осуществляется под контролем регуляторных элементов lac-оперона вектора pUABC. Штамм ВКПМ В-7666 дает 3.0 г клеточной биомассы на 1 л культуральной среды и производит мАПУТ преимущественно в проферментной форме (мол.м. 43 кДа) в количестве 200-250 000 ед. на 1 г биомассы (3-5 мг на 1 л культуры). Благодаря применению двух нетранслируемых ДНК-элементов, эффективность системы экспрессии мАПУТ в новом штамме-продуценте ВКПМ В-7666 в 3-4 раз выше, чем у известного штамма ВКПМ В-4534.
Для получения активного рекомбинантного мАПУТ штамм-продуцент выращивают на LB-среде, клетки осаждают центрифугированием, вскрывают обработкой лизоцимом и ультразвуком, осадочную фракцию белков растворяют в гуанидинхлориде с 2-меркаптоэтанолом, разбавляют и проводят реконституцию в присутствии денатурирующего агента гуанидинхлорида и окисленной и восстановленной форм глютатиона, после чего препарат диализуют. Активность продукта измеряют при помощи теста на фибринолизис на фибриновых пластинках.
Пример 1. Конструирование плазмиды pUABC22.
Плазмиду pUABC гидролизуют рестриктазой AvaII и производят достройку липких концов с помощью фрагмента Кленова ДНК-полимеразы I. После фенольной депротеинизации и переосаждения этанолом производят гидролиз рестриктазой BamHI. После электрофоретического разделения рестрикционных фрагментов в 10% полиакриламидном геле фрагмент длиной 50 п.н. элюируют из геля, очищают и клонируют в вектор Bluescript KS+, гидролизованный рестриктазами BamHI и SmaI Полученные рекомбинанты идентифицируют по длине рестриктного фрагмента KpnI-SacI. Последовательность нуклеотидов вставки определяют по Сэнгеру.
Полученную плазмиду pBCOO гидролизуют рестриктазами PstI и KpnI и используют в качестве векторной последовательности. Синтетические олигонуклеотиды RRE1, RRE2, RRE3 и RRE4, последовательности которых представлены на фиг. 4, фосфорилируют при помощи полинуклеотидкиназы фага T4, попарно отжигают и легируют с вектором при помощи ДНК-лигазы фага T4. Полученные рекомбинанты идентифицируют по длине рестриктного фрагмента KpnI-SacI и последовательность нуклеотидов определяют по Сэнгеру.
Полученную плазмиду pRE4, содержащую последовательность МГП14, используют для конструирования плазмиды pNO1. Для этого плазмиду pUABC гидролизуют рестриктазами BamHI и XmnI, фрагмент размером 3 т.п.н. выделяют с помощью электрофореза в 0.8% агарозном геле. Плазмиду pUC19 гидролизуют рестриктазами KpnI и XmnI, фрагмент размером 0.79 т.п.н. выделяют с помощью электрофореза в 0.8% агарозном геле. Плазмиду pRE4 гидролизуют рестриктазами KpnI и BamHI и выделяют фрагмент размером 0.177 т.п.н. с помощью электрофореза в 1.2% агарозном геле. Полученные три фрагмента легируют при помощи ДНК-лигазы фага T4 и получают плазмиду pNO1.
Для получения фрагмента тРНК Arg используют полимеразную цепную реакцию (ПЦР), которую проводят на матрице ДНК E.coli 294 с использованием в качестве праймеров олигонуклеотидов YI и Y2:
5'-GCTGATTCAGTCAGGCGTCCCATTATCAGTG-3' и
5'-CAGGAAGGTAAAACCGTCTGTTCCGGGCA-3'
Условия реакции ПЦР: концентрация олигонуклеотидов составляет 50 uM, концентрация каждого из 4-х дезоксинуклеотидтрифосфатов составляет 250 uM. Используют буфер HEPES - NaOH (50 mM, pH 8.5), концентрация MgCl2 составляет 1.6 mM. Режим РЦР: 93oC 1 мин; далее 35 циклов (93oC 30 сек; 67oC 3 мин). Продукт ПЦР по результатам анализа в 1% агарозном геле имеет длину 0.5 т.п. н. Продукт ПЦР гидролизуют рестриктазами SphI и ClaI и выделяют фрагмент размером 0.57 т.п.н. с помощью электрофореза в агарозном геле. К полученному фрагменту присоединяют при помощи ДНК-лигазы фага T4 фланкирующие последовательности - олигонуклеотиды KC1, KC2 и SP1, SP2 соответственно
5'-CCGATCCGT-3';
3'-CATGGGCTAGGCAGC-5';
5'-CATGCGGCCGCAATTCGAGCT-3';
3'-GTACGTACGCCGGCGTTAAGC-5'
и клонируют между участками узнавания рестриктаз KpnI и SacI плазмиды pNO1. B результате получают плазмиду pUABC22. Правильность сборки рестриктных фрагментов подтверждают путем определения нуклеотидной последовательности по методу Сэнгера.
Пример 2. Конструирование плазмиды pR4.
Плазмиду pACYC184 гидролизуют рестриктазой PvuII с образованием фрагментов размером 0.5 и 3.7 т.п.н., гидролизат легируют с синтетическим SalI- линкером (5'-GGTCGACC-3') и, после инактивации ДНК-лигазы, гидролизуют сначала рестриктазой SalI с образованием набора фрагментов длиной 0.5, 1.6 и 2.1 т. п. н., а затем рестриктазой HindIII с образованием фрагментов длиной 0.5, 1.0, 1.6 и 2.1 т. п.н. Фрагмент длиной 1.0 т.п.н. очищают и используют в дальнейшем. Плазмиду pNEO гидролизуют рестриктазами SalI и HindIII с образованием фрагментов размером 1.8 и 3.7 т.п.н. Фрагмент длиной 1.8 т.п.н. очищают и используют в дальнейшем. Полученные фрагменты легируют и образовавшимся фрагментом трансформируют клетки штамма E.coli JM109. Полученная плазмида pK0 размером 2.8 т.п.н. устойчива к канамицину. Идентификацию производят по длинам рестриктных фрагментов SalI - HindIII.
Плазмиду pK0 гидролизуют рестриктазой AvaII таким образом, чтобы один акт гидролиза приходился в среднем на одну молекулу плазмиды. После фенольной депротеинизации полученный гидролизат обрабатывают при помощи нуклеазы Mung bean. После фенольной депротеинизации гидролизат легируют с синтетическим SalI-линкером (5'-GGTCGACC-3') и после инактивации ДНК-лигазы гидролизуют рестриктазой SalI. После фенольной депротеинизации смесь обрабатывают ДНК-лигазой фага T4 и трансформируют клетки штамма E.coli JM109. Среди рекомбинантов, устойчивых к канамицину, отбирают клон, имеющий размер 2.5 т.п.н. и содержащий уникальный участок узнавания рестриктазы SalI и получают плазмиду pK1.
Плазмиду pMC9 расщепляют рестриктазой EcoRI, достраивают липкие концы с помощью фрагмента Кленова ДНК-полимеразы I. После фенольной депротеинизации и переосаждения этанолом гидролизат легируют с синтетическим SalI-линкером (5'-GGTCGACC-3') и после инактивации ДНК-лигазы гидролизуют рестриктазой SalI. Фрагмент длиной 1.3 т.п.н. очищают и легируют с плазмидой K1, расщепленной с помощью рестриктазы SalI. Полученной лигазной смесью трансформируют клетки штамма E.coli JM109. Колонии трансформантов высевают на чашки с L-агаром, содержащим канамицин 25 мкг/мл и выращивают в LB-среде, содержащей канамицин 25 мкг/мл). Выделяют плазмидную ДНК, отбирают клон, содержащий фрагмент SalI-SalI длиной 1.3 т.п.н. и получают плазмиду pR4 размером 3.8 т. п.н.
Пример 3. Получение штамма-продуцента.
Клетки штамма Escherichia coli JM109 трансформируют двумя плазмидами: pR4 и pUABC22 и получают штамм-продуцент модифицированного активатора плазминогена урокиназного типа.
Пример 4. Получение рекомбинантного модифицированного активатора плазминогена урокиназного типа.
Бактерии штамма E. coli ВКПМ В-766, содержащие плазмиды pUABC22 и pR4, выращивают до плотности OD600 = 2.5 в течение 16 ч в 50 мл LB-среды с ампициллином (100 мкг/мл) при 37oC и интенсивной аэрации. По окончании выращивания клетки собирают центрифугированием 30 мин при 4000 об/мин, суспендируют в 2.5 мл 20 мМ Трис-HCl, pH 6.7, 30 мМ NaCl, добавляют 2.5 мг лизоцима, инкубируют 10 мин при 4oC, добавляют Трис-HCl, pH 8.3 до 50 мМ, ЭДТА до 20 мМ, инкубируют 30 мин при 4oC, после чего обрабатывают ультразвуком 1 мин. Осадочную фракцию клеточного экстракта отделяют центрифугированием в течение 90 мин при 5000 об/мин, суспендируют в 1 мл 2%-ного Тритона Х-100, центрифугируют 5 мин при 14000 об/мин, суспендируют в 100 мкл 200 мМ ЭДТА, 500 мМ Трис-HCl, pH 8.0, добавляют 800 мкл денатурирующего раствора (6 М гуанидинхлорид, 100 мМ 2-меркаптоэтанол), инкубируют 20 мин при 65oC нерастворимый осадок убирают центрифугированием.
Процедуру реконституции ферментативной активности проводят следующим образом. Раствор разбавляют в 20 раз буфером: 100 мМ Трис-HCl, pH 9.0, 200 мМ аргинин-хлорид, 5 мМ восстановленный глютатион, 1 мМ окисленный глютатион, денатурирующий агент (1 М гуанидинхлорид), инкубируют 40 ч при 4oC, после чего диализуют против двух смен по 1 л 100 мМ NaCl, 20 мМ Трис-HCl, pH 8.0, в течение 6 ч. Выпавший осадок удаляют центрифугированием и измеряют активность в тесте на фибринолизис как описано выше. Активность мАПУТ в образце составляет 1500.
Ренатурированный рекомбинантный модифицированный активатор плазминогена представлен, главным образом, проферментной формой с молекулярной массой 43 кДа, что демонстрируют данные электрофоретического и зимографических анализов. Выход активного мАПУТ составляет 200000-250000 ед. на 1 г биомассы, что в 4 раза превосходит выход мАПУТ, получаемый в аналогичных условиях в случае штамма-продуцента ВПКМ В-4534.

Изобретение относится к генной инженерии, а именно к технологии получения высокопродуктивных штаммов Eserichia coli - продуцентов рекомбинантных белков человека, используемых в современной медицине в качестве тромболитических агентов. Новая рекомбинантная плазмидная ДНК рUABC22, кодирующая модифицированный активатор плазминогена урокиназного типа (мАПУТ) имеет размер 4,5 т.п.н. и содержит: XmnI - BamHI - фрагмент ДНК плазмиды рUАВС22 размером 2,99 т. п. н.; BamHI - KpnI - фрагмент ДНК размером 0,177 т.п.н., содержащий участок кодирующей области гена мАПУТ, соответствующий 12 С-концевым аминокислотам мАПУТ, и нетранслируемый элемент - искусственную межгенную последовательность МГП14; Kpn I - SacI - фрагмент ДНК размером 0,57 т.п. н. , содержащий ген тРНК Аrg; SасI - XmnI - фрагмент ДНК вектора рUС19 размером 0,79 т. п. н.; участок инициации репликации и промоторно-операторную область lас-оперона; генетические маркеры; ген устойчивости к ампициллину. Нетранслируемые ДНК-элементы - искусственная межгенная последовательность МГП14 и ген тРНК Аrg повышают общую стабильность системы экспрессии мАПУТ в клетках Escherichia coli и усиливают ее транслирующую активность в отношении эукариотических генов. Новый штамм ВКПМ В-7666 дает 3,0 г клеточной биомассы на 1 л культуральной среды и производит мАПУТ преимущественно в проферментной форме (мол.м. 43 кДа) в количестве 200000 - 250000 ед. на 1 г биомассы. 3 с.п. ф-лы, 4 ил.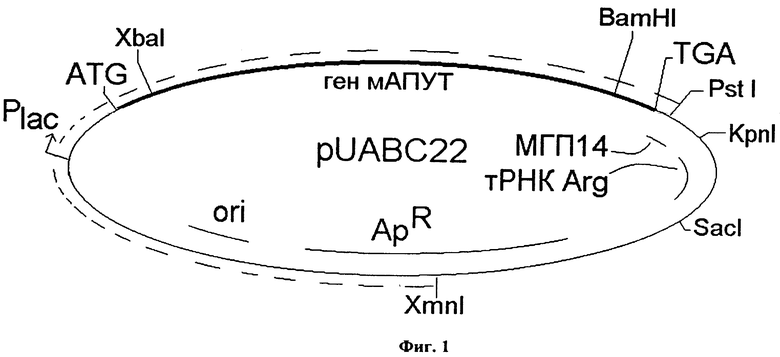
| 1990 |
|
RU1692151C | |
| EP 0405285 A1, 02.01.91 | |||
| DE 4020438 A1, 31.01.91. | |||
Авторы
Даты
1999-10-27—Публикация
1999-04-06—Подача