Изобретение относится к новым амидам органических кислот формулы I
где A означает остатки формул
и их стереоизомерные формы и/или их физиологически переносимые соли,
при этом если A имеет значение остатка a) R1 означает:
а) водород;
b) алкил с 1-6 C-атомами;
c) алкил с 1-4 C-атомами, одно- или многократно замещенный, содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод;
d) фенил;
R2 означает
a) алкенил с 2-3 C-атомами;
b) бензил;
R3 означает
a) пиридил, одно- или многократно замещенный, содержащий в качестве заместителей
1) водород,
2) галоген, как фтор, хлор, бром или иод,
3) нитро,
4) алкил с 1-3 C-атомами
b) группу формулы II
в которой R4, R5 и R6 могут быть одинаковыми или различными и означают
1) галоген, как фтор, хлор, бром или иод,
2) нитро,
3) бензоил, незамещенный или одно- или многократно замещенный и содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод, метил, метокси,
4) (C1-C3)-алкокси, одно- или многократно замещенный и содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод,
5) гидрокси,
6) алкилсульфонил с 1-3 C-атомами в алкильной цепи,
7) циано,
8) бензоил,
9) (C1-C3)-алкил;
c) пиримидинил, одно- или многократно замещенный и содержащий в качестве заместителей
1) алкил с 1-3 C-атомами;
d) индолил или
e) индазолинил,
в случае, если A имеет значение остатков b)
R3 означает фенил, одно- или многократно замещенный и содержащий в качестве заместителей галоген или алкил с 1-3 C-атомами, одно- или многократно замещенный, содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод;
R7 означает водород или алкил с 2-4 C-атомами,
b) R3 означает 1) пиридил,
2) пиридил, одно- или многократно замещенный и содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод, алкил с 1-3 C-атомами,
3) пиримидинил, замещенный алкилом с 1-3 C-атомами,
4) индазолил,
5) фенил, одно- или многократно замещенный и содержащий в качестве заместителей бензоил, незамещенный или одно- или многократно замещенный и содержащий в качестве заместителей галоген, как фтор, хлор, бром или иод,
R7 1) алкил с 1-4 C-атомами,
2) водород,
3) CF3.
Было показано, что амиды формулы I обладают противоопухолевой активностью. Многие из известных противоопухолевых средств во время терапии вызывают в качестве побочного действия тошноту, рвоту или понос, что также делает необходимым пребывание в больнице. Далее, эти лекарства изменяют также скорость обмена других аутогенных клеток, что приводит затем к таким симптомам, как, например, выпадение волос или малокровие (анемия). Эти симптомы не наблюдаются при лечении людей и животных соединениями формулы I. Эти активные вещества, в противоположность известным до сих пор цитотоксическим противораковым средствам, не наносят вреда иммунной системе (Bartlett, Int. J. Immunophamuac. 1986, 8: 199-204). Тем самым открываются новые пути опухолевой терапии, так как аутогенной защитной системе вреда не наносится, в то время как рост опухолевых клеток затрудняется. Неожиданно, большое число опухолевых клеток подавляется этими веществами, в то время как клетки иммунной системы, как, например, T-лимфоциты, подавляются только при 50-кратной концентрации вещества.
Соединение формулы I и его физиологически переносимые соли пригодны, в частности, для лечения большого числа раковых заболеваний. К видам рака, которые особенно хорошо подавляются этими соединениями, относятся, например, лейкемия, в частности, хроническая лейкемия T- и B-типа клеток, рак лимфатических узлов, например, лимфома Ходжкина и неходжкинская лимфома, карциномы, саркомы и рак кожи. Активные вещества могут применяться либо самостоятельно, к примеру, в форме микрокапсул, в смесях друг с другом, либо в комбинации с пригодными вспомогательными веществами и/или веществами носителями.
Соединения согласно изобретению получают путем взаимодействия соединения формулы V
в которой X означает атом галогена, предпочтительно хлор или бром, и R1 имеет вышеуказанное значение с амином формулы
в которой R2 и R3 имеют вышеуказанное значение, и при необходимости, соединение формулы I, где A имеет значение остатка a) обрабатывают основанием.
Соединения согласно изобретению или их соли могут применяться для изготовления лекарств для профилактики и/или лечения ревматических заболеваний.
Предметом изобретения являются также фармацевтические композиции, которые состоят по меньшей мере из одного соединения формулы I и/или по меньшей мере одной из его физиологически переносимых солей, или по меньшей мере этого активного вещества наряду с пригодными и физиологически переносимыми носителями, растворителями и/или другими вспомогательными веществами.
Предлагаемые по изобретению лекарственные средства могут применяться орально, топически, ректально или, в случае необходимости, также парэнтерально, причем оральное применение является предпочтительным.
Пригодными твердыми или жидкими формами изготовления являются, например, грануляты, порошок, драже, таблетки, (микро)капсулы, свечи, сиропы, соки, суспензии, эмульсии, капли или растворы для инъекций, а также препараты с замедленным освобождением активного вещества, при приготовлении которых используются обычные вспомогательные вещества, такие как носители, связующие средства, средства для покрытия, средства, вызывающие набухание, мягчители и смачивающие добавки, вкусовые добавки, сахаристое средство и агент растворения. Как часто используемые вспомогательные вещества, следует назвать, например, карбонат магния, диоксид титана, лактозу, маннит и другие сахара, тальк, молочный белок, желатин, крахмал, целлюлозу и ее производные, животные и растительные масла, полиэтиленгликоли и растворители, как, например, стерильная вода и одно- или многоатомные спирты, например, глицерин.
Фармацевтические препараты изготавливаются и применяются предпочтительно в дозированном виде, причем каждая дозировочная единица в качестве активной компоненты содержит определенную дозу по меньшей мере одного соединения формулы I и/или по меньшей мере одной из его физиологически переносимых солей. В случае твердых дозировочных единиц, таких как таблетки, капсулы, драже или свечи, эта доза может составлять до, приблизительно, 300 мг, предпочтительно, однако, приблизительно от 10 до 50 мг.
Для лечения больных лейкемией взрослых пациентов (70 кг) при оральном применении показаны, - в зависимости от эффективности воздействия соединений формулы I и/или их физиологически переносимых солей на человека, - дневные дозы от, приблизительно, 5 до 300 мг активного вещества, предпочтительно, от, приблизительно, 25 до 100 мг. Смотря по обстоятельствам, могут, однако, применяться также более высокие или более низкие дневные дозы. Прием дневной дозы может осуществляться как в виде единичного приема в форме отдельной дозировочной единицы или нескольких меньших дозированных единиц, так и в виде многократного приема разделенной дозы через определенные интервалы времени.
В заключение, соединения формулы I и/или по меньшей мере одна из их физиологически переносимых солей при изготовлении названных выше лекарственных форм могут входить в рецептуру также и вместе с другими пригодными активными веществами, к примеру, другими противоопухолевыми средствами, иммуноглобулинами, моноклональными антителами, иммуностимулирующими агентами или антибиотиками. Эти соединения могут также применяться в дополнение к лучевой терапии.
Фармакологические испытания и результаты
В качестве эффективного теста химиотерапии применялся ин витро тест пролиферации культур клеток.
Пример 1. Испытание (тест) пролиферации.
Clicks -/RPMI 1640 среда (50:50) с L-глутамином без NaHCO3 в порошкообразной форме для 10 л (Серомед, Биохром, Берлин, ФРГ) растворяется в 9 л воды и стерильно фильтруется в флаконы емкостью 900 мл.
Среда для промывания
900 мл основной среды смешиваются с 9,6 мл 7%-го раствора гидрокарбоната натрия и 5 мл HEPES (N-2-гидроксиэтил-пиперазин-N-2-этанолсульфоновая кислота) (Гибко, Эггенштейн, ФРГ).
Рабочая среда (среда для употребления)
900 мл основной среды плюс 19 мл NaHCO3-раствора (7,5%; 10 мл HEPES-раствора и 10 мл L-глутамин-раствора (200 мМ)).
Среда для митогениндуцированной пролиферации лимфоцитов
Рабочая среда смешивается с 1% термически активированной (30 мин, 56oC) эмбриональной телячьей сывороткой.
Среда опухолевых клеток.
Для выдерживания опухолевых клеток и гибридомных клеток рабочая среда смешивается с 5% эмбриональной телячьей сыворотки (FCS).
Культурная среда для клеточных линий.
Для выдерживания клеточных линий 900 мл рабочей среды смешиваются с 10% FCS, 10 мл NEA (non-essentil amino acids - заменимые аминокислоты) - раствора (Гибко), 10 мл раствора пирувата натрия (100 мМ, Гибко) и 5 мл 10-2 М меркаптоэтанола. Получение и обработка клеток селезенки для митогениндуцированной пролиферации лимфоцитов.
Мыши умерщвляются посредством цирвикальной дислокации и селезенки извлекаются в асептических условиях. На стерильном сите с размером пор 80 меш селезенки размельчаются и с помощью пластикового шприца (10 мл) осторожно вносятся в чашку Петри с рабочей средой. Для удаления эритроцитов из суспензии клеток селезенки смесь приблизительно в течение 1 минуты инкубируется при комнатной температуре при периодическом встряхивании в гипотоническом 0,17 М растворе хлорида аммония. При этом эритроциты лизируются, в то время как на жизненность и реактивность лимфоцитов влияния не оказывается. После центрифугирования (7 минут/340 г) лизат отбрасывается, клетки дважды промываются водой и затем вносятся в соответствующую тестовую (опытную) среду.
Митогениндуцированная пролиферация лимфоцитов.
5 • 105 обработанных клеток селезенки из женских особей NMRI-мышей вместе с различными митогенами и препаратами в 200 мл тестовой среды вносились пипеткой в лунки плейтов для титрования с плоским дном. Использовались следующие концентрации митогенов и препарата:
конканавалин A (Серва): 0,5 - 0,25 - 0,12 мкг/мл
липополисахарид (Кальбиохем): 1,0 - 0,5 - 0,1 мкг/мл
фитогемагглютинин (Гибко): 0,5 - 0,25 - 0,12% исходного раствора Pokeweed митоген (Гибко) соединение 1 или 2: 50, 25, 10, 7,5, 5, 2,5, 1, 0,5, 0,1 мкмоль
Как положительный контроль определялась группа с добавками митогена без препарата. В случае отрицательного контроля речь идет о клетках в культурной среде с препаратом, без добавок митогена. Каждая концентрация митогена перепроверялась 4 раза со всеми концентрациями препарата. После 48 часов инкубирования при 37oC/5% CO2 к клеткам добавлялось 25 мкл/лунку тритий-тимидина (Эмершем) с активностью 0,25 мкКи/лунку (9,25 • 103 Бк). После этого проводится дальнейшее инкубирование при тех же условиях в течение 16 часов. Затем клетки при помощи прибора для сбора клеток (Флоу Лаборэторис) собираются на фильтровальную бумагу, причем не включенный тимидин собирается в специальный флакон. Фильтровальная бумага высушивается, штампуется и вместе с 2 мл сцинтиллятора (Rotiszint 22, фирма Рот) помещается в колбу, которая затем еще 2 часа охлаждается при 4oC. Количество радиоактивности, "исходящей" от клеток, измеряется в Бета-счетчике (фирма Пакард, Tricarb - 460 c).
Подготовка опухолевых клеток и клеточных линий для опыта по пролиферации
Используемые в опыте опухолевые клетки или клеточные линии берутся в логарифмической фазе роста, дважды промываются средой для промывания и суспендируются в соответствующую среду.
Проведение и анализ опыта по пролиферации.
Опыт по пролиферации проводился в плейтах для титрования с круглым дном. Соединение 1 и интерлейкины растворялись в 50 мкл соответствующей среды /каждую лунку, и число клеток (5 • 105) устанавливалось 100 мкл/лунку, так что конечный объем получался 200 мкл/лунку. Во всех опытах значения определялись 4 раза. Клетки без препарата и без фактора роста определялись как отрицательный контроль, и клетки без препарата с фактором роста давали значения для положительного контроля. Значение отрицательного контроля вычиталось из всех установленных значений, и разность положительный контроль минус отрицательный контроль устанавливалась 100%.
Плейты инкубировались 72 часа при 37oC/5% CO2, и скорость пролиферации определялась соответственно тому, как это осуществлялось при митогениндуцированной пролиферации лимфоцитов.
Клеточные линии извлекались из исходного (маточного) раствора ATCC, American Type Culture Collection.
Таблица 1 показывает концентрации, при которых происходит 50%-ное подавление ингибирования.
В таблице 1а приводятся результаты испытаний на пролиферацию.
В таблице 1б приводятся результаты испытаний на пролиферацию.
Пример 2. Острая токсичность при оральном применении.
Соединение 1 для определения острой токсичности применялось орально на мышах и крысах.
LD50-значения определялись по Литчфилду и Вилкоксону (Litchfield & Wilcoxon).
Вес NMRI-мышей (NMRI: Naval Medical Research Institute) составлял от 20 до 25 г, и вес SD-кры (SD: Spraque-Dawley) составлял от 120 до 165 г. Перед экспериментом мыши выдерживались без пищи приблизительно 18 часов. Через 5 часов после приема испытываемого вещества мышей снова нормально кормили. Через 3 недели животные умерщвлялись хлороформом и вскрывались. На 1 дозировку использовались 6 животных. Результаты обобщены в таблице 2.
Пример 3. Острая токсичность после внутрибрюшинного применения.
Острая токсичность после внутрибрюшинного применения испытываемых веществ определялась на NMRI-мышах (вес 20 - 25 г) и на SD-крысах (вес 120 - 195 г). Испытываемое вещество суспендировалось в 1%-й раствор натрийкарбоксиметилцеллюлозы. Различные дозировки тестируемого вещества вводились мышам в количество 10 мл/кг веса тела и крысам - в количестве 5 мл/кг веса тела. На одну дозировку использовались 10 животных. Через 3 недели острая токсичность определялась по методу Литчфилда и Вилкоксона. Результаты опытов обобщены в таблице 3.
Примеры изготовления
Структура всех описанных ниже соединений устанавливалась при помощи элементарного анализа и ИК-, а также 1H-ЯМР-спектров (таблица 4).
4. N-(4-хлордифторметокси)фенил-5-этилизоксазол-4-карбоксамид
0,1 моль (19,4 г) 4-хлордифторометоксианилина, растворенного в 180 мл ацетонитрила, при комнатной температуре, по каплям смешиваются с раствором 0,05 моль (7,3 г) хлорида 5-метилизоксазол-4-карбоновой кислоты в 30 мл ацетонитрила при перемешивании. Перемешивают еще 20 минут и отфильтровывают жидкость от выпавшей соли. Фильтрат высушивают при пониженном давлении. Получают таким образом 28,5 г (94,2% от теории) кристаллического продукта. Температура плавления (из смеси циклогексан-ацетон 20-1 (объем/объем): 112 - 113oC.
Аналогично описанному выше примеру получаются следующие соединения формулы I:
5. N-(4-фторфенил)-изоксазол-4-карбоксамид (температура плавления от 162 до 164oC) из хлорида изоксазол-4-карбоновой кислоты и 4-фторанилина.
6. N-(4-хлорфенил)-изоксазол-4-карбоксамид (температура плавления 175 - 177oC /разложение/) из хлорида изоксазол-4-карбоновой кислоты и 4-хлоранилина.
7. N-(4-бромфенил)-изоксазол-4-карбоксамид (температура плавления 184 - 186oC /разлож./) из хлорида изоксазол-4-карбоновой кислоты и 4-броманилина.
8. N-(4-иодфенил)-изоксазол-4-карбоксамид (температура плавления 207 - 208oC) из хлорида изоксазол-4-карбоновой кислоты и 4-иоданилина.
9. N-(4-нитрофенил)-изоксазол-4-карбоксамид (температура плавления 208 - 210oC /разлож./) из хлорида изоксазол-4-карбоновой кислоты и 4-нитроанилина.
10. N-(3,4-метилендиоксифенил)-изоксазол-4-карбоксамид (температура плавления 168 - 169oC) из хлорида изоксазол-4-карбоновой кислоты и 3,4-метилендиоксианилина.
11. N-(4-бензоилфенил)-изоксазол-4-карбоксамид (температура плавления 197 - 199oC /разлож./) из хлорида изоксазол-4-карбоновой кислоты и 4-аминобензофенона.
12. N-(4-фторфенил)-5-этилизоксазол-4-карбоксамид (температура плавления 75 - 77oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-фторанилина.
13. N-(4-хлорфенил)-5-этилизоксазол-4-карбоксамид (температура плавления 103 - 105oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-хлоранилина.
14. N-(4-бромфенил)-5-этилизоксазол-4-карбоксамид (температура плавления 117 - 118oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-броманилина.
15. N-(4-нитрофенил)-5-этилизоксазол-4-карбоксамид (температура плавления 139 - 141oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-нитроанилина.
16. N-(3,4-метилендиоксифенил)-5-этилизоксазол-4-карбоксамид (температура плавления 105 - 106oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 3,4-метилендиоксианилина.
17. N-(4-трифторметоксифенил)-5-этилизоксазол-4-карбоксамид (температура плавления 52 - 54oC) из 5-этилизоксазол-4-карбоксиамида и 4-трифторметоксианилина.
18. N-(4-бензоилфенил)-5-этилизоксазол-4-карбоксамид (температура плавления 168 - 170oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-аминобензофенона.
19. N-(4-(4-фторбензоил)фенил)-5-этилизоксазол-4-карбоксамид (температура плавления 153 - 155oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-(4-фторбензоил)анилина.
20. N-(4-(4-хлорбензоил)фенил)-5-этилизоксазол-4-карбоксамид (температура плавления 159 - 161oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-(4-хлорбензоил)анилина.
21. N-(4-(4-бромбензоил)фенил)-5-этилизоксазол-4-карбоксамид (температура плавления 178 - 181oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 4-(4-бромбензоил)анилина.
22. N-(4-бензоилфенил)-5-пропилизоксазол-4-карбоксамид (температура плавления 134 - 135oC) из хлорида 5-пропилизоксазол-4-карбоновой кислоты и 4-аминобензофенона.
23. N-(4-хлорфенил)-5-бутилизоксазол-4-карбоксамид (температура плавления 91 - 92oC) из хлорида 5-бутилизоксазол-4-карбоновой кислоты и 4-хлоранилина.
24. N-(4-бензоилфенил)-5-бутилизоксазол)-4-карбоксамид (температура плавления 108 - 110oC) из хлорида 5-бутилизоксазол-4-карбоновой кислоты и 4-аминобензофенона.
25. N-(4-фторфенил)-5-трифторметилизоксазол-4-карбоксамид (температура плавления 97oC) из хлорида 5-трифторметилизоксазол-4-карбоновой кислоты и 4-фторанилина.
26. N-(4-хлорфенил)-5-трифторметилизоксазол-4-карбоксамид (температура плавления 90 - 92oC) из хлорида 5-трифторметилизоксазол-4-карбоновой кислоты и 4-хлоранилина.
27. N-(4-нитрофенил)-5-трифторметилизоксазол-4-карбоксамид (температура плавления 136 - 138oC) из хлорида 5-трифторметилизоксазол-4-карбоновой кислоты и 4-нитроанилина.
28. N-(3,4-метилендиоксифенил)-5-трифторметилизоксазол-4- карбоксамид (температура плавления 114 - 116oC) из хлорида 5-трифторметилизоксазол-4-карбоновой кислоты и 3,4-метилендиоксианилина.
29. N-(4-трифторметилфенил)-5-хлорметилизоксазол-4- карбоксамид (температура плавления 136 - 137oC) из хлорида 5-хлорметилизоксазол-4-карбоновой кислоты и 4-трифторметиланилина.
30. N-(4-трифторметилфенил)-5-фенилизоксазол-4-карбоксамид (температура плавления 159 - 160oC) из хлорида 5-фенилизоксазол-4-карбоновой кислоты и 4-трифторметиланилина.
31. N-(4-фторфенил)-5-фенилизоксазол-4-карбоксамид (температура плавления 151 - 153oC) из хлорида 5-фенилизоксазол-4-карбоновой кислоты и 4-фторанилина.
32. N-(4-метилсульфонилфенил)-5-метилизоксазол-4- карбоксамид (температура плавления 170 - 172oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 4-метилсульфониланилина.
33. N-бензил-N-(4-трифторметилфенил)-5-метилизоксазол-4- карбоксамид (температура плавления 87 - 89oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 11-бензил-4-трифторметиланилина.
34. N-(5-хлор-2-пиридил)-изоксазол-4-карбоксамид (температура плавления 254 - 255oC) из хлорида изоксазол-4-карбоновой кислоты и 2-амино-5-хлорпиридина.
35. N-(5-хлор-2-пиридил)-5-этилизоксазол-4-карбоксамид (температура плавления 133 - 136oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 2-амино-5-хлорпиридина.
36. N-(5-бром-2-пиридил)-5-этилизоксазол-4-карбоксамид (температура плавления 144 - 145oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 2-амино-5-бромпиридина.
37. N-(5-нитро-2-пиридил)-5-этилизоксазол-4-карбоксамид (температура плавления 236 - 237oC) из хлорида 5-этилизоксазол-4-карбоновой кислоты и 2-амино-5-нитропиридина.
38. N-(5-хлор-2-пиридил)-5-фенилизоксазол-4-карбоксамид (температура плавления 160 - 161oC) из хлорида 5-фенилизоксазол-4-карбоновой кислоты и 2-амино-5-хлорпиридина.
39. N-(5-индолил)-5-метилизоксазол-4-карбоксамид (температура плавления 155 - 157oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 5-аминоиндола.
40. N-(6-индазолил)-5-метилизоксазол-4-карбоксамид (температура плавления 198 - 202oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 6-аминоиндазола.
41. N-(5-индазолил)-5-метилизоксазол-4-карбоксамид (температура плавления 218 - 220oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 5-аминоиндазола.
42. N-аллил-N-фенил-5-метилизоксазол-4-карбоксамид (температура плавления 79 - 85oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 11-аллиланилина.
43. N-(3-(1,1,2,2-тетрафторэтокси)фенил-5- метилизоксазол-4-карбоксамид (температура плавления 97oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 3-(1,1,2,2-тетрафторэтокси)анилина.
44. N-(4-цианофенил)-5-метилизоксазол-4-карбоксамид (температура плавления 197 - 200oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 4-цианоанилина.
45. N-(4-метилмеркаптофенил)-5-метилизоксазол-4-карбоксамид (температура плавления 134 - 136oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 4-метилмеркаптоанилина.
46. N-(4,6-диметил-2-пиридил)-5-метилизоксазол-4-карбоксамид (температура плавления 210oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 2-амино-4,6-диметилпиридина.
47. N-(4,6-диметил)-2-пиразинил)-5-метилизоксазол-4-карбоксамид (температура плавления 222 - 226oC) из хлорида 5-метилизоксазол-4-карбоновой кислоты и 2-амино-4,6-диметилпиразина.
48. N-(трифторметоксифенил)амид 2-циано-3-гидроксикротоновой кислоты
1,1 моля (28,6 г) N-(4-трифторметоксифенил)-5-метилизоксазол-4- карбоксамида растворялись в 100 мл этанола и при 20oC смешивались с раствором 0,11 моль (4,4 г) едкого натра в 100 мл воды. Смесь перемешивалась в течение 30 минут и после разбавления водой подкисляется концентрированной соляной кислотой. Выпавшая кристаллическая масса отсасывается, промывается водой и высушивается на воздухе. Таким образом получают 27,7 г (97,1% от теории) N-(трифторметоксифенил)амида 2-циано-3-гидроксикротоновой кислоты с температурой плавления 171 - 176oC (из этанола).
Аналогично описанному выше примеру получаются следующие соединения формулы Iа или Iб.
49. N-(4-(1,1,2,2-тетрафторэтокси)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 166 - 164oC) из N-(4-(1,1,2,2-тетрафторэтокси)фенил)-5-метилизоксазол-4-карбоксамида.
50. N-(5-хлор-2-пиридил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 213 - 215oC /разлож./) из N-(5-хлор-2-пиридил)-5-метилизоксазол-4-карбоксамида.
51. N-(2-хлор-3-пиридил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 218 - 131oC) из N-(2-хлор-3-пиридил)-5-метилизоксазол-4-карбоксамида.
52. N-(4-бензолфенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 186 - 188oC) из N-(4-бензоилфенил)-5-метил-изоксазол-4-карбоксамида.
53. N-(4-(4-хлорбензоил)фенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 157 - 159oC) из N-(4-(4-хлорбензоил)фенил)-5-этилизоксазол-4-карбоксамида.
54. N-(4-(4-бромбензоил)фенил)амид 2-циано-3-гидрокси кротоновой кислоты (температура плавления 221 - 223oC) из N-(4-(4-бромбензоил)фенил)-5-метилизоксазол-4-карбоксамида.
55. N-(4-(4-метоксибензоил)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 74 - 75oC) из N-(4-(4-метоксибензоил)фенил)-5-метилизоксазол-4-карбоксамида.
56. N-(4-(4-метилбензоил)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 177 - 179oC) из N-(4-(4-метилбензоил)фенил)-5-метилизоксазол-4-карбоксамида.
57. N-(5-хлор-2-пиридин)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 206 - 208oC) из N-(5-хлор-2-пиридил)-5-этилизоксазол-4-карбоксамида.
58. N-(5-бром-2-пиридил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 200 - 202oC /разлож./) из N-(5-бром-2-пиридил)-5-этилизоксазол-4-карбоксамида.
59. N-(4-нитрофенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 202 - 203oC /разлож./) из N-(4-нитрофенил)-5-этилизоксазол-4-карбоксамида.
60. N-(3,4-метилендиоксифенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 99 - 100oC) из N-(3,4-метилендиоксифенил)-5-этилизоксазол-4-карбоксамида.
61. N-(4-бензоилфенил)амид 2-циано-3-гидрокси-4-пропилкротоновой кислоты из N-(4-бензоилфенил)-5-бутилизоксазол-4-карбоксамида.
62. N-(5-бром-2-пиридил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 220 - 223oC /разлож./) из N-(5-бром-2-пиридил)-5-метилизоксазол-4-карбоксамида.
63. N-(4-(4-хлорбензоил)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 219 - 223oC /разлож. /) из N-(4-(4-хлорбензоил)фенил)-5-метилизоксазол-4-карбоксамида.
64. N-(4-(4-фторбензоил)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 229 - 231oC /разлож. /) из N-(4-(4-фторбензоил)фенил)-5-метилизоксазол-4-карбоксамида.
65. N-(4-(4-фторбензоил)фенил)амид 2-циано-4-метил-3-гидроксикротоновой кислоты (температура плавления 147 - 148oC) из N-(4-(4-фторбензоил)фенил)-5-этилизоксазол-4-карбоксамида.
66. N-(4-(4-бромбензоил)фенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 153 - 155oC) из N-(4-(4-бромбензоил)фенил)-5-этилизоксазол-4-карбоксамида.
67. N-(4-трифторметокси)фениламид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 166 - 167oC) из N-(4-трифторметокси)фенил)-5-этилизоксазол-4-карбоксамида.
68. N-(4-трифторфенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 145oC) из N-(4-фторфенил)-5-этилизоксазол-4-карбоксамида.
69. N-(3,4-метилендиоксифенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 99 - 100oC) из N-(3,4-метилендиоксифенил)-5-этилизоксазол-4-карбоксамида.
70. N-(4-метилсульфонил)фениламид 2-циано-3-гидроксикротоновой кислоты (температура плавления 196 - 198oC) из N-(4-метилсульфонил)фенил-5-метилизоксазол-4-карбоксамида.
71. N-аллил-N-фениламид 2-циано-3-гидроксикротоновой кислоты (температура плавления 57 - 50oC) из N-аллил-N-фенил-5-метилизоксазол-4-карбоксамида.
72. N-(4-этоксикарбонилметил-2-тиазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 147oC) из N-(4-этоксикарбонилметил-2-тиазолил)-5-метилизоксазол-4-карбоксамида.
73. N-(2-бензимидазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура разложения > 300oC) из N-(2-бензимидазолил)-5-метилизоксазол-4-карбоксамида.
74. N-(4-метил-2-тиазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 210 - 212oC /разлож./) из N-(4-метил-2-тиазолил)-5-метилизоксазол-4-карбоксамида.
75. N-(4-хлор-2-бензотиазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 211 - 213oC /разлож./) из N-(4-хлор-2-бензотиазолил)-5-метилизоксазол-4-карбоксамида.
76. N-(3-пиридил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 240 - 250oC /разлож./) из N-(3-пиридил)-5-метилизоксазол-4-карбоксамида.
77. N-(4,6-диметил-2-пиридил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 184 - 186oC) из N-(4,6-диметил-2-пиридил)-5-метилизоксазол-4-карбоксамида.
78. N-(4,6-диметил-2-пиримидил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 221oC) из N-(4,6-диметил-2-пиридил)-5-метилизоксазол-4-карбоксамида.
79. N-(6-индазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления > 300oC) из N-(6-индазолил)-5-метилизоксазол-4-карбоксамида.
80. N-(5-индазолил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 220 - 223oC) из N-(5-индазолил)-5-метилизоксазол-4-карбоксамида.
81. N-(4-карбокси-3-гидроксифенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 242 - 246oC /разлож./) из N-(4-карбокси-3-гидроксифенил)-5-метилизоксазол-4-карбоксамида.
82. N-(3-карбокси-4-гидроксифенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 248 - 252oC /разлож./) из N-(3-карбокси-4-гидроксифенил)-5-метилизоксазол-4-карбоксамида.
83. N-(4-карбокси-3-хлорфенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 218 - 224oC /разлож./) из N-(4-карбокси-3-хлорфенил)-5-метилизоксазол-4-карбоксамида.
84. N-(4-гидроксифенил)амид 2-циано-3-гидроксикротоновой кислоты (температура разложения 184 - 186oC /разлож./) из N-(4-гидроксифенил)-5-метилизоксазол-4-карбоксамида.
85. N-(4-(4-трифторметилфенокси)фенил)амид 2-циано-3-гидрокси-4-метилкротоновой кислоты (температура плавления 147 - 149oC) из N-(4-(4-трифторметилфенокси)фенил)-5-этилизоксазол-4-карбоксамида.
86. N-(4-(4-трифторметилфенокси)фенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 171 - 173oC) из N-(4-(4-трифторметилфенокси)фенил)-5-метилизоксазол-4-карбоксамида.
87. N-метил-N-(4-трифторметилфенил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 69 - 70oC) из N-метил-N-(4-трифторметилфенил)-5-метилизоксазол-4-карбоксамида.
88. 2-гидроксиэтилиденциануксусная кислота-пиперидид из N-(5-метил-4-изоксазолилкарбонил)пиперидина.
89. 2-гидроксиэтилиденциануксусная кислота-4-метилпиперидид из N-(5-метил-4-изоксазолил-карбонил)-4-гидроксипиперидина.
90. N-(4-карбоксибутил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 92oC) из N-(5-метил-4-изоксазолилкарбонил)-5-аминовалериановой кислоты.
91. N-(4-этоксикарбоксибутил)амид 2-циано-3-гидроксикротоновой кислоты из N-(4-этоксикарбонилбутил)-5-метилизоксазол-4-карбоксамида.
92. N-(6-карбоксигексил)амид 2-циано-3-гидроксикротоновой кислоты (температура плавления 93 - 94oC) из N-(5-метил-4-изоксазолил-карбонил)-7-аминогептановой кислоты.
93. N-(3-хлор-4-трифторметилфенил)- 2-циан-3-гидрокси-кротонамид (точка разложения 205 - 208oC) из N-(3-хлор-4-трифторметилфенил)-5-метилизоксазол-4-карбоксамида (Т.пл. 139 - 144oC), полученного из 5-метилизоксазол-4-карбонила и 3-хлор-4-трифторметиланилина.
94. N-(4-трифторметилфенил)- 2-циан-3-гидрокси-метилкротонамид (Т.пл. 177 - 179oC) из N-(4-трифторметилфенил)-5-этил-изоксазол-4-карбоксамида (Т. пл. 104 - 105oC), полученного из 5-этилизоксазол-4-карбонилхлорида и 4-трифторметиланилина.
95. N-(2-хлор-4-трифторметилфенил)- 2-циан-3-гидроксикротонамид (Т.пл. 160oC) из N-(2-хлор-4-трифторметилфенил)-5-метилизоксазол-4-карбоксамида (Т. пл. 106 - 107oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 2-хлор-4-трифторметиланилина.
96. N-(4-хлорфенил)-2-циан-4-гидрокси-4-метилкротонамид (Т.пл. 155oC) из N-(4-хлорфенил)-5-этилизоксазол-4-карбоксамида (Т.пл. 103 - 104oC), полученного из 5-этилизоксазол-4-карбонилхлорида и 4-хлоранилина.
97. N-[4-(3-хлор-4-трифторметилфенокси)фенил] -2-циан-3- гидроксикротонамид (Т. пл. 170 - 172oC, из N-[4-(3-хлор-4-трифторметилфенокси)фенил]-5-метилизоксазол-4- карбоксамида (Т.пл. 175 - 180oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 4-(3-хлор-4-трифторметилфенокси)анилина.
98. N-(4-бромфенил)-2-циан-3- гидрокси-4-метил кротонамид (Т.пл. 161 - 162oC) из N-(4-бромфенил)-5-этилизоксазол-4-карбоксамида (Т. пл. 115 - 118oC), полученного из 5-этилизоксазол-4-карбонилхлорида и 4-броманилина.
99. N-(4-фторфенил)-2-циан-3- гидрокси-4-метилкротонамид (Т.пл. 145oC) из N-(4-фторфенил)-5-этилизоксазол-4-карбоксамида (Т.пл. 175 - 177oC), полученного из 5-этилизоксазол-4-карбонилхлорида и 4-фторанилина.
100. N-(4-бензоил)-2-циан-3-гидрокси-4-метилкротонамид (Т. пл. 139 - 141oC) из N-(4-бензоил)-5-этилизоксазол-4-карбоксамида (Т.пл. 168 - 170oC), полученного из 5-этилизоксазол-4-карбонилхлорида и 4-бензоиланилина.
101. N-[3-(1,1,2,2-тетрафторэтокси)-фенил]-2-циан-3- гидроксикротонамид (Т. пл. 149oC) из N-[3-(1,1,2,2-тетрафторэтокси)фенил]-5-метилизоксазол- 4-карбоксамида (Т.пл. 98oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 3-(1,1,2,2-тетрафторэтокси)анилина.
102. N-[4-(1,1,2,2-гексафторпропокси)-фенил] - 2-циан-3-гидроксикротонамид (Т. пл. 146 - 147oC) из N-[4-(1,1,2,2-гексафторпропокси)-фенил]-5-метилизоксазол-4- карбоксамида (Т.пл. 108 - 109oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 4-(1,1,2,3,3,3-гексафторпропокси)анилин.
103. N-(4-хлордифторметоксифенил)- 2-циан-3-гидроксикротонамид (Т.пл. 147 - 153oC) из N-(4-хлордифторметоксифенил)-5-метилизоксазол-4-карбоксамида (Т. пл. 112 - 115oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 4-хлордифторметоксианилина.
104. N-[3,5-дихлор-4-(1,1,2,2-тетрафторэтоксифенил] - 2-циан-3-гидроксикротонамид (Т. пл. 211 - 215oC) из N-[3,5-дихлор-4-(1,1,2,2-тетрафторэтокси)-фенил]-5-метилизоксазол-4- карбоксамида (Т.пл. 146oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 3,5-дихлор-4-(1,1,2,2-тетрафторэтокси)анилина.
105. N-(4-трет-бутилфенил)- 2-циан-3-гидроксикротонамид (Т. пл. 128 - 135oC) из N-(4-трет. -бутилфенил)-5-метил-изоксазол-4- карбоксамида (Т.пл. 122 - 128oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 4-трет.-бутиланилина.
106. N-(4-хлорфенил)-2-циан-3-гидроксикротонамид (Т.пл. 205 - 206oC) из N-(4-хлорфенил)-5-метилизоксазол-4-карбоксамида (Т. пл. 150oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 4-хлоранилина.
107. N-(3-хлорфенил)-2-циан-3-гидроксикротонамид (Т.пл. 163 - 169oC) из N-(3-хлорфенил)-5-метилизоксазол-4-карбоксамида (Т.пл. 97oC), полученного из 5-метилизоксазол-4-карбонилхлорида и 3-хлоранилина.
108. N-(3,4-метилендиоксифенил)-2-циан-3-гидроксикротонамид (Т.пл. 166 - 167oC) из N-(3,4-метилендиоксифенил)-5-метилизоксазол-4-карбоксамида (Т.пл. 125oC), полученный из 5-метилизоксазол-4-карбонилхлорида и 3,4-метилендиоксианилина.
109. N-(4-трифторметил)фенил-5-этилизоксазол-4-карбоксамид (Т.пл. 104 - 105oC) получают из 5-этилизоксазол-4-карбонилхлорида и 4-трифторметиланилина.
110. N-[4-трифторметилфенокси)-фенил]-5-этилизоксазол-4- карбоксамид (Т. пл. 92 - 94oC) получают из 5-этилизоксазол-4-карбонилхлорида и 4-(4-трифторметилфенокси)-анилина.
111. N-[4-(4-хлорбензоил)-фенил]-5-метилизоксазол-4- карбоксамид (Т.пл. 169 - 173oC) получают из 5-метилизоксазол-4-карбонилхлорида и 4-(4-хлорбензоил)-анилина.
112. N-(3-хлор-4-трифторметилфенил)-5-метилизоксазол-4- карбоксамид (Т. пл. 139 - 144oC) получают из 5-метилизоксазол-4-карбонилхлорида и 3-хлор-4-трифторметиланилина.






Описываются новые амиды органических кислот формулы (I)
где значения А, R2, R3 указаны в п.1 формулы, которые пригодны для лечения большого числа раковых заболеваний. Описываются также способы их получения и фармацевтическая композиция на основе соединений формулы (I). 3 с. и 2 з.п. ф-лы, 6 табл.

где А - остатки формул
и их стереоизомерные формы и/или их физиологически переносимые соли,
при этом если А имеет значение остатка формулы а), то R1 - водород, алкил с 1-6 С-атомами, алкил с 1-4 С-атомами, одно- или многократно замещенный, содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром, или йод, фенил;
R2 - алкенил с 2-3 С-атомами, бензил;
R3 - а) пиридил, одно- или многократно замещенный, содержащий в качестве заместителей водород, галоген, такой, как фтор, хлор, бром или иод, нитро, алкил с 1-3 С-атомами; б) группа формулы II
в которой R4, R5 и R6, одинаковые или различные, - галоген, такой, как фтор, хлор, бром или иод, нитро, бензоил, незамещенный или одно- или многократно замещенный и содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром или иод, метил, метокси, (С1-С3)- алкокси, одно- или многократно замещенный и содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром или иод, гидрокси, алкилсульфонил с 1-3 С-атомами в алкильной цепи, циано, бензоил, (С1-С3)- алкил, с) пиримидинил, одно- или многократно замещенный и содержащий в качестве заместителей алкил с 1-3 С-атомами, индолил или индазолинил,
в случае, если А имеет значение остатков формулы б), то R3 - фенил, одно- или многократно замещенный и содержащий в качестве заместителей галоген или алкил с 1-3 С-атомами, одно- или многократно замещенный, содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром, или иод;
R7 - водород или алкил с 2-4 С-атомами;
R3 - пиридил; пиридил, одно- или многократно замещенный и содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром или иод, алкил с 1-3 С-атомами, пиримидинил, замещенный алкилом с 1-3 С-атомами, индазолинил, фенил, одно- или многократно замещенный и содержащий в качестве заместителей бензоил, незамещенный или одно- или многократно замещенный и содержащий в качестве заместителей галоген, такой, как фтор, хлор, бром или иод;
R7 - алкил с 1-4 С-атомами, водород, CF3.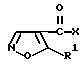
в которой Х - атом галогена, предпочтительно хлор или бром;
R1 имеет значение, указанное в формуле I,
подвергают взаимодействию с амином формулы VI
где R2 и R3 имеют значения, указанные в п.1.
| Bartlett R.R | |||
| Int | |||
| J | |||
| Immunopharmac | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОСЕРИНА ИЗ ЭФИРОВ СЕРИНА | 0 |
|
SU163621A1 |
| ТЕХНИЧЕСКАЯ БИБЛИОТЕКАБ. И. Поливода | 0 |
|
SU252459A1 |
| CA 1102341 A, 04.12.76 | |||
| DE 3405727 A1, 22.08.85 | |||
| US 4087535 A, 02.05.78 | |||
| 0 |
|
SU257882A1 | |
Авторы
Даты
1999-12-20—Публикация
1990-10-24—Подача