Изобретение относится к области медицины, а именно к клинической иммунологии, и касается разработки и использования нового иммуноглобулинового препарата против вирусного гепатита B.
Известен препарат иммуноглобулина против гепатита B (IgG HBs), получаемый из плазмы переболевших гепатитом B, содержащий высокий титр анти-HBs при полном отсутствии HBsAg (Соринсон С.Н. Вирусные гепатиты - СПб.: ТЕЗА 1998, с. 111).
Однако имеются данные, что при отсутствии HBsAg, в крови некоторых больных продолжает обнаруживаться HBV-ДНК, что характеризует их потенциальную эпидемиологическую опасность (Elghouzzi М.Н., Courouce А.М., Magnius L.O., et al. Transmission of hepatitis В virus by HBV-negative blood transfusion. - Lancet, 1995, V. 346, N 8980, H. 964). В России в соответствии с инструктивными указаниями лица, перенесшие гепатит B, от донорства отстраняются бессрочно ("Инструкция по проведению донорского плазмафереза" (утверждена МЗ РФМ. , 29.05.95 г.). Известен способ получения иммуноглобулинового препарата для профилактики и терапии бактериальных и вирусных заболеваний. К осадку Б /III фракция Кона/ добавляют дистиллированную воду. К экстракту осадка Б добавляют хлороформ и через 2 ч добавляют хлорид натрия, центрифугируют до получения прозрачного центрифугата.
Осадок удаляют. К центрифугату для выделения фракции иммуноглобулинов добавляют 50%-ный раствор ПЭГ /м.м. 6 тыс./. Осадок иммуноглобулинов отделяют путем декантации и центрифугирования, промывают дистиллированной водой, подкисленной до pH 5, растворяют в охлажденном 0,9%-ном растворе хлорида натрия до содержания белка 5-8%, pH 7,2. После растворения осадка препарат центрифугируют для удаления нерастворимых примесей. В качестве стабилизатора используют глюкозу до 2% (RU 2084229, 1997, A 61 K 35/14).
Известен также способ получения специфических иммуноглобулинов из сыворотки (плазмы) доноров, иммунизированных соответствующими антигенами и проверенных на отсутствие поверхностного антигена вируса гепатита B (HBsAg), антител к вирусу иммунодефицита человека (ВИЧ), антител к вирусу гепатита C, методом фракционирования этиловым спиртом при температуре ниже 0oC (Регламент производства иммуноглобулина из крови иммунизированных доноров N 28-97, утвержден 14.02.97).
Известен лекарственный препарат противовирусного действия, включающий человеческий интерферон и иммуноглобулин человека при массовом соотношении соответственно 1: 600-300000. В качестве человеческого интерферона препарат содержит рекомбинантный альфа-, бета- или гамма-интерферон человека, а в качестве иммуноглобулинов человека смесь lgA, lgM и lgG.
Препарат дополнительно содержит фармацевтически приемлемые целевые добавки (RU 2073522, 1997, A 61 K 38/21).
Однако способов получения иммуноглобулина против гепатита B из плазмы иммунизированных доноров не известно. Кроме того, имеются данные, что при спиртовом фракционировании необратимо образуются аггрегированные белки, количество которых возрастает в процессе лиофилизации и которые могут попадать в конечный препарат. Наличие аггрегированных молекул может вызывать реакции непереносимости при внутривенном введении, побочные реакции при внутримышечном введении, что существенно ухудшает профилактическую ценность иммуноглобулинов.
Задача изобретения заключается в разработке способа получения нового эффективного препарата - иммуноглобулина против гепатита B, не вызывающего никаких побочных реакций при его введениях в организм за счет иммунизации доноров рекомбинантной дрожжевой вакциной против гепатита B и за счет высокой степени очистки целевого продукта.
Поставленная задача решена предложенным способом получения иммуноглобулинов (IgG) и с помощью разработанного препарата для профилактики вирусных заболеваний.
Сущность изобретения заключается в следующем.
Для иммунизации доноров используют рекомбинантную дрожжевую вакцину против гепатита В производства АОЗТ НПК "Комбиотех Лтд.", представляющую собой поверхностный антиген вируса гепатита B (HBsAg), выделенный из штамма продуцента Saccharomyces cerevisiae, сорбированный на алюминии гидроксиде (RU 2088664 фирма "Комбиотех Лтд", Государственный реестр лекарственных средств под N 94/266/1 и 96/144/53/7).
Доноров, проверенных на отсутствие маркеров гепатита B (HBsAg и анти-HBs), иммунизируют рекомбинантной дрожжевой вакциной против гепатита B по экстренной схеме на фоне иммуномодуляторов, активную белковую фракцию выделяют спиртовым фракционированием, затем дополнительно очищают и концентрируют на ультрафильтрационных мембранах с порогом задержания веществ по молекулярной массе 100 кД, а мелкодисперсные примеси перед стерилизующей фильтрацией удаляют микрофильтрацией.
Сравнительный анализ существенных признаков заявляемого способа и ближайшего аналога свидетельствует, что общими признаками у них являются: иммунизация доноров специфическим антигеном, получение иммунной плазмы методом плазмафереза, выделение активной фракции спиртовым фракционированием.
Отличительными признаками в предлагаемом способе являются:
- обследование доноров перед иммунизацией на наличие анти-HBs,
- иммунизация рекомбинантной дрожжевой вакциной против гепатита B по экстренной схеме на фоне введения иммуномодуляторов,
- очистка и концентрирование иммуноглобулина (фракция KOH-III) ультрафильтрацией на мембранах с порогом задержания веществ по молекулярной массе 100 кД, с последующим удалением мелкодисперных примесей микрофильтрацией.
Причинно-следственная связь между совокупностью существенных признаков заявляемого изобретения и достигаемым результатом заключается в следующем:
Обнаружение анти-HBs при отсутствии HBsAg позволяет исключить из числа доноров лиц, ранее перенесших гепатит B, и тем самым уменьшить потенциальную опасность заражения больных при использовании крови и приготовленных из нее препаратов.
Разработанная схема иммунизации доноров рекомбинантной вакциной против гепатита B на фоне иммуномодуляторов обеспечивает получение пула плазм, используемого для приготовления иммуноглобулина, с уровнем анти-HBs не ниже 2000 мМЕ/мл.
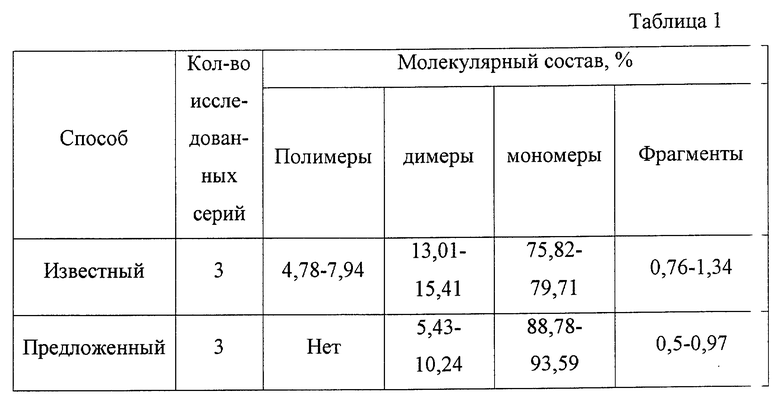
Использование ультрафильтрации для очистки и концентрирования иммуноглобулина позволяет получить препарат с максимальным содержанием мономерной фракции при полном отсутствии полимеров (табл. 1).
Таким образом, предложенный способ позволяет получить иммуноглобулин против гепатита B из плазмы иммунизированных доноров с высоким уровнем анти-HBs в короткие сроки с улучшенными молекулярными параметрами.
Способ осуществляют следующим образом:
Для получения предложенного препарата подбирают контингент доноров преимущественно молодого возраста (20-40 лет) согласно "Инструкции по медицинскому освидетельствованию доноров крови, плазмы, клеток крови", утвержденной МЗ РФ М., 29.05.95.
Доноров, проверенных на отсутствие поверхностного антигена вируса гепатита B (HBsAg), антител к вирусу иммунодефицита человека (ВИЧ), антител к вирусу гепатита C, дополнительно тестируют на наличие антител к вирусу гепатита B (анти-HBs).
Доноров, не содержащих в крови маркеров гепатита B, активно иммунизируют рекомбинантной дрожжевой вакциной против гепатита B на фоне иммуномодулятора (лактобактерин или тимоген).
Рекомбинантную дрожжевую вакцину против гепатита B вводят внутримышечно в дельтовидную мышцу трехкратно, при этом на фоне применения иммуномодуляторов получают пул плазм с высоким титром специфических антител.
Этап спиртового фракционирования иммунной плазмы проводят стандартным методом. Затем осадок KOH-III растворяют в стерильном апирогенном 0,9%-ном растворе хлорида натрия до концентрации 3-5% по белку. Раствор иммуноглобулина очищают на мембранах с диаметром пор 3 мкм и подвергают очистке и концентрированию ультрафильтрацией. При этом очистку раствора иммуноглобулина и концентрирование проводят на ультрафильтрационной установке, состоящей из перистальтического насоса и мембранных аппаратов с пределом задержания веществ по молекулярной массе 100 кД. В начале ведут концентрирование фракции KOH-III до 1/5 исходного объема, затем проводят диафильтрацию в постоянном объеме, для чего при работающей установке добавляют в концентрат диафильтрующий раствор - стерильный апирогенный 0,9%-ный раствор натрия хлорида. Диафильтрацию проводят до полного исчезновения азотистых веществ в пермеате (оптическая плотность меньше 0,1 при длине волны 280 нм по показаниям спектрофотометра). После диафильтрации проводят окончательную концентрацию до содержания белка в препарате 10-16%, корректируют pH до (7 ± 0,4), добавляют в качестве стабилизатора глицин в концентрации (2,25±0,75)% и перед стерилизующей фильтрацией освобождают от мелкодисперсных примесей микрофильтрацией на мембранах с размером пор 3 мкм.
Иммуноглобулин против гепатита B содержит не менее 50 МЕ/мл анти-HBs, 10-16% белка.
Способ иллюстрируется следующим конкретным примером.
Пример
Для получения предложенного препарата подбирают контингент доноров преимущественно молодого возраста (20-40 лет) согласно "Инструкции по медицинскому освидетельствованию доноров крови, плазмы, клеток крови", утвержденной МЗ РФ М., 29.05.95.
Доноров, проверенных на отсутствие поверхностного антигена вируса гепатита B (HBsAg), антител к вирусу иммунодефицита человека (ВИЧ), антител к вирусу гепатита C, дополнительно тестируют на наличие антител к вирусу гепатита B (анти-HBs).
Доноров, не содержащих в крови маркеров гепатита B, активно иммунизируют рекомбинантной дрожжевой вакциной против гепатита B на фоне иммуномодуляторов (лактобактерин или тимоген).
Принципиальная схема иммунизации
Перед началом вакцинации доноры принимают в течение 10 дней лактобактерин по 5 доз ежедневно или тимоген 50-100 мкг интраназально в течение 10 дней.
Рекомбинантную дрожжевую вакцину против гепатита B вводят внутримышечно в дельтовидную мышцу трехкратно (разовая доза 20 мкг HBsAg) по экстренным схемам: 0-7-21 день или 0-1-2 месяца.
В процессе иммунизации доноры находятся под систематическим врачебным, клинико-морфологическим, биохимическим, иммунологическим контролем. На 14 день после последней иммунизации контролируют титр антител в сыворотке крови иммунизированных доноров.
Доноров, содержащих в сыворотке крови не менее 100 мМЕ/мл анти-HBs, подвергают систематическому плазмаферезу два раза в месяц. Полученную таким методом противогепатитную плазму накапливают и хранят в стерильных пластикатных мешках при температуре от -20oC до -30oC. Из этой противогепатитной плазмы выделяют иммуноглобулин против гепатита B путем фракционирования плазмы этиловым спиртом при отрицательных температурах.
80,0 л противогепатитной плазмы загружают в реактор и охлаждают до 0oC при непрерывном перемешивании подачей охлаждающего рассола в рубашку реактора. Затем в реактор добавляют предварительно охлажденный до -20oC этиловый спирт до конечной концентрации в плазме 8,0%, постепенно понижая температуру смеси в реакторе во время осаждения от 0oC до -3oC. Выдерживают смесь при перемешивании в течение часа при температуре -3oC. Образовавшийся осадок, состоящий из фибриногена, стромы эритроцитов, нерастворимых белков крови, отделяют центрифугированием на скоростной центрифуге СГО - 150 при 15000 об/мин.
Центрифугат помещают в реактор и производят отделение глобулинов от альбумина. Для этого в реактор добавляют 50%-ный спирт, предварительно охлажденный до -20oC, при непрерывном перемешивании в течение 4-5 ч, снижая постепенно температуру смеси от -3oC до -10oC, до конечной концентрации спирта в смеси 25%. pH при этом должна составлять 7,0-7,4. При отклонении pH от указанных значений производят корректирование с помощью 1 моль/л раствора бикарбоната натрия. Затем подают спиртово-белковую смесь на центрифугу СГО-150 для отделения осадка глобулинов от раствора альбумина. Общий вес осадка глобулинов - 3,6 кг.
На следующей стадии производят разделение бета-глобулина и иммуноглобулина. Для этого осадок глобулинов растворяют в охлажденной до 0oC дистиллированной воде из расчета 25 л на 1 кг осадка. К полученному раствору добавляют хлорид натрия из расчета 0,812 г на 1 л воды. В растворе устанавливают pH (5,0 ± 0,1) добавлением 1 моль/л ацетатного буфера из расчета 110-120 мл на 1 кг осадка и перемешивают не менее 1 ч. После этого к раствору добавляют охлажденный 50%-ный спирт до конечной концентрации 17%. Осаждение ведут 4-5 ч при постепенном снижении температуры в реакторе от 0oC до -5oC. После этого производят отделение осадка бета-глобулина и липопротеидов от раствора иммуноглобулина центрифугированием на центрифуге СГО-150.
На следующей стадии проводят выделение осадка иммуноглобулина. Для этого к центрифугату добавляют охлажденный 5 моль/л раствор хлорида натрия из расчета 10 мл на 1 л центрифугата. Устанавливают pH (6,9 ± 0,1) путем добавления 1 моль/л раствора бикарбоната натрия. К раствору добавляют охлажденный спирт в течение 4-5 ч, постепенно понижая температуру от -5oC до -10oC до конечной концентрации спирта в смеси 25%. Смесь при температуре -10oC перемешивают в течение 1 ч. После этого отделяют осадок иммуноглобулина центрифугированием, собирают осадок иммуноглобулина и взвешивают. Вес осадка - 1,7 кг (фракция KOH-III) или 21,2 г очищенного иммуноглобулина с 1 л плазмы.
Осадок (KOH-III) растворяют в стерильном 0.9%-ном растворе хлорида натрия до конечной концентрации по белку 2-3%. Полученный раствор освобождают от мелкодисперсных примесей микрофильтрацией на мембранах с диаметром пор 3 мкм. Фильтрат (объем 18 л) собирают в бачок из нержавеющей стали с двумя патрубками, соединенными с подготовленной к работе ультрафильтрационной установкой, состоящей из перистальтического насоса и мембранного аппарата с полыми волокнами марки ВПУ -100. При давлении (0,06 ± 0,02) МПа проводят концентрацию материала до 1/5 исходного объема, а затем диафильтрацию в постоянном объеме, для чего при работающей установке добавляют в концентрат диафильтрующий раствор - стерильный апирогенный 0,9%-ный раствор натрия хлорида. Диафильтрацию проводят до полного исчезновения азотистых веществ в пермеате (оптическая плотность меньше 0,1 при длине волны 280 нм по показанию спектрофотометра). Затем проводят окончательную концентрацию до объема 3,2 л (содержание общего белка 11,2 %). Пермеат во время всего процесса очистки сбрасывают в канализацию.
В препарате устанавливают pH (7,0 ± 0,4), добавляют в качестве стабилизатора глицин в концентрации (2,25±0,75)% и перед стерилизующей фильтрацией освобождают от мелкодисперсных примесей микрофильтрацией на мембранах с размером пор 3 мкм.
Содержание белка определяют по методу Лоури, иммуноспецифическая активность (титр анти-HBs) определяется иммуноферментным анализом с использованием наборов фирмы Эбботт (США) для определения анти-HBs.
Содержание в белке плазмы человека иммуноглобулинов (IgG) устанавливают методом зонного электрофореза в полиакриламидном геле.
Предлагаемый способ обеспечивает получение иммуноглобулина (IgG) против гепатита B с содержанием белка 10-16%, титром анти-HBs не менее 50 МЕ/мл.
Выделенная фракция является активным компонентом разработанного на ее основе препарата против гепатита B. В состав препарата входят следующие компоненты: иммуноглобулиновая фракция IgG, полученная предлагаемым способом 10-16 мас. %; в качестве стабилизатора - глицин в количестве 1,5-3,0 мас.%, 0,9 %-ный раствор хлорида натрия с pH 6,6-7,4 до 1 или 2 мл.
Препарат дополнительно может содержать другие активные компоненты, такие, например, как иммуномодуляторы, иммуноглобулины против сопутствующих инфекций. Получают препарат традиционным методом смешения всех составляющих его компонентов. При необходимости раствор препарата подвергают лиофилизации любым известным способом.
Пример 1
Иммуноглобулиновая фракция lgG,с содержанием анти-HBs 50 МЕ/мл - 10 мас. %
Глицин - 1,5 мас.%
0,9 %-ный раствор хлорида натрия с pH 6,6 - До 2 мл
Пример 2
Иммуноглобулиновая фракция IgG, с содержанием анти-HBs 100 МЕ/мл - 16 мас.%
Глицин - 3,0 мас.%
0,9%-ный раствор хлорида натрия с pH 7,4 - До 1 мл
Пример 3
Иммуноглобулиновая фракция IgG, с содержанием анти-HBs 100 МЕ/мл - 15 мас. %
Глицин - 2,0 мас.%
Иммуномодулятор - - 0,0005 мас.%
0,9 %-ный раствор хлорида натрия с pH 7,0 - До 1 мл
Препарат представляет собой прозрачную или слегка опалесцирующую жидкость, бесцветную или со слабой желтой окраской. В процессе хранения допускается появление незначительного осадка, исчезающего при встряхивании при температуре препарата (20 ± 2)oC.
Действующим началом препарата являются иммуноглобулины, обладающие активностью антител к поверхностному HBsAg вируса гепатита B. Применяют препарат для предупреждения заболевания вирусным гепатитом B, а также в следующих случаях:
1. После случайных заражений (при уколах, стоматологических манипуляциях, при переливаниях крови и т.д.) людей, не проходивших ранее вакцинацию против вирусного гепатита B, или лиц, у которых вакцинация не закончена, или в случае, когда уровень HBs-антител ниже защитного (менее 10 МЕ/л) или неизвестен.
2. У лиц или пациентов, жизнедеятельность которых требует постоянных профилактических мероприятий в связи с риском заражения вирусом гепатита B, или у тех, у кого проведение вакцинации невозможно или она не приводит к формированию поствакцинального иммунитета (например, у персонала отделения гемодиализа, который занимается наблюдением за пациентами с положительным результатом на HBs-антиген или у сексуальных партнеров - хронических носителей HBs- антигена).
Пример применения препарата:
Препарат вводят внутримышечно в верхний наружный квадрант ягодичной мышцы. До начала инъекции ампулы с препаратом выдерживают в течение 2 ч при комнатной температуре (20 ± 2)oC. Вскрытие ампул и процедуру введения осуществляют при строгом соблюдении правил асептики и антисептики. Доза препарата и кратность его введения зависят от показаний к применению:
1. После случайных заражений препарат вводят в количестве 8 ME на 1 кг веса в течение 24 ч после заражения. Предпочтительно в течение 7 дней после пассивной иммунизации необходимо вводят одну дозу рекомбинантной вакцины против гепатита B и впоследствии вводят дополнительные дозы вакцины в соответствии с указаниями "Инструкции по применению вакцины гепатита B рекомбинантной дрожжевой жидкой".
2. Для групп риска (персонал отделения гемодиализа, сексуальные партнеры - хронические носители HBs-антигена и т.д.), а также в случаях, когда вакцинация против гепатита B невозможна или она не приводит к формированию достаточного уровня антител (ниже 10 МЕ/л) - 8 ME на 1 кг веса 1 раз в два месяца.
При употреблении больших доз (более 5 мл) препарата рекомендуется делить дозу на несколько уколов в разные части тела. Максимальная концентрация антител в крови достигается через 24 ч, период полувыведения антител из организма составляет 4-5 недель.
Реакции на введение иммуноглобулина, как правило, отсутствуют. В редких случаях могут развиваться местные реакции в виде гиперемии и повышения температуры до 37,5oC в течение первых суток после введения. Препарат выпускают в жидком виде в ампулах по 1 или 2 мл. Одна доза препарата (1 или 2 мл) содержит не менее 100 ME HBs-антител. Препарат хранят в сухом и темном помещении при температуре (6 ± 4)oC.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В, СТОЛБНЯКА, ДИФТЕРИИ И КОКЛЮША | 1998 |
|
RU2130778C1 |
| ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К HBs-АНТИГЕНУ И БЛОКАТОР В ТЕСТ-СИСТЕМЕ | 2001 |
|
RU2206095C1 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В, СТОЛБНЯКА И ДИФТЕРИИ | 1998 |
|
RU2130779C1 |
| СПОСОБ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА В | 1999 |
|
RU2166961C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА B | 1998 |
|
RU2135209C1 |
| СПОСОБ ВАКЦИНАЦИИ ПРОТИВ ВИРУСНОГО ГЕПАТИТА B | 1997 |
|
RU2116086C1 |
| ТЕСТ-СИСТЕМА ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТИ-HBS В БИОЛОГИЧЕСКОМ ОБРАЗЦЕ | 2005 |
|
RU2290642C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ КОКЛЮША, ДИФТЕРИИ, СТОЛБНЯКА И ВИРУСНОГО ГЕПАТИТА В И Д | 2003 |
|
RU2233673C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНОВ ИЗ ФРАКЦИЙ, КОТОРЫЕ ОБРАЗУЮТСЯ ПРИ ФРАКЦИОНИРОВАНИИ ЧЕЛОВЕЧЕСКОЙ ПЛАЗМЫ КРОВИ | 1996 |
|
RU2157240C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В И Д, СТОЛБНЯКА И ДИФТЕРИИ | 2003 |
|
RU2233672C1 |
Использование: относится к области медицины, а именно клинической иммунологии, и касается разработки и использования нового иммуноглобулинового препарата против вирусного гепатита В. Сущность изобретения заключается в том, что доноров, проверенных на отсутствие маркеров гепатита В (HBsAg и анти-НBs), иммунизируют рекомбинантной дрожжевой вакциной против гепатита В по экстренной схеме на фоне иммуномодуляторов. Активную белковую фракцию выделяют спиртовым фракционированием, очищают и концентрируют на ультрафильтрационных мембранах с порогом задержания веществ по молекулярной массе 100 кД, мелкодисперсные примеси перед стерилизующей фильтрацией удаляют микрофильтрацией. Препарат, полученный согласно изобретению, представляет собой фракцию, выделенную из плазмы доноров предложенным способом. Препарат содержит в качестве активного начала анти-HBs с титром не менее 50 МЕ/мл, белки - 10-16% и в качестве стабилизатора глицин 2,25+0,75% и 0,9%-ный раствор хлорида натрия. Впервые разработан препарат, содержащий иммуноглобулин, против гепатита В. 2 с. и 2 з.п. ф-лы, 1 табл.
Иммуноглобулиновая фракция IgG с содержанием анти-HBs не менее 50 МЕ/мл, мас.% - 10 - 16
Глицин, мас.% - 1,5 - 3,0
0,9%-ный раствор хлорида натрия с рН 6,6 - 7,4, мл - До 1
2. Иммуноглобулиновый препарат против вирусного гепатита В по п.1, отличающийся тем, что он дополнительно содержит иммуномодулятор.
| RU 2060034 C1, 20.05.96 | |||
| US 5248767 A, 28.09.93 | |||
| JP 61078371 A, 22.04.86 | |||
| JP 62283933 A, 09.12.87 | |||
| JP 04124142 A, 24.04.92 | |||
| Руководство по вакцинному и сывороточному делу, под ред | |||
| П.Н.Буртасова, М., Медицина, 1978, стр.308-339. |
Авторы
Даты
2000-01-20—Публикация
1999-04-19—Подача